Материал для подготовки к ЕГЭ (ГИА) по химии (9 класс) на тему: Пробный экзамен ОГЭ по химии 2018
Тренировочный тест для подготовки к ОГЭ – 2018 по химии в 9 классе
Инструкция по выполнению работы
На выполнение работы отводится 2 часа (120 минут). Работа состоит из 2 частей, включающих 22 задания. Часть 1 содержит 19 заданий с кратким ответом, часть 2 содержит 3 задания с развернутым ответом.
Ответы к заданиям 1-15 записываются в виде одной цифры, которая соответствует номеру правильного ответа.
Ответы к заданиям 16-19 записываются в виде последовательности цифр.
К заданиям 20-22 следует дать полный развёрнутый ответ, включающий в себя необходимые уравнения реакций и решение задачи.
При выполнении работы можно пользоваться Периодической системой химических элементов Д.И. Менделеева, таблицей растворимости солей, кислот и оснований в воде, электрохимическим рядом напряжений металлов и непрограммируемым калькулятором.
Часть 1
При выполнении заданий 1-15 из четырех предложенных вам вариантов ответов выберите один верный. |
1.Химическому элементу 2-го периода VIA-группы соответствует схема распределения электронов
1) Рис. 1
2) Рис. 2
3) Рис. 3
4) Рис. 4
Ответ:
2. Неметаллические свойства простых веществ усиливаются в ряду
1) фосфор → кремний → алюминий
2) фтор → хлор → бром
3) селен → сера → кислород
4) азот → фосфор → мышьяк
Ответ:
3. Ковалентная полярная связь реализуется в веществе
1) CuO
2) P4
3) SO2
4) MgCl2
Ответ:
4. В каком соединении степень окисления хлора равна +7?
1)HCl
2) Cl2O
3) KClO3
4) KClO4
Ответ:
5. Вещества, формулы которых — ZnO и Na2SO4, являются соответственно
1) оснόвным оксидом и кислотой
2) амфотерным гидроксидом и солью
3) амфотерным оксидом и солью
4) оснόвным оксидом и основанием
Ответ:
6. Реакция, уравнение которой
2NaOH + CuCl2 = Cu(OH)2 + 2NaCl
относится к реакциям
1) разложения
2) соединения
3) замещения
4) обмена
Ответ:
7. Наименьшее количество положительных ионов образуется при диссоциации 1 моль
1) азотной кислоты
2) карбоната натрия
3) сульфата алюминия
4) фосфата калия
Ответ:
8. Необратимое протекание реакции ионного обмена между растворами гидроксида бария и карбоната калия обусловлено взаимодействием ионов
1) K+ и OH―
2) K+ и CO32―
3) Ba2+ и CO32―
4) Ba2+ и OH―
Ответ:
9. Медь реагирует с раствором
1) AgNO3
2) Al2(SO4)3
3) Fe SO4
4) NaOH
Ответ:
10. Оксид меди(II) может реагировать с каждым веществом пары
1) HCl, O2
2) Ag, SO3
3) h3, SO4
4) Al, N2
Ответ:
11. Определите формулу неизвестного вещества в схеме реакции:
KOH + …→ K2CO3 +h3O
1) CO
2) CO2
3) Ch5
4) C
Ответ:
12. Превратить CaNO3 в CaSO3 можно с помощью
1) сероводорода
2) сульфита бария
3) сульфита натрия
4) сернистого газа
Ответ:
13. Верны ли суждения о способах разделения смесей?
А. Выпаривание относят к физическим способам разделения смесей.
Б. Разделение смеси воды и этанола возможно способом фильтрования.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Ответ:
14. В реакции 3CuO + 2Nh4 =3Cu+ N2+ 3h3O
изменение степени окисления окислителя соответствует схеме
1) +2 → 0
2) −3 → 0
3) −2 → 0
4) 0 → +2
Ответ:
15. На какой диаграмме распределение массовых долей элементов
соответствует NHNO3
Часть 2
При выполнении заданий 16, 17 из предложенного перечня ответов выберите два правильных и обведите их номера. Цифры выбранных ответов запишите в указанном месте в порядке возрастания без дополнительных символов. |
16. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
В ряду химических элементов Be- Mg- Ca
1) увеличивается атомный радиус
2) возрастает высшая степень окисления
3) увеличивается значение электроотрицательности
4) увеличиваются основные свойства образуемых гидроксидов
5) уменьшается число электронов на внешнем уровне
Ответ:
17. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
Для метилового спирта верны следующие утверждения:
1) является газообразным веществом (н. у.)
2) в молекуле имеется гидроксильная группа
3) ядовит
4) плохо растворим в воде
5) вступает в реакцию с серебром
При выполнении заданий 18,19 к каждому элементу первого столбца подберите соответствующий элемент из второго столбца. Выбранные цифры запишите в таблицу под соответствующими буквами. |
Ответ:
18. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
ВЕЩЕСТВА |
| РЕАКТИВ |
А) NaNO3 и Ca(NO3)2 Б) FeCl2 и FeCl3 В) h3SO4 и HNO3 |
| 1) BaCl2 2) Na2CO3 3) HCl 4) NaOH |
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
19. Установите соответствие между веществом и реагентами, с каждым из которых оно может вступать в реакцию.
ВЕЩЕСТВО | РЕАГЕНТЫ |
A) гидроксид калия | 1) SO2, FeSO4 |
Б) гидроксид цинка | 2) NaOH, h3SO4 |
B) соляная кислота | 3) Na2SO3, AgNO3 |
4) KCl, CaO |
Ответ:
Часть 2
Для ответов на задания 20-22 используйте отдельный лист. Запишите сначала номер задания (20,21, или 22), а затем развернутый ответ к нему. |
20. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой
P + h3SO4 →h4PO4 + SO2 + h30
Определите окислитель и восстановитель
21. При взаимодействии избытка раствора карбоната калия с 10%-ным раствором нитрата бария выпало 3,94 г осадка. Определить массу взятого для опыта раствора нитрата бария.
22. Даны вещества:CuO, NaCl, KOH, MnO2, h3SO4, CaCO3
Используя воду и необходимые вещества только из этого списка, получите в две стадии хлорид меди(II). Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Система оценивания тестовой работы по химии
Верное выполнение каждого из заданий части 1 базового уровня сложности (1–15) оценивается 1 баллом.
Верное выполненное каждого из заданий части 1 повышенного уровня сложности (16–19) максимально оценивается 2 баллами. Задания 16 и 17 считаются верно выполненными, если в каждом из них правильно выбраны два варианта ответа. За неполный ответ – правильно назван один из двух ответов или названы три ответа, из которых два верные, – выставляется 1 балл. Остальные варианты ответов считаются неверными и оцениваются в 0 баллов.
Задания 18 и 19 считаются выполненными верно, если правильно установлены три соответствия. Частично верным считается ответ, в котором установлены два соответствия из трех; он оценивается 1 баллом. Остальные варианты считаются неверным ответом и оцениваются в 0 баллов.
Часть 1
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
4 | 3 | 3 | 4 | 3 | 4 | 1 | 3 | 1 | 3 |
11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | |
2 | 3 | 1 | 1 | 4 | 14 | 23 | 241 | 123 |
Часть 2
20. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
HNO3 +Zn = Zn(NO3)2 + NO + h3O
Укажите окислитель и восстановитель.
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысл) | |
1) Составим электронный баланс: S+6 + 2ē = S+4 │2 │5 10 P0 — 5ē = P+5 │5 │2
2) Укажем, что S+6 (h3SO4) — окислитель, а P0(P) —восстановитель
3) Расставим коэффициенты в уравнений реакции: 2P + 5h3SO4 →2h4PO4 + 5SO2 + 2h30 | |
Критерии оценивания | Баллы |
Ответ правильный и полный, включает все названные элементы | 3 |
В ответе допущена ошибка только в одном из элементов | 2 |
В ответе допущены ошибки в двух элементах | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 3 |
21. При взаимодействии избытка раствора карбоната калия с 10%-ным раствором нитрата бария выпало 3,94 г осадка. Определить массу взятого для опыта раствора нитрата бария.
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысл) | |
Пояснение.
K2CO3 + Ba(NO3)2 = ↓ + 2KNO3 2) Рассчитано количество вещества карбоната бария и масса нитрата бария: n(BaCO3) = m(BaCO3) / M(BaCO3) = 3,94 : 197 = 0,02 моль n (Ba(NO3)2) = n(BaCO3) = 0,02 моль m (Ba(NO3)2) = n (Ba(NO3)2) •M (Ba(NO3)2) = 0,02• 261= 5,22 г. 3) Определена масса раствора нитрата бария: m (раствора) = m(Ba(NO3)2 / ω (Ba(NO3)2 = 5,22 / 0,1= 52,2 г
Ответ: 52,2 г. | |
Критерии оценивания | Баллы |
Ответ правильный и полный, включает все названные элементы | 3 |
Правильно записаны 2 элемента из названных выше | 2 |
Правильно записан 1 элемент из названных выше (1-ый или 2-ой) | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 3 |
22. Даны вещества:CuO, NaCl, KOH, MnO2, h3SO4, CaCO3
Используя воду и необходимые вещества только из этого списка, получите в две стадии хлорид меди(II). Опишите признаки проводимых реакций. Для второй реакции напишите сокращённое ионное уравнение реакции.
Элементы ответа (допускаются иные формулировки ответа, не искажающие его смысл) | |
Напишем 2 уравнения реакций: 2NaCl + h3SO4 =2HCl↑+ Na2SO4 CuO +2HCl =CuCl2 +h3O
Укажем признаки реакций. Для первой реакции — выделение газа. Для реакции растворения CuO — изменение цвета, образование голубого раствора. Составим сокращённое ионное уравнение для первой реакции: CuO +2H+ =Cu2+ +h3O | |
Критерии оценивания | Баллы |
Ответ правильный и полный, включает все названные элементы | 5 |
Правильно записаны четыре элемента ответа | 4 |
Правильно записаны три элемента ответа | 3 |
Правильно записаны два элемента ответа | 2 |
Правильно записан один элемент ответа | 1 |
Все элементы ответа записаны неверно | 0 |
Максимальный балл | 5 |
2018 год.
Максимальное количество баллов, которое может получить экзаменуемый за выполнение всей экзаменационной работы (без реального эксперимента), — 34 балла.
Таблица 4
Шкала пересчета первичного балла за выполнение экзаменационной работы в отметку по пятибалльной шкале (работа без реального эксперимента, демоверсия 1)
- 0—8 баллов — отметка «2»
- 9—17 баллов — отметка «3»
- 18—26 баллов — отметка «4»
- 27—34 баллов — отметка «5»
Отметку «5» рекомендуется выставлять в том случае, если из общей суммы баллов, достаточной для получения этой отметки, выпускник набрал 5 и более баллов за выполнение заданий части 3. Результаты экзамена могут быть использованы при приеме учащихся в профильные классы средней школы. Ориентиром при отборе в профильные классы может быть показатель, нижняя граница которого соответствует 23 баллам.
Пробный (репетиционный) вариант ОГЭ по химии 2018 (Санкт-Петербург)
Пробный ОГЭ по химии
Вариант № 1
1. В атоме химического элемента содержится 16 электронов. Сколько из них находятся на внешнем энергетическом уровне?
1) 2 2) 4 3) 6 4) 8
2. В каком ряду химических элементов усиливаются неметаллические свойства соответствующих им простых веществ?
1) алюминий → фосфор → хлор
2) фтор → азот → углерод
3) хлор → бром → иод
4) кремний → сера → фосфор
3. Какой вид химической связи характерен для меди?
1) ионная 2) металлическая 3) ковалентная полярная 4) ковалентная неполярная
4. В каком соединении сера имеет наивысшую степень окисления?
1) 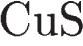 2)
2) 
 4)
4) 
5. Сложным является каждое из двух веществ:
1) нитрат калия и хлор 2) белый фосфор и озон
3) гидроксид калия и аргон 4) угарный газ и аммиак
6. Взаимодействие между оксидом меди(II) и водородом при нагревании – это
реакция
1) разложения 2) замещения 3) соединения 4) обмена
7. Больше всего ионов водорода образуется в водном растворе из одного моля
1)  2)
2)  3)
3) 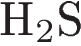 4)
4) 
8. Осадок образуется при взаимодействии водных растворов
1) нитрата аммония и гидроксида калия
2) соляной кислоты и гидроксида бария
3) нитрата серебра и бромида кальция
4) азотной кислоты и карбоната натрия
9. С кислородом может реагировать
1) медь
2) оксид углерода(IV)
3) гидроксид натрия
4) серная кислота
10. Оксид серы(VI) реагирует с
1) нитратом натрия
2) хлором
3) оксидом алюминия
4) оксидом кремния
11. Азотная кислота образуется в реакции между соляной кислотой и
1) аммиаком
2) нитратом бария
3) азотом
4) нитратом серебра
12. В реакцию и с гидроксидом кальция, и с нитратом серебра вступает
1) карбонат магния
2) хлорид аммония
3) нитрат натрия
4) сульфат бария
13. Верны ли следующие суждения о правилах безопасной работы в лаборатории?
А. При получении кислорода из раствора пероксида водорода необходимо использовать резиновые перчатки.
Б. При растворении соды в воде необходимо надеть защитные очки.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
14. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
ВЕЩЕСТВА
РЕАКТИВ
А) 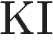
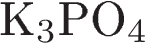 (р-р)
(р-р) Б)  (р-р) и
(р-р) и  (р-р)
(р-р)
В)  (р-р) и
(р-р) и 
1)  (р-р)
(р-р)
2)  (р-р)
(р-р)
3)  (р-р)
(р-р)
4) 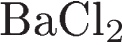
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
15. На какой диаграмме распределение массовых долей элементов соответствует  ?
?
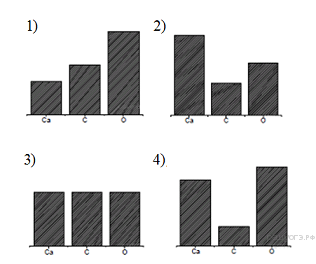
16.
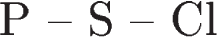 происходит уменьшение (ослабление)
происходит уменьшение (ослабление)1) заряда ядра
2) степени окисления в высших оксидах
3) числа атомов водорода в летучем водородном соединении
4) радиуса атома
5) числа электронов на внешнем энергетическом уровне
17. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
Этилен
1) относится к непредельным углеводородам
2) не реагирует с кислородом
4) имеет только одинарные связи
5) вступает в реакции замещения
18. Хлороводород является восстановителем в реакции с
1)  2)
2)  3)
3) 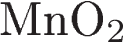 4)
4) 
19. Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВАПРОДУКТЫ РЕАКЦИИ
А) 
Б) 
В) 
1) 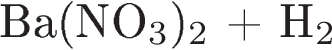
2) 
3) 
4) 
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
20. Используя метод электронного баланса, составьте уравнение реакции по схеме:
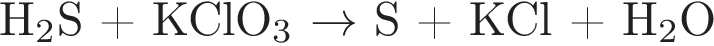
Определите окислитель и восстановитель
21. К 340 г раствора с массовой долей нитрата серебра 6 % добавили избыток раствора хлорида железа (III). Вычислите массу образовавшегося осадка.
22. Даны вещества: FeCl3, H2SO4(конц.), Fe, Cu, NaOH, CuSO4.
Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид железа(II).
Запишите уравнения проведённых химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
Пробный ОГЭ по химии
Вариант № 2
1. На внешнем энергетическом уровне элемента 2-го периода – в два раза больше электронов, чем на внутреннем уровне. Этот элемент –
1) литий 2) бериллий 3) углерод 4) кислород
2. Неметаллические свойства углерода выражены сильнее, чем неметаллические свойства
1) кислорода 2) кремния 3) азота 4) фтора
3. Ковалентной полярной связью образовано каждое из веществ в группе
1) 
2) 
3) 
4) 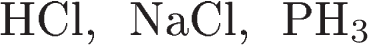
4. Сера имеет самую низкую степень окисления в
1) 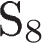 2)
2) 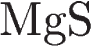 3)
3)  4)
4) 
5. Оксиду меди(I) и гидроксиду меди(I) соответствуют формулы
1) 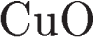 и
и  2)
2)  и
и 
3)  и
и  4)
4) 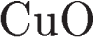 и
и 
6. Пример реакции обмена:
1) 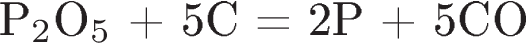
2) 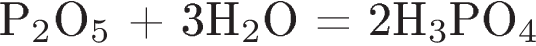
3) 
4) 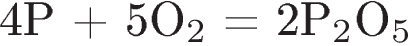
7. В растворе сульфата аммония находится 0,6 моль положительных ионов. Количество отрицательных ионов в этом растворе равно
1) 0,2 моль 2) 0,3 моль 3) 0,6 моль 4) 1,2 моль
8. Взаимодействию карбоната магния с бромоводородной кислотой соответствует сокращённое ионное уравнение
1) 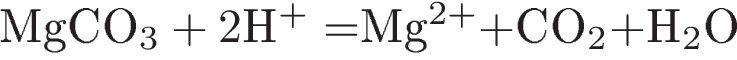
2) 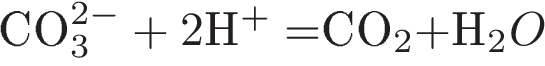
3) 
4) 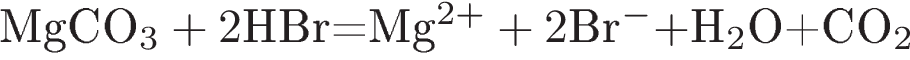
9. Хлор реагирует с
1)  2)
2) 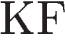 3)
3)  4)
4) 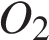
10. Химическая реакция возможна между
1) оксидом серы(IV) и соляной кислотой
2) оксидом алюминия и гидроксидом натрия
3) оксидом бериллия и кислородом
4) оксидом железа(II) и оксидом калия
11. Какие вещества из приведённых ниже образуются при взаимодействии гидроксида меди(II) с соляной кислотой?
A) 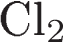 Б)
Б) 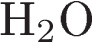 B)
B)  Г)
Г)  Д)
Д) 
Выберите ответ с набором букв, которые соответствуют образующимся веществам.
1) БГ 2) БВ 3) АД 4) АГ
12. При взаимодействии растворов силиката натрия и соляной кислоты образуется(-ются) хлорид натрия и
1) 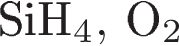 2)
2) 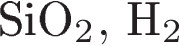 3)
3)  4)
4) 
13. Верны ли следующие суждения об обращении с растворами щелочей?
А. При попадании раствора щелочи на кожу рук его надо смыть водой.
Б. При попадании раствора щелочи на кожу рук его надо смыть раствором соды.
1) верно только А 2) верно только Б 3) верны оба суждения 4) оба суждения неверны
14. Установите соответствие между двумя веществами и реактивом, с помощью которого можно различить эти вещества.
ВЕЩЕСТВА
РЕАКТИВ
А)  (р-р) и
(р-р) и  (р-р)
(р-р)
Б)  (р-р) и
(р-р) и  (р-р)
(р-р)
В)  (р-р) и
(р-р) и  (р-р)
(р-р)
1) лакмус (р-р)
2)  (р-р)
(р-р)
3)  (р-р)
(р-р)
4)  (р-р)
(р-р)
Запишите в ответ цифры, расположив их в порядке, соответствующем буквам:
АБ
В
15. На какой диаграмме распределение массовых долей элементов соответствует  ?
?
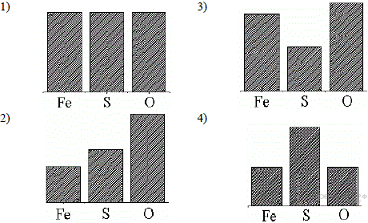
1) 1 2) 2 3) 3 4) 4
16. При выполнении задания из предложенного перечня ответов выберите два правильных и запишите цифры, под которыми они указаны.
В ряду химических элементов 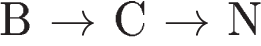
1) увеличивается заряд ядер атомов
2) возрастают кислотные свойства образуемых гидроксидов
3) увеличивается число электронных уровней
4) уменьшается электроотрицательность
5) возрастает атомный радиус
17. Для этилена верны следующие утверждения:
1) составу молекулы соответствует общая формула 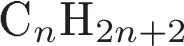
2) является непредельным углеводородом
3) атомы углерода в молекуле соединены одинарной связью
4) вступает в реакции присоединения
5) при горении образуется углерод и водород
18. Подтвердить качественный состав сульфата железа(II) можно с помощью двух растворов, содержащих соответственно ионы
1) 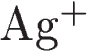 и
и  2)
2) 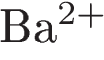 и
и  3)
3)  и
и  4)
4) 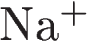 и
и 
19. Установите соответствие между исходными веществами и продуктами реакции.
ИСХОДНЫЕ ВЕЩЕСТВАПРОДУКТЫ РЕАКЦИИ
A) 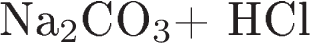
1) 
Б) 
2) 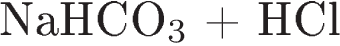
B) 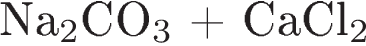
3) 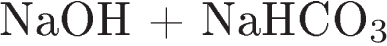
4) 
5) 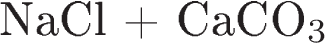
20. Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
21. Для определения концентрации серной кислоты к её раствору добавляли хлорид бария до прекращения выпадения осадка. Для взаимодействия с 20 г раствора кислоты потребовалось 52 г 10-процентного раствора хлорида бария. Определите массовую долю серной кислоты в исходном растворе.
22. Даны вещества: Cu, NaOH, HCl, AgNO3, MgSO4.
Используя воду и необходимые вещества только из этого списка, получите в две стадии гидроксид меди (II).
Запишите уравнения проведённых химических реакций. Опишите признаки этих реакций. Для реакции ионного обмена напишите сокращённое ионное уравнение реакции.
Демоверсия ОГЭ по химии 2018 год (ГИА 9 класс)
На официальном сайте ФИПИ опубликованы проекты демоверсии ОГЭ 2018 года по химии (ГИА 9 класс).
Максимальное количество баллов, которое может получить экзаменуемый за выполнение всей экзаменационной работы, – 34/38 баллов.
Результаты экзамена ОГЭ по химии в 9 классе могут быть использованы при приеме обучающихся в профильные классы средней школы.
Ориентиром при отборе в профильные классы может быть показатель, нижняя граница которого соответствует 25 баллам.
Демоверсия ОГЭ по химии 2018 год (9 класс) от ФИПИ
Продолжительность ОГЭ по химии— 120/140 минут
На выполнение экзаменационной работы в соответствии с моделью 1 отводится 120 минут; в соответствии с моделью 2 – 140 минут (на лабораторную работу (задание 23) дополнительно выделяется 20 минут).
Примерное время, отводимое на выполнение отдельных заданий, составляет:
1) для каждого задания части 1 – 3–8 минуты;
2) для каждого задания части 2 – 12–17 минут;
Изменения в КИМ 2018 года по сравнению с КИМ 2017 года — отсутствуют
Максимальный первичный балл – 34/38.
Каждый вариант экзаменационной работы состоит из двух частей.
Часть 1 содержит 19 заданий с кратким ответом, в их числе 15 заданий базового уровня сложности (порядковые номера этих заданий: 1, 2, 3, 4, …15) и 4 задания повышенного уровня сложности (порядковые номера этих заданий: 16, 17, 18, 19). При всем своем различии задания этой части сходны в том, что ответ к каждому из них записывается кратко в виде одной цифры или последовательности цифр (двух или трех). Последовательность цифр записывается в бланк ответов без пробелов и других дополнительных символов.
Часть 2 в зависимости от модели КИМ содержит 3 или 4 задания высокого уровня сложности, с развернутым ответом. Различие экзаменационных моделей 1 и 2 состоит в содержании и подходах к выполнению последних заданий экзаменационных вариантов:
• экзаменационная модель 1 содержит задание 22, предусматривающее выполнение «мысленного эксперимента»;
• экзаменационная модель 2 содержит задания 22 и 23, предусматривающие выполнение лабораторной работы (реального химического эксперимента).
Задания расположены по принципу постепенного нарастания уровня их сложности. Доля заданий базового, повышенного и высокого уровней сложности составила в работе 68, 18 и 14% соответственно.
Условия проведения ОГЭ по химии в 9 классе
При проведении экзамена по модели 1 в аудиторию не допускаются специалисты по химии. При проведении ОГЭ по химии по модели 2 подготовку и выдачу лабораторных комплектов осуществляют специалисты.
Для оценки проведения химического эксперимента, предусмотренного моделью 2, в аудиторию должны обязательно приглашаться эксперты.
Дополнительные материалы и оборудование
Перечень дополнительных материалов и оборудования, пользование которыми разрешено на ОГЭ, утвержден приказом Минобрнауки России. На экзамене по химии разрешается использовать следующие материалы и оборудование:
– Периодическая система химических элементов Д.И. Менделеева;
– таблица растворимости солей, кислот и оснований в воде;
– электрохимический ряд напряжений металлов;
– непрограммируемый калькулятор.
Проведение лабораторной работы в соответствии с экзаменационной моделью 2 осуществляется в специально помещении – химической лаборатории, оборудование которой должно отвечать требованиям СанПиН.
Смотрите также:
Я решу ЕГЭ : Тесты ОГЭ по химии в 2019
ОГЭ по химии сдается только по выбору ученика, это испытание не входит в перечень обязательных. Выбирают химию ученики, которые после 9-го класса планируют поступать в профильный 10-й класс школы или специализированный колледж, техникум. Для поступления в медицинское училище требуется сдавать не только химию, но и биологию. Экзамен подразумевает ориентацию в теории, успешное применение ее на практике. Испытуемому необходимо решить немало заданий разных уровней сложности из широкого спектра тем. Чтобы определиться в том, на какие темы обратить внимание, ознакомьтесь с Программой подготовки в ОГЭ по химии.
Экзамен состоит из заданий, который делятся на два логических блока:
- В первую часть входят задания на знание теории: здесь нужно дать краткий ответ – цифра, последовательность чисел, слово.
- Во второй части – несколько вопросов, на которые нужно дать развернутые, полные ответы, провести лабораторный эксперимент, написать заключения, выполнить расчеты. Крайне важно умение пользоваться специальным оборудованием, использовать алгоритмы решения задач разного уровня сложности.
На экзамене у испытуемого есть подсказки: таблицы растворимости солей, кислот, оснований в воде, периодическая таблица Менделеева, таблицы напряжений металлов. При условии умения пользоваться этими материалами, можно решить многие задания без трудностей.
- Главный совет, актуальный на каждом экзамене – планируйте свое обучение. Без четкого плана вы не сможете достичь высокого уровня подготовки. Чтобы планирование было максимально эффективным, ознакомьтесь с Программой подготовки – в ней указаны темы и разделы, на которые нужно обратить особое внимание.
- Оцените свои силы: наиболее простой способ – онлайн тестирование. По факту прохождения теста, вы получаете результат, и можете оценить – какие типы заданий и темы вызывают у вас наибольшие трудности.
- Когда вы определили проблемные темы, уделите им большее внимание, чем остальным. Для обучения возьмите учебники, справочники.
- Обязательно решайте задачи! Чем больше задач вы решите для подготовки, тем проще будет на экзамене.
- Задавайте вопросы: найдите специалиста, который сможет вам помочь в проблемных ситуациях. Это может быть репетитор или школьный учитель. Только специалист может помочь вам проанализировать свои ошибки и больше не совершать их.
- Научитесь пользоваться подсказками – теми таблицами, которые можно брать с собой на экзамен.
- Изучать теорию — мало, очень важно тренироваться выполнять тесты. Данная форма проверки знаний у многих вызывает трудности, особенно, если на уроках она не использовалась. Решайте больше тестовых заданий разных типов, чтобы на экзамене они не вызывали страха и непонимания.
- «Решу ОГЭ по химии» поможет вам подготовиться к экзамену и успешно сдать его, рационально используя отведенное время, без стресса.
Тренировочные варианты (2019 год)
Тренировочные варианты (2018 год)
Подготовка к ОГЭ (ГИА) по химии. Тематические тесты для подготовки к ОГЭ по химии.
Для кого предназначены эти тесты?
Данные материалы предназначены для школьников, готовящихся к ОГЭ-2018 по химии. Их также можно использовать для самоконтроля при изучении школьного курса химии. Каждый тест посвящен определенной теме, которая встретится девятикласснику на экзамене. Номер теста — это номер соответствующего задания в бланке ОГЭ.
Как устроены тематические тесты?
Каждый тренировочный тест состоит из 10 заданий различного уровня сложности. Задачи 1-5 наиболее легкие, подойдут для тех, кто начинает готовиться к ОГЭ по химии «с нуля». Задания 6-10 соответствуют уровню ГИА или немного сложнее.
Чем отличаются тематические тесты от «обычных» тестов ОГЭ?
«Обычные» тесты проверяют общий уровень знаний по химии. Каждый из тематических тестов посвящен только одной теме.
Полные варианты ОГЭ (например, этот или этот) целесообразно использовать для периодического самоконтроля в процессе подготовки к экзамену, тематические тесты — для работы над конкретными разделами программы по химии, которые вызывают наибольшие сложности.
Какое место занимают тематические тесты в подготовке к ОГЭ по химии?
Разумеется, данные тренировочные тесты нельзя рассматривать как замену школьного учебника химии. Прежде чем начинать работать над тестом, следует внимательно изучить соответствующую тему по учебнику или обратиться к помощи преподавателя. Тесты ничего не объясняют. Они лишь помогают вам лучше усвоить соответствующий материал и оценить уровень своей подготовки.
Как интерпретировать результаты тестов?
Если вы набираете 4-5 баллов в первой части и 4-5 баллов во второй, можете считать, что соответствующая тема усвоена вами отлично. Если во второй части вы сможете решить правильно 2-3 задания и 3-4 задания в первой части, советую еще немного потренироваться.
Если вы даже в I части делаете более трех ошибок, результат неудовлетворительный! Тренируйтесь! Попробуйте еще раз разобрать соответствующую тему. Если возникают сложности, обратитесь к помощи репетитора.
Будут ли на этом сайте публиковаться другие тематические тесты?
Безусловно! Я планирую разместить тесты по 23 темам, по 10 заданий в каждом. Следите за обновлениями!
Что еще есть на этом сайте для готовящихся к ОГЭ-2018 по химии?
Демонстрационные тесты ОГЭ и ЕГЭ и тесты по химии для школьников 8 — 11 классов. Статьи, посвященные решению сложных задач, и справочник по химии.Вам кажется, что чего-то не хватает? Вам хотелось бы расширить какие-то разделы? Нужны какие-то новые материалы? Что-то надо исправить? Нашли ошибки?
Пожалуйста, свяжитесь со мной.
Успехов всем готовящимся к ОГЭ и ЕГЭ!
У нас есть более 400+ вопросов по химии с темами, включающими ядерную химию, атомную структуру и химические связи, твердое состояние, химическую кинетику, химическую термодинамику и энергетику, растворы и коллигативные свойства, элементы D-блока, электрохимию, ионное равновесие и т. Д. Эти тесты полезны при подготовке конкурсных экзаменов, вступительных испытаний и собеседований.Ядерно-химический тест50 вопросов — Автор: Прити Чоудхари — 25 июля 2013 г. на 13:36 Атомный Тест на структуру и химическую связь25 вопросов — Автор: Прити Чоудхари — 26 июля, 2013 в 10:45 Химия твердого тела Тест25 вопросов — Автор: Прити Чоудхари — 27 июля, г. 2013 в 23:16 Тест химической кинетики50 вопросов — Автор: Прити Чоудхари — 28 июля 2013 г. на 14:05 Химическая промышленность термодинамика и энергетика Тест50 вопросов — Автор: Прити Чоудхари — 29 июля 2013 г. на 08:36 Решения и коллигативные свойства Тест50 вопросов — Автор: Прити Чоудхари — 30 июля 2013 г. на 12:55 Элементы блока D Тест50 вопросов — Автор: Прити Чоудхари — 31 июля 2013 г. на 07:16 Электрохимический тест50 вопросов — Автор: Прити Чоудхари — 1 августа 2013 г. в 18:36 Тест ионного равновесия50 вопросов — Автор: Прити Чоудхари — 2 августа 2013 г. в 22:36 |
Практический тест SAT Chemistry: Organic Chemistry_cracksat.net
1. Какой углеводород вступит в реакцию замещения с галогеном?
A. Пентин
B. Этен
C. Пропин
D. Бутан
E. Пропен
2. Какой тип органической реакции представлен уравнением C 3 H 6 + H 2 → С 3 H 8 ?
A. Дополнение
B. Замена
C.Конденсация
D. Полимеризация
E. Дегидратационный синтез
3. Когда аминогруппа одной аминокислоты вступает в реакцию с группой карбоновой кислоты другой аминокислоты, образовавшаяся функциональная группа называется
A. амин
B .. амид
C. сложный эфир
D. пластик
E. полимер
4. Какой из следующих полимеров является синтетическим?
A. Нуклеиновые кислоты
B. Пластик
C. Белки
D. Целлюлоза
E.Крахмал
5. Какие два соединения не являются изомерами друг друга?
A. н-пентан и 2-метилбутан
B. CH 3 CH 2 OH и CH 3 OCH 3
C. CH 3 COOH и CH 3 CH 2 COOH
D. CH 3 COCH 3 и CH 3 CH 2 CHO
E. CH 3 CH 2 CH 2 Cl и CH 3 CHClCH 3
6 , Карбонильная группа присутствует во всех этих функциональных группах, за исключением:
A. кетонов
B. альдегидов
C. сложных эфиров
D. амидов
E. простых эфиров
7. Органическое соединение имеет молекулярную формулу C3h5 , Какое соединение ниже
относится к тому же классу углеводородов?
A. C2H6
B. C3H6
C. C4H8
D. C2h3
E. Ch5
8. Какое утверждение неверно?
A. CH 3 CH 2 NH 2 — этанамин.
B. CH 3 CHBrCHBrCH 3 — 2,3-дибромбутан.
C. CH 3 CH 2 OH представляет собой эфир.
D. Циклопентан и 2-пентен имеют молекулярную формулу C 5 H 10 .
E. Алкены и алкины ненасыщенные.

Leave A Comment