Медицинский колледж «Семей» — Колледж осуществляет образовательную деятельность
Несколько слов о нашем колледже
Миссия Учреждения Медицинский колледж «Семей».
Миссия и Видение колледжа, представлящая собой смысл его деятельности, направленной на конечный результат, декларирующая статус колледжа, принципы работы и намерения руководства.
Миссия колледжа: Создание условий для развития человеческого капитала страны и региона через внедрение образовательных программ базовой подготовки кадров здравоохранения на основе интегрированной модели, с применением компетентного подхода и профессиональных стандартов.
Уникальность колледжа будет заключаться в создании эффективной модели практикоориентированного профессионального медицинского образования, через поэтапное расширение компетенций среднего медицинского персонала параллельно с изменением стандартов их образования и переподготовки.
Видение колледжа: Учреждение «Медицинский колледж «Семей» – колледж инновационного типа, признанный в мировом образовательном пространстве, как лучший медицинский колледж Восточно-Казахстанской области.
Анализ миссии колледжа позволяет выделить важные элементы:
- Сфера деятельности — подготовка высококвалифицированных специалистов с учетом расширения компетенций среднего медицинского персонала.
- Главный результат деятельности колледжа удовлетволять потребности рынка труда.
В ХХ веке, в условиях плановой экономики гарантом карьерного развития выпускника выступало государство. В условиях рыночной экономики все экономические риски карьерного развития принимают на себя сами выпускники. Именно поэтому колледж ставит своей целью подготовку специалистов с высокой степенью адаптивности и социализации, способных действовать максимально эффективно в условиях быстроизменяющегося мира.
- Сфера присутствия учреждения — Учреждение «Медицинский колледж «Семей» Восточно-Казахсанская область
Поскольку колледж определил для себя сферой влияния прежде всего, Восточно-Казахстанскую область, то при определении миссии руководством колледжа учитывались потребности и особенности развития региона.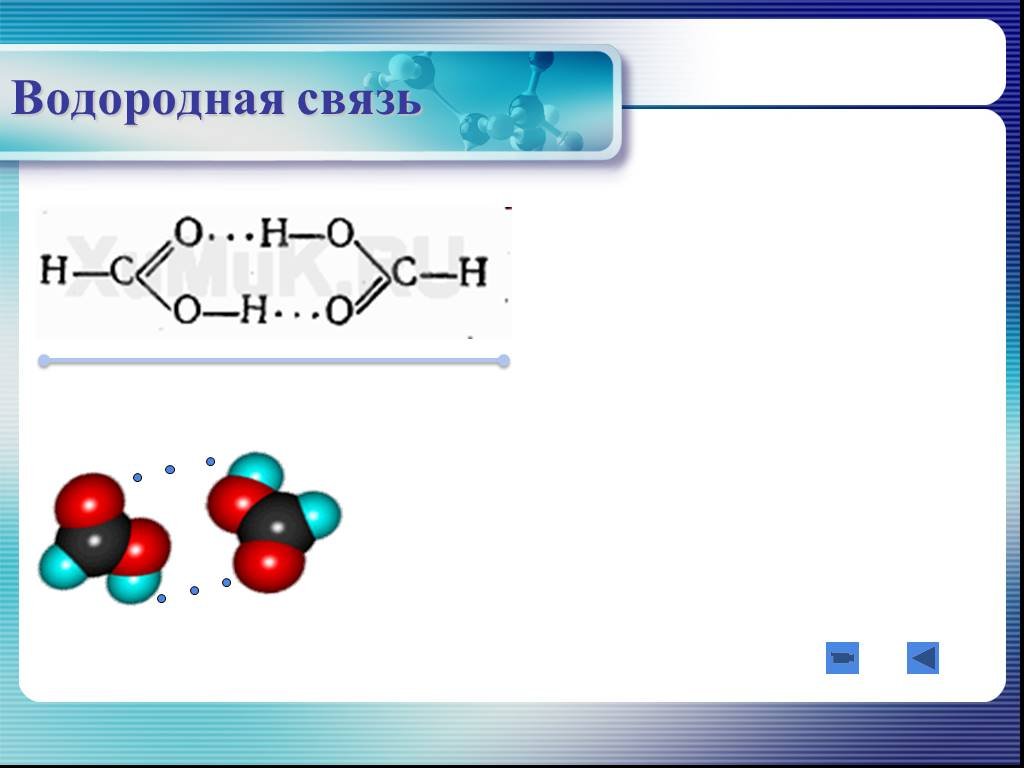
- Каким интересам служит – создание условий для развития человеческого капитала страны и региона, организация рабочих мест, уменьшение количества безработных.
5.Реализуя свою миссию, определяет стратегические приоритеты в своей деятельности, обеспечивающие устойчивое развитие в перспективе и в текущих целях. Эти приоритеты и стратегические цели являются концептуальной основой при разработке ежегодно разрабатываемых планов работы колледжа на учебный год.
Стратегия колледжа направлена на реализацию задач Государственной программы развития образования Республики Казахстан на 2016-2019 годы, Государственной программы развития здравоохранения РК «Денсалық» на 2016-2019 годы;
На основании миссии и видения определена стратегическая цель деятельности колледжа: Обеспечение качества профессиональной подготовки специалистов, востребованных на рынке труда, на основе внедрения новых подходов в преподавании и обучении.
Приоритетными направлениями развития являются:
- обеспечение качества профессионального образования на основе его фундаментальности и соответствия актуальным и перспективным потребностям личности, общества и государства;
- подготовка кадров в соответствии с реальными потребностями рынка труда региона;
- развитие образовательной среды, обеспечивающей доступность, качество и эффективность;
- совершенствование системы управления колледжем;
- развитие и реализация потенциала молодежи в интересах страны;
- внедрение современных технологий, образовательных программ;
- развитие дуальной и модульной систем обучения.

Данные приоритеты согласуются с приоритетами развития здравоохранения РК. Основные направления и перспективы развития на 5 лет заложены в Стратегическом плане развития Учреждения «Медицинский колледж «Семей» на 2017-2022 годы.
При определении стратегических приоритетов и целей развития УМКС были использованы следующие документы стратегического характера, отражающие общую линию государства в развитии профессионального образования и его роли в обществе:
- Послание Главы государства народу Казахстана от 17.01.2014 года «Казахстанский путь — 2050: единая цель, единые интересы, единое будущее»;
- Послание Главы государства народу Казахстана от 11.2014 года «Нұрлы жол – путь в будущее»;
- Статья Главы государства «Взгляд в будущее: модернизация общественного сознания» от 12.04.2017 г.;
- Закон Республики Казахстан «Об образовании» от 27 июля 2007 года;
- Стратегический план развития РК до 2020 года;
- Государственная программа развития образования Республики Казахстан на 2016-2019 годы;
- Государственная программа развития здравоохранения РК «Денсаулық» на 2016-2019 годы;
Таким образом, миссия, видение и стратегия отображают его место в образовательном пространстве Казахстана, согласованность с национальными приоритетами, направленность на удовлетворение потребностей заинтересованных сторон, а также уникальность и индивидуальность стратегии колледжа.
Стратегические направления:
- обеспечение высокого уровня подготовки специалистов в условиях реализации Государственной программы развития здравоохранения РК «Денсаулық» на 2016-2019 годы;
- подготовка кадров с учетом потребности рынка труда;
- внедрение инновационных технологий обучения: дуальной системы, модульных программ;
- расширение социального партнерства, тесное взаимодействие с работодателями по формированию траектории учебного процесса, их запросов и потребностей в вопросах подготовки кадров.
- «Система контроля за исполнением программы развития»
В стратегический план развития колледжа на 2017-2022 годы включен раздел «Система контроля за исполнением программы развития», согласно которому колледж планирует и периодически пересматривает выполнении миссии, целей и задач, вопросов стратегического планирования, решений на заседаниях педагогического совета и в рамках работы методического совета колледжа.
Одной из основных функций колледжа, определенных законами и нормативными актами, является обеспечение качества профессионального образования, которое зависит от организации методической работы с инженерно — педагогическими кадрами.
Учебно-методическая работа колледжа — это одно из определяющих направлений работы педагогического коллектива колледжа. УМР осуществляется в соответствии с Правилами организации и осуществления учебно-методической работы в техническом и профессиональном образовании, утвержденным приказом Министра образования и науки РК (№ 583 от 29 ноября 2007 года) и на основе ежегодных планов учебно-методической работы колледжа.
I Базовые компетенции
- Понимать сущность подготовки высококвалифицированных специалистов с учетом расширения компетенции среднего медицинского персонала.
- Быть готовым к реальным потребностям рынка труда региона и проявлению ответственности за выполняемую работу, способным самостоятельно и эффективно решать проблемы в области профессиональной деятельности.
- Быть готовым к проявлению создания эффективной модели практикоориентированного профессионального медицинского образования.
II Личностные компетенции
- Личность с развитым интеллектом в реализации потенциала молодежи в интересах страны.

- Личность адаптированная к жизни в динамичных социально- экономических условиях.
- Конкурентноспособная личность, сочетающая высокую нравственность с чувством профессиональности за качество и результат своего труда.
- Личность способная к здоровому образу жизни.
III Профессиональные компетенции
- Применять знания в области здравоохранения на основе интегрированной модели, с применением компетентного подхода и профессиональных стандартов.
- Соблюдать правила трудовой дисциплины и обеспечение качества профессионального стандарта на основе его фундаментальности и соответствия актуальным и перспективным потребностям личности, общества и государства.
- Самостоятельно определять задачи профессионального и личностного развития, заниматься самообразованием, осознанно планировать и осуществлять повышение квалификации.
IV Информационные компетенции
- Способность ориентироваться в информационном потоке: умение находить и систематизировать различные источники информации по определенному критерию, внедряемыми современными технологиями.

- Осуществлять поиски и использование информации, необходимой для эффективного выполнения профессиональных задач, профессионального и личностного развития.
V Коммуникативные компетенции
- Знание особенностей профессиональной этики и понимание ценности сотруднических взаимоотношений.
- Имеет реалистические представления по отношению к себе и другим людям, высокие духовные эстетические и культурные ценности, умеет отстаивать свои идеи и убеждения.
- Владеет коммуникативными навыками.
Государственные услуги и информация онлайн
Министерство здравоохранения Республики Казахстан | Официальный Интернет-ресурс
Информационно-правовая система нормативных правовых актов РК
Министерство образования и науки Республики Казахстан
Официальный сайт Президента Республики Казахстан
Для наших студентов
«ПРАВА И ОБЯЗАННОСТИ СТУДЕНТОВ МЕДИЦИНСКОГО КОЛЛЕДЖА «СЕМЕЙ»
Права и обязанности учащегося:— Овладевать знаниями, умениями и практическими навыками в полном объеме государственных образовательных стандартов образования.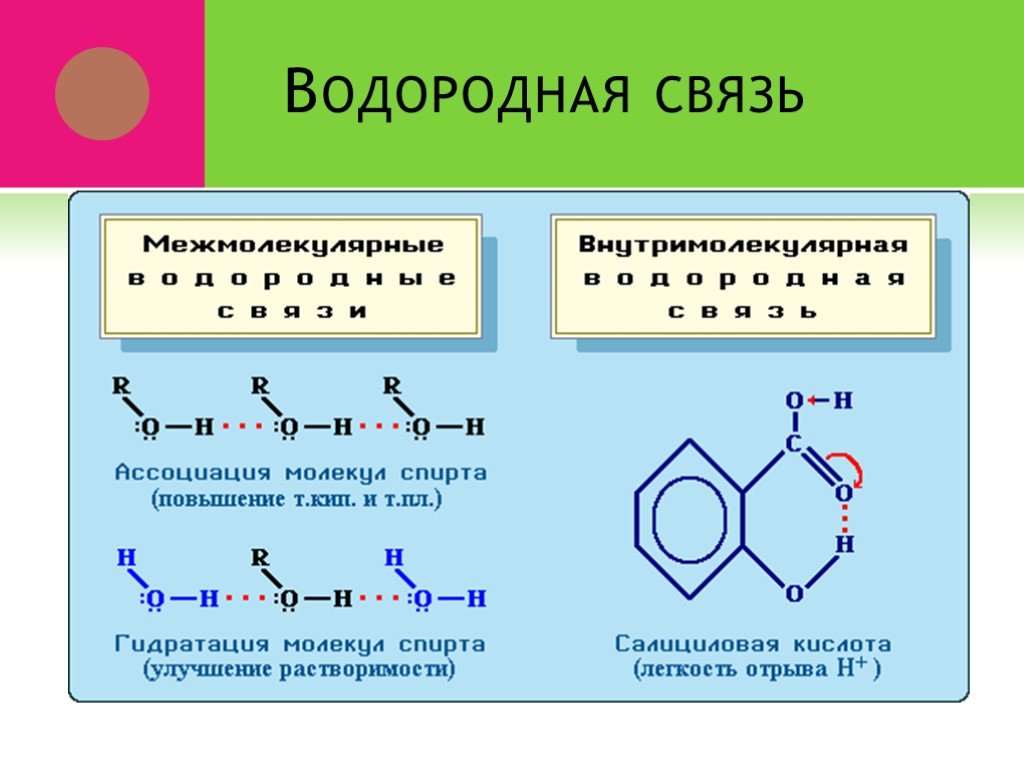 Выполнять учебную программу в соответствии с учебным планом и графиком учебного процесса Колледжа.
Выполнять учебную программу в соответствии с учебным планом и графиком учебного процесса Колледжа.
— Исполнять соответствующие приказы, инструкции и распоряжения Министерства образования и науки РК, приказы и распоряжения Директора Колледжа, распоряжения заместителя директора по учебной и воспитательной работе.
— Своевременно перечислять на счет Колледжа деньги за обучение в порядке, предусмотренном договором.
— Участвовать в коллективном договоре с Колледжем о материальной ответственности закрепленной аудитории и нести ответственность за порчу имущества Колледжа в полном его объеме.
— В случае пропуска учебных занятий по болезни предоставить Колледжу соответствующий документ.
— Отработать 50 (пятьдесят) часов за один академический год на общественно-полезных работах по распоряжениям Правительства РК, акиматов города Семей и области, администрации Колледжа.
— Организация дополнительных занятий, консультаций, зачетов и экзаменов, в целях ликвидации задолженностей, образовавшихся по вине Учащегося, оплачивается им дополнительно, в соответствии с понесенными затратами Колледжа.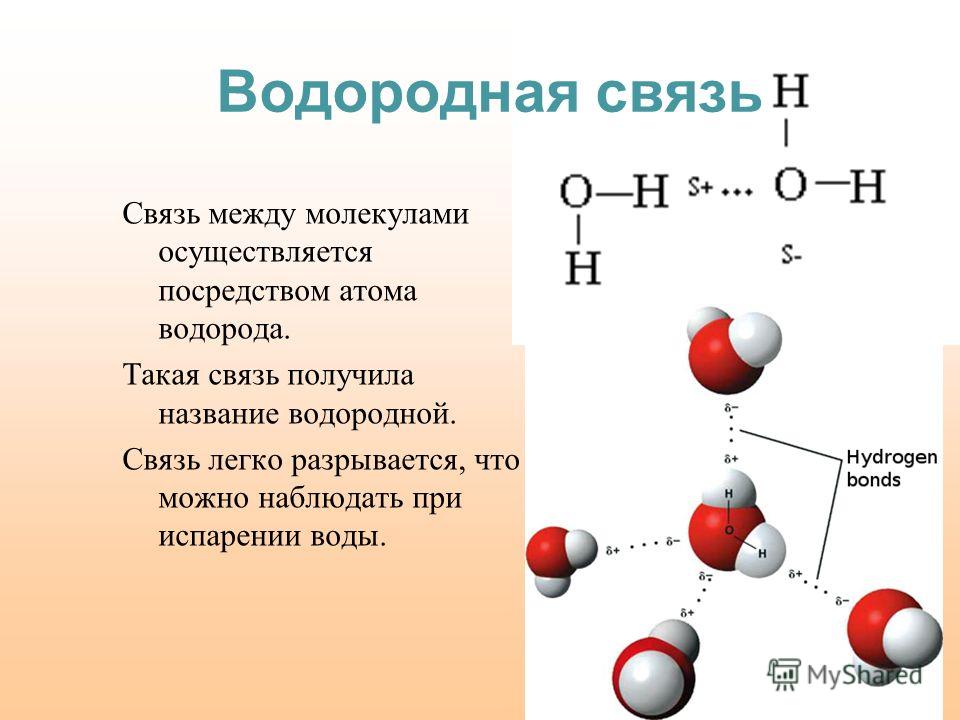
— В случае перевода Студента из другого учебного заведения, устанавливается дополнительная оплата для возмещения затрат, связанных со сдачей разницы в предметах.
— При отчислении Студента из Колледжа за неуспеваемость, нарушения правил учебной дисциплины, аморальные поступки оплаченная сумма за обучение возврату не подлежит.
— В случае отчисления Студента из Колледжа по причине неуплаты за обучение академическая справка не выдается до полного погашения задолженности по оплате.
— В случае отчисления Студента из Колледжа по собственному желанию документы не выдаются до полного погашения задолженности по оплате.
— Диплом об окончании Колледжа не выдается до полного погашения задолженности по оплате за истекший срок обучения.
— В случае неоплаты за обучение, учащийся не допускается к экзаменационной сессии и отчисляется из учебного заведения.
— За нарушение обязанностей, предусмотренных Уставом «Колледжа», Договором, за нарушение правил внутреннего распорядка, Учащемуся могут быть применены следующие меры дисциплинарного воздействия:

В помещениях Колледжа запрещаются:

Колледж имеет право:
Для наших студентов
Устав колледжа
250 тысяч
численность медицинских кадров в Казахстане
100 %
трудоустройство ждёт отличников учёбы
35
дипломами и грамотами награждён колледж «Семей»
7 лет
мы выпускаем прекрасных специалистов
Кузница медицинских кадров.
404 Cтраница не найдена
Мы используем файлы cookies для улучшения работы сайта МГТУ и большего удобства его использования. Более подробную информацию об использовании файлов cookies можно найти здесь. Продолжая пользоваться сайтом, вы подтверждаете, что были проинформированы об использовании файлов cookies сайтом ФГБОУ ВО «МГТУ» и согласны с нашими правилами обработки персональных данных.
Размер:
AAA
Изображения Вкл. Выкл.
Обычная версия сайта
К сожалению запрашиваемая страница не найдена.
Но вы можете воспользоваться поиском или картой сайта ниже
|
|
Водородная связь — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 1230
- Уильям Ройш
- Университет штата Мичиган
Наиболее мощной межмолекулярной силой, влияющей на нейтральные (незаряженные) молекулы, является водородная связь. Если мы сравним точки кипения метана (CH 4 ) -161ºC, аммиака (NH 3 ) -33ºC, воды (H 2 O) 100ºC и фтористого водорода (HF) 19ºC, мы увидим больший разброс для эти молекулы аналогичного размера, чем ожидалось из данных, представленных выше для полярных соединений. Это показано графически на следующей диаграмме. Большинство простых гидридов элементов групп IV, V, VI и VII демонстрируют ожидаемое повышение температуры кипения с увеличением молекулярной массы, но гидриды наиболее электроотрицательных элементов (азота, кислорода и фтора) имеют аномально высокие температуры кипения для своей массы.
Если мы сравним точки кипения метана (CH 4 ) -161ºC, аммиака (NH 3 ) -33ºC, воды (H 2 O) 100ºC и фтористого водорода (HF) 19ºC, мы увидим больший разброс для эти молекулы аналогичного размера, чем ожидалось из данных, представленных выше для полярных соединений. Это показано графически на следующей диаграмме. Большинство простых гидридов элементов групп IV, V, VI и VII демонстрируют ожидаемое повышение температуры кипения с увеличением молекулярной массы, но гидриды наиболее электроотрицательных элементов (азота, кислорода и фтора) имеют аномально высокие температуры кипения для своей массы.
Исключительно сильное диполь-дипольное притяжение, вызывающее такое поведение, называется водородной связью . Водород образует полярные ковалентные связи с более электроотрицательными атомами, такими как кислород, и, поскольку атом водорода довольно мал, положительный конец диполя связи (водород) может приближаться к соседним нуклеофильным или основным центрам ближе, чем другие полярные связи.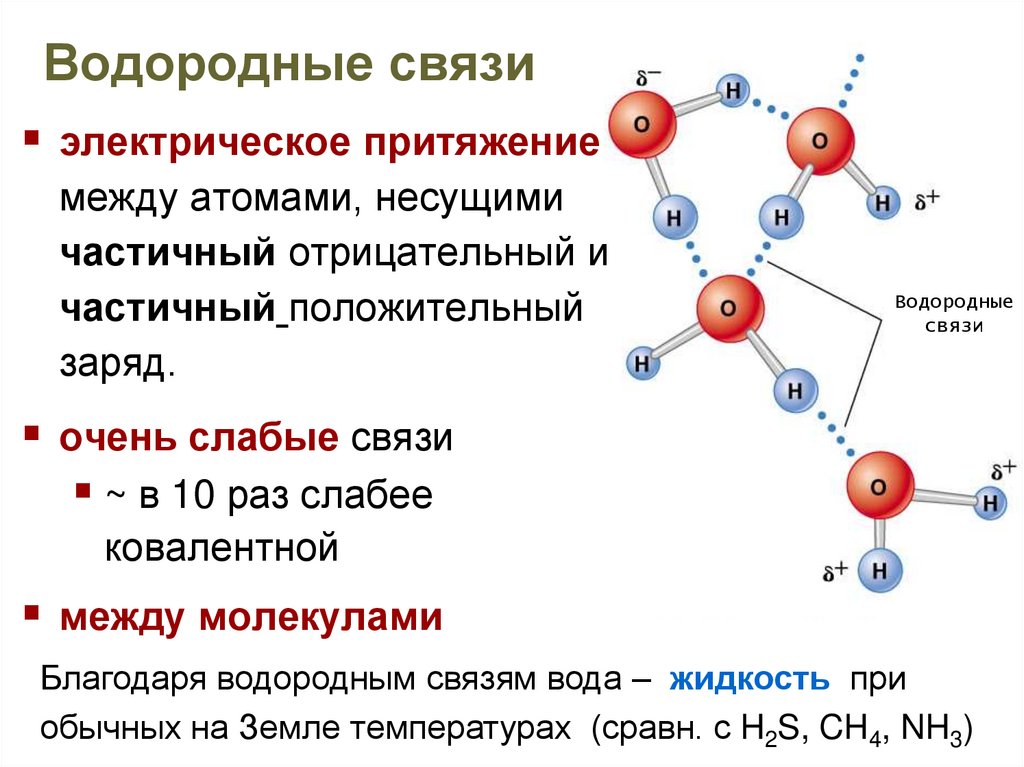 Кулоновские силы обратно пропорциональны шестой степени расстояния между диполями, что делает эти взаимодействия относительно сильными, хотя и слабыми (9).0044 ок. от 4 до 5 ккал на моль) по сравнению с большинством ковалентных связей. Уникальные свойства воды во многом обусловлены прочными водородными связями, возникающими между ее молекулами. На следующей диаграмме водородные связи изображены пурпурными пунктирными линиями.
Кулоновские силы обратно пропорциональны шестой степени расстояния между диполями, что делает эти взаимодействия относительно сильными, хотя и слабыми (9).0044 ок. от 4 до 5 ккал на моль) по сравнению с большинством ковалентных связей. Уникальные свойства воды во многом обусловлены прочными водородными связями, возникающими между ее молекулами. На следующей диаграмме водородные связи изображены пурпурными пунктирными линиями.
Молекула, обеспечивающая полярный водород для водородной связи, называется донором . Молекула, которая обеспечивает богатый электронами участок, к которому притягивается водород, называется акцептором 9.0043 . Вода и спирты могут служить как донорами, так и акцепторами, тогда как простые эфиры, альдегиды, кетоны и сложные эфиры могут действовать только как акцепторы. Точно так же первичные и вторичные амины являются как донорами, так и акцепторами, а третичные амины функционируют только как акцепторы. Как только вы научитесь распознавать соединения, которые могут образовывать межмолекулярные водородные связи, станет понятным их относительно высокая температура кипения. Данные в следующей таблице иллюстрируют этот момент.
Данные в следующей таблице иллюстрируют этот момент.
| Соединение | Формула | Мол. Вес. | Точка кипения | Точка плавления |
|---|---|---|---|---|
| диметиловый эфир | СН 3 ОСН 3 | 46 | –24°С | –138°С |
| этанол | СН 3 СН 2 ОН | 46 | 78°С | –130°С |
| пропанол | СН 3 (СН 2 ) 2 ОН | Wt.»> 60 | 98°С | –127°С |
| диэтиловый эфир | (СН 3 СН 2 ) 2 О | 74 | 34°С | –116°С |
| пропиламин | CH 3 (CH 2 ) 2 NH 2 | 59 | 48ºC | –83°С |
| метиламиноэтан | СН 3 СН 2 NHCH 3 | Wt.»> 59 | 37°С | |
| триметиламин | (CH 3 ) 3 N | 59 | 3ºC | –117°С |
| этиленгликоль | НОСН 2 СН 2 ОН | 62 | 197°С | –13°С |
| уксусная кислота | CH 3 CO 2 H | 60 | 118°С | 17ºC |
| этилендиамин | H 2 NCH 2 CH 2 NH 2 | Wt.»> 60 | 118°С | 8,5ºC |
Спирты кипят значительно выше, чем сравнимые по размеру простые эфиры (первые два пункта), а изомерные 1º, 2º и 3º-амины, соответственно, демонстрируют пониженные температуры кипения, при этом два изомера с водородными связями имеют значительно более высокую температуру кипения, чем 3º-амин (записи 5-7). Кроме того, водородные связи O-H—O явно прочнее, чем водородные связи N-H—N, как мы видим, сравнивая пропанол с аминами.
Как и ожидалось, наличие двух групп водородных связей в соединении еще больше повышает температуру кипения. Уксусная кислота (девятая запись) — интересный случай. Димерные частицы, показанные справа, удерживаемые вместе двумя водородными связями, являются основным компонентом жидкого состояния. Если это точное представление состава этого соединения, то можно ожидать, что его точка кипения будет эквивалентна температуре кипения соединения C 4 H 8 O 4 (масса формулы = 120).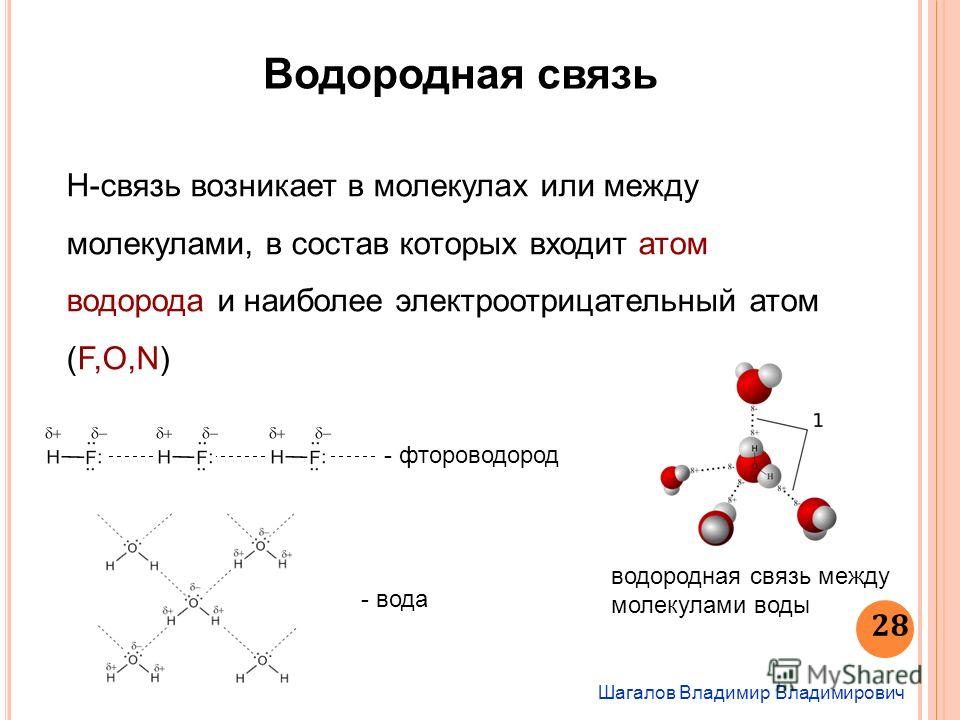 Подходящим приближением такого соединения является тетраметоксиметан (CH 3 O) 4 C, который на самом деле немного больше (масса формулы = 136) и имеет температуру кипения 114ºC. Таким образом, димерная структура с водородными связями, по-видимому, является хорошим представлением уксусной кислоты в конденсированном состоянии.
Подходящим приближением такого соединения является тетраметоксиметан (CH 3 O) 4 C, который на самом деле немного больше (масса формулы = 136) и имеет температуру кипения 114ºC. Таким образом, димерная структура с водородными связями, по-видимому, является хорошим представлением уксусной кислоты в конденсированном состоянии.
В этом месте стоит отметить родственный принцип. Хотя водородная связь относительно слабая ( ок. от 4 до 5 ккал на моль), когда существует несколько таких связей, результирующая структура может быть довольно прочной. Водородные связи между волокнами целлюлозы придают большую прочность древесине и связанным с ней материалам. Для получения дополнительной информации по этому вопросу нажмите здесь.
Авторы
- Уильям Ройш, почетный профессор (штат Мичиган, Университет штата Мичиган), Виртуальный учебник органической химии
Эта страница под названием Hydrogen Bonding публикуется в соответствии с лицензией CC BY-NC-SA 4. 0, ее автором, ремиксом и/или куратором выступил Уильям Ройш.
0, ее автором, ремиксом и/или куратором выступил Уильям Ройш.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- Уильям Ройш
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.
- Теги

Уксусная кислота – Полное руководство
Определение
Уксусная кислота представляет собой монокарбоновую кислоту со слабой коррозионной активностью. Это органическое соединение, также известное как этановая кислота, метанкарбоновая кислота, гидроацетат или этиловая кислота, используется в химическом производстве, в качестве пищевой добавки и в нефтедобыче. Молекулярная формула уксусной кислоты C 2 H 4 O 2 или CH 3 COOH, где –COOH определяет наличие одной карбоксильной группы.
Уксус: раствор уксусной кислотыСтруктура уксусной кислоты
Структура уксусной кислоты аналогична структуре простой карбоновой кислоты и состоит из метильной группы, присоединенной к карбоксильной группе, как показано на изображении ниже. Уксусная кислота или этановая кислота являются протонными растворителями; способен отдавать протоны в виде гидронов (положительно заряженных атомов водорода). Эта характеристика означает, что он является членом группы кислот Бренстеда, где протоны отдаются акцепторным молекулам, известным как основания Бренстеда. Пожертвованный водород диссоциирует от карбоксильной группы. Уксус представляет собой раствор уксусной кислоты и воды, в котором примерно 0,4% молекул уксусной кислоты отдают свои H + атомов, что приводит к кислому раствору примерно с рН 2,4. По сравнению с самой сильной кислотой в мире — карбоновой кислотой (H(CHB 11 Cl 11 )) — со значением pH -18, уксусная кислота по сравнению с ней является слабокислой.
Эта характеристика означает, что он является членом группы кислот Бренстеда, где протоны отдаются акцепторным молекулам, известным как основания Бренстеда. Пожертвованный водород диссоциирует от карбоксильной группы. Уксус представляет собой раствор уксусной кислоты и воды, в котором примерно 0,4% молекул уксусной кислоты отдают свои H + атомов, что приводит к кислому раствору примерно с рН 2,4. По сравнению с самой сильной кислотой в мире — карбоновой кислотой (H(CHB 11 Cl 11 )) — со значением pH -18, уксусная кислота по сравнению с ней является слабокислой.
Следует пояснить, что не присутствие одного атома водорода изменяет рН раствора . Нейтральные растворы (ни кислые, ни щелочные) содержат сбалансированное количество ионов гидроксония (H 3 0 + ) и ионы гидроксила (OH – ). Две молекулы воды (H 2 0) образуются, когда ион гидроксония и гидроксил связываются, а положительный и отрицательный заряды уравновешиваются. При добавлении уксусной кислоты к воде она распадается на отрицательно заряженный ацетат-ион (CH 3 COO – ) и H + . Отсюда можно понять альтернативное название уксусной кислоты – ацетат водорода. Небольшой процент положительно заряженных ионов водорода связывается с молекулами воды и превращает их в H 3 0 + . Это означает, что ионов гидроксония больше и, следовательно, создается положительно заряженный (или кислый) раствор. Таким образом, рН раствора зависит от баланса гидроксония и гидроксила, а не от количества ионов водорода, хотя они будут влиять на этот баланс. Значение pH также дается только раствору. Раствор всегда содержит воду; даже современные суперкислоты, такие как карборан, растворяются в концентрированных водных растворах других кислот. Даже в ледяной уксусной кислоте содержится небольшое количество воды.
При добавлении уксусной кислоты к воде она распадается на отрицательно заряженный ацетат-ион (CH 3 COO – ) и H + . Отсюда можно понять альтернативное название уксусной кислоты – ацетат водорода. Небольшой процент положительно заряженных ионов водорода связывается с молекулами воды и превращает их в H 3 0 + . Это означает, что ионов гидроксония больше и, следовательно, создается положительно заряженный (или кислый) раствор. Таким образом, рН раствора зависит от баланса гидроксония и гидроксила, а не от количества ионов водорода, хотя они будут влиять на этот баланс. Значение pH также дается только раствору. Раствор всегда содержит воду; даже современные суперкислоты, такие как карборан, растворяются в концентрированных водных растворах других кислот. Даже в ледяной уксусной кислоте содержится небольшое количество воды.
На следующем изображении показана диссоциация уксусной кислоты до ацетата в воде. Слева одна молекула уксусной кислоты и одна молекула воды. Уксусная кислота передает ион водорода молекуле воды с образованием иона гидроксония. Мы говорим, что молекула воды протонирована или ей был передан протон (гидрон).
Уксусная кислота передает ион водорода молекуле воды с образованием иона гидроксония. Мы говорим, что молекула воды протонирована или ей был передан протон (гидрон).
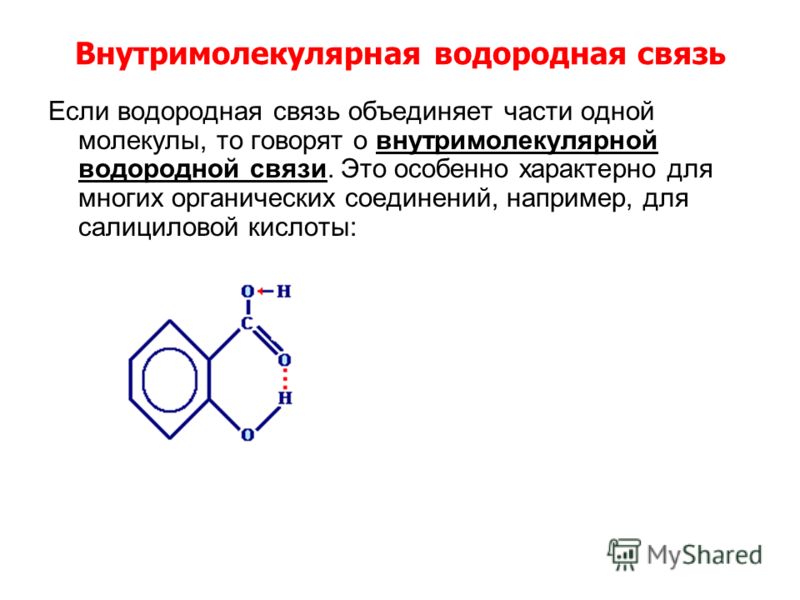
В качестве растворителя жидкая уксусная кислота растворяет полярные (гидрофильные) соединения, такие как соли и сахара, а также неполярные соединения, включающие жиры и масла. Это означает, что он имеет множество применений в промышленном химическом производстве, но также имеет приобрел репутацию добавки для похудения , так как он влияет на жировой и сахарный обмен. Более подробная информация об использовании уксусной кислоты будет обсуждаться далее в этой статье. В кристаллической форме две молекулы уксусной кислоты соединяются водородными связями, образуя димер. При добавлении воды эти связи разрываются, и кристаллическая форма растворяется.
Димер уксусной кислотыФормула уксусной кислоты
Формула уксусной кислоты проста и состоит из метильной и карбоксильной групп. Метильные группы являются одними из самых распространенных органических соединений на планете, но редко встречаются в виде отдельных образований. Они состоят из трех атомов водорода и одного атома углерода (CH 3 ). Поскольку углерод имеет четыре электрона, свободный электрон обычно связывается с другими молекулами посредством ковалентной связи. Простейшей молекулой углерода является метан (CH 4 ), хорошо известный своим вкладом в глобальное потепление. Со свободным электроном метан реагирует с озоном (O 3 ) с образованием углекислого газа и воды в следующей реакции: (3)CH 4 + (4)O 3 = (3)CO 2 + (6)H 2 O. На рисунке показана молекула метана, состоящая из метильной группы и дополнительного атома водорода.
Метильные группы являются одними из самых распространенных органических соединений на планете, но редко встречаются в виде отдельных образований. Они состоят из трех атомов водорода и одного атома углерода (CH 3 ). Поскольку углерод имеет четыре электрона, свободный электрон обычно связывается с другими молекулами посредством ковалентной связи. Простейшей молекулой углерода является метан (CH 4 ), хорошо известный своим вкладом в глобальное потепление. Со свободным электроном метан реагирует с озоном (O 3 ) с образованием углекислого газа и воды в следующей реакции: (3)CH 4 + (4)O 3 = (3)CO 2 + (6)H 2 O. На рисунке показана молекула метана, состоящая из метильной группы и дополнительного атома водорода.
В случае уксусной кислоты свободный электрон связывается с карбоксильной группой (CO 2 H, -COOH или -C(=O)OH), которая представляет собой один атом углерода, связанный с гидроксильной группой (- ОН) и двойной связью с атомом кислорода. На изображении ниже показана карбоксильная группа, где R представляет собой остальную часть молекулы, к которой присоединена карбоксильная группа; буква R иногда заменяется волнистой линией. В случае уксусной кислоты R представляет собой метильную группу. Некоторые предпочитают описывать карбоксильную группу как комбинацию карбонильной группы (С=0, где = означает двойную связь) и гидроксильной группы (ОН). Карбоновые кислоты входят в состав аминокислот и необходимы каждому живому организму.
На изображении ниже показана карбоксильная группа, где R представляет собой остальную часть молекулы, к которой присоединена карбоксильная группа; буква R иногда заменяется волнистой линией. В случае уксусной кислоты R представляет собой метильную группу. Некоторые предпочитают описывать карбоксильную группу как комбинацию карбонильной группы (С=0, где = означает двойную связь) и гидроксильной группы (ОН). Карбоновые кислоты входят в состав аминокислот и необходимы каждому живому организму.
Существует общая молекулярная формула для всех карбоновых кислот, а именно C n H 2n + 1 COOH. Это означает, что каждая карбоновая кислота содержит в два раза больше атомов водорода, чем атомов углерода, после удаления карбоксильной группы ; формула, идеально сочетающаяся с формулой уксусной кислоты – C2h5O2. Когда вы удаляете карбоксильную группу из этой формулы уксусной кислоты, у вас остается один атом углерода и два атома водорода.
Факты об уксусной кислоте
Факты об уксусной кислоте для тех, кто хочет узнать немного больше!
Молярная масса уксусной кислоты составляет 60,052 грамма на моль (г/моль). Молярная масса — это общая масса элемента или соединения (атомная масса), измеренная в единицах атомной массы или «а.е.м.», деленная на его количество в молях (моль). Один моль основан на числе Авогадро 6,02214076×10 23 , поскольку это число означает, что сравнение между молями и дальтонами, другой научной единицей атомной массы, проще.
Ледяная уксусная кислота представляет собой раствор уксусной кислоты в очень небольшом количестве воды – менее 1%. Слово «ледниковый» относится к его кристаллоподобной твердой форме при комнатной температуре. Другое название ледяной уксусной кислоты – безводная уксусная кислота. Эта форма представляет собой слабую кислоту, но едкий яд, вызывающий образование волдырей и ожоги. Поскольку воды для диссоциации очень мало, ледяная уксусная кислота передает свои протоны воде в коже или слизистых оболочках.
Чтобы найти правильный буферный агент для такой кислоты, как уксусная кислота, необходимо знать pH, K a или pK a кислоты. pH, K и и pK и связаны друг с другом. Уксусная кислота имеет значение K a , равное 1,8 x 10-5, или более легкое для расчета значение pK a , равное 4,756. pH измеряет количество ионов водорода (H + ) в любом растворе, содержащем воду, и колеблется от 0 (кислая) до 14 (щелочная). Чем ниже рН, тем выше концентрация ионов водорода. K a и pK a относятся к кислотам и относятся к константе диссоциации кислоты, которая показывает, насколько вероятно, что кислота отдаст свои протоны. Высокий К a говорит нам, что кислота сильная и будет реагировать на любое добавленное к ней химическое вещество. У pK и все наоборот – чем меньше число, тем сильнее кислота. Это потому, что pK a является отрицательным логарифмом K a .
Однако концентрированная уксусная кислота может иметь более низкий pH, чем сильная кислота. Благодаря pK a , которое является постоянным значением, мы можем производить расчеты, не задумываясь о концентрациях. pK a уксусной кислоты составляет 4,756, и это говорит нам о том, насколько вероятно, что она отдаст свои протоны в растворе. Основания измеряются в соответствии с вероятностью удаления протонов из раствора.
Температура кипения уксусной кислоты составляет от 244 до 246°F (от 118 до 119°C), а точка плавления от 61 до 62°F (от 16 до 17°C) или чуть ниже комнатной температуры. Плотность уксусной кислоты составляет 1,049 г см -3 в жидком состоянии и 1,27 г см -3 в твердом состоянии.
Наиболее распространенной формой уксусной кислоты является уксус , который содержит 5-20% уксусной кислоты. Насколько велико разбавление (и, следовательно, сила кислоты), называется силой ее зерна. Вы можете легко вычислить это, умножив концентрацию на 10. Уксус, содержащий 5% уксусной кислоты, будет иметь силу зерна 50.
Уксус, содержащий 5% уксусной кислоты, будет иметь силу зерна 50.
Применение уксусной кислоты
Использование уксусной кислоты разнообразно. Эта кислота используется в производстве товаров, в пищевой промышленности, в клининговой промышленности, в медицине и в качестве пищевой добавки. Уксусная кислота также является биохимически незаменимой в форме ацетильной группы, где она необходима для построения аминокислот и, следовательно, без нее невозможно существование. Давайте рассмотрим некоторые из этих применений уксусной кислоты более подробно.
Уксусная кислота в производстве товаров
Уксусная кислота является важным химическим реагентом, используемым для производства ацетата, клеев, клеев и синтетических тканей. Уксусная кислота также используется в гальванике, когда металлическое покрытие наносится на объект путем помещения его в раствор, содержащий определенную соль металла. Раствор должен быть проводящим, а кислоты, отдающие ионы водорода, создают идеальные условия. Кроме того, гальваническое покрытие может происходить только в растворе, а соли металлов растворяются только в растворах с низким (кислым) значением pH.
Кроме того, гальваническое покрытие может происходить только в растворе, а соли металлов растворяются только в растворах с низким (кислым) значением pH.
Уксусная кислота является сырьем, используемым для производства ацетата целлюлозы, уксусного ангидрида (пластмассы) и хлоруксусной кислоты, используемых в производстве красителей и пестицидов, а также некоторых лекарств.
Уксусная кислота в пищевой промышленности
Уксусная кислота, используемая в пищевой промышленности для регулирования уровня кислотности или щелочности пищевых продуктов. Свод федеральных правил (CFR) классифицирует уксусную кислоту как пищевую добавку общего назначения, которая безопасна при использовании в соответствии с надлежащей производственной практикой. В Европе правила E-номера применяются ко всем пищевым добавкам. Уксусной кислоте присвоен код E260, и она считается безопасным ингредиентом, который контролирует бактериальную колонизацию и может использоваться без ограничений. Это не новая находка. Говорят, что древние вавилоняне использовали уксус в качестве консерванта для пищевых продуктов.
Это не новая находка. Говорят, что древние вавилоняне использовали уксус в качестве консерванта для пищевых продуктов.
Уксус используется для производства заправок для салатов, приправ, включающих горчицу, кетчуп и майонез, а также в соусах и соленьях.
Уксусная кислота для очистки
Уксусная кислота использовалась в качестве чистящего средства и дезодоранта на протяжении столетий, если не тысячелетий; губки с уксусом были помещены в дорогие филигранные кольца, которые носили богатые, когда они ступали по грязным и вонючим улицам восемнадцатого века. Дезодорирующие свойства уксуса также использовались поколениями. Моряки использовали уксус для чистки палуб кораблей, на которых они работали и жили. Принципы микробного контроля, возможно, не были поняты в то время, но освежающий запах, чистота и способность предотвращать болезни этого органического раствора были определенно хорошо известны.
Добавление щелочного продукта к кислоте вызывает реакцию образования пузырей и шипения. Некоторые традиционные чистящие средства считают, что этот эффект обеспечивает более глубокую очистку устойчивых поверхностей. Например, чистка заднего двора щелочным едким натром (гидроксидом натрия), а затем добавлением смеси уксуса вызовет реакцию, которая, безусловно, выглядит так, как будто она оказывает глубокое очищающее действие; однако это очень мало повышает гигиенический эффект, а скорее смягчает или работает против щелочной очищающей способности едкого натра с кислотными свойствами уксуса.
Некоторые традиционные чистящие средства считают, что этот эффект обеспечивает более глубокую очистку устойчивых поверхностей. Например, чистка заднего двора щелочным едким натром (гидроксидом натрия), а затем добавлением смеси уксуса вызовет реакцию, которая, безусловно, выглядит так, как будто она оказывает глубокое очищающее действие; однако это очень мало повышает гигиенический эффект, а скорее смягчает или работает против щелочной очищающей способности едкого натра с кислотными свойствами уксуса.
Сегодня многие преданные любители белого уксуса рекламируют экологические преимущества использования разбавленной уксусной кислоты для очистки ванных комнат, стирки одежды, удаления запахов и обеспечения чистоты и безопасности поверхностей для приготовления пищи. Уксусная кислота также удаляет ржавчину и известковые отложения.
Уксусная кислота в медицине
Уксусная кислота или уксус, вероятно, использовались в медицине еще до появления письменности. Если вы пострадали от открытой раны на острове Кос в четвертом веке до нашей эры, возможно, Гиппократ прописал вам ежедневное омовение уксусом. Если у вас болело горло, он также мог попросить вас смешать мед и уксус, чтобы приготовить Оксимель, древнегреческое лекарство от кашля; если вы служили в Европе во время Первой мировой войны, у вас, возможно, был доступ только к уксусу, чтобы оставаться чистым и не заразиться.
Если вы пострадали от открытой раны на острове Кос в четвертом веке до нашей эры, возможно, Гиппократ прописал вам ежедневное омовение уксусом. Если у вас болело горло, он также мог попросить вас смешать мед и уксус, чтобы приготовить Оксимель, древнегреческое лекарство от кашля; если вы служили в Европе во время Первой мировой войны, у вас, возможно, был доступ только к уксусу, чтобы оставаться чистым и не заразиться.
Сегодня растворы уксусной кислоты используются в процессах лабораторного анализа крови в качестве промывки предметных стекол. Они удаляют бактериальные биопленки в ранах и пищеварительной системе и часто используются при инфекциях наружного уха, что позволяет избежать использования антибиотиков. Употребление уксуса повышает уровень ацетата в толстой кишке и способствует поглощению кальция , в результате чего снижается кровяное давление и повышается плотность костей. Исследования изучают использование ацетата в качестве противоопухолевого препарата.
Уксусная кислота в качестве пищевой добавки
Уксусная кислота является популярной пищевой добавкой и употребляется в виде уксуса, чаще всего яблочного уксуса. При связывании с коферментом А ацетильная группа уксусной кислоты играет центральную роль в метаболизме углеводов и жиров .
Было проведено много исследований связи между потреблением уксуса и снижением уровня глюкозы в крови. Там, где продукты с высоким гликемическим индексом потребляются после приема двух-трех столовых ложек яблочного уксуса, их гликемические значения снижаются на 35%. Для диабетиков это может означать более низкие постпрандиальные пики глюкозы в крови и лучший гликемический контроль, а для недиабетиков более низкий риск развития резистентности к инсулину . Замена обычного огурца маринованным огурцом показала снижение общего гликемического индекса еды на 30 %.
На следующем рисунке показано влияние продуктов с низким и высоким гликемическим индексом (ГИ) на уровень глюкозы в крови.

 Педагогический (научно-педагогический) состав
Педагогический (научно-педагогический) состав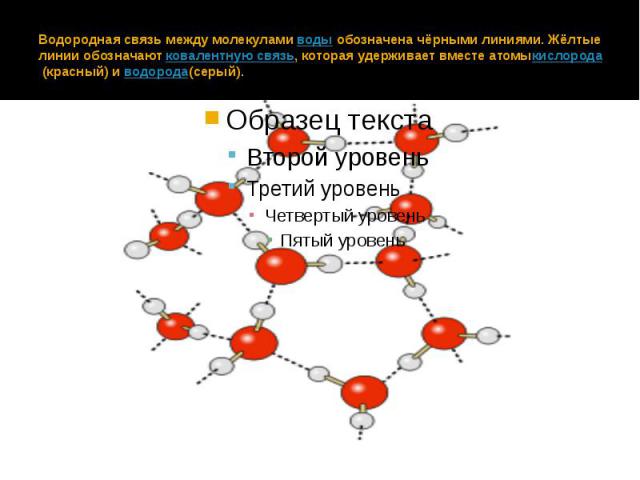
Leave A Comment