Закон постоянства состава вещества – практическое значение, формула (химия 8 класс)
4.4
Средняя оценка: 4.4
Всего получено оценок: 514.
4.4
Средняя оценка: 4.4
Всего получено оценок: 514.
Закон постоянства состава вещества является одним из главных законов химии. Он вытекает из атомно-молекулярного учения. Его суть заключается в том, что вещества состоят из одних и тех же молекул, потому и состав таких веществ постоянен.
Общие сведения
Француз Ж. Пруст – ученый, открывший закон постоянства состава химического соединения. Произошло это в 1808 году.
Рис. 1. Портрет Жозефа Луи ПрустаСовременная формулировка закона заключается в следующем: всякое чистое вещество независимо от способа его получения имеет постоянный качественный и количественный состав.
Чистое вещество в данном случае – вещество, в котором отсутствует даже малое количество примеси.
Рис. 2. Формула закона постоянства состава веществаДанный закон правдив лишь для элементов с молекулярной структурой.
При образовании из двух элементов нескольких соединений атомы этих элементов соединяются друг с другом в молекулы различного, но определенного состава. Например, азот с кислородом образует шесть соединений.
Закон постоянства состава вещества имеет значимое практическое значение. Он позволяет выводить химические формулы.
Соединения постоянного и переменного состава
Русский ученый Н.С. Курнаков в начале XX века обнаружил соединения переменного состава при изучении сплавов металлов. В них на одну единицу массы элемента может приходиться различная масса другого элемента. При рассмотрении соединения висмута с таллием на 1 единицу массы таллия приходится от 1,24 до 1,82 единиц массы висмута.
Курнаков предложил соединения постоянного состава назвать дальтонидами, а соединения переменного состава – бертоллидами.
Дальтониды были названы в честь английского ученого Дальтона, а бертоллиды – в честь французского химика Бертолле, который предвидел такие соединения.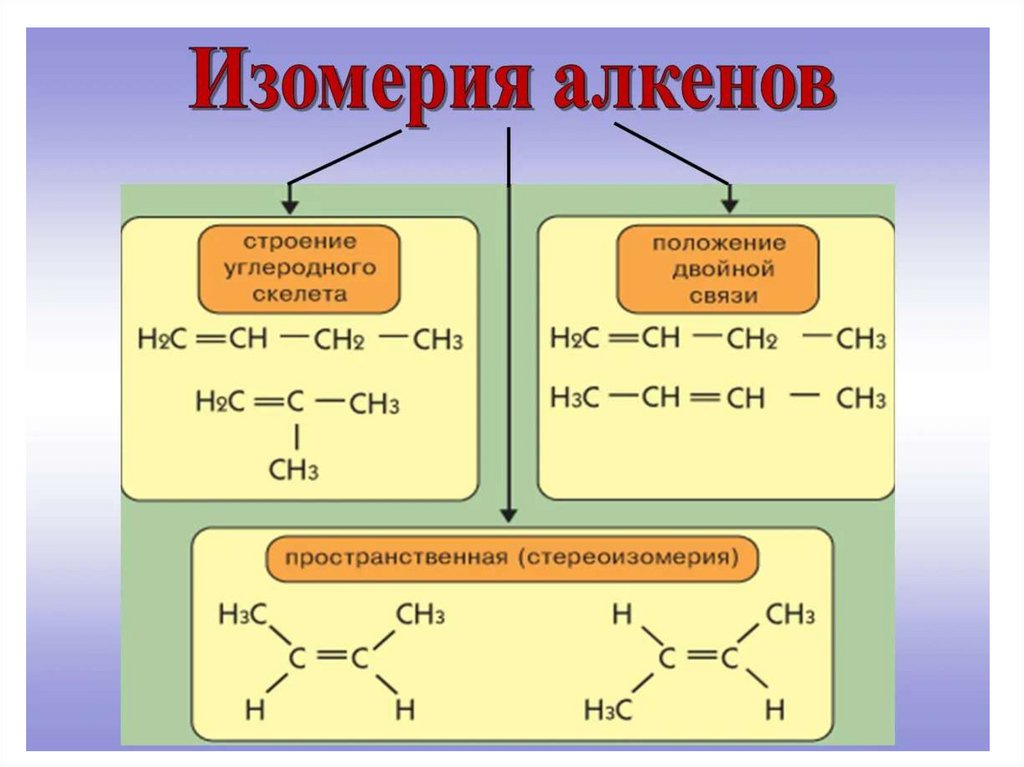
Во второй четверти 20 века обнаружилось, что соединения переменного состава могут встретиться не только среди соединений металлов друг с другом, но и среди других твердых тел, например оксидов, сульфидов, карбидов и т.д.
Уточненная формулировка закона постоянства вещества
Для многих бертоллидов существуют границы, в пределах которых может изменяться их состав. Например,
оксид урана (IV) имеет состав от UO2,5 до UO3, оксид ванадия (II) – от VO0,9 до VO1,3.
Таким образом, имеет смысл внести уточнения в существующую формулировку закона постоянства состава:
Состав соединений молекулярной структуры, т.е. состоящих из молекул, является постоянным независимо от способа получения. Если состав соединений имеет немолекулярную структуру ( а, например, атомную, ионную), то он не является постоянным и зависит от условий получения.
Что мы узнали?
В учебнике химии 8 класса кратко раскрывается определение закона постоянства состава вещества, дается его четкая формулировка, а также рассматриваются соединения переменного и постоянного состава.
Тест по теме
Доска почёта
Чтобы попасть сюда — пройдите тест.
Барият Кадиева
9/10
Александр Котков
9/10
Александр Котков
10/10
Дмитрий Амелехин
10/10
Оценка доклада
4.4
Средняя оценка: 4.4
Всего получено оценок: 514.
А какая ваша оценка?
Виды соли, используемые при приготовлении пищи
Соль можно классифицировать, например, по способу производства и/или добычи, степени измельчения и очистки, содержанию натрия и примесей.
Хотя некоторые соли могут содержать больше разных минералов, чем обычная поваренная соль, их все же никак нельзя считать источниками соответствующих минералов (за искл. йодированной соли). При умеренном потреблении, независимо от вида соли, сопутствующие натрию минералы поступают в крайне малых количествах.
Никакая соль не может стать полноценным источником минеральных веществ. Это означает, что не нужно есть соль с целью получения минеральных веществ.
МОРСКАЯ СОЛЬ
Морскую соль получают путем выпаривания морской воды в специальных ваннах или прудах под действием солнца. Чистота морской соли зависит от состава и чистоты морской воды, из которой она производится. Кристаллы этой соли крупные, неровные. Помимо хлорида натрия, морская соль может содержать некоторое количество йода, кальция, магния и калия.
СОЛЬ ГРУБОГО ПОМОЛА, ИЛИ КАМЕННАЯ СОЛЬ
Грубую, или каменную соль по преимуществу добывают из подземных залежей. Каменная соль имеет грязно-серый цвет. В залежах каждого конкретного месторождения содержатся различные примеси, поэтому стабильной и/или равномерной чистоты каменной соли добиться почти невозможно.
ПОВАРЕННАЯ, ИЛИ СТОЛОВАЯ СОЛЬ
В случае поваренной соли основная часть воды удаляется из соляного раствора кипячением или выпариванием, после чего при помощи мощных центрифуг отделяется оставшаяся вода, чтобы в конце процесса влажность соли составляла около 3%.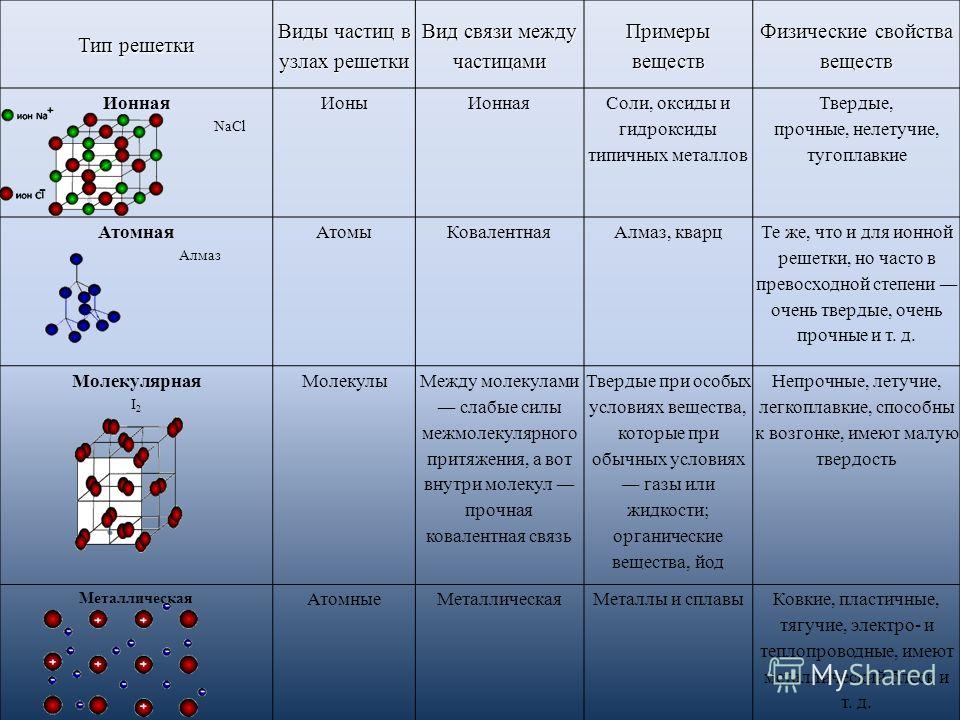 После дополнительной сушки получается равномерно чистая, мелкозернистая качественная поваренная соль.
После дополнительной сушки получается равномерно чистая, мелкозернистая качественная поваренная соль.
ЙОДИРОВАННАЯ СОЛЬ
Йодированная соль обычно представляет собой столовую или минеральную соль с добавлением йода. Добавление йода не меняет вкуса соли. Йодированная соль – хороший способ получить недостающее количество необходимого организму йода.
ПАН-СОЛЬ
Пан-соль получают путем уменьшения содержания натрия в обычной столовой соли и добавлением 25–40% хлорида калия и 10% сульфата магния. Кроме того, в пан-соли есть аминокислота лизин, которая устраняет металлический привкус йода. В двух чайных ложках пан-соли содержится столько же натрия, сколько в одной чайной ложке поваренной соли. В действительности при употреблении пан-соли потребление натрия нередко не сокращается, поскольку ее добавляют в пищу в больших количествах, чтобы добиться привычного вкуса пищи.
Источниками значимого количества минеральных веществ являются зерновые (особенно цельнозерновые продукты), картофель, фрукты и овощи, а также ягоды, молоко и молочные продукты, рыба, птица, яйца, мясо, добавляемые пищевые жиры, орехи, семена, плоды масличных культур, но не соль.
Только йодированную соль можно считать полноценным источником йода.
Помимо обычной соли, в продаже можно найти разноцветные соли с разными названиями (например, Rose, Himaalaja, Hawai, Pärsia), состав и цвет которых зависят от места производства. Несмотря на то, что в их составе зачастую приведен целый список минералов, ни одна из этих солей не содержит ни один из минералов в таком количестве, чтобы оно покрыло значимую часть суточной потребности.
Кроме того, выпускается соль с различными вкусовыми нюансами. Это, например, ароматизированная, чесночная, копченая соль. Соль добавляется и во многие смеси пряностей (например, в перцовую смесь). Так что в случае смесей пряностей нужно обязательно читать маркировку, чтобы узнать, сколько соли они содержат.
В производстве мяса часто используется соль с добавлением нитрита. Нитритная соль – соль высокой степени очистки, специально предназначенная для мясной промышленности. Эта соль придает мясу розовато-красный цвет и сдерживает развитие нежелательных микроорганизмов, продлевая тем самым срок годности продукта.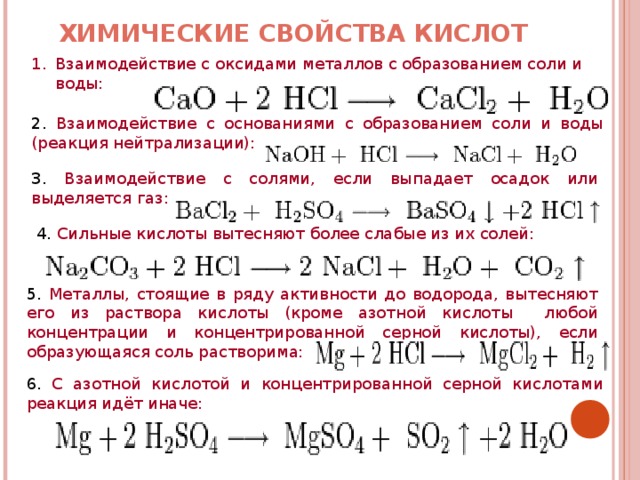
1.2: Классификация вещества — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 21692
Цели обучения
- Классифицировать материю.
Химики изучают структуру, физические свойства и химические свойства материальных веществ. Они состоят из материи , то есть всего, что занимает пространство и имеет массу. Золото и иридий — это материя, как и арахис, люди и почтовые марки. Дым, смог и веселящий газ — это материя. Однако энергия, свет и звук не являются материей; идеи и эмоции тоже не имеют значения.
Масса объекта — это количество содержащейся в нем материи.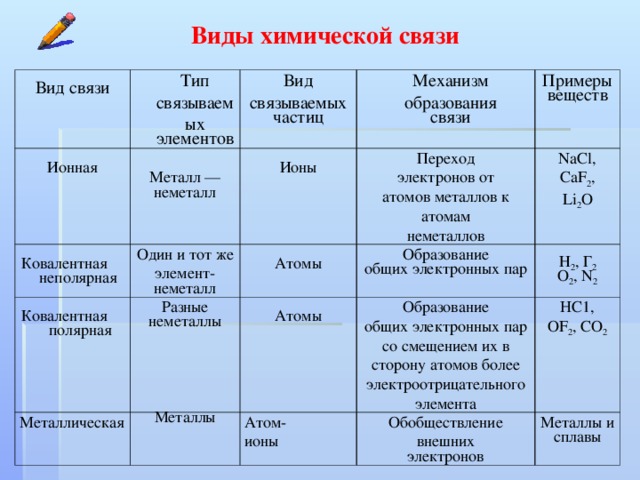 Не путайте массу объекта с его вес , который представляет собой силу, вызванную гравитационным притяжением, которое действует на объект. Масса — это фундаментальное свойство объекта, не зависящее от его местоположения. С физической точки зрения масса объекта прямо пропорциональна силе, необходимой для изменения его скорости или направления. Более подробное обсуждение различий между весом и массой и единицами, используемыми для их измерения, включено в Основные навыки 1 (раздел 1.9). Вес, с другой стороны, зависит от местоположения объекта. Космонавт, масса которого равна 95 кг весит около 210 фунтов на Земле, но только около 35 фунтов на Луне, потому что гравитационная сила, которую он или она испытывает на Луне, составляет примерно одну шестую силы, испытываемой на Земле. В практических целях в лабораториях вес и масса часто используются взаимозаменяемо. Поскольку считается, что сила тяжести одинакова на всей поверхности Земли, 2,2 фунта (вес) равняется 1,0 кг (масса), независимо от местоположения лаборатории на Земле.
Не путайте массу объекта с его вес , который представляет собой силу, вызванную гравитационным притяжением, которое действует на объект. Масса — это фундаментальное свойство объекта, не зависящее от его местоположения. С физической точки зрения масса объекта прямо пропорциональна силе, необходимой для изменения его скорости или направления. Более подробное обсуждение различий между весом и массой и единицами, используемыми для их измерения, включено в Основные навыки 1 (раздел 1.9). Вес, с другой стороны, зависит от местоположения объекта. Космонавт, масса которого равна 95 кг весит около 210 фунтов на Земле, но только около 35 фунтов на Луне, потому что гравитационная сила, которую он или она испытывает на Луне, составляет примерно одну шестую силы, испытываемой на Земле. В практических целях в лабораториях вес и масса часто используются взаимозаменяемо. Поскольку считается, что сила тяжести одинакова на всей поверхности Земли, 2,2 фунта (вес) равняется 1,0 кг (масса), независимо от местоположения лаборатории на Земле.
При нормальных условиях существует три различных состояния вещества: твердое, жидкое и газообразное. Твердые тела относительно жесткие и имеют фиксированные формы и объемы. Камень, например, является твердым телом. Напротив, жидкости имеют фиксированный объем, но текут, принимая форму своих емкостей, таких как напиток в банке. Газы , такие как воздух в автомобильной шине, не имеют ни фиксированной формы, ни фиксированного объема и расширяются, чтобы полностью заполнить свои сосуды. В то время как объем газов сильно зависит от их температуры  Однако такие изменения состояния не влияют на химический состав вещества.
Однако такие изменения состояния не влияют на химический состав вещества.
Чистые вещества и смеси
Чистое химическое вещество – это любое вещество, имеющее фиксированный химический состав и характерные свойства. Кислород, например, представляет собой чистое химическое вещество, представляющее собой бесцветный газ без запаха при температуре 25°C. Очень немногие образцы материи состоят из чистых веществ; вместо этого большинство из них представляют собой смеси, представляющие собой комбинации двух или более чистых веществ в различных пропорциях, в которых отдельные вещества сохраняют свою идентичность. Воздух, водопроводная вода, молоко, сыр с плесенью, хлеб и грязь — все это смеси. Если все части материала находятся в одном и том же состоянии, не имеют видимых границ и однородны на всем протяжении, то материал 9. 0030 однородный . Примерами однородных смесей являются воздух, которым мы дышим, и водопроводная вода, которую мы пьем. Однородные смеси также называют растворами. Так, воздух есть раствор азота, кислорода, водяного пара, двуокиси углерода и некоторых других газов; водопроводная вода представляет собой раствор небольшого количества нескольких веществ в воде. Однако конкретные составы обоих этих растворов не фиксированы, а зависят как от источника, так и от местоположения; например, состав водопроводной воды в Бойсе, штат Айдахо, отличается от состава водопроводной воды в Буффало, штат Нью-Йорк. Хотя большинство растворов, с которыми мы сталкиваемся, являются жидкими, растворы также могут быть твердыми. Серое вещество, до сих пор используемое некоторыми стоматологами для пломбирования полостей зубов, представляет собой сложный твердый раствор, содержащий 50 % ртути и 50 % порошка, состоящего в основном из серебра, олова и меди с небольшими количествами цинка и ртути. Твердые растворы двух и более металлов принято называть сплавами.
0030 однородный . Примерами однородных смесей являются воздух, которым мы дышим, и водопроводная вода, которую мы пьем. Однородные смеси также называют растворами. Так, воздух есть раствор азота, кислорода, водяного пара, двуокиси углерода и некоторых других газов; водопроводная вода представляет собой раствор небольшого количества нескольких веществ в воде. Однако конкретные составы обоих этих растворов не фиксированы, а зависят как от источника, так и от местоположения; например, состав водопроводной воды в Бойсе, штат Айдахо, отличается от состава водопроводной воды в Буффало, штат Нью-Йорк. Хотя большинство растворов, с которыми мы сталкиваемся, являются жидкими, растворы также могут быть твердыми. Серое вещество, до сих пор используемое некоторыми стоматологами для пломбирования полостей зубов, представляет собой сложный твердый раствор, содержащий 50 % ртути и 50 % порошка, состоящего в основном из серебра, олова и меди с небольшими количествами цинка и ртути. Твердые растворы двух и более металлов принято называть сплавами.
Если состав материала не совсем однороден, то он гетерогенен (например, тесто для печенья с шоколадной крошкой, сыр с плесенью и грязь). Смеси, которые кажутся гомогенными, после микроскопического исследования часто оказываются гетерогенными. Молоко, например, кажется однородным, но при рассмотрении под микроскопом оно явно состоит из крошечных шариков жира и белка, диспергированных в воде. Компоненты гетерогенных смесей обычно можно разделить простыми средствами. Смеси твердой и жидкой фаз, такие как песок в воде или чайные листья в чае, легко отделяются путем фильтрации, которая заключается в пропускании смеси через барьер, такой как сито, с отверстиями или порами, которые меньше, чем твердые частицы. В принципе, смеси двух или более твердых веществ, таких как сахар и соль, можно разделить путем микроскопического исследования и сортировки. Однако обычно необходимы более сложные операции, например, при отделении золотых самородков от речного гравия путем промывки. Сначала из речной воды отфильтровывают твердый материал; затем твердые вещества отделяют путем осмотра. Если золото внедрено в горную породу, возможно, его придется выделять химическими методами.
Сначала из речной воды отфильтровывают твердый материал; затем твердые вещества отделяют путем осмотра. Если золото внедрено в горную породу, возможно, его придется выделять химическими методами.
. Гомогенные смеси (растворы) могут быть разделены на составляющие их вещества физическими процессами, основанными на различиях в некоторых физических свойствах, таких как различия в их температурах кипения. Двумя из этих методов разделения являются дистилляция и кристаллизация. Дистилляция использует разницу в летучести, меру того, насколько легко вещество превращается в газ при данной температуре. Простой перегонный аппарат для разделения смеси веществ, хотя бы одно из которых является жидкостью. Наиболее летучий компонент закипает первым и снова конденсируется в жидкость в водоохлаждаемом холодильнике, из которого стекает в приемную колбу. Если перегоняют, например, раствор соли и воды, то более летучий компонент, чистая вода, собирается в приемной колбе, а соль остается в перегонной колбе.
Если перегоняют, например, раствор соли и воды, то более летучий компонент, чистая вода, собирается в приемной колбе, а соль остается в перегонной колбе.
Смеси двух или более жидкостей с разными точками кипения можно разделить с помощью более сложного перегонного аппарата. Одним из примеров является переработка сырой нефти в ряд полезных продуктов: авиационное топливо, бензин, керосин, дизельное топливо и смазочное масло (в приблизительном порядке убывания летучести). Другим примером является дистилляция спиртных напитков, таких как бренди или виски. (Эта относительно простая процедура доставила немало головной боли федеральным властям в XIX веке.20-е годы в эпоху Сухого закона, когда нелегальные перегонные аппараты распространялись в отдаленных регионах Соединенных Штатов!)
Кристаллизация разделяет смеси на основе различий в растворимости, мера того, сколько твердого вещества остается растворенным в заданном количестве указанной жидкости . Большинство веществ лучше растворяются при более высоких температурах, поэтому смесь двух или более веществ можно растворить при повышенной температуре, а затем дать медленно остыть. В качестве альтернативы жидкости, называемой растворителем, можно позволить испариться. В любом случае наименее растворимое из растворенных веществ, то, которое с наименьшей вероятностью останется в растворе, обычно сначала образует кристаллы, и эти кристаллы можно удалить из оставшегося раствора фильтрованием.
Большинство веществ лучше растворяются при более высоких температурах, поэтому смесь двух или более веществ можно растворить при повышенной температуре, а затем дать медленно остыть. В качестве альтернативы жидкости, называемой растворителем, можно позволить испариться. В любом случае наименее растворимое из растворенных веществ, то, которое с наименьшей вероятностью останется в растворе, обычно сначала образует кристаллы, и эти кристаллы можно удалить из оставшегося раствора фильтрованием.
Большинство смесей можно разделить на чистые вещества, которые могут быть элементами или соединениями. элемент , такой как серый металлический натрий, представляет собой вещество, которое нельзя разложить на более простые путем химических превращений; соединение , такое как белый кристаллический хлорид натрия, содержит два или более элементов и имеет химические и физические свойства, которые обычно отличаются от свойств элементов, из которых оно состоит. Лишь за некоторыми исключениями, конкретное соединение имеет один и тот же элементный состав (одинаковые элементы в одних и тех же пропорциях) независимо от его источника или истории. Химический состав вещества изменяется в процессе, называемом химическая замена . Превращение двух или более элементов, таких как натрий и хлор, в химическое соединение, хлорид натрия, является примером химического изменения, часто называемого химической реакцией. В настоящее время известно около 118 элементов, но из этих 118 элементов получены миллионы химических соединений. Известные элементы перечислены в периодической таблице.
элемент , такой как серый металлический натрий, представляет собой вещество, которое нельзя разложить на более простые путем химических превращений; соединение , такое как белый кристаллический хлорид натрия, содержит два или более элементов и имеет химические и физические свойства, которые обычно отличаются от свойств элементов, из которых оно состоит. Лишь за некоторыми исключениями, конкретное соединение имеет один и тот же элементный состав (одинаковые элементы в одних и тех же пропорциях) независимо от его источника или истории. Химический состав вещества изменяется в процессе, называемом химическая замена . Превращение двух или более элементов, таких как натрий и хлор, в химическое соединение, хлорид натрия, является примером химического изменения, часто называемого химической реакцией. В настоящее время известно около 118 элементов, но из этих 118 элементов получены миллионы химических соединений. Известные элементы перечислены в периодической таблице.
Рисунок \(\PageIndex{5}\): Разложение воды на водород и кислород с помощью электролиза. Вода — это химическое соединение; водород и кислород являются элементами. батарея подключена к аноду и катоду, помещенному в химический стакан, наполненный водой. Две перевернутые пробирки погружают в воду и помещают над каждым из электродов для сбора газообразных продуктов. Увеличительные указатели показывают молекулярную структуру воды в стакане, а также газообразный водород, собранный на стороне анода, и газообразный кислород на стороне катода.
Различные определения материи: Различные определения материи, YouTube (открывается в новом окне) [youtu.be]
В общем, обратный химический процесс расщепляет соединения на их элементы. Например, вода (соединение) может быть разложена на водород и кислород (оба элемента) в процессе, называемом электролизом. При электролизе электричество обеспечивает энергию, необходимую для разделения соединения на составные элементы (рис. \(\PageIndex{5}\)). Подобный метод широко используется для получения чистого алюминия, элемента, из его руд, представляющих собой смеси соединений. Поскольку для электролиза требуется много энергии, стоимость электроэнергии является самой большой статьей расходов, связанных с производством чистого алюминия. Таким образом, переработка алюминия является экономически выгодной и экологически чистой.
\(\PageIndex{5}\)). Подобный метод широко используется для получения чистого алюминия, элемента, из его руд, представляющих собой смеси соединений. Поскольку для электролиза требуется много энергии, стоимость электроэнергии является самой большой статьей расходов, связанных с производством чистого алюминия. Таким образом, переработка алюминия является экономически выгодной и экологически чистой.
Общая организация материи и методы разделения смесей представлены на рисунке \(\PageIndex{6}\).
Рисунок \(\PageIndex{6}\): Взаимосвязь между типами вещества и методами, используемыми для разделения смесейПример \(\PageIndex{1}\)
- фильтрованный чай
- свежевыжатый апельсиновый сок
- компакт-диск
- оксид алюминия, белый порошок, содержащий атомы алюминия и кислорода в соотношении 2:3
- селен
Дано : химическое вещество
Вопрос : его классификация
Стратегия:
- Решите, является ли вещество химически чистым.

- Если вещество не является химически чистым, оно представляет собой либо гетерогенную смесь, либо гомогенную смесь. Если его состав везде однороден, то это однородная смесь.
Раствор
- A Чай представляет собой раствор соединений в воде, поэтому он не является химически чистым. Обычно его отделяют от чайных листьев фильтрованием. B Поскольку состав раствора везде однороден, это однородная смесь.
- А Апельсиновый сок содержит как твердые, так и жидкие частицы (мякоть); он не является химически чистым. B Поскольку его состав неоднороден, апельсиновый сок представляет собой неоднородную смесь.
- A Компакт-диск представляет собой твердый материал, содержащий более одного элемента, по краям которого видны области разного состава.
 Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.
Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь. - A Селен — один из известных элементов.
Упражнение \(\PageIndex{1}\)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- белое вино
- ртуть
- Заправка для салата «ранчо»
- сахар столовый (сахароза)
- Ответ А
раствор
- Ответ Б
элемент
- Ответ C
гетерогенная смесь
- Ответ D
компаунд
Различные определения изменений: Различные определения изменений, YouTube(opens in new window) [youtu.be] (opens in new window)
Резюме
Вещество можно классифицировать по физическим и химическим свойствам. Материя – это все, что занимает пространство и имеет массу. Три состояния вещества – твердое, жидкое и газообразное. Физическое изменение предполагает переход вещества из одного состояния вещества в другое без изменения его химического состава. Большая часть материи состоит из смесей чистых веществ, которые могут быть гомогенными (однородными по составу) или гетерогенными (разные области обладают разным составом и свойствами). Чистые вещества могут быть как химическими соединениями, так и элементами. Соединения можно разложить на элементы химическими реакциями, но нельзя разделить химическими средствами элементы на более простые вещества. Свойства веществ можно разделить на физические и химические. Ученые могут наблюдать физические свойства без изменения состава вещества, тогда как химические свойства описывают склонность вещества к химическим изменениям (химическим реакциям), которые изменяют его химический состав. Физические свойства могут быть интенсивными или экстенсивными. Интенсивные свойства одинаковы для всех образцов; не зависят от размера выборки; и включают, например, цвет, физическое состояние и температуры плавления и кипения. Экстенсивные свойства зависят от количества материала и включают массу и объем. Соотношение двух экстенсивных свойств, массы и объема, является важным интенсивным свойством, называемым плотностью.
Ученые могут наблюдать физические свойства без изменения состава вещества, тогда как химические свойства описывают склонность вещества к химическим изменениям (химическим реакциям), которые изменяют его химический состав. Физические свойства могут быть интенсивными или экстенсивными. Интенсивные свойства одинаковы для всех образцов; не зависят от размера выборки; и включают, например, цвет, физическое состояние и температуры плавления и кипения. Экстенсивные свойства зависят от количества материала и включают массу и объем. Соотношение двух экстенсивных свойств, массы и объема, является важным интенсивным свойством, называемым плотностью.
Авторы и авторство
1.2: Classification of Matter распространяется под лицензией CC BY-NC-SA 3.0 и был создан, изменен и/или курирован LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Показать страницу TOC
- № на стр.

- Теги
- химическая замена
- компаунд
- Кристаллизация
- дистилляция
- элемент
- газ
- гетерогенная смесь
- гомогенная смесь
- жидкость
- масса
- материя
- Физическое изменение
- давление
- твердый
- вес
1.3: Классификация вещества — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 13777
Цели обучения
- Для классификации материи.

Химики изучают структуру, физические свойства и химические свойства материальных веществ. Они состоят из материи , то есть всего, что занимает пространство и имеет массу. Золото и иридий — это материя, как и арахис, люди и почтовые марки. Дым, смог и веселящий газ — это материя. Однако энергия, свет и звук не являются материей; идеи и эмоции тоже не имеют значения.
Масса объекта — это количество содержащейся в нем материи. Не путайте массу объекта с его вес , который представляет собой силу, вызванную гравитационным притяжением, которое действует на объект. Масса — это фундаментальное свойство объекта, не зависящее от его местоположения. С физической точки зрения масса объекта прямо пропорциональна силе, необходимой для изменения его скорости или направления. Более подробное обсуждение различий между весом и массой и единицами, используемыми для их измерения, включено в Основные навыки 1 (раздел 1.9). Вес, с другой стороны, зависит от местоположения объекта.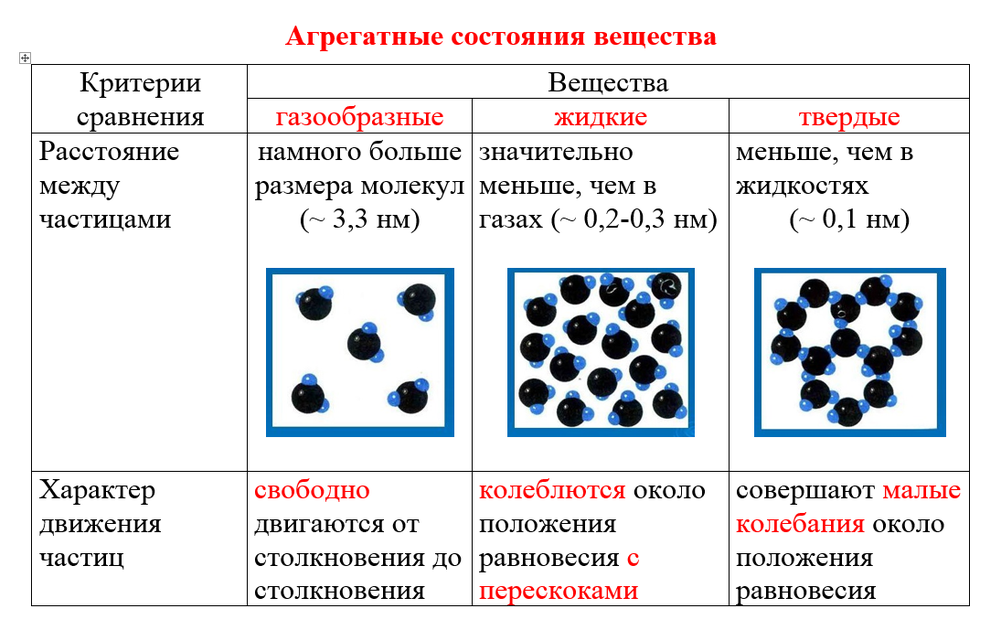 Космонавт, масса которого равна 95 кг весит около 210 фунтов на Земле, но только около 35 фунтов на Луне, потому что гравитационная сила, которую он или она испытывает на Луне, составляет примерно одну шестую силы, испытываемой на Земле. В практических целях в лабораториях вес и масса часто используются взаимозаменяемо. Поскольку считается, что сила тяжести одинакова на всей поверхности Земли, 2,2 фунта (вес) равняется 1,0 кг (масса), независимо от местоположения лаборатории на Земле.
Космонавт, масса которого равна 95 кг весит около 210 фунтов на Земле, но только около 35 фунтов на Луне, потому что гравитационная сила, которую он или она испытывает на Луне, составляет примерно одну шестую силы, испытываемой на Земле. В практических целях в лабораториях вес и масса часто используются взаимозаменяемо. Поскольку считается, что сила тяжести одинакова на всей поверхности Земли, 2,2 фунта (вес) равняется 1,0 кг (масса), независимо от местоположения лаборатории на Земле.
При нормальных условиях существует три различных состояния вещества: твердое, жидкое и газообразное. Твердые тела относительно жесткие и имеют фиксированные формы и объемы. Камень, например, является твердым телом. Напротив, жидкости имеют фиксированный объем, но текут, принимая форму своих емкостей, таких как напиток в банке. Газы , такие как воздух в автомобильной шине, не имеют ни фиксированной формы, ни фиксированного объема и расширяются, чтобы полностью заполнить свои сосуды. В то время как объем газов сильно зависит от их температуры и давления (величины силы, действующей на данную площадь), объемы жидкостей и твердых тел практически не зависят от температуры и давления. Материя часто может переходить из одного физического состояния в другое в процессе, называемом физическое изменение . Например, жидкую воду можно нагреть с образованием газа, называемого паром, или пар можно охладить с образованием жидкой воды. Однако такие изменения состояния не влияют на химический состав вещества.
В то время как объем газов сильно зависит от их температуры и давления (величины силы, действующей на данную площадь), объемы жидкостей и твердых тел практически не зависят от температуры и давления. Материя часто может переходить из одного физического состояния в другое в процессе, называемом физическое изменение . Например, жидкую воду можно нагреть с образованием газа, называемого паром, или пар можно охладить с образованием жидкой воды. Однако такие изменения состояния не влияют на химический состав вещества.
Чистые вещества и смеси
Чистое химическое вещество – это любое вещество, имеющее фиксированный химический состав и характерные свойства. Кислород, например, представляет собой чистое химическое вещество, представляющее собой бесцветный газ без запаха при температуре 25°C. Очень немногие образцы материи состоят из чистых веществ; вместо этого большинство из них представляют собой смеси, представляющие собой комбинации двух или более чистых веществ в различных пропорциях, в которых отдельные вещества сохраняют свою идентичность. Воздух, водопроводная вода, молоко, сыр с плесенью, хлеб и грязь — все это смеси. Если все части материала находятся в одном и том же состоянии, не имеют видимых границ и однородны на всем протяжении, то материал 9.0030 однородный . Примерами однородных смесей являются воздух, которым мы дышим, и водопроводная вода, которую мы пьем. Однородные смеси также называют растворами. Так, воздух есть раствор азота, кислорода, водяного пара, двуокиси углерода и некоторых других газов; водопроводная вода представляет собой раствор небольшого количества нескольких веществ в воде. Однако конкретные составы обоих этих растворов не фиксированы, а зависят как от источника, так и от местоположения; например, состав водопроводной воды в Бойсе, штат Айдахо, отличается от состава водопроводной воды в Буффало, штат Нью-Йорк.
Очень немногие образцы материи состоят из чистых веществ; вместо этого большинство из них представляют собой смеси, представляющие собой комбинации двух или более чистых веществ в различных пропорциях, в которых отдельные вещества сохраняют свою идентичность. Воздух, водопроводная вода, молоко, сыр с плесенью, хлеб и грязь — все это смеси. Если все части материала находятся в одном и том же состоянии, не имеют видимых границ и однородны на всем протяжении, то материал 9.0030 однородный . Примерами однородных смесей являются воздух, которым мы дышим, и водопроводная вода, которую мы пьем. Однородные смеси также называют растворами. Так, воздух есть раствор азота, кислорода, водяного пара, двуокиси углерода и некоторых других газов; водопроводная вода представляет собой раствор небольшого количества нескольких веществ в воде. Однако конкретные составы обоих этих растворов не фиксированы, а зависят как от источника, так и от местоположения; например, состав водопроводной воды в Бойсе, штат Айдахо, отличается от состава водопроводной воды в Буффало, штат Нью-Йорк. Хотя большинство растворов, с которыми мы сталкиваемся, являются жидкими, растворы также могут быть твердыми. Серое вещество, до сих пор используемое некоторыми стоматологами для пломбирования полостей зубов, представляет собой сложный твердый раствор, содержащий 50 % ртути и 50 % порошка, состоящего в основном из серебра, олова и меди с небольшими количествами цинка и ртути. Твердые растворы двух и более металлов принято называть сплавами.
Хотя большинство растворов, с которыми мы сталкиваемся, являются жидкими, растворы также могут быть твердыми. Серое вещество, до сих пор используемое некоторыми стоматологами для пломбирования полостей зубов, представляет собой сложный твердый раствор, содержащий 50 % ртути и 50 % порошка, состоящего в основном из серебра, олова и меди с небольшими количествами цинка и ртути. Твердые растворы двух и более металлов принято называть сплавами.
Если состав материала не совсем однороден, то он гетерогенен (например, тесто для печенья с шоколадной крошкой, сыр с плесенью и грязь). Смеси, которые кажутся гомогенными, после микроскопического исследования часто оказываются гетерогенными. Молоко, например, кажется однородным, но при рассмотрении под микроскопом оно явно состоит из крошечных шариков жира и белка, диспергированных в воде. Компоненты гетерогенных смесей обычно можно разделить простыми средствами. Смеси твердой и жидкой фаз, такие как песок в воде или чайные листья в чае, легко отделяются путем фильтрации, которая заключается в пропускании смеси через барьер, такой как сито, с отверстиями или порами, которые меньше, чем твердые частицы. В принципе, смеси двух или более твердых веществ, таких как сахар и соль, можно разделить путем микроскопического исследования и сортировки. Однако обычно необходимы более сложные операции, например, при отделении золотых самородков от речного гравия путем промывки. Сначала из речной воды отфильтровывают твердый материал; затем твердые вещества отделяют путем осмотра. Если золото внедрено в горную породу, возможно, его придется выделять химическими методами.
В принципе, смеси двух или более твердых веществ, таких как сахар и соль, можно разделить путем микроскопического исследования и сортировки. Однако обычно необходимы более сложные операции, например, при отделении золотых самородков от речного гравия путем промывки. Сначала из речной воды отфильтровывают твердый материал; затем твердые вещества отделяют путем осмотра. Если золото внедрено в горную породу, возможно, его придется выделять химическими методами.
Рисунок \(\PageIndex{2}\): Гетерогенная смесь. Под микроскопом цельное молоко на самом деле представляет собой гетерогенную смесь, состоящую из шариков жира и белка, диспергированных в воде. Рисунок использован с разрешения Википедии
. Гомогенные смеси (растворы) могут быть разделены на составляющие их вещества физическими процессами, основанными на различиях в некоторых физических свойствах, таких как различия в их температурах кипения. Двумя из этих методов разделения являются дистилляция и кристаллизация. Дистилляция использует разницу в летучести, меру того, насколько легко вещество превращается в газ при данной температуре. Простой перегонный аппарат для разделения смеси веществ, хотя бы одно из которых является жидкостью. Наиболее летучий компонент закипает первым и снова конденсируется в жидкость в водоохлаждаемом холодильнике, из которого стекает в приемную колбу. Если перегоняют, например, раствор соли и воды, то более летучий компонент, чистая вода, собирается в приемной колбе, а соль остается в перегонной колбе.
Простой перегонный аппарат для разделения смеси веществ, хотя бы одно из которых является жидкостью. Наиболее летучий компонент закипает первым и снова конденсируется в жидкость в водоохлаждаемом холодильнике, из которого стекает в приемную колбу. Если перегоняют, например, раствор соли и воды, то более летучий компонент, чистая вода, собирается в приемной колбе, а соль остается в перегонной колбе.
Рисунок \(\PageIndex{3}\): Перегонка раствора поваренной соли в воде. Раствор соли в воде нагревают в перегонной колбе до кипения. Образующийся пар обогащается более летучим компонентом (водой), который конденсируется в жидкость в холодном холодильнике и затем собирается в приемной колбе.
Смеси двух или более жидкостей с разными точками кипения можно разделить с помощью более сложного перегонного аппарата. Одним из примеров является переработка сырой нефти в ряд полезных продуктов: авиационное топливо, бензин, керосин, дизельное топливо и смазочное масло (в приблизительном порядке убывания летучести). Другим примером является дистилляция спиртных напитков, таких как бренди или виски. Эта относительно простая процедура доставила немало головной боли федеральным властям в XIX веке.20-х годов в эпоху сухого закона, когда нелегальные перегонные аппараты распространялись в отдаленных регионах США.
Другим примером является дистилляция спиртных напитков, таких как бренди или виски. Эта относительно простая процедура доставила немало головной боли федеральным властям в XIX веке.20-х годов в эпоху сухого закона, когда нелегальные перегонные аппараты распространялись в отдаленных регионах США.
Кристаллизация разделяет смеси на основе различий в растворимости, которая показывает, сколько твердого вещества остается растворенным в заданном количестве определенной жидкости. Большинство веществ лучше растворяются при более высоких температурах, поэтому смесь двух или более веществ можно растворить при повышенной температуре, а затем дать медленно остыть. В качестве альтернативы жидкости, называемой растворителем, можно позволить испариться. И в том, и в другом случае наименее растворимое из растворенных веществ, то, которое с наименьшей вероятностью остается в растворе, обычно сначала образует кристаллы, и эти кристаллы можно удалить из оставшегося раствора фильтрованием.
Рисунок \(\PageIndex{4}\): Кристаллизация ацетата натрия из концентрированного раствора ацетата натрия в воде. Добавление небольшого «затравочного» кристалла (а) приводит к тому, что соединение образует белые кристаллы, которые растут и в конечном итоге занимают большую часть колбы. Видео можно найти здесь: https://www.youtube.com/watch?v=BLq5NibwV5g
Большинство смесей можно разделить на чистые вещества, которые могут быть как элементами, так и соединениями. Элемент , такой как серый металлический натрий, представляет собой вещество, которое нельзя разложить на более простые путем химических превращений; 9Соединение 0030 , такое как белый кристаллический хлорид натрия, содержит два или более элемента и имеет химические и физические свойства, которые обычно отличаются от свойств элементов, из которых оно состоит. Лишь за некоторыми исключениями, конкретное соединение имеет один и тот же элементный состав (одинаковые элементы в одних и тех же пропорциях) независимо от его источника или истории. Химический состав вещества изменяется в процессе, называемом химическим изменением . Превращение двух или более элементов, таких как натрий и хлор, в химическое соединение, хлорид натрия, является примером химического изменения, часто называемого химической реакцией. В настоящее время известно около 115 элементов, но из этих 115 элементов получены миллионы химических соединений. Известные элементы перечислены в периодической таблице.
Химический состав вещества изменяется в процессе, называемом химическим изменением . Превращение двух или более элементов, таких как натрий и хлор, в химическое соединение, хлорид натрия, является примером химического изменения, часто называемого химической реакцией. В настоящее время известно около 115 элементов, но из этих 115 элементов получены миллионы химических соединений. Известные элементы перечислены в периодической таблице.
В общем, обратный химический процесс расщепляет соединения на их элементы. Например, вода (соединение) может быть разложена на водород и кислород (оба элемента) в процессе, называемом электролизом. При электролизе электричество обеспечивает энергию, необходимую для разделения соединения на составные элементы (рис. \(\PageIndex{5}\)). Подобный метод широко используется для получения чистого алюминия, элемента, из его руд, представляющих собой смеси соединений. Поскольку для электролиза требуется много энергии, стоимость электроэнергии является самой большой статьей расходов, связанных с производством чистого алюминия. Таким образом, переработка алюминия является экономически выгодной и экологически чистой. Общая организация материи и методы, используемые для разделения смесей, представлены на рисунке \(\PageIndex{6}\).
Поскольку для электролиза требуется много энергии, стоимость электроэнергии является самой большой статьей расходов, связанных с производством чистого алюминия. Таким образом, переработка алюминия является экономически выгодной и экологически чистой. Общая организация материи и методы, используемые для разделения смесей, представлены на рисунке \(\PageIndex{6}\).
Рисунок \(\PageIndex{6}\): Взаимосвязь между типами вещества и методами, используемыми для разделения смесей
Пример \(\PageIndex{1}\)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- фильтрованный чай
- свежевыжатый апельсиновый сок
- компакт-диск
- оксид алюминия, белый порошок, содержащий атомы алюминия и кислорода в соотношении 2:3
- селен
Дано : химическое вещество
Вопрос : его классификация
Стратегия:
- Решите, является ли вещество химически чистым.
 Если оно чистое, то вещество является либо элементом, либо соединением. Если вещество можно разделить на элементы, оно является соединением.
Если оно чистое, то вещество является либо элементом, либо соединением. Если вещество можно разделить на элементы, оно является соединением. - Если вещество не является химически чистым, оно представляет собой либо гетерогенную смесь, либо гомогенную смесь. Если его состав везде однороден, то это однородная смесь.
Раствор
- A Чай представляет собой раствор соединений в воде, поэтому он не является химически чистым. Обычно его отделяют от чайных листьев фильтрованием. B Поскольку состав раствора везде однороден, это однородная смесь.
- A Апельсиновый сок содержит как твердые, так и жидкие частицы (мякоть); он не является химически чистым. B Поскольку его состав неоднороден, апельсиновый сок представляет собой неоднородную смесь.
- A Компакт-диск представляет собой твердый материал, содержащий более одного элемента, по краям которого видны области разного состава.
 Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.
Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь. - A Оксид алюминия представляет собой отдельное химически чистое соединение.
- A Селен — один из известных элементов.
Упражнение \(\PageIndex{1}\)
Определите каждое вещество как соединение, элемент, гетерогенную смесь или гомогенную смесь (раствор).
- белое вино
- ртуть
- Заправка для салата «ранчо»
- сахар столовый (сахароза)
Ответ
- решение
- элемент
- гетерогенная смесь
- соединение
Разные определения материи: https://youtu.be/qi_qLHc8wLk
Резюме
Вещество можно классифицировать по физическим и химическим свойствам. Материя – это все, что занимает пространство и имеет массу. Три состояния вещества – твердое, жидкое и газообразное. Физическое изменение предполагает переход вещества из одного состояния вещества в другое без изменения его химического состава. Большая часть материи состоит из смесей чистых веществ, которые могут быть гомогенными (однородными по составу) или гетерогенными (разные области обладают разным составом и свойствами). Чистые вещества могут быть как химическими соединениями, так и элементами. Соединения можно разложить на элементы химическими реакциями, но нельзя разделить химическими средствами элементы на более простые вещества. Свойства веществ можно разделить на физические и химические. Ученые могут наблюдать физические свойства без изменения состава вещества, тогда как химические свойства описывают склонность вещества к химическим изменениям (химическим реакциям), которые изменяют его химический состав. Физические свойства могут быть интенсивными или экстенсивными. Интенсивные свойства одинаковы для всех образцов; не зависят от размера выборки; и включают, например, цвет, физическое состояние и температуры плавления и кипения.
Материя – это все, что занимает пространство и имеет массу. Три состояния вещества – твердое, жидкое и газообразное. Физическое изменение предполагает переход вещества из одного состояния вещества в другое без изменения его химического состава. Большая часть материи состоит из смесей чистых веществ, которые могут быть гомогенными (однородными по составу) или гетерогенными (разные области обладают разным составом и свойствами). Чистые вещества могут быть как химическими соединениями, так и элементами. Соединения можно разложить на элементы химическими реакциями, но нельзя разделить химическими средствами элементы на более простые вещества. Свойства веществ можно разделить на физические и химические. Ученые могут наблюдать физические свойства без изменения состава вещества, тогда как химические свойства описывают склонность вещества к химическим изменениям (химическим реакциям), которые изменяют его химический состав. Физические свойства могут быть интенсивными или экстенсивными. Интенсивные свойства одинаковы для всех образцов; не зависят от размера выборки; и включают, например, цвет, физическое состояние и температуры плавления и кипения. Экстенсивные свойства зависят от количества материала и включают массу и объем. Соотношение двух экстенсивных свойств, массы и объема, является важным интенсивным свойством, называемым плотностью.
Экстенсивные свойства зависят от количества материала и включают массу и объем. Соотношение двух экстенсивных свойств, массы и объема, является важным интенсивным свойством, называемым плотностью.
Участники и авторство
Изменено Джошуа Халперном (Университет Говарда)
1.3: Classification of Matter распространяется под лицензией CC BY-NC-SA 4.0 и был создан, изменен и/или курирован LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.


 Только йодированную соль можно считать полноценным источником йода.
Только йодированную соль можно считать полноценным источником йода.
 Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.
Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.

 Если оно чистое, то вещество является либо элементом, либо соединением. Если вещество можно разделить на элементы, оно является соединением.
Если оно чистое, то вещество является либо элементом, либо соединением. Если вещество можно разделить на элементы, оно является соединением. Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.
Следовательно, компакт-диск не является химически чистым. B Области разного состава указывают на то, что компакт-диск представляет собой неоднородную смесь.
Leave A Comment