как изменяется внутренняя энергия тела при его охлаждении без совершения работы
РЕШИТЕ ФИЗИКУ ДАЮ 100 баллов 6. В цепи R = 12 Ом, R2 = 18 Ом, R3 = 40 Ом. Определите сопротивление резистора R4, если показание вольтметра U = ОВ (см. … рисунок). R3 R4
Пжу скільки разів зображення більше від свого предмета якщо предмет знаходить на віддалі 1,2F?
СРОЧНО! Даю 30 бточкове джерело світла силою 150кд створює на книзі освітленість 100 лк. під яким кутом падає світло на книгу якщо відаль між неї до … джерел світла 1 м?
До какой температуры была нагрета вода, полученная из 100 кг снега, взятого при температуре — 10 градусов Цельсия, если для этого в печи с КПД 20% сож … гли 22 кг дров? Удельная теплота сгорания дров равна 10 МДж/кг.
Щоб перетворити на воду 2 кг снігу, що має температуру-30°С, потрібна кількість теплоти щонайменше: А) 126 кДж Б) 660 кДж В) 330 кДж Г) 786 кДж С объя … снением пожалуйста
До какой температуры была нагрета вода, полученная из 100 кг снега, взятого при температуре — 10 градусов Цельсия, если для этого в печи с КПД 20% сож … гли 22 кг дров? Удельная теплота сгорания дров равна 10 МДж/кг.
До какой температуры была нагрета вода, полученная из 100 кг снега, взятого при температуре — 10 градусов Цельсия, если для этого в печи с КПД 20% сож … гли 22 кг дров? Удельная теплота сгорания дров равна 10 МДж/кг.
Дізнавшись, що вірні учні вирішили підкласти йому кнопку, учитель надів куленепробивні штани. Тепер кнопці, щоб подолати перешкоду між своїм вістрям і … вчителем, потрібно чинити тиск 4 000 000 000 Па. Чи зуміє кнопка дістатися до вчителя, якщо вага вчителя 700 Н, а площа вістря самої кнопки 0,2 мм2 ? пожалуйста срочно надо
СРОЧНО! ПЖ точкове джерело світла силою 150кд створює на книзі освітленість 100 лк. під яким кутом падає світло на книгу якщо відаль між неї до джерел … світла 1 м?
Помогите пожалуйста, надо найти к. к.д. цикла
к.д. цикла
1 Способы изменения внутренней энергии
1.4. Способы изменения внутренней энергии
I уровень: Прочитайте +§ 3
Внутренняя
энергия тела зависит от средней
кинетической энергии его молекул, а эта
энергия, в свою очередь, зависит от
температуры. Поэтому, изменяя температуру
тела, мы изменяем и его внутреннюю
энергию. При
нагревании тела его внутренняя энергия
увеличивается, при охлаждении уменьшается.
Изменяя внутреннюю энергию куска дерева путем трения, наши предки добывали огонь. Температура воспламенения дерева равна 250 °С. Поэтому, чтобы получить огонь, нужно тереть одним куском дерева по другому до тех пор, пока их температура не достигнет этого значения. Легко ли это? Когда таким способом попробовали добыть огонь герои романа Жюля Верна «Таинственный остров», у них ничего не вышло.
«Если бы энергию, которую затратили Наб с Пенкрофом, можно было превратить в тепло, ее, наверное, хватило бы для отопления котла океанского парохода. Но результат их усилий равнялся нулю. Куски дерева, правда, разогрелись, но значительно меньше, чем сами участники этой операции.
После
часа работы Пенкроф был весь в поту и с
досадой отбросил куски дерева, сказав:
—
Не говорите мне, что дикари добывают
огонь таким образом! Я скорее поверю,
что летом идет снег. Легче, пожалуй,
зажечь собственные ладони, потирая их
одну о другую».
Причина их неудачи заключалась в том, что огонь следовало добывать не простым трением одного куска дерева о другой, а сверлением дощечки заостренной палочкой
Многие
люди и в наше время «добывают» огонь
трением — трением спичек о спичечный
коробок. Давно ли появились спички?
Производство первых (фосфорных) спичек
началось в 30-х гг. XIX в. Фосфор загорается
при достаточно слабом нагревании — всего
до 60 °С. Поэтому, чтобы зажечь фосфорную
спичку, достаточно было чиркнуть ею
практически о любую поверхность (начиная
от ближайшей стены и кончая голенищем
сапог).
Итак, путем трения можно повысить температуру вещества. Совершая над телом работу (например, ударяя по куску свинца молотком, сгибая и разгибая проволоку, перемещая один предмет по поверхности другого или сжимая газ, находящийся в цилиндре с поршнем), мы увеличиваем его внутреннюю энергию. Если же тело само совершает работу
Внутреннюю энергию тела можно изменить и без совершения работы. Так, например, ее можно увеличить, нагрев на плите чайник с водой или опустив ложку в стакан с горячим чаем. Нагревается камин, в котором разведен огонь, крыша дома, освещаемая солнцем, и т. д. Повышение температуры тел во всех этих случаях означает увеличение их внутренней энергии, но это увеличение происходит без совершения работы.
Изменение внутренней энергии тела без совершения работы называется теплообменом. Теплообмен возникает между телами (или частями одного и того же тела), имеющими разную температуру.
Итак, существуют два способа изменения внутренней энергии: 1)совершение работы и 2) теплообмен.
Существенные признаки изменения внутренней энергии тела:
А. Изменение температуры тела (охлаждение, нагревание или даже переход в другое агрегатное состояние).
Б. Изменение объема (расширение, сжатие).
Интересно,
что оба рассмотренных способа могут
приводить к совершенно одинаковым
результатам. Поэтому по конечному
результату невозможно определить, каким
именно из этих способов он достигнут.
Так, взяв со стола нагретую стальную
спицу, мы не сможем сказать, каким
способом ее нагрели — путем трения или
соприкосновения с горячим телом.
II уровень: Ответьте на вопросы.
Укажите, в каких из перечисленных ниже случаях внутренняя энергия воды не меняется:
а) воду несут в ведре; б) переливают ее из ведра в чайник; в) нагревают до кипения.
Как можно отогреть озябшие руки, не используя нагретых предметов или теплых перчаток?
Каким способом — совершением работы или теплопередачей — изменялась внутренняя энергия детали при ее нагревании в печи перед закалкой? При сверлении в ней отверстия?
Почему при быстром скольжении вниз по шесту или канату можно обжечь руки?
Спичку можно зажечь, если поместить ее в пламя свечи или при ее трении о коробок. Одинаковы ли способы изменения внутренней энергии спички при ее возгорании?
III уровень: Ответьте на вопросы письменно:
Как изменится внутренняя энергия газа при его внезапном сжатии? Что будет свидетельствовать об изменении его внутренней энергии?
Чем объяснить, что при вколачивании гвоздя его шляпка почти не нагревается, но, когда гвоздь вбит, достаточно нескольких ударов, чтобы шляпка сильно нагрелась?
IV уровень: Сделайте опыт и ответе на вопросы письменно!
Возьмите медную монету, положите ее на лист картона или на деревянную, не покрытую лаком поверхность. Начинайте интенсивно двигать монету по поверхности. Посчитайте, сколько раз нужно передвинуть монету, чтобы она стала теплой, горячей. Почему монета нагрелась? Как изменилась внутренняя энергия монеты и за счет чего?
Возьмите гвоздь и деревянную палочку (можно карандаш ). Опустите их в сосуды с горячей водой. Что чувствуют ваши пальцы? Какой предмет нагрелся больше и почему? За счет чего изменяется внутренняя энергия этих предметов?
Способы изменения внутренней энергии | Физика
Внутренняя энергия тела зависит от средней кинетической энергии его молекул, а эта энергия, в свою очередь, зависит от температуры. Поэтому, изменяя температуру тела, мы изменяем и его внутреннюю энергию. При нагревании тела его внутренняя энергия увеличивается, при охлаждении уменьшается.
Поэтому, изменяя температуру тела, мы изменяем и его внутреннюю энергию. При нагревании тела его внутренняя энергия увеличивается, при охлаждении уменьшается.
Проделаем опыт. Укрепим на подставке тонкостенную латунную трубку. Нальем в нее немного эфира и плотно закроем пробкой. Теперь обовьем трубку веревкой и начнем натирать ею трубку, быстро вытягивая веревку то в одну, то в другую сторону. Через некоторое время внутренняя энергия трубки с эфиром возрастет настолько, что эфир закипит и образовавшийся пар вытолкнет пробку (рис. 60).
Этот опыт показывает, что внутреннюю энергию тела можно изменить путем совершения над телом работы, в частности трением.
Изменяя внутреннюю энергию куска дерева путем трения, наши предки добывали огонь. Температура воспламенения дерева равна 250 °С. Поэтому, чтобы получить огонь, нужно тереть одним куском дерева по другому до тех пор, пока их температура не достигнет этого значения. Легко ли это? Когда таким способом попробовали добыть огонь герои романа Жюля Верна «Таинственный остров», у них ничего не вышло.
«Если бы энергию, которую затратили Наб с Пенкрофом, можно было превратить в тепло, ее, наверное, хватило бы для отопления котла океанского парохода. Но результат их усилий равнялся нулю. Куски дерева, правда, разогрелись, но значительно меньше, чем сами участники этой операции.
После часа работы Пенкроф был весь в поту и с досадой отбросил куски дерева, сказав:
— Не говорите мне, что дикари добывают огонь таким образом! Я скорее поверю, что летом идет снег. Легче, пожалуй, зажечь собственные ладони, потирая их одну о другую».
Причина их неудачи заключалась в том, что огонь следовало добывать не простым трением одного куска дерева о другой, а сверлением дощечки заостренной палочкой (рис. 61). Тогда при определенной сноровке можно за 1 с увеличить температуру в гнезде палочки на 20 °С. А чтобы довести палочку до горения, потребуется всего лишь 250/20=12,5 секунды!
Многие люди и в наше время «добывают» огонь трением — трением спичек о спичечный коробок. Давно ли появились спички? Производство первых (фосфорных) спичек началось в 30-х гг. XIX в. Фосфор загорается при достаточно слабом нагревании — всего до 60 °С. Поэтому, чтобы зажечь фосфорную спичку, достаточно было чиркнуть ею практически о любую поверхность (начиная от ближайшей стены и кончая голенищем сапог). Однако эти спички были очень опасны: они были ядовиты и из-за легкого возгорания часто служили причиной пожара. Безопасные спички (которыми мы пользуемся до сих пор) были изобретены в 1855 г. в Швеции (отсюда их название «шведские спички») Фосфор в этих спичках заменен другими горючими веществами.
Давно ли появились спички? Производство первых (фосфорных) спичек началось в 30-х гг. XIX в. Фосфор загорается при достаточно слабом нагревании — всего до 60 °С. Поэтому, чтобы зажечь фосфорную спичку, достаточно было чиркнуть ею практически о любую поверхность (начиная от ближайшей стены и кончая голенищем сапог). Однако эти спички были очень опасны: они были ядовиты и из-за легкого возгорания часто служили причиной пожара. Безопасные спички (которыми мы пользуемся до сих пор) были изобретены в 1855 г. в Швеции (отсюда их название «шведские спички») Фосфор в этих спичках заменен другими горючими веществами.
Итак, путем трения можно повысить температуру вещества. Совершая над телом работу (например, ударяя по куску свинца молотком, сгибая и разгибая проволоку, перемещая один предмет по поверхности другого или сжимая газ, находящийся в цилиндре с поршнем), мы увеличиваем его внутреннюю энергию. Если же тело само совершает работу (за счет своей внутренней энергии), то внутренняя энергия тела уменьшается и тело охлаждается.
Пронаблюдаем это на опыте. Возьмем толстостенный стеклянный сосуд и плотно закроем его резиновой пробкой с отверстием. Через это отверстие с помощью насоса начнем накачивать в сосуд воздух. Через некоторое время пробка с шумом вылетит из сосуда, а в самом сосуде появится туман (рис. 62). Появление тумана означает, что воздух в сосуде стал холоднее и, следовательно, его внутренняя энергия уменьшилась. Объясняется это тем, что находившийся в сосуде сжатый воздух, выталкивая пробку, совершил работу за счет уменьшения своей внутренней энергии. Поэтому температура воздуха и понизилась.
Внутреннюю энергию тела можно изменить и без совершения работы. Так, например, ее можно увеличить, нагрев на плите чайник с водой или опустив ложку в стакан с горячим чаем. Нагревается камин, в котором разведен огонь, крыша дома, освещаемая солнцем, и т. д.
Повышение температуры тел во всех этих случаях означает увеличение их внутренней энергии, но это увеличение происходит без совершения работы.
Изменение внутренней энергии тела без совершения работы называется теплообменом. Теплообмен возникает между телами (или частями одного и того же тела), имеющими разную температуру.
Как, например, происходит теплообмен при контакте холодной ложки с горячей водой? Сначала средняя скорость и кинетическая энергия молекул горячей воды превышают среднюю скорость и кинетическую энергию частиц металла, из которого изготовлена ложка. Но в тех местах, где ложка соприкасается с водой, молекулы горячей воды начинают передавать часть своей кинетической энергии частицам ложки, и те начинают двигаться быстрее. Кинетическая энергия молекул воды при этом уменьшается, а кинетическая энергия частиц ложки увеличивается. Вместе с энергией изменяется и температура: вода постепенно остывает, а ложка нагревается. Изменение их температуры происходит до тех пор, пока она и у воды, и у ложки не станет одинаковой.
Часть внутренней энергии, переданной от одного тела к другому при теплообмене, обозначают буквой Q и называют количеством теплоты.
Q — количество теплоты.
Количество теплоты не следует путать с температурой. Температура измеряется в градусах, а количество теплоты (как и любая другая энергия) — в джоулях.
При контакте тел с разной температурой более горячее тело отдает некоторое количество теплоты, а более холодное тело его получает.
Итак, существуют два способа изменения внутренней энергии: 1) совершение работы и 2) теплообмен. При осуществлении первого из этих способов внутренняя энергия тела изменяется на величину совершенной работы А, а при осуществлении второго из них — на величину, равную количеству переданной теплоты Q.
Интересно, что оба рассмотренных способа могут приводить к совершенно одинаковым результатам. Поэтому по конечному результату невозможно определить, каким именно из этих способов он достигнут. Так, взяв со стола нагретую стальную спицу, мы не сможем сказать, каким способом ее нагрели — путем трения или соприкосновения с горячим телом. В принципе могло быть как то, так и другое.
В принципе могло быть как то, так и другое.
1. Назовите два способа изменения внутренней энергии тела. 2. Приведите примеры увеличения внутренней энергии тела путем совершения над ним работы. 3. Приведите примеры увеличения и уменьшения внутренней энергии тела в результате теплообмена. 4. Что такое количество теплоты? Как оно обозначается? 5. В каких единицах измеряется количество теплоты? 6. Какими способами можно добыть огонь? 7. Когда началось производство спичек?
Экспериментальное задание. Прижмите монету или кусочек фольги к картону или какой-либо дощечке. Сделав сначала 10, затем 20 и т. д. движений то в одну, то в другую сторону, заметьте, что происходит с температурой тел в процессе трения. Как зависит изменение внутренней энергии тела от величины совершенной работы?
Füüsika 9. klassile. Soojusõpetus
20
ȁ
ȌȒȑȏȄȌȌȞȞ ȜȌȄȏȂȇȞ
Мы очень часто используем слово
теплота
и производные от него другие
слова:
тепло, холодно, нагревание
и т. д. В быту мы говорим, что
суп теплый,
комната холодная, электрорадиатор нагревает комнату, радиатор передает
тепло воздуху.
Два первых утверждения можно выразить на языке физики,
используя понятие температуры:
температура супа 50
°
С, температура
воздуха в комнате 16
°
С.
Что же в физике понимают под словом
теплота
?
Внутренняя энергия тела
Объясним это следующим образом. Чтобы радиатор потеплел, необходи-
ма энергия. Эта энергия расходуется на увеличение скорости движения ча-
стиц вещества. Благодаря тепловому движению частицы вещества обладают
кинетической энергией. При увеличении скорости движения частиц увели-
чивается и их кинетическая энергия.
Результатом нагревания является уве-
личение кинетической энергии частиц
.
Когда радиатор нагревает воздух, кинетическая энергия частиц воздуха
увеличивается, увеличивается и полная энергия этих частиц.
С газами – проще, у них частицы вещества практически не взаимодей-
ствуют, поэтому вся кинетическая энергия частиц газа и является его
вну-
тренней энергией
. В твердых и жидких веществах частицы взаимодействуют
друг с другом. Взаимодействующие тела обладают потенциальной энергией.
Следовательно, потенциальной энергией обладают и взаимодействующие
друг с другом частицы. Сумма кинетической и потенциальной энергий ча-
стиц вещества является
внутренней энергией тела
. Таким образом, внутрен-
няя энергия тела складывается из кинетической и потенциальной энергий.
Внутренняя энергия зависит от скорости движения частиц вещества и их вза-
имного расположения.
Скорость движения частиц вещества изменяется при нагревании или
охлаждении тела, при этом изменяются и расстояния между частицами (теп-
ловое расширение). Расстояние между частицами изменяется также при
изменении состояния вещества: отвердевании жидкостей или плавлении
твердых тел, а также испарении жидкостей и конденсации пара.
Внутренняя
энергия тела изменяется как при изменении температуры вещества, так и
при изменении его состояния
.
Теплота, тепловая энергия и количество теплоты
Используемое в обычном разговорном языке слово
теплота
в физике по-
нимается как кинетическая компонента внутренней энергии, в этом же значе-
нии понимаются и слова тепловая энергия (см. таблицу 2.6.1.).
таблицу 2.6.1.).
Разговорный язык
Язык физики
тепло, холодно = температура
тепло, теплота,
тепловая энергия = кинетическая компонента
внутренней энергии
нагревание = увеличение кинетической компоненты
внутренней энергии
охлаждение = уменьшение кинетической компоненты
внутренней энергии
Таблица 2.6.1. Соответ-
ствие между значениями
физических терминов и
слов разговорного языка.
3. В каком случае
изменяется внутренняя
энергия тела?
4. Что в физике понимают
под словом
теплота
?
2. От чего зависит
величина внутренней
энергии тела?
1. Что происходит
с частицами вещества
при его нагревании и
охлаждении?
6
Тепло, теплота и внутренняя энергия тела Текст научной статьи по специальности «Физика»
Научный журнал КубГАУ, №111(07), 2015 года
1
УДК 536.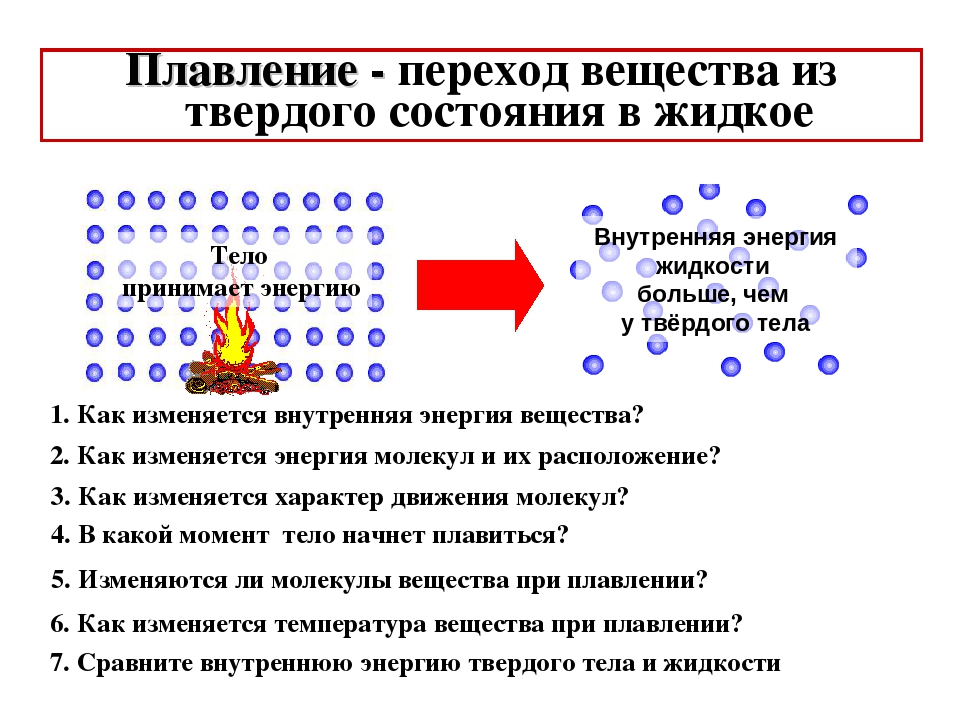 1 UDC 536.1
1 UDC 536.1
01.00.00 Физико-математические науки Physics and mathematical sciences
ТЕПЛО, ТЕПЛОТА И ВНУТРЕННЯЯ ЭНЕРГИЯ WARM, WARMTH AND INTERNAL ENERGY OF A ТЕЛА BODY
Александров Борис Леонтьевич Alexandrov Boris Leontievich
д.г.-м..н., профессор Dr.Sci.Geol.-Min., professor
[email protected] [email protected]
Кубанский государственный аграрный университет, Kuban state agrarian University, Krasnodar, Russia Краснодар, Россия
Обсуждается вопрос понятия теплоты и внутренней энергией тела. Дается анализ этих понятий в историческом аспекте и представления автора, основанные на новой фотонной теории строения атома. Анализ исторического аспекта этого вопроса показывает, что понятия тепла, теплоты и внутренней энергии тела долгое время ассоциировалось с понятием теплорода, который может перетекать в веществе. Следующим этапом отождествления понятия теплоты явилась энергия, связанная с движением и работой. В соответствии с этим, Клаузиус обосновал эквивалентность тепла и работы как первое начало теории тепла и ввел понятие внутренней энергии, которую можно увеличить двумя путями — производя над телом работу и подводя к нему тепло. Таким образом, энергия явилась главным объединяющим фактором работы и теплоты. Далее кинетическая теория тепла, как энергия движения молекул, была развита Максвеллом и модель теплорода оказалась помехой в развитии теории тепла. Фактически внутреннюю энергию тела определяют фотоны, вращающиеся вокруг заряженных частиц в атомах по своим орбиталям. Определенные серии фотонов объединяются в отдельные фотонные орбитали, направления вращения фотонов в которых отличаются друг от друга. Таким образом, тело обладает внутренней энергией или внутренней теплотой. Она обусловлена энергией фотонов, вращающихся вокруг электронов на внешней оболочке каждого атома, а также вокруг заряженных частиц — протонов и электронов в ядре атома. Эта внутренняя энергия может увеличиваться при механическом воздействии на тело, приводящее к увеличению результирующей частоты колебаний фотонов вокруг заряженных частиц атомов и эта внутренняя теплота, содержащаяся в теле, может перетекать от тела с большей концентрацией теплоты к телу с меньшей концентрацией теплоты
Она обусловлена энергией фотонов, вращающихся вокруг электронов на внешней оболочке каждого атома, а также вокруг заряженных частиц — протонов и электронов в ядре атома. Эта внутренняя энергия может увеличиваться при механическом воздействии на тело, приводящее к увеличению результирующей частоты колебаний фотонов вокруг заряженных частиц атомов и эта внутренняя теплота, содержащаяся в теле, может перетекать от тела с большей концентрацией теплоты к телу с меньшей концентрацией теплоты
The article discusses the question of the concepts of heat and internal energy of a body. The analysis of these concepts in the historical aspect and the views of the author, based on the new photon theory of atomic structure were presented in this study. The analysis of the historical aspect of this question tells that the concepts of heat and internal energy of the body for a long time were associated with the concept of caloric, which can flow in the substance. The next step was the identification of the concept of heat with energy linked with the movement and work. In accordance with this, Clausius proved the equivalence of heat and work as the first principle of the theory of heat and introduced the concept of internal energy, which can be increased in two ways — making work on body, and summing heat to it. Thus, energy was the main uniting factor of work and heat. Then, the kinetic theory of heat, as the energy of motion of molecules, was developed by Maxwell and caloric model turned out to be a hindrance in the development of the theory of heat. In fact, the internal energy of the body is determined photons, rotating around charged particles in atoms in their orbitals. The series of photons are combined into a single photon orbital direction of rotation of the photons, which are different from each other. Thus, the body has an internal energy or internal heat. It is due to the energy of photons, orbiting electrons in the outer shell of each atom, as well as around the charged particles -electrons and protons in the nucleus of an atom. This internal energy may be increased by mechanical action on the body, leading to an increase in resulting oscillation frequency of photons around charged particles of atoms and the internal heat contained in the body can flow of the body with a higher concentration of heat to the body with a lower concentration of heat
This internal energy may be increased by mechanical action on the body, leading to an increase in resulting oscillation frequency of photons around charged particles of atoms and the internal heat contained in the body can flow of the body with a higher concentration of heat to the body with a lower concentration of heat
Ключевые слова: ТЕПЛОТА, РАБОТА, ЭНЕРГИЯ, Keywords: HEAT, WORK, ENERGY, PHOTON
ФОТОН
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
2
Введение
Теория тепла возникла не сразу. Очень долго не могли понять что такое тепло, теплота и какая разница между температурой и теплом. Понятие «тепло», «теплота» и «температура» разделить было очень трудно. И в настоящее время этим понятиям нет ясного определения. Так, в соответствии со словарем русского языка С.И. Ожегова [3], «тепло»- это «нагретое состояние чего-нибудь», а «теплота» означает «теплый» или это «форма движения материи — энергия, образуемая беспорядочным движением частиц тела (молекул, атомов и т.п.)» Поэтому всем вроде бы ясно, что когда нагревают тело, температура его повышается. Когда тепло перетекает от одного тела к другому, температура одного тела падает, а другого — повышается. Тепло во многих случаях ведет себя, как ручей, текущий с горы в долину. Поэтому многие ученые прошлого времени думали, что теплота — это вещество. Они считали ее жидкостью (флюидом), которая может перетекать от одного тела к другому. Этот флюид получил название теплорода. Аналогия между теплом и жидкостью стала еще более убедительной после открытия электрических явлений: электрический ток также течет по проводам, как река, выравнивания потенциал между двумя заряженными телами. Модель теплорода объясняла очень многое и завоевала широкое признание в последней четверти XVIII века. Теплород, казалось, хорошо объяснял свойства тепла. Теория теплового двигателя, построенного Карно, была основана на модели теплорода. Тот факт, что большинство веществ расширяется при нагревании и сжимается при охлаждении, казалось, подтверждал материальную теорию теплоты, потому что теплород занимает место.
Модель теплорода объясняла очень многое и завоевала широкое признание в последней четверти XVIII века. Теплород, казалось, хорошо объяснял свойства тепла. Теория теплового двигателя, построенного Карно, была основана на модели теплорода. Тот факт, что большинство веществ расширяется при нагревании и сжимается при охлаждении, казалось, подтверждал материальную теорию теплоты, потому что теплород занимает место.
Смущало только то обстоятельство, что имеется несколько веществ, которые при нагревании сжимаются, а при охлаждении расширяются. Кроме того, если теплота есть вещество, то в горячем состоянии тело должно весить больше, чем в холодном. Опыт, однако, показывал, что это не так. Таким
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
3
образом, модель теплорода не выдерживала испытаний, когда дело касалось закона сохранения. Рассуждали так: если бы тепло было какой-то жидкостью, то она, протекая, сохранялась бы, ее количество не должно было изменяться. Сколько тепла забрали от нагревателя, столько должен получить и холодильник.
На первый взгляд так оно и есть: охлаждается чайник, нагревается воздух. Но часто бывает совсем не так.
Исторический обзор изменения представлений о теплоте и энергии
Первым, кто обратил на это внимание, был Бенджамен Томсон (граф Румфорд). Наблюдая за сверлением пушечных стволов, он заметил выделение большого количества тепла, — особенно, если сверла были тупые. Это заставило его задуматься, что могло быть источником теплоты. Согласно теории теплорода, теплота могла появиться или из металла, или из окружающего пространства. Но, ни то, ни другое, по мнению Румфорда, не являлось источником теплоты. Чтобы проверить теорию, Румфорд взвесил заготовку ствола до сверления и потом взвесил ствол и стружки после сверления. Оба взвешивания дали одинаковый результат. Единственное решение могло бы состоять в том, что в стружках содержится меньше теплорода, чем в сплошной отливке, и избыток его выделяется при сверлении. Но тогда стружку было бы легче нагреть, чем сплошной металл, у стружек должна была быть меньше теплоемкость, чем у сплошного металла. Но это также не подтвердилось опытом. Он применил для охлаждения ствола воду, но все равно ствол при сверлении нагревался.
Но, ни то, ни другое, по мнению Румфорда, не являлось источником теплоты. Чтобы проверить теорию, Румфорд взвесил заготовку ствола до сверления и потом взвесил ствол и стружки после сверления. Оба взвешивания дали одинаковый результат. Единственное решение могло бы состоять в том, что в стружках содержится меньше теплорода, чем в сплошной отливке, и избыток его выделяется при сверлении. Но тогда стружку было бы легче нагреть, чем сплошной металл, у стружек должна была быть меньше теплоемкость, чем у сплошного металла. Но это также не подтвердилось опытом. Он применил для охлаждения ствола воду, но все равно ствол при сверлении нагревался.
Полученные результаты убедили Румфорда, что теплород, если он действительно существует, не мог прийти ни из металла, ни из окружающего пространства. Все это никак не укладывалось в простую модель перетекающего с места на место теплорода.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
4
Так как никаких других возможных источников теплоты не было, Румфорд заключил, что теплота получалась как результат работы сверления. Другими словами, он пришел к выводу, что теплота — энергия. Как описано в [8], для дальнейшей проверки гипотезы Румфорда, что теплота — это энергия, современник Румфорда Хемфри Дэви (1778-1829) придумал очень простой решающий опыт. Опыт состоял в трении двух кусков льда друг о друга при температуре ниже температуры плавления этих кусков льда. Оказалось, что при этом лед плавился, и отсюда неизбежно вытекало заключение, что теплота, которая расплавляла лед, получалась из работы на преодоление трения кусков льда. Таким образом, чаша весов склонялась к тому, чтобы связать природу теплоты с движением.
Понятие о величине, характеризующей движение и имеющей по современной терминологии размерность «энергии», впервые появилось в механике. Основоположниками здесь являются Галилей (1564-1642), Гюйгенс (1629-1695) и Ньютон (1642-1727). Согласно этим авторам при падении тела массой m с высоты h и ускорении силы тяжести g убыль потенциальной энергии тела (его гравитационной энергии) Д( mgh) равна
Основоположниками здесь являются Галилей (1564-1642), Гюйгенс (1629-1695) и Ньютон (1642-1727). Согласно этим авторам при падении тела массой m с высоты h и ускорении силы тяжести g убыль потенциальной энергии тела (его гравитационной энергии) Д( mgh) равна
mvL
приращению его кинетической энергии ——.
Сформулированный здесь закон сохранения энергии до середины XIX века казался частным случаем, реализующимся в «чистой механике» в отсутствии трения. Да и самого понятия «энергия» не было до начала XIX века, когда оно было введено в механику Юнгом. Р.Клаузиусу (1864) приписывают идею окончательного введения этого термина в физику.
Так что же такое энергия? Ее нельзя увидеть, потрогать или понюхать как какое-нибудь вещество. Она представляет для нас более абстрактное понятие. Поэтому следует попытаться проанализировать
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
5
существующие определения энергии и рассмотреть это понятие с общих позиций, прежде чем углубляться в дальнейшее обсуждение.
Энергия (от греческого energeia — действие, деятельность) — общая количественная мера движения и взаимодействия всех видов материи [6]. Энергия не возникает из ничего и не исчезает, она может только переходить их одной формы в другую. Энергия связывает воедино все явления природы.
Ранее часто вместо энергии говорили «сила», приписывая один и тот же термин величинам разной размерности. Даже Гельмгольц (1874) статью, посвященную закону сохранения энергии, озаглавил «О сохранении силы». Между тем по Ньютону сила — это причина, вызывающая движение, которая, совершая на известном пути работу, сообщает телу энергию. Таким образом, с понятием энергии неразрывно связано другое понятие той же размерности — «работа».
Между тем по Ньютону сила — это причина, вызывающая движение, которая, совершая на известном пути работу, сообщает телу энергию. Таким образом, с понятием энергии неразрывно связано другое понятие той же размерности — «работа».
Работа (А), совершаемая системой, обусловлена взаимодействием между системой и внешней средой, в результате которого преодолеваются внешние силы, нарушившие равновесие в системе. Работа определяется суммой произведений действующих на систему сил на соответствующий путь (давление, изменение объема, поверхностного натяжения, изменение поверхности и т.д.)
Таким образом, работа процесса — это энергия, передаваемая одним телом другому при их взаимодействии, не зависящая от температуры этих тел и не связанная с переносом вещества от одного тела к другому [2].
Наиболее затруднительным явилось установление общего закона сохранения энергии, включая действия диссипативных сил, приводящих к рассеянию работы и превращению ее в теплоту.
Р.Клаузиус (1850) первый заговорил об эквиваленте тепла и работы как о первом начале теории тепла и написал уравнение, которого не хватало Карно. Для этого надо было, прежде всего, сказать простую вещь:
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
6
всякое тело имеет внутреннюю энергию. Принято считать [6], что внутренняя энергия равна сумме кинетической энергии хаотического движения молекул относительно центра масс тел и потенциальной энергии взаимодействия молекул друг с другом. Внутреннюю энергию можно увеличить двумя путями — производя над телом работу (АЛ) и подводя к нему тепло (AQ).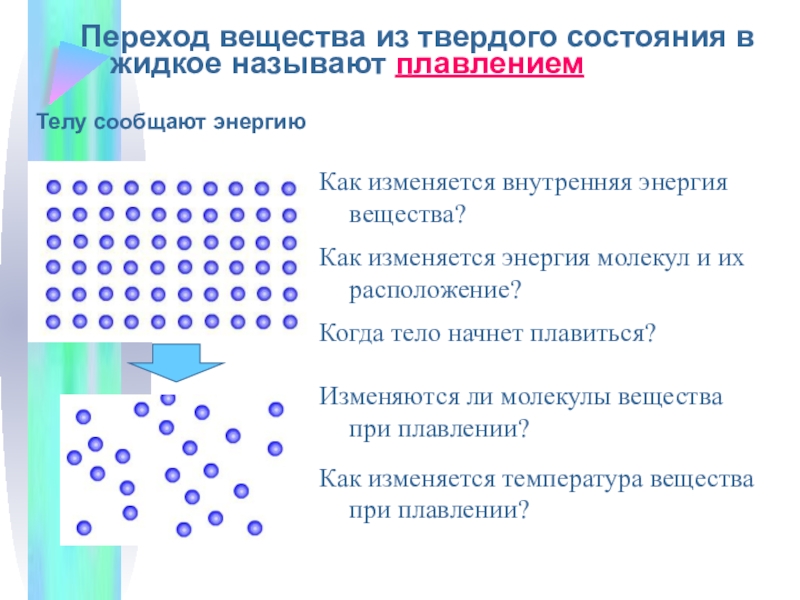
Смысл этого глубокого утверждения заключен в союзе «и» и описывается простой формулой
AU = AQ + АЛ (1)
Очень важно понимать, что по конечному состоянию системы нельзя никаким образом обнаружить, за счет чего система увеличила свою энергию: за счет тепла или за счет работы. Сам Р.Клаузиус называл U -«теплом, содержащимся в теле», противопоставляя ему Q — «тепло, сообщенное телу». В этом отличии кроется глубокий смысл. Сейчас U называют внутренней энергией (или просто энергией), а AU есть ее приращение.
Таким образом, единственный элемент — энергия — связывает воедино чрезвычайно широкое многообразие явлений, а закон сохранения этого «элемента» не знает исключений ни в макро-, ни в микромире. Энергия, по Ф.Энгельсу, есть мера движения при переходе одной формы движения в другую [9]. Это определение философа дополняет определение физика М.Планка: «Энергия материальной системы в определенном состоянии, взятая по отношению к другому определенному «нулевому» состоянии, имеет однозначное значение» [4]. На основании этого можно говорить о запасе или о «содержании» энергии в системе. Энергия системы однозначно зависит от параметров, характеризующих состояние системы. В случае непрерывной среды или поля вводятся понятия плотности энергии, т.е. энергии в единице объема, и плотности потока энергии, равной произведению плотности энергии на скорость ее перемещения.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
7
А.Эйнштейн показал, что энергия тела (E) неразрывно связана с его массой т соотношением
E = mc2, (2)
где с — скорость света.
Любое тело обладает энергией. Если масса покоящегося тела m0, то его энергия покоя Е0 = т0с ; эта энергия может переходить в другие виды энергии при превращениях частиц (распадах, ядерных реакциях и так далее). Ю.Г.Белостоцкий [7, стр.15] высказал предположение, что при ускорении материального тела происходит увеличение его собственного гравиполя, причем запас кинетической энергии содержится в гравитационном поле движущегося тела. Это, по его мнению, позволяет определить энергию как процесс превращения вещества в поле. Поэтому
формула E = тс2 характеризует зависимость количества энергии тела от количества превращенного вещества в поле, причем т в этой формуле является полевой массой.
Рассматривая идеальные газы на базе эфирной природы теплоты С.Д.Брусин и Л.Д.Брусин [7, стр.24] отмечают, что количество тепловой энергии Q характеризуется массой эфира «т» и определяется простым
соотношением Q = тс2 (где с — скорость света). Газы представляются состоящими из частичек, сгруппированных в молекулы, и эфира, находящегося как между частичками молекул (молекулярная область), так и между молекулами (межмолекулярная область).
Согласно классической физике энергия любой системы меняется непрерывно и может принимать любые значения. Квантовая теория утверждает, что энергия микрочастиц, движение которых происходит в ограниченном объеме пространства (например, электронов в атоме), принимает дискретный ряд значений. Так, атомы испускают
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
8
электромагнитную энергию в виде дискретных порций — световых квантов или фотонов.
Опыт, накопленный при наблюдении множества различных процессов, свидетельствует о том, что хотя энергия может передаваться от одного тела к другому, а также переходить из одной формы в другую, она никогда не создается из ничего и не исчезает.
Подобные наблюдения, подтвержденные количественными измерениями теплоты и работы, лежат в основе первого закона термодинамики.
Ситуация с энергией во многом напоминает ситуацию с веществом — при любом приращении энергии некоторая часть ее всегда превращается в теплоту, которая рассеивается в окружающую среду и, следовательно, не может быть использована для выполнения работы. Так, на практике большая часть энергии, запасенной в угле или бензине, превращается в теплоту. Таким образом, энергия — это способность к выполнению работы, переносу тепла, а работа и теплота являются количественными характеристиками двух форм обмена энергией между системой и окружающей средой, причем работа является макрофизической формой передачи энергии, а теплота микрофизической. Эти превращения, согласно Майеру, осуществляются в определенных эквивалентах соотношениях. Однако, согласно второму закону термодинамики эти формы не равноценны и если в каком-то процессе работа превращается в теплоту (например, посредством трения), то такое превращение ничем не ограниченно, обратное же превращение теплоты в работу ограниченно определенными условиями. В этом и заключается главная «хитрость» природы, путь к пониманию которой оказался столь трудным и долгим [8]. Была еще одна трудность, которую встретила модель теплорода. Если теплород — это род жидкости, которая совершает работу при перетекании от более высокого уровня (от более высокой температуры) к более
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
9
низкому, то нельзя было понять, что происходит в неоднородно нагретом теле в процессе выравнивания температуры. Куда девается работа, которая должна возникнуть при перетекании теплорода.
Куда девается работа, которая должна возникнуть при перетекании теплорода.
Но даже если не обращать внимания на «пропажу» работы, такая картина не смогла объяснить, как передается тепло через вакуум -например, от Солнца к Земле. Говорили о колебаниях эфира, но получить из таких представлений сколько-нибудь убедительную теорию было нельзя. Теория теплорода явно терпела одну неудачу за другой. Согласившись, что теплота есть энергия, естественно было задать вопрос: на что идет эта энергия? Известно, что потенциальная энергия есть энергия положения, а кинетическая — энергия движения. Может ли теплота быть одним из этих видов энергии или быть может, и тем и другим сразу? Мы уже знаем, что вещество построено из молекул, и что если газ или жидкость нагревается, то броуновское движение, как показывают наблюдения, становится более оживленным. Это указывает на усиление движения молекул. Такие наблюдения возможны только в жидкостях и газах, но легко согласиться, что при нагревании, увеличиваются колебания молекул и в твердых телах. Таким образом, экспериментальные наблюдения в сочетании с логическими заключениями привели к выводу, что теплота есть кинетическая энергия молекулярного движения. О том, что теплота связана с движением, говорили многие естествоиспытатели. Писал об этом Декарт. Галилей был одним из первых, кто писал о механической природе тепла. Даниил Бернулли пытался вывести формулу для давления газа. Гук очень ясно говорил о связи между теплотой и движением — колебаниями частиц в нагретом теле. Подобные идеи высказывали Ломоносов, многие философы. Но они не могли превратить эти высказывания в физическую теорию, которую можно проверить на опыте.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
10
Количественная связь энергии с теплотой была установлена в опыте Джеймса Джоуля (1873). Джоуль показал, что, размешивая мешалкой жидкость и нагревая ее таким образом, надо тратить 460 кгс-м (килограмм-сила на метр) работы на каждую большую калорию, полученную жидкостью. Несколько раньше Джоуля эту же величину, но с меньшей точностью (365 кгс-м/ккал) вычислил Роберт Майер, использовав результаты опытов Г ей-Люссака по расширению газов в пустоту.
Джоуль показал, что, размешивая мешалкой жидкость и нагревая ее таким образом, надо тратить 460 кгс-м (килограмм-сила на метр) работы на каждую большую калорию, полученную жидкостью. Несколько раньше Джоуля эту же величину, но с меньшей точностью (365 кгс-м/ккал) вычислил Роберт Майер, использовав результаты опытов Г ей-Люссака по расширению газов в пустоту.
Дальше всех продвинулся Максвелл. Принято считать, что кинетическая теория тепла, созданная Максвеллом, позволила понять тепловые явления на основе классической механики. В работе Максвелла появилась формула для распределения движущихся частиц по скоростям: формула позволила вычислить постоянные, характеризующие свойства тел, — такие, как теплопроводность и вязкость газа, и установить их зависимость от температуры. Максвелл положил начало статистической физики или кинетической теории газов. Но как отмечает Я.А.Смородинский [5], у Максвелла был предшественник — Ватерсон, первую формулу новой теории тепла которого мало кто заметил. Как описано в [5], в 1845г. в английскую академию наук (Королевское общество) была представлена работа Ватерсона. В ней было показано, что давление газа на стенки сосуда можно объяснить ударами атомов. Хотя сама идея о том, что газ состоит из атомов, была не нова, мало кто принимал всерьез утверждение, что атомы могут свободно двигаться в сосуде от стенки к стенке, а упругие свойства газа можно свести просто к классической механике атомов.
Работа Ватерсона не понравилась членам ученого общества и рецензентом королевского общества была отклонена. Лишь много лет спустя в 1892г. Рэлей нашел ее в архиве и опубликовал в журнале «философские сообщения Королевского общества». То, что было сделано одним человеком и осталось незамеченным, было открыто впоследствии
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
11
лишь в результате работы нескольких ученых, а окончательная формула была написана Максвеллом только в 1859г. nst = 100°С, безусловно имеет более высокую кинетическую энергию. Но так как система не выявляет себя нагревом, а кинетическая энергия молекул системы, как принято и сегодня, растет только с увеличением температуры, то и
nst = 100°С, безусловно имеет более высокую кинетическую энергию. Но так как система не выявляет себя нагревом, а кинетическая энергия молекул системы, как принято и сегодня, растет только с увеличением температуры, то и
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
12
делается неверный вывод, что полученное системой тепло затрачивается только на изменение потенциальной энергии. Более того, как можно интерпретировать работу расширения воды при ее охлаждении от +4оС до 0оС в жидком состоянии? При охлаждении выделяется теплота и одновременно совершается работа расширения можно считать за счет убыли внутренней энергии в соответствии с формулой (1) .
Однако при кристаллизации температура не изменяется, т.е. внутренняя энергия должна оставаться постоянной, но происходит увеличение объема, т.е. совершается работа расширения. За счет чего же совершается работа расширения, если одновременно с этим при кристаллизации выделяется теплота кристаллизации? Ответа на этот вопрос в научной литературе нет.
Современное представление сущности теплоты и внутренней
энергии
По нашим представлениям [1], это возможно лишь в том случае, если принять, что внутреннюю энергию в любом теле определяют фотоны, вращающиеся вокруг заряженных частиц в атомах по своим орбитам, причем энергия (е) каждого фотона, в соответствии с формулой Планка (e=hv), пропорциональна его частоте v (где h — постоянная Планка). Определенные серии фотонов объединяются в отдельные фотонные орбитали, направления вращения фотонов в которых отличаются друг от друга. Химическое взаимодействие атомов происходит не просто через валентные электроны атомов, а с учетом внешних фотонных орбиталей вокруг этих электронов. Когда излучаются фотоны внешних орбиталей, то происходит перестройка кристаллической решетки атомов и в целом молекул, например воды, между собой за счет контакта их следующими фотонными орбиталями, направления вращения которых вокруг электронов иное.
Химическое взаимодействие атомов происходит не просто через валентные электроны атомов, а с учетом внешних фотонных орбиталей вокруг этих электронов. Когда излучаются фотоны внешних орбиталей, то происходит перестройка кристаллической решетки атомов и в целом молекул, например воды, между собой за счет контакта их следующими фотонными орбиталями, направления вращения которых вокруг электронов иное.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
13
Таким образом, тело обладает внутренней энергией или внутренней теплотой. Она обусловлена энергией фотонов, вращающихся вокруг электронов на внешней оболочке каждого атома тела, а также вокруг заряженных частиц — протонов и электронов в ядре атома. Эта внутренняя энергия тела может увеличиваться при механическом воздействии на тело, приводящее к увеличению результирующей частоты колебаний фотонов вокруг заряженных частиц атомов вещества и эта внутренняя теплота, содержащаяся в теле, может перетекать от тела с большей концентрацией теплоты к телу с меньшей концентрацией теплоты или при наличии перепада температур с окружающей средой путем теплового электромагнитного излучения за счет внешних фотонных орбиталей электронов атомов или при ядерных процессах за счет излучения фотонов гамма-квантов, вращающихся вокруг нуклонов в ядрах.
Выводы
1.Энергию любого тела можно подразделить на механическую энергию, включая кинетические энергии поступательного и вращательного движений и потенциальную энергию тела относительно поверхности Земли, и внутреннюю энергию тела или внутреннюю теплоту. Последняя обусловлена энергией фотонов, вращающихся вокруг электронов на внешней оболочке атома, а также вокруг заряженных частиц — протонов и электронов в ядре атома. Внутренняя энергия тела может увеличиваться не только за счет дополнительного поглощения фотонов, но и при механическом воздействии на тело, приводящее к увеличению результирующей частоты колебаний фотонов вокруг заряженных частиц атомов вещества. Таким образом, теплота — это сконцентрированная энергия фотонов, обусловленная как собственной частотой этих фотонов, так и дополнительной частотой за счет механической работы. Последняя приводит к повышению результирующей частоты колебания фотонов и, следовательно, их энергии. Без наличия
Внутренняя энергия тела может увеличиваться не только за счет дополнительного поглощения фотонов, но и при механическом воздействии на тело, приводящее к увеличению результирующей частоты колебаний фотонов вокруг заряженных частиц атомов вещества. Таким образом, теплота — это сконцентрированная энергия фотонов, обусловленная как собственной частотой этих фотонов, так и дополнительной частотой за счет механической работы. Последняя приводит к повышению результирующей частоты колебания фотонов и, следовательно, их энергии. Без наличия
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
14
фотонов в веществе механически невозможно повысить количества теплоты в нем.
2.Роль теплорода в веществе выполняют фотоны, вращающиеся вокруг заряженных частиц в атомах. При наличии перепада концентрации фотонов вокруг внешних валентных электронов, происходит их перераспределение в область более низкой концентрации, т.е. внутренняя энергия тела может перетекать от тела с большей концентрацией теплоты к телу с меньшей концентрацией теплоты.
Литература
1. Александров Б. Л. Роль фотонов в физических и химических явлениях// Б. Л. Александров, М.Б. Родченко, А.Б. Александров. — Краснодар, ГУП «Печатный двор Кубани», 2002- 543 с.
2. Каркапетьянц М.Х. Химическая термодинамика. Изд. 3-е переработанное и дополненное// М.Х. Каркапетьянц,- М.: «Химия», 1975- 584 с.
3. Ожегов С.И. Словарь русского языка. Издание 17-е, стереотипное // С.И. Ожегов.- М.: «Русский язык», 1985 — 797 с.
4. Планк М. Принцип сохранения энергии // М. Планк.- М. — Л.: ГОНТИ, 1938.
Планк М. Принцип сохранения энергии // М. Планк.- М. — Л.: ГОНТИ, 1938.
5. Смородинский Я.А. Температура. Библиотека квант // Я.А. Смородинский. -М.: «Наука», 1981 -160 с.
6. Физический энциклопедический словарь. Главный редактор А.М. Прохоров, М.:, «Советская энциклопедия» 1984.
7. Фундаментальные проблемы естествознания. Международный научный конгресс. 22-27 июня 1998г., Санкт-Петербург, Россия.
8. Эллиот Л. Физика. Перевод с английского под редакцией проф.
А.И.Китайгородского // Л. Эллиот, У. Уилкокс.- Издание третье. М.: «Наука», 1975736 с.
9. Энгельс Ф. Диалектика природы М., «Политиздат» 1965.
References
1. Aleksandrov B.L. Rol’ fotonov v fizicheskih i himicheskih javlenijah// B.L. Aleksandrov, M.B. Rodchenko, A.B. Aleksandrov. — Krasnodar, GUP «Pechatnyj dvor Kubani», 2002- 543 s.
2. Karkapet’janc M.H. Himicheskaja termodinamika. Izd. 3-e pererabotannoe i dopolnennoe// M.H. Karkapet’janc,- M.: «Himija», 1975- 584 s.
3. Ozhegov S.I. Slovar’ russkogo jazyka. Izdanie 17-e, stereotipnoe // S.I. Ozhegov.-M.: «Russkij jazyk», 1985 — 797 s.
4. Plank M. Princip sohranenija jenergii // M. Plank.- M. — L.: GONTI, 1938.
5. Smorodinskij Ja.A. Temperatura. Biblioteka kvant // Ja.A. Smorodinskij. — M.: «Nauka», 1981 -160 s.
6. Fizicheskij jenciklopedicheskij slovar’. Glavnyj redaktor A. M. Prohorov, M.:, «Sovetskaj a j enciklopedij a» 1984.
M. Prohorov, M.:, «Sovetskaj a j enciklopedij a» 1984.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
Научный журнал КубГАУ, №111(07), 2015 года
15
7. Fundamental’nye problemy estestvoznanija. Mezhdunarodnyj nauchnyj kongress. 2227 ijunja 1998g., Sankt-Peterburg, Rossija.
8. Jelliot L. Fizika. Perevod s anglijskogo pod redakciej prof. A.I.Kitajgorodskogo // L. Jelliot, U. Uilkoks.- Izdanie tret’e. M.: «Nauka», 1975-736 s.
9. Jengel’s F. Dialektika prirody M., «Politizdat» 1965.
http://ej.kubagro.ru/2015/07/pdf/38.pdf
100 ballov.kz образовательный портал для подготовки к ЕНТ и КТА
В 2021 году казахстанские школьники будут сдавать по-новому Единое национальное тестирование. Помимо того, что главный школьный экзамен будет проходить электронно, выпускникам предоставят возможность испытать свою удачу дважды. Корреспондент zakon.kz побеседовал с вице-министром образования и науки Мирасом Дауленовым и узнал, к чему готовиться будущим абитуриентам.
— О переводе ЕНТ на электронный формат говорилось не раз. И вот, с 2021 года тестирование начнут проводить по-новому. Мирас Мухтарович, расскажите, как это будет?
— По содержанию все остается по-прежнему, но меняется формат. Если раньше школьник садился за парту и ему выдавали бумажный вариант книжки и лист ответа, то теперь тест будут сдавать за компьютером в электронном формате. У каждого выпускника будет свое место, огороженное оргстеклом.
Зарегистрироваться можно будет электронно на сайте Национального центра тестирования. Но, удобство в том, что школьник сам сможет выбрать дату, время и место сдачи тестирования.
Кроме того, в этом году ЕНТ для претендующих на грант будет длиться три месяца, и в течение 100 дней сдать его можно будет два раза.
— Расскажите поподробнее?
— В марте пройдет тестирование для желающих поступить на платной основе, а для претендующих на грант мы ввели новые правила. Школьник, чтобы поступить на грант, по желанию может сдать ЕНТ два раза в апреле, мае или в июне, а наилучший результат отправить на конкурс. Но есть ограничение — два раза в один день сдавать тест нельзя. К примеру, если ты сдал ЕНТ в апреле, то потом повторно можно пересдать его через несколько дней или в мае, июне. Мы рекомендуем все-таки брать небольшой перерыв, чтобы еще лучше подготовиться. Но в любом случае это выбор школьника.
— Система оценивания останется прежней?
— Количество предметов остается прежним — три обязательных предмета и два на выбор. Если в бумажном формате закрашенный вариант ответа уже нельзя было исправить, то в электронном формате школьник сможет вернуться к вопросу и поменять ответ, но до того, как завершил тест.
Самое главное — результаты теста можно будет получить сразу же после нажатия кнопки «завершить тестирование». Раньше уходило очень много времени на проверку ответов, дети и родители переживали, ждали вечера, чтобы узнать результат. Сейчас мы все автоматизировали и набранное количество баллов будет выведено на экран сразу же после завершения тестирования.
Максимальное количество баллов остается прежним — 140.
— А апелляция?
— Если сдающий не будет согласен с какими-то вопросами, посчитает их некорректными, то он сразу же на месте сможет подать заявку на апелляцию. Не нужно будет ждать следующего дня, идти в центр тестирования, вуз или школу, все это будет электронно.
— С учетом того, что школьникам не придется вручную закрашивать листы ответов, будет ли изменено время сдачи тестирования?
— Мы решили оставить прежнее время — 240 минут. Но теперь, как вы отметили, школьникам не нужно будет тратить час на то, чтобы правильно закрасить лист ответов, они спокойно смогут использовать это время на решение задач.
— Не секрет, что в некоторых селах и отдаленных населенных пунктах не хватает компьютеров. Как сельские школьники будут сдавать ЕНТ по новому формату?
— Задача в том, чтобы правильно выбрать время и дату тестирования. Центры тестирования есть во всех регионах, в Нур-Султане, Алматы и Шымкенте их несколько. Школьники, проживающие в отдаленных населенных пунктах, как и раньше смогут приехать в город, где есть эти центры, и сдать тестирование.
— На сколько процентов будет обновлена база вопросов?
— База вопросов ежегодно обновляется как минимум на 30%. В этом году мы добавили контекстные задания, то что школьники всегда просили. Мы уделили большое внимание истории Казахстана и всемирной истории — исключили практически все даты. Для нас главное не зазубривание дат, а понимание значения исторических событий. Но по каждому предмету будут контекстные вопросы.
— По вашему мнению система справится с возможными хакерскими атаками, взломами?
— Информационная безопасность — это первостепенный и приоритетный вопрос. Центральный аппарат всей системы находится в Нур-Султане. Связь с региональными центрами сдачи ЕНТ проводится по закрытому VPN-каналу. Коды правильных ответов только в Национальном центре тестирования.
Кроме того, дополнительно через ГТС КНБ (Государственная техническая служба) все тесты проходят проверку на предмет возможного вмешательства. Здесь все не просто, это специальные защищенные каналы связи.
— А что с санитарными требованиями? Нужно ли будет школьникам сдавать ПЦР-тест перед ЕНТ?
— ПЦР-тест сдавать не нужно будет. Требование по маскам будет. При необходимости Центр национального тестирования будет выдавать маски школьникам во время сдачи ЕНТ. И, конечно же, будем измерять температуру. Социальная дистанция будет соблюдаться в каждой аудитории.
— Сколько человек будет сидеть в одной аудитории?
— Участники ЕНТ не за семь дней будут сдавать тестирование, как это было раньше, а в течение трех месяцев. Поэтому по заполняемости аудитории вопросов не будет.
— Будут ли ужесточены требования по дисциплине, запрещенным предметам?
— Мы уделяем большое внимание академической честности. На входе в центры тестирования, как и в предыдущие годы, будут стоять металлоискатели. Перечень запрещенных предметов остается прежним — телефоны, шпаргалки и прочее. Но, помимо фронтальной камеры, которая будет транслировать происходящее в аудитории, над каждым столом будет установлена еще одна камера. Она же будет использоваться в качестве идентификации школьника — как Face ID. Сел, зарегистрировался и приступил к заданиям. Мы применеям систему прокторинга.
Понятно, что каждое движение абитуриента нам будет видно. Если во время сдачи ЕНТ обнаружим, что сдающий использовал телефон или шпаргалку, то тестирование автоматически будет прекращено, система отключится.
— А наблюдатели будут присутствовать во время сдачи тестирования?
— Когда в бумажном формате проводили ЕНТ, мы привлекали очень много дежурных. В одной аудитории было по 3-4 человека. При электронной сдаче такого не будет, максимум один наблюдатель, потому что все будет видно по камерам.
— По вашим наблюдениям школьники стали меньше использовать запрещенные предметы, к примеру, пользоваться телефонами?
— Практика показывает, что школьники стали ответственнее относиться к ЕНТ. Если в 2019 году на 120 тыс. школьников мы изъяли 120 тыс. запрещенных предметов, по сути у каждого сдающего был телефон. То в прошлом году мы на 120 тыс. школьников обнаружили всего 2,5 тыс. телефонов, и у всех были аннулированы результаты.
Напомню, что в 2020 году мы также начали использовать систему искусственного интеллекта. Это анализ видеозаписей, который проводится после тестирования. Так, в прошлом году 100 абитуриентов лишились грантов за то, что во время сдачи ЕНТ использовали запрещенные предметы.
— Сколько средств выделено на проведение ЕНТ в этом году?
Если раньше на ЕНТ требовалось 1,5 млрд тенге из-за распечатки книжек и листов ответов, то сейчас расходы значительно сокращены за счет перехода на электронный формат. Они будут, но несущественные.
— Все-таки почему именно в 2021 году было принято решение проводить ЕНТ в электронном формате. Это как-то связано с пандемией?
— Это не связано с пандемией. Просто нужно переходить на качественно новый уровень. Мы апробировали данный формат на педагогах школ, вы знаете, что они сдают квалификационный тест, на магистрантах, так почему бы не использовать этот же формат при сдаче ЕНТ. Тем более, что это удобно, и для школьников теперь будет много плюсов.
Контрольная работа №1 «Внутренняя энергия»
Контрольная работа №1 «Тепловые явления»
Вариант 1
Часть 1
1. Внутренняя энергия тела зависит…
А) От скорости движения тела.
Б) От энергии движения частиц, из которых состоит тело.
В) От энергии взаимодействия частиц, из которых состоит тело.
Г) От энергии движения частиц и от энергии их взаимодействия.
2. Первый стакан с водой охладили, получив от него 1 Дж количества теплоты, а второй стакан подняли вверх, совершив работу в 1 Дж. Изменилась ли внутренняя энергия воды в первом и втором стаканах?
А) Ни в одном стакане не изменилась.
Б) В 1 — уменьшилась, во 2 — не изменилась.
В) В 1 — не изменилась, во 2 — увеличилась.
Г) В обоих стаканах уменьшилась.
Д) В 1 — уменьшилась, во 2 — увеличилась.
3. После того как распилили бревно, пила нагрелась. Каким способом изменили внутреннюю энергию пилы?
А) При совершении работы.
Б) При теплопередаче.
4. Чтобы увеличить внутреннюю энергию автомобильной шины, нужно…
А) Выпустить из шины воздух.
Б) Накачать в шину воздух.
5. Два одинаковых пакета с молоком вынули из холодильника. Один пакет оставили на столе, а второй перелили в кастрюлю и вскипятили. В каком случае внутренняя энергия молока изменилась меньше?
А) В обоих случаях не изменилась.
Б) В обоих случаях изменилась одинаково.
В) В первом случае.
Г) Во втором случае.
6. В каких единицах измеряют удельную теплоемкость?
А) Дж. Г) Дж/ С.
Б) Вт Д) Дж/ кгС.
В) Дж/кг.
7. Какое количество теплоты потребуется для нагревания 10 г меди на 15 °С?
А) 600 Дж. Г) 266,7 Дж.
Б) 3,75 Дж. Д) 60 000 Дж.
В) 60 Дж.
8. При охлаждении медного прута на 25 °С выделилось 200 Дж энергии. Какова масса медного прута?
А) 50 кг. Г) 0,5 кг.
Б) 0,02 кг. Д) 2 000 000 кг.
В) 2 кг.
9. Конвекцией называют вид теплопередачи, при котором энергия…
А) Передается от нагретого тела с помощью лучей.
Б) От нагретого конца тела передается к холодному, но само вещество при этом не перемещается.
В) Переносится самими частицами вещества.
10. Каков способ теплопередачи от костра?
А) Излучение.
Б) Теплопроводность.
В) Конвекция.
Часть 2
Для нагревания кирпича массой 4 кг от 15 оС до 30 оС израсходовано 48 кДж теплоты. Найти удельную теплоемкость кирпича.
Какое количество теплоты потребуется для нагревания 2 кг воды в алюминиевой кастрюле массой 800г от 20 оС до кипения?
Контрольная работа №1 «Тепловые явления»
Вариант 2
Часть 1
1. Каким способом можно изменить внутреннюю энергию тела?
А) Только совершением работы.
Б) Совершением работы и теплопередачей.
В) Только теплопередачей.
Г) Внутреннюю энергию тела изменить нельзя.
2. Первая пластина перемещалась по горизонтальной поверхности и в результате действия силы трения нагрелась, а вторая пластина была поднята вверх над горизонтальной поверхностью. В обоих случаях была совершена одинаковая работа. Изменилась ли внутренняя энергия пластин?
А) У первой пластины не изменилась, у второй увеличилась.
Б) У обеих пластин увеличилась.
В) У первой пластины увеличилась, а у второй не изменилась.
Г) Не изменилась ни у первой, ни у второй пластин.
3. Сок поставили в холодильник и охладили. Каким способом изменили внутреннюю энергию сока?
А) При совершении работы.
Б) При теплопередаче.
4. Резиновую нить слегка растянули. Чтобы внутренняя энергия нити увеличилась ее надо…
А) Растянуть сильнее.
Б) Отпустить.
5. Два алюминиевых бруска массами 100 и 300 г, взятых при комнатной температуре, нагрели до одинаковой температуры. У какого бруска внутренняя энергия изменилась больше?
А) У обоих не изменилась.
Б) У обоих одинаково.
В) У первого бруска.
Г) У второго бруска.
6. В каких единицах измеряют внутреннюю энергию?
А) Дж/ С. Г) Вт.
Б) Дж Д) Дж/кг.
В) Дж/ кгС.
7. Какое количество теплоты выделится при охлаждении 20 г спирта на 6 °С?
А) 300 Дж. Г) 300 000 Дж.
Б) 8 333,3 Дж. Д) 750 Дж.
В) 0,048 Дж.
8. При нагревании 4 г спирта передано 200 Дж количества теплоты. На сколько градусов изменилась температура спирта?
А) 2 000 000 °С. Г) 0,05 °С.
Б) 50 °С. Д) 20 °С.
В) 2000 °С.
9. Вид теплопередачи, при котором энергия от нагретого тела передается холодному с помощью лучей, называется…
А) Излучением.
Б) Конвекцией.
В) Теплопроводностью.
10. Каков способ теплопередачи водяного отопления?
А) Излучение.
Б) Теплопроводность.
В) Конвекция.
Часть 2
Какое количество воды можно нагреть от 15 оС до кипения, затратив 714 кДж теплоты?
Какое количество теплоты потребуется для нагревания 200 г спирта от 18 оС до 48 оС в стеклянной колбе массой 50 г?
Контрольная работа №1 «Тепловые явления»
Вариант 3
Часть 1
1. Внутренней энергией тела называют…
А) Энергию движения и взаимодействия частиц, из которых состоит тело.
Б) Энергию движущегося тела.
В) Энергию взаимодействия молекул.
Г) Энергию тела, поднятого над Землей.
Д) Энергию движения молекул.
2. Два одинаковых камня лежали на земле. Первый камень подняли и положили на стол, а второй подбросили вверх. Изменилась ли внутренняя энергия камней?
А) У первого камня не изменилась, у второго — увеличилась.
Б) У обоих камней увеличилась.
В) У первого камня увеличилась, а у второго не изменилась.
Г) У обоих камней не изменилась.
3. Чайник с водой поставили на огонь и вскипятили воду. Каким способом изменилась внутренняя энергия воды?
А) При теплопередаче.
Б) При совершении работы.
4. В сосуде находится газ. Чтобы внутренняя энергия газа уменьшилась, нужно…
А) Сжать газ.
Б) Увеличить объем газа.
5. В две одинаковые кастрюли налили одинаковое количество воды. В первой кастрюле воду довели до кипения, а во второй слегка подогрели. В каком случае внутренняя энергия воды изменилась меньше?
А) В обоих случаях не изменилась.
Б) В первой кастрюле.
В) Во второй кастрюле.
Г) В обоих случаях одинаково.
6. В каких единицах измеряют количество теплоты?
А) Дж/ кгС. Г) Дж.
Б) Дж/кг. Д) Вт.
В) Дж/ С.
7. Какое количество теплоты потребуется для нагревания цинка массой 50 г на 25 °С?
А) 200 Дж. Г) 3,125 Дж.
Б) 500 Дж. Д) 500 000 Дж.
В) 800 Дж.
8. На сколько градусов изменилась температура цинка массой 20 г, если при его охлаждении выделилось 200 Дж энергии?
А) 16 000 °С. Г) 1 600 000 °С.
Б) 0,04 °С. Д) 40 °С.
В) 25 °С.
9. Теплопроводностью называют вид теплопередачи, при котором энергия…
А) Переносится самими частицами вещества.
Б) Передается от нагретого конца тела холодному, но само вещество при этом не перемещается.
В) Передается с помощью лучей.
10. На чем основано ощущение тепла, если рука находится над горячей плитой?
А) Конвекции.
Б) Излучении.
В) Теплопроводности.
Часть 2
Какое количество теплоты потребуется для нагревания смеси, состоящей из 500г воды и 100г спирта от 20 оС до 60 оС?
Сколько потребуется спирта, чтобы довести до кипения 200 г воды, взятой при температуре 25 оС, считая, что вся теплота, полученная при сгорании спирта, пойдет на нагрев воды.
Контрольная работа №1 «Тепловые явления»
Вариант 4
Часть 1
1. От чего зависит внутренняя энергия тела?
А) От энергии взаимодействия частиц, из которых состоит тело.
Б) От энергии движения этих частиц.
В) От энергии движения частиц и от энергии их взаимодействия. Г) От скорости движения тела.
2. Один стакан с водой подняли вверх, совершив работу 1 Дж, а второй нагрели, передав ему 1 Дж количества теплоты. Изменилась ли внутренняя энергия воды в каждом стакане?
А) В обоих стаканах увеличилась.
Б) В первом стакане уменьшилась, во втором увеличилась.
В) Нигде не изменилась.
Г) В первом увеличилась, во втором не изменилась.
Д) В первом не изменилась, во втором увеличилась
3. При затачивании топор нагревается. Каков способ изменения внутренней энергии топора?
А) При теплопередаче.
Б) При совершении работы.
4. В каком из перечисленных случаев внутренняя энергия воды не меняется: 1) воду несут в ведре; 2) воду переливают из ведра в чайник; 3) воду нагревают до кипения.
А) 1. Д) 1 и 3.
Б) 2. Е) 2иЗ.
В) 3. Ж) 1, 2, 3.
Г) 1и2.
5. Два медных бруска массами 400 и 200 г, взятых при комнатной температуре, охладили до одной и той же температуры. У какого бруска внутренняя энергия изменилась больше?
А) У первого бруска.
Б) У второго бруска.
В) У обоих одинаково.
Г) У обоих не изменилась.
6. В каких единицах измеряют удельную теплоемкость?
А) Дж/ С. Г) Вт.
Б) Дж. Д) Дж/кг.
В) Дж/ кгС.
7. Какое количество теплоты выделится при охлаждении 10 г стали на 8°С?
А) 40 000 Дж. Г) 40 Дж.
Б) 0,16 Дж. Д) 400 Дж.
В) 625 Дж.
8. Какую массу стали нагрели до температуры 20 °С, если ей сообщили 200 Дж количества теплоты?
А) 0,02 кг. Г) 0,5 кг.
Б) 50 кг. Д) 2 000 000 кг.
В) 2 кг.
9. Вид теплопередачи, при котором энергия переносится самими частицами вещества, называется…
А) Конвекцией.
Б) Излучением.
В) Теплопроводностью.
10. Какой способ теплопередачи используется при поджаривании яичницы?
А) Излучение.
Б) Теплопроводность.
В) Конвекция.
Часть 2
На сколько градусов охладится 40 кг льда, если отнять от него 400 кДж теплоты?
В медной кастрюле массой 1,6 кг находится 2,3 кг воды. Сколько теплоты потребуется для нагревания от 10 оС до 100 оС кастрюли с водой?
Контрольная работа №1 «Тепловые явления»
Вариант 5
Часть 1
1. Каким способом можно изменить внутреннюю энергию тела?
А) Совершением работы и теплопередачей.
Б) Внутреннюю энергию тела изменить нельзя.
В) Только совершением работы.
Г) Только теплопередачей.
2. Первую пластину подняли вверх над горизонтальной поверхностью, а вторую несколько раз изогнули, в результате чего она нагрелась. Работа в обоих случаях была совершена одинаковая. Изменилась ли внутренняя энергия пластин?
А) У первой пластины увеличилась, а у второй не изменилась. Б) Нигде не изменилась.
В) У первой не изменилась, а у второй увеличилась.
Г) У обеих пластин увеличилась.
3. Кувшин с молоком отнесли в погреб, где оно охладилось. Каким способом изменилась внутренняя энергия молока?
А) При совершении работы.
Б) При теплопередаче.
4. Пружину слегка сжали. Что нужно сделать, чтобы увеличить внутреннюю энергию пружины?
А) Сжать пружину сильнее.
Б) Отпустить пружину.
5. Одну из двух одинаковых серебряных ложек опустили в стакан с кипятком, а другую в стакан с теплой водой. В каком случае внутренняя энергия ложки изменится меньше?
А) В обоих случаях не изменится.
Б) В обоих случаях одинаково.
В) В первом случае.
Г) Во втором случае.
6. В каких единицах измеряют внутреннюю энергию?
А) Дж. Г) Дж/ кгС.
Б) Дж/кг. Д) Вт.
В) Дж/ С.
7. Какое количество теплоты потребуется для нагревания 20 г латуни на 5 °С?
А) 100 Дж. Г) 1600 Дж.
Б) 40 Дж. Д) 0,25 Дж.
В) 40 000 Дж.
8. При охлаждении латуни на 50 °С выделилось 200 Дж энергии. Какова масса латуни?
А) 4000 кг. Г) 0,01 кг.
Б) 1 кг. Д) 100 кг.
В) 4 000 000 кг.
9. Как осуществляется передача энергии глиняной посуде, находящейся в печи?
А) Излучением.
Б) Конвекцией.
В) Работой.
Г) Теплопроводностью.
10. Какой способ теплопередачи осуществляется при хранении продуктов в погребе?
А) Конвекция.
Б) Излучение.
В) Теплопроводность.
Часть 2
Для нагревания кирпича массой 4 кг от 15 оС до 30 оС израсходовано 48 кДж теплоты. Найти удельную теплоемкость кирпича.
Какое количество теплоты потребуется для нагревания 2 кг воды в алюминиевой кастрюле массой 800г от 20 оС до кипения?
Контрольная работа №1 «Тепловые явления»
Вариант 6
Часть 1
1. Энергию движения и взаимодействия частиц, из которых состоит тело, называют…
А) Механической энергией.
Б) Кинетической энергией.
В) Потенциальной энергией.
Г) Внутренней энергией.
2. Два камня лежали на столе. Первый камень начал падать со стола, а второй взяли и положили на землю. Изменилась ли внутренняя энергия камней?
А) У первого увеличилась, а у второго не изменилась.
Б) У обоих камней уменьшилась.
В) У первого не изменилась, а у второго уменьшилась.
Г) Ни у одного камня не изменилась.
3. После того как деталь обработали напильником, деталь нагрелась. Каким способом изменили внутреннюю энергию детали?
А) При совершении работы.
Б) При теплопередаче.
4. В каком из перечисленных случаев внутренняя энергия чашки не изменилась: 1) чашку переставили из шкафа на стол; 2) чашку передвинули по столу; 3) в чашку налили горячий чай.
А) 1,2, 3. Г) 3. Ж) 2 и 3.
Б) 1. Д) 1 и 2.
В) 2. Е) 1 и 3.
5. Два железных бруска массами 200 и 300 г, взятых при комнатной температуре, охладили до одинаковой температуры. У какого бруска внутренняя энергия изменилась больше?
А) У первого бруска.
Б) У второго бруска.
В) У обоих не изменилась.
Г) У обоих одинаково.
6. В каких единицах измеряют количество теплоты?
А) Вт. Г) Дж/кг.
Б) Дж. Д) Дж/ С.
В) Дж/ кгС.
7. Какое количество теплоты выделится при охлаждении 50 г серебра на 4 °С?
А) 3 125 Дж. Г) 0,8 Дж.
Б) 20 Дж. Д) 50 Дж.
В) 50 000 Дж.
8. На сколько градусов нагрелось серебро массой 20 г, если ему сообщили 200 Дж количества теплоты?
А) 1 000 000 °С. Г) 1000 °С.
Б) 0,025 °С. Д) 25 °С.
В) 40 °С.
9. Вид теплопередачи, при котором энергия передается от нагретого конца тела холодному, но само вещество при этом не перемещается, называют…
А) Излучением.
Б) Теплопроводностью.
В) Конвекцией.
10. Благодаря какому способу теплопередачи нагревается термометр, вывешенный за окно?
А) Теплопроводность.
Б) Конвекция.
В) Излучение.
Часть 2
Какое количество воды можно нагреть от 15 оС до кипения, затратив 714 кДж теплоты?
Какое количество теплоты потребуется для нагревания 200 г спирта от 18 оС до 48 оС в стеклянной колбе массой 50 г?
8 класс
Контрольная работа
«Тепловые явления»
(6 вариантов тест + задачи)
Ответы
Вариант 1
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
Вариант 2
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
Вариант 3
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
Вариант 4
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
Вариант 5
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
Вариант 6
Часть 1
1
2
3
4
5
6
7
8
9
10
Ответ
Часть 2
1.
2.
термодинамика — Как работа над телом учитывает увеличение внутренней энергии?
Для идеального газа нет взаимодействия между молекулами, поэтому внутренняя энергия — это полная кинетическая энергия всех его молекул. Сжатие газа увеличивает кинетическую энергию (и, следовательно, внутреннюю энергию и температуру) газа, тогда как разрешение газу расширяться снижает кинетическую энергию.
Когда стенки контейнера зафиксированы, молекулы, которые отскакивают от стенок, после отскока имеют тот же KE, что и раньше.Скорость меняется на противоположную, но кинетическая энергия остается неизменной. Температура газа не повышается и не понижается.
Когда вы нажимаете на поршень, чтобы сжать газ, молекулы отскакивают от поршня с большей скоростью, чем когда они приближаются к нему. Столкновения с поршнем, движущимся навстречу молекулам газа, увеличивают среднюю скорость молекул и, следовательно, температуру. Когда поршень удаляется от молекул, это снижает температуру газа.
Тот факт, что поршень обычно движется очень медленно (например, 1 мм / с) по сравнению со скоростью молекул газа (около 400 м / с), может указывать на то, что движение поршня может иметь лишь незначительное влияние на скорость молекул. . Однако высокая скорость молекул означает, что происходит большое количество столкновений, каждое из которых увеличивает скорость молекулы на крошечную величину, поэтому общий эффект может быть значительным.
Например, в контейнере высотой 25 см каждая молекула будет сталкиваться с поршнем примерно 800 раз в секунду.2 $, что увеличивается в 1%. Температура увеличивается с 300 К примерно на 3 К.
Работа поршня над газом — это работа над его молекулами. Это равносильно увеличению KE молекул, то есть увеличению внутренней энергии.
В свободном расширении объем газа увеличивается внезапно, при этом молекулы не успевают столкнуться с поршнем. Это не приводит к снижению температуры. Это показывает, что не изменение объема изменяет температуру газа, а работу, совершаемую поршнем, которая либо передает кинетическую энергию его молекулам, либо забирает у них кинетическую энергию.
Учебное пособие по физике
Урок 1 этой главы был посвящен значению температуры и тепла. Особое внимание было уделено развитию модели частиц материи, способной объяснить макроскопические наблюдения. Были предприняты попытки развить твердое концептуальное понимание темы в отсутствие математических формул. Мы узнали, что тепло передается от одного объекта к другому (между системой и окружающей средой), когда существует разница температур между системой и окружающей средой.Теперь в этом модуле мы исследуем тему измерения количества тепла, которое передается между системой и окружающей средой. Этот урок посвящен калориметрии — науке, связанной с определением изменений энергии системы путем измерения теплообмена с окружающей средой. Прежде чем мы сможем понять математику калориметрии, мы должны ответить на важный вопрос, который хотя бы частично рассматривался в Уроке 1. Вопрос: что делает тепло? Что он делает, когда объект теряет или получает тепло?
Для некоторых студентов вопрос , что делает тепло? сбивает с толку.Подумайте немного над вопросом. Вас смущает вопрос (а не только ответ)? Путаница в вопросе иногда вызывается неправильными представлениями о том, что такое heat . Причина длительных обсуждений в Уроке 1 заключалась в том, чтобы обеспечить прочную концептуальную основу для понимания математики Урока 2. Если вопрос сбивает с толку, вы можете пересмотреть Урок 1 или, по крайней мере, пересмотреть обсуждение, относящееся к теме «Что такое тепло?». В Уроке 1 подчеркивалось, что тепло — это не то, что содержится в объекте.Объекты не содержат тепла . Объекты, состоящие из атомов, молекул и ионов, содержат энергию. Тепло — это передача энергии от объекта к его окружению или к объекту из его окружения. На этой странице задается вопрос: что делает это тепло с объектом и с окружающей средой, когда оно передается? Как и многие другие вопросы физики, это простой ответ с глубоким смыслом. Простые ответы с глубоким смыслом всегда тренируют мозг. Так что надевайте шапку на размышления и давайте перейдем к ответу.
Тепло изменяет температуру объектовЧто делает тепло? Во-первых, он изменяет температуру объекта. Если тепло передается от объекта к окружающему, то объект может остыть, а окружающее — нагреться. Когда тепло передается объекту из-за его окружения, он может нагреваться, а окружение — охлаждаться. Тепло, когда-то поглощенное в виде энергии, вносит вклад в общую внутреннюю энергию объекта.Одна из форм этой внутренней энергии — кинетическая энергия; частицы начинают двигаться быстрее, что приводит к большей кинетической энергии. Это более энергичное движение частиц отражается повышением температуры. Также применима обратная логика. Энергия, когда-то выделяемая в виде тепла, приводит к уменьшению общей внутренней энергии объекта. Поскольку кинетическая энергия является одной из форм внутренней энергии, выделение тепла от объекта вызывает уменьшение средней кинетической энергии его частиц.Это означает, что частицы движутся медленнее и температура объекта снижается. Высвобождение или поглощение энергии в форме тепла объектом часто связано с изменением температуры этого объекта. Это было целью термометров как спидометров в Уроке 1. Что можно сказать об объекте, можно сказать и об окружающей среде. Высвобождение или поглощение энергии в форме тепла окружающей средой часто связано с изменением температуры окружающей среды.Мы часто обнаруживаем, что передача тепла вызывает изменение температуры как в системе, так и в окружающей среде. Один нагревается, а другой остывает.
Тепло изменяет состояние веществаНо всегда ли поглощение или выделение энергии в виде тепла вызывает изменение температуры? Удивительно, но ответ отрицательный. Чтобы проиллюстрировать, почему, рассмотрим следующую ситуацию, которую часто демонстрируют или даже экспериментируют в школе по теплофизике.Пара-дихлорбензол, основной ингредиент многих форм нафталина, имеет температуру плавления около 54 ° C. Предположим, что образец химического вещества собирают в пробирку и нагревают примерно до 80 ° C. Пара-дихлорбензол будет в жидком состоянии (хотя большая его часть сублимирована и наполняет комнату наиболее заметным ароматом). Теперь предположим, что в пробирку вставлен термометр, а пробирка помещена в стакан с водой комнатной температуры. Данные температуры и времени можно собирать каждые 10 секунд.Совершенно неожиданно можно заметить, что температура пара-дихлорбензола постепенно понижается. По мере передачи тепла от высокотемпературной пробирки к воде с низкой температурой температура жидкого пара-дихлорбензола снижается. Но затем совершенно неожиданно можно было заметить, что это устойчивое снижение температуры прекращается примерно при 54 ° C. Как только температура жидкого пара-дихлорбензола снижается до 54 ° C, уровень термометра внезапно останавливается на отметке . Судя по показаниям термометра, можно подумать, что тепло не передается.Но взгляд в пробирку показывает, что происходят драматические изменения. Жидкий пара-дихлорбензол кристаллизуется с образованием твердого пара-дихлорбензола. Как только последний след жидкого пара-дихлорбензола исчезает (и он находится в твердой форме), температура снова начинает снижаться с 54 ° C до температуры воды. Как эти наблюдения могут помочь нам понять вопрос о том, что делает тепло?
Во-первых, снижение температуры с 80 ° C до 54 ° C легко объяснить.В Уроке 1 мы узнали, что тепло передается между двумя соседними объектами, имеющими разную температуру. Пробирка и пара-дихлорбензол имеют более высокую температуру, чем вода, окружающая химический стакан. Тепло будет течь из пробирки с пара-дихлорбензолом в воду, вызывая охлаждение пара-дихлорбензола и нагревание воды. Понижение температуры с 54 ° C до температуры воды в стакане тоже легко объяснимо. Два соседних объекта с разной температурой будут передавать тепло между собой, пока не будет достигнуто тепловое равновесие.Сложное объяснение включает объяснение того, что происходит при 54 ° C. Почему температура больше не снижается, когда жидкий пара-дихлорбензол начинает кристаллизоваться? Есть ли по-прежнему передача тепла между пробиркой с пара-дихлорбензолом и стаканом с водой, даже если температура не меняется?
Ответ на вопрос Передается ли тепло? — это громкое да! В конце концов, принцип состоит в том, что тепло всегда передается между двумя соседними объектами, имеющими разную температуру.Термометр, помещенный в воду, показывает, что вода все еще нагревается, даже несмотря на то, что в пара-дихлорбензоле нет изменений температуры. Итак, тепло однозначно передается от пара-дихлорбензола к воде. Но почему температура пара-дихлорбензола остается постоянной в течение этого периода кристаллизации? Прежде чем пара-дихлорбензол сможет продолжать понижать свою температуру, он должен сначала перейти из жидкого состояния в твердое состояние. Кристаллизация пара-дихлорбензола происходит при 54 ° C — температуре замерзания вещества.При этой температуре энергия, теряемая пара-дихлорбензолом, связана с изменением другой формы внутренней энергии — потенциальной энергии. Вещество не только обладает кинетической энергией из-за движения своих частиц, но также обладает потенциальной энергией из-за межмолекулярного притяжения между частицами. Поскольку пара-дихлорбензол кристаллизуется при 54 ° C, потеря энергии отражается уменьшением потенциальной энергии пара-дихлорбензола при изменении его состояния. Как только весь пара-дихлорбензол переходит в твердое состояние, потеря энергии снова отражается уменьшением кинетической энергии вещества; его температура снижается.
Итак, второй ответ на вопрос Что делает тепло? заключается в том, что он способствует изменению состояния вещества. Большинство студентов знакомы как минимум с тремя состояниями материи — твердым, жидким и газообразным. Добавление тепла к образцу вещества может привести к тому, что твердые вещества превратятся в жидкости, а жидкости — в газы. Точно так же отвод тепла от образца вещества может заставить газы превратиться в жидкости, а жидкости — в твердые тела.Каждый из этих переходов между состояниями происходит при определенных температурах, обычно называемых температурой точки плавления, температурой точки замерзания, температурой точки кипения и температурой точки конденсации.
Чтобы дополнительно проиллюстрировать эту взаимосвязь между теплопередачей, изменением температуры и изменением состояния, рассмотрим следующий мысленный эксперимент . Предположим, что образец воды помещен в чашку из пенополистирола с цифровым термометром. И предположим, что вода помещена в морозильную камеру (температура = -20 ° C) и заморожена.Предположим, что термометр можно подключить к компьютеру с программным обеспечением, способным собирать данные о температуре и времени. После того, как вода замерзла и оставалась в морозильной камере в течение нескольких часов, ее удаляли и помещали в химический стакан на нагревательную плиту . Плита включается, нагревается и начинает передавать энергию в виде тепла стакану и воде. Какие изменения будут наблюдаться в температуре и состоянии вещества воды с течением времени?
На приведенной ниже диаграмме изображена так называемая кривая нагрева воды.Кривая нагрева представляет изменения температуры во времени для образца вещества (например, воды), которому передается тепло.
Обратите внимание, что на графике температура-время есть три наклонных и два горизонтальных участка. Первый наклонный участок соответствует изменению температуры льда с -20 ° C до 0 ° C. Вода в твердом состоянии нагревается до точки плавления — температуры, при которой вода переходит из твердого состояния в жидкое.Тепло, передаваемое льду, вызывает изменение температуры. После достижения температуры перехода (точки плавления) 0 ° C тепло, добавляемое к воде, заставляет воду переходить из твердого состояния в жидкое. Это называется плавлением. Плавление происходит при постоянной температуре. На этом этапе эксперимента энергия, поглощаемая водой, используется для ослабления притяжения, удерживающего одну частицу льда на другой. Как только все эти притяжения будут ослаблены, лед полностью растает.Содержимое стакана из пенополистирола полностью жидкое. Следующий участок кривой нагрева представляет собой наклонный участок. Температура жидкой воды повышается с 0 ° C до 100 ° C. Температура кипения воды 100 ° C; это температура, при которой вода переходит из жидкого состояния в газообразное. Как только образец воды достигает этой температуры, происходит кипение. Можно было бы наблюдать образование больших пузырьков газа в объеме жидкости. Тепло, добавляемое к жидкости на этом этапе мысленного эксперимента, вызывает ослабление притяжения, удерживающего частицы воды в жидком состоянии.Температура остается постоянной, а состояние воды меняется. Как только вся вода переходит из жидкого в газообразное состояние, образец воды (теперь в газообразном состоянии) снова начинает повышать свою температуру.
Таким образом, три наклонных участка представляют тепло, вызывающее изменение температуры вещества, которое его поглощает. И два участка плато представляют тепло, вызывающее изменение состояния вещества, которое его поглощает. Любознательный студент может спросить: «Каково объяснение этих изменений на уровне частиц?» (Спасибо за вопрос.) Температурные изменения являются результатом дополнительной энергии, заставляющей частицы воды двигаться более энергично. Либо частицы твердого вещества более энергично колеблются вокруг своих фиксированных положений, либо частицы жидкости и газа перемещаются по своему контейнеру быстрее. В любом случае добавление тепла вызывает увеличение средней кинетической энергии частиц в пробе воды. Изменения состояния являются результатом добавленной энергии, вызывающей изменения силы притяжения между частицами.Преодолеваются притяжения, удерживающие воду в твердом или жидком состоянии. Энергия используется, чтобы ослабить это притяжение и перейти в состояние большей потенциальной энергии.
Flickr Physics Фото(а) Вода в колбе нагревается до температуры кипения. Выходящий из колбы газ охлаждается, проходя через медную трубку. Видны капли конденсированной воды, выходящие из конца медной трубки.
(b) Температура этой конденсированной воды намного меньше 100 ° C. Он недостаточно горячий, чтобы вызвать ожог.
(c) Пламя горелки Бунзена используется для нагрева змеевиков конденсатора медной трубки. Это поднимает температуру выходящей воды выше точки кипения. Это газообразная вода с температурой выше 100 ° C, которая выходит из медных трубок.
(d) Этот водяной пар настолько горячий, что мгновенно воспламеняет спичку, вставленную в его отверстие.
(e) По-прежнему нагреваясь пламенем горелки Бунзена, выходящий водяной пар достаточно горячий, чтобы обжечь лист бумаги…
(f) … и это заклинание phun для людей, которые проводят и смотрят демонстрацию! Тепло работает Работает
Итак, передача энергии в виде тепла связана с изменениями температуры или изменениями состояния образца вещества. Но это все? Может ли тепло на что-нибудь еще? И снова ответ — да! Передача энергии в виде тепла может привести к работе системы или окружающей среды.Устройства, которые используют тепло для работы, часто называют тепловыми двигателями. В общем, двигатель — это устройство, которое действительно работает. Тепловой двигатель — это устройство, использующее теплопередачу в качестве источника энергии для выполнения работы.
Двигатель внутреннего сгорания автомобиля является примером теплового двигателя. В большинстве двигателей внутреннего сгорания используется четырехтактный процесс, показанный на анимации справа. Когда топливо сгорает (реагирует с кислородом) в двигателе, энергия выделяется из системы химикатов.Происходит передача тепла от горячей системы к окружающему воздуху цилиндра. Эта передача тепла воздуху в цилиндре воздействует на поршень, толкая его вниз. Поршень соединен с коленчатым валом автомобиля. Возвратно-поступательное движение поршня внутри цилиндра приводит к вращению коленчатого вала и выработке энергии, необходимой для приведения автомобиля в движение. Двигатель внутреннего сгорания является примером теплового двигателя. В этом случае внутренняя энергия, запасенная в химическом веществе (бензине), преобразуется в тепловую энергию (поток тепла), что приводит к выполнению работы.Тепловые двигатели будут обсуждаться более подробно в главе «Термодинамика» учебного курса по физике. (Особая благодарность UtzOnBike и WikiMedia Commons за анимацию четырехтактного двигателя Отто, использованного выше.)
Тепло — это поток энергии из места с высокой температурой в место с низкой температурой. Этот поток энергии всегда связан с изменениями в системе и в окружающей среде. Могут быть изменения температуры, изменения состояния вещества и изменения, возникающие в результате выполнения работы.В следующем разделе мы рассмотрим калориметрию. Мы обнаружим, что с этими изменениями связан очень предсказуемый набор математических расчетов. Фактически, они настолько предсказуемы, что ученые могут использовать их для измерения количества потока энергии.
Работа, тепло и внутренняя энергия — Университетская физика, том 2
Цели обучения
К концу этого раздела вы сможете:
- Опишите работу, выполняемую системой, теплопередачу между объектами и изменение внутренней энергии системы
- Рассчитайте работу, теплопередачу и изменение внутренней энергии с помощью простого процесса
Мы обсуждали концепции работы и энергии ранее в механике.Примеры и связанные с ними вопросы теплопередачи между различными объектами также обсуждались в предыдущих главах. Здесь мы хотим расширить эти концепции до термодинамической системы и окружающей ее среды. В частности, мы подробно остановились на концепциях теплопередачи и теплопередачи в предыдущих двух главах. Здесь мы хотим понять, как работа выполняется термодинамической системой или с ней; как тепло передается между системой и окружающей средой; и как общая энергия системы изменяется под влиянием проделанной работы и теплопередачи.
Работа, выполняемая системой
Сила, созданная из любого источника, может выполнять работу, перемещая объект через смещение. Тогда как же работает термодинамическая система? (Рисунок) показывает газ, заключенный в цилиндр с подвижным поршнем на одном конце. Если газ расширяется относительно поршня, он передает силу на расстояние и действует на поршень. Если поршень сжимает газ при движении внутрь, работа также выполняется — в данном случае с газом. Работа, связанная с такими изменениями объема, может быть определена следующим образом: Пусть давление газа на торце поршня будет p .Тогда сила, действующая на поршень за счет газа, составляет пА, , где , А, — площадь торца. Когда поршень выталкивается наружу на бесконечно малое расстояние dx , величина работы, выполняемой газом, составляет
.Так как объем газа изменяется, это становится
.Для конечного изменения объема от мы можем проинтегрировать это уравнение от, чтобы найти чистую работу:
Работа, совершаемая ограниченным газом при перемещении поршня на расстояние dx , определяется выражениемЭтот интеграл имеет смысл только для квазистатического процесса, что означает процесс, который происходит бесконечно малыми шагами, поддерживая систему в тепловом равновесии.(Мы рассмотрим эту идею более подробно позже в этой главе.) Только тогда существует четко определенная математическая связь (уравнение состояния) между давлением и объемом. Эту зависимость можно изобразить на диаграмме зависимости давления от объема pV , где кривая представляет собой изменение состояния. Мы можем аппроксимировать такой процесс как процесс, который происходит медленно, через серию состояний равновесия. Интеграл интерпретируется графически как площадь под кривой pV (заштрихованная область на (Рисунок)).Работа, совершаемая газом, положительна для расширения и отрицательна для сжатия.
Когда газ расширяется медленно, работа, выполняемая системой, представлена заштрихованной областью под кривой pV .Рассмотрим два процесса с участием идеального газа, которые представлены путями AC и ABC на (рисунок). Первый процесс представляет собой изотермическое расширение, при котором объем газа изменяется от. Этот изотермический процесс представлен кривой между точками A и C .Газ поддерживается при постоянной температуре T , поддерживая его в тепловом равновесии с тепловым резервуаром при этой температуре. Из (Рисунок) и закона идеального газа,
Пути ABC , AC и ADC представляют три различных квазистатических перехода между состояниями равновесия A и C .
Расширение изотермическое, поэтому T остается постоянным на протяжении всего процесса. Поскольку n и R также постоянны, единственная переменная в подынтегральном выражении — В , поэтому работа, совершаемая идеальным газом в изотермическом процессе, составляет
.Обратите внимание, что if (расширение), W положительно, как и ожидалось.
Прямые линии от A до B и затем от B до C представляют собой другой процесс. Здесь газ под давлением сначала расширяется изобарно (постоянное давление) и квазистатически из, после чего он охлаждается квазистатически при постоянном объеме, пока его давление не упадет до. От A до B давление постоянно на уровне p , поэтому работа на этом участке пути составляет
.С B на C объем не изменился, и, следовательно, работы не производились.Тогда чистая работа по пути ABC равна
.Сравнение выражений для работы, совершаемой газом в двух процессах (рисунок), показывает, что они совершенно разные. Это иллюстрирует очень важное свойство термодинамической работы: путь зависимый . Мы не можем определить работу, совершаемую системой при переходе из одного состояния равновесия в другое, если не знаем ее термодинамический путь. Разные ценности работы связаны с разными путями.
Проверьте свое понимание Сколько работы совершает газ, как показано на (Рисунок), когда он квазистатически расширяется по пути ADC ?
Внутренняя энергия
Внутренняя энергия термодинамической системы — это, по определению, сумма механических энергий всех молекул или объектов в системе. Если кинетическая и потенциальная энергии молекулы и равны и соответственно, то внутренняя энергия системы является средним значением полной механической энергии всех сущностей:
, где суммирование ведется по всем молекулам системы, а полосы над K и U указывают средние значения.Кинетическая энергия отдельной молекулы включает вклады, обусловленные ее вращением и вибрацией, а также ее поступательную энергию, где скорость молекулы измеряется относительно центра масс системы. Потенциальная энергия связана только с взаимодействиями между молекулой и и другими молекулами системы. Фактически, ни расположение системы, ни ее движение не имеют никакого значения с точки зрения внутренней энергии. На внутреннюю энергию системы не влияет ее перемещение из подвала на крышу 100-этажного дома или установка на движущийся поезд.
В идеальном одноатомном газе каждая молекула представляет собой отдельный атом. Следовательно, нет вращательной или колебательной кинетической энергии и. Кроме того, нет межатомных взаимодействий (несмотря на столкновения), поэтому мы устанавливаем его равным нулю. Следовательно, внутренняя энергия обусловлена только поступательной кинетической энергией и
Из обсуждения в предыдущей главе мы знаем, что средняя кинетическая энергия молекулы в идеальном одноатомном газе равна
., где T — температура газа по Кельвину.Следовательно, средняя механическая энергия, приходящаяся на молекулу идеального одноатомного газа, также равна
.Внутренняя энергия — это просто количество молекул, умноженное на среднюю механическую энергию на молекулу. Таким образом, для n моль идеального одноатомного газа,
Обратите внимание, что внутренняя энергия данного количества идеального одноатомного газа зависит только от температуры и полностью не зависит от давления и объема газа. Для других систем внутреннюю энергию нельзя выразить так просто.Однако увеличение внутренней энергии часто может быть связано с повышением температуры.
Из нулевого закона термодинамики мы знаем, что, когда две системы находятся в тепловом контакте, они в конечном итоге достигают теплового равновесия, в этот момент они имеют одинаковую температуру. В качестве примера предположим, что мы смешиваем два одноатомных идеальных газа. Теперь энергия, приходящаяся на молекулу идеального одноатомного газа, пропорциональна его температуре. Таким образом, когда два газа смешиваются, молекулы более горячего газа должны терять энергию, а молекулы более холодного газа должны получать энергию.Это продолжается до тех пор, пока не будет достигнуто тепловое равновесие, после чего температура и, следовательно, средняя кинетическая энергия поступательного движения, приходящаяся на одну молекулу, одинаковы для обоих газов. Подход к равновесию для реальных систем несколько сложнее, чем для идеального одноатомного газа. Тем не менее, мы все же можем сказать, что между системами происходит обмен энергией до тех пор, пока их температуры не станут одинаковыми.
Сводка
- Положительная (отрицательная) работа выполняется термодинамической системой, когда она расширяется (сжимается) под внешним давлением.
- Тепло — это энергия, передаваемая между двумя объектами (или двумя частями системы) из-за разницы температур.
- Внутренняя энергия термодинамической системы — это ее полная механическая энергия.
Концептуальные вопросы
Можно ли определить, вызвано ли изменение внутренней энергии теплопередачей, выполненной работой или их комбинацией?
Когда жидкость испаряется, ее внутренняя энергия не равна добавленному теплу.Почему?
Часть энергии уходит на преобразование фазы жидкости в газ.
Почему при накачивании шины велосипедный насос нагревается?
Возможно ли, чтобы температура системы оставалась постоянной, когда тепло поступает в нее или из нее? Если да, приведите примеры.
Да, до тех пор, пока проделанная работа равна добавленному теплу, внутренняя энергия не изменится, а следовательно, и температура не изменится. Когда вода замерзает или когда лед тает при отводе или добавлении тепла, соответственно, температура остается постоянной.
Проблемы
Газ под давлением 2,00 атм подвергается квазистатическому изобарическому расширению с 3,00 до 5,00 л. Сколько работы совершает газ?
Для квазистатического сжатия 0,50 моль идеального газа до одной пятой его первоначального объема требуется 500 Дж работы. Рассчитайте температуру газа, предполагая, что она остается постоянной во время сжатия.
Установлено, что при квазистатическом расширении разреженного газа от 0,50 до 4,0 л он совершает 250 Дж работы.Если предположить, что температура газа остается постоянной на уровне 300 К, сколько молей газа присутствует?
При квазистатическом изобарическом расширении 500 Дж работы совершает газ. Если давление газа составляет 0,80 атм, каково частичное увеличение объема газа, если исходное значение составляло 20,0 л?
Когда газ претерпевает квазистатическое изобарическое изменение объема от 10,0 до 2,0 л, требуется 15 Дж работы от внешнего источника. Какое давление газа?
Идеальный газ квазистатически и изотермически расширяется из состояния с давлением p и объемом V в состояние с объемом 4V.Покажите, что работа, совершаемая газом при расширении, равна pV (ln 4).
Как показано ниже, рассчитайте работу, совершаемую газом в квазистатических процессах, представленных путями (a) AB; (б) АБР; (c) ACB; и (d) ADCB.
(a) Рассчитайте работу, совершаемую газом по замкнутому пути, показанному ниже. Изогнутая часть между R и S полукруглая. б) Если процесс осуществляется в обратном направлении, какую работу выполняет газ?
Идеальный газ квазистатически расширяется до трехкратного первоначального объема.Какой процесс требует большей работы от газа, изотермический или изобарический? Определите соотношение проделанной работы в этих процессах.
Разбавленный газ под давлением 2,0 атм и объемом 4,0 л проходит следующие квазистатические этапы: (а) изобарическое расширение до объема 10,0 л, (б) изохорическое изменение до давления 0,50 атм, (c) изобарическое сжатие до объема 4,0 л, и (d) изохорическое изменение до давления 2,0 атм. Покажите эти шаги на диаграмме pV и определите по вашему графику чистую работу, выполненную газом.
Какова средняя механическая энергия атомов идеального одноатомного газа при 300 К?
Какова внутренняя энергия 6,00 моль идеального одноатомного газа?
Рассчитайте внутреннюю энергию 15 мг гелия при температуре
Два одноатомных идеальных газа A и B имеют одинаковую температуру. Если 1,0 г газа A имеет ту же внутреннюю энергию, что и 0,10 г газа B, каково (а) отношение количества молей каждого газа и (б) отношение атомных масс двух газов?
Коэффициенты Ван-дер-Ваальса для кислорода равны и.Используйте эти значения, чтобы построить изотерму Ван-дер-Ваальса кислорода при 100 К. На том же графике изотермы одного моля идеального газа.
Найдите работу, выполненную в квазистатических процессах, показанных ниже. Состояния представлены как значения (p, V) для точек в плоскости pV: 1 (3 атм, 4 L), 2 (3 атм, 6 L), 3 (5 атм, 4 L), 4 (2 атм. , 6 л), 5 (4 атм, 2 л), 6 (5 атм, 5 л) и 7 (2 атм, 5 л).
а. 600 Дж; б. 0; c. 500 Дж; d. 200 Дж; е. 800 Дж; f. 500 Дж
Глоссарий
- внутренняя энергия
- среднее значение полной механической энергии всех молекул или объектов в системе
- квазистатический процесс
- эволюция системы, которая идет так медленно, что вовлеченная система всегда находится в термодинамическом равновесии
Первый закон термодинамики — Университетская физика, том 2
Цели обучения
К концу этого раздела вы сможете:
- Сформулируйте первый закон термодинамики и объясните, как его применять
- Объясните, как теплопередача, выполненная работа и изменение внутренней энергии связаны в любом термодинамическом процессе
Теперь, когда мы увидели, как рассчитать внутреннюю энергию, тепло и работу, проделанную для термодинамической системы, претерпевающей изменения во время некоторого процесса, мы можем увидеть, как эти величины взаимодействуют, чтобы повлиять на величину изменения, которое может произойти.Это взаимодействие задается первым законом термодинамики. Британскому ученому и писателю К. П. Сноу (1905–1980) приписывают шутку о четырех законах термодинамики. Его юмористическое заявление о первом законе термодинамики гласит: «Вы не можете победить», или, другими словами, вы не можете получить больше энергии из системы, чем вложили в нее. В этой главе мы увидим, как внутренняя энергия, тепло и работа играют роль в первом законе термодинамики.
Предположим, что Q представляет собой теплообмен между системой и окружающей средой, а Вт, — это работа, выполняемая системой или над ней.Первый закон гласит, что изменение внутренней энергии этой системы определяется выражением. Поскольку добавленное тепло увеличивает внутреннюю энергию системы, Q является положительным, когда оно добавляется в систему, и отрицательным, когда оно удаляется из системы.
Когда газ расширяется, он работает, и его внутренняя энергия уменьшается. Таким образом, Вт, является положительным, когда работа выполняется системой, и отрицательным, когда работа выполняется в системе. Это соглашение о знаках кратко изложено на (Рисунок). Первый закон термодинамики сформулирован следующим образом:
Первый закон термодинамики
С каждым состоянием равновесия системы связана ее внутренняя энергия. Изменение для любого перехода между двумя состояниями равновесия равно
., где Q и W представляют, соответственно, тепло, передаваемое системой, и работу, выполняемую системой или над ней.
| Условные обозначения термодинамических знаков для тепла и работы | |
|---|---|
| Процесс | Конвенция |
| Тепло добавлено в систему | |
| Отвод тепла из системы | |
| Работа, выполненная системой | |
| Работа выполнена в системе | |
Первый закон — это закон сохранения энергии.Он говорит нам, что система может обмениваться энергией с окружающей средой за счет передачи тепла и выполнения работы. Таким образом, обменная чистая энергия равна изменению полной механической энергии молекул системы (то есть внутренней энергии системы). Таким образом, если система изолирована, ее внутренняя энергия должна оставаться постоянной.
Хотя Q и W оба зависят от термодинамического пути между двумя состояниями равновесия, их разница не зависит.(Рисунок) показывает диаграмму pV системы, которая многократно совершает переход от A к B по различным термодинамическим путям. По пути 1 система поглощает тепло и работает по пути 2, она поглощает тепло и выполняет работу и так далее. Значения и могут варьироваться от пути к пути, но у нас
или
То есть изменение внутренней энергии системы между A и B не зависит от пути. В главе о потенциальной энергии и сохранении энергии мы столкнулись с другой величиной, не зависящей от пути: изменением потенциальной энергии между двумя произвольными точками в пространстве.Это изменение представляет собой отрицательный результат работы, проделанной консервативной силой между двумя точками. Потенциальная энергия является функцией пространственных координат, тогда как внутренняя энергия является функцией термодинамических переменных. Например, мы могли бы написать для внутренней энергии. Такие функции, как внутренняя энергия и потенциальная энергия, известны как функции состояния , , потому что их значения зависят исключительно от состояния системы.
Различные термодинамические пути, используемые системой при переходе от состояния A к состоянию B .Для всех переходов изменение внутренней энергии системы одинаково.Часто первый закон используется в его дифференциальной форме, то есть
.Вот бесконечно малое изменение внутренней энергии, когда бесконечно малое количество тепла dQ обменивается с системой, и бесконечно малое количество работы dW выполняет (положительный знак) или (отрицательный знак) система.
Изменения состояния и первый закон Во время термодинамического процесса система переходит из состояния A в состояние B , она получает 400 Дж тепла и выполняет 100 Дж работы.(а) Каково изменение внутренней энергии системы при этом переходе? (b) Если система затем переходит из состояния B обратно в состояние A , каково изменение ее внутренней энергии? (c) Если при переходе от A к B по другому пути работа выполняется в системе, сколько тепла она поглощает?
Стратегия Первый закон термодинамики связывает изменение внутренней энергии, работу, выполняемую системой, и тепло, передаваемое системе, в простом уравнении.Внутренняя энергия является функцией состояния и поэтому фиксируется в любой заданной точке независимо от того, как система достигает этого состояния.
Решение
- Из первого закона изменение внутренней энергии системы составляет
- Рассмотрим замкнутый путь, который проходит через состояния A и B . Внутренняя энергия — это функция состояния, поэтому для замкнутого пути она равна нулю. Таким образом,
и
Это дает - Изменение внутренней энергии одинаково для любого пути, поэтому
и теплообменник
Знак минус указывает на то, что при этом переходе система теряет тепло.
Значение Когда замкнутый цикл рассматривается в качестве первого закона термодинамики, изменение внутренней энергии на всем пути равно нулю. Если бы трение играло роль в этом примере, добавление тепла привело бы к меньшему объему работы. (Рисунок) учитывает, что происходит, если трение играет роль.
Обратите внимание, что на (Рисунок) мы не предполагали, что переходы были квазистатическими. Это потому, что первый закон не подлежит такому ограничению.Он описывает переходы между состояниями равновесия, но не касается промежуточных состояний. Система не должна проходить только через состояния равновесия. Например, если газ в стальном контейнере при четко определенной температуре и давлении заставить взорваться с помощью искры, часть газа может конденсироваться, различные молекулы газа могут объединяться с образованием новых соединений, и могут быть все своего рода турбулентность в контейнере, но в конечном итоге система придет к новому состоянию равновесия.Эта система явно не находится в равновесии во время своего перехода; однако его поведение по-прежнему определяется первым законом, потому что процесс начинается и заканчивается, когда система находится в состоянии равновесия.
Полировка фитинга Машинист полирует медный фитинг весом 0,50 кг кусочком наждачной бумаги в течение 2,0 мин. Он перемещает ткань по фитингу с постоянной скоростью 1,0 м / с, прилагая усилие 20 Н по касательной к поверхности фитинга. (а) Какая общая работа, проделанная машинистом на фитинге? (б) Каково увеличение внутренней энергии фитинга? Предположим, что изменение внутренней энергии ткани незначительно и между фитингом и окружающей средой не происходит теплообмена.(c) Каково повышение температуры арматуры?
Стратегия Сила машиниста на расстоянии, которую можно рассчитать по заданной скорости и времени, — это работа, проделанная в системе. Работа, в свою очередь, увеличивает внутреннюю энергию системы. Эту энергию можно интерпретировать как тепло, которое повышает температуру системы за счет ее теплоемкости. Будьте осторожны со знаком каждого количества.
Решение
- Мощность, создаваемая силой, действующей на объект, или скорость, с которой механик выполняет работу трения с фитингом, равна.Таким образом, за истекшее время (2,0 мин) на фитинге проделано
работ. - Предполагается, что между фитингом и окружающей средой не происходит теплообмена, поэтому первый закон дает изменение внутренней энергии фитинга:
- Так как не зависит от пути, эффект работы такой же, как если бы он подавался при атмосферном давлении посредством передачи тепла. Таким образом,
и повышение температуры штуцера
, где мы использовали значение удельной теплоемкости меди,.
Значение Если выделялось тепло, изменение внутренней энергии было бы меньшим и вызвало бы меньшее изменение температуры, чем то, что было рассчитано в задаче.
Проверьте свое понимание г Приведенные ниже величины представляют четыре различных перехода между одним и тем же начальным и конечным состоянием. Заполнить бланки.
| Q (Дж) | Вт (Дж) | |
|---|---|---|
| –80 | –120 | |
| 90 | ||
| 40 | ||
| –40 |
Проверьте свое понимание Почему было необходимо утверждать, что процесс (рисунок) является квазистатическим?
Таким образом, процесс представлен кривой на графике pV для оценки работы.
Проверьте свое понимание Когда 1,00 г аммиака закипает при атмосферном давлении и его объем изменяется от 1,47 до. Его теплота испарения при этом давлении равна. Каково изменение внутренней энергии аммиака при его испарении?
Сводка
- Внутренняя энергия термодинамической системы является функцией состояния и, таким образом, уникальна для каждого состояния равновесия системы.
- Увеличение внутренней энергии термодинамической системы дается за счет тепла, добавляемого к системе, за вычетом работы, выполняемой системой в любом термодинамическом процессе.
Концептуальные вопросы
Что первый закон термодинамики говорит нам об энергии Вселенной?
Всегда ли добавление тепла к системе увеличивает ее внутреннюю энергию?
Если в системе выполняется больше работы, чем добавляется тепла, внутренняя энергия системы фактически уменьшается.
Много усилий, времени и денег было потрачено на поиски так называемой машины с вечным двигателем, которая определяется как гипотетическая машина, которая работает или производит полезную работу бесконечно долго, и / или гипотетическую машину, которая производит больше работы или энергии, чем потребляет.Объясните в терминах первого закона термодинамики, почему или почему не может быть построена такая машина.
Проблемы
Когда разбавленный газ квазистатически расширяется от 0,50 до 4,0 л, он совершает 250 Дж работы. Если предположить, что температура газа остается постоянной на уровне 300 К, (а) каково изменение внутренней энергии газа? б) Сколько тепла поглощается газом в этом процессе?
При квазистатическом изобарическом расширении 500 Дж работы совершает газ.Давление газа составляет 0,80 атм, и первоначально оно составляло 20,0 л. Если внутренняя энергия газа увеличилась на 80 Дж при расширении, сколько тепла газ поглотит?
Идеальный газ квазистатически и изотермически расширяется из состояния с давлением p и объемом V в состояние с объемом 4V. Сколько тепла добавляется расширяющемуся газу?
Как показано ниже, если тепло, поглощаемое газом вдоль AB, составляет 400 Дж, определите количество тепла, поглощенного вдоль (a) ADB; (б) ACB; и (c) ADCB.
а. 600 Дж; б. 600 Дж; c. 800 Дж
Во время изобарного расширения от A до B, представленного ниже, из газа отводится 130 Дж тепла. Как изменилась его внутренняя энергия?
(a) Каково изменение внутренней энергии процесса, представленного замкнутым путем, показанным ниже? б) Сколько тепла передается? (c) Если путь проходит в противоположном направлении, сколько тепла передается?
а.0; б. 160 Дж; c. –160 Дж
Когда газ расширяется по пути AC, показанному ниже, он совершает 400 Дж работы и поглощает 200 или 400 Дж тепла. (а) Предположим, вам сказали, что на пути ABC газ поглощает 200 или 400 Дж тепла. Какое из этих значений правильное? (б) Дайте правильный ответ из части (а), сколько работы выполняет газ вдоль линии ABC? (c) Вдоль CD внутренняя энергия газа уменьшается на 50 Дж. Сколько тепла передается газом на этом пути?
Когда газ расширяется вдоль AB (см. Ниже), он совершает 500 Дж работы и поглощает 250 Дж тепла.Когда газ расширяется вдоль AC , он выполняет 700 Дж работы и поглощает 300 Дж тепла. (а) Сколько тепла обменивается газом вдоль BC ? (b) Когда газ осуществляет передачу от C к A по CDA , на нем выполняется 800 Дж работы от C до D . Сколько тепла передает CDA ?
Разбавленный газ хранится в левой камере контейнера, стенки которого идеально изолируют (см. Ниже), а правая камера откачивается.Когда перегородка снимается, газ расширяется и заполняет всю емкость. Посчитайте работу, проделанную газом. Меняется ли при этом внутренняя энергия газа?
Идеальные газы A и B хранятся в левой и правой камерах изолированного контейнера, как показано ниже. Перегородка снимается и газы смешиваются. Выполняется ли какая-либо работа в этом процессе? Если температуры A и B изначально равны, что произойдет с их общей температурой после их смешивания?
Никаких работ не выполняется, и они достигают одинаковой общей температуры.
Идеальный одноатомный газ при давлении и температуре 300 K претерпевает квазистатическое изобарическое расширение из (а) Какую работу совершает газ? б) Какова температура газа после расширения? (c) Сколько там молей газа? (г) Как изменяется внутренняя энергия газа? (e) Сколько тепла добавляется к газу?
Рассмотрим процесс для пара в цилиндре, показанный ниже. Предположим, изменение внутренней энергии в этом процессе составляет 30 кДж.Найдите тепло, поступающее в систему.
Состояние 30 моль пара в цилиндре изменяется циклически от abca, где давление и объем состояний равны: a (30 атм, 20 л), b (50 атм, 20 л) и c (50 атм, 45 л). Предположим, что каждое изменение происходит вдоль линии, соединяющей начальное и конечное состояния в плоскости pV. (а) Отобразите цикл в плоскости pV. (б) Найдите чистую работу, выполненную паром за один цикл. (c) Найдите чистое количество теплового потока в паре в течение одного цикла.
Металлический контейнер фиксированного объема, погруженный в большой резервуар с температурой, содержит два отсека, разделенных свободно подвижной стенкой. Первоначально стенка удерживается на месте пробкой, так что 0,02 моль газообразного азота с одной стороны и 0,03 моль газообразного кислорода с другой стороны, каждый из которых занимает половину объема. Когда стопор снимается, стена перемещается и принимает окончательное положение. Движение стены контролируется так, что стена движется бесконечно малыми квазистатическими шагами.(а) Найдите окончательные объемы двух сторон, принимая идеальное поведение газов для двух газов. б) Сколько работы каждый газ выполняет над другим? (c) Как изменяется внутренняя энергия каждого газа? (d) Найдите количество тепла, которое входит или выходит из каждого газа.
Газ в цилиндрическом закрытом контейнере адиабатически и квазистатически расширяется от состояния A (3 МПа, 2 л) до состояния B с объемом 6 л вдоль пути (a) Постройте путь в пВ самолет.(б) Найдите количество работы, совершаемой газом, и изменение внутренней энергии газа во время процесса.
а.
;
г.
Глоссарий
- первый закон термодинамики
- изменение внутренней энергии для любого перехода между двумя состояниями равновесия равно
35A: температура, внутренняя энергия, тепло и удельная теплоемкость
Как вы знаете, температура — это мера того, насколько что-то горячее.Потрите две палочки вместе, и вы заметите, что температура каждой увеличивается. Вы поработали с палками, и их температура повысилась. Работа — это передача энергии. Итак, вы передали энергию палкам, и их температура повысилась. Это означает, что повышение температуры системы является показателем увеличения внутренней энергии (также известной как тепловая энергия) системы. (В этом контексте слово «система» — это термодинамический жаргон для обобщения слова «объект».Действительно, объект, скажем, железный шар, может быть системой. Система — это просто предмет наших исследований или размышлений. Система может быть такой же простой, как проба одного вида газа или кусок одного вида металла, или может быть более сложной, как в случае банки плюс немного воды в банке плюс термометр в воде плюс крышка на банке. В данном случае система представляет собой две палки.) Внутренняя энергия системы — это энергия, связанная с движением молекул, атомов и частиц, составляющих атомы, относительно центра масс системы, а также потенциал энергия, соответствующая положениям и скоростям вышеупомянутых субмикроскопических составляющих системы относительно друг друга.Как обычно при учете энергии, абсолютный ноль энергии в случае внутренней энергии не имеет значения — только изменения внутренней энергии имеют значение. Таким образом, вы или издатель таблицы значений внутренней энергии (для данного вещества издатели фактически указывают внутреннюю энергию на массу или внутреннюю энергию на моль вещества при определенных условиях, а не внутреннюю энергию образца такого вещества). вещество), свободны выбирать нуль внутренней энергии для данной системы.Делая какие-либо прогнозы относительно физического процесса с участием этой системы, пока вы придерживаетесь одного и того же нуля внутренней энергии на протяжении всего анализа, измеримые результаты вашего прогноза или объяснения не будут зависеть от вашего выбора нуля внутренней энергии.
Другой способ повысить температуру пары палочек — это привести их в контакт с чем-то более горячим, чем палочки. Когда вы это сделаете, температура палочек автоматически повысится — вам не придется с ними работать.Опять же, повышение температуры любой ручки указывает на увеличение внутренней энергии этой ручки. Откуда взялась эта энергия? Должно быть, он исходил от более горячего объекта. Вы также можете заметить, что температура более горячего предмета снизилась, когда вы соприкоснулись с палками. Снижение температуры более горячего объекта является показателем того, что количество внутренней энергии более горячего объекта уменьшилось. Вы соприкасались более горячим предметом с палками, и энергия автоматически передавалась от более горячего объекта к палкам.Передача энергии в этом случае называется потоком тепла. Тепло — это энергия, которая автоматически передается от более горячего объекта к более холодному, когда вы приводите два объекта в контакт друг с другом. Тепло — это не то, что есть в системе, а энергия, которая передается или передается. Как только он попадает в систему, в которую он передается, мы называем это внутренней энергией. Идея состоит в том, чтобы различать то, что делается с системой: «В системе выполняется работа и / или в нее поступает тепло», от того, как система изменяется в результате того, что с ней было сделано, « внутренняя энергия системы увеличивается.”
Тот факт, что повышение температуры объекта является показателем энергии, передаваемой этому объекту, может означать, что каждый раз, когда вы передаете энергию объекту, его температура увеличивается. Но это не так. Попробуйте положить горячую ложку в стакан с ледяной водой. (Здесь мы рассматриваем случай, когда льда достаточно, чтобы не весь лед растаял.) Ложка становится такой же холодной, как ледяная вода, и часть льда тает, но температура ледяной воды остается той же (0 ° С).Охлаждение ложки указывает на то, что от нее передавалась энергия, и поскольку ложка контактировала с ледяной водой, энергия должна была передаваться ледяной воде. Действительно, лед претерпевает заметные изменения; часть тает. Наличие большего количества жидкой воды и меньшего количества льда указывает на то, что в ледяной воде больше энергии. И снова произошла передача энергии от ложки к ледяной воде. Эта передача представляет собой автоматический поток тепла, который происходит, когда две системы контактируют друг с другом.Очевидно, что тепловой поток не всегда приводит к повышению температуры.
Эксперимент показывает, что когда объект с более высокой температурой контактирует с объектом с более низкой температурой, тепло передается от объекта с более высокой температурой к объекту с более низкой температурой. Поток тепла сохраняется до тех пор, пока два объекта не достигнут одной и той же температуры. Мы определяем среднюю поступательную кинетическую энергию молекулы системы как сумму поступательных кинетических энергий всех молекул, составляющих систему, деленную на общее количество молекул.Когда две простые идеальные газовые системы, каждая из которых включает множество одиночных атомных молекул, взаимодействующих посредством упругих столкновений, объединяются, мы обнаруживаем, что поток тепла от системы, в которой средняя поступательная кинетическая энергия на молекулу больше, чем у системы, в которой средняя кинетическая энергия поступательная кинетическая энергия на молекулу меньше. Это означает, что первая система имеет более высокую температуру. То есть, чем выше поступательная кинетическая энергия в среднем частиц, составляющих систему, тем выше температура.Это верно для многих систем.
Твердые тела состоят из атомов, которые связаны с соседними атомами, так что молекулы стремятся удерживаться в своем положении относительно основной массы твердого тела за счет электростатических сил. Пара молекул, которые связаны друг с другом, имеет меньшее количество внутренней потенциальной энергии по сравнению с той же парой молекул, когда они не связаны вместе, потому что мы должны добавить энергию связанной паре в состоянии покоя, чтобы получить свободную пару в состоянии покоя. . В случае ледяной воды передача энергии ледяной воде приводит к разрыву связей между молекулами воды, что мы видим как таяние льда.Таким образом, передача энергии ледяной воде приводит к увеличению внутренней потенциальной энергии системы.
Два различных вида внутренней энергии, которые мы обсудили, — это внутренняя потенциальная энергия и внутренняя кинетическая энергия. Когда есть чистая передача энергии в систему, а макроскопическая механическая энергия системы не изменяется (например, в случае объекта вблизи поверхности земли, скорость объекта в целом не увеличивается, и высота объекта не увеличивается), внутренняя энергия (внутренняя кинетическая энергия, внутренняя потенциальная энергия или и то, и другое) системы увеличивается.В некоторых, но не во всех случаях, увеличение внутренней энергии сопровождается повышением температуры системы. Если температура не повышается, то, вероятно, мы имеем дело со случаем, когда увеличивается внутренняя потенциальная энергия системы.
Теплоемкость и удельная теплоемкость
Обратим внимание на случаи, когда поток тепла в образец вещества сопровождается повышением температуры образца. Для многих веществ в определенных температурных диапазонах изменение температуры (по крайней мере приблизительно) пропорционально количеству тепла, поступающего в вещество.
\ [\ Delta T \ propto Q \]
Традиционно коэффициент пропорциональности записывается как \ (\ frac {1} {C} \), так что
\ [\ Delta T = \ frac {1} {C} Q \]
, где верхний регистр \ (C \) — теплоемкость. Это уравнение чаще записывается как
\ [Q = C \ Delta T \ label {35-1} \]
, в котором указано, что количество тепла, которое должно поступать в систему, чтобы изменить температуру этой системы на \ (\ Delta T \), представляет собой теплоемкость \ (C \), умноженную на желаемое изменение температуры \ (\ Delta T \) .Таким образом, теплоемкость \ (C \) — это «количество тепла при изменении температуры». Это обратная величина — это мера температурной чувствительности системы к тепловому потоку.
Давайте сосредоточим наше внимание на простейшем виде системы, на образце одного вида материи, например, на определенном количестве воды. Количество тепла, необходимое для изменения температуры образца на определенное количество, прямо пропорционально массе отдельного вещества; Например, если вы удвоите массу образца, потребуется вдвое больше тепла, чтобы повысить его температуру, например, на 1 ° C.Математически мы можем записать этот факт как
\ [C \ propto \ space m \]
Для константы пропорциональности традиционно используется строчная буква c. Тогда
\ [C = см \]
, где коэффициент пропорциональности \ (C \) — это удельная теплоемкость вещества на массу. Удельная теплоемкость \ (C \) называется удельной теплоемкостью по массе или просто удельной теплоемкостью рассматриваемого вещества. (В этом контексте прилагательное «специфический» означает «на сумму.Поскольку количество может быть указано более чем одним способом, у нас есть выражение «удельная масса», означающая «на количество массы», и выражение «удельная молярность», означающая «на число молей». Здесь, поскольку мы имеем дело только с удельной теплоемкостью массы, мы можем опустить слово «масса», не вызывая путаницы.{\circ}}]\)»> 448
\ (\ ast \) Удельная теплоемкость вещества зависит от температуры и давления.Приведенные значения соответствуют атмосферному давлению. Можно ожидать, что использование этих репрезентативных постоянных значений для случаев, включающих диапазоны атмосферного давления и температуры от -100 ° C до + 600 ° C, в зависимости от фазы материала, даст разумные результаты, но если требуется точность, или информация о насколько разумны ваши результаты, вам следует обратиться к учебнику по термодинамике и таблицам термодинамики и провести более сложный анализ.
Обратите внимание, на сколько джоулей энергии необходимо больше, чтобы поднять температуру 1 кг жидкой воды на 1 ° C, чем требуется для повышения температуры 1 кг металла на 1 ° C.
Температура
Несмотря на то, что вы хорошо с ним знакомы, уместно еще поговорить о температуре. Каждый раз, когда вы что-то измеряете, вы на самом деле просто сравниваете это с произвольно установленным стандартом. Например, когда вы измеряете длину стола метровой палкой, вы сравниваете длину стола с современным эквивалентом того, что исторически считалось одной десятитысячной расстояния от северного полюса Земли до экватора. .Что касается температуры, стандарт, теперь называемый «градусом Цельсия», был установлен следующим образом: при давлении в 1 атмосферу температура, при которой вода замерзает, была определена как 0 ° C, а температура, при которой вода закипала, была определена как быть 100 ° C. Затем для интерполяции и экстраполяции температурного диапазона использовалось вещество с измеряемой характеристикой, зависящей от температуры, такой как длина столба жидкой ртути. (Отметьте положение конца столбика ртути на трубке, содержащей эту ртуть, когда он находится при температуре замерзающей воды, и еще раз, когда он имеет температуру кипящей воды.Разделите интервал между двумя отметками на сто частей. Используйте одинаковую длину каждой из этих частей, чтобы удлинить шкалу в обоих направлениях и назовите ее температурной шкалой.)
Обратите внимание на произвольную установку нуля шкалы Цельсия. Выбор нуля не имеет значения для наших целей, поскольку уравнения \ (\ ref {35-1} \) (\ (Q = C \ Delta T \)) и \ (\ ref {35-2} \) (\ (Q = mc \ Delta T \)) связывает изменение температуры, а не саму температуру, с количеством теплового потока.Для системы единиц СИ установлена шкала абсолютной температуры. Нуль температуры на этой шкале устанавливается на максимально возможную температуру, так что теоретически невозможно, чтобы температура любой системы в равновесии была ниже нуля шкалы Кельвина. Единицей измерения температуры по шкале Кельвина является Кельвин, сокращенно К. Обратите внимание на отсутствие символа градуса в этой единице. Шкала Кельвина похожа на шкалу Цельсия в том, что изменение температуры, скажем, на 1 К эквивалентно изменению температуры на 1 ° С.(Примечание относительно обозначения единиц измерения: единицы ° C используются для температуры по шкале Цельсия, а единицы C ° используются для изменения температуры по шкале Цельсия.)
По шкале Кельвина при давлении в одну атмосферу вода замерзает при температуре \ (273,15 К \). Итак, температура в кельвинах связана с температурой в ° C на
.\ [\ mbox {Температура в K} = (\ mbox {Температура в ° C}) \ cdot \ Big (\ frac {1K} {C} \ Big) +273,15 K \]
Авторы и авторство
7.3: Внутренняя энергия, работа и тепло
Работа
Мы уже определили работу как силу, действующую на расстоянии. Оказывается, есть и другие эквивалентные определения работы, которые также важны в химии.
Когда определенный объем газа расширяется, он работает против внешнего давления и расширяется (Рис. 7.3.1 — Объем в зависимости от давления)
То есть газ должен выполнять работу. Предполагая, что внешнее давление P ext является постоянным, объем работы, выполняемой газом, определяется уравнением
w = — P внешний × Δ V
где Δ V — изменение объема газа.Этот термин всегда представляет собой конечный объем минус начальный объем,
.Δ В = В окончательный — В начальный
и может быть положительным или отрицательным, в зависимости от того, V final больше (расширяется) или меньше (сокращается), чем V initial . Отрицательный знак в уравнении для работы важен и означает, что по мере увеличения объема (Δ V положительно) газ в системе теряет энергию в качестве работы.С другой стороны, если газ сжимается, Δ V отрицательно, и два отрицательных знака делают работу положительной, поэтому в систему добавляется энергия.
Рис. 7.3.1 Зависимость объема от давления
Когда газ расширяется против внешнего давления, газ действительно работает.
Наконец, рассмотрим единицы. Изменения объема обычно выражаются в таких единицах, как литры, тогда как давление обычно выражается в атмосферах.Когда мы используем уравнение для определения работы, единица измерения работы получается как литр · атмосфера или л · атм. Это не очень распространенная единица для работы. Однако существует переводной коэффициент между л · атм и обычной единицей работы, джоулями:
.1 л · атм = 101,32 Дж
Используя этот коэффициент преобразования и предыдущее уравнение для работы, мы можем рассчитать работу, выполняемую при расширении или сжатии газа.
Пример \ (\ PageIndex {1} \):
Какую работу совершает газ, если он расширяется от 3.44 л до 6,19 л при постоянном внешнем давлении 1,26 атм? Выразите окончательный ответ в джоулях.
Решение
Сначала нам нужно определить изменение объема, Δ В . Изменением всегда является конечное значение минус начальное значение:
Δ В = В окончательный — В начальный = 6,19 л — 3,44 л = 2,75 л
Теперь мы можем использовать определение работы для определения проделанной работы:
w = — P внешний · Δ V = — (1.26 атм) (2,75 л) = −3,47 л · атм
Теперь мы построим коэффициент преобразования из отношения между литром · атмосферой и джоулями:
\ [- 3.47 \ not {L.atm} \ times \ times \ frac {101.32 \, J} {1 \ not {L.atm}} = — 351 \, J \]
Мы ограничиваем окончательный ответ тремя значащими цифрами, если это необходимо.
Упражнение \ (\ PageIndex {1} \)
Проверьте себя
Какая работа выполняется, когда газ расширяется с 0,66 л до 1,33 л при внешнем давлении 0.775 атм?
Ответ
−53 Дж
Тепло
Тепло — еще один аспект энергии. Тепло — это передача энергии от одного тела к другому из-за разницы температур. Например, когда мы касаемся чего-то руками, мы интерпретируем этот объект как горячий или холодный, в зависимости от того, как передается энергия: если энергия передается в ваши руки, объект ощущается горячим. Если энергия передается от ваших рук к объекту, они становятся холодными.Поскольку тепло является мерой передачи энергии, оно также измеряется в джоулях.
Для данного объекта количество тепла ( q ) пропорционально двум вещам: массе объекта ( m ) и изменению температуры (Δ T ), вызванному передачей энергии. Мы можем записать это математически как
\ [q \ alpha \, m \ times \ Delta T \]
, где ∝ означает «пропорционально». Чтобы сделать пропорциональность равенством, мы включаем константу пропорциональности.В этом случае константа пропорциональности обозначена как c и называется удельной теплоемкостью , или, более кратко, удельной теплоемкостью :
.q = мк Δ T
, где масса, удельная теплоемкость и изменение температуры умножаются. Удельная теплоемкость — это мера того, сколько энергии необходимо для изменения температуры вещества; чем больше удельная теплоемкость, тем больше энергии требуется для изменения температуры. {\ circ} C)} \]
Соединив числа и собрав все единицы, получим
\ [c = 0.{\ circ} C} \]
Упражнение \ (\ PageIndex {3} \)
Проверьте себя
Золото имеет удельную теплоемкость 0,129 Дж / г · ° C. Если для повышения температуры образца золота на 99,9 ° C требуется 1377 Дж, какова масса золота?
Ответ
107 г
| Вещество | Удельная теплоемкость (Дж / г · ° C) |
|---|---|
| вода | 4,184 |
| утюг | 0,449 |
| золото | 0,129 |
| ртуть | 0.139 |
| алюминий | 0,900 |
| спирт этиловый | 2,419 |
| магний | 1,03 |
| гелий | 5,171 |
| кислород | 0,918 |
Таблица 7.3.1 Удельная теплоемкость различных веществ
Внутренняя энергия
Внутренняя энергия определяется как сумма всей энергии в системе.Эта энергия может принимать форму, работать или нагреваться. Мы используем символ ΔE для обозначения любых изменений внутренней энергии системы и учитываем эти изменения через работу и тепло
\ [\ Delta E = w + q \]
Мы знаем, что при экзотермической реакции система теряет тепло, а знак q отрицательный. Если у нас есть эндотермическая реакция, система получает тепло и знак q положительный. Любая работа, выполняемая системой, требует энергии, и система теряет энергию, поэтому знак w отрицательный.Если над системой выполняется работа, система получает энергию и знак w положительный.
| Энергетика | Изменение | Знак |
|---|---|---|
| кв | Тепло выделяется системой (эндотермическое) | + д |
| Теплоотвод в системе (экзотермический) | -q | |
| Вт | Работа выполнена по системе (компрессия) | + w |
| Работа ведется системой (расширение) | -w |
Путем сохранения энергии любое изменение энергии системы должно учитывать любую энергию, полученную системой, и любую энергию, потерянную системой.
Пример \ (\ PageIndex {4} \):
Как изменится внутренняя энергия газа, если газ получит 10 кДж тепла и расширится, совершив работу 5 кДж?
Решение
Мы можем использовать
\ [\ Delta E = q + w \]
Поскольку газ (наша система) получил 10 кДж тепла, q положительно
\ [q = +10 \, кДж \]
Система работала, используя энергию в процессе, поэтому система потеряла энергии, а w отрицательна.
\ [w = -5 \, кДж \]
Собираем вместе
\ [\ Delta E = q + w = 10 \, кДж + (-5 \, кДж) = 10 \, кДж — 5 \, кДж = +5 \, кДж \]
Таким образом, система получила всего 5 кДж энергии.
Ключевые выводы
- Работа может быть определена как изменение объема газа при постоянном внешнем давлении.
- Тепло — это передача энергии из-за разницы температур.
- Теплота может быть рассчитана через массу, изменение температуры и удельную теплоемкость.
- Общее изменение внутренней энергии для системы представляет собой сумму работы и тепла
Упражнение \ (\ PageIndex {1} \)
- Дайте два определения работы.
Какой знак работы при увеличении объема пробы газа? Объясните, почему у работы есть этот знак.
Что происходит, когда газ расширяется с 3,00 л до 12,60 л при внешнем давлении 0,888 атм?
Что есть работа, когда газ расширяется от 0.666 л до 2,334 л при внешнем давлении 2,07 атм?
Какова работа, когда газ сжимается с 3,45 л до 0,97 л при внешнем давлении 0,985 атм?
Какова работа, когда газ сжимается с 4,66 л до 1,22 л при внешнем давлении 3,97 атм?
Как и работа, знак тепла может быть положительным или отрицательным. Что происходит с общей энергией системы, если тепло положительно?
Как и работа, знак тепла может быть положительным или отрицательным.Что происходит с полной энергией системы, если тепло отрицательно?
Что такое тепло, когда 55,6 г Fe повышают температуру с 25,6 ° C до 177,9 ° C? Теплоемкость Fe приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Что такое тепло, когда 0,444 г золота повышают температуру с 17,8 ° C до 222,5 ° C? Теплоемкость золота приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Что такое тепло, когда 245 г H 2 O охлаждают с 355 K до 298 K? Теплоемкость H 2 O приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Что такое тепло, когда 100,0 г Mg охлаждают с 725 K до 552 K? Теплоемкость Mg приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Для повышения температуры до 36 требуется 452 Дж тепла.8 г образца металла от 22,9 ° C до 98,2 ° C. Какова теплоемкость металла?
Требуется 2267 Дж тепла, чтобы поднять температуру образца металла массой 44,5 г с 33,9 ° C до 288,3 ° C. Какова теплоемкость металла?
Экспериментатор добавляет 336 Дж тепла к 56,2 г образца Hg. Каково его изменение температуры? Теплоемкость Hg приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
К навеске 0,444 г H 2 O добавляют 23,4 Дж тепла. Каково его изменение температуры? Теплоемкость H 2 O приведена в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Неизвестная масса алюминия поглощает 187,9 Дж тепла и увеличивает его температуру с 23,5 ° C до 35,6 ° C. Какая масса у алюминия? Сколько это молей алюминия?
- Образец He идет от 19.От 4 ° C до 55,9 ° C при добавлении 448 Дж энергии. Какая масса у гелия? Сколько это молей гелия?
- Образец газа He нагревается с добавлением 34 кДж тепла и 52 кДж работы выполняется для сжатия газа. Какое значение ΔE?
- Образец газа He нагревается, добавляется 51 кДж тепла, и газ расширяется, выполняя работу 12 кДж. Каково значение ΔE?
- Образец газа He охлаждается, теряет 42 кДж тепла, а газ расширяется, выполняя 13 кДж работы. Каково значение ΔE?
Ответы
- Работа — это сила, действующая через расстояние или объем, изменяющийся против некоторого давления.
При положительном нагреве общая энергия системы увеличивается.
Набор вопросов 10
Набор вопросов 101 .Количество, показывающее, насколько тепло или холодно тело. относительно некоторого стандартного тела называется
А) тепло.
Б) внутренняя энергия.
C) температура.
Г) молекулярная кинетическая энергия.
2. Внутренняя энергия, передаваемая от одного кузов на другой из-за разницы температур называется
А) тепло.
Б) потенциальная энергия.
В) температура.
Г) молекулярная кинетическая энергия.
3. Температура является мерой
А) потенциальная энергия молекул
Б) количество тепла в теле
В) средняя кинетическая энергия молекул
Г) полная энергия всех молекул в теле
4. Контейнер с газообразным водородом такой же температуры как контейнер с более плотным газообразным кислородом.Атомы газа, имеющие более высокая средняя кинетическая энергия у
А) водород,
Б) кислород,
В) то же самое,
Рассуждение: Поскольку они имеют одинаковую температуру, их средние кинетические энергии должны быть одинаковыми.
5. а атомы газа, имеющие большую среднюю скорость
А) водород.
Б) кислород.
В) оба одинаковые.
Рассуждение: Атомы водорода имеют меньшие размеры. масса, чем кислород. Таким образом, их скорости должны быть выше, чтобы производить то же самое. средние кинетические энергии.
6. Что из следующего расширяется больше всего при повышении температуры?
А) утюг
Б) ледяная вода
В) гелий
Г) все расширяют одинаковые
Рассуждение: Гелий расширяется больше, потому что это газ.
7. Что из следующего больше всего расширяется при повышении температуры? уменьшается?
A) железо
B) ледяная вода
В) гелий
Г) все расширяют одинаковые
Рассуждение: Обычно, когда объекты Охлажденные, они сжимаются, однако ледяная вода является исключением. Он будет расширяться как он охлаждается и замерзает до большего объема.
8. Разница температур льда и пара точек воды
A) 180 oC
B) 100 K
В) 100 ° F
D) 273 oC
Рассуждение: Вода имеет температуру точки замерзания. 273 К (означает шкалу Кельвина), а температура кипения 373 К. составляет 100 К.
9. При понижении температуры 2,0 кг воды на 10 ° C количество удаляемого тепла составит
A) 10 ккал
B) 20 ккал
C) 20 ккал
D) 10 кал
10. Когда образец воздуха сжимается, его температура
A) увеличивается.
Б) убывает.
C) остается без изменений.
11. Одна из причин этого заключается в том, что молекула газа в сжатый воздух сталкивается с другими, что в среднем составляет
А) движущиеся.
Б) расширяющийся.
В) отступление.
D) приближается.
12. Какая из них имеет наибольшую тепловую энергию?
А) кубик льда объемом 1 куб. Дюйм
Б) чайник объемом 1 литр, наполненный кипятком
В) ванна, наполненная 20 галлонами теплой воды
Рассуждение: Тепловая энергия — это сумма всех внутренних энергий объекта. В ванне больше молекул ванна и сумма их энергий больше, чем чайник.
13. Направление передачи тепла между два тела зависит от
A) их температура
Б) их давления
В) их тепловая энергия
D) твердые, жидкие или газообразные
14. Когда вода нагревается до 4oC, она расширяется. Когда вода при 4oC охлаждается, это
A) контракты,
B) расширяется,
В) ни сжимается, ни расширяется,
D)… недостаточно информации дано.
15. что следует из того, что
A) охлаждение снижает кинетическую энергию молекул h3O.
B) вода имеет максимальную плотность при 4oC.
В) мы не знаем, как вода охлаждается.
Рассуждение: См. Стр. 300.
16. Почему пар при 100 ° C опаснее воды при 100 oC?
A) пар более горячий
B) пар имеет больше внутренней энергии на грамм
В) пар имеет более высокую удельную теплоемкость, чем вода
Г) пар имеет меньшую вязкость
17. В процессе испарения
A) более тяжелые атомы наиболее склонны покидать жидкость,
Б) есть чистый выигрыш в количестве атомов в жидкости,
В) энергия поглощается жидкостью,
D) все это,
E) ни одно из этих
18. Когда молекула сталкивается с другой, приближающейся с большим импульсом, его скорость отскока
A) остается прежним,
B) увеличивается,
В) убавки,
19. И когда одна молекула сталкивается с другой, то есть отступая, его скорость отскока
A) остается прежним.
Б) увеличивается.
C) убывает.
20. Требуется ли больше тепла для повышения температуры 5 граммов льда или 5 граммов воды при температуре 6 oC?
A) лед
B) вода
C) ….. в обоих случаях требуется одинаковое количество тепла
21. Сколько джоулей эквивалентно 21 калории?
А) 4,18
Б) 17
В) 25
Г) 88
Рассуждение: Одна кал = 4,18 джоуля. Таким образом, 21 кал = 21 х 4,18 = 88 джоулей.
22. При условии, что в каждом случае погонная энергия одинакова, кипение происходит быстрее
A) на уровне моря.
Б) в долине.
В) в гор.
23. Это потому, что
А) повышенное давление на поверхность жидкости снижает ее точка кипения.
B) пониженное давление на поверхности жидкости снижает ее кипение точка.
В) вода всегда закипает быстрее всего на уровне моря.
24. Когда твердое вещество превращается в жидкость, а затем в газ, энергия
A) освобождено,
B) поглощено,
25.

Leave A Comment