Необратимые и обратимые реакции | АЛХИМИК
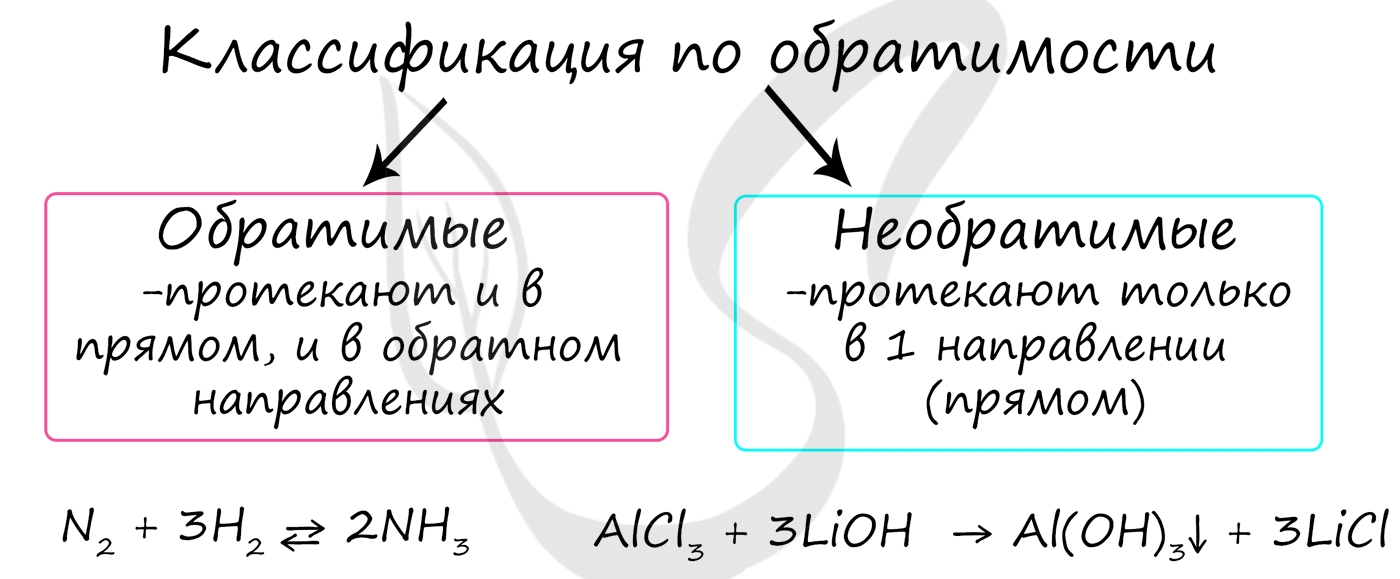
Все химические реакции делятся на два типа: обратимые и необратимые.
Необратимыми называются реакции, которые протекают только в одном направлении, т. е. продукты этих реакций не взаимодействуют друг с другом с образованием исходных веществ.
Необратимая реакция заканчивается тогда, когда полностью расходуется хотя бы одно из исходных веществ. Необратимыми являются реакции горения; многие реакции термического разложения сложных веществ; большинство реакций, в результате которых образуются осадки или выделяются газообразные вещества, и др. Например:
C2H5OH + 3O2 → 2CO2 + 3H2O
2KMnO4 = K2MnO4 + MnO2 + O2↑
BaCl2 + H2SO4 = BaSO4↓ + 2HCl
Обратимыми называются реакции, которые одновременно протекают в прямом и в обратом направлениях:

В уравнениях обратимых реакций используется знак обратимости  .
.
Примером обратимой реакции является синтез йодоводорода из водорода и йода:
Через некоторое время после начала химической реакции в газовой смеси можно обнаружить не только конечный продукт реакции НI, но и исходные вещества —H2 и I2. Как бы долго ни продолжалась реакция, в реакционной смеси при 350oС всегда будет содержаться приблизительно 80% HI,10% Н2 и 10% I2
Если в качестве исходных веществ взяты водород и йод в концентрациях [H2] и [I2], то скорость прямой реакции в начальный момент времени была равна: vпр = kпр[H2] ∙ [I2]. Скорость обратной реакции vобр = kобр[HI]2 в начальный момент времени равна нулю, так как йодоводород в реакционной смеси отсутствует ([HI] = 0). Постепенно скорость прямой реакции уменьшается, так как водород и йод вступают в реакцию и их концентрации понижаются. При этом скорость обратной реакции увеличивается, потому что концентрация образующегося йодоводорода постепенно возрастает. Когда скорости прямой и обратной реакций станут одинаковыми, наступает химическое равновесие. В состоянии равновесия за определенный промежуток времени образуется столько же молекул НI, сколько их распадается на Н
Состояние обратимой реакции, при котором скорость прямой реакции равна скорости обратной реакции, называется химическим равновесием.
Химическое равновесие является динамическим равновесием. В равновесном состоянии продолжают протекать и прямая, и обратная реакции, но так как скорости их равны, концентрации всех веществ в реакционной системе не изменяются. Эти концентрации называются равновесными концентрациями.
Смещение химического равновесия
Принцип Ле-Шателье
Химическое равновесие является подвижным. При изменении внешних условий скорости прямой и обратной реакций могут стать неодинаковыми, что обусловливает смещение (сдвиг) равновесия.
Если в результате внешнего воздействия скорость прямой реакции становится больше скорости обратной реакции, то говорят о смещении равновесия вправо
Направление смещения равновесия определяется принципом, который был сформулирован французским ученым Ле-Шателье (1884 г):
Если на равновесную систему оказывается внешнее воздействие, то равновесие смещается в сторону той реакции (прямой или обратной), которая противодействует этому воздействию.
Важнейшими внешними факторами, которые могут приводить к смещению химического равновесия, являются:
а) концентрации реагирующих веществ;
б) температура;
в) давление.
Влияние концентрации реагирующих веществ
Если в равновесную систему вводится какое-либо из участвующих в реакции веществ, то равновесие смещается в сторону той реакции, при протекании которой данное вещество расходуется. Если из равновесной системы выводится какое-либо вещество, то равновесие смещается в сторону той реакции, при протекании которой данное вещество образуется.
Например, рассмотрим, какие вещества следует вводить и какие вещества выводить из равновесной системы для смещения обратимой реакции синтеза аммиака вправо: 
Для смещения равновесия вправо (в сторону прямой реакции образования аммиака) необходимо в равновесную смесь вводить азот и водород (т. е. увеличивать их концентрации) и выводить из равновесной смеси аммиак (т. е. уменьшать его концентрацию).
Влияние температуры
Прямая и обратная реакции имеют противоположные тепловые эффекты: если прямая реакция экзотермическая, то обратная реакция эндотермическая (и наоборот). При нагревании системы (т. е. повышении ее температуры) равновесие смещается в сторону эндотермической реакции; при охлаждении (понижении температуры) равновесие смещается в сторону экзотермической реакции.
Например, реакция синтеза аммиака является экзотермической: N2(г) + 3H2(г) → 2NH3(г) + 92кДж, а реакция разложения аммиака (обратная реакция) является эндотермической: 2NH3(г)→ N2(г) + 3H2(г) — 92кДж. Поэтому повышение температуры смещает равновесие в сторону обратной реакции разложения аммиака.
Влияние давления
Давление влияет на равновесие реакций, в которых принимают участие газообразные вещества. Если внешнее давление повышается, то равновесие смещается в сторону той реакции, при протекании которой число молекул газа уменьшается. И наоборот, равновесие смещается в сторону образования большего числа газообразных молекул при понижении внешнего давления. Если реакция протекает без изменения числа молекул газообразных веществ, то давление не влияет на равновесие в данной системе.
Например, для увеличения выхода аммиака (смещение вправо) необходимо повышать давление в системе обратимой реакции  , так как при протекании прямой реакции число газообразных молекул уменьшается (из четырех молекул газов азота и водорода образуются две молекулы газа аммиака).
, так как при протекании прямой реакции число газообразных молекул уменьшается (из четырех молекул газов азота и водорода образуются две молекулы газа аммиака).
Похожее
Обратимые и необратимые химические реакции
Реакции, идущие до конца и не изменяющие своего направления при изменении температуры и давления, называются необратимыми.
Химические реакции принято считать необратимыми, если:
Один из продуктов реакции выводится из сферы реакции в виде:
А) газа BaCO3 =t= BaO +CO2↑
Б) осадка Pb(NO3)2 + 2NaCl = PbCl2 ↓+ 2NaNO3
В) малодиссоциированного соединения – воды, слабой кислоты или основания, комплексной соли.
KOH +HCl = KCl + H2O
CH
Al(OH)3 NaOH = Na ⌈Al(OH)4⌉
Г) выделяется большое количество тепла, например, реакция горения:
C +О2 = CO2 ΔH = + 393,5 кДж
Однако, большинство химических реакций являются обратимыми: при одних условиях (P, t, kat) они идут в одном направлении, при других – в обратном, а при некоторых промежуточных – протекают одновременно в двух взаимно противоположных направлениях.
Примером обратимых реакций служат реакции термического разложения гидроксида кальция, синтез аммиака:
Ca(OH) ↔ CaO + H2O – Q
N2+3H2 ↔ 2NH3 + Q
Реакцию, идущую слева направо называют прямой, а справа налево – обратной.
Если прямая реакция экзотермическая, то обратная – эндотермическая. Причем, по закону сохранения энергии, количество теплоты, выделившееся в результате прямой реакции, равно количеству теплоты, поглощенному при обратном процессе, а наоборот.
Понятия «обратимая реакция» и «необратимая реакция» относительны: любая обратимая реакция может стать необратимой, если:
- одно из веществ выводить из сферы реакции;
- изменить условия протекания реакции;
С другой стороны, многие реакции, протекающие необратимо, можно сделать обратимыми, изменив условия их протекания.
Автор: Метельский А.В.
Источник: Метельский А.В., Химия в Экзаменационных вопросах и ответах, Минск, изд. «Беларуская энцыклапедыя», 1999 год
Дата в источнике: 1999 год
Классификация реакций, подготовка к ЕГЭ по химии
Существует несколько классификаций реакций, протекающих в неорганической и органической химии.
По характеру процесса
- Соединения
- Разложения
- Замещения
- Обмена
Так называют химические реакции, где из нескольких простых или сложных веществ получается одно сложное вещество. Примеры:
4Na + O2 = 2Na2O
P2O5 + 3H2O = 2H3PO4
В результате реакции разложения сложное вещество распадается на несколько сложных или простых веществ. Примеры:
2KMnO4 = K2MnO4 + MnO2 + 2O2
Сa(OH)2 = CaO + H2O
В ходе реакций замещения атом или группа атомов в молекуле замещаются на другой атом или группу атомов. Примеры:
CuSO4 + Fe = FeSO4 + Cu
2KI + Cl2 = 2KCl + I2
К реакциям обмена относятся те, которые протекают без изменения степеней окисления и выражаются в обмене компонентов между веществами. Часто обмен происходит анионами/катионами:
2KOH + MgCl2 = Mg(OH)2↓ + 2KCl
AgF + NaCl = AgCl↓ + NaF

Окислительно-восстановительные реакции (ОВР)
Это те химические реакции, в процессе которых происходит изменение степеней окисления химических элементов, входящих в состав исходных веществ. ОВР подразделяются на:
- Межмолекулярные — атомы окислителя и восстановителя входят в состав разных молекул. Примеры:
- Внутримолекулярные — атомы окислителя и восстановителя в составе одного сложного вещества. Примеры:
- Диспропорционирование — один и тот же атом является и окислителем, и восстановителем
KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
K2SO3 + K2Cr2O7 + H2SO4 → K2SO4 + Cr2(SO4)3 + H2O
KMnO4 → K2MnO4 + MnO2 + O2
KClO3 → KCl + O2
KOH + Cl2 → (t) KCl + KClO3 + H2O
KOH + Cl2 → KCl + KClO + H2O

Замечу, что окислителем и восстановителем могут являться только исходные вещества (а не продукты!) Окислитель всегда понижает свою СО, принимая электроны в процессе восстановления. Восстановитель всегда повышает свою СО, отдавая электроны в процессе окисления.
От обилия информации можно запутаться. Я рекомендую сформулировать четко: «Окислитель — понижает СО, восстановитель — повышает СО». Запомнив эту информацию таким образом, вы не будете путаться.

ОВР уравнивают методом электронного баланса, с которым мы подробно познакомимся в разделе «Решения задач».
Обратимые и необратимые реакции
Обратимые реакции — такие химические реакции, которые протекают одновременно в двух противоположных направлениях: прямом и обратном. При записи реакции в таких случаях вместо знака «=» ставят знак обратимости «⇆».
Классическим примером обратимой реакции является синтез аммиака и реакция этерификации (из органической химии):
N2 + 3H2 ⇆ 2NH3
CH3COOH + C2H5OH ⇆ CH3COOC2H5 + H2O
Необратимые реакции протекают только в одном направлении, до полного расходования одного из исходных веществ. Главное отличие их от обратимых реакций в том, что образовавшиеся продукты реакции не взаимодействуют между собой с образованием исходных веществ.
Иногда сложно бывает отличить обратимую реакцию от необратимой, однако я дам несколько советов, которые советую взять на вооружение. В результате необратимых реакций:
- Образуются малодиссоциирующие вещества (например — вода, однако есть исключения — реакция этерификации)
- Реакция сопровождается выделение большого количества тепла
- В ходе реакции образуется газ или выпадает осадок
Примеры необратимых реакций:
BaCl2 + H2SO4 = BaSO4↓ + 2HCl (выпадает осадок)
NaOH + HCl = NaCl + H2O (образуется вода)
2Na + 2H2O = 2NaOH + H2 (сопровождается выделением большого количества тепла)
Реакции и агрегатное состояние фаз
Фазой в химии называют часть объема равновесной системы, однородную во всех своих точках по химическому составу и физическим свойствам и отделенную от других частей того же объема поверхностью раздела. Фаза бывает жидкой, твердой и газообразной.
Все реакции можно разделить на гетеро- и гомогенные. Гетерогенные реакции (греч. heterogenes — разнородный) — реакции, протекающие на границе раздела фаз, в неоднородной среде. Скорость таких реакций зависит от площади соприкосновения реагирующих веществ.
К гетерогенным реакциям относятся следующие реакции (примеры): жидкость + газ, газ + твердое вещество, твердое вещество + жидкость. Примером такой реакции может послужить взаимодействие твердого цинка и раствора соляной кислоты:
Zn(тв.) + 2HCl(р-р.) = ZnCl2(р-р.) + H2(газ.)↑
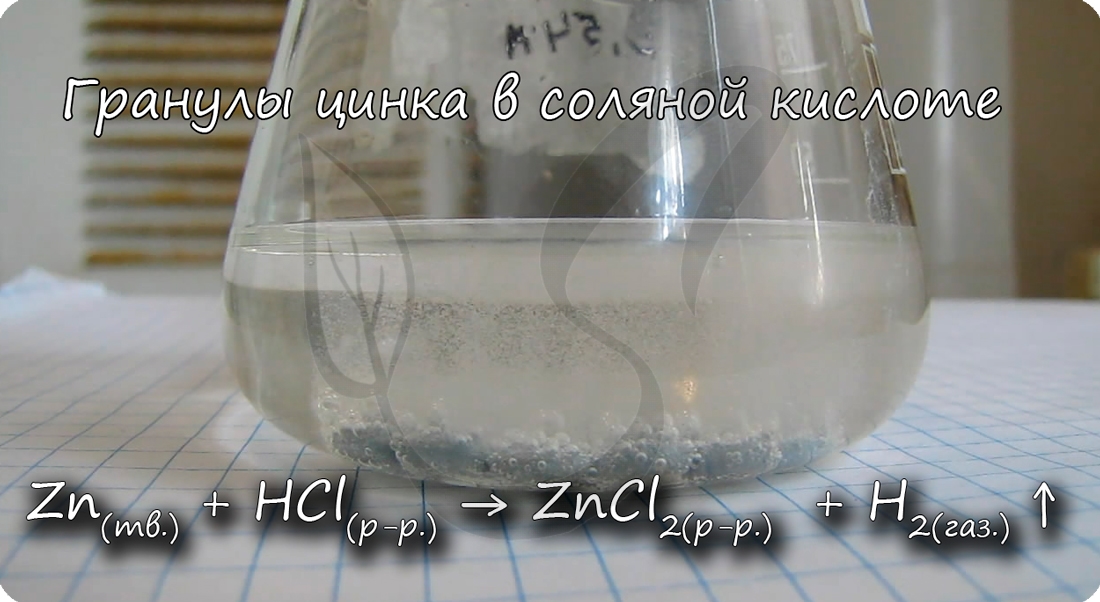
Гомогенные реакции (греч. homogenes — однородный) — реакции, протекающие между веществами, находящимися в одной фазе.
К гомогенным реакциям относятся (примеры): жидкость + жидкость, газ + газ, твердое вещество + твердое вещество. Примером такой реакции может служить взаимодействие между растворами уксусной кислоты и едкого натра.
NaOH(р-р.) + CH3COOH(р-р.) = CH3COONa(р-р.) + H2O(р-р.)

Реакции и их тепловой эффект
Все реакции можно разделить на те, в ходе которых тепло поглощается, или, наоборот, тепло выделяется. Представьте пробирку, охлаждающуюся или нагревающуюся в вашей руке — это и есть тот самый тепловой эффект. Иногда тепла выделяется так много, что реакции сопровождаются воспламенением или взрывом (натрий с водой).
- Экзотермические реакции
- Эндотермические реакции
Экзотермические реакции (греч. exo — вне) — химические реакции, сопровождающиеся потерей энергии системой и выделением тепла (той самой энергии) во внешнюю среду. При написании химических реакций в конце экзотермических ставят «+ Q» (Q — тепло), иногда бывает указано точное количество выделяющегося тепла. Например:
2Mg + O2 = 2MgO + Q
NaOH + HCl = NaCl + H2O + 56 кДж

К экзотермическим реакциям часто относятся реакции горения, соединения. Исключением является взаимодействие азота и кислорода, при котором тепло поглощается:
N2 + O2 ⇄ 2NO — Q
Как уже было отмечено выше, если тепло выделяется во внешнюю среду, значит, система реагирующих веществ потеряло это тепло. Поэтому не должно казаться противоречием, что внутренняя энергия веществ в результате экзотермической реакции уменьшается.
Энтальпией называют (обозначение Н), количество термодинамической (тепловой) энергии, содержащееся в веществе. Иногда с целью «запутывания» в реакции вместо явного +Q при экзотермической реакции могут написать ΔH < 0. Например:
2Na + 2H2O = 2NaOH + H2; ΔH < 0 (это значит, что тепло выделяется — реакция экзотермическая)

Эндотермические реакции (греч. ἔνδον — внутри) — химические реакции, сопровождающиеся поглощением тепла, в результате которых образуются вещества с более высоким энергетическим уровнем (их внутренняя энергия увеличивается).
К таким реакциям наиболее часто относятся реакции разложения. При написании эндотермических реакций в конце ставят «-Q», либо указывают точное количество поглощенной энергии. Примеры таких реакций:
2HgO = Hg + O2 — Q
4NH3 + 5O2 = 4NO + 6H2O — Q
CaCO3 = CaO + CO2↑ — Q
С целью «запутывания» может быть дана энтальпия, она при таких реакциях всегда: ΔH > 0, так как внутренняя энергия веществ увеличивается. Например:
CaCO3 = CaO + CO2↑ ; ΔH > 0 (значит реакция эндотермическая, так как внутренняя энергия увеличивается)

Замечу, что не все реакции разложения являются эндотермическими. Широко известная реакция разложения дихромата аммония («вулканчик») является примером экзотермического разложения, при котором тепло выделяется.

© Беллевич Юрий Сергеевич 2018-2020
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Необратимые и обратимые реакции — HimHelp.ru
Примером/>/> такой/>/> реакции/>/> может/>/> служить/> разложение/>/> хлората/>/> калия/> (бертолетовой/>/> соли/>)/> при/> нагревании: />
2/>KClO 3/> = 2/>KCl + 3/>O 2/> ↑/>
Реакция/> прекратится/>/> тогда/>,/> когда/> весь/>/> хлорат/>/> калия/> превратится в хлорид/> калия/>/> и кислород/>./> Необратимых/> />реакций/>/> не так много. Большинство/>/> реакций/> являются/> обратимыми. />
Обратимыми/> называются/> такие/>/> реакции/>,/> которые одновременно протекают в/> двух/>/> взаимно противоположных/> направлениях/>./>
В/>/> уравнениях/>/> обратимых/> реакций/>/> между/> левой/>/> и/>/> правой/> частями ставят две/> стрелки,/> направленные/> />в/> />противоположные/>/> стороны./> Примером/> такой/> реакции/>/> может/> служить/> синтез/> аммиака/> из/> водорода/> и азота:/>
 ,
,
∆/>H = -46,2 />кДж/> //> моль/>
В/>/> технике/> обратимые/> реакции/>,/> как/> правило,/> невыгодны./> Поэтому различными/>/> методами/> (изменение/> />температуры,/> давления/> и/>/> др.) их делают практически/> необратимыми./>
Необратимыми/> называются/> такие/>/> реакции,/> при/> протекании/> />которых:/>
1) образующиеся/> />продукты/> />уходят/> />из/> />сферы реакции/> – выпадают/> в виде/> осадка,/> выделяются/> в виде/> />газа, например/>
ВаС/>l2 + />Н/> 2/>SО/> 4/> = />Ва/>SО4/>↓ + 2НС/>l
Na 2/>CO 3/> + 2/>HCl = 2/>NaCl + />CO2/> ↓/> + />H2/>O
2) образуется/> />малодиссоциированное соединение/>, например/> вода:/>
НС/>l + />NаОН/> =/> Н2О/> + />NаСl/>
3) реакция/>/> сопровождается/> большим/>/> выделением/> энергии,/> например/>/> горение/> магния/>
Mg/> + 1/2/> О/>2/> = />М/>gО, ∆/>H = -602,5 />кДж/> //> моль/>
В/> />уравнениях/> />необратимых реакций между/>/> левой/>/> и/> правой/>/> частями ставится/>/> знак/> равенства/> или/> стрелка. />
ОБРАТИМЫЕ И НЕОБРАТИМЫЕ РЕАКЦИИ • Большая российская энциклопедия
-

-

-

В книжной версии
Том 23. Москва, 2013, стр. 533
-

Скопировать библиографическую ссылку:
Авторы: Е. Т. Денисов
ОБРАТИ́МЫЕ И НЕОБРАТИ́МЫЕ РЕА́КЦИИ, типы реакций в химич. кинетике. Реакции, протекающие при заданных условиях одновременно как в прямом, так и обратном направлении, называют обратимыми. Обратимые реакции приводят систему в состояние химического равновесия, в котором скорости в двух противоположных направлениях равны. Если скоростью обратного процесса можно пренебречь по сравнению со скоростью прямого процесса, реакцию называют необратимой.
Простейшая обратимая реакция – превращение типа $A⇄Z$. Кинетич. характеристики этого процесса: константы скорости прямой $(k_1)$ и обратной ($k_{–1})$ реакции, энергии активации $(E_1$ и $E_{–1}$) и время релаксации $τ=(k_1+k_{-1})^{-1}$ – время, за которое система приближается к состоянию равновесия в $e$ раз $(e=2,718$ – основание натуральных логарифмов). Кинетика обратимой реакции описывается уравнениями: $[A]=[A]_∞+ ([A]_0- [A]_∞ )e^{–t/τ} \quadи\quad [Z]=[Z]_∞ (1-e^{-t/τ }). Если\quad t=0, [A]=[A]_0$, если же $t→∞ , [A]→ [A]_∞ и [Z]→ [Z]_∞$ , т. е. система стремится к равновесию. Константа равновесия K=k1/k-1= [Z]∞ /[A]∞ . Состояние равновесия характеризуется следующими термодинамич. величинами: энтальпией равновесия $ΔH$, энтропией равновесия $ΔS$ и энергией Гиббса $ΔG=ΔH-TΔS$. Константа равновесия $K$ связана с энергией Гиббса соотношением: $ΔG=–RTlnK$. Напр., реакция образования иодоводорода $H_2+I_2⇄2HI$ характеризуется следующими значениями: $ΔH=–9,4$ кДж/моль, $ΔS= 260,7$ Дж/(моль·К), $ΔG(298 К)=–64,3$ кДж/моль. К обратимым реакциям типа $A⇄Z $ относятся: цис-транс-изомеризация олефинов, напр. цис-$CH_3CH═CHCH_3$⇄ ⇄транс-$CH_3CH═ CHCH_3$; енолизация кетонов, напр. $CH_3C(O)CH_2COOC_2H_5⇄CH_3C(OH)═CHCOOC_2H_5$; изомеризация свободных радикалов, напр. $CH_3C^•H(CH_2)_3CH(CH_3)_2⇄ CH_3CH_2(CH_2)_3C^•(CH_3)_2$; изомеризация ионов, напр. $CH_3CHNH_2COOH⇄ CH_3CHN^+H_3COO^-$. Примерами обратимых реакций типа $A+B⇄Y+Z$ служат диссоциация карбоновых кислот $(C_2H_5COOH+ H_2O⇄ C_2H_5COO^–+H_3O^+)$ и катализируемая кислотами этерификация $(CH_3COOH+ C_2H_5OH⇄ CH_3COOC_2H_5+H_2O)$.
К необратимым относятся реакции, в результате которых образуются стабильные конечные продукты. Кинетика необратимой реакции $А→Z$ описывается уравнениями: $[A]=[A]_0e^{–kt}, [Z]=[A]_0(1-e^{–kt}).$ Если $t→∞, [A]→0$ (не к конечному значению, как для обратимой реакции) и $[Z]→ [A]_0$. Необратимые реакции со стабильным конечным продуктом можно рассматривать как обратимые с $K≫ 1 и ΔG< –200$ кДж/моль, поскольку $K⩾ exp(200000/RT)$. Следует иметь в виду, что $K$ зависит от темп-ры и может уменьшаться с её ростом. Напр., реакция образования бромоводорода $H_2+Br_2⇄2HBr$ характеризуется следующими значениями: $ΔH=-130,5$ кДж/моль и $ΔS=21,2$ Дж/(моль·К), $K=8·10^{16}$ при $300 К$ (реакция практически необратима) и $K=2·10^4$ при $1000 К$ (реакцию можно рассматривать как обратимую). Реакции, в которых продукты превращения вступают в последующие быстрые реакции, в силу чего равновесие становится невозможным, также относятся к необратимым.
Необратимые реакции — Энциклопедия по машиностроению XXL
Реакции бывают обратимыми и необратимыми. Необратимая реакция протекает только в одном направлении, обратимая — как в одном, так и в противоположном направлениях. [c.54]Таким образом, вместо системы двух уравнений второго порядка достаточно решить одно уравнение сохранения энергии, которое для необратимой реакции первого порядка, следующей закону Аррениуса, имеет вид [c.353]
В случае недостаточного подвода сульфат-ионов в реакционную зону (например, при наличии большого отрицательного заряда поверхности электрода или низкой концентрации этих ионов) наряду с необратимой реакцией (149) или вместо нее может протекать другая необратимая реакция, например [901 [c.112]
Два закона термодинамики означают существование двух функций состояния рассматриваемой системы ее внутренней энергии и энтропии. Исходя из свойств некомпенсированной теплоты, я в 1922 г. установил существование еще одной функции состояния, связанной с физикохимическими изменениями, а именно сродства А. Чтобы получить этот результат, я ввожу понятие координаты химической реакции проходящей в закрытой системе, а также необходимые и достаточные условия, чтобы функция А оставалась постоянной, если меняется тип превращения. Этот метод дает возможность непосредственно использовать классические теоремы термодинамики для необратимых реакций в системе и выявляет роль, которую играет скорость реакции d ldt. [c.14]
До сих пор мы рассматривали необратимые реакции. Введем в 1 хшу (2.53) обратные реакции [c.56]
ОДНОЙ НЕОБРАТИМОЙ РЕАКЦИИ [c.314]
Рассмотрим тепловое взаимодействие потока с однородным телом, на поверхности которого протекает одна необратимая реакция типа [c.314]
V. Тепло выделяется в результате необратимой реакции первого порядка. В этом случае, допуская, что скорость реакции не зависит от температуры, можно считать, что количество тепла, выделяющегося в единицу времени, равно КАС, где А — постоянная, а С — концентрация диффундирующего вещества. Последняя определяется дифференциальным уравнением [c.400]
Недостижимость абсолютного нуля температуры 7, 90 Неидеальные растворы 192 Ненасыщенный пар 173 Необратимое смешение 128 Необратимые реакции 189 [c.334]
Реакция может быть химически обратимой, если она идет как в прямом, так и в обратном направлении. При горении топлива скорость прямого процесса несоизмеримо больше скорости обратного процесса, поэтому горение топлива практически сопровождается химически необратимыми реакциями. [c.98]
Если отказаться от условий (2.3), то появится также остаточная компонента деформаций и уравнениями (2.2) можно будет описывать также необратимую реакцию (ползучесть). [c.371]
Реакции образования окислов азота из элементов в диапазоне 298—2000° К в действительности являются необратимыми реакциями диссоциации окислов на элементы. [c.298]
Температура равновесия необратимых реакций [c.360]
Понятие о необратимых реакциях весьма, условно. С термодинамических позиций следует признать, что необратимых реакций нет. Есть реакции, равновесие которых сильно сдвинуто в сторону необычно высоких (или, наоборот, низких) температур или давлений. [c.360]
Наиболее простым для изучения объектом является скорость гомогенных необратимых реакций, так как в этом случае все молекулы реагирующих веществ находятся в одинаковых условиях (одна фаза) и реакция может развиваться только в одном направлении. Поэтому обычно стараются свести решение задачи к этому случаю, так как иначе получаются уравнения скорости, решаемые в отдельных частных случаях. [c.235]
НЕОБРАТИМЫЕ РЕАКЦИИ — химические процессы, протекающие практически до полного превращения исходных веществ в конечные продукты реакции (ср. Обратимые реакции). [c.89]
ОБРАТИМЫЕ РЕАКЦИИ — химические превращения, в которых продукты взаимодействия исходных веществ (прямая реакция), реагируя друг с другом, снова образуют исходные вещества (обратная реакция). В результате система приходит в состояние химического равновесия, характеризующегося равенством скоростей прямой и обратной реакций. При этом концентрации участвующих в обратимой реакции веществ нри неизменных условиях остаются постоянными сколь угодно долгое время. Теоретически все химические реакции являются обратимыми, однако во многих случаях скорость обратного процесса весьма мала и в целом реакция практически необратима (см. Необратимые реакции). [c.92]
Если же учесть необратимые химические реакции, возникающие в образцах из СиО с цинковыми электродами в процессе термообработки, и реакции, возникающие в полупроводящем веществе и у электродов этих термисторов в рабочих условиях, то экспериментальному значению энергии активации можно дать теоретическое объяснение. Действительно, согласно данным Менделеева [4], цинк при нагреве легко окисляется и обладает способностью восстанавливать медь, окисел цинка плавится при 1975° без разложения. Следовательно, в процессе отжига образцов из СиО с цинковыми электродами у их контактов возникают необратимые реакции [c.217]
За осно ву действия кислородомера МЭИ принята необратимая реакция взаимодействия растворенного в воде кислорода с вводимой извне окисью азота, в результате чего происходит изменение электропроводности раствора. Окись азота быстро и полно взаимодействует с растворенным в воде кислородом с образованием азотистой кислоты и не вступает в реакцию с водой и ее (примесями. В результате реакции электропроводность раствора увеличивается пропорциональ- [c.160]
Что касается термокинетических колебаний при горемйй угольных частиц, то они были замечены в экспериментах Б. Д. Кацнельсона при горении угольных частиц, падающих в атмосфере, содержащей окислитель. Количественное сравнение экспериментальных и теоретических данных не представляется возможным, однако отмеченные Кацнельсо-ном термокпнетические колебания можно объяснить тем, что характерные времена гомогенных и гетерогенных экзотермических Необратимых реакций значительно меньше характерного аэродинамического времени, которое по порядку величин совпадает с временем тепловой релаксации в пограничном слое (см. 5.4 и 7.8). [c.423]
В ЭТО сложное уравнение объединены четыре самостоятельные реакции, тесно связанные одна с другой. Реакция (1) представляет собой термический распад ионов бикарбоната и ею определяется образование накипи. До осаждения кристалла накипи СаСОз или Mg(OH)o должен произойти термический распад двух ионов бикарбоната. В условиях работы испарителя морской воды — это необратимая реакция, так как освобождающийся СО2 уходит вместе с паром. Скорость термического распада возрастает с повышением температуры. Протекание реакции (2) зависит от произведения растворимости СаСОз и для его осаждения в накипь эта величина должна быть превышена, т. е. [Са++]х[СОз—] должно быть больше произведения растворимости. Точно так же протекание реакции (3) зависит от произведения растворимости Mg (ОН) 2, а произведение [Mg++]X Х[0Н ]2 должно быть больше произведения растворимости Mg (ОН) 2 в концентрированном рассоле до начала осаждения. [c.81]
S-состояниях термодинамического равновесия Ч Для необратимой реакции это означает, что если в G- или 5-состояниях Шок имеет конечную величину, то т оп здесь должно быть равно нулю и, наоборот, для конечных значений Штоп должно быть /тгок= 0. Рассмотрим только несколько вероятных следствий этого допущения. [c.77]
Вязкое тело относится к системам с последействием (с нулевой мгновенной реакцией) и с полной необратимой реакцией в этом случае в уравнениях (1.1) Aijmn = ij = 0. При этом естественно считать Вц обычными функциями ац, Zij и Т. В простейшем случае, когда В,, представляют собой линейные функции Oij, получается классическая модель вязкой жидкости. [c.13]
В слое, образованном в системе Ре—Рез04—РегОз — электролит протекает необратимая реакция Ре-1-4Ре20зЗРез04. Принимается, что скорость коррозии лимитируется при этом скоростью растворения Рез04 [295]. [c.105]
Вязкое тело относится к системам с последействием (с нулевой мгновенной реакцией) и с необратимой реакцией при этом в уравнениях (2.1) Aijmn — ij = 0. При ЭТОМ естественно считать B j обычными функциями uij, ij и Г. В простейшем случае, когда Bij представляют собой линейные функции Gij, получается классическая модель вязкой жидкости. [c.370]
Онсагер (Onaager) Ларе (1903-1976) — американский физик и химик, один из создателей термодинамики неравновесных процессов. Окончил Норвежскую высшую техническую школу (1925 г.), с 1928 г. жил в США работал в Йельском университете и университете в Майами. Установил в 1931 г. одну из основных теорем термодинамики неравновесных процессов и свойство симметрии кинетических коэффициентов (теорема Онсаге ра), разработал теорию термодинамических свойств плоской решетки (теория Онсагера), открыл необратимую реакцию (реакция Онсагера) в термодинамике необратимых ироцессов (Нобелевская премия по химии, 1968 г.). [c.286]
Высокое абсолютное значение константы равновесия говорит о практической необратимости реакции, а положительный знак для lgKp свидетельствует о самопроизвольном течении процесса в сторону образования паров воды до получения исчезающе малых парциальных давлений водорода и кислорода. [c.360]
КИНЕТИКА ХИМИЧЕСКАЯ, отрасль тео-ретич. химии, изучающая скорости химич. реакций. В основе опытной методики этого изучения лежит определение концентрации прореагировавшего либо появляющегося вещества в функциональной зависимости от времени. Различают кинетику о б-ратимых и необратимых реакций. К необратимым относятся те реакции, к-рые практически протекают лишь в одном направлении это имеет место в случаях, когда продукты, к-рые образовались в результате химич. процесса, удаляются из сферы реак -ции и тем самым лишаются возможности обратного взаимодействия или когда обратная реакция протекает лишь с незначительной скоростью. В случае обратимых реакций продукты вступают между собой во взаимодействие, давая исходные вещества прн [c.85]
Вернемся теперь к ядру релаксации, основанному на анализе кинетики процесса взаимодействия релаксаторов и перехода их в нерелаксирующий материал. Ядро (270) получено при условии, что процесс взаимодействия релаксаторов представляет собой односторонгоою необратимую реакцию и-го порядка, т.е, считается, что провзаимодействующие релаксаторы переходят в [c.301]
Рассмотренная здесь необратимая реакция сплошной среды полностью описывается уравнениями (6.84) и (6.80). Эти определяющие уравнения были установлены Гогенем-зером и Прагером [16] (см. также Прагер [27], стр. 138). Для их обращения будем исходить из (6.80) и вычислим инвариант [c.114]
Дополнительным важным свойством рассматриваемой модели является влияние обратной реакции на интерпретацию измеряемых времен затухания и т . Если реакция обратима, времена затухания зависят от четырех кинетических констант — Гр, и 8 противоположность этому в случае необратимой реакции ( 2 = 0) из уравнения (12.14) находим т = и = Гр + Для = О измеренные значения времен затухания представляют собой собственное время жизни состояния, образовавшегося в результате реакции (т ), и время жизни первоначально возбужденного состояния (Тр). На затухание флуоресценции из состояния Р обратимость реакции также оказывает влияние. Когда к 4 О, затухание флуоресценции из состояния Р двухэкспоиенциально [уравнение (12.12)]. Однако, когда к — О, из уравнения (12.14) находим, что а из уравнения (12.15) а (у) = О, В отсутствие обратной реакции затухание флуоресценции из состояпия Р становится одноэкспоненциальным. [c.396]
Диссоциация 2-нафтола в возбужденном состоянии — поучительный пример обратимой реокции с участием двух состояний. При возбуждении нафтола уменьшается от 9,2 в основном состоянии до 2,0 в возбужденном состоянии [3]. В кислом растворе наблюдается испускание нафтола с максимумом 357 пм (рис. 12.3, кривая V), а в щелочном — испускание нафтолят-аниопа, центр которого находится при 409 нм (кривая 2). При промежуточных значениях рИ испускают оба вида частиц. Из рассмотрения спектров видно, что при 350 нм испускание обусловлено только нафтолом, что как раз и требуется для использования процедуры обратной свертки при различных длинах воли. Реакция диссоциации нафтола в зависимости от pH может быть либо обратимой, либо необратимой. При значениях pH, близких к 3, реакция обратима, а при рИ > 6 необратима [ 15]. Следовательно, эта система пригодна для демонстрации характеристик как обратимых, так и необратимых реакций. [c.400]
Необратимые реакции — это… Что такое Необратимые реакции?
- Необратимые реакции
Большая советская энциклопедия. — М.: Советская энциклопедия. 1969—1978.
- Необратимые процессы
- Необходимая оборона
Смотреть что такое «Необратимые реакции» в других словарях:
Необратимые реакции — реакции, при которых взятые вещества нацело превращаются в продукты реакции, не реагирующие между собой при данных условиях, например, разложение взрывчатых веществ, горение углеводородов, образование малодиссоциирующих соединений, выпадение… … Википедия
НЕОБРАТИМЫЕ РЕАКЦИИ — см. Обратимые реакции … Большой Энциклопедический словарь
необратимые реакции — – химические реакции, протекающие только в прямом направлении с образованием продуктов, не взаимодействующих между собой. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
необратимые реакции — см. Обратимые реакции. * * * НЕОБРАТИМЫЕ РЕАКЦИИ НЕОБРАТИМЫЕ РЕАКЦИИ, см. Обратимые реакции (см. ОБРАТИМЫЕ РЕАКЦИИ) … Энциклопедический словарь
НЕОБРАТИМЫЕ РЕАКЦИИ — см. Обратимые и необратимые процессы … Химическая энциклопедия
НЕОБРАТИМЫЕ РЕАКЦИИ — см. Обратимые реакции … Естествознание. Энциклопедический словарь
Необратимые реакции — химические процессы, протекающие в одном направлении до полного расходования исходных веществ (например, горение топлива, как наиболее универсальный самоорганизующийся процесс) … Начала современного естествознания
Обратимые и необратимые реакции — типы реакций химических (См. Реакции химические). Реакцию называют обратимой, если её направление зависит от концентраций веществ участников реакции. Например, в случае гетерогенно каталитической реакции N2 + 3h3 = 2Nh4 (1)… … Большая советская энциклопедия
Реакции химические — превращения одних веществ в другие, отличные от исходных по химическому составу или строению. Общее число атомов каждого данного элемента, а также сами химические элементы, составляющие вещества, остаются в Р. х. неизмененными; этим Р. х … Большая советская энциклопедия
Необратимые процессы — изменения состояния термодинамической системы, которые самопроизвольно (независимо от внешнего воздействия, из за внутренних причин) всегда протекают только в одном направлении; к ним относятся выравнивание температур, давлений, плотностей,… … Начала современного естествознания
Обратимые и необратимые реакции — Chemistry LibreTexts
Обратимые и необратимые реакции распространены по природе и ответственны за такие реакции, как разложение аммиака.
Введение
Считалось, что все химические реакции являются необратимыми до 1803 года, когда французский химик Клод Луи Бертолле представил концепцию обратимых реакций. Первоначально он заметил, что карбонат натрия и хлорид кальция реагируют с образованием карбоната кальция и хлорида натрия; однако, наблюдая за образованием карбоната натрия по краям соляных озер, он понял, что большое количество солей в испаряющейся воде реагирует с карбонатом кальция с образованием карбоната натрия, что указывает на то, что имеет место обратная реакция.
Химические реакции представлены химическими уравнениями. Эти уравнения обычно имеют однонаправленную стрелку (\ (\ rightarrow \)) для обозначения необратимых реакций. Другие химические уравнения могут иметь двунаправленные гарпуны (\ (\ rightleftharpoons \)), которые представляют обратимые реакции (не путать с двойными стрелками \ (\ leftrightarrow \), используемыми для обозначения резонансных структур). Чтобы ознакомиться с основами химических реакций, щелкните здесь: Химические реакции
Необратимые реакции
Фундаментальная концепция химии заключается в том, что химические реакции происходят, когда реагенты взаимодействуют друг с другом с образованием продуктов.Эти однонаправленные реакции известны как необратимые реакции, реакции, в которых реагенты превращаются в продукты, а продукты не могут, превращаться обратно в реагенты. Эти реакции по сути похожи на выпечку. Ингредиенты, действующие как реагенты, смешиваются и выпекаются вместе, образуя пирог, который действует как продукт. Этот осадок нельзя превратить обратно в реагенты (яйца, муку и т. Д.), Так же как продукты необратимой реакции не могут снова превратиться в реагенты.
Пример необратимой реакции — горение. Горение включает сжигание органического соединения, такого как углеводород, и кислорода с образованием диоксида углерода и воды. Поскольку вода и диоксид углерода стабильны, они не вступают в реакцию друг с другом с образованием реагентов. Реакции горения имеют следующий вид:
\ [C_xH_y + O_2 \ rightarrow CO_2 + H_2O \]
Обратимые реакции
В обратимых реакциях реагенты и продукты никогда не расходуются полностью; каждый из них постоянно реагирует и производится.Обратимая реакция может иметь следующий обобщенный вид:
\ [A + B \ underset {k _ {- 1}} {\ overset {k_1} {\ rightleftharpoons}} C + D \]
Эту обратимую реакцию можно разделить на две реакции.
Реакция 1: \ [A + B \ xrightarrow {k_1} C + D \]
Реакция 2: \ [C + D \ xrightarrow {k _ {- 1}} A + B \]
Эти две реакции происходят одновременно , это означает, что реагенты реагируют с образованием продуктов, так как продукты реагируют с образованием реагентов.Столкновения реагирующих молекул вызывают химические реакции в замкнутой системе. После образования продуктов связи между этими продуктами разрываются, когда молекулы сталкиваются друг с другом, производя достаточную энергию, необходимую для разрыва связей продукта и молекул реагента.
Ниже приведен пример обобщенной формы обратимой реакции и разрыва обратимой реакции N 2 O 4 ↔ 2NO 2
Реакция 1 и Реакция 2 происходят одновременно, потому что они находятся в закрытой системе.
Синий: азот Красный: кислород
Реакция 1 Реакция 2
Представьте себе бальный зал. Пусть реагентом A будет 10 девочек, а реагентом B — 10 мальчиков. Когда каждая девочка и мальчик выходят на танцпол, они объединяются в пары, чтобы стать продуктом. Когда пять девочек и пять мальчиков выходят на танцпол, одна из пяти пар распадается и уходит в сторону, снова становясь реагентами.Когда эта пара покидает танцпол, еще один мальчик и девочка в сторонке объединяются, чтобы снова сформировать продукт. Этот процесс продолжается снова и снова, представляя обратимую реакцию.
В отличие от необратимых реакций, обратимые реакции приводят к равновесию: в обратимых реакциях реакция протекает в обоих направлениях, тогда как в необратимых реакциях реакция протекает только в одном направлении. Чтобы узнать больше об этом явлении, щелкните здесь: Химическое равновесие
Если реагенты образуются с той же скоростью, что и продукты, существует динамическое равновесие.Например, если резервуар для воды наполняется водой с такой же скоростью, как вода выходит из резервуара (через гипотетическое отверстие), количество воды, остающейся в резервуаре, остается постоянным.
Связь с биологией
Белок гемоглобина имеет четыре сайта связывания. Молекулы гемоглобина могут связываться с углекислым газом или кислородом. Когда кровь проходит через альвеолы легких, молекулы гемоглобина улавливают богатые кислородом молекулы и связываются с кислородом. По мере того, как гемоглобин проходит через остальную часть тела, он отдает кислород в капиллярах, чтобы система органов могла использовать кислород.Удалив кислород, он улавливает углекислый газ. Поскольку этот процесс постоянно происходит в организме, всегда есть молекулы гемоглобина, улавливающие или вытесняющие кислород, и другие молекулы гемоглобина, которые захватывают или вытесняют диоксид углерода. Таким образом, молекулы гемоглобина, кислорода и углекислого газа являются реагентами, а молекулы гемоглобина со связанными с ними кислородом или углекислым газом являются продуктами. В этой замкнутой системе некоторые реагенты превращаются в продукты, поскольку некоторые продукты превращаются в реагенты, что делает эту реакцию похожей на обратимую реакцию.
Авторы и авторство
- Хизер Йи (UCD), Мандип Сохал (UCD)
Обратимые и необратимые реакции — Chemistry LibreTexts
- Последнее обновление
- Сохранить как PDF
- Авторы и авторство
Обычно наблюдается, что большинство реакций, проводимых в закрытых сосудах, не завершаются при заданном наборе условий температуры и давления.Фактически во всех таких случаях в исходном состоянии присутствуют только реагенты, но по мере протекания реакции концентрация реагентов уменьшается, а концентрация продуктов увеличивается. Наконец, достигается стадия, когда не наблюдается дальнейшего изменения концентрации реагентов и продуктов.
| Пример 1 |
|---|
Если смесь газообразного водорода и паров йода заставить реагировать при 717 К в закрытом сосуде в течение примерно 2–3 часов, газообразный йодистый водород образуется в соответствии со следующим уравнением: \ [H_ {2 \; (g)} + I_ {2 \; (g)} \ rightarrow 2HI _ {(g)} \] Но вместе с газообразным йодистым водородом останется некоторое количество непрореагировавшего газообразного водорода и газообразного йода.С другой стороны, если газообразный йодистый водород выдерживается при температуре 717 К в закрытом сосуде в течение примерно 2–3 часов, он разлагается с образованием газообразного водорода и газообразного йода. \ [2HI _ {(g)} \ rightarrow H_ {2 \; (g)} + I_ {2 \; (g)} \] В этом случае также останется непрореагировавшее количество газообразного иодистого водорода. Это означает, что продукты определенных реакций можно превратить обратно в реагенты. Эти типы реакций называются обратимыми реакциями . Таким образом, в обратимых реакциях продукты могут реагировать друг с другом в подходящих условиях с возвращением реагентов.Другими словами, в обратимых реакциях реакция протекает как в прямом, так и в обратном направлении. Обратимая реакция может быть выражена как: \ [H_ {2 \; (g)} + I_ {2 \; (g)} \ rightleftharpoons 2HI _ {(g)} \] Эти обратимые реакции никогда не завершаются, если они проводятся в закрытом контейнере. Для обратимой химической реакции состояние равновесия достигается, когда скорость, с которой протекает химическая реакция в прямом направлении, равна скорости, с которой протекает обратная реакция. |

Leave A Comment