Фотосинтезирующие цианобактерии выжили в темноте глубоко под землей
Ученые нашли цианобактерии в образцах породы из 613-метровой скважины. На такой глубине нет солнечного света, необходимого, как считалось ранее, цианобактериям для фотосинтеза. Исследователи предположили, что эти цианобактерии используют хемолитоавтотрофный тип питания. Исследование опубликовано в Proceedings of the National Academy of Sciences.
Цианобактерии, которых раньше относили к растениям под названием сине-зеленые водоросли, встречаются во всех местообитаниях на планете — в пресной и соленой воде, в почве, в составе лишайников, а также могут образовывать бактериальные маты. Они наиболее близки к древнейшим микроорганизмам, останки которых были обнаружены на Земле, цианобактерии первыми изобрели кислородный фотосинтез, и считается что цианобактериям обязательно нужен солнечный свет для фотосинтеза.
Фернандо Пуэнте-Санчес (Fernando Puente-Sánchez) из Астробиологического Центра в Мадриде и его коллеги из Испании, Германии и США собрали образцы породы из 613-метровой континентальной скважине в Иберийском пиритовом поясе, крупнейшем месторождении сульфидов, в Испании. Геохимические условия в этой скважине напоминают условия под поверхностью Марса, а также, возможно, и Европы, спутника Юпитера.
Геохимические условия в этой скважине напоминают условия под поверхностью Марса, а также, возможно, и Европы, спутника Юпитера.
Используя микроскопию, амплификацию 16s РНК и иммуноферментный анализ исследователи проанализировали состав и численность жизнеспособных микроорганизмов в образцах пород. В образцах преобладали цианобактерии, в основном представители родов Calothrix, Chroococcidiopsis и Microcoleus, встречающиеся под камнями и в камнях. При этом в найденных цианобактериях не было активных пигментов фотосинтеза.
Содержание водорода отрицательно коррелировало с обилием цианобактерий, а в метагеномных данных присутствовали свидетельства метаболических путей использования водорода, в том числе два вида гидрогеназ — ферментов, участвующих в окислительно-восстановительных реакциях. Исходя из этого авторы предположили, что цианобактерии используют водород в качестве донора электронов и, потенциально, железо, марганец, оксид азота или другие продукты органического вещества в качестве акцепторов электронов. Подземные цианобактерии получают энергию из окислительно-восстановительных реакций, то есть являются хемоавтотрофами.
Подземные цианобактерии получают энергию из окислительно-восстановительных реакций, то есть являются хемоавтотрофами.
Ранее в другом исследовании цианобактерии были найдены под поверхностью земли, но в водоносном слое. Авторы предположили, что бактерии попали туда вместе с водой с поверхности и смогли выжить. По мнению авторов новой статьи, здесь мы имеем дело именно с бактериями, живущими в толще породы, эти цианобактерии могут служить важными первичными продуцентами глубоко под землей. Возможно, так жили предки цианобактерий, еще не способные к фотосинтезу. Полученные данные свидетельствуют о необходимости переоценки возможных условий жизни цианобактерий. Как на Земле, так и на других планетах существуют сходные условия, в которых теоретически цианобактерии могли выжить.
У цианобактерий серьезная роль в истории жизни на Земле. Самой древней окаменелостью считается строматолит возрастом примерно 3,7 миллиарда лет, подобный цианобактериальным строматолитам. Цианобактерии, которые первыми изобрели оксигенный фотосинтез, стали причиной обогащения всей атмосферы Земли кислородом, благодаря которому появилось аэробное дыхание. За время своего долгого существования на Земле разные классы цианобактерии трижды независимо изобретали кислородное дыхание.
За время своего долгого существования на Земле разные классы цианобактерии трижды независимо изобретали кислородное дыхание.
Александра Кочеткова
Нашли опечатку? Выделите фрагмент и нажмите Ctrl+Enter.
Фотосинтез и возможности его использования в альтернативной энергетике
###1###Фотосинтез — эволюционный прорыв древней Земли
Более трех миллиардов лет назад живущие на земле организмы приобрели способность эффективно захватывать солнечную энергию и использовать ее для синтеза органических молекул путем фотосинтеза.
Процесс фотосинтеза привел к беспрецедентному взрыву биологической активности на Земле, позволив жизни процветать и изменяться огромными шагами,
о чем свидетельствуют ископаемые останки животных и растительных организмов, сохранившиеся в земной коре с прежних геологических эпох, а также количество и разнообразие живущих организмов на нашей планете сегодня. Энергия солнца — это единственный имеющийся в избытке источник возобновляемой энергии, и фотосинтетический аппарат использует эту энергию для осуществления термодинамически и химически затратной реакции расщепления воды.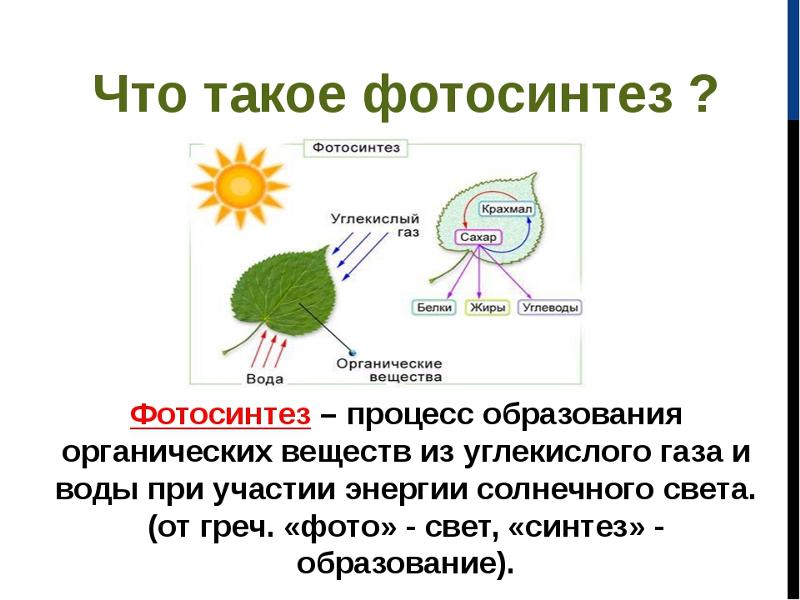 Осуществляя этот процесс, фотосинтез снабжает биологию неограниченными поставками водорода (электронов и протонов), необходимого для того, чтобы превратить двуокись углерода в органические молекулы жизни.
Осуществляя этот процесс, фотосинтез снабжает биологию неограниченными поставками водорода (электронов и протонов), необходимого для того, чтобы превратить двуокись углерода в органические молекулы жизни.
До эволюции фотосинтеза биология зависела от доноров водорода/электронов, то есть веществ-восстановителей, таких как сероводород H2S или аммиак NH3, которые присутствовали на Земле в гораздо более ограниченном количестве по сравнению с океанами воды.
Накопление выделяемого кислорода привело к возникновению аэробной атмосферы. Образование озонового слоя позволило организмам выйти из океанов на сушу. С появлением кислорода эффективность метаболизма увеличилась, поскольку аэробное дыхание дает почти в 20 раз больше клеточной энергии, чем анаэробное. Эта улучшенная эффективность в превращении энергии была, очевидно, основным фактором, ответственным за последующую эволюцию эукариотических клеток в многоклеточных организмах. Поэтому можно утверждать, что
одним из наиболее значимых событий в истории Земли была эволюция фотосинтезирующих организмов, способных окислять воду.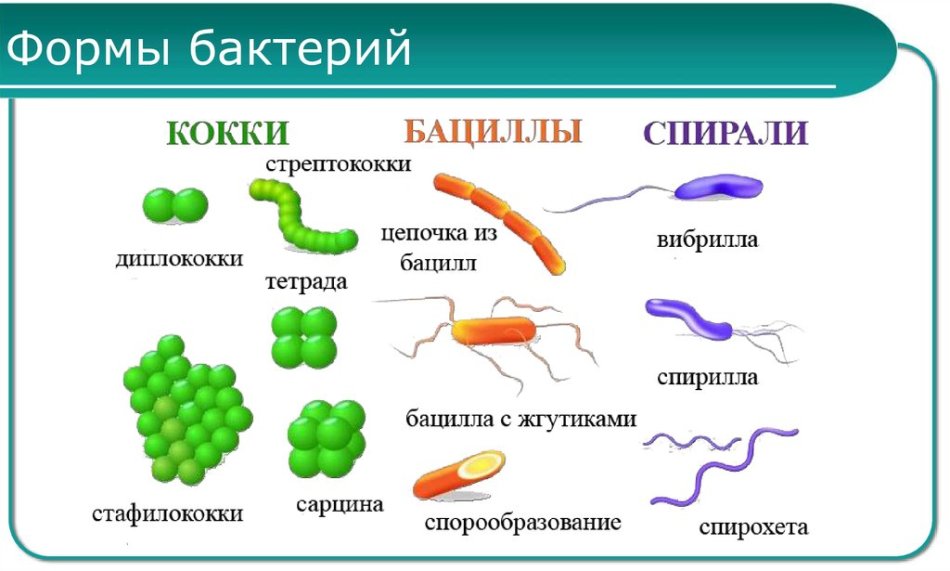
Фотосинтез может быть либо оксигенным (O2 продуцирующим), либо аноксигенным. Оксигенные организмы используют энергию солнца, чтобы отрывать электроны и протоны от воды, главным образом, для цикла ассимиляции СО2, и продуцируют О2 в качестве побочного продукта. Аноксигенные организмы не обладают редокс потенциалом, необходимым для того, чтобы окислить Н2О, и потому вынуждены брать электроны от других электрон-донорных субстратов, таких как H2S или органические кислоты. Оксигенный фотосинтез имеет место в высших растениях, водорослях и цианобактериях, тогда как аноксигенный фотосинтез происходит в организмах, таких как зеленые серные и пурпурные несерные бактерии.
Благодаря фотосинтезу энергия солнца захватывается и накапливается в форме биотоплива, такого как уголь, нефть и газ. Однако эти виды топлива, даваемые фотосинтезирующими организмами, интенсивно используются и становятся ограниченными. Из всего объема потребленной энергии на Земле в 2005 году 86% было получено из ископаемых видов топлива. Кроме того, глобальное потребление энергии будет увеличиваться от настоящего уровня до 12.8-27 ТВт к 2050 году. Это приведет к дальнейшему глобальному потеплению на нашей планете, поскольку повышаются уровни двуокиси углерода и других парниковых газов в атмосфере Земли.
Кроме того, глобальное потребление энергии будет увеличиваться от настоящего уровня до 12.8-27 ТВт к 2050 году. Это приведет к дальнейшему глобальному потеплению на нашей планете, поскольку повышаются уровни двуокиси углерода и других парниковых газов в атмосфере Земли.
За последние 50 лет концентрация двуокиси углерода в атмосфере увеличилась более чем на 18%, а температура поверхности Земли увеличилась на 0,64 градуса.
Все еще не решен вопрос о том, насколько индустриальная активность человечества ответственна за эти глобальные изменения нашего климата,
так как эти изменения могут вызвать множество факторов. Тем не менее причина, за которую активность человечества, безусловно, ответственна, — это разработка только тех промышленных процессов, которые приводят к выделению двуокиси углерода, и ни одного из тех, которые бы были сопряжены с ее ассимиляцией. И это является существенной проблемой, потому что мы нарушаем равновесие в круговороте углерода, поглощая унаследованные нами источники углерода без какой-либо надежды на их возобновление. Поэтому очень важно в самом ближайшем будущем разработать источники возобновляемой, чистой энергии. В этом отношении
Поэтому очень важно в самом ближайшем будущем разработать источники возобновляемой, чистой энергии. В этом отношении
фотосинтез представляет собой успешный пример того, как энергия солнца может превращаться в топливо,
когда электроны отнимаются от воды, используя свет в качестве единственного источника энергии. Было бы разумно более детально изучить фотосинтез, потому что процессы фотосинтеза содержат много загадок, разгадав которые, человечество могло бы многому научиться.+++
###2###Водородное топливо
Экономика и транспортная структура, основанные на молекулярном водороде и «топливе клеток», могли бы уменьшить нашу зависимость от нефти, а также последствия загрязнения окружающей среды. Такой подход также положительно повлиял бы на энергетическую безопасность, одновременно уменьшая загрязнения воздуха и изменения глобального климата. Биологическое производство водорода с помощью фотосинтеза может однажды дать ценную альтернативу химическим и электрохимическим технологиям. Во-первых,
Во-первых,
энергия Солнца и вода — чистые и возобновляемые источники энергии.
Во-вторых, сжигание Н2 — экологически чистый, дающий воду в качестве конечного продукта сгорания и возобновляемый процесс. Фотосинтез лежит в основе производства водорода всеми биологическими методами за счет энергии солнца в зеленых водорослях, цианобактериях и высших растениях.
Некоторые из аноксигенных организмов способны генерировать водород довольно эффективно. Однако, поскольку они не могут получать электроны от воды, экономически невыгодно использовать их для фотопроизводства водорода в промышленных масштабах. Все оксигенные фототрофы отнимают электроны и протоны от воды и затем восстанавливают пластохинон и вещество NADP+ (никотинамидадениндинуклеотидфосфат), которое используется в качестве источника энергии для метаболизма клетки. В этом случае оксигенные фототрофы, включая цианобактерии и микроводоросли, могут кратковременно производить Н2 в анаэробных условиях путем восстановления протонов.
Этот процесс катализируется ключевым ферментом гидрогеназой (или нирогеназой) и конкурирует с другими внутриклеточными процессами. В случае оксигенных фототрофов электроны и протоны, произведенные в процессе окисления воды, переносятся через ферредоксин/NADPH к гидрогеназе. Таким образом, восстановленные за счет фотосинтеза вещества — ферредоксин (или NADPH) — могут служить в качестве физиологических доноров электрона для гидрогеназы и звеном, связывающим гидрогеназы (нирогеназы) с электрон-транспортной цепью.
Исследование биологического производства водорода в зеленых водорослях было начато из простого любопытства, и после 75-летних исследований его эволюционный источник все еще остается загадкой.
Основной прогресс в этой области начинается с 1940-х годов, когда Ганс Гафрон (Hans Gaffron) открыл, что зеленая водоросль Scenedesmus obliquus продуцирует водород. Однако последнее десятилетие было отмечено существенными достижениями в этой области, что было обусловлено повышенным интересом к проблеме фотобиологического производства водорода. Некоторые водоросли в анаэробных условиях могут использовать крахмал в качестве источника протонов и электронов для продуцирования Н2 с помощью гидрогеназ. В цианобактериях протон и электрон, оторванные от воды, могут превращаться в водород с помощью нитрогеназ или в процессе ферментации (см. рисунок).
Некоторые водоросли в анаэробных условиях могут использовать крахмал в качестве источника протонов и электронов для продуцирования Н2 с помощью гидрогеназ. В цианобактериях протон и электрон, оторванные от воды, могут превращаться в водород с помощью нитрогеназ или в процессе ферментации (см. рисунок).
В частности, для некоторых видов зеленых водорослей были секвенированы гены, кодирующие гидрогеназы, и определена кристаллическая структура этих ферментов. Кроме того, в результате интенсивных исследований структуры процессов сборки и биологических свойств гидрогеназ был выяснен механизм, с помощью которого гидрогеназа создает молекулярный водород.
Очевидно, что
коммерческое производство так называемого фотосинтетического водорода (получаемого за счет фотосинтеза) будет невозможно до тех пор, пока не будут решены две главные проблемы, которые мешают гидрогеназе продуцировать значительные количества молекулярного водорода.
Во-первых, гидрогеназа имеет короткое время жизни — фермент не может быть использован для продуцирования водорода дольше одной минуты. Во-вторых, необходимо сделать так, чтобы гидрогеназа стала устойчивой к кислороду. Поскольку все известные в настоящее время гидрогеназы имеют короткое время жизни даже в присутствии очень низких концентраций кислорода, то только модифицированные гидрогеназы с увеличенной способностью продуцировать водород и/или уменьшенной чувствительностью к кислороду позволят перейти к коммерческому производству фотосинтетически генерируемого водорода. Фотосинтетическая эффективность также важна для производства водорода. Поэтому необходима разработка подходов для улучшения связи между фотосинтетической эффективностью, стабильностью, продуктами фотосинтеза и производством водорода.+++
Во-вторых, необходимо сделать так, чтобы гидрогеназа стала устойчивой к кислороду. Поскольку все известные в настоящее время гидрогеназы имеют короткое время жизни даже в присутствии очень низких концентраций кислорода, то только модифицированные гидрогеназы с увеличенной способностью продуцировать водород и/или уменьшенной чувствительностью к кислороду позволят перейти к коммерческому производству фотосинтетически генерируемого водорода. Фотосинтетическая эффективность также важна для производства водорода. Поэтому необходима разработка подходов для улучшения связи между фотосинтетической эффективностью, стабильностью, продуктами фотосинтеза и производством водорода.+++
###3###Как происходит фотосинтез?
Фотосинтез растений — важный биологический процесс, от которого зависит жизнь всех живых организмов. Сальдо химического равновесия фотосинтеза растений — это образование карбогидратов и молекулярного кислорода из двуокиси углерода и воды с помощью энергии солнечного света.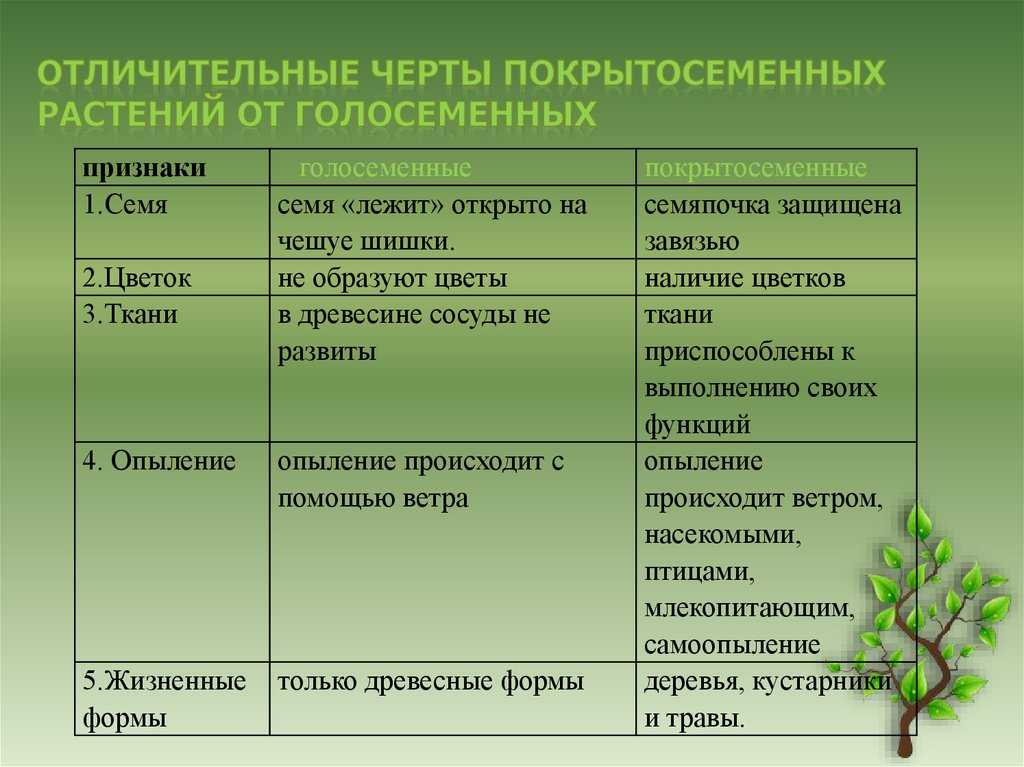 Важной характеристикой этого фантастического преобразования является «расщепление воды», а именно образование одной молекулы кислорода из двух молекул воды, сопровождающееся выделением двух «эквивалентов водорода». Эти «эквиваленты» водорода в конечном итоге используются на образование биологического топлива, такого как крахмал.
Важной характеристикой этого фантастического преобразования является «расщепление воды», а именно образование одной молекулы кислорода из двух молекул воды, сопровождающееся выделением двух «эквивалентов водорода». Эти «эквиваленты» водорода в конечном итоге используются на образование биологического топлива, такого как крахмал.
Энергия, необходимая для реакции расщепления воды, потребляется от солнечного света с помощью особого фермента, называемого фотосистемой 2 (ФС-2).
Фотосинтез инициируется серией фотохимических реакций, в которых энергия поглощенного молекулами хлорофилла света превращается в химическую энергию, которая может быть использована для серии метаболических реакций. Реакции поглощения света в фотосинтетических организмах можно разделить на два раздельных процесса. В первом свет поглощается пигментами антенны, которые связаны с белками антенны. Молекулы хлорофилла, которые поглотили свет, могут передавать эту энергию другим соседним пигментам в процессе, который некоторые называют переносом экситона. Структура и организация антенных пигмент-белковых комплексов показала, что эти белки функционируют в качестве неких строительных лесов, которые связывают их молекулы хлорофилла в высокоорганизованные комплексы (см. рисунок).
Структура и организация антенных пигмент-белковых комплексов показала, что эти белки функционируют в качестве неких строительных лесов, которые связывают их молекулы хлорофилла в высокоорганизованные комплексы (см. рисунок).
Оксигенные организмы (цианобактерии, водоросли и растения) с двумя фотосистемами (ФС-1 и ФС-2) (см. рисунок), а также фотосинтетические бактерии с одной фотосистемой содержат фотосинтетические реакционные центры (РЦ), которые представляют собой белковые мембранные комплексы, состоящие из множества субъединиц, и функционируют в качестве превосходных фотохимических устройств.
Пигменты реакционных центров захватывают энергию, поставляемую, главным образом, процессом переноса энергии возбуждения от антенны, а также прямым поглощением света. Здесь, в реакционных центрах, энергия света превращается в потенциальную энергию окисления-восстановления и стабилизируется в форме, которая имеет время жизни, достаточно долгое, чтобы позволить электронам быть экстрагированными из системы. Перенос этих электронов к другим интермедиатам сопровождается генерированием ионной силы и градиента рН, что дает энергию для синтеза АТФ, а также восстанавливающую энергию, которая используется для превращения СО2 в сахар, крахмал и другие метаболиты.
Перенос этих электронов к другим интермедиатам сопровождается генерированием ионной силы и градиента рН, что дает энергию для синтеза АТФ, а также восстанавливающую энергию, которая используется для превращения СО2 в сахар, крахмал и другие метаболиты.
Все реакционные центры имеют поразительную аналогию в структуре и составе.
В ФС-2 РЦ состоят из двух внутренних мембранных белков Д1 и Д2, чьи аминокислотные последовательности аналогичны, но не идентичны, в аноксигенных фотосинтетических бактериях найдены аналогичные белки L и M. Взаимодействия между этими двумя белками во всех фототрофных организмах образует гетеродимерную структуру, которая предоставляет связывающие участки для кофакторов, которые участвуют в реакциях фотохимического разделения зарядов (см. рисунок выше).
«Фермент», который дал существенный толчок эволюции, известен как ФС-2 и является поэтому ферментом глобального значения. Все типы растений, водоросли и цианобактерии содержат этот многобелковый комплекс, расположенный в тилакоидных мембранах.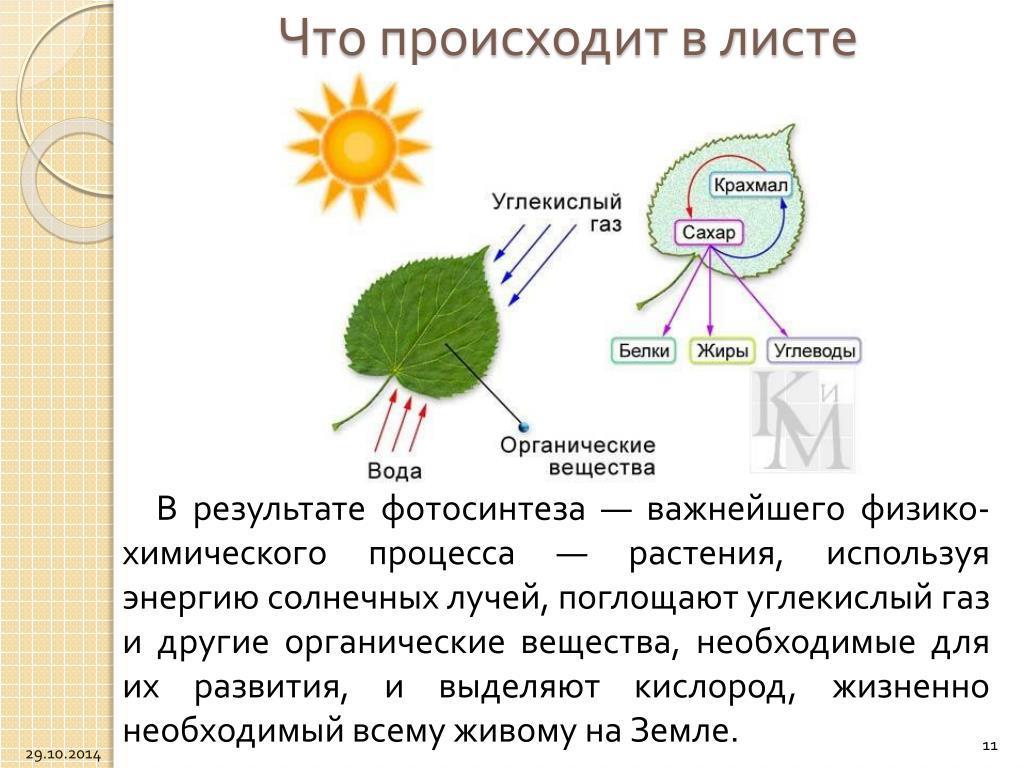 В отличие от химического и электрохимического расщепления воды, которые термодинамически высокозатратные, биологический механизм расщепления воды, катализируемый ФС-2, по-настоящему удивительный, потому что он происходит за счет очень незначительной движущей силы, имеет только умеренные энергии активации, на языке электрохимиков, он имеет малое перенапряжение. Эти свойства побудили химиков обратить завистливые взгляды на фермент, окисляющий воду, в поисках разгадок того, как построить эффективные фотохимические системы, имитирующие, подражающие этой природной реакции. Выигрыш в эффективности от такого катализа мог бы быть значительным и мог бы сделать существенный вклад в производство альтернативного топлива (электрохимическое и фотохимическое расщепление воды).
В отличие от химического и электрохимического расщепления воды, которые термодинамически высокозатратные, биологический механизм расщепления воды, катализируемый ФС-2, по-настоящему удивительный, потому что он происходит за счет очень незначительной движущей силы, имеет только умеренные энергии активации, на языке электрохимиков, он имеет малое перенапряжение. Эти свойства побудили химиков обратить завистливые взгляды на фермент, окисляющий воду, в поисках разгадок того, как построить эффективные фотохимические системы, имитирующие, подражающие этой природной реакции. Выигрыш в эффективности от такого катализа мог бы быть значительным и мог бы сделать существенный вклад в производство альтернативного топлива (электрохимическое и фотохимическое расщепление воды).
Постепенно молекулярные энзимологии медленно открывали секреты фотосинтетического водорасщепляющего фермента.
Было показано, что фотохимический РЦ ФС-2 подобен более простому и гораздо более изученному РЦ пурпурных бактерий. Это впервые было показано в 1980-х с помощью спектроскопии, биохимии и молекулярной биологии, а позже подтверждено кристаллографией. Однако каталитический участок окисления воды все еще изучен недостаточно. Одним из наиболее важных достижений в структурной биологии в конце 20-го столетия была кристаллизация бактериальных РЦ и
Это впервые было показано в 1980-х с помощью спектроскопии, биохимии и молекулярной биологии, а позже подтверждено кристаллографией. Однако каталитический участок окисления воды все еще изучен недостаточно. Одним из наиболее важных достижений в структурной биологии в конце 20-го столетия была кристаллизация бактериальных РЦ и
определение их структуры, сделанное Дейзенхофером и Михелем (Deisenhofer and Michel), которые наряду с Робертом Хубером (Robert Huber) получили Нобелевскую премию по химии за эту работу в 1988 году.
Это открыло дверь к кристаллизации и определению структуры большого числа различных мембранных белков, а также привело в конечном итоге к кристаллизации ФС-1 и ФС-2, и выяснению их структур с разрешением, соответственно, 2.5 и 3.0 Å. Несколько интересных аспектов функции РЦ были выяснены с помощью этих кристаллических структур. РЦ бактерий, ФС-1 и ФС-2 обладают псевдо С2 симметрией: можно разделить центры пополам, чтобы получить зеркальные изображения, которые будут аналогичными, подобными, но не идентичными; имеются две ветви кофакторов транспорта электрона, каждая из которых может служить в качестве пути транспорта электрона.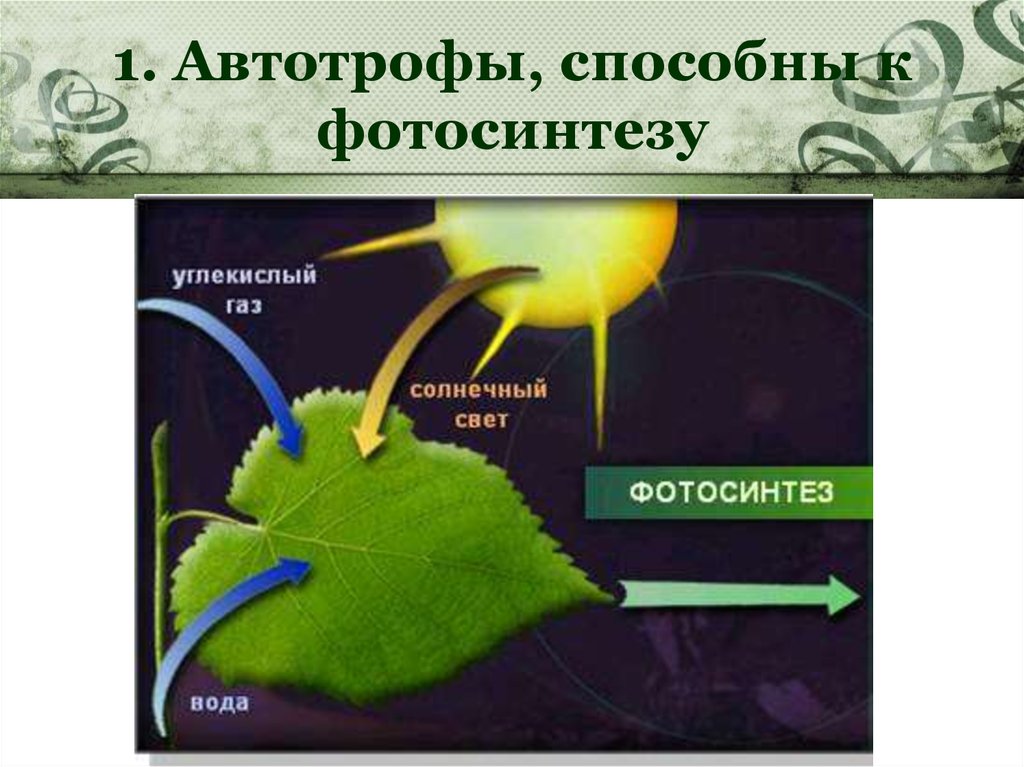 Кофакторы переноса электрона организованы так, что поглощение света приводило бы к переносу электрона через липидный бислой тилакоидной мембраны. Поскольку структура и функция бактериального РЦ, или РЦ тип II, хорошо охарактеризована, структура этой системы используется в качестве основы для понимания функции всех фотосинтетических реакционных центров.
Кофакторы переноса электрона организованы так, что поглощение света приводило бы к переносу электрона через липидный бислой тилакоидной мембраны. Поскольку структура и функция бактериального РЦ, или РЦ тип II, хорошо охарактеризована, структура этой системы используется в качестве основы для понимания функции всех фотосинтетических реакционных центров.
Точная кинетическая модель окислительно-восстановительных интермедиатов, система (машина) была установлена в течение последних десятилетий. Общепринято, что активный участок состоит из кластера из четырех ионов Mn, близко расположенных к активной тирозиновой группе. Была также показана роль близлежащего иона Са. С помощью направленного мутагенеза и спектроскопии были получены данные о специфических аминокислотах, вероятных лигандах Mn. Кроме того, накоплено много спектроскопической информации о структурной геометрии этого кластера. Но поскольку Mn — это один из наименее кооперативных переходных металлов, однозначная структура водорасщепляющего участка не определена.
Однако эта картина изменилась вследствие появления рентгеноструктурных кристаллографических моделей.
Первые грубые структурные модели подтвердили существующие модели относительно мест расположения и конфигураций кофакторов фотохимического реакционного центра и основные аспекты белковой структуры. Они оказались, как и ожидалось, неким реакционным центром пурпурных бактерий с Mn-содержащим комплексом в основании. Несколько давнишних неопределенностей также были решены: например, расположение Mn-содержащего кластера и вопрос о том, на какой стороне реакционного центра расположен цитохром b559 и т. д. Первая кристаллографическая модель с высоким разрешением, включая большую часть боковых аминокислотных цепей многих субъединиц, впервые появилась в 2004 году. Это дало не только множество прямых новых данных, но также богатый источник структурной информации для значительного ряда текущих и будущих исследований. Хотя имеющиеся на настоящий момент кристаллические структуры еще не дают ясной недвусмысленной модели структуры и конфигурации водорасщепляющего участка, они дали заметный количественный прыжок.
Сегодня мы знаем много о ФС-2 и реакции окисления воды. Однако остается много вопросов, на которые еще предстоит ответить. Ясно, что структурные свойства и динамика структурообразующих белков ФС-2 являются критичными для переноса электронов, который приводит к окислению воды до молекулярного кислорода. Тем не менее необходимо полностью понять эти белковые взаимодействия, получить кристаллическую структуру с более высоким разрешением, а также усовершенствовать и/или разработать методы определения динамики белков.
Полностью понять реакции ФС-2 необходимо не только для развития наших фундаментальных знаний, но и для разработки новых технологий, использующих энергию солнца для расщепления воды на чистый молекулярный кислород и водород, которые будут использованы в качестве потенциального источника топлива, как указывал на это Жюль Верн еще 136 лет назад (см. рисунок).
«Я думаю, что воду когда-нибудь будут употреблять как топливо, что водород и кислород, которые входят в ее состав, будут использованы вместе или поодиночке и явятся неисчерпаемым источником света и тепла, значительно более интенсивным, чем уголь. Придет день, когда котлы паровозов, пароходов и тендеры локомотивов будут вместо угля нагружены сжатыми газами, и они станут гореть в топках с огромной энергией… Вода — уголь будущего», — писал Жюль Верн в своей книге «Таинственный остров».
Придет день, когда котлы паровозов, пароходов и тендеры локомотивов будут вместо угля нагружены сжатыми газами, и они станут гореть в топках с огромной энергией… Вода — уголь будущего», — писал Жюль Верн в своей книге «Таинственный остров».
В следующей лекции профессор Аллахвердиев расскажет о новейших исследованиях свойств и функций ФС-2, а также об экспериментальном устройстве, позволяющем вырабатывать энергию из воды и солнечного света.+++
История жизни и экология цианобактерий
История жизни и экология цианобактерийЦианобактерии фотосинтезируют.
Хотя цианобактерии не отличаются большим разнообразием форм, и хотя они
микроскопичны, они богаты химическим разнообразием. Цианобактерии получают свое
название от голубоватого пигмента фикоцианин ,
которые они используют для захвата света для фотосинтеза. Они также содержат хлорофилл а , тот же фотосинтетический пигмент, что и
используют растения. В
Дело в том, что хлоропласты растений представляют собой симбиотические цианобактерии, поглощаемые
зеленые водоросли предки растений где-то в докембрии. Однако,
не все «сине-зеленые» бактерии синие; некоторые распространенные формы красные или розовые
из пигмента фикоэритрин . Эти бактерии часто встречаются
растет на тепличном стекле или вокруг раковин и водостоков. Красное море получает
свое название от случайных цветков красноватого вида
В
Дело в том, что хлоропласты растений представляют собой симбиотические цианобактерии, поглощаемые
зеленые водоросли предки растений где-то в докембрии. Однако,
не все «сине-зеленые» бактерии синие; некоторые распространенные формы красные или розовые
из пигмента фикоэритрин . Эти бактерии часто встречаются
растет на тепличном стекле или вокруг раковин и водостоков. Красное море получает
свое название от случайных цветков красноватого вида
Каким бы ни был их цвет, цианобактерии способны к фотосинтезу. производят себе еду. За это их прозвали «сине-зелеными». водоросли», хотя они не имеют никакого отношения ни к одному из различных эукайотических водоросли. Термин «водоросли» просто относится к любым водным организмам, способным фотосинтеза, и поэтому относится к нескольким группам.
Цианобактерии играют важную роль в круговороте азота.
Цианобактерии являются очень важными организмами для здоровья и роста
много растений.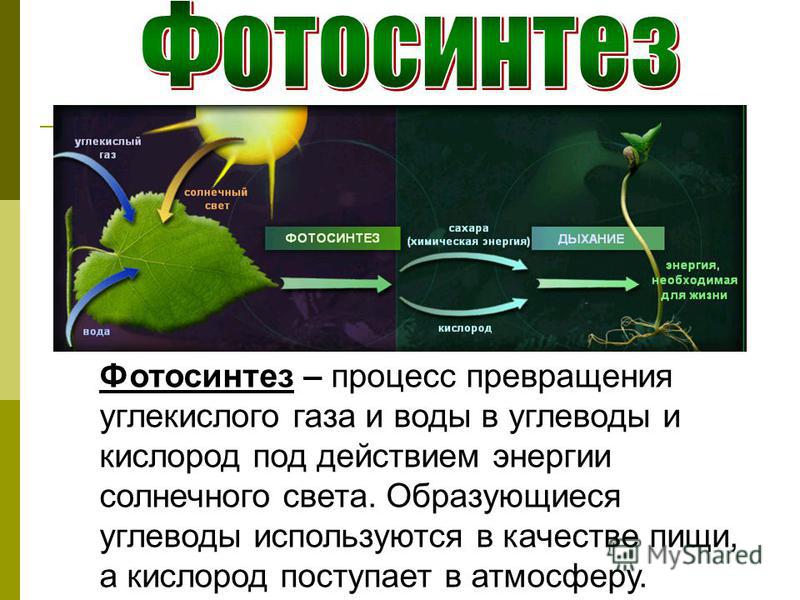 Это одна из очень немногих групп организмов, способных преобразовывать
инертный атмосферный азот в органическую форму, такую как
Это одна из очень немногих групп организмов, способных преобразовывать
инертный атмосферный азот в органическую форму, такую как
Нитрификация не может происходить в присутствии кислорода, поэтому азот фиксируется в специализированные клетки называются гетероцистами . Эти клетки имеют особенно утолщенная стенка, содержащая анаэробную среду. Вы можете увидеть эти более крупные клетки среди нитей Nostoc , показанные справа.
Многие растения, особенно бобовые
 папоротник содержит колонии цианобактерий Anabaena в своем
листья, где он фиксирует азот. Затем папоротники обеспечивают недорогой
естественное удобрение и источник азота для растений риса, когда они умирают в
конец сезона.
папоротник содержит колонии цианобактерий Anabaena в своем
листья, где он фиксирует азот. Затем папоротники обеспечивают недорогой
естественное удобрение и источник азота для растений риса, когда они умирают в
конец сезона.Цианобактерии также образуют симбиотические отношения со многими грибы, образуя сложные симбиотические «организмы», известные как лишайники.
Питательный или ядовитый?
Цианобактерия Spirulina , показанная справа, давно был оценен как источник еды; он богат белком, и его довольно легко выращивать в прудах. В тропических странах это может быть очень важной частью рациона. регулярно ели ацтеки; его также подают в некоторых восточных блюдах. В США, популярность Spirulina в первую очередь как «здоровье еда», продаваемая в магазинах в виде сухого порошка или в виде таблеток.
Многие другие виды цианобактерий образуют популяции, токсичные для
люди и животные. Сине-зеленая пена пруда была связана с отравлением
крупный рогатый скот и собаки, а иногда и люди.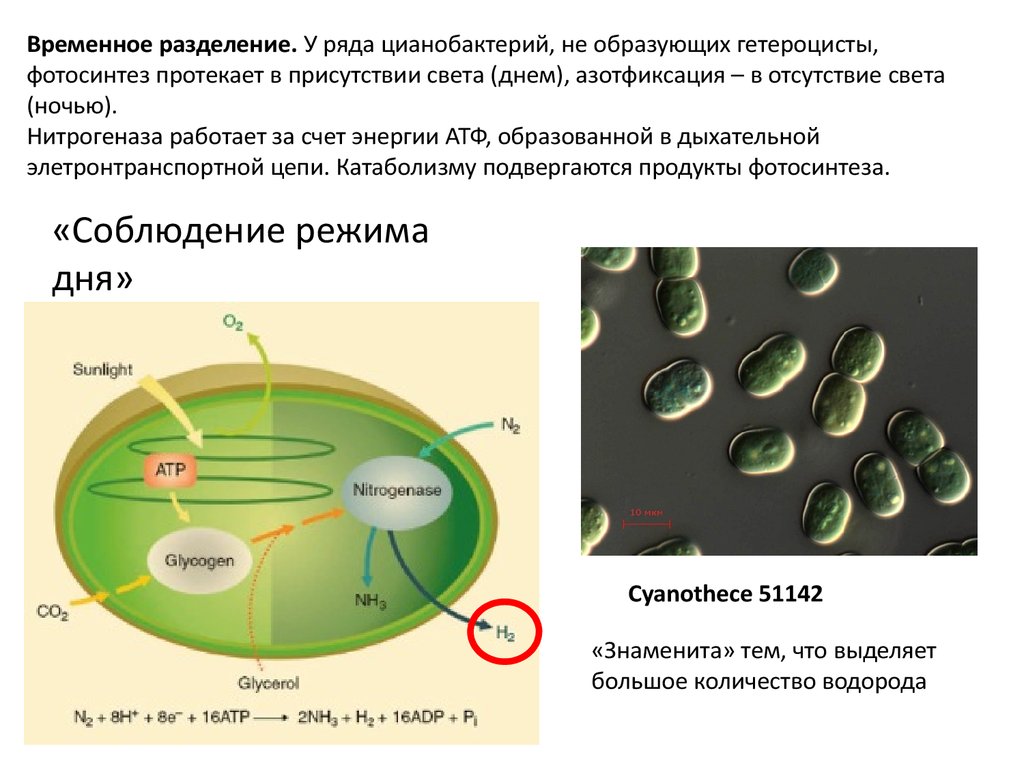
Цианобактерии могут вызывать и другие проблемы; разновидность Lyngbya вызывает одно из раздражений кожи. широко известный как «зуд пловца».
Узнайте больше о токсичных цианобактериях на Домашняя страница токсичных цианобактерий.
Изображения Nostoc и Spirulina предоставлены коллекцией ботанических изображений Университета Висконсина.
Фотосинтез у бактерий
Введение
Фотосинтезирующие бактерии существуют дольше, чем земная атмосфера может поддерживать человеческую жизнь. Однако только недавно ученые начали разгадывать тайну того, как эти микроорганизмы реализуют механизмы фотосинтеза.
Хотя ученые до сих пор не смогли правильно расставить все кусочки головоломки о фотосинтезирующих бактериях, они активно изучают их и получают ценные знания о том, как они фотосинтезируют и как эволюционировали. Фактически, они считают, что эти микроорганизмы, возможно, оказали огромное влияние на то, почему мир развивался так, как это было, и могут показать потенциал для жизни в местах, считающихся непригодными для жизни, включая экстремальные климатические условия, такие как Антарктида и даже другие планеты.
Фактически, они считают, что эти микроорганизмы, возможно, оказали огромное влияние на то, почему мир развивался так, как это было, и могут показать потенциал для жизни в местах, считающихся непригодными для жизни, включая экстремальные климатические условия, такие как Антарктида и даже другие планеты.
Что такое фотосинтезирующие бактерии?
Как следует из названия, эти микроорганизмы представляют собой особый тип бактерий, содержащих светопоглощающие пигменты и реакционные центры, благодаря которым они способны преобразовывать световую энергию в химическую.
Цианобактерии содержат хлорофилл, в то время как другие формы бактерий содержат бактериохлорофилл. Хотя бактериохлорофилл напоминает хлорофилл, он поглощает свет с большей длиной волны, чем хлорофилл. Бактериохлорофилл а является наиболее распространенной формой бактериохлорофилла, но другие формы включают b, c, d, e, f и g.
Бактерии, содержащие бактериохлорофилл, не используют воду в качестве донора электронов и, следовательно, не производят кислород.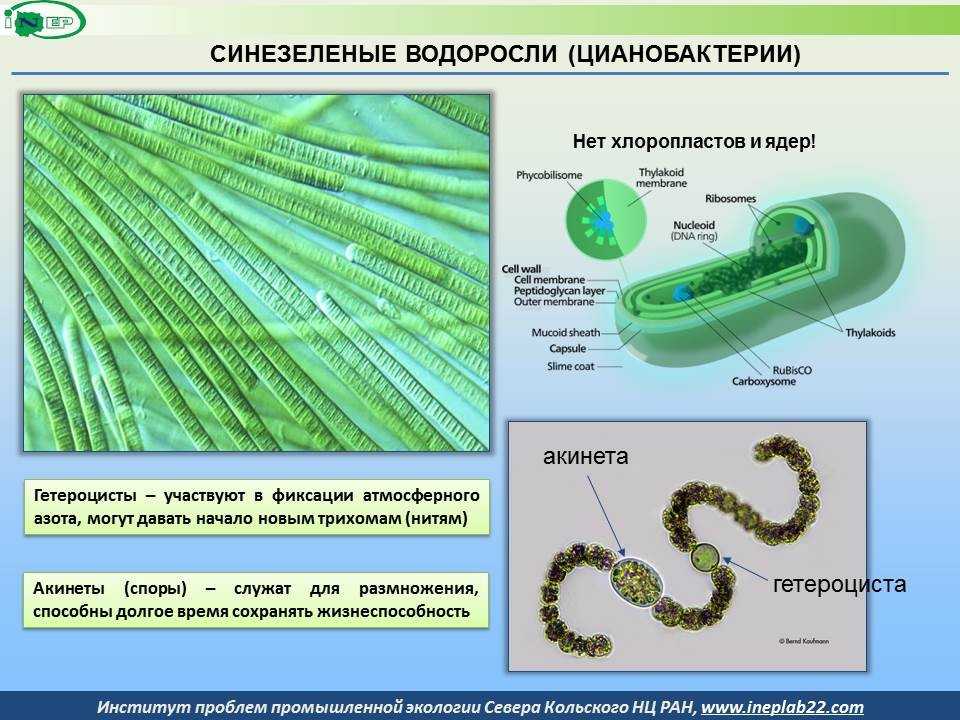 Это известно как аноксигенный фотосинтез. Цианобактерии осуществляют фотосинтез, используя воду в качестве донора электронов, подобно растениям. Это приводит к выработке кислорода и известно как оксигенный фотосинтез.
Это известно как аноксигенный фотосинтез. Цианобактерии осуществляют фотосинтез, используя воду в качестве донора электронов, подобно растениям. Это приводит к выработке кислорода и известно как оксигенный фотосинтез.
Классификация фотосинтезирующих бактерий
Кислородные фотосинтезирующие бактерии осуществляют фотосинтез аналогично растениям. Они содержат светособирающие пигменты, поглощают углекислый газ и выделяют кислород. Cyanobacteria или Cyanophyta — единственная известная на сегодняшний день форма оксигенных фотосинтезирующих бактерий. Однако существует несколько видов цианобактерий. Они часто имеют сине-зеленый цвет и, как считается, внесли свой вклад в биоразнообразие на Земле, помогая преобразовать раннюю атмосферу Земли с дефицитом кислорода в богатую кислородом среду. Эта трансформация означала, что большинство анаэробных организмов, которые процветали в отсутствие кислорода, в конечном итоге вымерли, и начали появляться новые организмы, зависящие от кислорода.
Цианобактерии в основном встречаются в воде, но могут выживать на суше, в камнях и даже в панцирях (или мехе) животных и в кораллах. Также известно, что они являются эндосимбионтами, что означает, что они могут жить в клетках или теле другого организма на взаимовыгодной основе. Цианобактерии также имеют тенденцию жить в экстремальных погодных условиях, таких как Антарктида, и интересны ученым, поскольку они могут указывать на возможность существования жизни на других планетах, таких как Марс.
Аноксигенные фотосинтезирующие бактерии потребляют углекислый газ, но не выделяют кислород. К ним относятся зеленые и фиолетовые бактерии, а также нитчатые аноксигенные фототрофы (FAP), фототрофные ацидобактерии и фототрофные гелиобактерии. Давайте посмотрим на различия между этими типами бактерий немного подробнее.
Пурпурные бактерии можно разделить на два основных типа: Chromatiaceae, которые производят частицы серы внутри своих клеток, и Ectothiorhodospiraceae, которые производят частицы серы вне своих клеток. Они не могут фотосинтезировать в местах с избытком кислорода, поэтому их обычно можно найти либо в стоячей воде, либо в горячих серных источниках.
Они не могут фотосинтезировать в местах с избытком кислорода, поэтому их обычно можно найти либо в стоячей воде, либо в горячих серных источниках.
Вместо того, чтобы использовать воду для фотосинтеза, подобно растениям и цианобактериям, пурпурные серобактерии используют сероводород в качестве восстановителя, поэтому они выделяют серу, а не кислород.
Пурпурные бактерии, вероятно, являются наиболее широко изученными фотосинтетическими бактериями, которые используются во всех видах научных исследований, включая теории о возможной микробиологической жизни на других планетах.
Пурпурные несерные бактерии не выделяют серу, потому что вместо сероводорода в качестве восстановителя они используют водород. Хотя эти бактерии могут переносить небольшое количество серы, они переносят гораздо меньше, чем фиолетовые или зеленые серные бактерии, и слишком много сероводорода для них токсично.
Зеленые серные бактерии , как правило, неподвижны (неподвижны) и могут принимать различные формы, такие как сферы, палочки и спирали.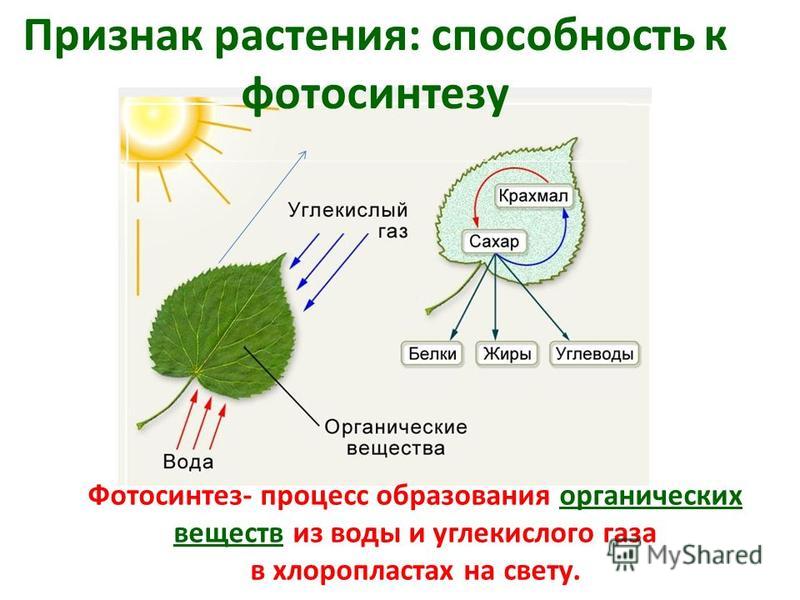 Эти бактерии были обнаружены глубоко в океане рядом с черным курильщиком в Мексике, где они выжили благодаря свету термального источника. Они также были найдены под водой недалеко от Индонезии. Эти бактерии могут выживать в экстремальных условиях, как и другие типы фотосинтезирующих бактерий, что предполагает эволюционный потенциал для жизни в местах, которые иначе считались бы непригодными для жизни.
Эти бактерии были обнаружены глубоко в океане рядом с черным курильщиком в Мексике, где они выжили благодаря свету термального источника. Они также были найдены под водой недалеко от Индонезии. Эти бактерии могут выживать в экстремальных условиях, как и другие типы фотосинтезирующих бактерий, что предполагает эволюционный потенциал для жизни в местах, которые иначе считались бы непригодными для жизни.
Фототрофные ацидобактерии встречаются во многих почвах и довольно разнообразны. Некоторые из них являются ацидофилами, что означает, что они процветают в очень кислых условиях. Однако мало что известно об этой группе бактерий, потому что они относительно новые, впервые обнаруженные в 1991 году. Они используют особый тип бактериохлорофилла, помеченный буквой g, что отличает их от других типов фотосинтезирующих бактерий. Они фотогетеротрофы, что означает, что они не могут использовать углекислый газ в качестве основного источника углерода.
Зеленые и красные нитчатые аноксигенные фототрофы (FAP) ранее назывались зелеными несерными бактериями, пока не было обнаружено, что они также могут использовать компоненты серы для работы в своих процессах. Этот тип бактерий использует нити для передвижения. Цвет зависит от типа бактериохлорофилла, который использует конкретный организм. Что еще уникально в этой форме бактерий, так это то, что они могут быть либо фотоавтотрофными, то есть они создают свою собственную энергию за счет энергии солнца; хемоорганотропный, требующий источника углерода; или фотогетеротрофные, что, как объяснялось выше, означает, что они не используют углекислый газ в качестве источника углерода.
Этот тип бактерий использует нити для передвижения. Цвет зависит от типа бактериохлорофилла, который использует конкретный организм. Что еще уникально в этой форме бактерий, так это то, что они могут быть либо фотоавтотрофными, то есть они создают свою собственную энергию за счет энергии солнца; хемоорганотропный, требующий источника углерода; или фотогетеротрофные, что, как объяснялось выше, означает, что они не используют углекислый газ в качестве источника углерода.
Полезные области применения фотосинтезирующих бактерий
В настоящее время фотосинтезирующие бактерии используются в различных областях, включая очистку воды, биоудобрения, корма для животных и биоремедиацию химикатов среди многих других. Их используют для очистки загрязненной воды, поскольку они могут расти и утилизировать токсичные вещества, такие как h3S или h3S203.
Исследователи из Гарвардского института Висса сконструировали фотосинтезирующие бактерии для производства простых сахаров и молочной кислоты.

Leave A Comment