решение задач (Антошин, А. Э.)
Антошин, А. Э.В пособии подробно разобраны решения всех типов задач базового, повышенного и высокого уровней сложности в соответствии с перечнем элементов содержания, проверяемых на ЕГЭ по химии. Регулярная работа с данным пособием позволит учащимся научиться быстро и без ошибок решать задачи по химии разных уровней сложности.
Полная информация о книге
- Вид товара:Книги
- Рубрика:Химия
- Целевое назначение:Рабочие тетр.,тесты и др. уч. пособ. д/уч.10-11 кл
- Серия:ЕГЭ. Сдаем без проблем
- Издательство: ЭКСМО
- Год издания:2019
- Тираж:3000
- Формат:60х90/16
- УДК:373:53
- Штрихкод:9785041026226

- Сведения об ответственности:Андрей Антошин
- Код товара:30459
ЕГЭ химия, ЕГЭ математика: решение задач на растворы
В ряде заданий ЕГЭ по математике встречаются задачи на смешивание растворов. Эти задания могут вызывать затруднения, поскольку математики склонны считать концентрацию растворов разделом химии. На самом деле, эти задания решаются чисто математическим способом, с помощью линейного уравнения.
Преимущества этого способа для ЕГЭ по химии: легко восстановить в памяти (в отличие от метода креста), решает задачу одним уравнением.
В основе метода лежит определение:
масса компонентамассовая доля = ––––––––––––––––– (1)
масса целого
mв-ва
т. е. ω = ––––––––
m
где ω — массовая доля растворенного вещества,
mв-ва — масса растворенного вещества,
m — масса раствора.
Следовательно, масса растворенного вещества равна произведению массы раствора на массовую долю растворенного вещества:
mв-ва = m • ω (2).
При сливании растворов складываются как массы растворов:
m1 + m2 = m3 (3)
так и массы растворенных веществ:
mв-ва1 + mв-ва2 = mв-ва3
Подставляя вместо массы растворенных веществ произведение (2), получаем:
m1 • ω1 + m2 • ω2 = m3 • ω3
Заменяя неизвестную массу на выражение (3), получаем:
m1 • ω1 + m2 • ω2= (m1
m1 • ω1 + (m3 − m1) • ω2 = m3 • ω3 (5)
Пример:
Определите массы 10%-ного и 50%-ного (по массе) растворов, необходимые для получения 200 г 20%-ного раствора.
Решение:
ω1 = 10 %, ω2 = 50 %, ω3 = 20 %, m3 = 200 г, m2 = 200 − m1
Составляем уравнение (5):
m1 • 10 + (200 − m1) • 50 = 200 • 20
40 • m1 = 6000
m1 = 150 (г),
m2 = 200 − m
Ответ: 150 г, 50 г.
Пример 2:
Определите массы 25%-ного (по массе) раствора и воды, необходимые для получения 200 г 10%-ного раствора.
Решение:
ω1 = 25 %, ω2 = 0 %, ω3 = 10 %, m3 = 200 г
Составляем уравнение (5):
m1 • 25 + m2 • 0 = 200 • 10
25 • m1 = 2000
m1 = 80 (г),
m2 = 200 − m1 = 200 − 80 = 120 (г)
Ответ: 80 г, 120 г.
Методика решения задач по химии на изменение концентрации раствора
В задачах, связанных с добавлением к раствору определенного количества растворителя или растворенного вещества, необходимо сначала рассчитать массу растворенного вещества в исходном растворе, а затем использовать ее для дальнейших вычислений. Условие каждой задачи для большей наглядности лучше изобразить в виде рисунка.
Задача 1.
К 180,0 г 8% -ного раствора хлорида натрия добавили 20 г NaС1. Массовая доля хлорида натрия в образовавшемся растворе равна ….% (запишите число с точностью до десятых).
Дано:
масса исходного раствора: mисх.р-ра = 180 г;
массовая доля NaС1 в исходном растворе: (NaС1)в исх р-ре = 8%;
масса добавленной соли NaС1: m(NaСl)добавл = 20 г.
Найти:
Решение:
Условие задачи удобно отобразить в виде рисунка:
1. Находим массу NaСl в исходном растворе:
Находим массу NaСl в исходном растворе:
2. Масса NaС1 в конечном растворе представляет собой сумму:
m(NаС1)в кон.р.ре = m(NаС1)в исх. р.ре + m(NаС1)добавл. = 14,4+ 20 = 34,4 г.
3. Массу добавленной соли учитываем и в массе конечного раствора:
mкон. р-ра = mисх. р-ра + m(NаС1)добавл. = 180 + 20 = 200 г.
4. Полученные данные позволяют определить массовую долю в конечном растворе:
Ответ: (NaС1)в исх р-ре = 17,2%.
Задача, в которой добавляется некоторое количество воды к порции раствора известной концентрации, решается по тому же алгоритму.
В задаче на смешение двух растворов требуется проводить немного большее количество расчетов. В этом случае необходимо вычислить массу растворенного вещества в каждом из
исходных растворов.
Задача 2.
Смешали 200 г 20%-ного раствора NаОН с 218 мл 10%-ного раствора того же вещества (p = 1,11 г/мл). Массовая доля щелочи в полученном растворе. …% (Запишите число с точностью до десятых).
Дано:
масса первого раствора NаОН: m
массовая доля NаОН в первом р-ре: со(МаОН) в 1 исх р-ре = 20% ;
объем второго раствора NаОН: V2исх.р-ра = 218 мл;
массовая доля NаОН во втором р-ре: (NаОН) во 2 исх. р-ре = 10% ;
плотность второго исходного раствора: р2 исх. р.р=1,11 г/мл.
Найти: массовую долю NаОН в конечном р-ре: (NаОН)в кон р-ре
Решение:
Условие задачи удобно отобразить в виде рисунка:
При решении данной задачи необходимо определить массу NаОН в каждом из исходных растворов. Далее найти суммарную массу конечного раствора и массу NаОН в нем. После этого вычисляем искомую величину.
1. Находим массу NаОН в первом исходном растворе:
Находим массу NаОН в первом исходном растворе:
2. Находим массу второго исходного раствора:
m2 исх. р-ра = V2 исх. р-ра. p 2 исх. р-ра = 218 . 1,11 = 242 г.
3. Находим массу NаОН во втором исходном растворе:
m(NaOH)в кон. р-ре = m(NaOH)в 1 исх. р-ре + m(NaOH)во 2 исх. р-ре = 40 + 24,2 = 64,2 г.
5. Находим массу конечного раствора:
mкон. р-ра = m1 исх. р-р
6. Находим массовую долю NаОН в конечном растворе:
Округляем полученное значение до десятых.
Ответ: (NaOH)в кон.р-ре = 14,5%.
В задаче на выпаривание масса раствора уменьшается обычно за счет удаления растворителя. При этом масса растворенного вещества остается прежней, что приводит к увеличению концентрации.
Задача 3.
Определите массу воды, которую необходимо выпарить из 2 л 10% раствора NаОН (р = 1,11 г/мл) для повышения массовой доли NаОН в нем до 15% . Ответ: … г (запишите число с точностью до целых).
Дано:
объем исходного раствора: Vисх. р-ра = 2 л;
плотность исходного раствора: рисх р-ра =1,11 г/мл;
массовая доля NаОН в исходном р-ре: (NаОН)в исх р.ре = 10% ;
массовая доля NаОН в конечном р-ре:(NаОН)в кон р-ре = 15%
Найти: массу испарившейся воды: m(Н2О)испарили = ?
Решение:
При выпаривании водного раствора NаОН улетучиваться будет только вода. Масса NаОН будет одинаковой как в исходном, так и в конечном растворе.
Схематично алгоритм решения можно представить следующим образом:
1. Найдем массу исходного раствора:
m исх. р-ра = V исх. р-ра. рисх. р-ра
рисх. р-ра
V исх. р-ра = 2 л = 2000 мл
mисх. р-ра = 2000 . 1,11 = 2220 г.
2. Найдем массу NаОН в исходном растворе:
3. Определим массу конечного раствора:
4. Уменьшение массы раствора произошло только из-за испарения воды, следовательно, по разнице масс исходного и конечного растворов можно найти массу улетучившейся воды:
m(Н2О)испарилось = mисх р-ра – mкон. р-ра = 2220 — 1480 = 740 г.
Ответ: m(Н2О)испарилось = 740 г.
В условиях некоторых задач предполагается выведение из раствора в виде газа легколетучего растворенного вещества (например МН3; НС1; Н2S или растворенного в воде органического вещества). Для решения таких задач необходимо считать неизменной массу растворителя (воды).
Задача 4.
При нагревании 200 г 25%-ного раствора аммиака 20 г этого вещества улетучилось. Массовая доля аммиака в растворе после нагревания равна… % (запишите число с точностью до десятых).
Дано:
масса исходного раствора: mисх р-ра = 200 г;
массовая доля NН3 в исходном растворе: (NН3)в исх. р-ре = 25% ;
масса улетучившегося аммиака: m(NН3)улетучилось = 20 г.
Найти: массовую долю NH3 в конечном р-ре: (NН3)в кон. р ре =?
Решение:
Схематично алгоритм решения можно представить следующим образом:
1. Находим массу NН3 в исходном растворе:
2. Находим массу NН3 в конечном растворе:
m(NH3) в кон. р-ре = m(NH3) в исх. р-ре — m(NН3)улетело = 50 — 20 = 30 г.
Находим массу конечного раствора1:
mкон р-ра = mисх р-ра — m(NН3)улетучилось = 200 — 20 = 180 г.
4. Находим массовую долю аммиака в конечном растворе:
Округляем значение, согласно требованию условия, и получаем: (NН3)в кон. р-ре = 16,7% .
Ответ: (NН3)в кон. р-ре = 16,7% .
Комментарии:
1При решении данной задачи учащиеся часто забывают найти массу
конечного раствора. После определения массы оставшегося аммиака они для нахождения массовой доли NH3 в конечном растворе ошибочно делят массу оставшегося NH3 на массу исходного раствора.
Избежать этой распространенной ошибки помогают комментарии каждой записанной величины. Например, следует записывать mкон. р-ра, а не mр-ра ; m(NH3)в кон. р-ре, а не m(NH3).
Источник:
ЕГЭ. Химия. Расчетные задачи в тестах ЕГЭ. Части А, В, С / Д.Н. Турчен. — М.: Издательство «Экзамен», 2009. — 399 [1]с. (Серия «ЕГЭ. 100 баллов»). I8ВN 978-5-377-02482-8.
Образовательный центр «Взлёт»
16 июля 2020 года состоится ЕГЭ по химии. Продолжаем активную подготовку к сдаче экзамена!
На сайте регионального Центра в разделе «Подготовка к ГИА» размещены видеоуроки по химии, подробные презентации, а также дополнительные учебные материалы к каждому уроку.
Урок №1. Тема: Строение атома.
Периодический закон и Периодическая система химических элементов Д.И. Менделеева, химическая связь и строение вещества.
olympmo.ru/chem11-1.html
Урок №2. Тема: Тепловой эффект химической реакции.
На уроке решаем термохимические уравнения. Скорость реакции, ее зависимость от различных факторов.
olympmo.ru/chem11-2.html
Урок №3. Тема: Классификация химических реакций в неорганической и органической химии.
Классификация химических реакций в неорганической и органической химии. Обратимые и необратимые химические реакции. Химическое равновесие.
olympmo.ru/chem11-3.html
Урок №4. Тема: Гидролиз в заданиях ЕГЭ по химии.
Изучаем гидролиз солей различных типов.
olympmo.ru/chem11-4.html
Урок №5. Тема: Электролиз в заданиях ЕГЭ по химии.
Электролиз расплавов и растворов электролитов (солей, оснований, кислот).
olympmo.ru/chem11-5.html
Урок №6. Тема: Качественные реакции на неорганические вещества и ионы.
Изучаем качественные реакции на неорганические вещества и ионы.
olympmo.ru/chem11-6.html
Урок №7. Тема: Методы решения задач № 27 ЕГЭ по химии.
При решении задач на приготовление растворов используем: «Метод креста»; «Метод стаканчиков».
olympmo.ru/chem11-7.html
Урок №8. Тема: Окислительно-восстановительные реакции и реакции ионного обмена.
Изучаем окислительно-восстановительные реакции и реакции ионного обмена. Решаем задания высокого уровня сложности, задачи № 30 и 31.
olympmo.ru/chem11-8.html
ЕГЭ по химии стал сложнее? Рассказываем, как улучшить подготовку
В 2017 году содержание заданий ЕГЭ по химии глобально изменилось, и по структуре, и по системе оценивания. Давайте разберемся, что делать, чтобы быть уверенным в своих силах на экзамене.
В ЕГЭ по химии больше не будет тестов, количество заданий уменьшится до 34, их структура станет соответствовать курсу химии – для этого введена группировка по темам. Свое решение об изменениях эксперты ФИПИ объясняют тем, что в таком виде экзамен по химии станет более качественной проверкой знаний.
Как подготовиться к ЕГЭ по химии? Девиз выпускника в процессе подготовки и сдачи ЕГЭ: «Делай, что должно, и будь что будет». Известны темы и типы заданий, которые будут на экзамене, а работа ученика – получить и закрепить системные знания по ним и натренироваться решать задачи. Решение задач – один из важнейших блоков подготовки по химии.
Известны темы и типы заданий, которые будут на экзамене, а работа ученика – получить и закрепить системные знания по ним и натренироваться решать задачи. Решение задач – один из важнейших блоков подготовки по химии.
Как научиться решать задачи по химии? Для этого нужно знать понятия, понимать принципы их взаимосвязей и, конечно, тренироваться в решении задач. Снова и снова.
Важный момент – самостоятельное решение! Необходимо отказаться от механического выбора из готовых вариантов ответа, находить решение и формулировать ответ самостоятельно. Также очень важно тщательно разбирать каждую задачу, чтобы понять, в чем была ошибка, почему этот ответный верный, а другой – нет.
Какие варианты есть у школьника для того, чтобы получить хорошую подготовку по химии? Школьных занятий многим не хватает, найти хорошего репетитора – зачастую проблема, интернет-сайты предлагают только тесты, которые не помогают освоить материал…
Специально для тех, кто сейчас готовится к ЕГЭ, разработано приложение «ХиШник». В нем ученики решают задачи: самостоятельно вводят ответ (никаких тестов!) и получают от программы обучающие подсказки и комментарии. Каталог задач «ХиШника» состоит из более чем 1500 задач по всем темам школьной химии, с 8 по 11 класс. Уровень заданий ученик выбирает самостоятельно – можно сразу переходить к повышенной сложности, а можно двигаться, постепенно повышая уровень.
Подготовка к ЕГЭ вместе с «ХиШником» – это отличное дополнение к школьным урокам и факультативным занятиям. Это индивидуальный подход к каждому ученику и обучающие подсказки по каждой задаче. Выпускник получает возможность тренироваться по темам и типам задач, которые нужны именно ему.
В «ХиШнике» можно решать расчетные задачи, вводить молекулярные, структурные, электронные формулы и уравнения реакции. Это настоящая химия! Все задачи составлены в соответствии с требованиями ФГОС.
Качественная тренировка в решении задач – залог успеха при подготовке к ЕГЭ по химии. Готовьтесь вместе с «ХиШником» и получайте самые высокие баллы!
Начать работу в приложении очень просто – скачайте приложение и активируйте лицензионный ключ для полного доступа ко всем задачам. Подробности на сайте www.hishnik-school.com.
Рабочее место ученика в приложении «ХиШник»
Текстовые задачи: проценты, сплавы, растворы
Цели: Оказать методическую помощь при подготовке выпускников к ЕГЭ по математике; проработать алгоритм решения химических задач.
Задачи.
Обучающие:
- активизировать знания учащихся по теме «Массовая доля вещества в растворе»;
- познакомить учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков»;
- закрепить умение решать задачи на растворы и сплавы;
- продолжить подготовку учащихся к сдаче ЕГЭ.
Развивающие:
- развивать познавательный интерес, реализуя межпредметные связи курсов химии и математики;
- развивать алгоритмический стиль мышления.
Воспитательные:
- продолжать формирование мотивации учебной деятельности, положительного отношения к знаниям;
- формировать информационную и коммуникативную культуру.
Оборудование. Компьютер, экран, мультимедийный проектор, презентация с алгоритмами решения задач на массовую долю вещества в растворе «методом стаканчиков», многовариантная проверочная работа с задачами трёх уровней сложности (10 вариантов), ключ к ответам.
Методы. Объяснительно-иллюстративный, репродуктивный.
План урока
1. Вводная часть:
– организационный момент;
– мотивация познавательной деятельности;
– сообщение темы и постановка целей урока.
2. Активизация знаний по теме «Массовая доля вещества в растворе».
3. Знакомство учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков».
4. Закрепление умения решать задачи на растворы и сплавы при помощи многовариантной проверочной работы с задачами трёх уровней сложности.
5. Самопроверка. Самооценка. Рефлексия.
6. Домашнее задание.
7. Подведение итогов.
Приложение 4
Ход урока
1. Вводная часть.
Проверка готовности класса к уроку, приветствие.
Учитель. У нас на уроке химии сегодня гости – это учителя математики. Как вы считаете, какая связь существует между учениками 11 класса, учителями математики и уроком химии?…. Да, это ЕГЭ по математике, в котором имеют место и химические задачи. С этими задачами вы уже встречались в 9 классе при сдаче экзаменов по химии и математике. А также умение решать эти задачи вам понадобится при подготовке к ЕГЭ по химии ( это задание В 9) и к ЕГЭ по математике (задание В 13). Поэтому закономерна тема нашего урока.
«Текстовые задачи: проценты, сплавы, растворы».
Далее учитель подводит учащихся к постановке целей урока.
- Повторить понятие массовой доли.
- Познакомиться с алгоритмом решения задач на растворы и сплавы методом стаканчиков».
- Отработать умение решать задачи на растворы и сплавы.
2. Активизация знаний по теме «Массовая доля вещества в растворе».
Как найти массу раствора?
– Надо сложить массу вещества и массу растворителя.
р-ра = т в-ва + т р-ля (запись на доске)т
Демонстрация приготовления раствора медного купороса (Приложение 1).
Что является основной характеристикой растворов?
– Массовая доля растворенного вещества.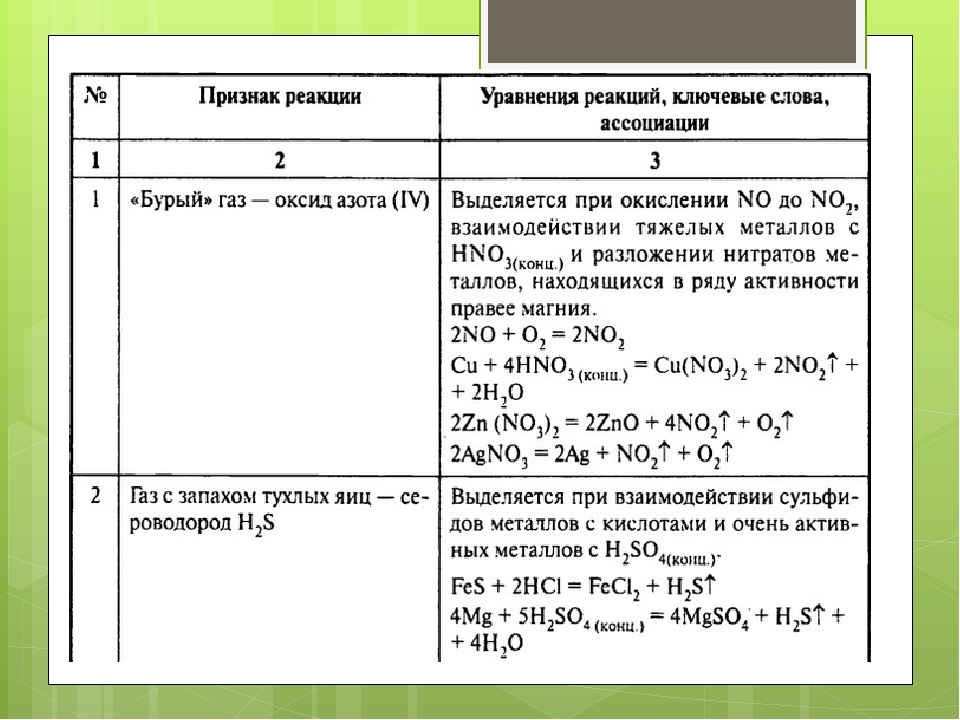
Как вычислить массовую долю?
– Надо найти отношение массы растворенного вещества к массе раствора.
ω = т в-ва : т р-ра ۰ 100% (запись на доске)
В каких единицах измерения выражается массовая доля вещества?
– В процентах или долях единицы.
Это основные теоретические сведения, необходимые для успешного решения задач на растворы и сплавы.
3. Знакомство учащихся с алгоритмом решения задач на растворы и сплавы «методом стаканчиков»
Схема и уравнение для решения задач с процентами.
Главное правило в задачах с растворами.
Решение задачи №1.
Составляется схема приготовления раствора. Затем составляется уравнение решается относительно х.
Решение задачи № 2.
Решение задачи №3.
Решение задачи №4.
4. Закрепление умения решать задачи на растворы и сплавы при помощи многовариант-ной проверочной работы с задачами трёх уровней сложности (Приложение 2).
5. Двое учащихся с заданием 3-го уровня работают у доски. Остальные выполняют решение задач на листочках самостоятельно. Ученики оценивают свою работу, сверив ответы с матрицей.
- За правильное решение задачи первого уровня – «3» .
- За правильное решение задачи второго уровня – «4».
- За правильное решение задач первого и второго уровня -«5».
- За правильное решение задачи третьего уровня –«5».
Матрица ответов для самопроверки.
Рефлексия.
6. Домашнее задание.
Поменяться с соседом вариантом и решить его дома.
7. Подведение итогов урока (Приложение 3).
Антошин А.Э. ЕГЭ-2021. Химия. Решение задач — Антошин А.Э. | 978-5-04-112812-8
Стоимость товара может отличаться от указанной на сайте!Наличие товара уточняйте в магазине или по телефону указанному ниже.
г. Липецк, пл.Плеханова, д. 7
8 (4742) 47-02-53
г. Богучар, ул. Дзержинского, д.4
8 (47366) 2-12-90
г. Воронеж, ул. Г. Лизюкова, д. 66 а
8 (473) 247-22-55
г.Поворино, ул.Советская, 87
8 (47376) 4-28-43
г. Воронеж, ул. Хользунова, д. 35
8 (473) 246-21-08
г. Старый Оскол, ул. Ленина, д. 22
22
8 (4725) 23-38-06
г. Воронеж, ул. Ростовская, д,58/24 ТЦ «Южный полюс»
8 (473) 280-22-42
г. Воронеж, ул. Пушкинская, 2
8 (473) 300-41-49
г. Липецк, ул.Стаханова,38 б
8 (4742) 78-68-01
г.Старый Оскол, мкр Олимпийский, д. 62
8 (4725) 39-00-10
г. Воронеж, Московский пр-т, д. 129/1
8 (473) 269-55-64
ТРЦ «Московский Проспект», 3-й этаж
г. Курск, ул. Щепкина, д. 4Б
8 (4712) 73-31-39
Экзамен по химическим реакциям1 и решения проблем
Экзамен по химическим реакциям1 и решения проблем
1. Остаток после химической реакции;
Остаток после химической реакции;
C 2 H 5 OH + O 2 → CO 2 + H 2 O
Решение:
C 2 H 5 OH + O 2 → CO 2 + H 2 O
У нас 2 атома углерода в реагентах, но 1 в продуктах.Итак, мы умножаем CO 2 на 2, чтобы уравновесить количество атомов C.
C 2 H 5 OH + O 2 → 2CO 2 + H 2 O
Теперь у нас есть 6 атомов H в реагентах, но 2 атома H в продуктах. Чтобы уравновесить их, умножаем H 2 O на 3.
.C 2 H 5 OH + O 2 → 2CO 2 + 3H 2 O
Наконец, мы уравновешиваем количество атомов O, чтобы уравновесить их, мы пишем 3 перед O 2 .
C 2 H 5 OH + 3O 2 → 2CO 2 + 3H 2 O
Все атомы в реагентах и продуктах уравновешены.
2. Если данная реакция сбалансирована; найти числа x, y и z в реагентах.
CxHy (OH) z + 5O 2 → 4CO 2 + 5H 2 O
Решение:
Поскольку реакция уравновешенная, количество атомов в обеих сторонах должно быть одинаковым.
CxHy (OH) z + 5O 2 → 4CO 2 + 5H 2 O
В товарах есть; 13 атомов O, в реагентах должно быть 13 атомов O. Но у нас 10, поэтому z должно быть 3.
В продуктах у нас есть 4 атома углерода, чтобы сбалансировать его, в реагентах должно быть 4, так что «x» равно 4.
C 4 Hy (OH) 3 + 5O 2 → 4CO 2 + 5H 2 O
В продуктах 10 атомов H, а в реагентах — 3. «y» должно быть 7, чтобы уравновесить количество атомов H с обеих сторон.Окончательная реакция;
C 4 H 7 (OH) 3 + 5O 2 → 4CO 2 + 5H 2 O
3. Найдите формулу соединения, обозначенного знаком «X», в следующей сбалансированной реакции.
Найдите формулу соединения, обозначенного знаком «X», в следующей сбалансированной реакции.
2I — + 2X + 4H +1 → I 2 + 2NO + 2H 2 O
Решение:
Мы должны проверить количество атомов с обеих сторон, чтобы найти формулу X.
В реагентах и продуктах есть 2 атома I, поэтому в X нет атома I.
В реагентах и продуктах 4 атома H, в X нет атома H.
В продуктах 2N атомов, но их нет в реагентах, поэтому в реагентах должно быть 2 N атомов.
Поскольку в продуктах 4 атома O, в реагентах должно быть 4 атома O.
X должен быть «NO 2 »
2I — + 2NO 2 + 4H +1 → I 2 + 2NO + 2H 2 O
Теперь мы должны сбалансировать количество зарядов с обеих сторон.
2I — + 2NO 2 + 4H +1 → I 2 + 2NO + 2H 2 O
2. (- 1) +2. (X) + 4. (+ 1) = 1,0 + 2,0 + 2,0
-2 + 2x + 4 = 0
x = -1, поэтому реакция становится;
2I — + 2НО 2 -1 + 4H +1 → I 2 + 2NO + 2H 2 O
и X = NO 2 -1
4. Какие из следующих реакций являются кислотно-основными?
И. N 2 (г) + 3H 2 (г) → 2NH 3 (г)
II. Mg (OH) 2 (т) + 2HCl (л) → MgCl2 (т) + 2h3O (л)
III. CH 4 (г) + 2O 2 (г) → CO 2 (г) + 2H 2 O (л)
Решение:
I. Это реакция синтеза или образования.
II. Mg (OH) 2 — основание, а HCl — кислота. Таким образом, это кислотно-основная реакция; образуются соль и вода.
III. Это реакция горения.
5. Какую из следующих пар можно записать вместо X и Y в приведенной ниже реакции;
X + Y → Соль + H 2 O
Решение:
X + Y → Salt + H 2 O — кислотно-основная реакция.Таким образом, X и Y должны быть кислотой и основанием или основанием и кислотой.
HCl + NaOH → NaCl + H 2 O
X Y
| Экзамены по химическим реакциям и решения проблем <Пред. | Далее> Экзамен по химическим реакциям2 и решения проблем |
|---|
Изучение химии: решения практических задач
решения практических вопросов- Раствор готовится путем смешивания 1,0 грамма бензола (C 6 H 6 ) в 100 г воды для создания раствора общим объемом 100 мл.Рассчитайте молярность, массу процент, мольная доля и моляльность бензола в растворе.
- Какой ион, по вашему мнению, будет более гидратирован?
- К + , Ca 2+
- На + , К +
- Cu 2+ , Cu +
- Предполагая, что парциальное давление CO 2 в воздухе над озером на уровне моря равно 4.0 х 10 -4 атм, какова равновесная концентрация CO 2 в озере при 25 o C? (Константа закона Генри 32 л . атм / моль)
- Коктейль был приготовлен путем смешивания 20,0 г этанола с 150 г воды при температуре 25 o ° C. вода имеет давление пара 23,76 торр. Каким будет новое давление пара?
- 10 граммов соли (NaCl) добавляют к 100 мл воды. Какие новые заморозки и
точки кипения? (К б =.
 51 o C кг / моль, K f = 0,1,86 o C
кг / моль)
51 o C кг / моль, K f = 0,1,86 o C
кг / моль) - Рассчитайте давление, необходимое для предотвращения осмоса при добавлении 10,0 г CaCl 2 на 100 мл воды?
Ответы
1.
молярность
(1,0 г бензола) / (78 г / моль) = 0,0128 моль бензола
(0,128 моль0 / (0,100 л) = 1,28 моль / литр
массовый процент
общая масса = 1.0 г бензола + 100 г воды = 101 г
1,0 грамм бензола / (общая масса)
1,0 г бенезина / 101 г * 100 = ,99% бензола
мольная доля
(1,0 г бензола) / (78 г / моль) = 0,0128 моль бензола
(100 г воды) / (16 г / моль) = 6,25 моль воды
(0,0128 моль бензола) / (0,0128 моль бензола + 6,25 моль воды) = ,20% бензола
моляльность
(1.0 г бензола) / (78 г / моль) = 0,0128 моль бензола
(0,0128 моль бензола) / (0,1 кг воды) = 1,28 моль / кг
2.
- Ca 2+ должен быть более гидратирован, потому что это более привлекательный усилие за счет надбавки, составляющей D H 3 подробнее отрицательный. D H 1 и D H 2 будут похожи, потому что это ионы одинакового размера.
- Na + должен быть более гидратирован, потому что это меньший ион, который будет уменьшить D H 1 и D H 2.
- Cu 2+ должен быть более гидратирован по тем же причинам, что и частично а.
3.
P CO2 = k CO2 C CO2
C CO2 = P CO2 / k CO2
C CO2 = 4,0 E -4 атм / 32 л атм / моль
C CO2 = 1,2 E -5 моль / л
4.
P = c растворитель P o
20 г этанола / 46 г / моль = 0,44 моль этанола
150 г воды / 16 г / моль = 9,4 моль воды
c растворитель = 9,4 моль воды / (9,4 моль воды + 0,44 моль воды). моль этанола)
c растворитель = 0,96
P = 0,96 * 23,76 мм рт. Ст. = 23 мм рт. Ст.
5.
м растворенное вещество = моль NaCl / кг воды
м растворенное вещество = (10 г / 58.5 г / моль) / .10 кг воды
м растворенное вещество = 1,7 моль / кг
T b = T o b + K b m растворенное вещество
T b = 100 + 0,51 * 1,7 * 2
T b = 102 o C
T f = T o f — K b m растворенное вещество
T f = 0 — 1.86 * 1,7 * 2
T f = -6,3 o C
Обратите внимание, что i в данном случае — 2
6.
1,0 г CaCl 2 / 111,0 г / моль = 0,00900 моль CaCl 2
0,00900 моль CaCl 2 / 0,100 L = 0,0900 M CaCl 2
p = i MRT
p = 3 * 0,0900 * 0,08206 * 298
p = 6,60 атм
Задания Домашняя страница UVic | Решение проблем: примеры к главе 2Мы используем четыре шага для решения проблем:
Примеры, приведенные ниже, являются ответами на вопросы в конце главы 2 ( Periodic Properties ) в вашей книге лекций. Прежде чем смотреть ответы модели, попробуйте задать вопросы самостоятельно. Когда вы застряли, воспроизведите фильм настолько, насколько вам нужно, чтобы продолжить. В конце каждого фильма дается полный ответ модели, так что вы также можете просто перейти к концу, чтобы узнать, правы ли вы. 1. Экранирование электронов | 2. Электронная конфигурация I | 3. Электронная конфигурация II | 4. Электронная конфигурация III | 5. Электронная конфигурация IV | 6. Эффективный ядерный заряд | 7. Периодическая таблица I | 8. Периодическая таблица II | 9. Периодические свойства
Химический факультет Университета Виктории.Обновлено 20 июня 2013 г. |
6.1.1: Практические проблемы — концентрация решения
ПРОБЛЕМА \ (\ PageIndex {1} \)
Объясните, что меняется, а что остается прежним, когда 1,00 л раствора NaCl разбавляется до 1,80 л.
- Ответ
Количество молей всегда остается неизменным в разбавлении.

Концентрация и объемы изменяются при разбавлении.
ПРОБЛЕМА \ (\ PageIndex {2} \)
Что означает, когда мы говорим, что образец объемом 200 мл и образец раствора соли объемом 400 мл имеют одинаковую молярность? В чем идентичность двух образцов? Чем отличаются эти два образца?
- Ответ
Два образца содержат одинаковое соотношение молей соли к литрам раствора, но имеют разное фактическое количество молей.
ПРОБЛЕМА \ (\ PageIndex {3} \)
Определите молярность для каждого из следующих растворов:
- 0,444 моль CoCl 2 в 0,654 л раствора
- 98,0 г фосфорной кислоты, H 3 PO 4 , в 1,00 л раствора
- 0,2074 г гидроксида кальция, Ca (OH) 2 , в 40,00 мл раствора
- 10,5 кг Na 2 SO 4 · 10H 2 O в 18.60 л раствора
- 7,0 × 10 −3 моль I 2 в 100,0 мл раствора
- 1,8 × 10 4 мг HCl в 0,075 л раствора
- Ответьте на
0,679 M
- Ответ b
1,00 M
- Ответ c
0,06998 М
- Ответ d
1.75 М
- Ответ e
0,070 M
- Ответ f
6,6 M
- Нажмите здесь, чтобы посмотреть видео о решении
ПРОБЛЕМА \ (\ PageIndex {4} \)
Определите молярность каждого из следующих растворов:
- 1.
 457 моль KCl в 1.500 л раствора
457 моль KCl в 1.500 л раствора - 0,515 г H 2 SO 4 в 1,00 л раствора
- 20,54 г Al (NO 3 ) 3 в 1575 мл раствора
- 2,76 кг CuSO 4 · 5H 2 O в 1,45 л раствора
- 0,005653 моль Br 2 в 10,00 мл раствора
- 0,000889 г глицина, C 2 H 5 NO 2 , в 1,05 мл раствора
- Ответьте на
0.9713 M
- Ответ b
5,25 × 10 -3 M
- Ответ c
6,122 × 10 -2 M
- Ответ d
7.62 M
- Ответ e
0.5653 M
- Ответ f
1.13 × 10 -2 М
ПРОБЛЕМА \ (\ PageIndex {5} \)
Рассчитайте количество молей и массу растворенного вещества в каждом из следующих растворов:
(а) 2,00 л 18,5 M H 2 SO 4 , концентрированная серная кислота
(б) 100,0 мл 3,8 × 10 −5 M NaCN, минимальная летальная концентрация цианида натрия в сыворотка крови
(c) 5,50 л 13,3 M H 2 CO, формальдегид, используемый для «фиксации» образцов ткани
(d) 325 мл 1.8 × 10 −6 M FeSO 4 , минимальная концентрация сульфата железа, определяемая по вкусу в питьевой воде
- Ответьте на
37,0 моль H 2 SO 4
3,63 × 10 3 г H 2 SO 4
- Ответ b
3.8 × 10 −6 моль NaCN
1,9 × 10 −4 г NaCN
- Ответ c
73.
 2 моль H 2 CO
2 моль H 2 CO2,20 кг H 2 CO
- Ответ d
5.9 × 10 −7 моль FeSO 4
8,9 × 10 −5 г FeSO 4
- Нажмите здесь, чтобы посмотреть видео о решении
ПРОБЛЕМА \ (\ PageIndex {6} \)
Рассчитайте молярность каждого из следующих растворов:
(а) 0.195 г холестерина, C 27 H 46 O, в 0,100 л сыворотки, средняя концентрация холестерина в сыворотке крови человека
(б) 4,25 г NH 3 в 0,500 л раствора, концентрация NH 3 в бытовом аммиаке
(c) 1,49 кг изопропилового спирта, C 3 H 7 OH, в 2,50 л раствора, концентрация изопропилового спирта в медицинском спирте
(d) 0,029 г I 2 в 0,100 л раствора, растворимость I 2 в воде при 20 ° C
- Ответьте на
5.04 × 10 −3 M
- Ответ b
0,499 М
- Ответ c
9.92 M
- Ответ d
1,1 × 10 −3 M
ПРОБЛЕМА \ (\ PageIndex {7} \)
В 1 г кальция содержится около 1,0 г кальция в виде Ca 2+ .0 л молока. Какова молярность Ca 2+ в молоке?
- Ответ
0,025 M
- Нажмите здесь, чтобы посмотреть видео о решении
ПРОБЛЕМА \ (\ PageIndex {8} \)
Какой объем раствора 1,00- M Fe (NO 3 ) 3 можно разбавить, чтобы приготовить 1,00 л раствора с концентрацией 0?250 M ?
- Ответ
0,250 л
ПРОБЛЕМА \ (\ PageIndex {9} \)
Если 0,1718 л раствора 0,3556- M C 3 H 7 OH разбавить до концентрации 0,1222 M , каков объем полученного раствора?
- Ответ
0,5000 л
- Нажмите здесь, чтобы посмотреть видео о решении
ПРОБЛЕМА \ (\ PageIndex {10} \)
Какой объем 0. 33- M C 12 H 22 O 11 раствор можно разбавить для приготовления 25 мл раствора с концентрацией 0,025 M ?
33- M C 12 H 22 O 11 раствор можно разбавить для приготовления 25 мл раствора с концентрацией 0,025 M ?
- Ответ
1,9 мл
ПРОБЛЕМА \ (\ PageIndex {11} \)
Какова концентрация раствора NaCl, которая получается, когда 0,150 л раствора 0,556- M дают испариться до тех пор, пока объем не уменьшится до 0,105 л?
- Ответ
0.794 M
- Щелкните здесь, чтобы просмотреть видео решения
ПРОБЛЕМА \ (\ PageIndex {12} \)
Какова молярность разбавленного раствора, когда каждый из следующих растворов разбавляется до заданного конечного объема?
- 1,00 л раствора Fe (NO 3 ) с концентрацией 0,250- M 3 разбавляют до конечного объема 2,00 л
- 0,5000 л раствора 0,1222- M C 3 H 7 OH разбавляют до конечного объема 1.250 л
- 2,35 л 0,350- M раствора H 3 PO 4 разбавляют до конечного объема 4,00 л
- 22,50 мл 0,025- M раствора C 12 H 22 O 11 разбавляют до 100,0 мл
- Ответьте на
0,125 М
- Ответ b
0,04888 M
- Ответ c
0.206 М
- Ответ d
0,0056 М
ПРОБЛЕМА \ (\ PageIndex {13} \)
Какова конечная концентрация полученного раствора, когда 225,5 мл 0,09988- M раствора Na 2 CO 3 дают испариться до тех пор, пока объем раствора не уменьшится до 45,00 мл?
- Ответ
0.
 5005 M
5005 M
- Нажмите здесь, чтобы посмотреть видео о решении
ПРОБЛЕМА \ (\ PageIndex {14} \)
Для лаборатории общей химии закуплен флакон объемом 2,00 л с раствором концентрированной HCl. Раствор содержал 868,8 г HCl. Какая молярность раствора?
- Ответ
11.9 M
ПРОБЛЕМА \ (\ PageIndex {15} \)
Эксперимент в лаборатории общей химии требует 2.00- M раствор HCl. Сколько мл 11,9 M HCl потребуется для получения 250 мл 2,00 M HCl?
- Ответ
42,0 мл
- Щелкните здесь, чтобы просмотреть видео решения
ПРОБЛЕМА \ (\ PageIndex {16} \)
Какой объем раствора 0,20- M K 2 SO 4 содержит 57 г K 2 SO 4 ?
- Ответ
1.6 л
ПРОБЛЕМА \ (\ PageIndex {17} \)
Агентство по охране окружающей среды США (EPA) устанавливает ограничения на количество токсичных веществ, которые могут сбрасываться в канализационную систему. Пределы были установлены для различных веществ, включая шестивалентный хром, который ограничен до 0,50 мг / л. Если промышленность выбрасывает шестивалентный хром в виде дихромата калия (K 2 Cr 2 O 7 ), какова максимально допустимая молярность этого вещества?
- Ответ
4.8 × 10 −6 M
- Нажмите здесь, чтобы посмотреть видео о решении
Химические решения практических задач | Carolina.com
1.
 Молярные растворы
Молярные растворыа. Опишите, как вы приготовили бы 1 л из 1 M раствор натрия хлорида. Вес хлорида натрия в граммах формулы составляет 58,44. г / моль.
Ответ: Сделать 1 М раствор натрия хлорид, растворить 58.44 г хлорида натрия в 500 мл воды в 1000 мл мерная колба. Когда все твердое вещество растворено и раствор находится при комнатной температуре. температуры, доведите до отметки и несколько раз переверните колбу для перемешивания.
г. Опишите, как вы приготовили бы 1 л из 2 M раствор уксусной кислоты. Граммовая формула веса уксусной кислоты составляет 60,05 г / моль, плотность 1.049 г / мл.
Ответ: Чтобы приготовить 2 М раствор уксусной кислоты, растворите 120,1 г уксусной кислоты в 500 мл дистиллированной или деионизированной воды в емкости объемом 1000 мл. мерная колба.Поскольку уксусная кислота является жидкостью, ее также можно измерить объем. Разделите массу кислоты на ее плотность (1,049 г / мл), чтобы определить объем (114 мл). Для приготовления раствора используйте 120,1 г или 114 мл уксусной кислоты. Осторожно покрутите колбу, чтобы перемешать раствор. Как только раствор будет в комнате температуры, доведите до отметки и несколько раз переверните колбу для перемешивания.
2. Процентные решения
а. Опишите, как бы вы приготовили 100 г 0,5% раствора. фенолфталеин по массе.
Ответ: Поскольку растворенное вещество (фенолфталеин) является твердое вещество, раствор в процентах по массе. Массовый процент означает количество граммов растворенного вещества на 100 г раствора.
массовый процент = (масса растворенного вещества / масса раствора) × 100%
масса растворенного вещества = массовый процент × масса раствора / 100%
= 0,5% x 100 г / 100%
= 0,5 г
Так как общая масса раствора равна 100 г, оставшиеся 99.5 г
раствор — вода. Для приготовления раствора растворите 0,5 г фенолфталеина.
в 99,5 г дистиллированной или деионизированной воды.
г. Опишите, как вы приготовили бы 100 мл раствор, содержащий 22% уксусную кислоту по объему.
Ответ: Объемный процент означает количество миллилитров растворенного вещества на 100 мл раствора. Разбавьте 22 мл уксусной кислоты дистиллированная или деионизированная вода для приготовления 100 мл раствора.
3. Разведения
а.Опишите, как приготовить 1,0 л 0,10 М раствора серной кислоты. кислота из 3,0 М раствора серной кислоты.
Ответ: Рассчитайте объем 3,0 М серной кислоты. кислота, необходимая для приготовления разведения.
M реагент × V реагент = M разбавление × V разбавление
3,0 M × V реагент = 0.10 М × 1,0 л
V реагент = 0,033 л = 33 мл
Медленно добавьте 33 мл 3,0 М серной кислоты в мерную колбу на 1000 мл. наполовину заполните дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать. Один раз раствор комнатной температуры, разбавить водой до метки и перевернуть колбу несколько раз перемешать.
б. Опишите, как бы вы приготовили 500 мл 0,25 М раствор гидроксида натрия из 5,0 М раствора гидроксида натрия.
Ответ: Рассчитать объем 5,0 М гидроксида натрия, необходимого для приготовления разведения.
M реагент × V реагент = M разбавление × V разбавление
5,0 M × V реагент = 0,25 M × 0,500 л
V реагент = 0.025 л = 25 мл
Медленно добавьте 25 мл 5,0 М гидроксида натрия в мерную колбу на 500 мл.
наполовину заполните дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать. Один раз
раствор комнатной температуры, разбавить водой до метки и перевернуть
колбу несколько раз перемешать.
4. Особые случаи
а. Опишите, как приготовить 500 мл 1,0 М раствора калия. хлорид с чистотой 93,0%. Вес хлорида калия в граммах формулы 74.56 г / моль.
Ответ: Рассчитайте массу нечистого хлорида калия. нужный.
масса нечистого хлорида калия = M чистый × V чистый × грамм формулы вес / процент чистота
= 1,0 M × 0,500 L × 74,56 г / моль
0,930= 40 г
Медленно добавьте 40 г 93% хлорида калия в мерную емкость 500 мл. колбу наполовину заполните дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать.Когда все твердое вещество растворится и раствор достигнет комнатной температуры, разбавьте до отметки и несколько раз переверните колбу для перемешивания.
г. Опишите, как бы вы готовились 500 мл 1,0 М раствора фосфорной кислоты из 85,0% фосфорной кислоты, т.е. чистый. Вес фосфорной кислоты по формуле в граммах составляет 98,00 г / моль, а плотность 85,0% фосфорной кислоты составляет 1,685 г / мл.
Ответ: Рассчитайте объем 85.Требуется 0% фосфорная кислота.
объем нечистой фосфорной кислоты = M чистый × V чистый × грамм формулы вес / (проценты чистота x плотность) = (1,0 M × 0,500 L x 98,00 г / моль) ÷ 1,685 г / мл
0,850= 34 мл
Медленно добавьте 34 мл 85,0% фосфорной кислоты в мерную емкость 500 мл. колбу наполовину заполните дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать. Как только раствор достигнет комнатной температуры, разбавьте водой до отметки и переверните колбу несколько раз, чтобы перемешать.
5. Нормальные решения
Опишите, как приготовить 1000 мл 1,0 н. Раствора магния. гидроксид. Граммовая формула веса гидроксида магния составляет 58,33 г / моль.
Ответ: Гидроксид магния.
содержит две гидроксильные группы. Половина моля гидроксида магния, следовательно, принимает один моль протонов. Чтобы приготовить 1,0 н раствор гидроксида магния, медленно добавьте 29 г гидроксида магния в 500-миллилитровую мерную колбу, заполненную наполовину. с дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать.Когда все твердое вещество растворяется и раствор при комнатной температуре доводится до метки. и несколько раз переверните колбу для перемешивания.
| Содержание | ||
| Состояния материи | Элементы, соединения и смеси | Жидкости |
| Решения | Координационные соединения | VSEPR |
| Как мне ее решить? | ||
| Атомные орбитали | Молекулярные орбитали бензола Pi | S N 2 Механизм реакции |
| Библиотека молекул | Библиотека кристаллической структуры | Благодарности |
| Спектроскопия | ||
| Колебательные моды малых молекул | 1 Спектры ЯМР Н малых молекул | |
| Номенклатура неорганических соединений (Drill & Practice) | ||
| Бинарные ионные соединения, содержащие ион металла с фиксированным зарядом (50 вопросов) | Гидратированные ионные соединения (20 вопросов) | Бинарные ковалентные соединения (50 вопросов) |
| Бинарные ионные соединения, содержащие ион металла с переменным зарядом (50 вопросов) | Ионные соединения, содержащие многоатомные ионы (70 вопросов) | |
| Инструменты | ||
| Использование звонка | Общие операции с использованием HyperChem | Периодическая таблица |
| Графики наименьших квадратов с использованием Microsoft Excel | Форматирование графиков с помощью Microsoft Excel | Общие операции с использованием Microsoft Excel |
10.
 10 экзаменов
10 экзаменов10.10 Введение в химическую инженерию
Осень 2002 г.
Exam 1 (PDF)
Exam 1 Solution — включая
точечная разбивка (PDF)
Экзамен 2 (PDF)
Экзамен 2 Решение (PDF)
Заключительный экзамен (PDF)
Окончательный экзамен Решение:
Задача 1:
Problem1script.m
Arrhenius.m
returns_zero_for_correct_T.m
бисс. М.
Проблема
2 (PDF)
Problem2script.м
кофе.м
событий.м
Задача 3
JetExamAnswer.m
Весна 2002
Образец
Экзамен 2
Решение
к образцу экзамена 2
Образец финала Экзамен
Осень 2002 г.
Домашнее задание 1 (PDF)Решение домашнего задания 1 (PDF)
Домашнее задание
2 (PDF)
Решение домашнего задания 2 (PDF)
Домашнее задание
3 (PDF)
Решение домашнего задания 3 (PDF)
Домашнее задание
4 (PDF)
Решение домашнего задания 4 (PDF)
Домашнее задание
5 (PDF)
Решение домашнего задания 5 (PDF)
Cv_RT_integral.м
Домашнее задание
6 (PDF)
Решение домашнего задания 6 (PDF)
M-файлы по части (а)
Cv_RT_integral.m
returns_zero_for_correctT.m
bisect_T.m
air_cools.m
M-файлы по части (b)
Метод 1:
returns_zero_for_correctT_b.m
bisect_T_b.m
Метод 2:
Cp_RT_integral.m
returns_zero_for_correctT_b2.m
bisect_T_b2.m
Домашнее задание
7 (PDF)
Решение домашнего задания 7 (PDF)
M-файлов:
hw7script.м
(Скрипт для выполнения всех остальных функций)
Shomate.m
(взято непосредственно из примеров
Страница)
бисс. М.
(взято непосредственно из примеров
Страница)
enthalpy_difference_a.m
enthalpy_difference_b.m
enthalpy_difference_c.m
enthalpy_difference_d.m
Домашнее задание
8 (PDF)
Решение домашнего задания 8
вых. м
м
Домашнее задание
9 (PDF)
Решение домашнего задания 9 (PDF)
Альтернативный
Решение, основанное на той же проблеме, было дано прошлой весной.
Номера задач не совпадают, но есть ответы
одинаковы, и это может дать вам другой способ взглянуть на это.
Также, hw9soln.m
это сценарий Matlab, который помещает все переменные потока аммиачного завода
и степень реакции в векторном формате.
Это будет очень полезно для начала домашнего задания
10.
Домашнее задание
10 (PDF)
Решение домашнего задания 10
хв10солн.м
Домашнее задание
11 (PDF)
hw11massbal.m
содержит уравнения сохранения массы для этой задачи, уже выраженные
в матричной форме.
Это должно помочь вам начать работу над решением
намного быстрее.
Решение домашнего задания 11
hw11soln.m
топливных ячеек. М
Домашнее задание
12 (PDF)
Усольве.м
— функция, которая решает уравнение Мартикс U * x = v, где U — верхний треугольник
матрица.
Он понадобится вам для решения домашнего задания 12.
Решение домашнего задания 12
хв12солн.м
Мацольве.м
RowReduce.m
Усольве.м
Домашнее задание 13 (PDF)
Домашнее задание
14 (PDF)
Решение домашнего задания 14
hw14soln.м
Домашнее задание 15 — Краткий отчет о бумажном испытании вертолета (см. Домашнее задание 13)
Домашнее задание
16 (PDF)
Решение домашнего задания 16
хв16солн.м
firstorderrxn.m
второй заказrxn.m
евро.м
Домашнее задание
17 (PDF)
Решение домашнего задания 17 (PDF)
хв17солн.м
масленкар.м
hotairballoon.m
hotairballoon_noheat.m
Домашнее задание
18 (PDF)
Решение домашнего задания 18
hw18soln.м
п.м.
Заключительный проект
Образец
Параметры для проверки вашей симуляции
Образец
сценарий оптимизации для создания графиков поверхностей и изолиний
последнее изменение: 29 января 2003 г.



 51 o C кг / моль, K f = 0,1,86 o C
кг / моль)
51 o C кг / моль, K f = 0,1,86 o C
кг / моль) Не думайте, что просто изучение этих задач — достаточная подготовка! Они представляют собой лишь небольшую выборку. Вам также следует попробовать задачи из MasteringChemistry, особенно примеры из руководства. Еще один полезный источник проблем — старые экзаменационные работы.
Не думайте, что просто изучение этих задач — достаточная подготовка! Они представляют собой лишь небольшую выборку. Вам также следует попробовать задачи из MasteringChemistry, особенно примеры из руководства. Еще один полезный источник проблем — старые экзаменационные работы.
 457 моль KCl в 1.500 л раствора
457 моль KCl в 1.500 л раствора 2 моль H 2 CO
2 моль H 2 CO 5005 M
5005 M содержит две гидроксильные группы. Половина моля гидроксида магния, следовательно,
принимает один моль протонов. Чтобы приготовить 1,0 н раствор гидроксида магния,
медленно добавьте 29 г гидроксида магния в 500-миллилитровую мерную колбу, заполненную наполовину.
с дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать.Когда все
твердое вещество растворяется и раствор при комнатной температуре доводится до метки.
и несколько раз переверните колбу для перемешивания.
содержит две гидроксильные группы. Половина моля гидроксида магния, следовательно,
принимает один моль протонов. Чтобы приготовить 1,0 н раствор гидроксида магния,
медленно добавьте 29 г гидроксида магния в 500-миллилитровую мерную колбу, заполненную наполовину.
с дистиллированной или деионизированной водой и встряхните колбу, чтобы перемешать.Когда все
твердое вещество растворяется и раствор при комнатной температуре доводится до метки.
и несколько раз переверните колбу для перемешивания.
Leave A Comment