[PDF] Билет — Free Download PDF
Download Билет…
Билет Блок А Выберите правильный ответ. А1. Чему равен заряд атома углерода? 1) 0; 2) +6; 3) +12; 4) −1. А2. Какой тип связи в молекуле HCl? 1) ионная; 2) водородная; 3) металлическая; 4) ковалентная полярная. А3. Наиболее выражены металлические свойства у атома: 1) лития; 2) натрия; 3) калия; 4) кальция. А4. Укажите вещество, в котором атом углерода имеет наибольшую степень окисления: 1) CCl4; 2) Ch5; 3) CHCl3; 4) HCOOH. А5. Бром – летучая жидкость с неприятным запахом. Кристаллическая решетка брома… 1) атомная; 2) молекулярная; 3) ионная; 4) металлическая. А6. Каким веществом надо подействовать на железо, чтобы получить хлорид железа (II)? 1) Cl2; 2) HCl; 3) ZnCl2; 4) KClO3. А7. Получение аммиака в промышленности основано на реакции: 1) Nh5NO3 + NaOH = NaNO3 + Nh4↑ + h3O 2) 3NaNO3 + 8Al + 5NaOH + 18h3O = 8Na[Al(OH)4] + 3Nh4↑ 3) 2NO2 + 7h3 = 2Nh4 + 4h3O 2NH 4) N 2 3H 2 3А8. Для системы: MgCO (т) 111,7 кДж MgO (т) CO2 3 выберите условия смещения равновесия в сторону поглощения CO2: 1) повышение температуры; 2) понижение температуры; 3) уменьшение концентрации CO2; 4) понижение давления. А9. Вещество, которое не является электролитом, имеет формулу: 1) NaOH; 2) NaCl; 3) (C2H5)2O; 4) Ch4COOH. А10. Наиболее выражены кислотные свойства у оксида: 1) MnO;
2) Mn2O3; 3) MnO2; 4) Mn2O7. А11. Наиболее экологически чистое топливо – это: 1) метан; 2) водород; 3) этанол; 4) керосин. А12. Реакцию аммиака с азотной кислотой относят к типу: 1) обмена; 2) разложения; 3) соединения; 4) замещения. А13. Кислотные свойства усиливаются в ряду: 1) HBr – HCl – HF 2) h4PO4 – h3SO4 – HClO4 3) HNO3 – h3CO3 – h4BO3 4) HNO3 – h4PO4 – h4AsO4 А14. В четырех сосудах содержится по одному литру перечисленных ниже веществ с концентрацией 1моль/л. Укажите, в каком растворе содержится больше всего ионов: 1) K2SO4; 2) KOH; 3) h4PO4; 4) C2H5OH. А15. Оцените правильность суждений о металлах: А. Химическая связь между атомами в неметаллах ковалентная неполярная.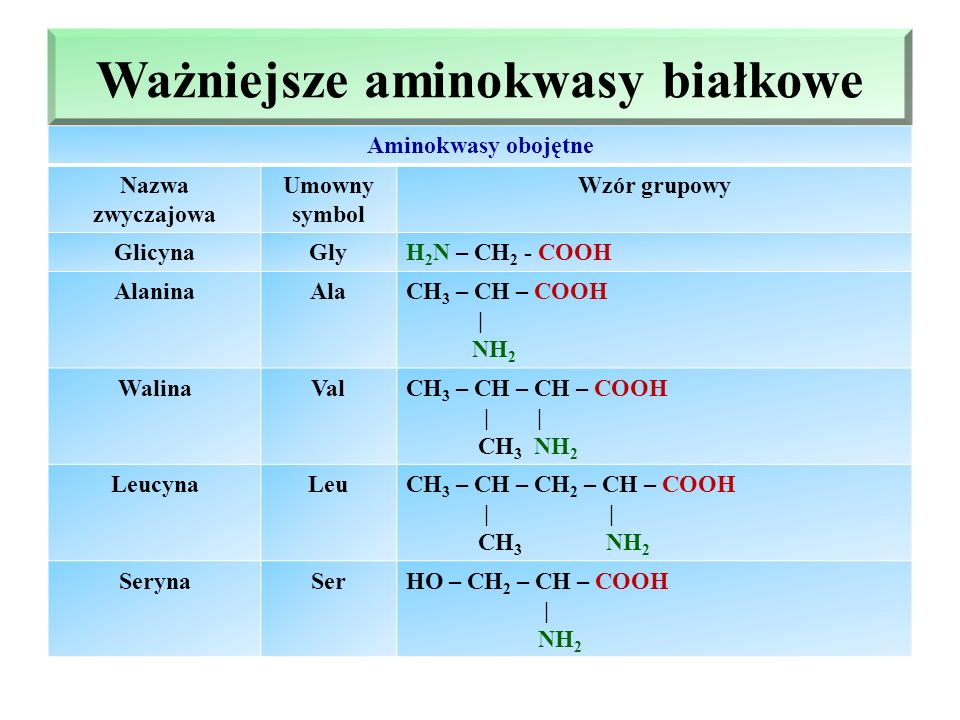
А20. Какое из перечисленных ароматических соединений обесцвечивает бромную воду? 1) C6H6; 2) C6H5NO2; 3) C6H5Cl; 4) C6H5 CH=Ch3. А21. Ацетилен и этин – это: 1) гомологи; 2) структурные изомеры; 3) геометрические изомеры; 4) одно и то же вещество. А22. С водородом в присутствии катализатора не реагирует: 1) бензол; 2) бутен; 3) толуол; 4) бутан. А23. Основной компонент природного газа: 1) CO2; 2) Ch5; 3) C6H6; 4) Nh4. А24. В схеме превращений: X
C2H5OH → C3H7COOC2H5 веществом «х» является: 1) пропиловый спирт; 2) масляная кислота; 3) пропан; 4) углекислый газ. А25. Изомерами являются: 1) пропан и пентан; 2) пропан и циклопропан; 3) пентан и пентен; 4) циклопропан и пропен. А26. Бензол, в отличие от гексана: 1) реагирует с хлором; 2) окисляется кислородом; 3) взаимодействует с бромметаном; 4) нитруется азотной кислотой. А27. Атом кислорода в молекуле фенола образует -связи в количестве: 1) одной; 2) двух; 3) трех; 4) четырех. А28. Взаимодействие этена с водой относится к реакциям: 1) этерификации; 2) присоединения; 3) дегидрогенизации; 4) замещения. А29. Сколько спиртов отвечает формуле C3H8O? 1) один; 2) два; 3) три; 4) пять.
А30. Для предельных углеводородов характерны реакции: 1) присоединения; 2) замещения; 3) полимеризации; 4) гидролиза. Блок В В1. Установите соответствие между названием неорганического соединения и классом, к которому оно принадлежит: Название соединения Класс соединений 1) углекислый газ А) средние соли 2) кальцинированная сода Б) кислые соли 3) пищевая сода В) основные соли 4) бромид гидроксомеди Г) кислоты Д) основания Е) оксиды В2. Установите соответствие между формулой вещества и классом органических соединений. Формула вещества Класс органических соединений 1) Ch4COOH А) сложный эфир 2) Ch4Ch3NO2 Б) карбоновая кислота O В) кетон 3) h3N Ch3 C OH Г) аминокислота 4)
Блок В В1. Установите соответствие между названием неорганического соединения и классом, к которому оно принадлежит: Название соединения Класс соединений 1) углекислый газ А) средние соли 2) кальцинированная сода Б) кислые соли 3) пищевая сода В) основные соли 4) бромид гидроксомеди Г) кислоты Д) основания Е) оксиды В2. Установите соответствие между формулой вещества и классом органических соединений. Формула вещества Класс органических соединений 1) Ch4COOH А) сложный эфир 2) Ch4Ch3NO2 Б) карбоновая кислота O В) кетон 3) h3N Ch3 C OH Г) аминокислота 4)
C
Ch4
O
Д) альдегид Е) нитросоединение В3. Установите соответствие между органическим веществом и продуктом его реакции с азотной кислотой: Формула вещества Формула продукта реакции 1) С6Н6 А) Ch4NO2 2) С2H6 Б) Ch4Nh4NO3 3) Ch4Nh3 В) C2H5NO2 4) C3H5 (OH)3 Г) C6H5 NO2 Д) C3H5 (ONO2) 3 В4. Установите соответствие между формулой вещества и продуктом, выделяющимся на катоде при электролизе водного раствора этого вещества: Формула вещества Катодный продукт 1) K3PO4 А) кислород 2) h3SO4 Б) только металл 3) CuCl2 В) только водород 4) NaHSO4 Г) металл и водород Д) сера Е) хлор В5. Установите соответствие между названием соли и средой ее водного раствора: Название соли Среда раствора 1) нитрит калия А) нейтральная 2) хлорацетат натрия Б) кислая
3) гидрокарбонат рубидия 4) сульфат алюминия
В) щелочная
В6. Установите соответствие между формулой соединения и степенью окисления, которую в этом соединении проявляет азот. Формула соединения Степень окисления 1) NaNO2 А) –3 2) Cr(NO3)3 Б) +2 3) N2O4 В) +3 4) (Nh5)2Cr2O7 Г) +4 Д) +5 В7. Среди перечисленных веществ укажите те, которые можно получить брожением глюкозы: А) фруктоза Б) Ch4OH В) C2H5OH Г) Ch4CH(OH)COOH Д) сахароза Е) CO2 В8. По термохимическому уравнению синтеза аммиака N 2 3H 2 2Nh4 92кДж 3 Рассчитайте, сколько теплоты выделится при образовании 1м аммиака (н.у.). В9. К 20 г раствора нитрата меди с массовой долей 5% добавили 5 г этой же соли и 5 г воды.
Nh4 → X1 → NO2
→
T
X2 → Cu(NO3)2 → X3
С3. Напишите уравнения реакций, с помощью которых можно осуществить превращения: 1
2
3
4
5
C2h5 → C2H5Cl → C2H5OH → C2H5Cl → C4h20 → Ch4COOH C4. Массовые доли углерода, водорода и кислорода в некотором веществе равны соответственно 40,0; 6,67 и 53,33%. Плотность паров этого вещества по водороду равна 30. Установите молекулярную формулу вещества. С5. Сероводород объемом 0,112 л (н.у.) пропустили через 90 г раствора бромида меди с массовой долей последнего 8%. Рассчитайте массовую долю бромида меди в полученном после этого растворе.
ОТВЕТЫ Блок А Вопрос А1 А2 А3 А4 А5 А6 А7 А8 А9 А10
Ответ 1 4 3 1 2 2 4 2 3 4
Вопрос А11 А12 А13 А14 А15 А16 А17 А18 А19 А20
Ответ 2 3 2 1 3 2 4 4 4 4
Вопрос А21 А22 А23 А24 А25 А26 А27 А28 А29 А30
Ответ 4 4 2 2 4 3 2 2 2 2
Блок В Вопрос В1 В2 В3 В4 В5 В6 В7 В8 В9
В10
Ответ 1-Е, 2-А, 3-Б, 4-В 1-Б, 2-Е, 3-Г, 4-В 1-Г, 2-В, 3-Б, 4-Д 1-В, 2-В, 3-Б, 4-В 1-В, 2-В, 3-В, 4-Б 1-В, 2-Д, 3-Г, 4-А В, Г, Е Решение: 44,8 л – 92 кДж 1000 л – х х=2054 кДж Решение: 20 0,05 5 100% 20% 20 10 (С2H5OH)=0,1 моль С2H5OH + 3O2 2CO2 +3h3O 1 моль С2H5OH – 3 моль O2 0,1 моль С2H5OH – х моль O2 x = 0,3 моль O2 =22,40,3=6,72 л
Блок С С1. 5h3SO4 (к) + 4Zn h3S + 4ZnSO4 + 4h3O +2
2e
Zn
S + 8e
S
Zn +6
2
4 1
Zn – восстановитель h3SO4 – окислитель С2. Pt, T
1) 4Nh4 + 5O2 4NO + 6h3O 2) 2NO + O2 2 NO2
3) 4NO2 + O2 +2h3O = 4HNO3 4) 4HNO3 (к) + Cu = Cu(NO3)2 + 2NO2 + 2h3O или 8HNO3 (р) + 3Cu = 3Cu(NO3)2 + 2NO + 4h3O T
5) 2Cu(NO3)2 = 2CuO +4NO2 + O2 C3.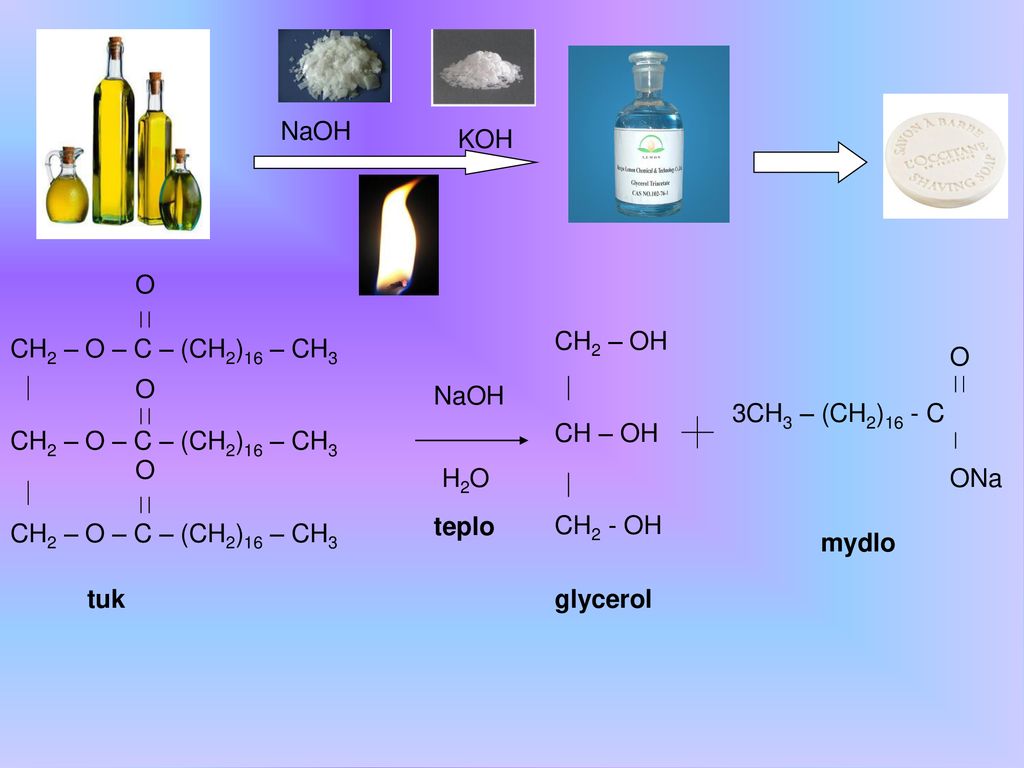
1) C2h5 + HCl C2H5Cl 2) C2H5Cl + KOH C2H5OH + KCl (водн. р-р)
h3SO4
3) C2H5OH + HCl
C2H5Cl + h3O
T
4) C2H5Cl + 2Na C4h20 + 2NaCl P, kat
5) 2 C4h20 + 5O2 4Ch4COOH + 2h3O C4. Число моль атомов данных элементов относятся друг к другу как: 40 6,67 53,33 : : (C) : (H) : (O) = = 3,33 : 6,67 : 3,33 = 1 : 2 : 1 12 1 16 Следовательно, простейшая формула вещества: Ch3O Молекулярная масса вещества: Mr = 2 30 = 60 Истинная формула: C2h5O2 C5. h3S
+
M=34 г/моль
h3S =
CuBr2 CuS M=223,5 г/моль M=95,5 г/моль
0,112 0,005 моль 22,4
(CuBr2) =
+
2HBr
90 0,08 0,0322моль 223,5
(CuBr2) осталось = 0,0322 – 0,005 = 0,0272 моль (CuBr2) =
mCuBr2 6,0792 100% 6,78% 100% = mH 2S mCuBr2 mCuS 0,005 34 90 95,5 0,027
АДУ АРМ — Хатолик
АДУ АРМ — ХатоликCDbConnection failed to open the DB connection: SQLSTATE[HY000] [2002] Попытка установить соединение была безуспешной, т.к. от другого компьютера за требуемое время не получен нужный отклик, или было разорвано уже установленное соединение из-за неверного отклика уже подключенного компьютера. (D:\VHosts\kutubxona.adu.uz\framework\db\CDbConnection.php:382)
#0 D:\VHosts\kutubxona.adu.uz\framework\db\CDbConnection.php(330): CDbConnection->open()
#1 D:\VHosts\kutubxona.adu.uz\framework\db\CDbConnection.php(308): CDbConnection->setActive(true)
#2 D:\VHosts\kutubxona.adu.uz\framework\base\CModule.php(387): CDbConnection->init()
#3 D:\VHosts\kutubxona.adu.uz\framework\base\CApplication.php(450): CModule->getComponent('db')
#4 D:\VHosts\kutubxona.adu.uz\framework\db\ar\CActiveRecord.php(674): CApplication->getDb()
#5 D:\VHosts\kutubxona.adu.uz\framework\db\ar\CActiveRecord.php(707): CActiveRecord->getDbConnection()
#6 D:\VHosts\kutubxona.adu.uz\framework\db\ar\CActiveRecord.php(1509): CActiveRecord->getCommandBuilder()
#7 D:\VHosts\kutubxona.adu. uz\themes\classic\views\layouts\main.php(19): CActiveRecord->findAll()
#8 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(126): require('D:\\VHosts\\kutub...')
#9 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(95): CBaseController->renderInternal('D:\\VHosts\\kutub...', Array, true)
#10 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(76): CBaseController->renderFile('D:\\VHosts\\kutub...', Array, true)
#11 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(54): CContentDecorator->decorate('
uz\themes\classic\views\layouts\main.php(19): CActiveRecord->findAll()
#8 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(126): require('D:\\VHosts\\kutub...')
#9 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(95): CBaseController->renderInternal('D:\\VHosts\\kutub...', Array, true)
#10 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(76): CBaseController->renderFile('D:\\VHosts\\kutub...', Array, true)
#11 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(54): CContentDecorator->decorate('run()
#14 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(300): CBaseController->endWidget('CContentDecorat...')
#15 D:\VHosts\kutubxona.adu.uz\themes\classic\views\layouts\column1.php(6): CBaseController->endContent()
#16 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(126): require('D:\\VHosts\\kutub...')
#17 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(95): CBaseController->renderInternal('D:\\VHosts\\kutub...', Array, true)
#18 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(784): CBaseController->renderFile('D:\\VHosts\\kutub...', Array, true)
#19 D:\VHosts\kutubxona.adu.uz\protected\controllers\SiteController.php(181): CController->render('error', Array)
#20 D:\VHosts\kutubxona.adu.uz\framework\web\actions\CInlineAction.php(49): SiteController->actionError()
#21 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(308): CInlineAction->runWithParams(Array)
#22 D:\VHosts\kutubxona.adu.uz\framework\web\filters\CFilterChain.php(133): CController->runAction(Object(CInlineAction))
#23 D:\VHosts\kutubxona.adu.uz\framework\web\filters\CFilter.php(40): CFilterChain->run()
#24 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(1145): CFilter->filter(Object(CFilterChain))
#25 D:\VHosts\kutubxona.adu.uz\framework\web\filters\CInlineFilter.php(58): CController->filterAccessControl(Object(CFilterChain))
#26 D:\VHosts\kutubxona. adu.uz\framework\web\filters\CFilterChain.php(130): CInlineFilter->filter(Object(CFilterChain))
#27 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(291): CFilterChain->run()
#28 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(265): CController->runActionWithFilters(Object(CInlineAction), Array)
#29 D:\VHosts\kutubxona.adu.uz\framework\web\CWebApplication.php(282): CController->run('error')
#30 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(331): CWebApplication->runController('site/error')
#31 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(204): CErrorHandler->render('error', Array)
#32 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(129): CErrorHandler->handleException(Object(CHttpException))
#33 D:\VHosts\kutubxona.adu.uz\framework\base\CApplication.php(732): CErrorHandler->handle(Object(CExceptionEvent))
#34 [internal function]: CApplication->handleException(Object(CHttpException))
#35 {main}
adu.uz\framework\web\filters\CFilterChain.php(130): CInlineFilter->filter(Object(CFilterChain))
#27 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(291): CFilterChain->run()
#28 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(265): CController->runActionWithFilters(Object(CInlineAction), Array)
#29 D:\VHosts\kutubxona.adu.uz\framework\web\CWebApplication.php(282): CController->run('error')
#30 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(331): CWebApplication->runController('site/error')
#31 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(204): CErrorHandler->render('error', Array)
#32 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(129): CErrorHandler->handleException(Object(CHttpException))
#33 D:\VHosts\kutubxona.adu.uz\framework\base\CApplication.php(732): CErrorHandler->handle(Object(CExceptionEvent))
#34 [internal function]: CApplication->handleException(Object(CHttpException))
#35 {main}
Тест. Ароматические углеводороды. Гомологический ряд, изомерия
© 2020, ООО КОМПЭДУ, http://compedu.ru При поддержке проекта http://videouroki.net
Будьте внимательны! У Вас есть 10 минут на прохождение теста. Система оценивания — 5 балльная. Разбалловка теста — 3,4,5 баллов, в зависимости от сложности вопроса. Порядок заданий и вариантов ответов в тесте случайный. С допущенными ошибками и верными ответами можно будет ознакомиться после прохождения теста. Удачи!Список вопросов теста
Вопрос 1
Охарактеризуйте вещество строения
Варианты ответов
- гомолог бензола
- изомер кумола
- называется 1, 4-диметилбензол
- в молекуле 18 связей σ-типа
Вопрос 2
Гомологи бензола — это:
Варианты ответов
- винилбензол
- бромбензол
- изопропилбензол
- 1, 2-диметилбензол
Вопрос 3
Чему равно число изомерных диметилпроизводных бензола?
Вопрос 4
В каких парах оба вещества по отношению друг к другу являются гомологами?
Варианты ответов
- стирол и бензол
- толуол и бензол
- толуол и этилбензол
- бутилбензол и 1, 2, 3, 4-тетраметилбензол
Вопрос 5
Толуол отличается от бензола:
Варианты ответов
- числом электронов в π-системе
- химической активностью в реакциях замещения в бензольном кольце
- числом σ-связей в молекуле
- молярной массой
Вопрос 6
Укажите молярную массу гомолога бензола (г/моль), в молекуле которого содержится 7 атомов углерода.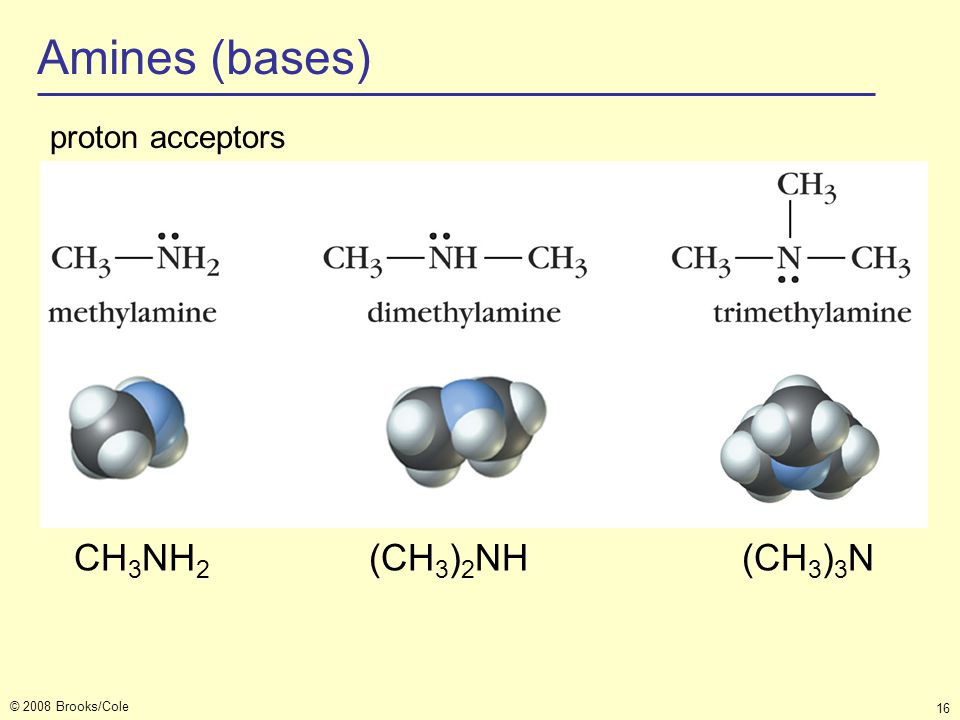
Вопрос 7
В молекуле бензола сформированы:
Варианты ответов
- три π-связи
- шесть σ-связей
- одна шестиэлектронная π-система
- двенадцать σ-связей
Вопрос 8
В каких парах оба вещества являются изомерами по отношению друг к другу?
Варианты ответов
- 1, 2-диметилбензол и 1, 4-диметилбензол
- 1-метил-3-этилбензол и пропилбензол
- винилбензол и этилбензол
- кумол и пропилбензол
Вопрос 9
Отметьте формулу фенильной группы:
Варианты ответов
CH2 = CH —
C6H5CH2 —
C6H5 —
H3C — C6H4 —
Вопрос 10
Гомологам бензола могут отвечать формулы:
Варианты ответов
C6H5Cl
C7H8
С8H10
C6H6O
Строение внешнего электронного ✅ уровня калий
Объяснение:
1. Строение внешнего электронного уровня алюминия:
Строение внешнего электронного уровня алюминия:
а) 3s23p4 б) 2s22p1 в) 3s23p1 г) 3s23p2
2.Молекулярную кристаллическую решётку имеет:
а) бромид кальция б) лёд в) алмаз г) графит
3.Экзотермической реакцией является:
а) разложение карбоната кальция;
б) взаимодействие азота с кислородом;
в) взаимодействие цинка с соляной кислотой;
г) взаимодействие меди с кислородом.
4.Гидроксид цинка, хлорид бария, гидрокарбонат натрия – это соответственно:
а) основание, кислая соль, основная соль;
б) амфотерный гидроксид, основная соль, кислая соль;
в) щёлочь, средняя соль, основная соль;
г) амфотерный гидроксид, средняя соль, кислая соль.
5.Для вытеснения меди из водного раствора её соли нельзя использовать:
а) серебро б) железо в) свинец г) цинк
6.Найдите формулу дигидрофосфата натрия:
а) Na2HPO4 б) NaHCO3 в) Na3PO4 г)Nah3PO4
7.Степень окисления +5 азот имеет в соединении:
а) Nh5Cl б)HNO2 в) KNO3 г)NO2
8.На состояние химического равновесия не влияет:
а) концентрация б) катализатор в) температура г) давление
9.Водородным соединением кремния является:
а) силан б) метан в) фосфин г) аммиак
10.Изомером бутена является:
а) 2-метилпропан б) циклобутан в) бутин-1 г) 2-метилбутен-1
11.Бромную воду обесцвечивает:
а) бензол б) метан в) этилен г) этан
12.Формула метанола:
а) Ch4NO2 б) Ch4OH в) C2H5OH г) Ch4Nh3
13.Как фенол, так и спирты реагируют с:
а) Na б) NaOH в) HCl г)Br2
14.Функциональная группа — СО — называется:
а) карбоксильной б) карбонильной в) гидроксильной г) альдегидной
15.Каким реагентом нужно подействовать на нитросоединение, чтобы превратить его в амин?
а) кислородом б) хлороводородом в) бромом г) водородом
16 Как анилин, так и аминоуксусная кислота реагируют с:
а) HCl б) NaOH в) Br2 г)NaCl
17.Напишите молекулярное, полное и сокращённое ионное уравнение реакции:
Fe(ОН)3 + 3НNO3 = Fe(NO3)3 + 3h3O
Fe(OH)3 + 3H⁺ + 3NO3⁻ = Fe³⁺ + 3NO3⁻ + 3h3O
Fe(OH)3 + 3H⁺ = Fe³⁺ + 3h3O
18.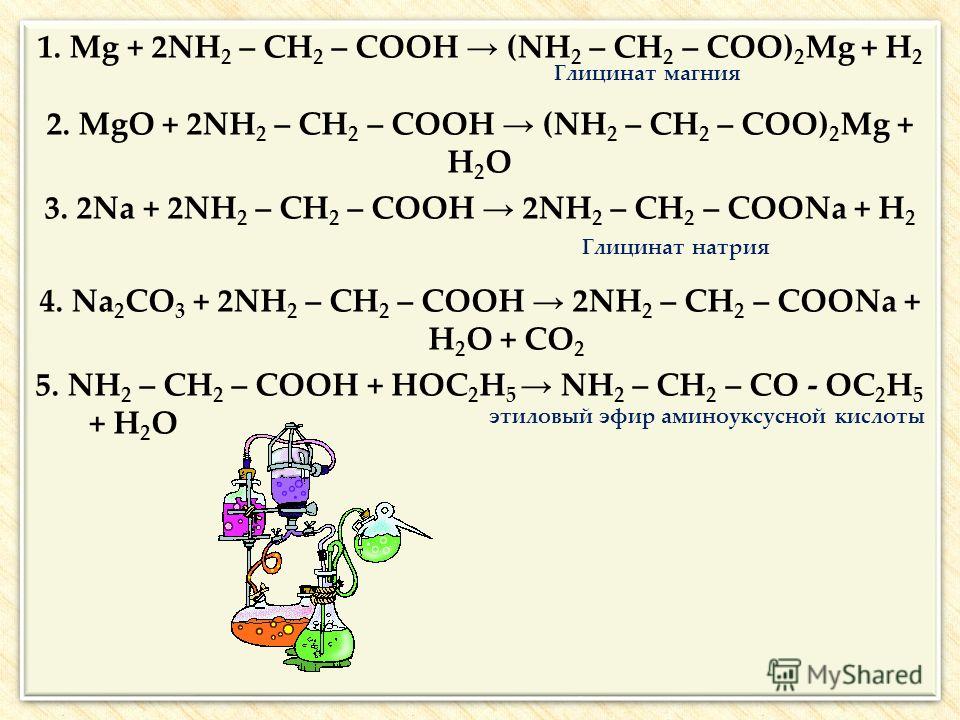 Для реакции: KClO3 + Р → KCl + Р2O5 составьте уравнение электронного баланса.
Для реакции: KClO3 + Р → KCl + Р2O5 составьте уравнение электронного баланса.
+5 0 -1 +5
5 KClO3 + 6Р →5 KCl + 3Р2O5
Cl+5 +6e = Cl-1 восстановление, Cl+5 — окислитель║5
2P(0) — 10e = P₂(+5) окисление, Р- восстановитель║3
Поставьте коэффициенты, уравнивающие реакцию. Укажите в уравнении эл. баланса
окислитель, восстановитель, процесс окисления и восстановления.
19.Напишите уравнение гидролиза силиката калия.
K2SiO3 + HOH ⇔ KOH + KHSiO3
2K⁺ + SiO3²⁻ + HOH ⇔ K⁺ + OH⁻ + K⁺ + HSiO3⁻
SiO3²⁻ + HOH ⇔ + OH⁻ + HSiO3⁻
В результате гидролиза в растворе появляются гидроксид-ионы и реакция раствора становится щелочной ( рН > 7)
Объяснение:
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г.,
браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.

- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с вашим системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Заключительный отчет: Химия элементов основной группы в сфере хранения и активации водорода (Технический отчет)
Диксон, Дэвид А., и Ардуенго, III, Энтони Дж. Заключительный отчет: Химия элементов основной группы на службе хранения и активации водорода . США: Н. П., 2010.
Интернет. DOI: 10,2172 / 989180.
Диксон, Дэвид А. и Ардуенго, III, Энтони Дж. Заключительный отчет: Химия элементов основной группы в сфере хранения и активации водорода . Соединенные Штаты. https://doi.org/10.2172/989180
Диксон, Дэвид А. и Ардуенго, III, Энтони Дж. Чт.
«Итоговый отчет: химия элементов основной группы в сфере хранения и активации водорода». Соединенные Штаты. https://doi.org/10.2172/989180. https: //www.osti.гов / сервлеты / изнаночная / 989180.
и Ардуенго, III, Энтони Дж. Чт.
«Итоговый отчет: химия элементов основной группы в сфере хранения и активации водорода». Соединенные Штаты. https://doi.org/10.2172/989180. https: //www.osti.гов / сервлеты / изнаночная / 989180.
@article {osti_989180,
title = {Итоговый отчет: химия элементов основной группы на службе хранения и активации водорода},
author = {Диксон, Дэвид А. и Ардуенго, III, Энтони Дж.},
abstractNote = {Замена сжигания углеродсодержащего топлива альтернативными источниками энергии, оказывающими минимальное воздействие на окружающую среду, является одной из важнейших научных и технологических задач начала 21 века.Не только критически важно улавливать энергию из новых возобновляемых источников, но также необходимо эффективно и эффективно хранить захваченную энергию для использования в точке обслуживания, когда и где она необходима, которая не может быть совмещена с местом сбора. Есть много потенциальных носителей информации, но мы сосредоточены на хранении энергии в химических связях. Более эффективно хранить энергию в расчете на массу в химических связях. Это связано с тем, что без использования химических связей сложно упаковать электроны в небольшие объемы с малым весом.В центре внимания проекта была разработка нового химического состава, чтобы позволить Министерству энергетики достичь своих технических целей по хранению водорода с использованием химических систем хранения водорода. Мы предоставили поддержку вычислительной химии с точки зрения термодинамики, кинетики и предсказания свойств в поддержку экспериментальных усилий Центра передового опыта Министерства энергетики в области химического хранения водорода. Целью центра является хранение энергии в химических связях с участием атомов водорода. Как только водород хранится в наборе связей X-H / Y-H, водород должен легко высвобождаться, а истощенное топливо регенерировать очень эффективно.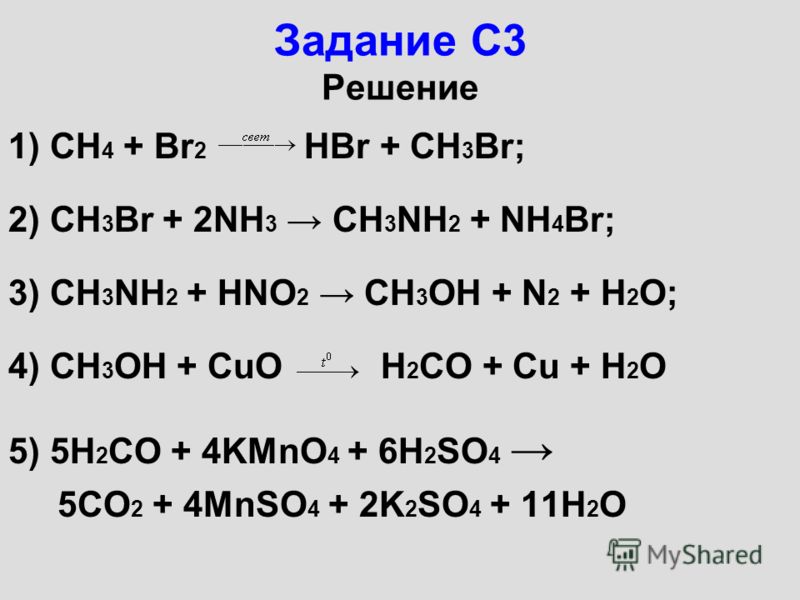 Это существенно отличается от нашего нынешнего использования источников энергии на ископаемом топливе, где реагент преобразуется в энергию плюс CO2 (уголь) или CO2 и h3O (бензин, природный газ), которые выбрасываются в атмосферу. В будущих сценариях хранения энергии отработанное топливо будет улавливаться, а среда для хранения энергии регенерироваться. Это накладывает существенные дополнительные ограничения на химию. Целью работы в области вычислительной химии было сокращение времени на разработку новых материалов и разработку материалов, которые соответствуют целям Министерства энергетики на 2010 и 2015 годы с точки зрения массового процента, объема, времени высвобождения и способности к регенерации.Эта цель была достигнута с точки зрения сокращения количества дорогостоящих экспериментов и помощи в сосредоточении экспериментальных усилий на потенциально оптимальных целях. Мы использовали подходы вычислительной химии для предсказания термодинамических свойств широкого спектра соединений, содержащих бор, азот, водород и другие элементы, в том числе углерод. Эти расчеты в большинстве случаев были выполнены с помощью методов теории молекулярных орбиталей высокого уровня, которые имеют небольшие погрешности порядка ± 1-2 ккал / моль.Результаты были использованы для тестирования более приближенных методов, таких как теория функционала плотности, для более крупных систем и для разработки баз данных. Мы предсказали надежную термодинамику для тысяч соединений для схем выделения и регенерации, чтобы помочь / направить дизайн материалов, а также процесс проектирования и моделирования. Это первые надежные вычисленные значения для этих соединений, и для многих они являются единственными доступными значениями. В целом, результаты расчетов позволили нам по-новому взглянуть на химию основных групп и химических водородных систем на основе органических соединений, от выделения водорода до регенерации отработавшего топлива.В этом проекте также был сделан ряд экспериментальных достижений.
Это существенно отличается от нашего нынешнего использования источников энергии на ископаемом топливе, где реагент преобразуется в энергию плюс CO2 (уголь) или CO2 и h3O (бензин, природный газ), которые выбрасываются в атмосферу. В будущих сценариях хранения энергии отработанное топливо будет улавливаться, а среда для хранения энергии регенерироваться. Это накладывает существенные дополнительные ограничения на химию. Целью работы в области вычислительной химии было сокращение времени на разработку новых материалов и разработку материалов, которые соответствуют целям Министерства энергетики на 2010 и 2015 годы с точки зрения массового процента, объема, времени высвобождения и способности к регенерации.Эта цель была достигнута с точки зрения сокращения количества дорогостоящих экспериментов и помощи в сосредоточении экспериментальных усилий на потенциально оптимальных целях. Мы использовали подходы вычислительной химии для предсказания термодинамических свойств широкого спектра соединений, содержащих бор, азот, водород и другие элементы, в том числе углерод. Эти расчеты в большинстве случаев были выполнены с помощью методов теории молекулярных орбиталей высокого уровня, которые имеют небольшие погрешности порядка ± 1-2 ккал / моль.Результаты были использованы для тестирования более приближенных методов, таких как теория функционала плотности, для более крупных систем и для разработки баз данных. Мы предсказали надежную термодинамику для тысяч соединений для схем выделения и регенерации, чтобы помочь / направить дизайн материалов, а также процесс проектирования и моделирования. Это первые надежные вычисленные значения для этих соединений, и для многих они являются единственными доступными значениями. В целом, результаты расчетов позволили нам по-новому взглянуть на химию основных групп и химических водородных систем на основе органических соединений, от выделения водорода до регенерации отработавшего топлива.В этом проекте также был сделан ряд экспериментальных достижений. Экспериментальная работа над материалами для хранения водорода была сосредоточена на активированных поляризованных каркасах с σ- или π-связями, которые обладают потенциалом для активации, поглощения и, в конечном итоге, высвобождения дигидрогена. С этой целью было синтезировано и исследовано большое количество нетрадиционных валентных систем, включая карбены, цианоуглероды, системы C-B и B-N. В ходе этих исследований важную роль сыграла новая валентность класса стабильных органических синглетных бирадикальных систем.Стратегия синтеза «бесконечного» полимера-накопителя водорода была разработана на основе нашей химии цианоуглерода. Ключевой проблемой синтетических усилий была возможность связать кинетику высвобождения с размером заместителей, поскольку было трудно разработать молекулу с низкой молекулярной массой с правильной кинетикой. Был разработан новый процесс активации водородом, который показал, что пары кислота-основание Льюиса не должны «нарушаться» в их реакционной способности по отношению к активации h3. Реакция может происходить при температуре до -80 ºC.Мы установили, что взаимодействие h3 с электрофилом является ключевым этапом в процессе активации.},
Экспериментальная работа над материалами для хранения водорода была сосредоточена на активированных поляризованных каркасах с σ- или π-связями, которые обладают потенциалом для активации, поглощения и, в конечном итоге, высвобождения дигидрогена. С этой целью было синтезировано и исследовано большое количество нетрадиционных валентных систем, включая карбены, цианоуглероды, системы C-B и B-N. В ходе этих исследований важную роль сыграла новая валентность класса стабильных органических синглетных бирадикальных систем.Стратегия синтеза «бесконечного» полимера-накопителя водорода была разработана на основе нашей химии цианоуглерода. Ключевой проблемой синтетических усилий была возможность связать кинетику высвобождения с размером заместителей, поскольку было трудно разработать молекулу с низкой молекулярной массой с правильной кинетикой. Был разработан новый процесс активации водородом, который показал, что пары кислота-основание Льюиса не должны «нарушаться» в их реакционной способности по отношению к активации h3. Реакция может происходить при температуре до -80 ºC.Мы установили, что взаимодействие h3 с электрофилом является ключевым этапом в процессе активации.},
doi = {10.2172 / 989180},
url = {https://www.osti.gov/biblio/989180},
journal = {},
number =,
объем =,
place = {United States},
год = {2010},
месяц = {9}
}
новых реакционных путей, участвующих в электронно-индуцированном разложении твердого нитрометана (Ch4NO2) и D3-нитрометана (CD3NO2)
Радиационно-индуцированная химическая обработка метанола и льдов метанол-монооксид углерода при 5.В этом исследовании сообщается о воздействии ионизирующего излучения в форме энергичных электронов на 5 К и последующей запрограммированной десорбции. Эндогенное образование сложных органических молекул отслеживалось онлайн и in situ с помощью инфракрасной спектроскопии в твердом состоянии и после облучения с температурно-программируемой десорбцией (TPD) с использованием высокочувствительной рефлектронной времяпролетной масс-спектрометрии (ReTOF) в сочетании с однократной фотоионизацией при 10,49 эВ.

 uz\themes\classic\views\layouts\main.php(19): CActiveRecord->findAll()
#8 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(126): require('D:\\VHosts\\kutub...')
#9 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(95): CBaseController->renderInternal('D:\\VHosts\\kutub...', Array, true)
#10 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(76): CBaseController->renderFile('D:\\VHosts\\kutub...', Array, true)
#11 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(54): CContentDecorator->decorate('
uz\themes\classic\views\layouts\main.php(19): CActiveRecord->findAll()
#8 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(126): require('D:\\VHosts\\kutub...')
#9 D:\VHosts\kutubxona.adu.uz\framework\web\CBaseController.php(95): CBaseController->renderInternal('D:\\VHosts\\kutub...', Array, true)
#10 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(76): CBaseController->renderFile('D:\\VHosts\\kutub...', Array, true)
#11 D:\VHosts\kutubxona.adu.uz\framework\web\widgets\CContentDecorator.php(54): CContentDecorator->decorate(' adu.uz\framework\web\filters\CFilterChain.php(130): CInlineFilter->filter(Object(CFilterChain))
#27 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(291): CFilterChain->run()
#28 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(265): CController->runActionWithFilters(Object(CInlineAction), Array)
#29 D:\VHosts\kutubxona.adu.uz\framework\web\CWebApplication.php(282): CController->run('error')
#30 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(331): CWebApplication->runController('site/error')
#31 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(204): CErrorHandler->render('error', Array)
#32 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(129): CErrorHandler->handleException(Object(CHttpException))
#33 D:\VHosts\kutubxona.adu.uz\framework\base\CApplication.php(732): CErrorHandler->handle(Object(CExceptionEvent))
#34 [internal function]: CApplication->handleException(Object(CHttpException))
#35 {main}
adu.uz\framework\web\filters\CFilterChain.php(130): CInlineFilter->filter(Object(CFilterChain))
#27 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(291): CFilterChain->run()
#28 D:\VHosts\kutubxona.adu.uz\framework\web\CController.php(265): CController->runActionWithFilters(Object(CInlineAction), Array)
#29 D:\VHosts\kutubxona.adu.uz\framework\web\CWebApplication.php(282): CController->run('error')
#30 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(331): CWebApplication->runController('site/error')
#31 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(204): CErrorHandler->render('error', Array)
#32 D:\VHosts\kutubxona.adu.uz\framework\base\CErrorHandler.php(129): CErrorHandler->handleException(Object(CHttpException))
#33 D:\VHosts\kutubxona.adu.uz\framework\base\CApplication.php(732): CErrorHandler->handle(Object(CExceptionEvent))
#34 [internal function]: CApplication->handleException(Object(CHttpException))
#35 {main}
Leave A Comment