4 А7. В каком ряду химические элементы расположены в порядке усиления металлических свойств? 1) Na, Мg, А1 3) Са, Мg, Ве 2)А1, Мg, Nа 4) Мg, Ве, Са
1) 2,24 л 2) 6,72 л 3) 8,96 л 4) 11,2 л. 1) F- 2) Ca2+ 3) P+5 4) Br- 1) Sr, Ca, Mg 2) Mg, Al, Si 3) Mg, Al, Ca 4) F, Cl, Br
Вариант демо14 стр. 1 из 9 Тест по химии Демонстрационный вариант 2014 г. ИНСТРУКЦИЯ Тест состоит из частей А и В. На его выполнение отводится 120 минут. Задания рекомендуем выполнять по порядку. Если
ПодробнееБанк заданий 11 класс химия
Банк заданий 11 класс химия 1. Электронная конфигурация соответствует иону: 2. Одинаковую кофигурацию имеют частицы и и и и 3. Сходную конфигурацию внешнего энергетического уровня имеют атомы магния и
ID_589 1/6 neznaika.pro
Вариант 1 Часть 1. При выполнении заданий 1 15 укажите только одну цифру, которая соответствует номеру правильного ответа. 1 Четыре электрона находятся во внешнем электронном слое атомов каждого из химических
ПодробнееДЕПАРТАМЕНТ ОБРАЗОВАНИЯ ГОР. МОСКВЫ
ДЕПАРТАМЕНТ ОБРАЗОВАНИЯ ГОР. МОСКВЫ Федеральное государственное автономное образовательное учреждение высшего профессионального образования «НАЦИОНАЛЬНЫЙ ИССЛЕДОВАТЕЛЬСКИЙ ТЕХНОЛОГИЧЕСКИЙ УНИВЕРСИТЕТ «МИСиС»
Зачет по теме «Химическая связь» 11класс
Зачет по теме «Химическая связь» 11класс 1. В аммиаке и хлориде бария химическая связь соответственно 1) ионная и ковалентная полярная 2) ковалентная полярная и ионная 3) ковалентная неполярная и металлическая
В аммиаке и хлориде бария химическая связь соответственно 1) ионная и ковалентная полярная 2) ковалентная полярная и ионная 3) ковалентная неполярная и металлическая
Банк заданий химия 9 класс
Банк заданий химия 9 класс 1. Элемент имеет три электрона на 2-м энергетическом уровне. Порядковый номер элемента 3 5 7 13 2. Сколько электронов находится на внешнем уровне элемента с порядковым номером
Часть 3 С3. Часть 3 С4
ШИФР Часть 1 Часть 2 С1 С2 С3 С4 С5 С6 Итоговый балл (из 100 баллов) Вступительная работа для поступающих в 10 ФХ и ХБ классы Часть 1 Обведите номер одного правильного ответа кружком. При правильном ответе
ПодробнееЭкзаменационная работа
Экзаменационная работа для проведения государственной (итоговой) аттестации выпускников IX классов общеобразовательных учреждений 2008 года (в новой форме) по ХИМИИ Демонстрационный вариант 2008 года Район
1) IV 2) V 3) VI 4) VII
2 1. В ряду: Na Mg Al Si 1) увеличивается число энергетических уровней в атомах 2) усиливаются металлические свойства элементов 3) уменьшается высшая степень окисления элементов 4) ослабевают металлические
ПодробнееВарианты контрольных работ по «Химии»
Варианты контрольных работ по «Химии» Задание к контрольной работе составлено в 4 вариантах. Студент должен выполнить работу по варианту, номер которого соответствует начальной букве фамилии. Вариант 1
Подробнее Банк заданий по химии 10 класс
Банк заданий по химии 10 класс 1. С каждым из указанных веществ: хлороводород, водород, бромная вода будет реагировать пропан метан этан этилен 5) ацетилен 2. При выполнении задания из предложенного перечня
При выполнении задания из предложенного перечня
ID_591 1/6 neznaika.pro
Вариант 3 Часть 1. При выполнении заданий 1 15 укажите только одну цифру, которая соответствует номеру правильного ответа. 1 На приведенном рисунке 1 изображен модель атома 1) кремния 2) серы 3) кислорода
ID_590 1/7 neznaika.pro
Вариант 2 Часть 1. При выполнении заданий 1 15 укажите только одну цифру, которая соответствует номеру правильного ответа. 1 Химический элемент, в атомах которого распределение электронов по слоям: 2,
Подробнее1) 2 2) 0 3) +4 4) +6
Химия Демонстрационный вариант 2015 г. (стр. 1 из 5) Тест по химии 6 Демонстрационный вариант 2015 г. ИНСТРУКЦИЯ Тест состоит из 30 заданий. На его выполнение отводится 120 минут. Задания рекомендуем выполнять
ПодробнееID_593 1/8 neznaika.pro
Вариант 5 Часть 1. При выполнении заданий 1 15 укажите только одну цифру, которая соответствует номеру правильного ответа. 1 Химическому элементу, в атоме которого распределение электронов по слоям 2е,
ПодробнееПояснительная записка
Пояснительная записка Рабочая тетрадь рекомендована для студентов очной формы обучения, реализующих образовательную программу среднего (полного) общего образования технического профиля. Данная рабочая
ПодробнееВариант 1. Желаем успеха
Федеральное агентство по рыболовству Федеральное государственное бюджетное образовательное учреждение высшего профессионального образования «Астраханский государственный технический университет» Разработка
2018/2019 учебный год
УТВЕРЖДЕНО Приказ Министра образования Республики Беларусь 03.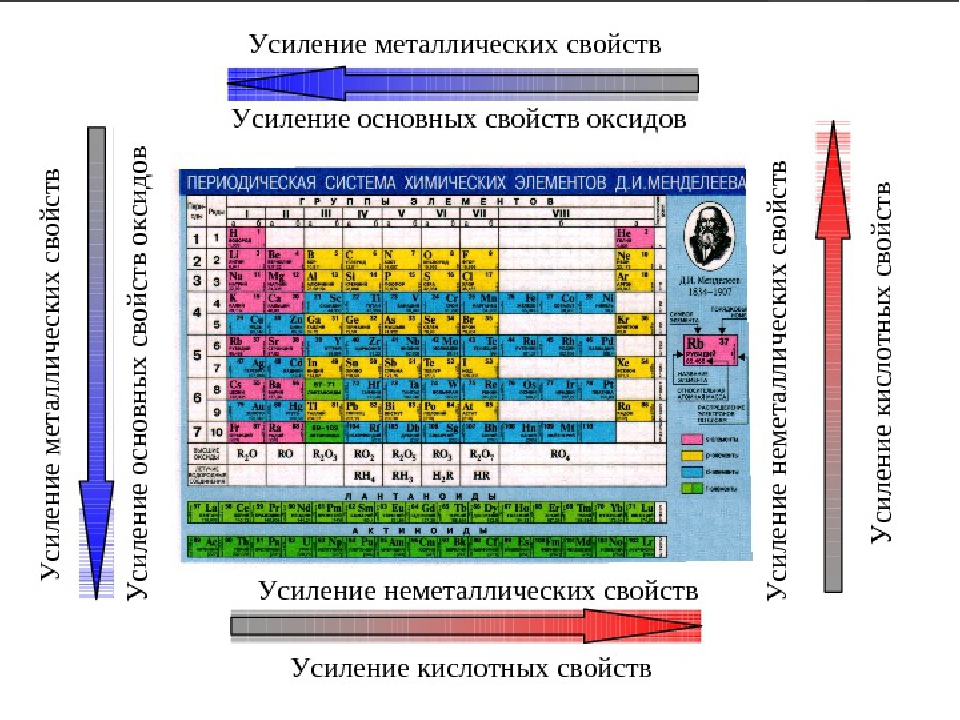 12.2018 836 Билеты для проведения экзамена в порядке экстерната при освоении содержания образовательной программы среднего образования по учебному
12.2018 836 Билеты для проведения экзамена в порядке экстерната при освоении содержания образовательной программы среднего образования по учебному
Демонстрационный вариант
Демонстрационный вариант Ссылка на вариант: https://bingoschool.ru/ege/chemistry/variants/demo/ Часть 1 1. 1) Na 2) K 3) Si 4) Mg 5) C Определите, атомы каких из указанных в ряду элементов в основном состоянии
ПодробнееФОНД ОЦЕНОЧНЫХ СРЕДСТВ
Муниципальное бюджетное общеобразовательное учреждение «Средняя общеобразовательная школа 1» Приложение 2 к ООП ООО ФОНД ОЦЕНОЧНЫХ СРЕДСТВ по текущей аттестации предмет: Химия. 9 класс Составители: Домнарева
Подробнеес. Веселая Лопань, 2015 год
Муниципальное общеобразовательное учреждение «Веселолопанская средняя общеобразовательная школа Белгородского района Белгородской области» Контрольное тестирование по химии 9 класс (промежуточный контроль)
Промежуточный контроль по химии в 9классе
Промежуточный контроль 9 класс
1 вариант.
Часть А
А1. (2 балла) В каком ряду химические элементы расположены в порядке увеличения радиуса атома?
1) K, Na, Li. 2) F, O, N. 3) P, S, Cl. 4) Ca, Mg, Be.
А2. (2 балла) В каком ряду химические элементы расположены в порядке усиления металлических свойств?
1) Na→ Mg → Al. 2) K → Na → Li 3) Ca→ Mg → Be 4) Al → Mg → Na
А3. (2 балла) В каком ряду химические элементы расположены в порядке усиления неметаллических свойств?
1) P → S → Cl 2) N → P → As 3) O → S → Se 4) S → P → Si
А4. (2 балла) В ряду оксидов MgO → Al2O3 → SiO2 свойства изменяются от
1) кислотных к амфотерным 2) амфотерных к основным
3) основных к кислотным 4) кислотных к основным
А5. (2 балла) В соединениях FeCl3 и Fe(OH)2 степени окисления железа, соответственно, равны:
(2 балла) В соединениях FeCl3 и Fe(OH)2 степени окисления железа, соответственно, равны:
1) +3 и +2 2) +2 и +2 3) +3 и +3 4) +3 и 0
А6. (2 балла) Сумма коэффициентов в уравнении реакции между оксидом натрия и серной кислотой равна
1) 7 2) 5 3) 6 4) 4
А7. (2 балла) Какие вещества образуются при взаимодействии цинка с разбавленной серной кислотой?
1) сульфат цинка, вода и оксид серы (IV) 2) сульфат цинка и водород
3) сульфит цинка и водород 4) сульфид цинка и вода
А8. (2 балла) Взаимодействие раствора серной кислоты с магнием относится к реакциям
1) соединения 2) замещения 3) разложения 4) обмена
А9. (2 балла) Осадок не образуется при смешивании растворов
1) гидроксида натрия и нитрата железа (II) 2) сульфата калия и гидроксида натрия
3) силиката калия и соляной кислоты 4) карбоната калия и хлорида кальция
А10. (2 балла) Выберите верную запись правой части уравнения реакции натрия с водой.
1) →2 NaOH + H2 2) → NaOH + H2
3) → 2 NaOH + H2O 4) → Na2O + H2
Часть В
В1. (4 балла) В ряду элементов Be – Mg – Ca
1) уменьшается радиус атомов
2) возрастает способность атомов отдавать электроны
3) увеличиваются заряды ядер атомов
4) уменьшается относительная атомная масса
5) увеличивается степень окисления в высших гидроксидах
В2. (4 балла) В реакцию с магнием вступают растворы:
1) K2SO4 2) Cu(NO3)2 3) Ba(OH)2 4) CaCl2 5) H2SO4
В3. (6 балла) Установите соответствие между исходными веществами и продуктами реакции
Исходные вещества Продукты реакции
А) Ca(OH)2 + SO3 1) CuSO4 + H2O
Б) Ca(OH)2 + H2SO4 2) CaSO4 + H2O
В) H2S + Ba(OH)2 3) CaSO3 + H2
4) Ba(HS)2 + H2O
5) CuSO4 +H2
Часть С
С1. (9 балла) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
(9 балла) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
СuO → X → Cu(NO3)2 → Cu(OH)2
С2. (7 балла) Вычислить объем оксида углерода (IV) (при н. у.), который может быть поглощен гидроксидом кальция, массой 160 г, содержащим 7,5% массовой доли примесей.
Промежуточный контроль 9 класс
2 вариант
А1. (2 балла) В каком ряду химические элементы расположены в порядке увеличения радиуса атома?
1) В, С, N 2) Br, Cl, F 3) O, S, Se 4) Ca, Mg, Be
А2. (2 балла) В каком ряду химические элементы расположены в порядке усиления металлических свойств?
1) Al → Si → P 2) B → Be → Li 3) Ca → Mg → Be 4) K → Na → Li
А3. (2 балла) В каком ряду химические элементы расположены в порядке усиления неметаллических свойств?
1) N→ P→As 2) Al→Si→P 3) O→S→Se 4) Cl→S→P
А4. (2 балла) В ряду оксидов Al2O3 → SiO2 → P2O5 свойства изменяются от
1) амфотерных к кислотным 2) основных к кислотным
3) амфотерных к основным 4) кислотных к основным
А5. (2 балла) В соединениях FeCl2 и Fe2(SO4)3 степени окисления железа, соответственно, равны:
1) +2 и +3 2) +2 и +2 3) +3 и +3 4) +3 и +6
А6. (2 балла) Сумма коэффициентов в уравнении реакции между алюминием и соляной кислотой равна
1) 13 2) 11 3) 12 4) 10
А7. (2 балла) При взаимодействии алюминия с разбавленной соляной кислотой образуются вещества формулы которых
1) AlН3 и H2 2) AlH3 и Cl2 3) AlCl3 и H2 4) AlСl3 и Cl2
А8. (2 балла) Взаимодействие раствора гидроксида натрия с фосфорной кислотой относится к реакциям
1) соединения 2) замещения 3) разложения 4) обмена
А 9. (2 балла) Осадок не образуется при смешивании растворов
1) хлорида натрия и нитрата меди(II) 2) сульфата калия и гидроксида бария
3) карбоната магния и фосфорной кислоты 4) фосфата калия и хлорида бария
А10. (2 балла) Выберите верную запись правой части уравнения реакции кальция с водой.
(2 балла) Выберите верную запись правой части уравнения реакции кальция с водой.
1) →Ca(OH)2 + H2
2) → CaO + H2
3) → CaH2 + O2
4) → Ca(OH)2
Часть В
В1. (4 балла) В ряду элементов Al – Mg – Na
1. уменьшается радиус атомов
2. усиливаются металлические свойства
3. уменьшаются заряды ядер атомов
4. увеличивается число электронов во внешнем электронном слое атомов
5. увеличивается число электронных слоев в атомах
В2. (4 балла) В реакцию с железом вступают растворы:
1) K2SO4 2) Hg(NO3)2 3) Ba(OH)2 4) CaCl2 5) HCl
В3. (6 балла) Установите соответствие между исходными веществами и продуктами реакции
Исходные вещества Продукты реакции
А) AgNO3 +BaCl2 1) Ba(NO3)2 +AgCl
Б) Ba(NO3)2 +H2SO4 2) BaSO4 +H2
В) Na2CO3 +HCl 3) BaSO4 +HNO3
4) NaCl+H2O+C
5) NaCl+H2O+CO2
Часть С
С1. (9 балла) Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Хлорид алюминия → Гидроксид алюминия →X →Алюминат натрия
С2. (7 балла) К 80 г раствора с массовой долей гидроксида натрия 5% добавили избыток раствора сульфата меди (II). Определите массу выпавшего осадка.
Ключи.
Вариант1
А1
А2
А3
А4
А5
А6
А7
А8
А9
А10
В1
В2
В3
2
4
1
3
1
4
2
2
2
1
2, 3
2, 5
224
С1
СuO → X → Cu(NO3)2 → Cu(OH)2
СuO + H2SO4 = CuSO4 + H2O x — CuSO4
CuSO4 + Ba(NO3)2 = Cu(NO3)2 + BaSO4
Cu(NO3)2 + 2 NaOH = Cu(OH)2 + NaNO3
С2.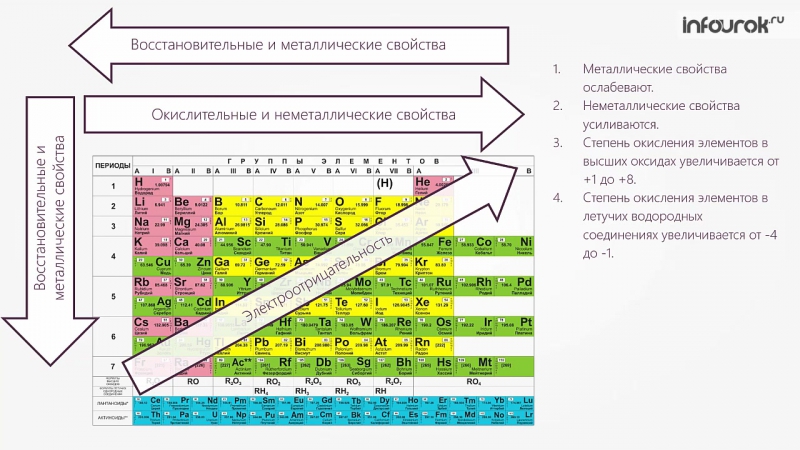
Дано:
m (Ca(OH)2) = 160/ 100 х 92,5 = 148г
m (Ca(OH)2) = 160г
148г V -?
w(прим) = 7,5%
Ca(OH)2 + CO2 = CaCO3 + H2O
Найти:
n = 1моль n = 1моль
V(CO2) — ?
M = 74г/моль VМ = 22,4л/моль
m =74г V = 22,4 л
148/74 = х/22,4
х = 44,8л
Ответ: 44,8 л
Вариант 2
А1
А2
А3
А4
А5
А6
А7
А8
А9
А10
В1
В2
В3
3
2
2
1
1
1
3
4
1
1
23
25
135
С1.
AlCl3 → Al(OH)3 → X → NaAlO2
AlCl3 + 3NaOH = 3NaCl + Al(OH)3
2Al(OH)3 = Al2O3 + 3H2O Х — Al2O3
Al2O3 + 2 NaOH = 2 NaAlO2 + H2O
С2.
Дано:
m (NaOH) = 80/ 100 х 5 = 4г
m (раст) = 80г
m = 4г m -?
w(NaOH) = 5%
2NaOH + CuSO4 = Na2SO4 + Cu(OH)2
Найти:
n = 2моль n = 1моль
m (CO2) — ?
M = 40г/моль M = 98г/моль
m =80г m =98г
4/80 = х/98
х = 4,9 г
Ответ: 4,9 г
Оценивание работы.
Часть А — каждое задание по 2 баллу — 20 баллов
Часть В — 14 баллов
В1 — 4 балла
В2 — 4 балла
В3 — 6 балла
Часть С —16 баллов
С1 — 9 баллов
С2 — 7 баллов
Итого: — 50 баллов
Оценка:
«5» — 88 –100 % ( 44 – 50 баллов)
«4» — 62 – 87 % ( 31 – 43 балла)
«3» — 36 – 61 % (18 – 30 баллов)
«2» — 0 – 35 % (0 – 17 баллов)
Задания а 2 Закономерности изменения химических свойств элементов и их соединений по периодам и группам
Задания А 2
Закономерности
изменения химических свойств элементов
и их соединений по периодам и группам.
Усиление металлических свойств простых веществ происходит в ряду:
Ba – Ca – Be 2) Ca – Ba – Be 3) Ba – Be – Ca 4) Be – Ca – Ba
В ряду элементов Cs – K – Li возрастает:
восстановительная способность простых веществ 3) электроотрицательность
радиус атома 4) химическая активность простых веществ
Основные свойства наиболее выражены у оксида:
натрия 2) калия 3) магния 4) бериллия
Металлические свойства усиливаются в ряду:
Ca – Mg – Be 2) Ca – Sr – Rb 3) Al – Mg – Be 4) Ba – Na – Li
Неметаллические свойства наиболее выражены у элемента:
Si 2) Ge 3) P 4) As
В порядке возрастания атомных радиусов расположены элементы:
F – Cl – Br 2) K – Ca – Mg 3) Na – Mg – Al 4) Ba – Be – Li
Кислотные свойства гидроксидов усиливаются в ряду:
H2SeO4 – HBrO4 – HClO4 2) HBrO4 – H2SeO4 – HClO4 3) H2SeO4 – HClO4– HBrO4
HClO4– HBrO4 – H2SeO4
Наиболее сильным основанием является:
NaOH 2) RbOH 3) KOH 4) LiOH
Наиболее активным металлом четвертого периода является:
калий 2) кальций 3) железо 4) германий
Наиболее сильные основные свойства проявляет водородное соединение:
CH4 2) PH3 3) NH3 4) H2O
В ряду элементов Сs – Rb – K – Na увеличивается:
число энергетических уровней 3) число валентных электронов
атомный радиус 4) электроотрицательность
В каком ряду вещества расположены в порядке увеличения металлических свойств?
Na, Mg, Al 2) Mg, Ca, Sr 3) Rb, Ca, Na 4) Ca, Mg, Be
В каком ряду простые вещества расположены в порядке уменьшения металлических свойств?
Sr, Ba, Ca 2) Na, K, Rb 3) Mg, Ca, Sr 4) Al, Mg, Na
Металлические свойства усиливаются в ряду веществ:
натрий – магний – алюминий 3) кальций – стронций – барий
рубидий – калий – натрий 4) кальций – магний – бериллий
При увеличении порядкового номера элемента неметаллические свойства:
усиливаются 2) ослабевают 3) не изменяются 4) изменяются периодически
Основные свойства летучих водородных соединений элементов VА группы Периодической системы химических элементов с увеличением порядкового номера химического элемента:
изменяются периодически 2) усиливаются 3) не изменяются 4) ослабевают
Восстановительные свойства металлов в главной подгруппе с увеличением порядкового номера элемента:
убывают 2) не изменяются 3) возрастают 4) сначала возрастают, затем убывают.

Радиусы атомов элементов, расположенных в третьем периоде ПСХЭ Д.И.Менделеева:
меняются периодически 2) увеличиваются 3) не изменяются 4) уменьшаются
Электроотрицательность в ряду Na – Mg – Al
не изменяется 2) уменьшается 3) увеличивается 4) сначала уменьшается, затем увеличивается.
Химический элемент расположен в третьем периоде и IIIА подгруппе ПСХЭ. Его гидроксид:
основный 2) амфотерный 3) безразличный 4) кислотный
Высший гидроксид хрома
проявляет кислотные свойства 3) проявляет амфотерные свойства
проявляет основные свойства 4) не проявляет кислотно-основных свойств
Высшие оксиды элементов VА группы ПСХЭ Д.И.Менделеева являются:
кислотными 2) основными 3) амфотерными 4) несолеобразующими
Формула высшего гидроксида мышьяка:
As2O3 2) As2O5 3) HAsO2 4) H3AsO4
Бром – это элемент:
Главной подгруппы IV группы 3) главной подгруппы VII группы
побочной подгруппы IVгруппы 4) побочной подгруппы VII группы
В периоде с увеличением порядкового номера элемента химические свойства оксидов меняются в ряду:
Основный, амфотерный, кислотный 3) кислотный, амфотерный, основный
Амфотерный, кислотный, основный 4) основный, кислотный, амфотерный
Радиус иона увеличивается в ряду:
Na+, Mg2+, Al3+ 2) Na+, K+, Rb+ 3) Br– , Cl–, F– 4) N3–, O2–, F–
Электроотрицательность элементов увеличивается в ряду:
F, Cl, Br 2) Na, K, Rb 3) Be, Mg, Ca 4) P, S, Cl
Электроотрицательность элементов уменьшается в ряду:
N, P, As 2) N, O, F 3) Li, Be, B 4) Se, S, O
В третьем периоде с увеличением порядкового номера элементов химические свойства гидроксидов, отвечающих высшей степени окисления, изменяются соответственно:
Основание, амфотерный гидроксид, кислота 3) кислота, амфотерный гидроксид, основание
Амфотерный гидроксид, основание, кислота 4) основание, кислота, амфотерный гидроксид
Радиус иона уменьшается в ряду:
1) Na+, Mg2+, Al3+ 2) Mg2+, Сa2+, Sr2+ 3) O2–, S2–, Se2– 4) F–, O2–, N3–
Электроотрицательность элементов уменьшается в ряду:
1)Li, Be, B 2) Na, K, Rb 3) Ca, Mg, Be 4) P, S, Cl
Неметаллические свойства элементов увеличиваются в ряду:
N, P, As 2) N, O, F 3) Li, Na, K 4) O, S, Se
В каком ряду элементы расположены в порядке усиления металлических свойств:
Si, P, S 2) F, Br, Cl 3) Li, K, Na 4) H, Be, Al
В каком ряду химические элементы расположены в порядке ослабления неметаллических свойств:
As, Se, Br 2) Br, Se, As 3) As, Br, Se 4) As, Bi, Sb
В каком ряду химические элементы расположены в порядке усиления неметаллических свойств:
B, Be, Li 2) B, Li, Be 3) Li, B, Be 4) Ga, Al, B
В каком ряду неметаллические свойства химических элементов убывают?
N, O, F 2) As, P, N 3) Cl, S, P 4) Cl, I, Br
В ряду Mg – Ca – Sr – Ba
увеличивается число заполненных энергетических уровней в атомах
увеличивается электроотрицательность 3) изменяется агрегатное состояние простых веществ
ослабевают металлические свойства элементов
В ряду F – Cl – Br – I
уменьшается радиус атома 3) усиливаются неметаллические свойства элементов
увеличивается электроотрицательность 4) увеличивается число заполненных энергетических уровней в атомах
В ряду Li – Na – K – Rb
изменяется агрегатное состояние простых веществ 3) изменяется заряд иона
увеличивается электроотрицательность 4) усиливаются металлические свойства элементов
В ряду Si – P – S – Cl
увеличивается радиус атома
агрегатное состояние простых веществ одинаковое при обычных условиях
увеличивается электроотрицательность 4) усиливаются металлические свойства
В ряду Mg – Al – Si – P
увеличивается радиус атома 3) увеличивается число заполненных энергетических уровней
усиливаются металлические свойства элементов 4) агрегатное состояние простых веществ одинаковое
Металличекие свойства элементов:
Возрастают в периоде слева направо 3) изменяются в периоде немонотонно
Возрастают в группе сверху вниз 4) характерны только для щелочных элементов
Среди всех элементов третьего периода элемент хлор обладает:
наиболее выраженными металлическими свойствами 3) самой высокой электроотрицательностью
самой большой атомной массой 4) самым большим радиусом атома
Среди всех элементов третьего периода элемент натрий обладает:
самой высокой электроотрицательностью 3) самым маленьким радиусом атома
наиболее выраженными металлическими свойствами 4) самой большой плотностью
Среди всех элементов главной подгруппы II группы элемент бериллий обладает:
наиболее выраженными металлическими свойствами 3) самой большой атомной массой
наименьшим радиусом атома 4) самой низкой электроотрицательностью
Среди всех элементов главной подгруппы IV группы элемент свинец обладает:
самым большим радиусом атома 3) наименее выраженными металлическими свойствами
самой высокой валентностью 4) самой высокой электроотрицательностью
Среди элементов второй группы максимальный радиус атома имеет:
бериллий 2) барий 3) кадмий 4) цинк
Среди элементов четвертого периода максимальный радиус атома имеет:
медь 2) калий 3) никель 4) криптон
Кислотные свойства в ряду высших оксидов углерода – кремния – фосфора:
возрастают 2) ослабевают 3) сначала возрастают, затем ослабевают 4) сначала ослабевают, затем возрастают
Кислотные свойства в ряду высших гидроксидов серы – хлора – йода:
возрастают 2) ослабевают 3) сначала возрастают, затем ослабевают 4) сначала ослабевают, затем возрастают
Наименьшим атомным радиусом обладает:
Алюминий 2) аргон 3) натрий 4) магний
В каком ряду химические элементы расположены в порядке возрастания атомного радиуса:
C, N, O 2) Na, Mg, Al 3) F, O, N 4) Br, Cl, F
Кислотность оксидов, образованных элементами IVА группы, сверху вниз:
Не изменяется 2) изменяется периодически 3) увеличивается 4) уменьшается
Атомный радиус элементов увеличивается в ряду:
Кислород, фтор, неон 2) хлор, сера, фосфор 3) сера, хлор, бром 4) сера, хлор, фтор
Кислотные свойства в ряду высших оксидов бора – углерода – кремния:
возрастают 2) ослабевают 3) сначала возрастают, затем ослабевают 4) сначала ослабевают, затем возрастают
Наименьшим атомным радиусом обладает:
Фтор 2) неон 3) йод 4) ксенон
1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 |
4 | 3 | 2 | 2 | 3 | 1 | 1 | 2 | 1 | 3 | 4 | 2 | 1 | 3 | 4 | 4 | 3 |
18 | 19 | 20 | 21 | 22 | 23 | 24 | 25 | 26 | 27 | 28 | 29 | 30 | 31 | 32 | 33 | 34 |
4 | 3 | 2 | 1 | 1 | 4 | 3 | 1 | 2 | 4 | 1 | 1 | 1 | 2 | 2 | 4 | 2 |
35 | 36 | 37 | 38 | 39 | 40 | 41 | 42 | 43 | 44 | 45 | 46 | 47 | 48 | 49 | 50 | 51 |
4 | 3 | 1 | 4 | 4 | 3 | 4 | 2 | 3 | 2 | 2 | 1 | 2 | 2 | 4 | 3 | 2 |
52 | 53 | 54 | 55 | 56 | ||||||||||||
3 | 4 | 2 | 3 | 2 |
Задания на сопоставление
Задание 2
Закономерности изменения химических свойств элементов и их соединений по периодам и группам. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов.
Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. Характеристика переходных элементов – меди, цинка, хрома, железа – по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов.
Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов.
1. Ответом к заданию является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1. Ряд: 1) H 2) N 3) F 4) Li 5) P
Выберите три элемента, которые в периодической системе находятся в одном периоде, и расположите эти элементы в порядке увеличения радиуса атома.
2. Ряд: 1) C 2) Si 3) O 4) Be 5) S
Выберите три элемента, которые в периодической системе находятся в одном периоде, и расположите эти элементы в порядке уменьшения радиуса атома.
3. Ряд: 1) Al 2) Cl 3) S 4) F 5) I
Выберите три элемента, которые в Периодической системе находятся в одной группе, и расположите эти элементы в порядке усиления неметаллических свойств.
4. Ряд: 1) Na 2) K 3) N 4) Li 5) Al
Выберите три элемента, которые в Периодической системе находятся в одной группе, и расположите эти элементы в порядке усиления металлических свойств.
5. Ряд: 1) S 2) Mg 3) C 4) B 5) Li
Выберите три элемента, которые в Периодической системе находятся в одном периоде, и расположите эти элементы в порядке увеличения электроотрицательности.
6. Ряд: 1) Li 2) Si 3) Be 4) Cl 5) O
Выберите три элемента, которые в Периодической системе находятся в одном периоде, и расположите эти элементы в порядке уменьшения элекроотрицательности.
7. Ряд: 1) Ne 2) Se 3) Mg 4) S 5) O
Выберите три элемента, которые в периодической системе находятся в одной группе, и расположите эти элементы в порядке увеличения электроотрицательности.
Правильных ответа из 5
1. В каких рядах химические элементы расположены в порядке усиления металлических свойств?
1) Na,Mg,Al 2) Al,Mg,Na 3) Tl,Ba,Cs4) Mg,Be,Cа 5)Cа,Mg, Be
2. Какие из элементов имеют наиболее ярко выраженные неметаллические свойства? 1)S 2) Se 3) Te4) As5) С1
3. У элементов 3 периода слева направо возрастают
1) основные свойства высших гидроксидов
2) восстановительные свойства водородных соединений;
3) электротрицательность элементов
4) кислотные свойства высших гидроксидов
5) основные свойства высших оксидов.
4. В ряду Be – B – C – N происходит
1) увеличение радиуса атомов; 2)увеличение электроотрицательности;3) увеличение числа валентных электронов; 4)уменьшение силы притяжения валентных электронов к ядру; 5) уменьшение числа неспаренных электронов в основном состоянии атома
5. В каких рядах простые вещества расположены в порядке усиления металлических свойств?
1) Mg,Ca,Ba 2) Na,Mg,Al 3)Ge,Sn,Pb 4) Sc,Ca,Mg 5) K,Ca, Fe
6. Формула высшего оксида элемента – Э2О. Какая конфигурация валентных электронов возможна у этого атома? 1) 3s1 2) 3s23p5 3) 2s22p1 4) 2s22p5 5) 3d14s2
7. Среди всех элементов 3-го периода элемент натрий обладает…1) самой высокой электроотрицательностью
2) наиболее выраженными металлическими свойствами
3) самым маленьким радиусом атома
4) самой большой плотностью
5) наименьшими неметаллическими свойствами
8. Среди всех элементов главной подгруппы VII группы (исключая водород) элемент фтор обладает
1) самыми слабыми неметаллическими свойствами 2) самой большой атомной массой 3) наименьшей электроотрицательностью 4) наименьшим радиусом атома
5) наибольшим сродством к электрону
9. Какие из приведенных ниже рядов химических элементов характеризуются возрастанием атомных радиусов?
Какие из приведенных ниже рядов химических элементов характеризуются возрастанием атомных радиусов?
1) Te, Se, S, O 2) Na, Mg, Al, Si
3) C, B, Be, Li 4) Ba, Al, Ga, Ge 5) K, Rb, Cs, Fr
10. Металлические свойства усиливаются в рядах:
1) K – Na – Li 2) Mg – Ca – K
3) Rb – Sr – Y 4) In – Ga – Ge 5) As – Sb – Bi
11. К s-элементам относятся:
1) натрий и цинк; 2) калий и барий; 3) серебро и золото
4) литий и стронций 5) рубидий и олово
12. У К и Rb одинаковы…
1) высшая валентность 2) значения относительной электроотрицательности3) заряды ядер 4) высшие степени окисления
5) атомные радиусы
13. Формула высшего оксида некоторого элемента – ЭО3. Какую конфигурацию валентных электронов может иметь этот элемент в основном состоянии?
1) 4d6 3) 3s23р4 2) 2s22р44) 3d54s1 5) 3s13d5
14. Наиболее и наименее выраженными металлическими свойствами обладают1) Nа 2) К 3) Mg 4) А1 5) Mn
15. В ряду: Al→ Si → P → S
1) увеличивается радиус атомов
2) усиливаются металлические свойства элементов
3) ослабевают металлические свойства элементов
4) ослабевают неметаллические свойства элементов
5) уменьшается высшая степень окисления элементов
16. Среди перечисленных элементов к металлам относятся: 1) барий 2) кремний 3) олово 4) бор 5) гелий
17. Наиболее и наименее выражены металлические свойства соответственно у 1) Al 2) Na 3) Mg 4) Fe 5) Ва
18. У Mg и Ва одинаковы…1) атомные радиусы 2) валентность в соединениях 3) заряды ядер 4) высшие степени окисления; 5) значения относительной электроотрицательности
19. Какие из элементов имеют наиболее и наименее ярко выраженные металлические свойства?1)K 2) Na3)Ca4)Mg 5) Li
20. B ряду химических элементов Na ® Mg ® Al ® Si
1) увеличивается число валентных электронов в атомах
2) уменьшается число электронных слоев в атомах
3) уменьшается число протонов в ядрах атомов
4) уменьшаются металлические свойства
5) увеличиваются радиусы атомов
21. Какие из групп элементов содержат только металлы?
Какие из групп элементов содержат только металлы?
1) Sr, Hg, Pt2) K, Ca,Sr 3) Li, Si, Na 4) Se, Te, Po 5) Li , Be, B
22. В порядке усиления неметаллических свойств расположены 1) S-Sе 2) Sе-Вr 3) I-Cl 4) I-Te 5) Вr-I
23. Неметаллические свойства у элементов А-групп усиливаются 1) в группах снизу вверх; 2)в группах сверху вниз; 3).справа налево в периоде в большом периоде; 4)слева направо в периоде в большом периоде; 5)справа налево в малом периоде
24. В каких рядах простые вещества расположены в порядке усиления их металлических свойств?
1) Na, Mg, Al 2) Se, Te, Po
3) Li, Na, K 4) Ba, Sr, Ca 5) K, Na, Be
25. В атомах каких металлов в основном состоянии на энергетическом d-подуровне содержится пять электронов: 1) железа 2) ванадия 3) марганца4) хрома 5)титана6) вольфрама
26. Способность отдаватьэлектроны атомом элемента увеличиваетсяв ряду l) Ca, Mg, Be 2) B, C, F 3) Al, Mg, Na 4) Si, Ge, Sn 5) S, Cl, F
27. В каких рядах химические элементы расположены в порядке возрастания их атомного радиуса?
1) Li, Na, K, Rb 2) Sr, Ca, Mg, Be
3) In, Ga, Al, B 4) I, Te, Sb, Sn 5) Sn, Ge, Si, C
28. Среди элементов VIА-группы максимальный и минимальный радиус атома соответственно имеют 1)кислород 2) сера 3) теллур 4) полоний 5) селен
29. Атомы каких химических элементов, из числа приведенных ниже, имеют наименьший радиус?
1) K 2) Al 3)Sn 4) O 5) N
30. У Cа и Sr одинаковы… 1) атомные радиусы 2) значения относительной электроотрицательности
3) степени окисления 4) строение внешнего электронного слоя 5) количества электронных слоев
31. Наименее и наиболее выраженными металлическими свойствами обладает1) Rb 2) Sr 3) Са 4) К 5) Ва
32. В ряду Вe-Mg-Сa-Sr происходит
1) ослабление металлических свойств ; 2)увеличение радиуса атома; 3)увеличение электроотрицателъности; 4)уменьшение числа валентных электронов; 5)уменьшение силы притяжения валентных электронов к ядру
33. Притяжение электронов внешнего слоя к ядру увеличивается в ряду:1)Si – P – N 2) Al – B – C 3) Na – K – Rb 4) Sr – Ca – K 5) S – P – As
Притяжение электронов внешнего слоя к ядру увеличивается в ряду:1)Si – P – N 2) Al – B – C 3) Na – K – Rb 4) Sr – Ca – K 5) S – P – As
34. Притяжение электронов внешнего слоя к ядру ослабевает в ряду:1) Al — Mg — Ca 2) Al — Si — C 3) Na — Mg — Be 4) Sr – Rb – Cs 5) Se — S — Cl
35. Способность атома притягивать валентные электроны других атомов увеличивается в ряду:
1) Sb, As, P 2) Si, S, Cl 3) Р, О, S 4) F, Cl, Br 5) Mg, Ca, Ba
36. Химические элементы расположены в порядкевозрастания их атомного радиуса в ряду: 1) Be, B, C, N 2) O, S, Se, Te 3) Rb, K, Na, Li 4) Ti, Sc, Ca, K 5)Mg, Al, Si, Р
37. Среди перечисленных элементов наибольший и наименьший атомный радиус соответственно имеют:
1) бериллий 2) фтор 3) литий 4) натрий 5) магний
38. Способность принимать электроны атомом элемента увеличивается в ряду с порядковыми номерами:
1) 16,20 2) 19, 34 3) 12,17 4) 9,10 5) 6, 11
39. Легче всего присоединяют электроны атомы
1) серы 2) хлора 3) селена 4) брома 5) кислорода
Задания на сопоставление
40. Установите соответствие между формулой оксида и электронной структурой атома
ФОРМУЛА ЭЛЕКТРОННАЯ СТРУКТУРА
А) R2O3 1) 1s22s22p63s23p2 Б) RO2 2) 1s22s22p63s23p4
В) RO3 3) 1s22s22p63s23p1 Г) R2O5 4) 1s22s22p3
5) 1s22s22p63s23p5 6) 1s22s22p63s2
41. Установите соответствие между формулой оксида элемента и формулой водородного соединения
ФОРМУЛА ОКСИДА ФОРМУЛА ВОДОРОДНОГО СОЕДИНЕНИЯ А) R2O7 1) RH3 Б) RO2 2) RH4
В) RO3 3) RH Г) R2O5 4) RH2
5) R2H2 6) R3H
42. Установите соответствие между формулой оксида и электронной структурой атома
Установите соответствие между формулой оксида и электронной структурой атома
ФОРМУЛА ЭЛЕКТРОННАЯ СТРУКТУРА
А) R2O 1) 1s22s22p63s2
Б) RO 2) 1s22s22p63s23p4
В) RO3 3) 1s22s22p63s23p1
Г) R2O7 4) 1s22s22p5
5) 1s22s22p63s23p5
6) 1s22s22p63s23p64s1
43. Установите соответствие между формулой оксида и конфигурацией внешнего электронного слоя
ФОРМУЛА КОНФИГУРАЦИЯ
А) R2O 1) ns2np2
Б) RO 2) ns2
В) RO3 3) ns2np3
Г) R2O7 4) ns1
5) ns2np4
6) ns2np5
44. Установите соответствие между конфигурацией внешнего электронного слоя атома и формулой водородного соединения КОНФИГУРАЦИЯ ФОРМУЛА
А) ns2np4 1) RН3
Б) ns2np3 2) Н2R
В) ns2np2 3) RН5
Г) ns2np5 4) НR
5) RН4
6) R2Н2
45. Установите соответствие между конфигурацией внешнего электронного слоя и формулой оксида
КОНФИГУРАЦИЯ ФОРМУЛА
А) ns2 1) R2O3
Б) ns2np1 2) RO2
В) ns2np2 3) R2O5
Г) ns2np3 4) RO3
5) R2O7
6) R2O
Тренировочный вариант заданий для подготовки к ГИА по химии
Тренировочный вариантзаданий для подготовки к
ГИА по химии
Работу выполнила
учащаяся 9в класса МАОУ СОШ № 18
Свистунова Дарья.

Руководитель: О.А. Муромцева
2. Цель
• Познакомить учащихся с заданиями по теме«Периодический закон и Периодическая система
химических элементов Д.И. Менделеева»;
• Проверить знания учащихся в ходе подготовки
ОГЭ по химии;
• Выявить вопросы, которые вызывают у учащихся
затруднения по данной теме.
3. Инструкция
• Чтобы ответить на вопрос наведите курсормыши на вариант ответа, который вы
выберете, и кликните на кружок, находящийся
около ответа, левой кнопкой мыши.
• При неверном ответе кружок загорится
красным цветом, а при правильном — зеленым
В каком ряду химические элементы
расположены в порядке усиления
неметаллических свойств?
1)
Si → S → Cl
2) S → O → Se
3) N → P → As
4) S → P → Si
В каком ряду химические элементы
расположены в порядке усиления металлических
свойств?
1) P → N →S
2) O → S → Se
3) I → Br → Cl
4) Be → B → C
Элемент образует высший оксид состава RO3.
Формула его водного соединения:
1) Rh3
2) Rh4
3) RH
4) Rh5
В каком ряду химические элементы расположены в по
Усиления металлических свойств?
1) Литий → натрий → калий
2) Кальций → магний → барий
3) Натрий → магний → алюминий
4) Кальций → калий → натрий
В каком ряду химические элементы расположены в
порядке уменьшения числа валентных электронов?
1) Li, Be, B
2) C, Si, Ge
3) Ca, Mg, Be
4) S, P, C
Наиболее сильными кислотными свойствами
обладает высший оксид:
1) Углерода
2) Фосфора
3) Азота
4) Кремния
Свойства оксидов в ряду Al2O3 → SiO2 → P2O5
изменяются от:
1) Амфотерных к кислотным
2) Основных к кислотным
3) Амфотерных к основным
4) Кислотных к основным
От кислотных к оснóвным
меняются свойства оксидов в ряду
1) CaO → SiO2 → SO3
2) CO2 → Al2O3 → MgO
3) SO3 → P2O5 → Al2O3
4) Na2O → MgO → Al2O3
В каком ряду химических элементов усиливаются
неметаллические свойства соответствующих им
простых веществ?
1) Алюминий → фосфор → хлор
2) Фтор → азот → углерод
3) Хлор → бром → иод
4) Кремний → сера → фосфор
Высший оксид состава ЭО3 образует:
1) N
2)Ga
3) C
4) Se
В порядке усиления кислотных свойств
расположены гидроксиды:
1) HNO3 → h4PO4
2) h3SO4 → HClO4
3) HClO4 → h3SeO4
4) h3SeO4 → h4AsO4
Наиболее сильной кислотой
среди приведенных ниже является:
1) h3SO4
2) h3SiO3
3) HClO4
4) HBrO4
Элементом, высший оксид которого проявляет
наиболее сильные кислотные свойства, является:
1) Углерод
2) Сера
3) Мышьяк
4) Алюминий
Неметаллические свойства наиболее выражены у
вещества
1) Si
2) Ge
3) P
4) As
В ряду элементов Si – P – S сила кислот,
соответствующих высшей степени окисления,
меняется следующим образом:
1) Слабая, слабая, средняя
2) Сильная, слабая, средняя
3) Слабая, средняя, сильная
4) Средняя, слабая, сильная
19.
 Использованная литература и Интернет-ресурсы: Использованная литература и Интернетресурсы:
Использованная литература и Интернет-ресурсы: Использованная литература и Интернетресурсы:• http://www.resolventa.ru/demo/him/demo
giahim.htm
• https://ege.yandex.ru/chemistry-gia/
• «Химия 8 класс О.С. Габриелян. Дрофа 2016»
• «Химия 9 класс О.С. Габриелян. Дрофа 2013»
20. Спасибо за внимание
ряд элементов,расположенных в порядке усиления их неметаллических свойств, химия
5-9 класс
1.фтор,хлор бром
2.кремний, фосфор,сера
3.кислород,азот,углерод
4.хлор,сера,фосфор
21 мая 2015 г., 6:47:15 (5 лет назад)
в периодической системе неметаллические свойства:
а) в периоде слева направо увеличиваются
б) в группе сверху вниз уменьшаются
2.кремний,фосфор,сера
Ответ:2
Ответить
Другие вопросы из категории
Читайте также
Lilka1612 / 28 авг. 2013 г., 21:16:48
Ряд элементов расположенных в порядке усиления их металических свойств1) литий , натрий, калий
2) натрий, магний, алюминий
3) водород, литий, бериллий,
4) кальций, магний, бериллий
Alim0007 / 05 мая 2013 г., 10:48:23
Помогите, пожалуйста! Очень нужно!!! Заранее, большое спасибо!)1. В каком ряду химические элементы расположены в порядке увеличения зарядов ядер атомов?
1) B, N, C 2) O, Se, S 3) Br, CI, F 4) Be, Mg, Ca
2. Наибольшей восстановительной активностью обладает
1) Si 2) P 3) S 4) CI
3. В каком ряду химических элементов В→ С→ N
1) усиливаются металлические свойства
2) ослабевают восстановительные свойства
3) уменьшается электроотрицательность атомов
4) уменьшается высшая степень окисления в оксидах
4. В каком ряду химические элементы расположены в порядке ослабления их неметаллических свойств?
1) Ве →В→ С 2) Ga → AI → B 3) S → CI → Ar 4) CI → Br → I
5) В каком ряду химические элементы расположены в порядке возрастания их атомных радиусов?
1) N, В, С 2) N, P, As 3) Na, Mg, K 4) B, Si, N
6) Низшая степень окисления в ряду химических элементов фтор — кислород — углерод
1) увеличивается 2) не изменяется 3) уменьшается 4) изменяется периодически
7) Высший оксид состава ЭО образуют все элементы
1) IV A группы 2) IIA группы 3) IV периода 4) II периода
8) В ряду гидроксидов В(ОН)3 → АI(ОН)3 → ТI(ОН)3 свойства гидроксидов изменяются от
1) основных к кислотным 2) амфотерных к кислотным
3) кислотных к основным 4) амфотерных к основным
Вы находитесь на странице вопроса «ряд элементов,расположенных в порядке усиления их неметаллических свойств«, категории «химия«. Данный вопрос относится к разделу «5-9» классов. Здесь вы сможете получить ответ, а также обсудить вопрос с посетителями сайта. Автоматический умный поиск поможет найти похожие вопросы в категории «химия«. Если ваш вопрос отличается или ответы не подходят, вы можете задать новый вопрос, воспользовавшись кнопкой в верхней части сайта.
Данный вопрос относится к разделу «5-9» классов. Здесь вы сможете получить ответ, а также обсудить вопрос с посетителями сайта. Автоматический умный поиск поможет найти похожие вопросы в категории «химия«. Если ваш вопрос отличается или ответы не подходят, вы можете задать новый вопрос, воспользовавшись кнопкой в верхней части сайта.
1. В ряду химических элементов О → S → Sе: 1) уменьшается радиус атомов 2) уменьшается электроотрицательность 3) усиливаются неметаллические свойства 4) увеличиваются заряды ядер атомов 5) уменьшается число заполненных электронных слоев в атомах
2. В ряду химических элементов Na → Al → P происходит увеличение (усиление): 1) числа нейронов в ядрах атомов 2) восстановительных свойств 3) степени окисления в высших оксидах 4) радиуса атома 5) металлических свойств
3. В ряду химических элементов Cl → Si → Al: 1) уменьшаются заряды ядер атомов 2) возрастают кислотные свойства летучих водородных соединений 3) высшая степень окисления уменьшается 4) уменьшается радиус атомов 5) усиливаются металлические свойства
4. 4.В ряду химических элементов Sе → S → О: 1) уменьшается валентность в высших оксидах 2) возрастают радиусы атомов хим. элементов 3) усиливаются неметаллические свойства 4) увеличивается электроотрицательность 5) увеличивается число электронных слоев в атомах
5. 5.В ряду химических элементов Si → Р → S: 1) уменьшается число протонов в ядре 2) уменьшается электроотрицательность 3) увеличивается радиус атомов 4) увеличивается число электронов во внешнем электронном слое 5) усиливаются неметаллические свойства
6. 1) уменьшается радиус атомов 2) возрастает способность атомов отдавать электроны 3) увеличиваются заряды ядер атомов 4) уменьшается относительная атомная масса 5) увеличивается степень окисления в высших гидроксидах
7. 7.В ряду химических элементов N → Р → Аs: 1) уменьшается электроотрицательность 2) уменьшаются радиусы атомов 3) ослабевают неметаллические свойства 4) увеличивается валентность в высших оксидах 5) уменьшается число заполненных электронных слоев в атомах
8. 8.В порядке ослабевания металлических свойств расположены элементы в рядах: 1) 1, Be → Mg → Ca 4, B → Be → Li 2) 2, Na → Mg → Al 5, Mg → Ca → Sr 3) 3, Rb → K → Na
9. Способность отдавать электроны возрастает у элементов следующих рядов: 1) Na → Al → P 2) Sr → Ca → Mg 3) C → N → O 4) Si → Al → Mg 5) B → Be → Li
10. В ряду химических элементов Al → Mg →Na: 1) усиливается электроотрицательность 2) усиливаются металлические свойства 3) усиливается основный характер их высших оксидов 4) уменьшается радиус атомов 5) усиливается кислотный характер их высших оксидов
| 11. В ряду химических элементов N → С → В: 1) увеличивается число протонов в ядре 2) увеличивается электроотрицательность 3) уменьшается радиус атомов 4) уменьшается число электронов во внешнем электронном слое 5) ослабевают неметаллические свойства
12. В порядке уменьшения числа электронов во внешнем слое расположены элементы следующих рядов: 1) N → O → F 2) С → Si → Ge 3) P → Si → Al 4) C → N → O 5) Br → Se → As
13. В ряду химических элементов Si → Ge → Sn: 1) увеличивается радиус атома 2) ослабевают металлические свойства соответствующих им простых веществ 3) ослабевает основный характер их высших оксидов 4) возрастает значение валентности в их высших оксидах 5) увеличивается число электронных слоёв в их атомах
14. В ряду химических элементов Cl → S → P → Si: 1) увеличиваются неметаллические свойства 2) уменьшается радиус атома 3) увеличивается число электронов во внешнем электронном слое 4) уменьшается низшая степень окисления 5) ослабевают неметаллические свойства
15. В ряду химических элементов Si → Аl → Мg: 1) уменьшается электроотрицательность 2) увеличиваются заряды ядер атомов 3) ослабевают неметаллические свойства 4) уменьшаются радиусы атомов 5) увеличивается число заполненных электронных слоев атомов
16. В ряду химических элементов Cl → P → Si: 1) уменьшаются заряды ядер атомов 2) уменьшается число электронных слоев 3) увеличивается атомный радиус 4) уменьшается низшая степень окисления 5) усиливаются неметаллические свойства
17. В ряду химических элементов I → Вr → Сl: 1) увеличивается степень окисления в высших оксидах 2) уменьшается число валентных электронов в атомах 3) увеличиваются заряды ядер атомов 4) усиливаются неметаллические свойства 5) уменьшается радиус атомов
18. В ряду химических элементов F → О → N: 1) увеличивается число электронных слоев в атомах 2) уменьшаются заряды ядер атомов 3) усиливаются неметаллические свойства 4) уменьшается радиус атомов 5) уменьшается число электронов во внешнем электронном слое
19. В ряду химических элементов Аl → Р → Сl: 1) увеличивается электроотрицательность 2) уменьшаются заряды ядер атомов 3) возрастают металлические свойства 4) уменьшаются радиусы атомов 5) уменьшается число электронов во внешнем электронном слое
20. В ряду химических элементов Li → Ве → В: 1) увеличивается электроотрицательность 2) уменьшаются металлические свойства 3) уменьшаются заряды ядер атомов 4) уменьшается число электронов во внешнем электронном слое 5) увеличивается число заполненных электронных слоев
|
Периодические тенденции в свойствах металлов
Цель обучения
- Опишите соединение металлических элементов.
Ключевые моменты
- Названия групп в периодической таблице дают подсказки о металлических свойствах элементов.
- Металлические элементы находятся в левой части таблицы Менделеева.
- Простая концепция металлов описывает их как решетку положительных ионов, погруженных в море электронов.
Условия
- Семейство
- , также известное как группа, столбец элементов в периодической таблице, которые имеют одинаковую реакционную способность из-за их аналогичной электронной конфигурации валентной оболочки.
- электроотрицательный: стремится притягивать электроны для образования химической связи.
Напомним, что в периодической таблице каждая строка называется периодом. Строки выровнены таким образом, что элементы в каждом вертикальном столбце имеют определенные характеристики.Каждый из столбцов периодической таблицы называется группой. Химики давно сочли удобным называть элементы различных групп, а в некоторых случаях и промежутков групп, именами, приведенными в таблице. Имейте в виду, что названия групп могут дать подсказку о металлических свойствах элементов.
Тенденции в периодической таблице. Семейства периодической таблицы часто группируются по металлическим свойствам.Когда два элемента соединены в химическую связь, элемент, который сильнее притягивает общие электроны, имеет большую электроотрицательность.Элементы с низкой электроотрицательностью, как правило, обладают более металлическими свойствами. Таким образом, металлические свойства элементов имеют тенденцию уменьшаться с течением времени и увеличиваться по группе. Тот факт, что металлические элементы находятся в левой части таблицы Менделеева, дает важный ключ к пониманию того, как они соединяются вместе, образуя твердые тела. Все эти элементы обладают низкой электроотрицательностью и легко образуют положительные ионы.
Металлы имеют тенденцию образовывать положительные ионы и отталкиваться друг от друга, так как же атомы металлов остаются связанными в твердом теле? Самая простая концепция металлов — это решетка положительных ионов, погруженных в «море электронов», которые могут свободно перемещаться по твердому телу.Фактически, электроположительная природа металлических атомов позволяет их валентным электронам существовать как подвижная жидкость. Это приводит к их высокой электропроводности. Поскольку каждый ион окружен электронной жидкостью во всех направлениях, связь не имеет направленных свойств; этим объясняется высокая пластичность и пластичность металлов.
Показать источникиBoundless проверяет и курирует высококачественный контент с открытой лицензией из Интернета. Этот конкретный ресурс использовал следующие источники:
Расположение элементов в Периодической таблице | Периодическая таблица элементов
Периодическая таблица — это система классификации элементов, из которых состоит материя и материалы в нашем мире.Сегодня известно более 100 различных элементов! Каждый элемент имеет собственное имя, символ, атомный номер и позицию в Периодической таблице.
Имена элементов
Гафний получил свое название от латинского названия Копенгагена — Hafnia , поскольку этот элемент был открыт двумя учеными, работавшими в то время в Копенгагене.
Как вас зовут? Возможно, это Тандо.Или Дэвид. Или Меган. Возможно, вам посчастливилось быть единственным человеком в классе с таким именем. Возможно, вам посчастливится быть единственным человеком в мире с таким именем! Это сделало бы ваше имя уникальным.
Каждый элемент имеет уникальное имя. Мы можем рассматривать каждое имя как уникальную «метку», которую мы можем использовать для идентификации элемента. Есть еще две уникальные метки, которые мы можем использовать для идентификации элементов. Это химический символ и атомный номер. Мы узнаем об этом больше в следующем разделе.Каждый элемент имеет свои уникальные свойства, и позже мы увидим, что элементы с некоторыми похожими свойствами могут быть сгруппированы вместе.
Есть ДВЕ песни, которые помогут вам запомнить элементы Периодической таблицы: и . Какой твой любимый? Сможете ли вы изучить один (или оба) из них?
Периодическая таблица элементов, как она есть сегодня.На внутренней стороне обложки вашей рабочей тетради есть увеличенная версия современной Периодической таблицы элементов.Вы можете использовать его для удобства.
Химические символы
Если вы ученый и работаете с элементами каждый день, записывать имена может быть очень утомительно. Чтобы упростить описание элементов, ученые присвоили каждому элементу короткий символ . Чтобы мы не запутались с разными элементами, когда пишем о них, символ для каждого элемента должен быть уникальным, как и его имя.
Названия и символы некоторых общих элементов показаны в следующей таблице.
Вам необходимо знать названия и символы перечисленных здесь элементов.
Элемент | Обозначение | Элемент | Обозначение |
Алюминий | Al | Магний | мг |
Бром | руб. | Азот | N |
Кальций | Ca | Кислород | O |
Углерод | С | фосфор | -П |
Хлор | Класс | Калий | К |
Медь | Cu | Кремний | Si |
Золото | Au | Серебро | Ag |
Водород | H | Натрий | Na |
Йод | Я | Сера | S |
Утюг | Fe | Олово | Sn |
Свинец | Пб | Цинк | Zn |
Обозначение углерода — C, обозначения серы — S и обозначения азота — N.Легко понять, почему были выбраны эти символы: они просто представляют первую букву каждого имени. Эта буква всегда заглавная (заглавная).
Что произойдет, если все элементы начинаются с одной и той же буквы? Например: кальций, углерод, хлор и медь начинаются с буквы «С»! Чтобы гарантировать, что все они имеют уникальный символ, к их символу была добавлена вторая буква. Эта буква всегда строчная (строчная).
Некоторые химические символы труднее понять.Например, Na — это символ натрия. Na происходит от латинского названия натрия — natrium . Эти символы были выбраны очень давно, когда многие предметы изучались на латыни. Представляете, насколько это было сложно ?!
Некоторые простые правила, которые следует помнить при использовании химических символов:
- Каждый элемент имеет свой уникальный символ.
- Символ обычно (но не всегда) — это первые одна или две буквы названия элемента.
- Первая буква символа всегда заглавная.
- Если символ состоит из двух букв, вторая буква всегда будет строчной.
- Некоторые элементы имеют символы, которые произошли от их латинских названий.
Символ свинца (Pb) происходит от латинского слова plumbum, обозначающего свинец. В течение многих лет свинец использовался для изготовления водопроводных труб. Отсюда и слово сантехник.
Атомные числа
Этот сайт содержит интерактивное объяснение истории Периодической таблицы и атома и объясняет, как эти концепции связаны между собой. Он содержит больше информации, чем требуется учащимся на этом уровне, но вы можете прочитать его как расширение: http://www.learner.org/interactives/periodic/basics_4_periodicity.html.
Важное примечание: Мы вкратце представили здесь атом (хотя он не был указан в CAPS), так что идея атомного номера имеет смысл, а не просто абстрактное число.Однако эти концепции будут дополнительно исследованы в Gr. 8. На данный момент важно, чтобы учащиеся понимали, что каждый элемент имеет уникальный атомный номер и что Периодическая таблица элементов — это способ классификации элементов таким образом, чтобы они были сгруппированы вместе с точки зрения схожих свойств.
Представляя субатомных частиц , вы можете нарисовать модель атома на доске, если хотите показать это своим ученикам. Однако не так важно, чтобы учащиеся понимали расположение субатомных частиц на этом этапе.Вот простая модель атома, которую вы можете изобразить на доске:
(Эта модель здесь иллюстрирует атомы азота в виде 7 протонов. Обратите внимание, что существует равное количество протонов и нейтронов. Вместе они составляют ядро атома. Протоны имеют положительный заряд, электроны имеют отрицательный заряд, а нейтроны нейтральны.Если количество электронов равно количеству протонов, то атом нейтрален и не имеет заряда.Атом может приобретать или терять электроны, что приводит к заряду, и тогда он называется ионом.)
Если вы посмотрите на Периодическую таблицу, вы увидите, что каждый элемент также имеет уникальный номер. Это называется атомным номером . Чтобы правильно понять, что такое атомный номер, нам нужно знать, что такое атом . Мы узнаем больше об атомах в Gr. 8, а пока вернемся к нашему уроку истории!
Вы помните, как мы говорили, что Менделеев разработал первую таблицу Менделеева в 1869 году? Задолго до этого, в начале 1800-х годов, человек по имени Джон Далтон сказал, что вся материя состоит из очень маленьких частиц, называемых атомами.Эти атомы различаются по массе и размеру. Вы помните, мы говорили, что элемент — это чистая субстанция? Теперь мы также можем сказать, что элемент — это вещество, которое содержит только один конкретный тип атома. Атомы одного элемента отличаются от атомов любого другого элемента.
Вам не нужно пока знать подробно об атоме. Подробнее об этом мы узнаем в гр. 8!
Все атомы состоят из еще более мелких частиц, которые мы называем субатомными частицами.Это протоны, нейтроны и электроны. Все, что вы должны сейчас помнить, это то, что протоны, электроны и нейтроны одного элемента в точности такие же, как , как протоны, электроны и нейтроны любого другого элемента. Их количество и расположение отличает элементы друг от друга.
Атомный номер элемента означает , сколько протонов этот элемент имеет в своих атомах. Поскольку каждый элемент имеет разное количество протонов в своих атомах, каждый элемент также имеет уникальный атомный номер.
Посмотрите на Периодическую таблицу. Какой атомный номер у водорода? Сколько протонов в его атомах?
Водород имеет атомный номер 1 и, следовательно, 1 протон.
Что такое атомный номер углерода? Сколько протонов в его атомах?
Атомный номер углерода равен 6. В его атомах 6 протонов.
Вы видите, как элементы расположены так, что их атомные номера увеличиваются слева направо по Периодической таблице? Это не совпадение! Когда Менделеев впервые создал Периодическую таблицу, он расположил 60 элементов, о которых он знал в то время, в порядке увеличения массы. Затем он увидел, что в других характеристиках этих элементов есть регулярный узор. Затем Менделеев сгруппировал их в столбцы и строки в соответствии с их свойствами.Это были физические и химические свойства, которые ученые наблюдали в ходе множества различных экспериментов. Это привело к расположению элементов в Периодической таблице.
Периодическая таблица Менделеева от 1872 года. Поля, отмеченные пустыми линиями, представляют элементы, которые, по мнению Менделеева, существовали, но они еще не были обнаружены в то время, поэтому он оставил для них места.Когда что-то показывает регулярный повторяющийся узор, мы говорим, что это периодический .Когда элементы были расположены в порядке возрастания массы, Менделеев наблюдал закономерность в их свойствах, что позволило ему расположить элементы в строки и столбцы в таблице, Периодической таблице . Элементы в одних и тех же строках и столбцах таблицы имеют схожие свойства друг с другом.
Периодическая таблица, которую мы используем сегодня, выглядит намного более современной, чем первоначальная версия Менделеева. Вы заметите, что в современной версии таблицы нет пустых блоков.Это говорит нам о том, что все элементы, которые еще не были открыты при жизни Менделеева, теперь известны.
В следующем упражнении мы сравним исходную Периодическую таблицу Менделеева с версией, которую мы используем сегодня. Это поможет показать нам, как научные открытия иногда являются медленным процессом.
Это необязательная дополнительная деятельность.
Когда Менделеев впервые расположил элементы в соответствии с их массой и свойствами, в рядах образовались пробелы.Но как хороший ученый Менделеев не видел в этом проблемы! Вместо этого он думал, что это просто означает, что есть элементы, которые еще не были обнаружены. И он был прав!
Менделеев поставил пустую строку и атомный номер, чтобы показать, что он думал, что там должен быть элемент, но он не был обнаружен. Посмотрите внимательно на оригинальную таблицу Менделеева. Посмотрите, сможете ли вы найти в таблице, где написано «_ = 44».
Посмотри, сможешь ли ты найти 2 других элемента, которые не были обнаружены в то время.Запишите их номера в поле ниже.
А теперь посмотрите на современную версию Периодической таблицы. Сможете ли вы найти элементы с этими числами? Какие у них символы? Как их зовут? Запишите свои ответы в предоставленную таблицу.
В качестве расширения этой деятельности вы можете искать названия этих элементов и исследовать, когда они были обнаружены, и добавлять эту информацию в таблицу.
Эту последнюю задачу можно разделить на группы из 3 или 6 учащихся, которые затем могут принести свои данные в класс, где их можно будет объединить. Если даты для каждого элемента не совпадают в точности, это дает возможность обсудить достоверность информации. Когда данные «правда»? Всегда ли мы можем верить в то, что читаем? Когда источник данных надежен?
Номер элемента | Обозначение элемента | Название элемента | Когда был обнаружен этот элемент? |
Номер элемента | Обозначение элемента | Название элемента | Когда был обнаружен этот элемент? |
44 | Ру | Рутений | 1844 |
68 | Er | Эрбий | 1843 |
72 | Hf | Гафний | 1923 |
В следующем упражнении мы собираемся использовать наши новые знания символов элементов и атомных чисел для охоты за очень ценным «сокровищем».Мы найдем сокровище, следуя некоторым подсказкам о Периодической таблице.
Это увлекательное занятие, цель которого — научить учащихся взаимодействовать с Периодической таблицей и выучить названия и символы первых 20 элементов.
Ваша задача — следовать подсказкам, чтобы найти сокровище. Инструкции помогут вам разобрать название клада в блоках ниже.
Подсказка 1: Какой символ у углерода (атомный номер 6)? Напишите этот символ в первом блоке выше.
Подсказка 2: Водород — самый легкий элемент. Вы можете найти это в Периодической таблице? Напишите его символ во втором блоке.
Самый первый элемент Периодической таблицы (вверху слева).Символ водорода — H.
.Подсказка 3: Какой элемент представляет собой газ, которым мы дышим, чтобы остаться в живых? Вот подсказка: он представлен атомным номером 8. Напишите его символ в третьем блоке и дайте имя элемента ниже.
Подсказка 4: Этот элемент находится в четвертой строке и девятом столбце Периодической таблицы.Это металл, который используется в магнитах. Напишите его символ в четвертом блоке. Вы знаете его название? Напишите его название ниже.
Подсказка 5: Этот элемент представлен атомным номером 57. Запишите его символ в пятом блоке. Посмотрите, сможете ли вы узнать название этого элемента и запишите его ниже.
Подсказка 6: Этот элемент представлен атомным номером 52.Это полуметалл, который используется при производстве солнечных батарей. Напишите его символ в последнем (шестом) блоке. Посмотрите, сможете ли вы узнать название этого элемента и запишите его ниже.
Какое «сокровище» вы нашли?
Важно указать учащимся, что это не «формула» шоколада, а просто забавное занятие, направленное на поиск элементов в Периодической таблице.Позже мы узнаем, как складывать символы элементов в формулы, представляющие реальные соединения.
Завершите следующее предложение, заменив названия элементов химическими символами. Вам придется поискать некоторые символы!
НАУКА … фтор, мышьяк, углерод, йод, азот, астат, эйнштейний … я!
Наука… F As C I N At Es (очаровывает) … меня!
Заполните следующую таблицу, чтобы узнать, сколько названий и символов элементов вы помните. Попробуйте сделать это, не обращаясь к Периодической таблице.
Элемент | Обозначение | Элемент | Обозначение |
Al | мг | ||
Бром | N | ||
Кальций | Кислород | ||
С | фосфор | ||
Класс | К | ||
Медь | Si | ||
Au | Серебро | ||
H | Na | ||
Йод | Сера | ||
Fe | Олово | ||
Свинец | Zn |
Элемент | Обозначение | Элемент | Обозначение |
Алюминий | Al | Магний | мг |
Бром | руб. | Азот | N |
Кальций | Ca | Кислород | O |
Углерод | С | фосфор | -П |
Хлор | Класс | Калий | К |
Медь | Cu | Кремний | Si |
Золото | Au | Серебро | Ag |
Водород | H | Натрий | Na |
Йод | Я | Сера | S |
Утюг | Fe | Олово | Sn |
Свинец | Пб | Цинк | Zn |
Периодическая таблица состоит из 103 элементов, но только 90 из них встречаются в природе.Остальное сделал человек.
Как устроена Периодическая таблица Менделеева?
В периодической таблице перечислены все известные элементы в порядке возрастания атомного номера, который представляет собой просто количество протонов в ядре. Если бы это было единственное соображение, диаграмма была бы просто линией, но это не так. Облако электронов окружает ядра каждого элемента, обычно по одному на каждый протон. Элементы объединяются с другими элементами и сами с собой, чтобы заполнить свои внешние электронные оболочки в соответствии с правилом октетов, которое указывает, что полная внешняя оболочка — это та, которая имеет восемь электронов.Хотя правило октетов не применяется так строго к более тяжелым элементам, как к более легким, оно все же обеспечивает основу для организации периодической таблицы.
TL; DR (слишком долго; не читал)
В периодической таблице элементы перечислены в порядке возрастания атомного номера. Форма диаграммы, состоящей из семи строк и восьми столбцов, основана на правиле октетов, которое указывает, что элементы комбинируются таким образом, чтобы получить стабильные внешние оболочки из восьми электронов.
Группы и периоды
Наиболее заметной особенностью периодической таблицы является то, что она организована в виде диаграммы с семью строками и восемью столбцами, хотя количество столбцов увеличивается к нижней части диаграммы.Химики называют каждую строку точкой, а каждый столбец — группой. Каждый элемент в периоде имеет одно и то же основное состояние, и элементы становятся менее металлическими при движении слева направо. Элементы в одной группе имеют разные основные состояния, но у них одинаковое количество электронов во внешних оболочках, что придает им схожие химические свойства.
Слева направо наблюдается тенденция к более высокой электроотрицательности, которая является мерой способности атома притягивать электроны.Например, натрий (Na) находится чуть ниже лития (Li) в первой группе, которая входит в состав щелочных металлов. Оба имеют по одному электрону на внешней оболочке, и оба обладают высокой реакционной способностью, стремясь отдать электрон для образования стабильного соединения. Фтор (F) и хлор (Cl) находятся в тех же периодах, что и Li и Na, соответственно, но они находятся в группе 7 на противоположной стороне диаграммы. Они входят в состав галогенидов. Они также очень реактивны, но являются акцепторами электронов.
Элементы группы 8, такие как гелий (He) и неон (Ne), имеют полные внешние оболочки и практически не реагируют.Они образуют особую группу, которую химики называют благородными газами.
Металлы и неметаллы
Тенденция к увеличению электроотрицательности означает, что элементы становятся все более неметаллическими по мере продвижения слева направо по периодической таблице. Металлы легко теряют свои валентные электроны, а неметаллы легко их приобретают. В результате металлы являются хорошими проводниками тепла и электричества, а неметаллы — изоляторами. Металлы являются пластичными и твердыми при комнатной температуре, тогда как неметаллы хрупки и могут существовать в твердом, жидком или газообразном состоянии.
Большинство элементов являются металлами или металлоидами, которые по своим свойствам находятся где-то между металлами и неметаллами. Элементы, имеющие наиболее металлическую природу, расположены в нижней левой части диаграммы. Те, у кого меньше всего металлических качеств, находятся в верхнем правом углу.
Переходные элементы
Основная часть элементов не вписывается в аккуратную схему групп и периодов, которую задумал русский химик Дмитрий Иванович Менделеев (1834–1907), который первым разработал таблицу Менделеева.Эти элементы, известные как переходные элементы, занимают середину таблицы с периодов с 4 по 7 и между группами II и III. Поскольку они могут разделять электроны более чем на одну оболочку, они явно не являются донорами или акцепторами электронов. В эту группу входят такие распространенные металлы, как золото, серебро, железо и медь.
Кроме того, в нижней части периодической таблицы появляются две группы элементов. Их называют соответственно лантаноидами и актинидами. Они там, потому что им не хватает места на графике.Лантаноиды входят в группу 6 и относятся к лантану (La) и гафнию (Hf). Актиниды принадлежат к группе 7 и находятся между актинием (Ac) и резерфордием (Rf).
Как устроена таблица Менделеева сегодня?
Таблица Менделеева — один из самых ценных инструментов для химиков и других ученых, потому что она упорядочивает химические элементы в удобном порядке. Как только вы поймете, как устроена современная периодическая таблица, вы сможете делать гораздо больше, чем просто искать факты об элементах, такие как их атомные номера и символы.
Схема организации
Организация периодической таблицы позволяет прогнозировать свойства элементов на основе их положения на диаграмме. Вот как это работает:
- Элементы перечислены в числовом порядке по атомным номерам. Атомный номер — это количество протонов в атоме этого элемента. Итак, элемент номер 1 (водород) — это первый элемент. На каждый атом водорода приходится 1 протон. Пока не будет обнаружен новый элемент, последним элементом в таблице будет номер 118.Каждый атом элемента 118 состоит из 118 протонов. Это самое большое различие между современной таблицей Менделеева и периодической таблицей Менделеева. В исходной таблице элементы организованы путем увеличения атомного веса.
- Каждая горизонтальная строка в периодической таблице называется периодом. В таблице Менделеева семь периодов. Все элементы в один и тот же период имеют один и тот же уровень энергии основного состояния электрона. При перемещении слева направо по периоду элементы переходят от отображения металлических характеристик к неметаллическим свойствам.
- Каждый вертикальный столбец в периодической таблице называется группой. Элементы, принадлежащие к одной из 18 групп, будут иметь аналогичные свойства. Атомы каждого элемента в группе имеют одинаковое количество электронов во внешней электронной оболочке. Например, все элементы галогенной группы имеют валентность -1 и обладают высокой реакционной способностью.
- Под основной частью таблицы Менделеева расположены два ряда элементов. Их поместили туда, потому что не было места, чтобы положить их туда, куда они должны были пойти.Эти ряды элементов, лантаноиды и актиниды, являются особыми переходными металлами. Верхняя строка идет с периодом 6, а нижняя строка — с периодом 7.
- Каждый элемент имеет свою плитку или ячейку в периодической таблице. Точная информация, предоставляемая для элемента, варьируется, но всегда есть атомный номер, символ элемента и атомный вес. Символ элемента представляет собой сокращенное обозначение, состоящее из одной заглавной буквы или заглавной буквы и строчной буквы. Исключение составляют элементы в самом конце периодической таблицы, у которых есть имена-заполнители (пока они не будут официально обнаружены и названы) и трехбуквенные символы.
- Двумя основными типами элементов являются металлы и неметаллы. Есть также элементы со свойствами, промежуточными между металлами и неметаллами. Эти элементы называют металлоидами или полуметаллами. Примеры групп элементов, которые являются металлами, включают щелочные металлы, щелочноземельные металлы, основные металлы и переходные металлы. Примерами групп элементов, которые не являются металлами, являются неметаллы (конечно), галогены и благородные газы.
Прогнозирование свойств
Даже если вы ничего не знаете о конкретном элементе, вы можете делать прогнозы на основе его положения в таблице и его отношения к элементам, которые вам знакомы.Например, вы можете ничего не знать об элементе осмий, но если вы посмотрите на его положение в периодической таблице, вы увидите, что он находится в той же группе (столбце), что и железо. Это означает, что у этих двух элементов есть общие свойства. Вы знаете, что железо — это плотный и твердый металл. Вы можете предсказать, что осмий также является плотным и твердым металлом.
По мере вашего прогресса в химии вам необходимо знать и другие тенденции в таблице Менделеева:
- Атомный радиус и ионный радиус увеличиваются при движении вниз по группе, но уменьшаются при перемещении по периоду.
- Сродство к электрону уменьшается по мере продвижения вниз по группе, но увеличивается по мере продвижения по периоду, пока вы не дойдете до последнего столбца. Элементы этой группы, благородные газы, практически не имеют сродства к электрону.
- Связанное свойство, электроотрицательность, уменьшается в группе вниз и увеличивается в течение периода. Благородные газы имеют практически нулевую электроотрицательность и сродство к электрону, потому что у них есть полные внешние электронные оболочки.
- Энергия ионизации уменьшается при движении вниз по группе, но увеличивается при перемещении по периоду.
- Элементы с наивысшим металлическим характером расположены в нижней левой части таблицы Менделеева. Элементы с наименее металлическим характером (наиболее неметаллические) находятся в верхней правой части таблицы.
| Определение, элементы, группы, сборы, тенденции и факты
Периодическая таблица , полностью Периодическая таблица элементов , в химии организованный массив всех химических элементов в порядке возрастания атомного номера — i.е., полное число протонов в атомном ядре. Когда химические элементы расположены таким образом, в их свойствах существует повторяющийся образец, называемый «периодическим законом», в котором элементы в одном столбце (группе) имеют схожие свойства. Первоначальное открытие, сделанное Дмитрием И. Менделеевым в середине XIX века, имело неоценимое значение для развития химии.
таблица МенделееваСовременная версия периодической таблицы элементов (для печати).
Британская энциклопедия, Inc.Популярные вопросы
Что такое таблица Менделеева?
Что общего у групп периодической таблицы?
Группы периодической таблицы отображаются в виде вертикальных столбцов, пронумерованных от 1 до 18. Элементы в группе имеют очень похожие химические свойства, которые возникают из числа присутствующих валентных электронов, то есть числа электронов в крайних электронах. оболочка атома.
Откуда взялась периодическая таблица Менделеева?
Расположение элементов в таблице Менделеева связано с их электронной конфигурацией.Из-за принципа исключения Паули не более двух электронов могут заполнить одну и ту же орбиталь. Первый ряд периодической таблицы состоит всего из двух элементов: водорода и гелия. Поскольку у атомов больше электронов, у них появляется больше орбит, доступных для заполнения, и поэтому строки содержат больше элементов, расположенных ниже в таблице.
Почему периодическая таблица Менделеева разделяется?
У периодической таблицы есть две строки внизу, которые обычно отделяются от основной части таблицы. Эти ряды содержат элементы ряда лантаноидов и актиноидов, обычно от 57 до 71 (от лантана до лютеция) и от 89 до 103 (от актиний до лоуренсия) соответственно.Для этого нет никаких научных причин. Это сделано только для того, чтобы стол стал более компактным.
Фактически не было признано до второго десятилетия 20-го века, что порядок элементов в периодической системе соответствует порядку их атомных номеров, целые числа которых равны положительным электрическим зарядам атомных ядер, выраженным в электронных единицах. . В последующие годы был достигнут большой прогресс в объяснении периодического закона с точки зрения электронного строения атомов и молекул.Это разъяснение повысило ценность закона, который используется сегодня так же активно, как и в начале 20 века, когда он выражал единственную известную взаимосвязь между элементами.
История периодического закона
В первые годы XIX века произошло быстрое развитие аналитической химии — искусства различения различных химических веществ — и, как следствие, накопление обширных знаний о химических и физических свойствах как элементы, так и соединения.Столь быстрое расширение химических знаний вскоре потребовало классификации, поскольку на классификации химических знаний основана не только систематизированная химическая литература, но и лабораторные искусства, посредством которых химия передается как живая наука от одного поколения химиков к другому. Связи между соединениями обнаруживались легче, чем между элементами; так получилось, что классификация элементов на много лет отстала от классификации соединений. Фактически, между химиками не было достигнуто общего согласия относительно классификации элементов в течение почти полувека после того, как системы классификации соединений стали общепринятыми.
интерактивная таблица МенделееваСовременная версия периодической таблицы элементов. Чтобы узнать название элемента, атомный номер, электронную конфигурацию, атомный вес и многое другое, выберите элемент из таблицы.
Encyclopædia Britannica, Inc.J.W. Доберейнер в 1817 году показал, что объединяющий вес, означающий атомный вес, стронция находится посередине между весом кальция и бария, а несколько лет спустя он показал, что существуют другие такие «триады» (хлор, бром и йод [галогены] и литий, натрий и калий [щелочные металлы]).Ж.-Б.-А. Дюма, Л. Гмелин, Э. Ленссен, Макс фон Петтенкофер и Дж. П. Кук расширили предложения Доберейнера между 1827 и 1858 годами, показав, что аналогичные отношения простираются дальше, чем триады элементов: фтор добавляется к галогенам, а магний — к щелочноземельным элементам. металлы, тогда как кислород, сера, селен и теллур были отнесены к одному семейству, а азот, фосфор, мышьяк, сурьма и висмут — к другому семейству элементов.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту.Подпишись сейчасПозднее были предприняты попытки показать, что атомные веса элементов могут быть выражены арифметической функцией, и в 1862 году А.-Э.-Б. де Шанкуртуа предложил классификацию элементов, основанную на новых значениях атомных весов, данных системой Станислао Канниццаро 1858 года. Де Шанкуртуа нанес атомные веса на поверхность цилиндра с окружностью 16 единиц, что соответствует приблизительному атомному весу кислород. Получившаяся спиральная кривая привела тесно связанные элементы в соответствующие точки над или под друг друга на цилиндре, и он предположил, как следствие, что «свойства элементов являются свойствами чисел», что является замечательным предсказанием в свете современных знаний.
Классификация элементов
В 1864 году J.A.R. Ньюлендс предложил классифицировать элементы в порядке возрастания атомного веса, при этом элементам присваиваются порядковые номера от единицы и выше и разделены на семь групп, обладающих свойствами, тесно связанными с первыми семью из известных на тот момент элементов: водород, литий, бериллий, бор, углерод. , азот и кислород. Это соотношение было названо законом октав по аналогии с семью интервалами музыкальной гаммы.
Затем в 1869 году, в результате обширной корреляции свойств и атомных весов элементов, уделяя особое внимание валентности (то есть количеству одинарных связей, которые может образовывать элемент), Менделеев предложил периодический закон: посредством которого «элементы, расположенные в соответствии с величиной атомного веса, демонстрируют периодическое изменение свойств». Лотар Мейер независимо пришел к аналогичному выводу, опубликованному после появления статьи Менделеева.
% PDF-1.4 % 1 0 obj > эндобдж 2 0 obj > эндобдж 3 0 obj > эндобдж 4 0 obj > /Шрифт > >> /Группа > >> эндобдж 5 0 obj > /Шрифт > / XObject > >> /Группа > >> эндобдж 6 0 obj > /Шрифт > >> /Группа > >> эндобдж 7 0 объект > /Шрифт > >> /Группа > >> эндобдж 8 0 объект > /Шрифт > / XObject > >> /Группа > >> эндобдж 9 0 объект > /Шрифт > >> /Группа > >> эндобдж 10 0 obj > /Шрифт > >> /Группа > >> эндобдж 11 0 объект > /Шрифт > / XObject > >> /Группа > >> эндобдж 12 0 объект > / XObject > /Шрифт > >> /Группа > >> эндобдж 13 0 объект > /Шрифт > / XObject > >> /Группа > >> эндобдж 14 0 объект > / XObject > /Шрифт > >> /Группа > >> эндобдж 15 0 объект > /Шрифт > / XObject > >> /Группа > >> эндобдж 16 0 объект > транслировать конечный поток эндобдж 17 0 объект > транслировать конечный поток эндобдж 18 0 объект > транслировать конечный поток эндобдж 19 0 объект > транслировать конечный поток эндобдж 20 0 объект > транслировать конечный поток эндобдж 21 0 объект > транслировать конечный поток эндобдж 22 0 объект > транслировать конечный поток эндобдж 23 0 объект > транслировать конечный поток эндобдж 24 0 объект > транслировать конечный поток эндобдж 25 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1.1 нед. 0 Дж 0 Дж [] 0 дн. / GS0 гс 0 0 мес. 0 0 л S Q Q конечный поток эндобдж 26 0 объект > эндобдж 27 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1,1 Вт 0 Дж 0 Дж [] 0 дн. / GS0 гс 20,25 57,75 м 591,75 57,75 л S Q Q конечный поток эндобдж 28 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1,1 Вт 0 Дж 0 Дж [] 0 дн. / GS0 гс 20,25 753 м 591,75 753 л S Q Q конечный поток эндобдж 29 0 объект > транслировать конечный поток эндобдж 30 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 109,6934 тд тдж ET Q Q конечный поток эндобдж 31 0 объект > эндобдж 32 0 объект > эндобдж 33 0 объект > транслировать / CIDInit / ProcSet findresource begin 12 дикт начать begincmap / CIDSystemInfo> def / CMapName / Adobe-Identity-UCS def / CMapType 2 def 1 начало кода endcodespacerange 72 beginbfrange конец endcmap CMapName currentdict / CMap defineresource pop end end конечный поток эндобдж 34 0 объект > / FontDescriptor 32 0 R / BaseFont / LXMDQH + TimesNewRoman / Вт [3 [250] 5 [408] 10 [180] 11 [333] 12 [333] 15 [250] 16 [333] 17 [250] 18 [277] 19 [500] 20 [500] 21 [500] ] 22 [500] 23 [500] 24 [500] 25 [500] 26 [500] 27 [500] 28 [500] 29 [277] 34 [443] 36 [722] 37 [666] 38 [666] 39 [722] 40 [610] 41 [556] 42 [722] 43 [722] 44 [333] 45 [389] 46 [722] 47 [610] 48 [889] 49 [722] 50 [722] 51 [556] ] 53 [666] 54 [556] 55 [610] 56 [722] 58 [943] 59 [722] 61 [610] 68 [443] 69 [500] 70 [443] 71 [500] 72 [443] 73 [333] 74 [500] 75 [500] 76 [277] 77 [277] 78 [500] 79 [277] 80 [777] 81 [500] 82 [500] 83 [500] 84 [500] 85 [333] ] 86 [389] 87 [277] 88 [500] 89 [500] 90 [722] 91 [500] 92 [500] 93 [443] 135 [350] 182 [333]] >> эндобдж 35 0 объект > эндобдж 36 0 объект > транслировать конечный поток эндобдж 37 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 109.6934 Td Tj ET Q Q конечный поток эндобдж 38 0 объект > транслировать конечный поток эндобдж 39 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 125,4434 тд тдж ET Q Q конечный поток эндобдж 40 0 объект > эндобдж 41 0 объект > транслировать / CIDInit / ProcSet findresource begin 12 дикт начать begincmap / CIDSystemInfo> def / CMapName / Adobe-Identity-UCS def / CMapType 2 def 1 начало кода endcodespacerange 49 начало конец endcmap CMapName currentdict / CMap defineresource pop end end конечный поток эндобдж 42 0 объект > / FontDescriptor 40 0 R / BaseFont / HZMLEJ + TimesNewRoman, полужирный / Вт [3 [250] 12 [333] 15 [250] 17 [250] 19 [500] 20 [500] 21 [500] 23 [500] 25 [500] 26 [500] 27 [500] 36 [722]) ] 37 [666] 38 [722] 39 [722] 40 [666] 44 [389] 45 [500] 46 [777] 48 [943] 49 [722] 50 [777] 51 [610] 54 [556] 55 [666] 68 [500] 69 [556] 70 [443] 71 [556] 72 [443] 73 [333] 74 [500] 75 [556] 76 [277] 78 [556] 79 [277] 80 [833] ] 81 [556] 82 [500] 83 [556] 85 [443] 86 [389] 87 [333] 88 [556] 89 [500] 90 [722] 91 [500] 92 [500] 93 [443]] >> эндобдж 43 0 объект > эндобдж 44 0 объект > транслировать конечный поток эндобдж 45 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 125.4434 тд тдж ET Q Q конечный поток эндобдж 46 0 объект > транслировать конечный поток эндобдж 47 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 141.1934 Td Tj ET Q Q конечный поток эндобдж 48 0 объект > транслировать конечный поток эндобдж 49 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 141.1934 Td Tj ET Q Q конечный поток эндобдж 50 0 объект > транслировать конечный поток эндобдж 51 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 156.9434 тд тдж ET Q Q конечный поток эндобдж 52 0 объект > транслировать конечный поток эндобдж 53 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 156.9434 Td Tj ET Q Q конечный поток эндобдж 54 0 объект > транслировать конечный поток эндобдж 55 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29,25 74,4434 тд тдж ET Q Q конечный поток эндобдж 56 0 объект > транслировать конечный поток эндобдж 57 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 74,4434 тд тдж ET Q Q конечный поток эндобдж 58 0 объект > транслировать конечный поток эндобдж 59 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 88.6934 тд тдж ET Q Q конечный поток эндобдж 60 0 объект > транслировать конечный поток эндобдж 61 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 212.4434 тд тдж ET Q Q конечный поток эндобдж 62 0 объект > транслировать конечный поток эндобдж 63 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 212,4434 тд тдж ET Q Q конечный поток эндобдж 64 0 объект > транслировать конечный поток эндобдж 65 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 228.1934 Td Tj ET Q Q конечный поток эндобдж 66 0 объект > транслировать конечный поток эндобдж 67 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 228.1934 Td Tj ET Q Q конечный поток эндобдж 68 0 объект > транслировать конечный поток эндобдж 69 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 243.9434 Td Tj ET Q Q конечный поток эндобдж 70 0 объект > транслировать конечный поток эндобдж 71 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 243,9434 тд тдж ET Q Q конечный поток эндобдж 72 0 объект > транслировать конечный поток эндобдж 73 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 259.6934 тд тдж ET Q Q конечный поток эндобдж 74 0 объект > транслировать конечный поток эндобдж 75 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 259.6934 тд тдж ET Q Q конечный поток эндобдж 76 0 объект > транслировать конечный поток эндобдж 77 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29.25 177.1934 Td Tj ET Q Q конечный поток эндобдж 78 0 объект > транслировать конечный поток эндобдж 79 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 177.1934 Td Tj ET Q Q конечный поток эндобдж 80 0 объект > транслировать конечный поток эндобдж 81 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 191.4434 тд тдж ET Q Q конечный поток эндобдж 82 0 объект > транслировать конечный поток эндобдж 83 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 315.1934 Td Tj ET Q Q конечный поток эндобдж 84 0 объект > транслировать конечный поток эндобдж 85 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 315.1934 Td Tj ET Q Q конечный поток эндобдж 86 0 объект > транслировать конечный поток эндобдж 87 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 315.1934 Td Tj ET Q Q конечный поток эндобдж 88 0 объект > транслировать конечный поток эндобдж 89 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 315.1934 Td Tj ET Q Q конечный поток эндобдж 90 0 объект > транслировать конечный поток эндобдж 91 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 330,9434 тд тдж ET Q Q конечный поток эндобдж 92 0 объект > транслировать конечный поток эндобдж 93 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 330.9434 Td Tj ET Q Q конечный поток эндобдж 94 0 объект > транслировать конечный поток эндобдж 95 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 330.9434 Td Tj ET Q Q конечный поток эндобдж 96 0 объект > транслировать конечный поток эндобдж 97 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 330.9434 Td Tj ET Q Q конечный поток эндобдж 98 0 объект > транслировать конечный поток эндобдж 99 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29,25 279,9434 тд тдж ET Q Q конечный поток эндобдж 100 0 объект > транслировать конечный поток эндобдж 101 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 279.9434 Td Tj ET Q Q конечный поток эндобдж 102 0 объект > транслировать конечный поток эндобдж 103 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 294.1934 Td Tj ET Q Q конечный поток эндобдж 104 0 объект > транслировать конечный поток эндобдж 105 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 386.4434 тд тдж ET Q Q конечный поток эндобдж 106 0 объект > транслировать конечный поток эндобдж 107 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 386.4434 тд тдж ET Q Q конечный поток эндобдж 108 0 объект > транслировать конечный поток эндобдж 109 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 159 386.4434 тд тдж ET Q Q конечный поток эндобдж 110 0 объект > транслировать конечный поток эндобдж 111 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 177 386,4434 тд тдж ET Q Q конечный поток эндобдж 112 0 объект > транслировать конечный поток эндобдж 113 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 402.1934 Td Tj ET Q Q конечный поток эндобдж 114 0 объект > транслировать конечный поток эндобдж 115 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 402.1934 Td Tj ET Q Q конечный поток эндобдж 116 0 объект > транслировать конечный поток эндобдж 117 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 402.1934 Td Tj ET Q Q конечный поток эндобдж 118 0 объект > транслировать конечный поток эндобдж 119 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 402.1934 Td Tj ET Q Q конечный поток эндобдж 120 0 объект > транслировать конечный поток эндобдж 121 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29.25 351.1934 Td Tj ET Q Q конечный поток эндобдж 122 0 объект > транслировать конечный поток эндобдж 123 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 351.1934 Td Tj ET Q Q конечный поток эндобдж 124 0 объект > транслировать конечный поток эндобдж 125 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 365.4434 тд тдж ET Q Q конечный поток эндобдж 126 0 объект > транслировать конечный поток эндобдж 127 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 457.6934 тд тдж ET Q Q конечный поток эндобдж 128 0 объект > транслировать конечный поток эндобдж 129 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 457.6934 тд тдж ET Q Q конечный поток эндобдж 130 0 объект > транслировать конечный поток эндобдж 131 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 457.6934 тд тдж ET Q Q конечный поток эндобдж 132 0 объект > транслировать конечный поток эндобдж 133 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 457.6934 Td Tj ET Q Q конечный поток эндобдж 134 0 объект > транслировать конечный поток эндобдж 135 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 473,4434 тд тдж ET Q Q конечный поток эндобдж 136 0 объект > транслировать конечный поток эндобдж 137 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 473,4434 тд тдж ET Q Q конечный поток эндобдж 138 0 объект > транслировать конечный поток эндобдж 139 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 473,4434 тд тдж ET Q Q конечный поток эндобдж 140 0 объект > транслировать конечный поток эндобдж 141 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 473.4434 тд тдж ET Q Q конечный поток эндобдж 142 0 объект > транслировать конечный поток эндобдж 143 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29,25 422,4434 тд тдж ET Q Q конечный поток эндобдж 144 0 объект > транслировать конечный поток эндобдж 145 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 422,4434 тд тдж ET Q Q конечный поток эндобдж 146 0 объект > транслировать конечный поток эндобдж 147 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 436.6934 тд тдж ET Q Q конечный поток эндобдж 148 0 объект > транслировать конечный поток эндобдж 149 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 514.6934 Td Tj ET Q Q конечный поток эндобдж 150 0 объект > транслировать конечный поток эндобдж 151 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 514.6934 тд тдж ET Q Q конечный поток эндобдж 152 0 объект > транслировать конечный поток эндобдж 153 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 514.6934 тд тдж ET Q Q конечный поток эндобдж 154 0 объект > транслировать конечный поток эндобдж 155 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 514.6934 тд тдж ET Q Q конечный поток эндобдж 156 0 объект > транслировать конечный поток эндобдж 157 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 530.4434 тд тдж ET Q Q конечный поток эндобдж 158 0 объект > транслировать конечный поток эндобдж 159 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 530,4434 тд тдж ET Q Q конечный поток эндобдж 160 0 объект > транслировать конечный поток эндобдж 161 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 159 530,4434 тд тдж ET Q Q конечный поток эндобдж 162 0 объект > транслировать конечный поток эндобдж 163 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 177 530,4434 тд тдж ET Q Q конечный поток эндобдж 164 0 объект > транслировать конечный поток эндобдж 165 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29.25 493,6934 тд тдж ET Q Q конечный поток эндобдж 166 0 объект > транслировать конечный поток эндобдж 167 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 493.6934 тд тдж ET Q Q конечный поток эндобдж 168 0 объект > транслировать конечный поток эндобдж 169 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 585.9434 тд тдж ET Q Q конечный поток эндобдж 170 0 объект > транслировать конечный поток эндобдж 171 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 585.9434 тд тдж ET Q Q конечный поток эндобдж 172 0 объект > транслировать конечный поток эндобдж 173 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 601.6934 Td Tj ET Q Q конечный поток эндобдж 174 0 объект > транслировать конечный поток эндобдж 175 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 601.6934 тд тдж ET Q Q конечный поток эндобдж 176 0 объект > транслировать конечный поток эндобдж 177 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 617,4434 тд тдж ET Q Q конечный поток эндобдж 178 0 объект > транслировать конечный поток эндобдж 179 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 617.4434 тд тдж ET Q Q конечный поток эндобдж 180 0 объект > транслировать конечный поток эндобдж 181 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 633.1934 Td Tj ET Q Q конечный поток эндобдж 182 0 объект > транслировать конечный поток эндобдж 183 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 633.1934 Td Tj ET Q Q конечный поток эндобдж 184 0 объект > транслировать конечный поток эндобдж 185 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29.25 550.6934 Td Tj ET Q Q конечный поток эндобдж 186 0 объект > транслировать конечный поток эндобдж 187 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 550,6934 тд тдж ET Q Q конечный поток эндобдж 188 0 объект > транслировать конечный поток эндобдж 189 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 564.9434 Td Tj ET Q Q конечный поток эндобдж 190 0 объект > транслировать конечный поток эндобдж 191 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 688.6934 тд тдж ET Q Q конечный поток эндобдж 192 0 объект > транслировать конечный поток эндобдж 193 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 688.6934 тд тдж ET Q Q конечный поток эндобдж 194 0 объект > транслировать конечный поток эндобдж 195 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 42 704.4434 тд тдж ET Q Q конечный поток эндобдж 196 0 объект > транслировать конечный поток эндобдж 197 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 60 704.4434 тд тдж ET Q Q конечный поток эндобдж 198 0 объект > транслировать конечный поток эндобдж 199 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 720.1934 Td Tj ET Q Q конечный поток эндобдж 200 0 объект > транслировать конечный поток эндобдж 201 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 720.1934 Td Tj ET Q Q конечный поток эндобдж 202 0 объект > транслировать конечный поток эндобдж 203 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 735.9434 тд тдж ET Q Q конечный поток эндобдж 204 0 объект > транслировать конечный поток эндобдж 205 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 60 735.9434 Td Tj ET Q Q конечный поток эндобдж 206 0 объект > транслировать конечный поток эндобдж 207 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29,25 653,4434 тд тдж ET Q Q конечный поток эндобдж 208 0 объект > транслировать конечный поток эндобдж 209 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 653,4434 тд тдж ET Q Q конечный поток эндобдж 210 0 объект > транслировать конечный поток эндобдж 211 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 42 667.6934 тд тдж ET Q Q конечный поток эндобдж 212 0 объект > транслировать конечный поток эндобдж 213 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 327.75 109,6934 тд тдж ET Q Q конечный поток эндобдж 214 0 объект > транслировать конечный поток эндобдж 215 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 345,75 109,6934 Тд Тдж ET Q Q конечный поток эндобдж 216 0 объект > транслировать конечный поток эндобдж 217 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 444,75 109,6934 тд тдж ET Q Q конечный поток эндобдж 218 0 объект > транслировать конечный поток эндобдж 219 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 462,75 109,6934 Тд Тдж ET Q Q конечный поток эндобдж 220 0 объект > транслировать конечный поток эндобдж 221 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 327.75 125,4434 тд тдж ET Q Q конечный поток эндобдж 222 0 объект > транслировать конечный поток эндобдж 223 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 345,75 125,4434 тд тдж ET Q Q конечный поток эндобдж 224 0 объект > транслировать конечный поток эндобдж 225 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 444,75 125,4434 тд тдж ET Q Q конечный поток эндобдж 226 0 объект > транслировать конечный поток эндобдж 227 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 462,75 125,4434 тд тдж ET Q Q конечный поток эндобдж 228 0 объект > транслировать конечный поток эндобдж 229 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 315 74.4434 тд тдж ET Q Q конечный поток эндобдж 230 0 объект > транслировать конечный поток эндобдж 231 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 327,75 74,4434 тд тдж ET Q Q конечный поток эндобдж 232 0 объект > транслировать конечный поток эндобдж 233 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 327,75 88,6934 тд тдж ET Q Q конечный поток эндобдж 234 0 объект > транслировать конечный поток эндобдж 235 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 333,75 166,6934 Td Tj ET Q Q конечный поток эндобдж 236 0 объект > транслировать конечный поток эндобдж 237 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 351.75 166.6934 тд тдж ET Q Q конечный поток эндобдж 238 0 объект > транслировать конечный поток эндобдж 239 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333,75 182,4434 тд тдж ET Q Q конечный поток эндобдж 240 0 объект > транслировать конечный поток эндобдж 241 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351,75 182,4434 тд тдж ET Q Q конечный поток эндобдж 242 0 объект > транслировать конечный поток эндобдж 243 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 198.1934 Td Tj ET Q Q конечный поток эндобдж 244 0 объект > транслировать конечный поток эндобдж 245 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351.75 198.1934 Td Tj ET Q Q конечный поток эндобдж 246 0 объект > транслировать конечный поток эндобдж 247 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351,75 212,4434 Тд Тдж ET Q Q конечный поток эндобдж 248 0 объект > транслировать конечный поток эндобдж 249 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 228.1934 Td Tj ET Q Q конечный поток эндобдж 250 0 объект > транслировать конечный поток эндобдж 251 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351.75 228.1934 Td Tj ET Q Q конечный поток эндобдж 252 0 объект > транслировать конечный поток эндобдж 253 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351.75 242,4434 тд тдж ET Q Q конечный поток эндобдж 254 0 объект > транслировать конечный поток эндобдж 255 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 315 145.6934 тд тдж ET Q Q конечный поток эндобдж 256 0 объект > транслировать конечный поток эндобдж 257 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333,75 145,6934 тд тдж ET Q Q конечный поток эндобдж 258 0 объект > транслировать конечный поток эндобдж 259 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333 297,9434 тд тдж ET Q Q конечный поток эндобдж 260 0 объект > транслировать конечный поток эндобдж 261 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351 297.9434 Td Tj ET Q Q конечный поток эндобдж 262 0 объект > транслировать конечный поток эндобдж 263 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 447,75 297,9434 тд тдж ET Q Q конечный поток эндобдж 264 0 объект > транслировать конечный поток эндобдж 265 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 465,75 297,9434 тд тдж ET Q Q конечный поток эндобдж 266 0 объект > транслировать конечный поток эндобдж 267 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 333 313.6934 тд тдж ET Q Q конечный поток эндобдж 268 0 объект > транслировать конечный поток эндобдж 269 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 351 313.6934 Td Tj ET Q Q конечный поток эндобдж 270 0 объект > транслировать конечный поток эндобдж 271 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 447,75 313,6934 тд тдж ET Q Q конечный поток эндобдж 272 0 объект > транслировать конечный поток эндобдж 273 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 465,75 313,6934 тд тдж ET Q Q конечный поток эндобдж 274 0 объект > транслировать конечный поток эндобдж 275 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 315 262,6934 тд тдж ET Q Q конечный поток эндобдж 276 0 объект > транслировать конечный поток эндобдж 277 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333 262.6934 Td Tj ET Q Q конечный поток эндобдж 278 0 объект > транслировать конечный поток эндобдж 279 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333 276.9434 тд тдж ET Q Q конечный поток эндобдж 280 0 объект > транслировать конечный поток эндобдж 281 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 369.1934 Td Tj ET Q Q конечный поток эндобдж 282 0 объект > транслировать конечный поток эндобдж 283 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351.75 369.1934 Td Tj ET Q Q конечный поток эндобдж 284 0 объект > транслировать конечный поток эндобдж 285 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 447.75 369.1934 Td Tj ET Q Q конечный поток эндобдж 286 0 объект > транслировать конечный поток эндобдж 287 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 465.75 369.1934 Td Tj ET Q Q конечный поток эндобдж 288 0 объект > транслировать конечный поток эндобдж 289 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 333,75 384,9434 тд тдж ET Q Q конечный поток эндобдж 290 0 объект > транслировать конечный поток эндобдж 291 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 351,75 384,9434 Td Tj ET Q Q конечный поток эндобдж 292 0 объект > транслировать конечный поток эндобдж 293 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 447.75 384.9434 тд тдж ET Q Q конечный поток эндобдж 294 0 объект > транслировать конечный поток эндобдж 295 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 465,75 384,9434 Td Tj ET Q Q конечный поток эндобдж 296 0 объект > транслировать конечный поток эндобдж 297 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 315 333,9434 тд тдж ET Q Q конечный поток эндобдж 298 0 объект > транслировать конечный поток эндобдж 299 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333,75 333,9434 Тд Тдж ET Q Q конечный поток эндобдж 300 0 объект > транслировать конечный поток эндобдж 301 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 348.1934 Td Tj ET Q Q конечный поток эндобдж 302 0 объект > транслировать конечный поток эндобдж 303 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333,75 440,4434 тд тдж ET Q Q конечный поток эндобдж 304 0 объект > транслировать конечный поток эндобдж 305 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351,75 440,4434 тд тдж ET Q Q конечный поток эндобдж 306 0 объект > транслировать конечный поток эндобдж 307 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 447,75 440,4434 тд тдж ET Q Q конечный поток эндобдж 308 0 объект > транслировать конечный поток эндобдж 309 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 465.75 440,4434 тд тдж ET Q Q конечный поток эндобдж 310 0 объект > транслировать конечный поток эндобдж 311 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 456.1934 Td Tj ET Q Q конечный поток эндобдж 312 0 объект > транслировать конечный поток эндобдж 313 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 351.75 456.1934 Td Tj ET Q Q конечный поток эндобдж 314 0 объект > транслировать конечный поток эндобдж 315 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 447.75 456.1934 Td Tj ET Q Q конечный поток эндобдж 316 0 объект > транслировать конечный поток эндобдж 317 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 465.75 456.1934 Td Tj ET Q Q конечный поток эндобдж 318 0 объект > транслировать конечный поток эндобдж 319 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 315 405.1934 Td Tj ET Q Q конечный поток эндобдж 320 0 объект > транслировать конечный поток эндобдж 321 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333.75 405.1934 Td Tj ET Q Q конечный поток эндобдж 322 0 объект > транслировать конечный поток эндобдж 323 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 333,75 419,4434 тд тдж ET Q Q конечный поток эндобдж 324 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1 нед. 0 Дж 0 Дж [] 0 дн. / GS0 гс 306 63.75 кв.м. 306 747 л S Q Q конечный поток эндобдж 325 0 объект > транслировать конечный поток эндобдж 326 0 объект > транслировать конечный поток эндобдж 327 0 объект > транслировать конечный поток эндобдж 328 0 объект > транслировать конечный поток эндобдж 329 0 объект > транслировать конечный поток эндобдж 330 0 объект > транслировать конечный поток эндобдж 331 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1,1 Вт 0 Дж 0 Дж [] 0 дн. / GS0 гс 0 0 мес. 0 0 л S Q Q конечный поток эндобдж 332 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1,1 Вт 0 Дж 0 Дж [] 0 дн. / GS0 гс 20,25 39 м 591.75 39 л S Q Q конечный поток эндобдж 333 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q 1.1 нед. 0 Дж 0 Дж [] 0 дн. / GS0 гс 20,25 753 м 591,75 753 л S Q Q конечный поток эндобдж 334 0 объект > транслировать конечный поток эндобдж 335 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 48 250,6934 тд тдж ET Q Q конечный поток эндобдж 336 0 объект > транслировать конечный поток эндобдж 337 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 66 250,6934 тд тдж ET Q Q конечный поток эндобдж 338 0 объект > транслировать конечный поток эндобдж 339 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 145.5 250,6934 тд тдж ET Q Q конечный поток эндобдж 340 0 объект > транслировать конечный поток эндобдж 341 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 163,5 250,6934 тд тдж ET Q Q конечный поток эндобдж 342 0 объект > транслировать конечный поток эндобдж 343 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 243 250,6934 тд тдж ET Q Q конечный поток эндобдж 344 0 объект > транслировать конечный поток эндобдж 345 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F1 -12 Тс 261 250,6934 тд тдж ET Q Q конечный поток эндобдж 346 0 объект > транслировать конечный поток эндобдж 347 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 340.5 250,6934 тд тдж ET Q Q конечный поток эндобдж 348 0 объект > транслировать конечный поток эндобдж 349 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 358,5 250,6934 тд тдж ET Q Q конечный поток эндобдж 350 0 объект > транслировать конечный поток эндобдж 351 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 29.25 55.6934 Td Tj ET Q Q конечный поток эндобдж 352 0 объект > транслировать конечный поток эндобдж 353 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q BT / GS1 GS / F0 -12 Тс 48 55.6934 тд тдж ET Q Q конечный поток эндобдж 354 0 объект > транслировать q 1 0 0-1 0 792 см -100 Тлз q q 384 0 0 -144.75 48204 см / I0 Do Q Q Q конечный поток эндобдж 355 0 объект > транслировать xo_ «R $ RP» (V * Pd9AO + HGG08 [S, xkh * sS ~ [b4I1ybgΞc {f ~ W̚Z {f 8
Periodic Table | Grandinetti Group
] Еще до того, как мы получили это хорошее понимание атомной структуры, Ученые определили определенные вещества как элементов . Таким образом, было много попыток расположить известные элементы так, чтобы существовала некоторая корреляция между их известными свойствами.Первая достаточно успешная попытка была сделана Дмитрием Менделеевым в 1869 году.У него была идея расположить элементы в порядке , увеличивая атомную массу , и, что наиболее важно, обнаружил, что элементы со схожими химическими и физическими свойствами периодически встречаются и . Он расположили эти похожие элементы друг под другом в столбцы.
В 1914 году Генри Мозли определил, что лучше расположить атомный номер , увеличивая атомный номер , что дает нам периодическую таблицу, которую мы имеем сегодня. Мы можем определить периодическую таблицу как , расположение элементов в порядке увеличения атомного номера, поместив элементы с аналогичными химическими и физическими свойствами в столбцы.
Характеристики Периодической таблицы элементов
Группы
Вертикальные столбцы называются группами. Элементы внутри группы имеют схожие химические и физические свойства. Группы обозначаются вверху цифрами 1-8 и буквами A и B. (Примечание: маркировка групп несколько произвольна, поэтому следите за другими обозначениями, особенно с A и B.)
Элементы группы A — Элементы репрезентативной или основной группы
Элементы группы В — Переходные элементы
Помимо буквенно-цифрового обозначения, некоторые группы имеют собственное название.
| 1A | → | щелочные металлы |
| 2A | → | щелочные земли |
| 7A | → | галогены |
| 8A | → | благородные газы или инертные газы |
Периоды
Горизонтальные строки называются периодами . Периоды обозначены числами слева в периодической таблице. Два длинных ряда, расположенные чуть ниже основной части стола, представляют собой внутренние переходные элементы
.Элементы 58-71 относятся к серии лантанидов
Элементы 90-103 относятся к серии актинидов
Три категории элементов
Есть три широкие категории элементов, которые называются
.- Металлы
- Неметаллы
- Металлоиды
Чтобы отделить металлы от неметаллов, мы проводим ступенчатую линию слева и ниже B, Si, As, Te и At.
Эта классификация или группа полезны, потому что определенные свойства связаны с каждой категорией.
Металлы
- твердые вещества при комнатной температуре (кроме Hg)
- металлический глянец
- ковкий и пластичный
- хорошие проводники тепла и электричества
Неметаллы
- газы или твердые вещества при комнатной температуре (кроме Br 2 )
- разнообразия цвета и внешнего вида
- хрупкие твердые вещества
- изоляторы (плохие проводники)
Металлоиды
- промежуточное звено по свойствам между металлами и неметаллами
- твердых частиц при комнатной температуре
- многие имеют более одной конструкции (одна металлическая, другая неметаллическая)
- некоторые полупроводники
Домашнее задание от
Chemisty, The Central Science, 10-е изд.


 6.В ряду химических элементов Ве → Мg → Са:
6.В ряду химических элементов Ве → Мg → Са:
Leave A Comment