Опасный тандем: никогда не сочетайте отбеливатель и уксус при чистке
Узнайте, почему эта чистящая комбинация двух отличных очистителей представляет опасность, которая может случиться при очистке дома.
Мощные скопления грязи, жира, плесени и грибков требуют мощных бытовых чистящих средств. И, скорее всего, у нас есть два самых мощных – отбеливатель и уксус. Используемые отдельно, эти чистящие средства безопасны и эффективны на кухне, в ванной комнате и за ее пределами. Но смешанные, умышленно или случайно, они объединяются, чтобы создать токсичный, потенциально смертельный продукт.
Хлорный отбеливатель полезен своими дезинфицирующими и осветляющими свойствами, а уксус известен своими дезодорирующими свойствами, удаляющими пятна. Поэтому неудивительно, что люди могут смешивать их в надежде создать мощный универсальный очиститель. И это большая ошибка.
Активным ингредиентом хлорного отбеливателя является щелочное химическое соединение гипохлорита натрия. Когда порошкообразный или жидкий хлорный отбеливатель смешивается с кислотой, в данном случае уксусом (уксусной кислотой), гипохлорит натрия превращается в хлорноватистую кислоту, которая выделяет газообразный хлор в окружающий воздух. Газообразный хлор очень токсичен — настолько, что во время Первой мировой войны его мощный вариант использовался в траншейной войне, чтобы выбить войска союзников. Газ выделяет чрезвычайно резкий запах, и, хотя в больших объемах он выглядит желто-зеленым, в небольших количествах он невидим.
Газообразный хлор очень токсичен — настолько, что во время Первой мировой войны его мощный вариант использовался в траншейной войне, чтобы выбить войска союзников. Газ выделяет чрезвычайно резкий запах, и, хотя в больших объемах он выглядит желто-зеленым, в небольших количествах он невидим.
Воздействие газообразного хлора может вызвать следующие симптомы:
• Жжение, покраснение или образование пузырей на коже.
• Ощущение жжения в глазах, носу и горле
• Стеснение в груди
• Затрудненное дыхание
• Тошнота и рвота
Длительное воздействие может привести к отеку легких (то есть накоплению жидкости в легких), что может привести к летальному исходу.
Как правило, уровень газового воздействия и тяжесть симптомов являются наибольшими, когда отбеливатель полной прочности (то есть неразбавленный) смешивают с уксусом. Однако риск воздействия газообразного хлора сохраняется, когда разбавленный водой отбеливатель смешивают с уксусом.
Как избежать несчастных случаев
Даже если вы сознательно не смешиваете отбеливатель и уксус, могут быть случайные смешения, когда вы можете смешать чистящие средства во время ежедневных домашних дел. Вот несколько советов, как разделить два мощных чистящих средства в некоторых наиболее распространенных сценариях, когда это может произойти.
Вот несколько советов, как разделить два мощных чистящих средства в некоторых наиболее распространенных сценариях, когда это может произойти.
• Используйте либо уксус, либо отбеливатель, но не оба одновременно, за один цикл очистки или стирки.
• Чтобы удалить стойкие пятна или осветлить белые ткани, некоторые люди предварительно обрабатывают моющиеся средства уксусом, а затем бросают полстакана отбеливателя в дозатор отбеливателя стиральной машины. Но смесь уксуса в одежде и отбеливателя в воде для стирки может выделять газообразный хлор в машину, и вы рискуете подвергнуться воздействию паров при удалении загрузки белья.
• Всегда сначала чистите и высушивайте внутренние компоненты кофеварки, а затем переходите к чистке внешней части устройства.
• Тщательно вымойте и высушите разделочные доски перед использованием уксуса во время приготовления пищи.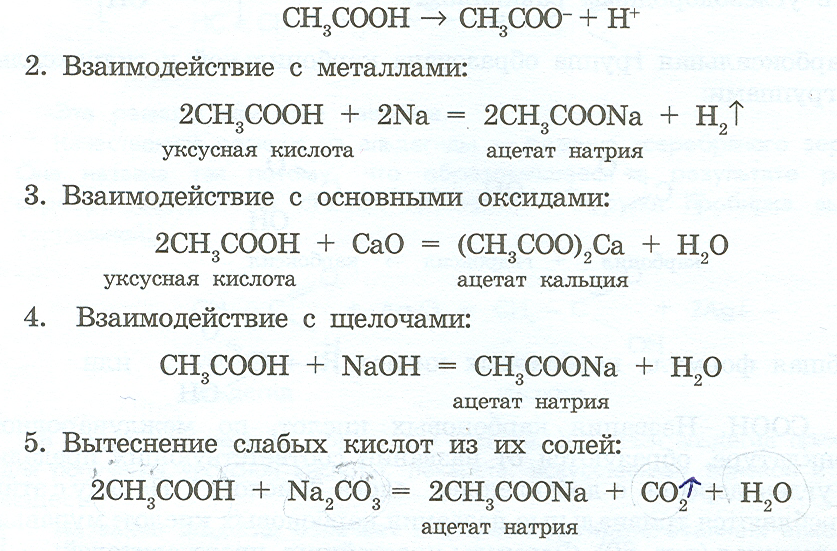 Но ни в коем случае не дезинфицируйте доски для разделки мяса с помощью одной чайной ложки отбеливателя и полгаллона воды, а затем уксусом – это опасно для здоровья.
Но ни в коем случае не дезинфицируйте доски для разделки мяса с помощью одной чайной ложки отбеливателя и полгаллона воды, а затем уксусом – это опасно для здоровья.
• При подготовке ванной комнаты дезинфицирующее средство – спрей из уксуса, смешанного наполовину с водой.
• Пометьте все контейнеры с отбеливателем или уксусом и храните их (и все чистящие средства) в недоступном для детей месте.
• При заправке немаркированных бутылок чистящего средства в шкафу для снабжения вы можете случайно добавить уксус в бутылку, в которой уже содержится небольшое количество отбеливателя, или наоборот.

Безопасное применение отбеливателя и уксуса
Сильно загрязненные поверхности могут выиграть от применения уксуса после применения отбеливателя или наоборот. Чтобы использовать отбеливатель и уксус по отдельности, один за другим полностью промойте первое чистящее средство с поверхности водой и высушите его перед нанесением другого, чтобы предотвратить смешивание и выделение газообразного хлора.
Рассмотрим грязные кафельные полы или душевые стены, например. Возможно, вы захотите использовать раствор из равных частей хлорного отбеливателя и воды, чтобы удалить плесень из раствора и продезинфицировать сами плитки с помощью раствора половинного стакана уксуса и одного галлона воды. В этом сценарии сначала обработайте раствором отбеливателя, промойте его простой водой до тех пор, пока не останется один раствор отбеливателя, высушите раствор полотенцами или полностью высушите на воздухе, и только затем нанесите раствор уксуса на плитки.
Хлоруксусная кислота, структурная формула, химические свойства
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
t°кип=4830°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
ФосфорФосфор
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
19
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип=3260°C
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
t°кип=907°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°пл=217°C
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d10
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s2 5p2
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Эффективные чистящие средства, которые вместе становятся смертельными
Отбеливатель и уксус — обычные бытовые чистящие средства, используемые для дезинфекции поверхностей, удаления грязи и удаления пятен. Несмотря на то, что у многих людей дома есть оба эти чистящих средства, смешивание их вместе потенциально опасно, и его следует избегать.
Тип отбеливателя, обычно используемого для бытовой уборки, состоит из гипохлорита натрия, разбавленного водой от 3 до 8%. Уксус представляет собой разбавленную форму уксусной кислоты. Когда гипохлорит натрия смешивается с уксусной кислотой или любым другим типом кислоты, он выделяет потенциально смертельный газообразный хлор.
В 2016 году Американская ассоциация токсикологических центров сообщила о более чем 6300 случаях воздействия газообразного хлора. Около 35% этих воздействий были вызваны смешиванием бытовых чистящих средств.
Продолжайте читать, чтобы узнать, есть ли ситуации, когда можно смешивать отбеливатель и уксус, и что делать, если вы случайно вдохнули газообразный хлор.
Отбеливатель может относиться к любому химическому веществу, которое используется для избавления от пятен или дезинфекции поверхностей. Наиболее типичной формой, используемой в качестве очистителя, является гипохлорит натрия. Сам по себе отбеливатель может повредить кожу, но не токсичен при вдыхании. Однако при смешивании с другими бытовыми чистящими средствами его вдыхание может привести к летальному исходу.
Гипохлорит натрия состоит из атомов натрия, кислорода и хлора. Когда эта молекула смешивается с уксусной кислотой в уксусе или другими типами кислоты, она выделяет газообразный хлор. Газообразный хлор чрезвычайно опасен для здоровья человека. Он настолько силен, что Германия использовала его во время Первой мировой войны в качестве химического оружия.
Уксус — не единственное чистящее средство, которое нужно осторожно смешивать с отбеливателем. Отбеливатель также реагирует с аммиаком с образованием газообразного хлора. Отбеливатель также может реагировать на некоторые чистящие средства для духовки, инсектициды и перекись водорода.
Многие бытовые чистящие средства содержат химическое вещество под названием лимонен, придающее им цитрусовый запах. Когда пары отбеливателя смешиваются с лимоненом, образуются мелкие частицы, которые могут нанести вред здоровью людей и животных. Однако необходимы дополнительные исследования для изучения потенциального риска для здоровья этих частиц.
По данным Департамента здравоохранения штата Вашингтон, даже низкий уровень газообразного хлора, менее 5 частей на миллион (промилле), может вызвать раздражение глаз, горла и носа. Никогда не рекомендуется смешивать эти два чистящих средства вместе.
В отличие от некоторых других опасных химических веществ, таких как окись углерода, хлор издает отчетливо резкий и раздражающий запах. Если вы заметили сильный запах после смешивания чистящих средств, рекомендуется немедленно покинуть это место.
Тяжесть симптомов, которые появляются у вас после вдыхания газообразного хлора, зависит от его концентрации, измеряемой в частях на миллион (ppm), и от того, как долго вы его вдыхаете.
- от 0,1 до 0,3 частей на миллион. На этом уровне люди могут чувствовать резкий запах газообразного хлора в воздухе.
- от 5 до 15 частей на миллион. Концентрация выше 5 частей на миллион вызывает раздражение слизистых оболочек рта и носа.
- Более 30 частей на миллион. При концентрации выше 30 частей на миллион газообразный хлор может вызывать боль в груди, одышку и кашель.
- Более 40 частей на миллион. Концентрация выше 40 частей на миллион может привести к потенциально опасному скоплению жидкости в легких.
- Более 430 частей на миллион . Вдыхание более 430 частей на миллион газообразного хлора может привести к летальному исходу в течение 30 минут.
- Более 1000 частей на миллион . Вдыхание газообразного хлора выше этого уровня может привести к немедленному летальному исходу.
Смешивать отбеливатель и уксус в стиральной машине — тоже плохая идея. Когда вы достаете одежду, из стиральной машины может выделяться газообразный хлор. Это также может оставить следы газообразного хлора на вашей одежде.
Когда вы достаете одежду, из стиральной машины может выделяться газообразный хлор. Это также может оставить следы газообразного хлора на вашей одежде.
Если вы используете отбеливатель для белья, рекомендуется подождать несколько загрузок, прежде чем использовать уксус.
Тяжесть симптомов, которые у вас разовьются после воздействия хлора, зависит от количества вдыхаемого газообразного хлора. Симптомы обычно начинаются довольно быстро. Большинство людей, подвергшихся воздействию небольшого количества газообразного хлора, выздоравливают без осложнений.
При относительно кратковременном воздействии газообразного хлора вы можете заметить раздражение носа, рта и горла. При глубоком вдыхании хлора может развиться раздражение легких.
По данным Центров по контролю и профилактике заболеваний, если вы случайно вдохнете хлор, вы можете испытать следующее:
- затуманенное зрение
- жжение в носу, горле или глазах
- кашель
- стеснение в твоя грудь
- затрудненное дыхание
- жидкость в легких
- тошнота
- рвота
- слезотечение
- свистящее дыхание
Нет лекарства от вдыхания газообразного хлора. Единственный вариант лечения — как можно быстрее удалить хлор из организма и немедленно обратиться за медицинской помощью для лечения симптомов.
Единственный вариант лечения — как можно быстрее удалить хлор из организма и немедленно обратиться за медицинской помощью для лечения симптомов.
Если вы вдыхаете газообразный хлор, выполните следующие действия, чтобы вывести хлор из организма:
- Немедленно отправляйтесь туда, где вы можете дышать свежим воздухом.
- Смените и постирайте всю одежду, которая могла быть загрязнена.
Неотложная медицинская помощьЕсли у вас серьезные симптомы, позвоните по номеру 911 или в Национальный столичный токсикологический центр (NCPC) по телефону 800-222-1222 и следуйте их инструкциям.
Пролитый отбеливатель может вызвать раздражение кожи. Вы можете предпринять следующие шаги, чтобы уменьшить вероятность развития осложнений:
- Снимите украшения или одежду, на которые попал отбеливатель, и очистите их после мытья кожи.
- Промойте кожу губкой или впитывающей тканью над раковиной.
- Во время чистки не прикасайтесь к другим частям тела, например к лицу.

- Немедленно обратитесь за медицинской помощью, если вы пролили отбеливатель в глаза или получили ожог кожи.
Уксус также может вызывать раздражение кожи. Несмотря на то, что это вряд ли вызовет какие-либо серьезные осложнения для здоровья, рекомендуется смыть уксус с кожи, чтобы избежать покраснения или болезненности.
При смешивании отбеливателя и уксуса образуется потенциально смертельный газообразный хлор. Если вы заметили резкий запах после смешивания бытовых чистящих средств, вам следует немедленно покинуть это место и попытаться подышать свежим воздухом.
Если вы или кто-то из ваших знакомых заметите какие-либо симптомы отравления газообразным хлором, рекомендуется немедленно позвонить по телефону 911 или в NCPC по телефону 800-222-1222 .
Химия 211 — неделя X
Лаборатория X:
Окисление и идентификация неизвестного спирта
Предварительная лаборатория Работа
Задание на чтение:
- Описание
эксперимента — см.
 ниже.
ниже. - Окисление
Реакции:
Hornback; 2-е изд.; стр. 380-385. теоретический
Предварительные вопросы:
(Пожалуйста, предоставьте ответы на эти вопросы по прибытии в лабораторию.)
2. Какова цель изопропанола в этом эксперименте?
3. Вам и вашему партнеру было поручено окислить следующие два спирта в вашей лаборатории окисления:
Какие 3 наиболее важные массы вы бы увидели в КАЖДОМ спектре масс продуктов окисления этих двух спиртов? Не могли бы вы отличить два окисленных продукта с помощью МС? Если да, то как?
Введение
В этом эксперименте вы будете использовать обычный бытовой отбеливатель.
в качестве окислителя. Большинство отбеливателей представляют собой водный раствор гипохлорита натрия.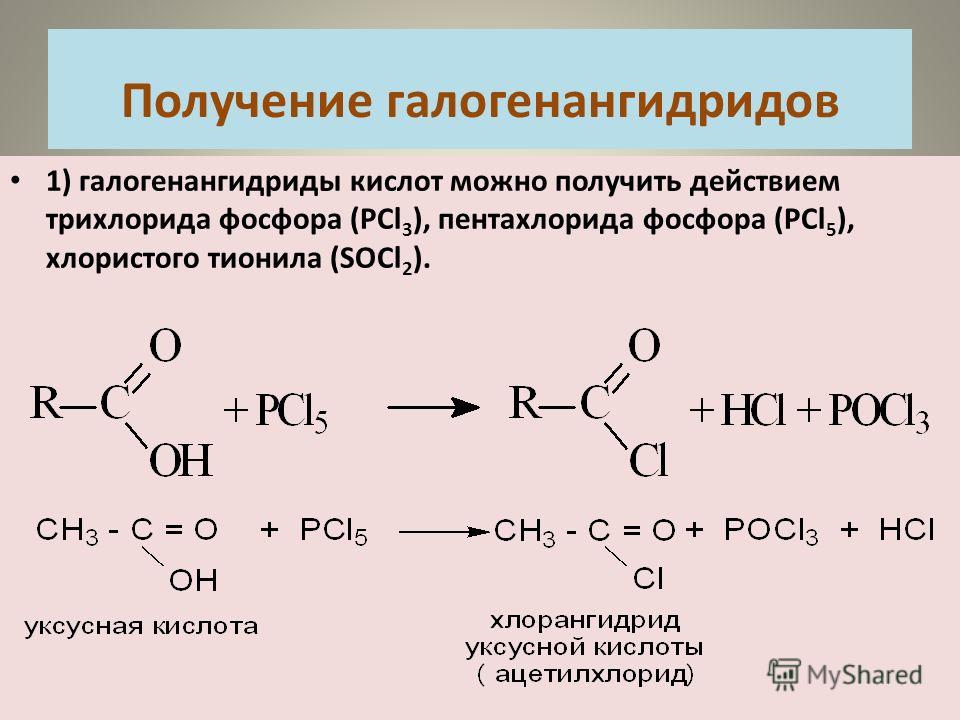 NaOCl (водн.). Это создается путем добавления хлора к гидроксиду натрия:
NaOCl (водн.). Это создается путем добавления хлора к гидроксиду натрия:
При гипохлорите натрия при добавлении к уксусной кислоте происходит следующая кислотно-щелочная реакция:
NaOCl, Cl2 и хлорноватистая кислота (HOCl) являются всеми возможными источниками положительно заряженных хлор (Cl + ). Хотя наличие дискретных ионов Cl + в водных растворах никогда не был обнаружен, очевидно, что ключевой этап в этих реакциях передача электронов с органического субстрата на Cl + вида для получения Cl —. Одно из возможных превращений окисления спирта с этими реагентами, на примере циклопентанола, является показано ниже:
Первый
шаг в механизме показывает замену гидроксильного протона на
положительный хлор. Следующим этапом является устранение HCl из
результирующий
алкилгипохлорита с образованием кетона, циклопентанона.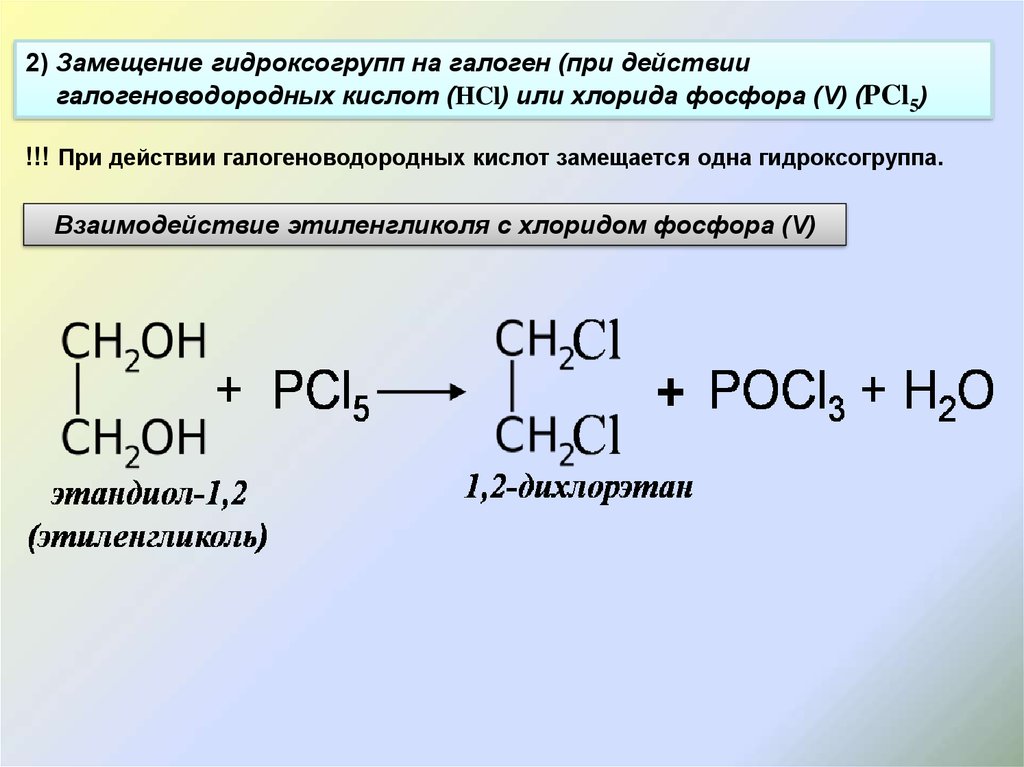 На первом шаге
кл + переносится на подложку; а во втором Cl — потерян. Изменение представляет собой восстановление на два электрона. Циклопентанол обеспечивает
эти два электрона и поэтому окисляются.
На первом шаге
кл + переносится на подложку; а во втором Cl — потерян. Изменение представляет собой восстановление на два электрона. Циклопентанол обеспечивает
эти два электрона и поэтому окисляются.
Окисление гипохлоритом дает явное преимущество перед другими окислителями реагенты, такие как реагенты Cr (VI), поскольку токсичность хрома реагенты создают трудности в обращении и утилизации отходов. Соль образующийся при окислении гипохлорита, можно смыть в раковину.
В этом эксперименте вы будете использовать NaOCl в смеси воды и уксусной кислоты.
окислить один из семи возможных спиртов в кетон. В связи с возможным
низкие температуры кипения некоторых кетоновых продуктов, мы никогда не сможем полностью
изолируйте свой кетоновый продукт. Вместо этого ваш продукт останется в растворе
дихлорметана (метиленхлорида), который можно вводить в
ГХ/МС для разделения
и идентификация отдельных соединений в вашем продукте.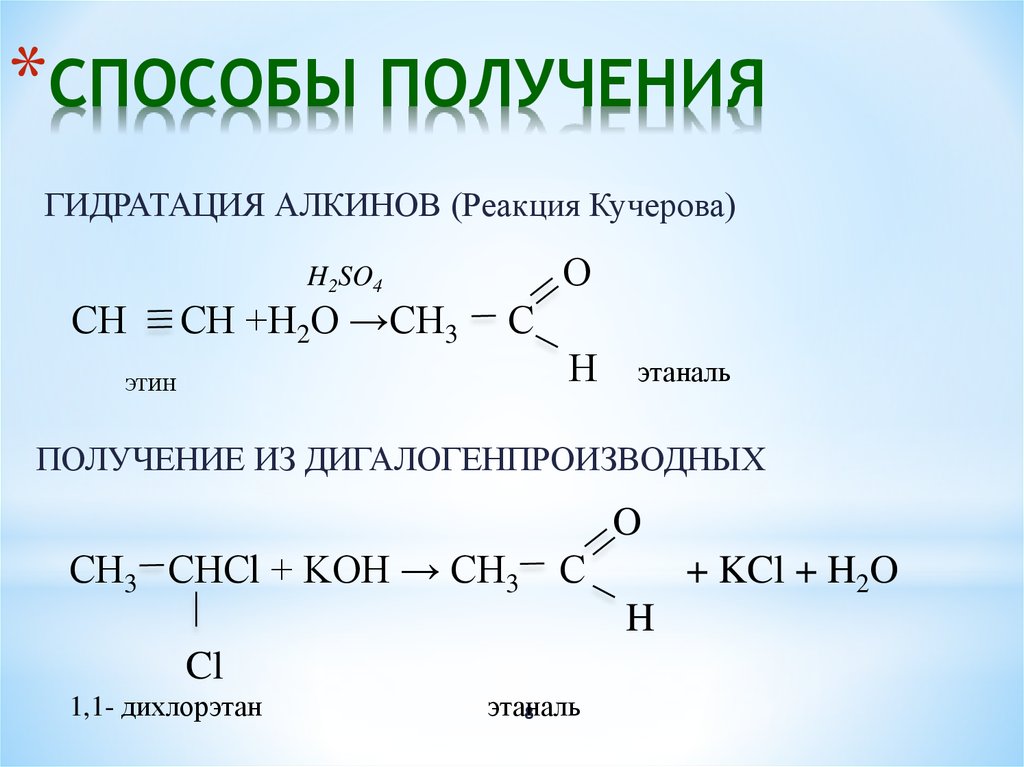 Поэтому,
ГХ/МС будет единственным инструментом, который позволит нам идентифицировать
соединения, присутствующие в вашей смеси продуктов. Идентификация вашего продукта
с помощью ГХ/МС должно позволить вам определить кетон, который вы создали. От
это, вы должны быть в состоянии определить, какой из следующих семи
спирты, которые вам дали в начале лаборатории.
Поэтому,
ГХ/МС будет единственным инструментом, который позволит нам идентифицировать
соединения, присутствующие в вашей смеси продуктов. Идентификация вашего продукта
с помощью ГХ/МС должно позволить вам определить кетон, который вы создали. От
это, вы должны быть в состоянии определить, какой из следующих семи
спирты, которые вам дали в начале лаборатории.
Стол 1: Список возможных спиртов | |
циклопентанол | 2-метилциклогексанол |
2,4-диметил-3-пентанол | 3-гексанол |
циклогексанол | 2-гептанол |
3,3-диметил-2-бутанол | |
Примечание по технике безопасности: Спирты, используемые в этом эксперименте, являются летучими, поэтому все работы следует выполнять в вытяжном шкафу. |
Экспериментальная работа
Отвесьте 1,5 грамма неизвестного спирта в колбу Эрленмейера на 125 мл.
Добавьте 1,0 мл ледяной уксусной кислоты и поместите колбу на мешалку.
Добавьте мешалку в колбу и осторожно перемешайте раствор. Вам необходимо точно отмерить количество реагентов? Почему или почему нет?
Добавить по каплям 20 мл водного раствора гипохлорита натрия в колбу в течение 10 минут, следя за поддержанием температуры раствора ниже 50 o C. Зачем нужно стараться поддерживать температуру ниже 50 o C?
После полного добавления водного гипохлорита натрия перемешайте смеси еще 20 минут. Примерно через 20 минут перемешивания, добавить 5 мл изопропанола и перемешать в течение 1-2 минут. Что делает изопропанол делать?
Перелейте смесь продуктов из колбы в делительную воронку на 125 мл.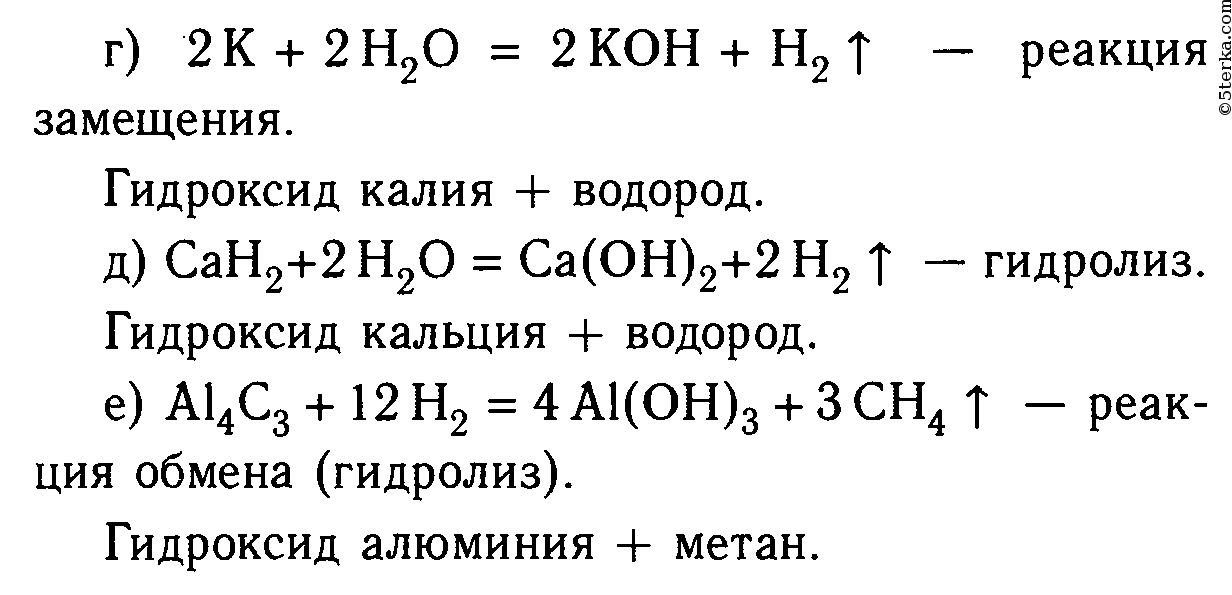 Добавьте 20-30 мл раствора NaCl. Часто встряхивайте и проветривайте! Почему
добавлен солевой раствор? Извлекайте органические продукты из водного слоя
добавлением примерно 10 мл дихлорметана. Встряхнуть и проветрить,
затем
удалить водный слой, который теперь должен быть свободен от каких-либо органических продуктов.
Органический слой промывают примерно 10 мл насыщенного
натрий
гидрокарбонатный раствор. Чаще проветривайте! Высушите органический слой фазой
бумаги и безводного сульфата магния и заполните промаркированный флакон для ГХ/МС.
с
высушенный органический слой.
Добавьте 20-30 мл раствора NaCl. Часто встряхивайте и проветривайте! Почему
добавлен солевой раствор? Извлекайте органические продукты из водного слоя
добавлением примерно 10 мл дихлорметана. Встряхнуть и проветрить,
затем
удалить водный слой, который теперь должен быть свободен от каких-либо органических продуктов.
Органический слой промывают примерно 10 мл насыщенного
натрий
гидрокарбонатный раствор. Чаще проветривайте! Высушите органический слой фазой
бумаги и безводного сульфата магния и заполните промаркированный флакон для ГХ/МС.
с
высушенный органический слой.
Проведите ГХ/МС этой смеси органических продуктов.
Проанализируйте ГХ/МС, чтобы определить образовавшийся кетон.
Удаление отходов и очистка
- Поместите все водные растворы и экстракты в бутыль для отходов гидрокарбоната натрия.

- Выбросьте все оставшиеся продукты в бутыль для горючих отходов.
- Промойте стеклянную посуду ацетоном и выбросьте ацетоновую промывку в бутыль для горючих отходов.
- Очистите стеклянную посуду горячей мыльной водой и верните ее в соответствующее место для хранения.
- Утилизируйте использованные пипетки Пастера в стеклянном контейнере для отходов .
Послелабораторные вопросы
(Пожалуйста, предоставьте ответы на эти вопросы по прибытии в СЛЕДУЮЩУЮ лабораторию.)
- С какой целью добавления изопропанола в вашу реакцию?
- Зачем ты добавил соли, прежде чем пытаться изолировать органический продукт от водного. решение?
- Использование массы
спектры, докажите, какой кетон был синтезирован в каждой реакции для каждого неизвестного спирта? Чтобы помочь обосновать свой ответ, пожалуйста, включите данные масс-спектра для каждого неизвестного и используйте структуры/фрагменты, чтобы аргументировать структуру каждого неизвестного кетона.


 ниже.
ниже.

Leave A Comment