2349432 HACH раствор нитрата серебра 1,88 н; 100 мл
Артикул: 2349432
Производитель: Hach
Наличие: Под заказ
Заказать Добавить в сравнение
Раствор является частью тест набора CD-51 (артикул 208601) для определения хлоридов в пробе воды методом капельного титрования (подсчет капель).
Маркированная бутылочка с дозатором.
Нитрат серебра, 1,88 н. 100 мл.
Титрант, нитрат серебра 0,0493 N (100 мл)
Артикул: 2349832
Индикаторный раствор фенолфталеина; 1 г/л, 15 мл
Артикул: 189736
Стандартный раствор, гидроксид натрия, 0,035 N, 100 мл
Артикул: 2349332
Описание Характеристики Рекомендуемые товары
Описание
Описание
Описание химической реакции: нитрат серебра используется в качестве титранта, а хромат калия — в качестве индикатора. Нитрат серебра сначала избирательно реагирует с хлоридом в образце, образуя нерастворимый белый хлорид серебра. После осаждения всего хлорида нитрат серебра вступает в реакцию с хроматом с образованием оранжевого или красно-коричневого осадка хромата серебра.
Нитрат серебра сначала избирательно реагирует с хлоридом в образце, образуя нерастворимый белый хлорид серебра. После осаждения всего хлорида нитрат серебра вступает в реакцию с хроматом с образованием оранжевого или красно-коричневого осадка хромата серебра.
Характеристики
Характеристики
| Область применения | Тест-наборы, Сточные воды, Питьевая вода |
| Тип | Жидкие реагенты |
| Индустрия | Еда и напитки, Муниципальная |
| Параметры | Хлорид |
| Метод измерений | капельное титрование |
| Объём | 100 мл |
Рекомендуемые товары
Рекомендуемые товары
Стандартный раствор серной кислоты, 0,100 N
Стандартный раствор серной кислоты, 0,100 N, бутылочка 1 л.
Артикул: 20253
Посмотреть товар Сравнить
CDTA титрант HexaVer, 0,02 Н, 1 л
Раствор для определения жесткости воды.
Артикул: 74053
Посмотреть товар Сравнить
Powder Pillows, реагент йодида калия для тест-наборов и лабораторных методов, 100 шт.
Powder Pillows, реагент йодида калия в герметичных упаковках для титрования. Используется совместно с тест-наборами и цифрофым титратором Hach.
Артикул: 107799
Посмотреть товар Сравнить
Индикаторный раствор фенолфталеина, 5 г/л, 1 л (APHA)
Индикатор pH для использования при титровании.
Артикул: 16253
Посмотреть товар Сравнить
Набор реагентов для цифрового титратора, хлорид, 10 — 10000 мг / л Cl
Для определения хлорида. В набор входит порошковый индикатор Chloride 2 и два картриджа для титрования (нитрат серебра).
Артикул: 2288000
Посмотреть товар Сравнить
Картридж для цифрового титратора, нитрат ртути, 0,2256 N, 1 шт.
Для определения хлорида титрованием, 10 — 160 мг/л Cl-.
Артикул: 1439301
Посмотреть товар Сравнить
Порошковый индикатор для определения жесткости ManVer 2, Powder Pillows, 100 шт.
Индикатор ManVer 2, Powder Pillows для определения общей жесткости титрованием, 100 шт.
Артикул: 85199
Посмотреть товар Сравнить
Порошковый индикатор, фенолфталеин, Powder Pillows, 100 шт.
Порошковый индикатор в герметичных упаковках для титрования кислотности, щелочности, углекислого газа и летучих кислот.
Артикул: 94299
Посмотреть товар Сравнить
Раствор гидроксида калия, 8 N., 100 мл
Для определения кальциевой жесткости, меди и общего азота по Кьельдалю (TKN).
Артикул: 28232H
Посмотреть товар Сравнить
Бромкрезоловый зеленый — индикатор метиловый красный, Powder Pillows, 100 шт.
Порошковый реагент Powder Pillows в герметичных упаковках для титрования (щелочность).
Артикул: 94399
Посмотреть товар Сравнить
Тест набор AL-TA на общую щелочность
Набор для определения общей щелочности методом капельного титрования: определение содержимого компонента происходит путем подсчета капель, добавляемого реагента до момента изменения окраски индикатора.
Артикул: 2314500
Посмотреть товар Сравнить
Картридж для цифрового титратора, гидроксид натрия, 3,636 N
Для определения углекислого газа методом цифрового титрования; 100 — 1000 мг/л CO2.
Артикул: 1438001
Посмотреть товар Сравнить
Порошковый индикатор для определения кальция CalVer 2, Powder Pillows, 100 шт.
Порошковый реагент в герметичных упаковках для определения кальция титрованием ЭДТА.
Артикул: 94799
Посмотреть товар Сравнить
Набор реагентов для цифрового титратора, диоксид углерода 10 — 1000 мг/л CO2
Для определения углекислого газа титрованием на цифровом титраторе. Метод Hach Lange 8205. Набора достаточно для проведения 40 -100 тестов.
Метод Hach Lange 8205. Набора достаточно для проведения 40 -100 тестов.
Артикул: 2272700
Посмотреть товар Сравнить
Порошковый реагент Powder Pillows аминосульфоновая кислота
Индивидуально запакованные пакетики (100 шт.) с реагентом для определения хлора, хрома и сульфитов.
Артикул: 105599
Посмотреть товар Сравнить
Порошковые реагенты Powder Pillows UniVer 3, жесткость
Артикул: 96299
Посмотреть товар Сравнить
Картридж для цифрового титратора, гидроксид натрия, 0,1600 N NaOH
Готовый к использованию раствор титранта для определения кислотности методом цифрового титрования 10 — 160 мг / л CaCO3.
Артикул: 1437701
Посмотреть товар Сравнить
Картридж для цифрового титратора, тиосульфат натрия (стабилизированный), 2,26 Н
Для определения гипохлорита (отбеливателя) титрованием на цифровом титраторе.
Артикул: 2686901
Посмотреть товар Сравнить
Набор реагентов (Высокий диапазон) для цифрового титратора, гипохлорит (отбеливатель)
Для определения гипохлорита (отбеливателя) титрованием на цифровом титраторе. Диапазон: 5 — 15% Cl2 (50 — 150 г / л Cl2). Состав стабилизированного тиосульфата натрия.
Артикул: 2687000
Посмотреть товар Сравнить
Стандартный раствор тиосульфата натрия
Титрант стабилизированный тиосульфат натрия для определения хлора йодометрическим титрованием.
Артикул: 2409232
Посмотреть товар Сравнить
Набор реагентов для определения жесткости в высоком диапазоне, 100 — 4000 мг/л CaCO3
Первое титрование дает результаты по кальциевой жесткости, а второе титрование дает общую жесткость. Разница между значениями — уровень жесткости магния. Все результаты по концентрации даны в мг/л CaCO3.
Артикул: 2448700
Посмотреть товар Сравнить
Картридж для цифрового титратора, серная кислота, 0,1600 Н
Готовый к использованию раствор титранта для определения щелочности.
Артикул: 1438801
Посмотреть товар Сравнить
Тест набор на общую жесткость воды, модель 5-B
Используется метод капельного титрования — простой и экономичный.
Артикул: 145300
Посмотреть товар Сравнить
Стандартный раствор серной кислоты, 0.500 н, 100 мл
Используется для определения щёлочности методом капельного титрования.
Артикул: 212132
Посмотреть товар Сравнить
Рекомендуемые товары
Порошковый реагент для определения кремния, Powder Pillows, 100 шт.
Порошковый реагент, Powder Pillows, в герметичных упаковках для определения содержания кремния (высокий диапазон), метод силикомолибдата.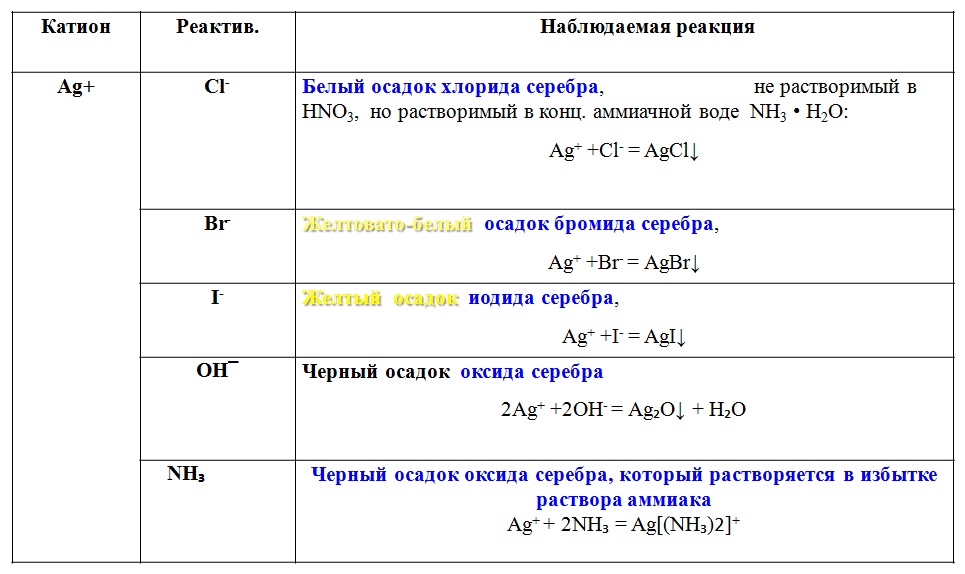
Артикул: 104299
Посмотреть товар Сравнить
Набор реагентов для цифрового титратора, диоксид углерода 10 — 1000 мг/л CO2
Для определения углекислого газа титрованием на цифровом титраторе. Метод Hach Lange 8205. Набора достаточно для проведения 40 -100 тестов.
Артикул: 2272700
Посмотреть товар Сравнить
Раствор Sulfite 3, 100 мл.
Для определения сульфита, метод капельного титрования, йодометрический, 0 — 200 мг/л SO3.
Артикул: 70532
Посмотреть товар Сравнить
Картридж для цифрового титратора, гидроксид натрия, 1,600 N
Готовый к использованию раствор титранта для кислотно-основного титрования (1-10 мэкв/л кислоты) и определения кислотности (100 — 4000 мг / л CaCO3).
Артикул: 1437901
Посмотреть товар Сравнить
Порошковый реагент Powder Pillows Sulfite 1
Реактив для определения общего хлора, перекиси водорода и сульфита.
Артикул: 220399
Посмотреть товар Сравнить
Набор реагентов для цифрового титратора, хлорид 10 — 8000 мг/л Cl
Титриметрическое определение хлоридов в сточной воде методом нитрата ртути (метод Hach 8206).
Артикул: 2272600
Посмотреть товар Сравнить
Стандартный раствор, гидроксид натрия, 0,035 N, 100 мл
Раствор для определения кислотности пробы воды.
Артикул: 2349332
Посмотреть товар Сравнить
Раствор гидроксида калия, 8 N., 100 мл
Для определения кальциевой жесткости, меди и общего азота по Кьельдалю (TKN).
Артикул: 28232H
Посмотреть товар Сравнить
Индикаторный раствор фенолфталеина, 5 г/л, 1 л (APHA)
Индикатор pH для использования при титровании.
Артикул: 16253
Посмотреть товар Сравнить
Обнаружение иона Cl-
Аналитическая группа иона: II
Уравнение реакции обнаружения:
Хлорид калия, нитрат серебра, хлорид серебра, нитрат калия
Тип аналитической реакции: групповая
Аналитический признак: белый творожистый осадок хлорида серебра, растворимый в 12 %-ном растворе карбоната аммония и в смеси (0,25 М гидроксида аммония + 0,01 М нитрата серебра + 0,25 М нитрата калия)
Условия проведения реакции: присутствие 2 М раствора азотной кислоты
Мешающие ионы: SCN-, Br-, I-, S2-
Предел обнаружения: 1,6 мкг
Действие растворов сильных и слабых кислот и оснований на продукты реакции обнаружения:
а) действие раствора HCl: —
б) действие раствора CН3COOH: —
в) действие раствора NaOH: —
г) действие раствора NH3:
Роль иона Cl- в жизни растений и человека
Хлор – один из
биогенных элементов, постоянный компонент
тканей растений и животных. С
пищей хлор поступает обычно в избытке
в виде хлорида натрия и хлорида калия.
Особенно богаты хлором хлеб, мясные и
молочные продукты. В организме животных
хлор – основное осмотически активное
вещество плазмы крови, лимфы, спинномозговой
жидкости и некоторых тканей. Играет
роль в водно-солевом обмене, способствуя
удержанию тканями воды. Регуляция
кислотно-щелочного равновесия в тканях
осуществляется наряду с другими
процессами путём изменения в распределении
хлора между кровью и другими тканями,
хлор участвует в энергетическом обмене
у растений, активируя как окислительное
фосфорилирование, так и фотофосфорилирование.
Хлор положительно влияет на поглощение
корнями кислорода. Хлор необходим для
образования кислорода в процессе
фотосинтеза изолированными хлоропластами.
В состав большинства питательных сред
для искусственного культивирования
растений хлор не входит. Возможно, для
развития растений достаточны весьма
малые концентрации хлора.
С
пищей хлор поступает обычно в избытке
в виде хлорида натрия и хлорида калия.
Особенно богаты хлором хлеб, мясные и
молочные продукты. В организме животных
хлор – основное осмотически активное
вещество плазмы крови, лимфы, спинномозговой
жидкости и некоторых тканей. Играет
роль в водно-солевом обмене, способствуя
удержанию тканями воды. Регуляция
кислотно-щелочного равновесия в тканях
осуществляется наряду с другими
процессами путём изменения в распределении
хлора между кровью и другими тканями,
хлор участвует в энергетическом обмене
у растений, активируя как окислительное
фосфорилирование, так и фотофосфорилирование.
Хлор положительно влияет на поглощение
корнями кислорода. Хлор необходим для
образования кислорода в процессе
фотосинтеза изолированными хлоропластами.
В состав большинства питательных сред
для искусственного культивирования
растений хлор не входит. Возможно, для
развития растений достаточны весьма
малые концентрации хлора.
Одной из важных
отраслей химической промышленности
является хлорная промышленность. Основные количества хлора перерабатываются
на месте его производства в хлорсодержащие
соединения. Хлор применяется также для
хлорирования некоторых руд с целью
извлечения титана, ниобия, циркония и
других.
Основные количества хлора перерабатываются
на месте его производства в хлорсодержащие
соединения. Хлор применяется также для
хлорирования некоторых руд с целью
извлечения титана, ниобия, циркония и
других.
Обнаружение иона co32-
Аналитическая группа иона: I
Уравнение реакции обнаружения:
Карбонат калия, соляная кислота, хлорид калия, углекислый газ, вода
Тип аналитической реакции: специфическая
Аналитический признак: выделение бесцветного газа со слегка кисловатым запахом и вкусом – CO2, вызывающего помутнение известковой воды:
Условия проведения реакции: —
Мешающие ионы: SO32-
Предел обнаружения: —
Действие растворов сильных и слабых кислот и оснований на продукты реакции обнаружения:
а) действие раствора HCl: —
б) действие раствора CН3COOH: —
в) действие раствора NaOH:
г) действие раствора NH3:
Роль иона co32- в жизни растений и человека
Карбонаты относятся
к труднорастворимым неорганическим
солям и в такой форме недоступны для
растения.
Карбонаты кальция,
магния, бария и др. применяют в строительном
деле, в химической промышленности,
оптике и др. В технике, промышленности
и быту широко применяется сода. Кислые
карбонаты выполняют важную физиологическую
роль, являясь буферными веществами,
регулирующими постоянство реакции
крови. Карбонаты
магния могут использоваться в пищевой
промышленности при приготовлении
шоколада и какао. Карбонаты
магния применяются как компоненты сыров
(сыры зрелые, сыры зрелые нарезанные и
тертые) и других продуктов питания.
Карбонат кальция,
состоящий преимущественно из раковин
морских животных и их обломков называется
ракушечником (ракушняком). Входящие в
состав карбоната кальция вещества
способны хотя и в малых количествах, но
растворяться в воде, а также медленно
разлагаться на углекислый газ и
соответствующие основания; первый
процесс – важнейший фактор образования
карстовых пещер, второй, происходящий
на больших глубинах под действием
глубинного тепла земли, даёт источник
газа для минеральных вод.
Вывод: определили качественный состав анализируемого раствора: K+, NH4+, Cl—, CO32-.
12
AgNO3 + NaCl = AgCl + NaNO3
При смешивании водного раствора AgNO 3 и водного раствора NaCl высока вероятность придание белого цвета осадок, если исходное серебро нитрат и исходный хлорид натрия концентрации значительно выше. Это означает, что AgNO 3 и NaCl являются реакцией осаждения. В этом уроке мы узнаем о различных аспектах этого реакция, такая как осаждение, и требуемые концентрации для осаждения.
AgNO
3(водн.) + NaCl (водн.) = AgCl (тв.) + NaNO 3(водн.) Растворы нитрата серебра и хлорида натрия представляют собой бесцветные растворы. Когда они реагируют друг с другом, выпадает белый осадок и
дают бесцветный раствор. Нитрат натрия представляет собой бесцветное водорастворимое соединение.
Наблюдения во время реакции
Когда вы медленно добавляете одно химическое вещество к другому химическому веществу по капле, в какой-то момент вы увидите белый осадок образуется в растворе. Если сразу добавить одно химическое вещество к другому, то осадок тоже сразу образуется. Но помните, что нужно быть осторожным с нитратом серебра и нитратом во время эксперимента, потому что это очень токсичное химическое вещество.
Концентрация, необходимая для образования осадка
При смешивании одинаковых объемов NaCl и AgNO 3 будет ли образовываться осадок? Оба раствора имеют концентрации 0,1 моль дм -3 .
Предположим, что при смешивании обоих растворов осадка нет, а затем рассчитаем концентрацию каждого соединения. Поскольку каждое соединение разбавлено в два раза, концентрация NaCl и AgNO3 уменьшается вдвое.
Тогда каждое соединение имеет концентрацию 0,05 моль дм -3 .
Затем мы можем применить выражение Ksp, чтобы проверить, будет ли выпадать осадок AgCl.
Начальная концентрация CL
— после смешивания = 0,05 моль дм -3Начальная концентрация AG
+ после смешивания = 0,05 моль DM -3Expray Exprodge для AGCL = AG
KSP. (водн.)
][Cl — (водн.) ][AG
+ (aq) ] [CL — (aq) ] = 0,05 моль DM -3 * 0,05 моль DM -3[AG
+ (ATQQ)[AG
+ (ATQQ)[AG
+ (AQQ)[AG
+ ][Cl — (aq) ] = 2.5 * 10 -3 mol 2 dm -6Ksp, AgCl = 1.7 * 10
-10 mol 2 dm -6 Поскольку расчетное значение выражения Ksp больше, чем значение Ksp AgCl. Следовательно, вы можете видеть, что AgCl
осаждается в растворе.
рН NaCl и AgNO
3 реакцияИ NaCl, и AgNO 3 являются нейтральными растворами. Продуктами реакции являются AgCl и NaNO 3 . AgCl выпадает в осадок и не вызывает реакции гидролиза. Кроме того, NaNO 3 является нейтральным соединением. Следовательно, итоговый раствор должен иметь значение pH, близкое к 7.
Вопросы студентов
Задайте свой вопрос и найдите ответ бесплатно.
Что касается нитрата серебра, какие другие неорганические соединения могут также давать белый осадок с нитратом натрия?
Нитрат свинца дает белый осадок с нитратом натрия, и соответствующая реакция приведена ниже.
Pb(NO 3 ) 2 + NaCl → PbCl 2 + NaNO 3
Что произойдет, если добавить вместо водного NaCl 49 водный раствор NaCl 90 к0 AgNO3?
В этом случае также дается осадок AgCl, потому что, когда твердый NaCl очень хорошо растворяется в воде и диссоциирует на Na + и Cl — ионов. Затем ион Cl — соединяется с ионами Ag + и дает белый осадок AgCl.
Затем ион Cl — соединяется с ионами Ag + и дает белый осадок AgCl.
Какого цвета осадок получается при реакции AgNO
3 и NaCl? Кроме того, будет ли выделяться газ в этой реакции?AgCl представляет собой белый осадок, во время реакции выделения газа не происходит.
Связанные руководства
FeCl 2 + реакция NaOHРеакция холодного и горячего NaOH + Cl 2 Растворимость гидроксидов металлов
Что происходит при добавлении раствора нитрата серебра к раствору хлорида натрия a Напишите уравнение…
Перейти к
- Упражнение
- Глава 1 Химические реакции и уравнения
- Глава 2 Кислоты, основания и соли
- Глава 3 Металлы и неметаллы
- Глава 4 Углерод и его соединения
- Глава 5 Периодическая классификация элементов
Главная > Лахмир Сингх Солюшнс Класс 10 Химия > Глава 1 — Глава 1 Химические реакции и уравнения > Упражнение > Вопрос 89
Вопрос 89 Упражнение
Что произойдет, если раствор нитрата серебра добавить к раствору хлорида натрия?
(а) Напишите уравнение протекающей реакции.
Ответ:
При добавлении раствора нитрата серебра к раствору хлорида натрия вместе с раствором нитрата натрия образуется белый осадок хлорида серебра.
(a) Agno 3 (aq) + NaCl (aq) → AGCL (S) + Nano 3 (AQ)
. **Объясните, почему пищевые продукты, содержащие жиры и масла (например, картофельные чипсы), упаковываются в азот.*…
**Что такое антиоксиданты? Почему их добавляют в продукты, содержащие жиры и масла?**
**Назовите важное применение реакций разложения.**
**Каково общее название химических веществ, которые добавляют в жиро- и маслосодержащие пищевые продукты для предотвращения…
** Какой тип химической реакции используется для извлечения металлов из их природных соединений, таких как оксид.

Leave A Comment