Исследование процесса конверсии сульфата натрия нитратом и нитритом кальция
Библиографическое описание:Рузиева, З. Т. Исследование процесса конверсии сульфата натрия нитратом и нитритом кальция / З. Т. Рузиева, У. Б. Сафаров, Ю. Х. Хидирова, Фарход Нормаматов. — Текст : непосредственный // Молодой ученый. — 2015. — № 9 (89). — С. 93-96. — URL: https://moluch.ru/archive/89/17922/ (дата обращения: 02.05.2023).
Исследована взаимосвязь основных технологических параметров, получены новые сведения по растворимости и характеру твёрдых фаз в двух четверных и тройных взаимных систем. Установлено оптимальные условия конверсии, фильтрация нитрит-нитрата кальция и натрия
В условиях мирового финансово-экономического кризиса очень своевременным оказалось издание книги Президента Республики Узбекистан Ислама Каримова “Мировой финансово — экономический кризис и меры по его преодолению в условиях Узбекистана”, где убедительно показаны принципиальные возможности нашей Республики по преодолению кризиса за счет широкого внедрения инновационных технологий и организации производства продукций, в том числе и минеральных удобрений из местных сырьевых материалов.
Одним из главных направлений экономического развития Узбекистана является освоение природных ресурсов, их комплексное использование и создание конкурентоспособных, импортозаменяющих продуктов на базе местных сырьевых ресурсов.
К таким важным химическим продуктам относятся нитриты, нитраты натрия и кальция, потребность в которых неуклонно растёт в связи с развитием отраслей народного хозяйства, потребляющих нитрит-нитратные соли натрия и кальция.
Основные потребители нитрит-нитратных солей натрия и кальция – станко-машиностроительная, металлургическая, бумажная, резиновая, текстильная, фармацевтическая, пищевая промышленность, строительная индустрия, медицина и сельское хозяйство.
Нитрит натрия можно получить по двум вариантам: взаимодействием сульфата натрия с нитритом кальция или нитрит-нитратом кальция, образующегося после абсорбции нитрозных газов известковым молоком.
Необходимо отметить, что для физико- химического обоснования и разработки технологии получения нитрит- нитратных солей натрия и кальция на основе нитрозных газов, известняка и сульфата натрия необходимо знание совместной растворимости нитратов, нитритов и сульфатов натрия и кальция в сложных водно- солевых системах. Изучение технологических параметров процесса получения предлагаемых нитрит — нитратных солей натрия и кальция необходимо для разработки технологии их производства.
Изучение технологических параметров процесса получения предлагаемых нитрит — нитратных солей натрия и кальция необходимо для разработки технологии их производства.
Равновесие фаз в системах Ca(NO2)2 — CaSO4 — H2O и NaNO2 — Na2SO4 — H2O при 250С устанавливалось при постоянном перемешивании и термостатировании соответственно через 1,5 и 1,0 суток. При количественном химическом анализе жидких и твердых фаз использовали общеизвестные методы аналитической химии [4]. Полученные данные использовали для определения составов твердых фаз по Шрейнемакерсу [2] и для построения изотермических диаграмм растворимости тройных систем нитрит кальция — сульфат кальция — вода и нитрит натрия — сульфат натрия — вода при 25 1 и 2).
1 и 2).
Диаграмма растворимости тройной системы нитрит натрия — сульфат натрия-вода при 250С характеризуется наличием двух ветвей кристаллизации твердых фаз — нитрита натрия и десятиводного кристаллогидрата сульфата натрия (рис. 1). Ветвь кристаллизации нитрата натрия значительно больше, чем десятиводного сульфата натрия. Полученные данные показывают, что в изученной системе не происходит образования ни твердых растворов, ни новых химических соединении на основе исходных компонентов. Особенность изотермы растворимости в том, что сульфат натрия оказывает высаливающие действие на нитрит натрия. Поэтому растворимость последнего в присутствии сульфата натрия понижается до эвтонической точки системы.
Рис. 1. Диаграмма растворимости системы нитрит натрия — сульфат натрия — вода при 250С
Как следует из рис. 1, первоначальная растворимость нитрита натрия в воде при 250С равна 46,7 %, а в присутствии 30,14–30,17 % сульфата натрия этот показатель составляет лишь 2,96–3,01 %.
Сульфат натрия в присутствии нитрита натрия при 25
Рис. 2. Диаграмма растворимости системы нитрит кальция — сульфат кальция — вода при 250С
На изотермической диаграмме растворимости тройной системы нитрит кальция — сульфат кальция — вода установлено наличие двух ветвей, отвечающих кристаллизации Ca(NO2)2∙4H2O и CaSO4∙2H
Таблица 1
Данные по растворимости в системе NaNO2—Na2SO4—H2O при 250С
|
№ |
Состав жидкой фазы, % |
Состав влажного “остатка”, % |
Твердая фаза |
||||
|
Са(NO2)2 |
Na2SO4 |
H2O |
Са(NO2)2 |
Na2SO4 |
H2O |
||
|
1 |
46,70 |
|
53,30 |
96,3 |
— |
3,7 |
NaNO2 |
|
2 |
42,84 |
1,99 |
55,17 |
91,42 |
0,61 |
7,97 |
“ ” “ “ |
|
3 |
25,44 |
11,59 |
62,97 |
85,11 |
2,01 |
12,88 |
“ ” “ “ |
|
4 |
9,24 |
22,70 |
68,06 |
80,85 |
4,59 |
14,56 |
“ ” “ “ |
|
5 |
2,96 |
30,17 |
66,87 |
17,1 |
34,5 |
48,40 |
“ ” “ “ |
|
6 |
3,01 |
30,17 |
66,85 |
4,05 |
40,13 |
55,82 |
NaNO2 +Na2SO4·10H2O |
|
7 |
2,75 |
28,45 |
68,80 |
0,81 |
39,2 |
59,99 |
Na2SO4·10H2O |
Благодаря хорошей растворимости в данной системе, нитрит кальция оказывает высаливающее действие на сульфат кальция, в результате чего растворимость последнего по сравнению с его первоначальной растворимостью в воде понижается до эвтонической точки системы с 0,21 до 0,017 %.
Опыт проводился на лабораторной установке, состоящей из стеклянного реактора, снабжённого лопастной мешалкой, помещённого в термостат, скорость вращения электродвигателя регулировали реостатным устройством и измеряли тахометром ТМ-ЗМ, c использованием датчика Д-1 мм. Температуру водяного термостата, нагревающего реактор, поддерживали с помощью контактного термометра ТК — 300 и электронного реле РТ — 230 Гц
Методика эксперимента заключалась в следующем: расчётное количество Са(NO3)2 или Са(NO2)2 загружалось в реактор. Туда же добавляли Na2SO4 и приготовленный раствор нитрата или нитрита натрия, а затем дистиллированную воду.
После чего реактор помещали в термостат с заданной температурой и пульпу перемешивали в течение 2 часов.
Фильтрация пульпы проводилась на фильтровальной воронке, помещённой в колбу Бюнзена, которая присоединялась к вакуум-фильтру [4].
Эксперименты по получению нитрита и нитрата натрия проводили при температурах 25, 30, и 400С и концентрации оборотного раствора нитрита и нитрата натрия 25,0; 40,0; 50,0 %.
Полученные данные показывают, что с уменьшением концентрации оборотных растворов нитрата и нитрита натрия и с увеличением соотношения твёрдой и жидкой фаз с 1:2,5 до 1:3,5 скорость фильтрации пульпы с осадками гипса возрастает.
При концентрации оборотного растворов NaNO3 40 и 50 % и соотношении Т:Ж=1:2,5 скорость фильтрации пульпы с осадками гипса составляет 1003,5 и 820,1 кг/м2. час. При соотношении Т:Ж=1:3,5; 1:5 и концентрации оборотных растворов NaNO3 40 и 50 % скорость фильтрации колеблется соответственно в пределах 5006,4 ¸ 3520,2 и 9086,3 7451,6 кг/м2.час.
При соотношении Т:Ж=1:2,5; 1:3; 1:5 и концентрации оборотного раствора нитрита натрия 40,0 % скорость фильтрации составляет соответственно 1010,41; 5091,56; 91273,51 кг/м2.час. т. е. привело к увеличению скорости фильтрации на 44,6 %.
Уменьшение скорости фильтрации с увеличением концентрации объясняется увеличением вязкости раствора, что ухудшает ее фильтруемость.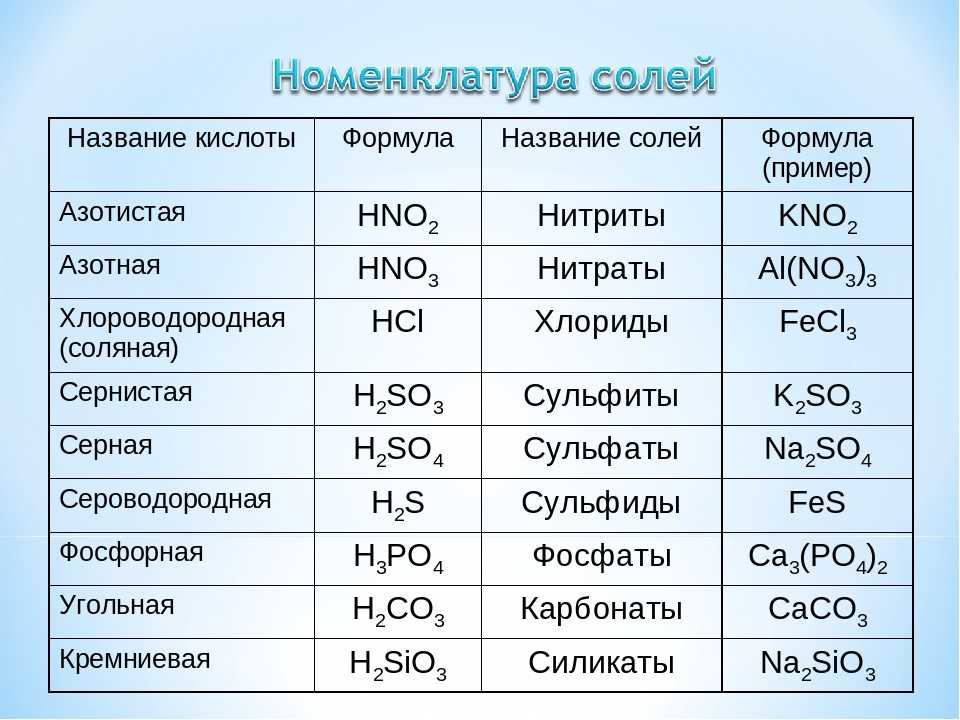
При соотношении Т:Ж=1:3,5 и 1:5 уменьшение скорости фильтрации с увеличением концентрации жидкой фазы происходит не так резко как при соотношении Т:Ж=1:2,5, что также объясняется ухудшением фильтруемости при повышении количества твёрдой фазы.
Таким образом, в результате вышеприведенных исследований, выявлены следующие оптимальные технологические параметры процесса конверсии нитрита кальция сульфатом натрия: температура — 25–300С, концентрация оборотного раствора нитрита и нитрата натрия 40–50,0 %. Также усановлено, что конверсионные пульпы обладают достаточно хорошей фильтруемостью.
Литература:
1. Каримов И. А. «Мировой финансово- экономический кризис, пути и меры по его преодолению в условиях Узбекистана» Т., Узбекистан, 2009 г.
2. Справочник по растворимости. В 3-х. т. / Коган В. Б., Огородников С. К., Кафаров В. В., под ред. В. В. Кафарова Т. 3. Кн. 1.- Л.: Наука. — 1969. — с 944.
3. Шварценбах Г. , Флашка Г. Комплексонометрическое титрование. — М.: Химия. — 1970. –360 с.
, Флашка Г. Комплексонометрическое титрование. — М.: Химия. — 1970. –360 с.
4. Атрошенко В. И. и др.Технология связанного азота. Киев. «Выш.школа».-1985.-327с.
Основные термины (генерируются автоматически): сульфат натрия, нитрит натрия, нитрит кальция, сульфат кальция, нитрат натрия, ветвь кристаллизации, вод, жидкая фаза, система, твердая фаза.
Натрия сульфат природный. «ХИМПЭК» — Крупный поставщик химического сырья и реагентов для всех отраслей промышленности и агропромышленного комплекса
Натрия сульфат природный получают из природного галургического сырья озера Кучук и используется в различных отраслях промышленности: химической, целлюлозно-бумажной, стекольной, строительной, нефтедобывающей, нефтеперерабатывающей, для производства синтетических моющих средств, а также в качестве кормовой добавки для животных. Цена: уточняйте у менеджера Узнать цену |
Физико-химические показатели
Общее описание
Внешний вид
Условия транспортировки и хранения
Области применения
| Наименование показателя | Норма по ТУ |
| Внешний вид | Сыпучий порошок белого цвета |
| Массовая доля сульфата натрия, (Na2SO4 ), %, не менее | 99,5 |
| Массовая доля нерастворимого в воде остатка, %, не более | 0,2 |
| Массовая доля хлоридов в пересчете на хлористый натрий (NaCl), %, не более | 0,2 |
| Массовая доля железа (в виде Fe), ppm, не более | 20 |
| Массовая доля воды, %, не более | 0,1 |
| Показатель активности водородных ионов водного 1%-ного раствора сульфата натрия, в пределах | 6,5 — 9,0 |
| Белизна (по Хантеру), не менее | 90 |
| Класс опасности по степени воздействия на организм человека | 4 |
| Виды опасности | |
| Взрыво- и пожароопасность | Не горюч, пожаро- и взрывобезопасен, не образует токсичных соединений в воздушной среде. |
| Опасность для человека | Малоопасное вещество, обладает раздражающим действием на кожные покровы и слизистые оболочки. |
| Средства индивидуальной защиты | Спецодежда. Противопыльные респираторы типа ШБ-1 «Лепесток-5». |
Гарантийный срок хранения продукта — 6 месяцев с даты изготовления.
Природный сульфат натрия (сернокислый натрий) имеет химическую формулу Na2SO4. В присутствии воды при температуре ниже 32 оС образует кристаллогидрат. В природе вещество встречается в виде тенардита и мирабилита. Значительное его количество содержится в донных отложениях хлоридно-сульфатных соленых озер, а также в рапе. Соединение характеризуется хорошей растворимостью в воде, не подвержено слеживанию. Может использоваться без дополнительной обработки.
Природный сульфат натрия является пожаро- и взрывобезопасным. Он относится к малоопасным веществам по степени воздействия на организм. Ему присвоена низшая токсичность по токсикологическому стандарту NFPA 704.
Ему присвоена низшая токсичность по токсикологическому стандарту NFPA 704.
Природный сульфат натрия — белый сыпучий порошок, состоящий из мелких кристаллов.
Сернокислый натрий упаковывается в полипропиленовые мягкие контейнеры или мешки. Вещество в таре может перевозиться в крытом и открытом транспорте, в том числе в морских контейнерах. Хранить его необходимо в заводской упаковке на закрытых складах с твердым покрытием. Мягкие контейнеры можно размещать на открытых площадках.
Природный сернокислый натрий наибольшее распространение получил в следующих отраслях:
- производство синтетических моющих средств, в том числе стиральных порошков и мыла;
- стекольное производство;
- химические исследования. Вещество применяется в качестве обезвоживающего средства. Его способность к обезвоживанию органических растворителей несколько ниже, чем у сульфата магния, но зато оно дешевле и легче поддается фильтрации;
- животноводство.
 Природный сульфат натрия является эффективной добавкой в комбикорма для птиц и крупного рогатого скота. Он обеспечивает коррекцию кислотно-щелочного баланса и представляет собой ценный источник бесхлорного натрия и серы;
Природный сульфат натрия является эффективной добавкой в комбикорма для птиц и крупного рогатого скота. Он обеспечивает коррекцию кислотно-щелочного баланса и представляет собой ценный источник бесхлорного натрия и серы; - пищевая промышленность. Вещество зарегистрировано как пищевая добавка Е514, которая предназначена для регулирования кислотности пищевых продуктов;
- легкая промышленность. Соединение применяется для обработки кожевенной продукции и окрашивания хлопчатобумажного текстиля.
Склад
В Московской области
Адрес: Истринский район, сельское поселение Ивановское, поселок станция Манихино, 50 км
Посмотреть на карте
Скачать схему проезда
Здесь возможно:
оплатить наличными;
купить от 1 мешка (канистры/мкр/куба/барабана) продукции.
С этим продуктом часто покупают:
| Продукция | Синонимы | CAS № | ГОСТ | Марка/сорт | Упаковка/вес |
| Калий азотнокислый удобрение | селитра калиевая, нитрат калия | 7757-79-1 | 2180-037-00203795-2009 | Мешок 25 кг | |
| Кальция формиат технический | муравьинокислый кальций, кальциевая соль муравьиной кислоты | 544-17-2 | импорт | Мешок 25 кг | |
| Натрия гидрокарбонат E500 (ii) | бикарбонат натрия, натрий двууглекислый, сода пищевая, питьевая сода, гидрокарбонат натрия | 144-55-8 | 32802-2014, импорт | первый, второй | Мешок 25 кг, 50 кг, пачки 500 г |
| Натрия нитрит технический | натрий азотистокислый технический | 7632-00-0 | 19906-74, импорт | высший, первый, второй | Мешок 25 кг, 50 кг |
| Натрия триполифосфат технический | натрия триполифосфат | 7758-29-4 | 13493-86 | технический | Мешок 45 кг |
| Натрия формиат технический | натрий муравьинокислый, натриевая соль муравьиной кислоты | 141-53-7 | 2432-011-00203803-98, импорт | Мешок 25 кг, 40 кг | |
| Свинцовый сурик | ортоплюмбат свинца, монооксид свинца, окись свинца | 1314-41-6 | импорт | Мешок 25 кг | |
| Калий углекислый технический (Поташ) | поташ, карбонат калия, калиевая соль угольной кислоты | 584-08-7 | 10690-73 | кальцинированный/первый, второй, третий полутораводный/первый, второй, третий | Мешок 25 кг, 38-42 кг |
| Барий углекислый технический (карбонат бария) | карбонат бария | 513-77-9 | 2149-75, импорт | А / гранулированный, Б сорт1/ порошкообразный | Мешок 25 кг |
| Бензойная кислота | кислота бензойная, бензолкарбоновая кислота | 65-85-0 | импорт | Мешок 25 кг | |
| Борная кислота | ортоборная кислота, кислота борная | 10043-35-3 | 18704-78, импорт | гранулированная NS, порошкообразная, малосульфатная LS | МКР 1000 кг, Мешок 25 кг |
| Глинозем | оксид алюминия | 1344-28-1 | 30558-98 | неметаллургический, металлургический | МКР/разновес (800-1000 кг) |
| Калий азотнокислый технический | селитра калиевая, нитрат калия, калиевая соль азотной кислоты | 7757-79-1 | P 53949-2010 | Б | Мешок 50 кг |
| Калия гидроокись (реактив) | гидроокись калия, калия гидрат окиси, гидрат окиси калия, едкий калий, гидроксид калия, кали едкое, калиевая щелочь, едкое кали твердое чешуированное | 1310-58-3 | 2132-025-52257004-2015, импорт | Ч | Мешок 25 кг |
| Кальций хлористый 2-водный (E509) | хлорид кальция | 10043-52-4 | 9199-087-00206457-2010 | Мешок 30 кг | |
| Магнезит | порошок магнезитовый каустический, магнезит каустический | 1309-48-4 | 1216 — 87, импорт | ПМК-87, ПМК-83, ПМК-75 | Мешок разновес, МКР разновес |
| Медный купорос | сульфат меди, меди (II) сульфат 5-ти водный, медь сульфат пентагидрат | 7758-99-8 | 19347-99 | Мешок 25 кг | |
| Натр едкий технический гранулированный | сода каустическая, натрия гидрат окиси технический, гидрат окиси натрия, едкий натр, гидроокись натрия, гидроксид натрия, натриевая щелочь | 1310-73-2 | 00203275-206-2007, импорт | ГР / высший, первый | Мешок 25 кг |
| Натр едкий технический чешуированный | сода каустическая, натрия гидрат окиси технический, гидрат окиси натрия, едкий натр, гидроокись натрия, гидроксид натрия, натриевая щелочь | 1310-73-2 | 00203312-017-2011,
изм. №1, №1, импорт | Мешок 25 кг, 50 кг | |
| Натрий азотнокислый технический | селитра натриевая, нитрат натрия, чилийская селитра, натриевая соль азотной кислоты | 7631-99-4 | 828-77 | Б | Мешок 50 кг |
| Сода кальцинированная техническая | натрий углекислый, карбонат натрия, динатрий карбонат | 497-19-8 | 5100-85 | А, Б | Мешок 25 кг, 50 кг, МКР 600 кг, 800 кг, 1250 кг |
| Соль таблетированная | соль таблетированная для водоподготовки | 7647-14-5 | Р 51574-2000, РБ 400087365.003-2002 | экстра, высший | Мешок 25 кг |
| Суперпластификатор С-3 | пластификатор С-3, «Полипласт СП-1» | 9084-06-4 | 5745-001-97474489-2007, 5870-002-58042865-2003 | Мешок 25 кг | |
| Трикальцийфосфат кормовой | ортофосфат кальция, кальциевая соль ортофосфорной кислоты, кальций фосфорнокислый, трехзамещенный фосфат кальция | 7758-87-4 | 390838120142-05-2010 | первый | Мешок 50 кг |
| Шпат плавиковый | концентрат плавиковошпатовый сварочный и кислотный керамический, флюорит, флюоритовый концентрат | 7789-75-5 | 29219-91, 4421-73 | ФФ-95А, ФФС-95 | МКР 1000 кг |
Острая и хроническая токсичность нитрата натрия и сульфата натрия для некоторых пресноводных организмов при контакте только с водой
. 2020 Май; 39 (5): 1071-1085.
2020 Май; 39 (5): 1071-1085.
дои: 10.1002/и т.д.4701. Epub 2020 9 апр.
Нин Ван 1 , Ребекка Дорман 1 , Кристофер Д. Айви 1 , Дэвид Дж. Соучек 2 , Эми Дикинсон 2 , Бетани К. Кунц 2 , Джеффри А. Стивенс 2 , Эдвард Дж. Хаммер 3 , Кэндис Р Бауэр 3
Принадлежности
- 1 Колумбийский центр экологических исследований, Геологическая служба США, Колумбия, штат Миссури, США.

- 2 Исследование естественной истории штата Иллинойс, Иллинойский университет, Урбана-Шампейн, Иллинойс, США.
- 3 Отдел качества воды, Агентство по охране окружающей среды США, Чикаго, Иллинойс, США.
- PMID: 32113188
- DOI: 10.1002/и др.4701
Нин Ван и др. Environ Toxicol Chem. 2020 Май.
. 2020 Май; 39 (5): 1071-1085.
дои: 10.1002/и т.д.4701.
Epub 2020 9 апр.
Авторы
Нин Ван 1 , Ребекка Дорман 1 , Кристофер Д. Айви 1 , Дэвид Дж. Соучек 2 , Эми Дикинсон 2 , Бетани К. Кунц 2 , Джеффри А. Стивенс 2 , Эдвард Дж. Хаммер 3 , Кэндис Р Бауэр 3
Принадлежности
- 1 Колумбийский центр экологических исследований, Геологическая служба США, Колумбия, Миссури, США.
- 2 Исследование естественной истории штата Иллинойс, Иллинойский университет, Урбана-Шампейн, Иллинойс, США.

- 3 Отдел качества воды, Агентство по охране окружающей среды США, Чикаго, Иллинойс, США.
- PMID: 32113188
- DOI: 10.1002/и др.4701
Абстрактный
Повышенное содержание нитратов (NO 3 ) и сульфатов (SO 4 ) в поверхностных водах вызывает глобальную озабоченность, и необходимы исследования для получения данных о токсичности для разработки экологических нормативных значений для NO 9.0107 3 и SO 4 . Настоящее исследование было разработано для заполнения существующих пробелов в базах данных о токсичности путем определения острой и/или хронической токсичности NO 3 (испытано как NaNO 3 ) по отношению к мидиям-юнионидам (Lampsilis siliquoidea), мошкам (Chironomus dilutus), рыба (радужная форель, Oncorhynchus mykiss) и 2 амфибии (Hyla versicolor и Lithobates sylvaticus), а также для определения острой и/или хронической токсичности SO 4 (испытано как Na 2 SO 4 ) до 2 мидий-юнионид (L. siliquoidea и Villosa iris), амфипод (Hyalella azteca) и 2 видов рыб (толстоголовый гольян, Pimephales promelas и O. mykiss). Среди различных испытуемых видов средние концентрации NO 3 при остром воздействии (EC50) колебались от 189 до >883 мг NO 3 -N/L, а концентрации NO 3 при хроническом воздействии 20% (EC20) основаны на наиболее чувствительная конечная точка варьировалась от 9,6 до 47 мг NO 3 -N/L. Мошка была наиболее чувствительным видом, а форель — наименее чувствительным видом как к острой, так и к хронической NO 9.0107 3 экспозиции. Острые значения EC50 SO 4 для 2 видов мидий (2071 и 2064 мг SO 4 /л) были аналогичны значениям EC50 для амфипод (2689 мг SO 4 /л), тогда как значения EC20 для хронических мидий ( 438 и 384 мг SO 4 /л) были более чем в 2 раза ниже, чем EC20 амфипод (1111 мг SO 4 /л), что указывает на высокую чувствительность мидий к хроническим воздействиям SO 4 .
siliquoidea и Villosa iris), амфипод (Hyalella azteca) и 2 видов рыб (толстоголовый гольян, Pimephales promelas и O. mykiss). Среди различных испытуемых видов средние концентрации NO 3 при остром воздействии (EC50) колебались от 189 до >883 мг NO 3 -N/L, а концентрации NO 3 при хроническом воздействии 20% (EC20) основаны на наиболее чувствительная конечная точка варьировалась от 9,6 до 47 мг NO 3 -N/L. Мошка была наиболее чувствительным видом, а форель — наименее чувствительным видом как к острой, так и к хронической NO 9.0107 3 экспозиции. Острые значения EC50 SO 4 для 2 видов мидий (2071 и 2064 мг SO 4 /л) были аналогичны значениям EC50 для амфипод (2689 мг SO 4 /л), тогда как значения EC20 для хронических мидий ( 438 и 384 мг SO 4 /л) были более чем в 2 раза ниже, чем EC20 амфипод (1111 мг SO 4 /л), что указывает на высокую чувствительность мидий к хроническим воздействиям SO 4 . Однако толстоголовый гольян с EC20 374 мг SO 4 /л, был наиболее чувствительным видом при хроническом воздействии SO 4 , тогда как радужная форель была наименее чувствительным видом (EC20 > 3240 мг SO 4 /л). Высокая чувствительность толстоголового гольяна согласовывалась с результатами предыдущего исследования хронического Na 2 SO 4 . Однако значения EC20 из настоящего исследования, проведенного в тестовой воде с более высокой концентрацией калия (3 мг K/л), были более чем в 2 раза выше, чем в предыдущем исследовании с более низкой концентрацией калия (1 мг K/л). что подтвердило влияние калия на хронический Na 2 SO 4 токсичность для гольяна. Environ Toxicol Chem 2020;39:1071-1085. © 2020 СЕТАК.
Однако толстоголовый гольян с EC20 374 мг SO 4 /л, был наиболее чувствительным видом при хроническом воздействии SO 4 , тогда как радужная форель была наименее чувствительным видом (EC20 > 3240 мг SO 4 /л). Высокая чувствительность толстоголового гольяна согласовывалась с результатами предыдущего исследования хронического Na 2 SO 4 . Однако значения EC20 из настоящего исследования, проведенного в тестовой воде с более высокой концентрацией калия (3 мг K/л), были более чем в 2 раза выше, чем в предыдущем исследовании с более низкой концентрацией калия (1 мг K/л). что подтвердило влияние калия на хронический Na 2 SO 4 токсичность для гольяна. Environ Toxicol Chem 2020;39:1071-1085. © 2020 СЕТАК.
Ключевые слова: Токсичность основных ионов; Видовая чувствительность; критерии качества воды; Рекомендации по качеству воды.
© 2020 СЕТАК.
Похожие статьи
Острая и хроническая токсичность алюминия для мидий-юнионид (Lampsilis siliquoidea) и амфипод (Hyalella azteca) при контакте только с водой.
Ван Н., Айви К.Д., Брансон Э.Л., Кливленд Д., Ингерсолл К.Г., Стаблфилд В.А., Кардуэлл А.С. Ван Н и др. Environ Toxicol Chem. 2018 Январь; 37(1):61-69. дои: 10.1002/и др.3850. Environ Toxicol Chem. 2018. PMID: 28475262
Острая и хроническая токсичность сульфата натрия для четырех пресноводных организмов при контакте только с водой.
Ван Н., Дорман Р.А., Ингерсолл К.Г., Хардести Д.К., Брамбо В.Г., Хаммер Э.Дж., Бауэр К.Р., Маунт Д.Р. Ван Н и др. Environ Toxicol Chem. 2016 янв; 35(1):115-27. дои: 10.
 1002/и др.3148. Epub 2015 15 декабря.
Environ Toxicol Chem. 2016.
PMID: 26139383
1002/и др.3148. Epub 2015 15 декабря.
Environ Toxicol Chem. 2016.
PMID: 26139383Хроническая токсичность азоксистробина для пресноводных амфипод, мошек, кладоцер и мидий при контакте только с водой.
Кунц Дж.Л., Ингерсолл К.Г., Смоллинг К.Л., Эльскус А.А., Куйвила К.М. Кунц Дж.Л. и соавт. Environ Toxicol Chem. 2017 сен; 36 (9): 2308-2315. doi: 10.1002/etc.3764. Epub 2017 15 марта. Environ Toxicol Chem. 2017. PMID: 28181697
Токсичность нитратов для водных животных: обзор с новыми данными по пресноводным беспозвоночным.
Камарго Х.А., Алонсо А., Саламанка А. Камарго Дж.А. и соавт. Хемосфера. 2005 март; 58(9):1255-67. doi: 10.1016/j.chemosphere.2004.10.
 044.
Хемосфера. 2005.
PMID: 15667845
Обзор.
044.
Хемосфера. 2005.
PMID: 15667845
Обзор.Обзор факторов качества воды, влияющих на биодоступность никеля для водных организмов: уточнение модели биотического лиганда для никеля при остром и хроническом воздействии.
Сантор Р.С., Крото К., Райан А.С., Шлекат С., Миддлтон Э., Гарман Э., Хоанг Т. Санторе Р.С. и др. Environ Toxicol Chem. 2021 авг;40(8):2121-2134. дои: 10.1002/и др.5109. Epub 2021 13 июля. Environ Toxicol Chem. 2021. PMID: 33945644 Обзор.
Посмотреть все похожие статьи
Цитируется
Определение острой и хронической токсичности сульфата в процессе автотрофной денитрификации серы для молоди рыбок данио ( Данио рерио ).

Цао Г., Чжао Дж., Чжао Г., Ван Д., У З., Ли Р., Хе Ц. Цао Г и др. АСУ Омега. 2022 12 декабря; 7(50):47165-47173. doi: 10.1021/acsomega.2c06320. Электронная коллекция 2022 20 декабря. АСУ Омега. 2022. PMID: 36570241 Бесплатная статья ЧВК.
Рекомендации
ССЫЛКИ
- АСТМ Интернэшнл. 2019а. Международное стандартное руководство ASTM по проведению испытаний на острую токсичность с участием рыб, макробеспозвоночных и амфибий. Е 729-96 2014. В Ежегоднике международных стандартов ASTM, Том 11.06. Филадельфия, Пенсильвания, США.
- АСТМ Интернэшнл. 2019б. Стандартное руководство по проведению лабораторных испытаний на токсичность пресноводных мидий. E 2455-06 2013. В Ежегодном сборнике стандартов ASTM, том 11.
 06. Филадельфия, Пенсильвания, США.
06. Филадельфия, Пенсильвания, США.
- АСТМ Интернэшнл. 2019б. Стандартное руководство по проведению лабораторных испытаний на токсичность пресноводных мидий. E 2455-06 2013. В Ежегодном сборнике стандартов ASTM, том 11.
- АСТМ Интернэшнл. 2019в. Стандартный метод испытаний для измерения токсичности загрязняющих веществ, связанных с отложениями, для пресноводных беспозвоночных. E 1706-05 2010. В Ежегодном сборнике стандартов ASTM, том 11.06. Филадельфия, Пенсильвания, США.
- АСТМ Интернэшнл. 2019г. Стандартное руководство по проведению тестов на токсичность на ранних стадиях жизни рыб. Е 1241-05. В Ежегодном сборнике стандартов ASTM, том 11.06. Филадельфия, Пенсильвания, США.
- Бейкер Дж. А., Гилрон Г., Чалмерс Б. А., Элфик Дж. Р. 2017. Оценка влияния типа воды на токсичность нитратов для гидробионтов. Хемосфера 168:435-440.

- Бейкер Дж. А., Гилрон Г., Чалмерс Б. А., Элфик Дж. Р. 2017. Оценка влияния типа воды на токсичность нитратов для гидробионтов. Хемосфера 168:435-440.


 Природный сульфат натрия является эффективной добавкой в комбикорма для птиц и крупного рогатого скота. Он обеспечивает коррекцию кислотно-щелочного баланса и представляет собой ценный источник бесхлорного натрия и серы;
Природный сульфат натрия является эффективной добавкой в комбикорма для птиц и крупного рогатого скота. Он обеспечивает коррекцию кислотно-щелочного баланса и представляет собой ценный источник бесхлорного натрия и серы;

 1002/и др.3148. Epub 2015 15 декабря.
Environ Toxicol Chem. 2016.
PMID: 26139383
1002/и др.3148. Epub 2015 15 декабря.
Environ Toxicol Chem. 2016.
PMID: 26139383 044.
Хемосфера. 2005.
PMID: 15667845
Обзор.
044.
Хемосфера. 2005.
PMID: 15667845
Обзор.
 06. Филадельфия, Пенсильвания, США.
06. Филадельфия, Пенсильвания, США.
Leave A Comment