Свойства хлорида серы (SO2Cl2) (25 полных фактов) —
By Сонали Джам
Сульфурилхлорид — сильная кислота с формулой SO2Cl2. Рассмотрим подробно сульфурилхлорид.
Хлористый сульфурил получают реакцией диоксида серы с хлором в присутствии активированного угля. катализатор. Сульфурилхлорид смешивается с бензолом, толуолом, хлороформом, CCl.4, ледяная уксусная кислота.
Давайте обсудим вязкость, молярную массу, степени окисления, молярную плотность и т. д. сульфурилхлорида в этой статье.
Сульфурилхлорид название IUPACНазвание IUPAC Sulfuryl Chloride — Sulfuryl Chloride.
Химическая формула сульфурилхлоридаХимическая формула сульфурилхлорида – SO.2Cl2.
Сульфурилхлорид номер CASКомпания CAS номер of Sсульфурилхлорид 7791-25-5.
Сульфурилхлорид ChemSpider IDSO2Cl2 имеет Идентификатор ChemSpider как 23050.
Химическая классификация SO2Cl2 составляет-
- SO2Cl2 является галогенангидридом.
- SO2Cl2 является неорганическим соединением.
- SO2Cl2 существует в жидком состоянии при комнатной температуре.
- Центральный атом S принадлежит к группе 16.
Молярная масса SO2Cl2 составляет 136.96 г/моль. молярная масса атома S составляет 32.065 г/моль, атома Cl составляет 35.5 г/моль и атома O составляет 16.00 г/моль.
Сульфурилхлоридный цветSO2Cl2 бесцветный. Становится желтым при стоянии при воздействии света или воздуха.
Становится желтым при стоянии при воздействии света или воздуха.
Компания вязкость of SO2Cl2 составляет 0.596 сП при 20 οC.
Молярная плотность хлорида сульфурилаМолярная плотность SO2Cl2 1.67 г / см3 в 20 οC.
Температура плавления хлористого сульфурилаТемпература плавления SO2Cl2 составляет -54.1 οС или 219.1 К.
Температура кипения хлористого сульфурилаТочка кипения SO2Cl2 является 69.4 οС или 342.5 К.
Сульфурилхлоридное состояние при комнатной температуреSO2Cl2 существует в виде бесцветной жидкости при комнатной температуре.
SO2Cl2 содержит 6 ковалентных связей. Каждый атом кислорода образует двойные связи с серой, а каждый атом Cl образует одинарную связь.
Ковалентный радиус хлорида серыСера имеет больший ковалентный радиус 105 пм. Ковалентный радиус Cl составляет 102 пм, а ковалентный радиус кислорода составляет 53 пм.
Электронные конфигурации сульфурилхлоридаЭлектронная конфигурация — это размещение электронов на атомных или молекулярных орбиталях. Выясним электронную конфигурацию атомов SO2Cl2 внизу.
Электронная конфигурация серы: [Ne] 3s.2 3p4, хлор [Ne] 3s2 3p5 а у кислорода [He] 2s2 2p4.
Степень окисления сульфурилхлоридаСтепень окисления серы в SO2Cl2 составляет +6. Степень окисления хлора -1, а степень окисления кислорода -2.
Степень окисления хлора -1, а степень окисления кислорода -2.
SO2Cl2 является сильной кислотой. Это летучий кислота.
Хлористый сульфурил без запаха?SO2Cl2 имеет резкий запах.
Парамагнитен ли хлористый сульфурил?Парамагнетик слабо притягивается магнитным полем, а диамагнетик отталкивается магнитным полем. Давайте обсудим это.
SO2Cl2 имеет диамагнитную природу, поскольку не содержит неспаренных электронов и отталкивается магнитным полем.
Гидраты хлорида серыSO2Cl2 образует гидраты с ледяной водой, SO2Cl2.15H2O. Этот гидрат SO2Cl2 по внешнему виду напоминает камфору.
SO2Cl2 + 15H2О -> ТАК2Cl2. 15H2O
15H2O
SO2Cl2 кристаллическая структура тетраэдрическая.
Полярность и проводимость сульфурилхлорида- SO2Cl2 является полярным соединением из-за неравномерного распределения заряда на центральном атоме серы.
- SO2Cl2 показывает ионную проводимость.
SO2Cl2 сама по себе является кислотой, поэтому она не будет реагировать с кислотой той же силы.
Реакция сульфурилхлорида с основаниемSO2Cl2 реагирует с NaOH с образованием Na2SO4, NaCl и H2O.
SO2Cl2 + 4NaOH –> Na2SO4 + 2NaCl + 2Н2O
Реакция хлорида серы с оксидомSO2Cl2 реагирует с оксидом кальция с образованием сульфата кальция и хлорида кальция.
SO2Cl2 + 2СаО —>Случай4 + CaCl2
Реакция хлорида сульфурилата с металломSO2Cl2 реагирует с Pt и превращает Pt в хлориды. В некоторых случаях образование хлорида зависит от температуры реакции.
SO2Cl2 + Pt –> PtCl2 + ТАК2
ЗаключениеДелаем вывод, что ТАК2Cl2 представляет собой неорганическое соединение диамагнитной природы, сильную кислоту с резким запахом, разъедающую металл.
степень окисления SO2Cl2 — Знания.site
Последние вопросы
Литература
5 минут назад
Якою є проблематика твору та про що твір «Тартюф» примушує замислитися…(Письмово 5-6 речень)Українська мова
5 минут назад
Написати портретний нарис у публіцистичному стилі про Сергія Жадана по плану: Перше враження. Портрет героя. Що я про нього дізналася. Що він розповів про себе. Як такі люди змінюють наше життя.
Портрет героя. Що я про нього дізналася. Що він розповів про себе. Як такі люди змінюють наше життя.Литература
10 минут назад
Скину фотку сейчасБиология
10 минут назад
Чем отличаются питекантропы от австралопитеков? И кто возник раньше?Алгебра
11 минут назад
Допожіть будь ласка, потрібно вирішити а, b, cИстория
15 минут назад
Дз по историиМатематика
20 минут назад
математика помогитеееееееИстория
25 минут назад
Назвать отличительные особенности развития древнерусской культуры после распада единого государства.
Русский язык
31 минут назад
Жабабот с жабами и лягушкамиГеография
31 минут назад
Помогите пожалуйста, дам 20 баллов! Не тот ответ — жалоба.Английский язык
31 минут назад
составить 10 предложений на английском со словами «Шоколад,какос,кофе,лемон,арбуз,мята,клубника,ваниль», даю 50 балов Другие предметы
35 минут назад
ПОЖАЛУЙСТА ПОМОГИТЕ МНЕКонтрольна робота №5 з теми «Поетичне бачення світу».

География
46 минут назад
2. Побудуй порiвняльну діаграму довжини найбільших річок Євразії в масштабі «в 1 см — 500 км. Янцзи Хуанхе Лена Об Дунайдопоможіть будь ласкадаю 100 балів Русский язык
50 минут назад
Помогите пожалуйста с сочинением!!!! Как вы понимаете смысл фразы из текста:« в жизни всегда есть место подвигам».
Физика
50 минут назад
На якій відстані одна від одної будуть взаємодіяти із силою 160 мН дві металеві кульки, якщо заряди кульок 10 нКл і 4 нКл.
Все предметы
Выберите язык и регион
English
United States
Polski
Polska
Português
Brasil
English
India
Türkçe
Türkiye
English
Philippines
Español
España
Indonesia
Русский
Россия
How much to ban the user?
1 hour 1 day 100 years
Свойства хлорида серы (SO2Cl2) (25 полных фактов) —
Автор: Sonali Jham
Хлорид сульфурила — сильная кислота с формулой SO 2 Cl 2 . Рассмотрим подробно сульфурилхлорид.
Рассмотрим подробно сульфурилхлорид.
Сульфурилхлорид может быть получен реакцией диоксида серы с хлором в присутствии активированного угля в качестве катализатора. Сульфурилхлорид смешивается с бензолом, толуолом, хлороформом, CCl 4, ледяной уксусной кислотой.
Давайте обсудим вязкость, молярную массу, степени окисления, молярную плотность и т. д. сульфурилхлорида в этой статье.
Сульфурилхлорид название IUPACНазвание IUPAC Sulfuryl Chloride — Sulfuryl Chloride.
Химическая формула хлорида серыХимическая формула хлорида серы: SO 2 Cl 2 .
Сульфурилхлорид Номер CASНомер CAS S сульфурилхлорид — 7791-25-5.
Sulfuryl chloride ChemSpider ID SO 2 Cl 2 has the ChemSpider ID as 23050.
The chemical classification of SO 2 Cl 2 выглядит следующим образом:
- SO 2 Cl 2 представляет собой галогенангидрид кислоты.
- SO 2 Cl 2 представляет собой неорганическое соединение.
- SO 2 Cl 2 существует в жидком состоянии при комнатной температуре.
- . Центральный атом S принадлежит группе 16.
SO 2 Cl 2 бесцветный. Становится желтым при стоянии при воздействии света или воздуха.
Становится желтым при стоянии при воздействии света или воздуха.
The viscosity of SO 2 Cl 2 is 0.596 cP at 20 ο C.
Sulfuryl chloride molar densityThe molar density of SO 2 CL 2 IS 1,67 г/см 3 на 20 гла C.
Sulfuryl Chloride Point. IS -54.1 ο C или 219,1 К.
СУЛЬНАЯ ХОЛИЧЕСКАЯ ПУНКА В точке кипения SO 2 Cl 2 IS 69,4 6 2 Cl 2 IS 69,4 65 2 CL 2 IS 69,4 65 2 . Состояние хлорида серы при комнатной температуре SO 2 Cl 2 существует в виде бесцветной жидкости при комнатной температуре. SO 2 Cl 2 содержит 6 ковалентных связей. Каждый атом кислорода образует двойные связи с серой, а каждый атом Cl образует одинарную связь. Сера имеет больший ковалентный радиус 105 пм. Ковалентный радиус Cl составляет 102 пм, а ковалентный радиус кислорода составляет 53 пм. Электронная конфигурация представляет собой размещение электронов на атомных или молекулярных орбиталях. Ниже выясним электронную конфигурацию атомов SO 2 Cl 2 . Электронная конфигурация серы [Ne] 3s 2 3p 4 , хлор [Ne] 3s 2 3p 5 и кислород [He] 2s 2 2p 4 . Степень окисления серы в SO 2 Cl 2 +6. SO 2 Cl 2 — сильная кислота. Это летучая кислота. SO 2 Cl 2 имеет резкий запах. Парамагнитное вещество, слабо притягивающееся магнитным полем, в то время как диамагнитное вещество отталкивается магнитным полем. Давайте обсудим это. SO 2 Cl 2 диамагнитен по своей природе, поскольку не содержит неспаренных электронов и отталкивается магнитным полем. SO 2 CL 2 Образуются гидраты с ледяной водой, поэтому 2 Cl 2 . SO 2 CL 2 + 15H 2 O -> SO 2 CL 2 .15H 2 O SO 2 Cl 2 Кристаллическая структура тетраэдрическая. SO 2 Cl 2 сам по себе является кислотой, поэтому он не будет реагировать с кислотой той же силы. Таким образом, 2 CL 2 реагирует с NAOH для формирования NA 2 SO 4, NACL и H 2 O . SO 2 Cl 2 + 4NaOH –> Na 2 SO 4 + 2NaCl + 2H 2 O SO 2 Cl 2 реагирует с оксидом кальция с образованием сульфата кальция и хлорида кальция. SO 2 Cl 2 + 2CaO –> CaSO 4 + CaCl 2 SO 2 Cl 2 реагирует с Pt и превращает Pt в хлориды. В некоторых случаях образование хлорида зависит от температуры реакции. SO 2 Cl 2 + Pt –> PtCl 2 + SO 2 We conclude that SO 2 Cl 2 is an неорганическое соединение диамагнитной природы, сильная кислота с резким запахом, разъедающая металл. Вопрос Вопрос Элементы Pradeep-P-Block-Every короткий ответ Реклама AB Padhai Karo Bina Ads KE Khareedo DN Pro и Dekho Sari Video Bina Kisi Ad Ki Rukatat Dn Pro Pro и Dekho Sari Videos Bina Kisi Ad Ki Rukatat! Обновлен: 27 июня 2022 г. ii) Na+.-O-S↑S∣∣O-O-Na+ Ответить Пошаговое решение, разработанное экспертами, чтобы помочь вам в решении вопросов и получении отличных оценок на экзаменах. Видео по теме Степень окисления серы в Na2S2O3 равна 30684298 Заполните следующее: 30712862 Уравнение вес. Na_(2)S_(2)O_(3) в качестве восстановителя в реакции, Na_(2)S_(2)O_(3)+H_(2)O+Cl_(2)rarrNa_(2)SO_(4) +2HCl+S IS: 41524568 Текстовое решение निम्नलिखित में S ऑक ऑक Вивра संख्या ज्ञात करो। — 
 Степень окисления хлора -1, а степень окисления кислорода -2.
Степень окисления хлора -1, а степень окисления кислорода -2.  Cl 2 внешне напоминает камфору.
Cl 2 внешне напоминает камфору.
Реакция хлорида серы с кислотой 

Определите степень окисления S в (i) SO(2)Cl(2) и (ii) Na(2)S(2)O(3)
Поскольку между двумя атомами S существует координационная связь, следовательно, акцепторный атом S имеет О.Н. из -2. О.Н. другого атома S можно рассчитать следующим образом:
2×(+1)(для Na+)+3×(-2)(для атомов O)+x+1×(-2)(для координаты S)или+2-6+x-2=0orx=+ 6
Таким образом, два атома S в Na2S2O3 имеют степени окисления -2 и +6.
(i) NaCl+h3SO4(конц. )→
)→
(ii) Na2SO3+HCl→
(iii) Cl2+h3O→
(iv) Cl2+NaOH(конц.)→
(v) Na2S2O3+h3O+Cl2→
(ii) H3S2O8
(iii) Na2S2O3
94847294
ऑक्सीकरण संख्या से क्या अभिपшить है? इसकी गणना करने के लिए प्रयुक्त नियमो का उल्लेख ख ख Na2S, Na2SO3, Na2SO4, Na2S2O3 तथा Na2S4O6 में S की ऑक्सीकरण संख्या की गान। की गान।
110395836
S की Na2S2O3 में
121204300
Найти степени окисления (i) атомов S в Na_(2)S_(2)O_(3) и атомов CI в хлорной извести CaOCI_(2)
90901471190 из числа окисления (i) атомов S в Na_(2)S_(2)O_(3) и атомов CI в хлорной извести CaOCI_(2)
148973553
Эквивалентная мас. Na_(2)S_(2)O_(3) в реакции, Na_(2)S_(2)O_(3) + H_(2)O + Cl_(2) в Na_(2)SO_(4) + 2HCl + S, равно
328698559
Расположите следующие соединения в порядке возрастания степени окисления S.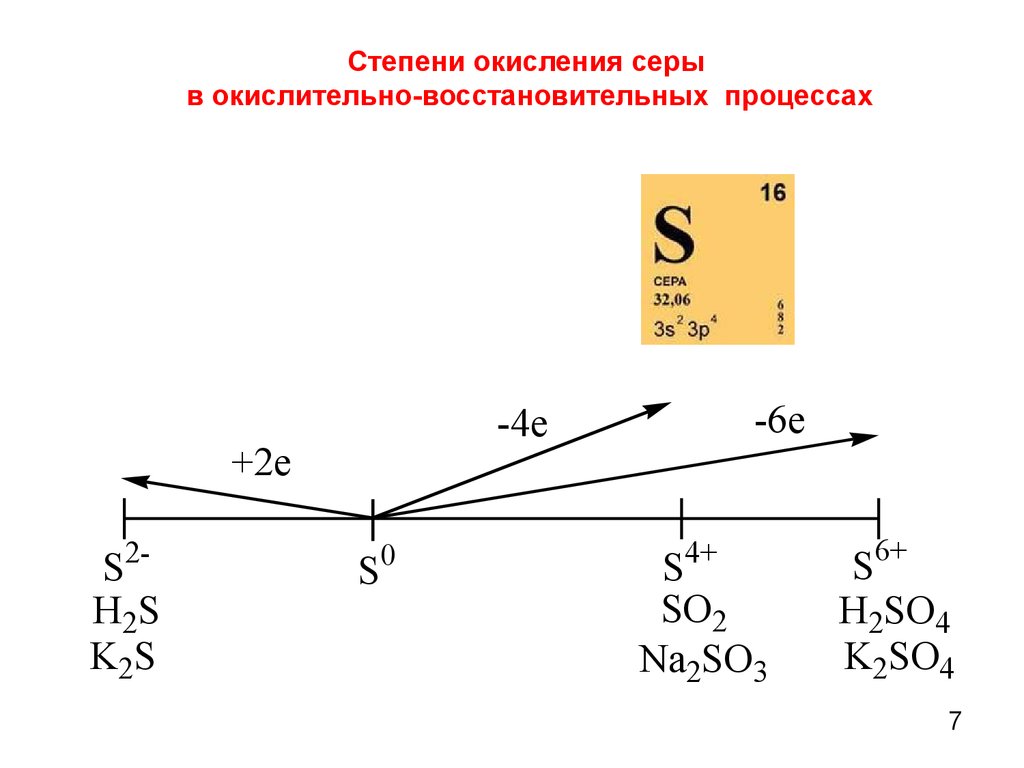

 Портрет героя. Що я про нього дізналася. Що він розповів про себе. Як такі люди змінюють наше життя.
Портрет героя. Що я про нього дізналася. Що він розповів про себе. Як такі люди змінюють наше життя.



Leave A Comment