Барьерные функции | это… Что такое Барьерные функции?
физиологические механизмы (барьеры), обеспечивающие защиту организма и отдельных его частей от изменений окружающей среды и сохранение необходимого для их нормальной жизнедеятельности постоянства состава, физико-химических и биологических свойств внутренней среды (крови, лимфы, тканевой жидкости).
Условно различают внешние и внутренние барьеры. К внешним барьерам относят кожу, органы дыхания, пищеварения, почки, а также слизистые оболочки рта, носа, глаз, половых органов. Кожа предохраняет организм от механических, радиационных и химических воздействий, препятствует проникновению в него микроорганизмов, ядовитых веществ, способствует выведению некоторых продуктов метаболизма. В органах дыхания, помимо обмена газов, происходит очистка вдыхаемого воздуха от пыли и мелкодисперсных вредных веществ. На протяжении пищеварительного тракта осуществляются специфическая обработка попадающих в него пищевых веществ, удаление не использованных организмом продуктов, а также газов, образующихся в кишечнике при брожении.
Внутренние барьеры регулируют поступление из крови в органы и ткани необходимых для их деятельности веществ и своевременное выведение конечных продуктов клеточного метаболизма, обеспечивают постоянство оптимального состава тканевой (внеклеточной) жидкости. Одновременно они препятствуют поступлению из крови в органы и ткани чужеродных и ядовитых веществ.
Внутренние барьеры получили различные названия: тканевых, гематопаренхиматозных, сосудисто-тканевых и т.д. Наибольшее распространение получил термин «гистогематический барьер». Особенностью гистогематического барьера является его избирательная (селективная) проницаемость, т.е. способность пропускать одни вещества и задерживать другие. Особо важное значение для жизнедеятельности организма имеют специализированные барьеры.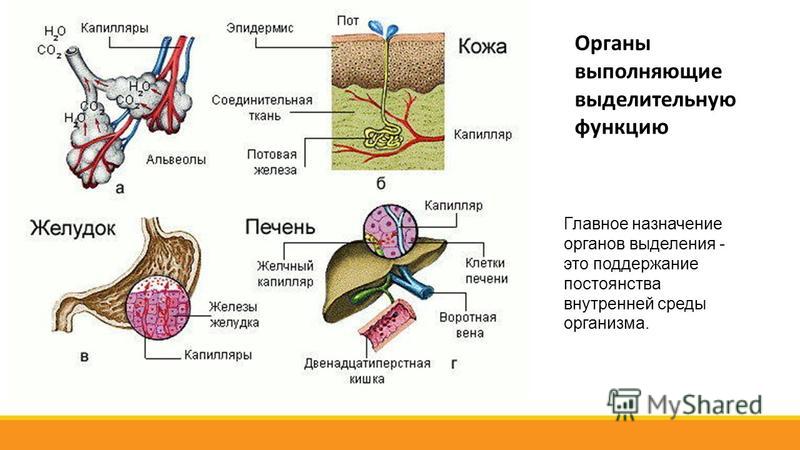
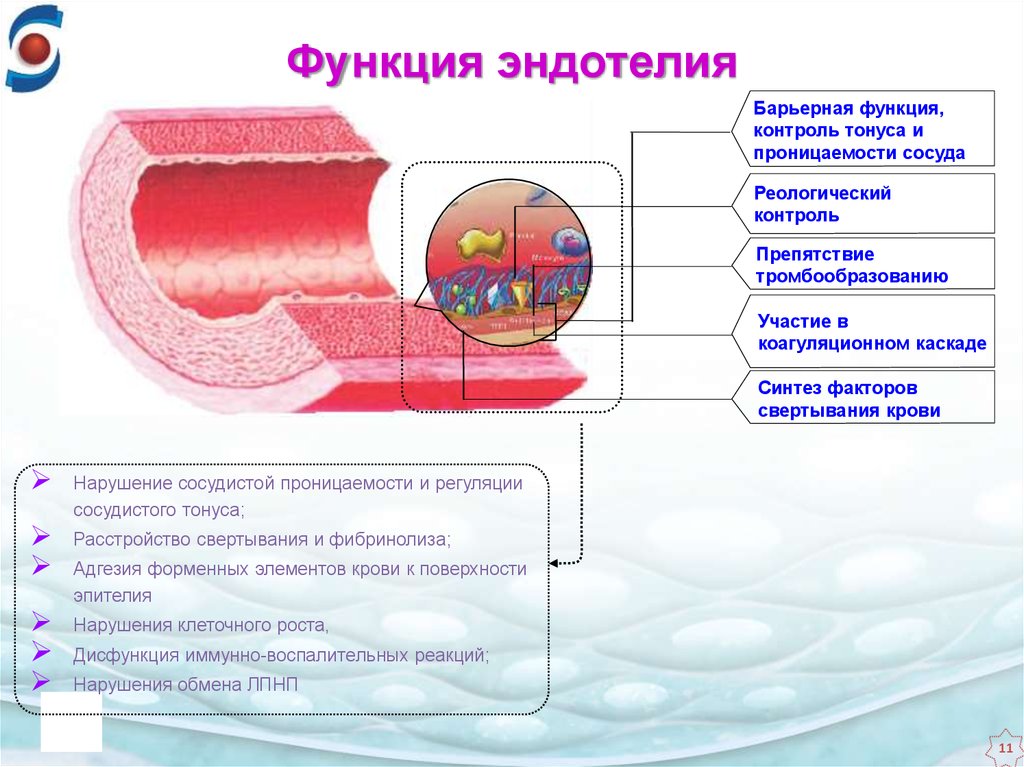
Основными структурными элементами гистогематических барьеров являются эндотелий кровеносных сосудов, базальная мембрана, в состав которой входит большое количество нейтральных мукополисахаридов, основное аморфное вещество, волокна и т.д. Структура гистогематических барьеров определяется в значительной степени особенностями строения органа и варьирует в зависимости от морфологических и физиологических особенностей органа и ткани.
В основе Б. ф. лежат процессы диализа, ультрафильтрации, осмоса, а также изменение электрических свойств, растворимости в липидах, тканевого сродства или метаболической активности клеточных элементов. Важное значение в функции некоторых гистогематических барьеров придается ферментному барьеру, например, в стенках микрососудов мозга и окружающей их соединительнотканной стромы (гематоэнцефалический барьер) — обнаружена высокая активность ферментов — холинэстеразы, карбоангидразы, ДОФА-декарбоксилазы и др. Эти ферменты, расщепляя некоторые биологически активные вещества, препятствуют их проникновению в мозг.
Функциональное состояние гистогематического барьера определяется соотношением концентраций того или иного вещества в органе и омывающей его крови. Эта величина получила название коэффициента проницаемости, или коэффициента распределения.
Б. ф. меняются в зависимости от возраста, пола, нервных, гуморальных и гормональных взаимоотношений в организме, тонуса вегетативной нервной системы, многочисленных внешних и внутренних воздействий.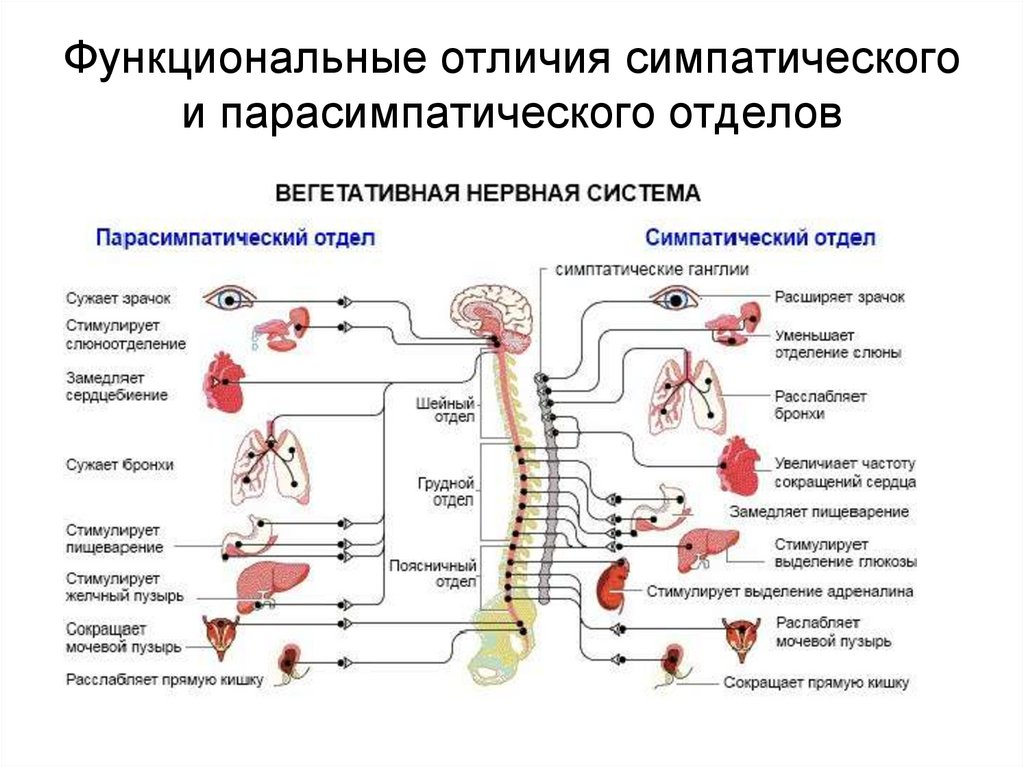 В частности, воздействие на организм ионизирующего излучения вызывает снижение защитной функции гистогематических барьеров, причем степень снижения и обратимость функциональных изменений зависят от величины поглощенной дозы. На проницаемость гистогематических барьеров влияют также механические и термические воздействия. Отмечено избирательное изменение проницаемости клеточных мембран гистогематических барьеров при введении в организм психотропных препаратов, этанола.
В частности, воздействие на организм ионизирующего излучения вызывает снижение защитной функции гистогематических барьеров, причем степень снижения и обратимость функциональных изменений зависят от величины поглощенной дозы. На проницаемость гистогематических барьеров влияют также механические и термические воздействия. Отмечено избирательное изменение проницаемости клеточных мембран гистогематических барьеров при введении в организм психотропных препаратов, этанола.
Различные патологические состояния могут нарушать проницаемость гистогематических барьеров. например, при менингоэнцефалите резко повышается проницаемость гематоэнцефалического барьера, что вызывает различного рода нарушения целостности окружающих тканей. Проницаемость гистогематических барьеров можно изменять направленно, что находит применение в клинике (например, для повышения эффективности химиотерапевтических препаратов).
Библиогр.: Бредбери М. Концепция гематоэнцефалического барьера, пер. с англ. , М., 1983; Физиология и патология гистогематических барьеров, под ред. Л.С. Штерн, М., 1968; Физиология человека, под ред. Р. Шмидта и Г. Тевса. пер. с англ., т. 2, М., 1985.
, М., 1983; Физиология и патология гистогематических барьеров, под ред. Л.С. Штерн, М., 1968; Физиология человека, под ред. Р. Шмидта и Г. Тевса. пер. с англ., т. 2, М., 1985.
1. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг.
Предотвратить «удар по печени» | газета «Копейский рабочий»
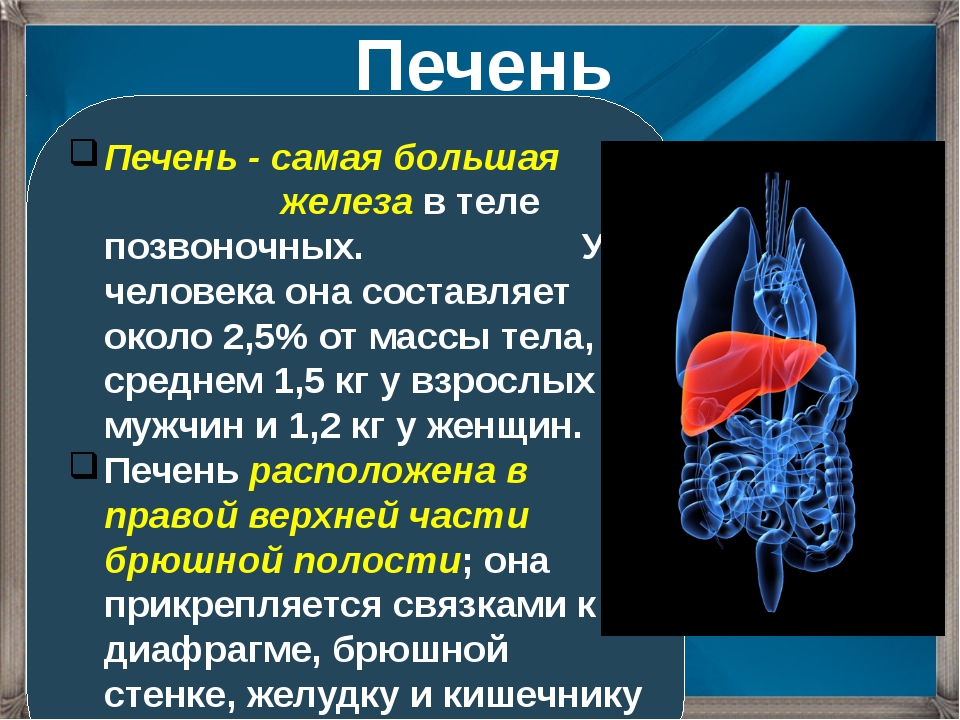
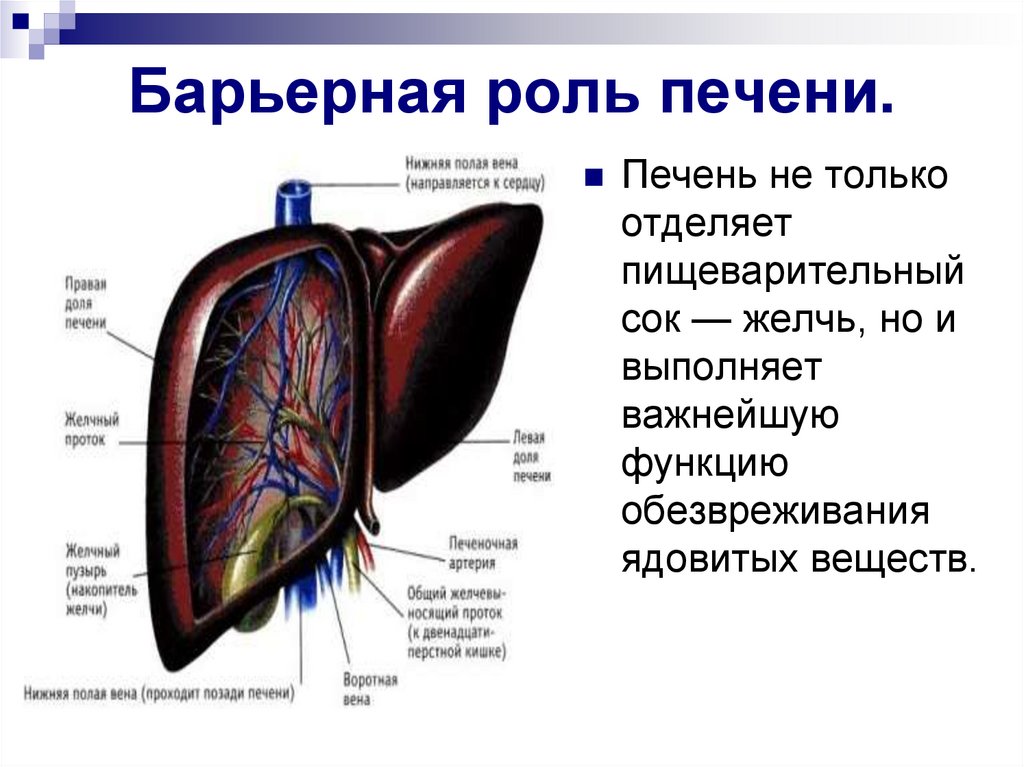
Печень — жизненно важный орган, участвующий в пищеварении, обмене веществ, гемодинамике, выполняющий защитную (барьерную) роль. Больная печень означает значительное снижение качества жизни, а в особо тяжелых случаях может привести к весьма печальным последствиям
Автор: Людмила Гейман Фото: из открытых интернет-источников
Печень — жизненно важный орган, участвующий в пищеварении, обмене веществ, гемодинамике, выполняющий защитную (барьерную) роль.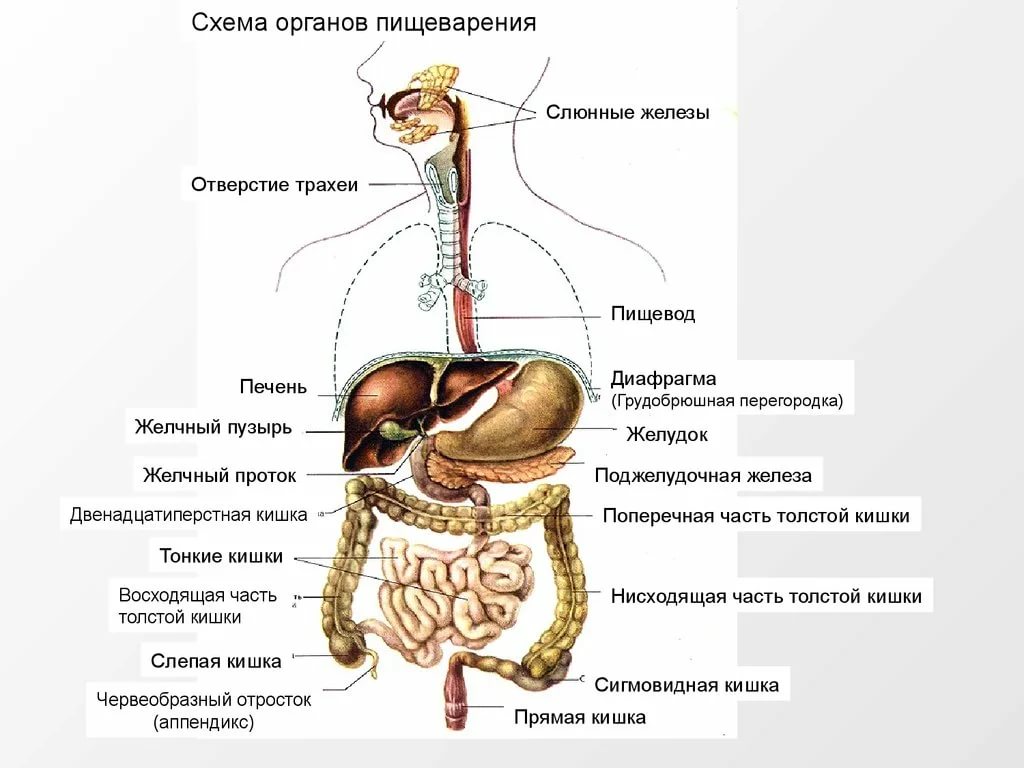
— Что такое цирроз печени? От чего он возникает? Действительно ли этот диагноз является для человека приговором? — эти вопросы мы задали врачу-эксперту высшей категории бюро №18 государственного бюро медико-социальной экспертизы по Челябинской области Ольге Крюковской.
— Цирроз — это конечная стадия многих заболеваний печени, он характеризуется прогрессирующим разрушением структуры органа, и при этом нарушаются его синтетическая и обезвреживающая функции. Более половины всех случаев цирроза печени в мире связаны с хроническим, в большинстве случаев многолетним злоупотреблением алкоголем. Однако примерно у 25 процентов больных есть указание на вирусный гепатит. И несмотря на сегодняшние диагностические возможности, приблизительно в 25 процентах случаев причина цирроза печени остается невыясненной.
Вы в группе риска по заболе-ваниям печени, если: регулярно подвергаетесь воздействию токсинов или химикатов, регулярно упот-ребляете алкоголь, курите или принимаете наркотики, вам когда-либо делали пере-ливание крови, неправильно питаетесь и имеете лишний вес, злоупотребляете сильно-действующими лекарствами, у вас диабет или повышенное содержание триглицеридов в кровиПо статистике, женщины попадают к врачу на более поздних стадиях болезни.
Признаками алкогольного поражения печени могут быть: двустороннее увеличение околоушных желез, у мужчин атрофия яичек и снижение половой функции. Наблюдается уменьшение мышечной массы, снижение памяти и концентрации внимания, бессонница, раздражительность, дрожание пальцев рук.
Настораживает тот факт, что возрастает число молодых людей с выявленным циррозом печени. Так, в Бюро МСЭ обратились и получили инвалидность в 2010 году — 30 человек молодого возраста, в 2011 году — 35, в 2012 году — 41 человек. Увеличивается и количество больных циррозом, лечение которых не приводит к компенсации состояния.
Как бы банально это ни звучало, действительно легче предупредить развитие заболеваний печени и его осложнений, чем бороться с ними. Но и в том случае, когда цирроз печени уже развился, можно задержать его прогрессирование, поэтому, чем раньше вы обратитесь за медицинской помощью, тем больше шансов на успешное лечение!
Барьеры снаружи и внутри — Основы
By
Александра Вилья-Форте
, доктор медицины, магистр здравоохранения, клиника Кливленда
Полный обзор/редакция, апрель 2022 г. | Изменено в сентябре 2022 г.
| Изменено в сентябре 2022 г.
ПОСМОТРЕТЬ ПРОФЕССИОНАЛЬНУЮ ВЕРСИЮ
Как это ни странно, определить, что снаружи, а что внутри тела, не всегда легко, потому что у тела много поверхностей. Кожа Структура и функции кожи Кожа является самым большим органом тела. Он выполняет множество важных функций, включая защиту тела от травм, регулирование температуры тела, поддержание водно-электролитного баланса, чувствительность… читать далее , которая на самом деле является системой органов, очевидно, находится снаружи тела. Он образует барьер, препятствующий проникновению в организм многих вредных веществ. Пищеварительная система Обзор пищеварительной системы Пищеварительная система, простирающаяся от рта до ануса, отвечает за прием пищи, расщепление ее на питательные вещества (процесс, называемый пищеварением), всасывание питательных веществ в… читать далее длинная трубка, которая начинается у рта, проходит через тело и заканчивается в анусе. Находится ли пища, проходя через эту трубку, внутри или снаружи тела? Питательные вещества и жидкость на самом деле не находятся внутри тела, пока они не впитаются в кровоток.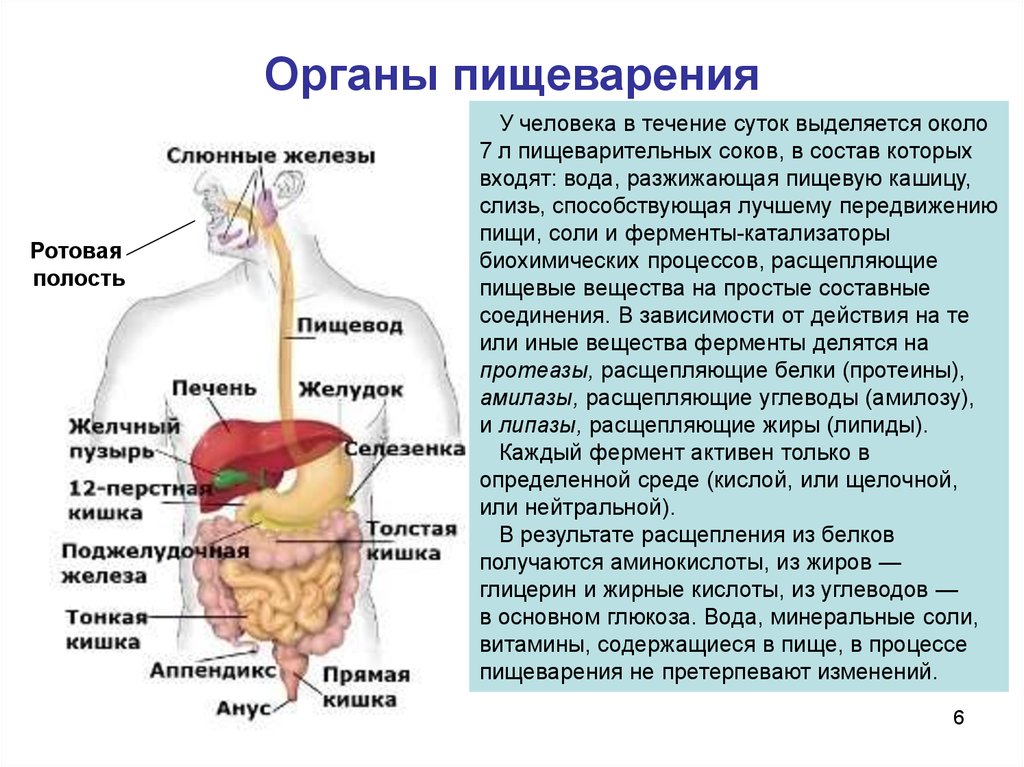
Воздух проходит через нос и глотку в трахею (трахею), затем в обширные ветвящиеся дыхательные пути легких (бронхи). В какой точке находится этот проход внутри тела? Кислород в легких ( см. Общие сведения о дыхательной системе Общие сведения о дыхательной системе Для поддержания жизни организм должен производить достаточное количество энергии. Энергия производится путем сжигания молекул пищи в процессе окисления (при котором молекулы пищи объединяются). с… читать далее ) бесполезен для организма, пока не попадет в кровоток.Чтобы попасть в кровоток, кислород должен пройти через тонкий слой клеток, выстилающих легкие.Этот слой действует как барьер для вирусов и бактерий, таких как те, которые вызывают туберкулез, которые могут переноситься в легкие с воздухом. Если эти организмы не проникают в клетки или не попадают в кровоток, они, как правило, не вызывают заболевания. Поскольку в легких есть много защитных механизмов, таких как антитела для борьбы с инфекцией и крошечные волоски называемые ресничками для удаления мусора из дыхательных путей, большинство переносимых по воздуху инфекционных организмов никогда не вызывают заболеваний.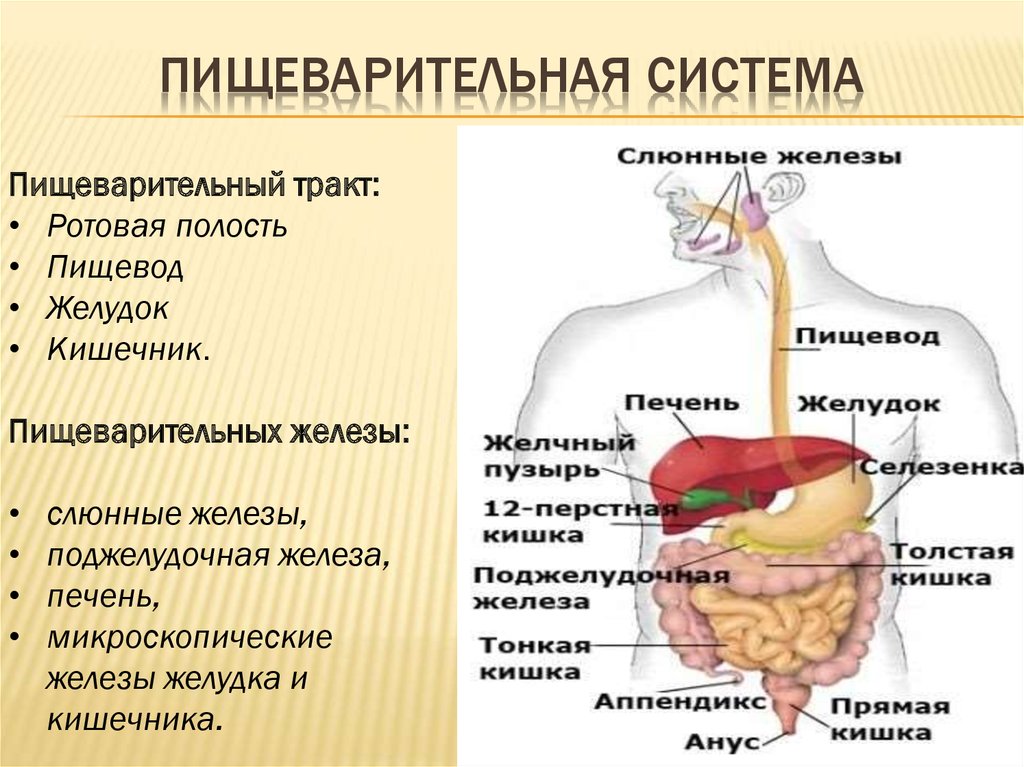 0003
0003
Поверхности тела не только отделяют внешнее от внутреннего, но и удерживают структуры и вещества на своих местах, чтобы они могли нормально функционировать. Например, внутренние органы не плавают в луже крови, потому что кровь обычно ограничена кровеносными сосудами. Если кровь вытекает из сосудов в другие части тела (кровоизлияние), она не только не доставляет кислород и питательные вещества к тканям, но и может причинить серьезный вред. Например, небольшое количество крови, просачивающееся в мозг, может разрушить мозговую ткань, потому что в черепе нет места для расширения. С другой стороны, аналогичное количество крови, просачивающееся в брюшную полость, не разрушает ткань, потому что брюшная полость имеет место для расширения.
Слюна, играющая столь важную роль во рту, может вызвать серьезные повреждения при попадании в легкие, поскольку слюна содержит бактерии, которые могут вызвать образование абсцесса в легком. Соляная кислота, вырабатываемая желудком, редко причиняет ему вред.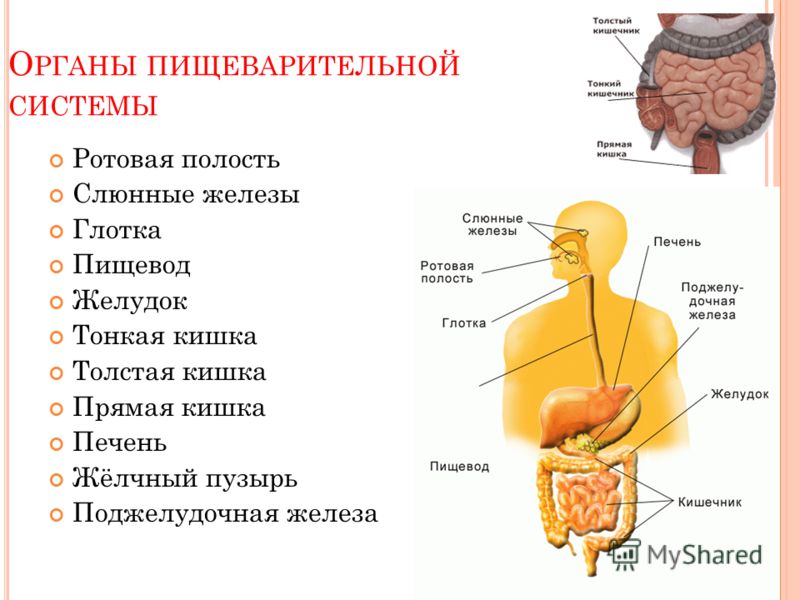 Однако кислота может обжечь и повредить пищевод, если она течет назад, и может повредить другие органы, если просочится через стенку желудка. Стул, непереваренная часть пищи, выбрасываемая через задний проход, может вызвать опасные для жизни инфекции, если он просачивается в брюшную полость, что может произойти, если в стенке кишечника образуется отверстие.
Однако кислота может обжечь и повредить пищевод, если она течет назад, и может повредить другие органы, если просочится через стенку желудка. Стул, непереваренная часть пищи, выбрасываемая через задний проход, может вызвать опасные для жизни инфекции, если он просачивается в брюшную полость, что может произойти, если в стенке кишечника образуется отверстие.
ПОСМОТРЕТЬ ПРОФЕССИОНАЛЬНУЮ ВЕРСИЮ
Авторские права © 2023 Merck & Co., Inc., Рэуэй, Нью-Джерси, США и ее филиалы. Все права защищены.
Проверьте свои знания
Пройди тест!Гематоэнцефалический барьер и церебральный метаболизм (Раздел 4, Глава 11) Неврология в Интернете: Электронный учебник по неврологии | Кафедра нейробиологии и анатомии
11. 1 Гематоэнцефалический барьер Поддерживает постоянство внутренней среды мозга
1 Гематоэнцефалический барьер Поддерживает постоянство внутренней среды мозга
Гематоэнцефалический барьер (ГЭБ) защищает нервную ткань от изменений состава крови и токсинов. В других частях тела внеклеточные концентрации гормонов, аминокислот и калия подвержены частым колебаниям, особенно после еды, физических упражнений или стрессовых ситуаций. Поскольку многие из этих молекул регулируют возбудимость нейронов, подобное изменение состава интерстициальной жидкости в ЦНС может привести к неконтролируемой активности мозга. Эндотелиальные клетки, образующие гематоэнцефалический барьер, узко специализированы, чтобы обеспечить точный контроль над веществами, которые входят или выходят из мозга.
Открытие гематоэнцефалического барьера. Открытие ГЭБ датируется более 100 лет назад, когда в 1880-х годах Пауль Эрлих заметил, что внутривенное введение некоторых красителей (например, трипанового синего) окрашивает все органы, кроме головного и спинного мозга. Он пришел к выводу, что красители имеют более низкое сродство к связыванию с нервной системой по сравнению с другими тканями.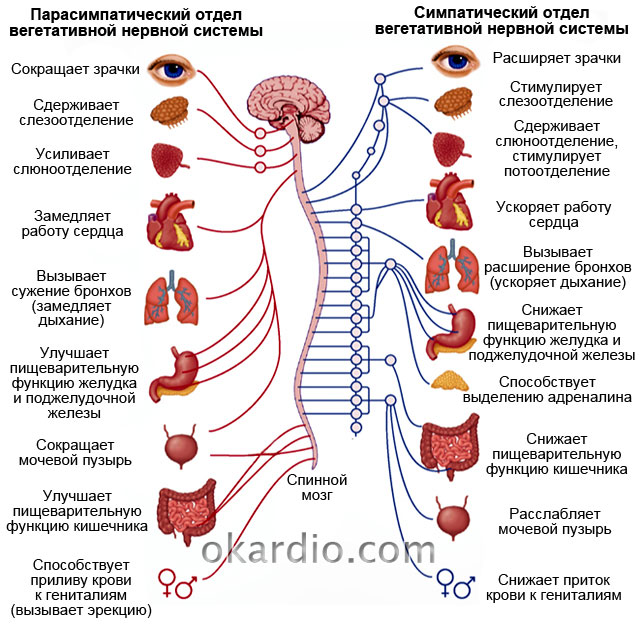 В 1913 году Эдвин Гольдман, сотрудник Эрлиха, продемонстрировал, что те же самые красители при непосредственном введении в спинномозговую жидкость (ЦСЖ) легко окрашивают нервную ткань, но не другие ткани. Однако термин «гематоэнцефалический барьер» был введен Левандовским в 189 г.8, после того как он и его коллеги провели эксперименты, чтобы продемонстрировать, что нейротоксические агенты влияют на функцию мозга только при прямом введении в мозг, но не при введении в сосудистую систему. Потребовалось еще 70 лет, пока Риз и его коллеги локализовали барьер для капиллярных эндотелиальных клеток в мозге с помощью электронно-микроскопических исследований.
В 1913 году Эдвин Гольдман, сотрудник Эрлиха, продемонстрировал, что те же самые красители при непосредственном введении в спинномозговую жидкость (ЦСЖ) легко окрашивают нервную ткань, но не другие ткани. Однако термин «гематоэнцефалический барьер» был введен Левандовским в 189 г.8, после того как он и его коллеги провели эксперименты, чтобы продемонстрировать, что нейротоксические агенты влияют на функцию мозга только при прямом введении в мозг, но не при введении в сосудистую систему. Потребовалось еще 70 лет, пока Риз и его коллеги локализовали барьер для капиллярных эндотелиальных клеток в мозге с помощью электронно-микроскопических исследований.
Рисунок 11.1a | Рисунок 11.1b |
Эндотелиальные клетки в капиллярах головного мозга являются местом ГЭБ. ГЭБ у взрослых состоит из сложной клеточной системы, состоящей из узкоспециализированной базальной мембраны, большого количества перицитов, встроенных в базальную мембрану, и концевых ножек астроцитов.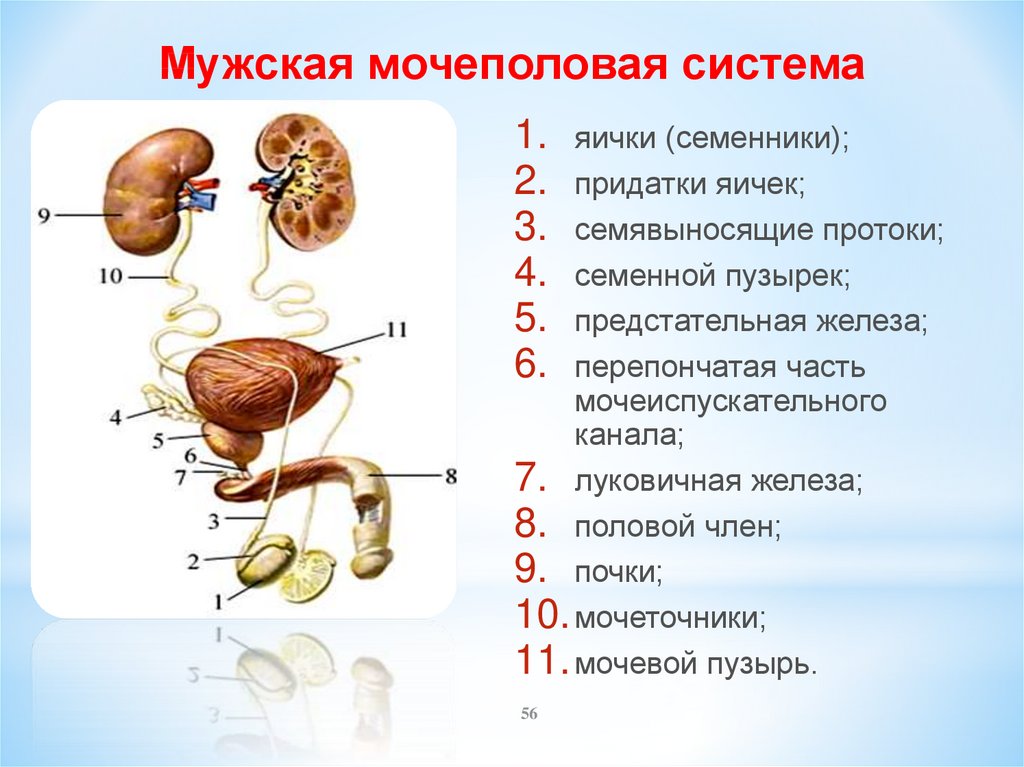 В то время как эндотелиальные клетки формируют собственно барьер, взаимодействие с соседними клетками, по-видимому, необходимо для развития барьера. Эндотелиальные клетки головного мозга отличаются от эндотелиальных клеток других органов по двум важным признакам. Во-первых, между эндотелиальными клетками головного мозга присутствуют непрерывные плотные контакты. Эти плотные соединения предотвращают парацеллюлярное движение молекул. Во-вторых, отсутствуют обнаруживаемые трансэндотелиальные пути, такие как внутриклеточные везикулы. Эти свойства эндотелиальных клеток головного мозга обеспечивают барьер между кровью и мозгом. Некоторые из ключевых процессов изображены на рис. 11.1.
В то время как эндотелиальные клетки формируют собственно барьер, взаимодействие с соседними клетками, по-видимому, необходимо для развития барьера. Эндотелиальные клетки головного мозга отличаются от эндотелиальных клеток других органов по двум важным признакам. Во-первых, между эндотелиальными клетками головного мозга присутствуют непрерывные плотные контакты. Эти плотные соединения предотвращают парацеллюлярное движение молекул. Во-вторых, отсутствуют обнаруживаемые трансэндотелиальные пути, такие как внутриклеточные везикулы. Эти свойства эндотелиальных клеток головного мозга обеспечивают барьер между кровью и мозгом. Некоторые из ключевых процессов изображены на рис. 11.1.
Рисунок 11.2 |
- Непрерывные плотные соединения, соединяющие эндотелиальные клетки в капиллярах головного мозга, ограничивают диффузию молекул через ГЭБ.

- Базальная (базальная) мембрана обеспечивает структурную поддержку капилляров, и предполагается, что специфические белки, присутствующие в базальной мембране, участвуют в развитии ГЭБ.
- Астроцитарные отростки стопы выделяют специфические факторы и необходимы для развития ГЭБ. Отростки астроцитов стопы содержат водные каналы (аквапорин-4), которые обеспечивают поглощение воды и способствуют отеку мозга.
- Транспортеры для глюкозы и незаменимых аминокислот облегчают перемещение этих растворенных веществ в мозг. Поскольку клетки мозга не могут синтезировать эти незаменимые аминокислоты, они поглощаются кровью.
- Вторичные транспортные системы вызывают отток малых молекул и заменимых аминокислот из мозга в кровь.
- Транспортеры ионов натрия на люминальной мембране и Na,K-АТФаза на антилюминальной мембране отвечают за перемещение натрия из крови в мозг. Большое количество митохондрий, присутствующих в эндотелиальных клетках головного мозга, обеспечивает энергию для функции этой Na,K-АТФазы.

- «Ферментный гематоэнцефалический барьер»: метаболические процессы в эндотелиальных клетках капилляров головного мозга важны для функции крови и головного мозга и контролируют поступление нейротрансмиттеров в мозг.
11.2 Молекулярные компоненты плотных контактов
Рисунок 11.3 |
Плотные контакты между эндотелиальными клетками отвечают за барьерную функцию. Окклюдин был первым интегральным мембранным белком, локализованным исключительно в пределах плотных контактов. Однако у мышей, несущих нулевую мутацию в гене occludin, развиваются морфологически нормальные плотные контакты, что указывает на то, что окклюзия не является существенной для правильного образования плотных контактов. Было показано, что в отличие от окклюзии клаудины необходимы для образования плотных контактов. Интегральные мембранные белки плотных контактов связаны с цитоскелетом через зоны окклюзии-1 (ЗО-1), ЗО-2 и ЗО-3. Кроме того, соединения, не связанные с окклюдином, перемежаются с плотными соединениями. В слипчивых соединениях обнаружены специфичные для эндотелия интегральные мембранные белки VE-кадгерины. Более того, семейство белков, называемых соединительными молекулами адгезии (JAM), и недавно открытые молекулы адгезии, селективной к эндотелиальным клеткам (ESAM), локализованы в плотных соединениях ГЭБ. Их точная функция в целостности ГЭБ еще предстоит определить.
Кроме того, соединения, не связанные с окклюдином, перемежаются с плотными соединениями. В слипчивых соединениях обнаружены специфичные для эндотелия интегральные мембранные белки VE-кадгерины. Более того, семейство белков, называемых соединительными молекулами адгезии (JAM), и недавно открытые молекулы адгезии, селективной к эндотелиальным клеткам (ESAM), локализованы в плотных соединениях ГЭБ. Их точная функция в целостности ГЭБ еще предстоит определить.
Все области головного мозга не имеют гематоэнцефалического барьера. Структуры, расположенные в стратегических позициях по средней линии желудочковой системы и лишенные ГЭБ, в совокупности называются околожелудочковыми органами (ОЦО). В этих небарьерных областях плотные соединения между эндотелиальными клетками прерывистые, что позволяет проникать молекулам. Многие из этих областей участвуют в гормональном контроле.
Области головного мозга без гематоэнцефалического барьера:
- Гипофиз
- Срединное возвышение
- Район пострема
- Преоптическое углубление
- Парафиз
- Шишковидная железа
- Эндотелий сосудистого сплетения
Рисунок 11. |
Вещества с высокой растворимостью в липидах могут перемещаться через ГЭБ путем простой диффузии. Диффузия является основным механизмом проникновения большинства психоактивных веществ. На рис. 11.2 показано, что скорость проникновения диффундирующих в мозг соединений зависит от их растворимости в липидах. Растворимость в липидах оценивают по коэффициенту распределения масло/вода.
На рис. 11.5а показано, как рассчитывается коэффициент распределения нефть/вода. На рис. 11.5b показана взаимосвязь между коэффициентом распределения нефть/вода и проникновением выбранных молекул в мозг.
Рисунок 11.5a | Рисунок 11.5b | Рисунок 11. |
Вода. Вода легко проникает в мозг. Вследствие высокой проницаемости вода свободно проникает в головной мозг и выходит из него по мере изменения осмолярности плазмы. Это явление имеет клиническое значение, поскольку внутривенное введение таких малопроницаемых соединений, как маннит, вызывает осмотическое обезвоживание мозга и снижает внутричерепное давление. Этот метод иногда используется у пациентов с черепно-мозговой травмой для снижения внутричерепного давления.
Газы. Газы, такие как CO2, O2 и летучие анестетики, быстро диффундируют в мозг. Как следствие, скорость, с которой их концентрация в мозгу приходит в равновесие с плазмой, ограничивается в первую очередь скоростью мозгового кровотока.
11.3 Транспорт глюкозы и аминокислот
Рисунок 11.7 |
Опосредованный переносчиком транспорт позволяет молекулам с низкой растворимостью в липидах преодолевать гематоэнцефалический барьер. Глюкоза из крови поступает в мозг транспортным белком. Глюкоза является основным энергетическим субстратом мозга. Транспортный белок глюкозы (GLUT-1) в большом количестве содержится в эндотелиальных клетках капилляров головного мозга. Эти транспортеры переносят молекулы глюкозы через гематоэнцефалический барьер. Хотя редко, у пациентов с дефицитом Glut-1 (вызванным генетическими мутациями) могут быть серьезные трудности с обучением. Низкий уровень сахара-глюкозы в спинномозговой системе, но не в крови, будет определять состояние.
Незаменимые аминокислоты не могут быть синтезированы мозгом и, следовательно, должны поступать в результате расщепления белков и пищи. Фенилаланин, лейцин, тирозин, изолейцин, валин, триптофан, метионин и гистидин, являющиеся незаменимыми аминокислотами, а также предшественник дофамина, L-ДОФА, попадают в мозг так же быстро, как и глюкоза.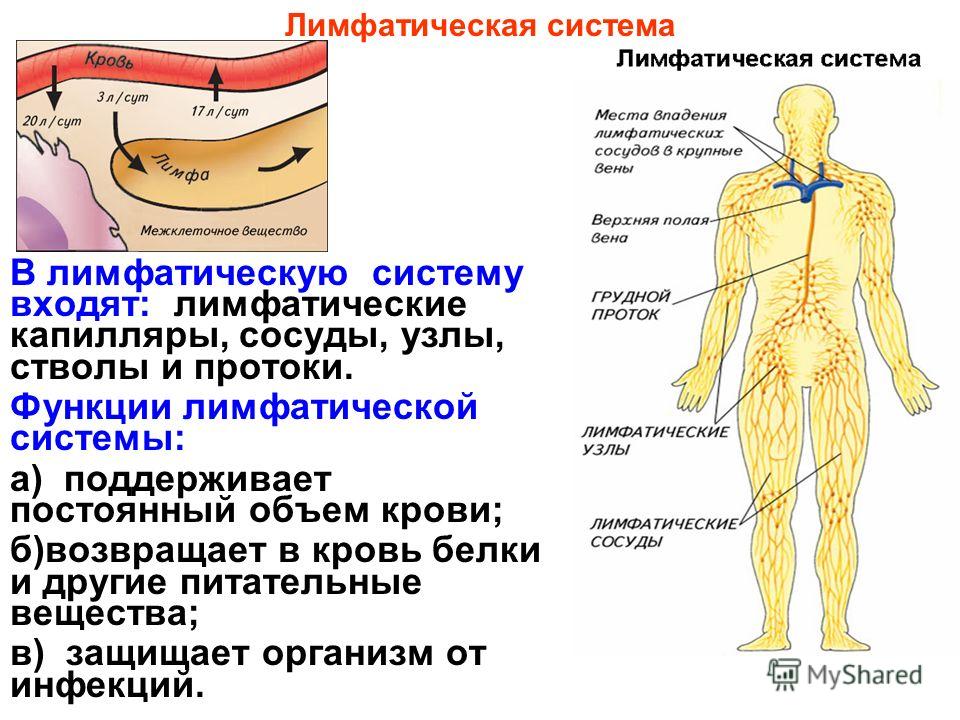 Эти аминокислоты транспортируются в мозг предпочитающими лейцин или транспортными белками L-типа. Эти соединения конкурируют друг с другом за проникновение в мозг. Следовательно, повышение уровня одного из них в плазме будет подавлять поглощение других. Эта конкуренция может быть важна при некоторых метаболических заболеваниях, таких как фенилкетонурия (ФКУ), когда высокие уровни фенилаланина в плазме снижают поглощение мозгом других незаменимых аминокислот.
Эти аминокислоты транспортируются в мозг предпочитающими лейцин или транспортными белками L-типа. Эти соединения конкурируют друг с другом за проникновение в мозг. Следовательно, повышение уровня одного из них в плазме будет подавлять поглощение других. Эта конкуренция может быть важна при некоторых метаболических заболеваниях, таких как фенилкетонурия (ФКУ), когда высокие уровни фенилаланина в плазме снижают поглощение мозгом других незаменимых аминокислот.
Небольшие нейтральные аминокислоты, такие как аланин, глицин, пролин и ГАМК (гамма-аминомасляная кислота), значительно ограничены в их поступлении в мозг. Эти аминокислоты являются заменимыми аминокислотами и транспортируются предпочитающим аланин транспортным белком или транспортным белком А-типа. Транспортный белок А-типа отсутствует на люминальной поверхности гематоэнцефалического барьера. Напротив, эти небольшие нейтральные аминокислоты, по-видимому, транспортируются из мозга через гематоэнцефалический барьер.
11. 4 Защита головного мозга от переносимых кровью нейротоксинов и лекарств
4 Защита головного мозга от переносимых кровью нейротоксинов и лекарств
P-гликопротеины представляют собой насосы, управляемые АТФ, которые обеспечивают множественную лекарственную устойчивость раковых клеток путем выкачивания лекарств из клеток. Эти белки экспрессируются в эндотелиальных клетках головного мозга, что может ограничивать проницаемость ГЭБ для гидрофобных соединений, таких как циклоспорин А и винбластин, путем перекачки их из эндотелиальных клеток обратно в кровь.
Метаболические процессы в эндотелиальных клетках капилляров головного мозга важны для функции крови и мозга. Большинство нейротрансмиттеров, присутствующих в крови, не попадают в мозг из-за их низкой растворимости в липидах и отсутствия специфических транспортных переносчиков в люминальной мембране эндотелиальных клеток капилляров (см. рис. 11.1). Напротив, L-ДОФА, предшественник дофамина, имеет сродство к переносчику L-типа. Следовательно, он легче попадает в мозг из крови, чем это можно было бы предсказать на основании его растворимости в липидах. По этой причине пациентов с болезнью Паркинсона лечат L-ДОФА, а не дофамином. Однако проникновение L-ДОФА в головной мозг ограничено наличием ферментов L-ДОФА-декарбоксилазы и моноаминоксидазы в эндотелиальных клетках капилляров. Этот «ферментативный гематоэнцефалический барьер» ограничивает проникновение L-ДОФА в мозг и объясняет необходимость больших доз L-ДОФА при лечении болезни Паркинсона. Терапия в настоящее время усиливается одновременным лечением ингибитором декарбоксилазы L-ДОФА.
По этой причине пациентов с болезнью Паркинсона лечат L-ДОФА, а не дофамином. Однако проникновение L-ДОФА в головной мозг ограничено наличием ферментов L-ДОФА-декарбоксилазы и моноаминоксидазы в эндотелиальных клетках капилляров. Этот «ферментативный гематоэнцефалический барьер» ограничивает проникновение L-ДОФА в мозг и объясняет необходимость больших доз L-ДОФА при лечении болезни Паркинсона. Терапия в настоящее время усиливается одновременным лечением ингибитором декарбоксилазы L-ДОФА.
| Рисунок 11.8a |
Рисунок 11.8b |
Эндотелиальная моноаминоксидаза также может играть роль в инактивации нейротрансмиттеров, высвобождаемых при активности нейронов. Моноамины демонстрируют очень малое поглощение при попадании со стороны просвета. Системы поглощения моноаминов присутствуют на антилюминальной поверхности эндотелиальных клеток капилляров головного мозга.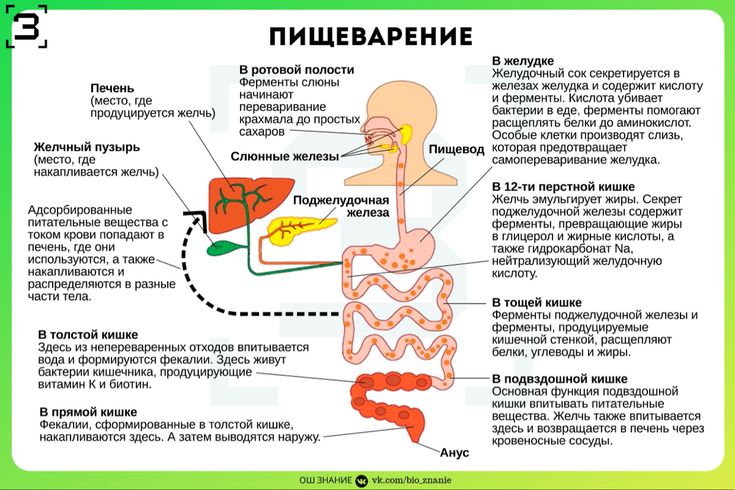 Эндотелиальные капилляры головного мозга также содержат множество других ферментов, метаболизирующих нейротрансмиттеры, таких как холинэстеразы, ГАМК-трансаминазы, аминопептидазы и эндопептидазы. Кроме того, в капиллярах головного мозга обнаружено несколько ферментов, метаболизирующих лекарства и токсины. Таким образом, «ферментативный гематоэнцефалический барьер» защищает мозг не только от циркулирующих нейротрансмиттеров, но и от многих токсинов.
Эндотелиальные капилляры головного мозга также содержат множество других ферментов, метаболизирующих нейротрансмиттеры, таких как холинэстеразы, ГАМК-трансаминазы, аминопептидазы и эндопептидазы. Кроме того, в капиллярах головного мозга обнаружено несколько ферментов, метаболизирующих лекарства и токсины. Таким образом, «ферментативный гематоэнцефалический барьер» защищает мозг не только от циркулирующих нейротрансмиттеров, но и от многих токсинов.
Нарушение ГЭБ и заболевание. Дисфункция ГЭБ может привести к повреждению нейронов и нарушению функции головного мозга. Такие заболевания, как энцефалит, рассеянный склероз (РС), инсульт или опухоли вызывают ухудшение ГЭБ с разрушительным влиянием на функцию нейронов. Эти условия снижают выработку белка плотных контактов клаудина. Опухоли головного мозга вызывают полное разрушение ГЭБ, что приводит к перитуморальному отеку. Кроме того, опухолевые клетки секретируют специфические факторы [например, фактор роста эндотелия сосудов (VEGF), который индуцирует образование новых кровеносных сосудов (или ангиогенез)], которые имеют тенденцию к негерметичности.
Рисунок 11.9 |
Обход ГЭБ лекарственными препаратами. Ряд лекарственных средств с потенциальной терапевтической ценностью с трудом проникает в головной мозг, поскольку они имеют низкую растворимость в липидах и не транспортируются специфическими переносчиками, присутствующими в ГЭБ. Чтобы преодолеть это ограничение, были разработаны схемы для улучшения проникновения лекарств в мозг. 1) Одним из способов обхода ГЭБ является введение препарата непосредственно в спинномозговую жидкость. Этот подход можно использовать для лечения пациентов с менингитом или раковыми клетками в спинномозговой жидкости. 2) Некоторые вазоактивные соединения, такие как брадикинин и гистамин, которые не изменяют ГЭБ у нормальных людей, могут повышать проницаемость ГЭБ при патологических состояниях. Эти соединения могут быть использованы для доставки химиотерапевтических агентов в головной мозг.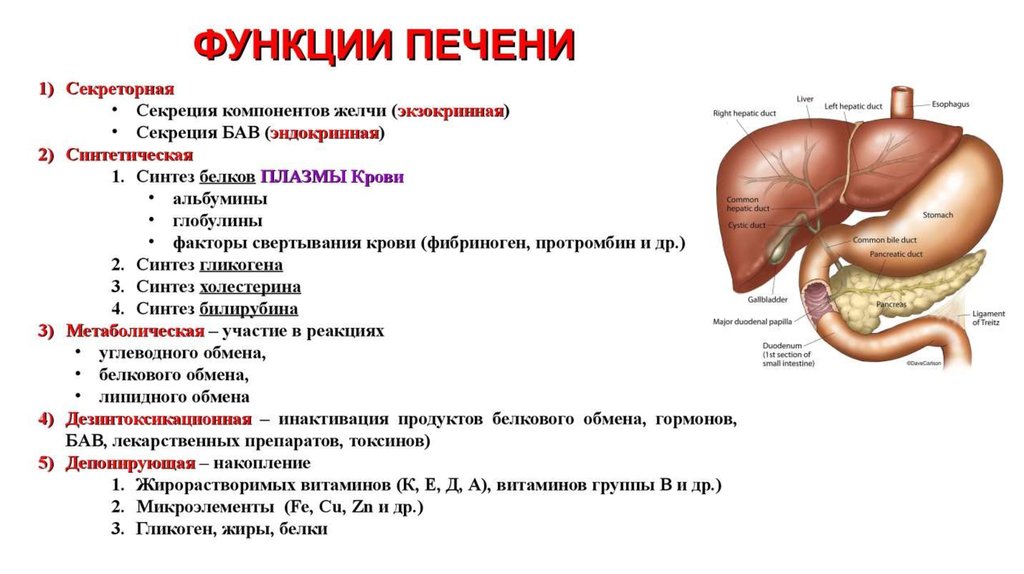 3) Препараты могут быть синтезированы с высокой проницаемостью ГЭБ для улучшения проникновения в головной мозг. Большинство нейроактивных препаратов эффективны, поскольку они растворяются в липидах и легко попадают в мозг. Например, героин и морфин очень похожи по структуре. Однако героин, содержащий две ацетильные группы, лучше растворим в липидах. Эта большая растворимость героина в липидах объясняет его более быстрое начало действия. Попав в мозг, ацетильная группа героина ферментативно удаляется с образованием морфина, который очень медленно покидает мозг. Понимание процесса транспорта имеет решающее значение для разработки следующего поколения лекарств, полезных для лечения заболеваний головного мозга.
3) Препараты могут быть синтезированы с высокой проницаемостью ГЭБ для улучшения проникновения в головной мозг. Большинство нейроактивных препаратов эффективны, поскольку они растворяются в липидах и легко попадают в мозг. Например, героин и морфин очень похожи по структуре. Однако героин, содержащий две ацетильные группы, лучше растворим в липидах. Эта большая растворимость героина в липидах объясняет его более быстрое начало действия. Попав в мозг, ацетильная группа героина ферментативно удаляется с образованием морфина, который очень медленно покидает мозг. Понимание процесса транспорта имеет решающее значение для разработки следующего поколения лекарств, полезных для лечения заболеваний головного мозга.
11.5 Мозговой метаболизм и кровоток
Мозговой метаболизм
Мозг метаболически является одним из наиболее активных органов тела. Мозг не хранит избыточную энергию и почти всю необходимую энергию получает за счет аэробного окисления глюкозы. Следовательно, для удовлетворения энергетических потребностей ему требуется непрерывная подача глюкозы и кислорода. Большая часть энергетических затрат мозга расходуется на активный транспорт ионов для поддержания и восстановления мембранных потенциалов, разряжающихся в процессе возбуждения и проведения. Когда приток крови к мозгу прекращается и возникает недостаток кислорода и крови, наступает потеря сознания через 5-10 секунд. Если кровоток не возобновляется в течение нескольких минут, происходит необратимое повреждение головного мозга. Хорошо известно, что при кризах, например при остановке сердца, поражение головного мозга наступает раньше всего и является наиболее решающим в определении степени выздоровления. Отсутствие глюкозы в равной степени разрушительно, но период времени, приводящий к необратимым повреждениям от гипогликемии, больше, поскольку можно использовать другие субстраты.
Большая часть энергетических затрат мозга расходуется на активный транспорт ионов для поддержания и восстановления мембранных потенциалов, разряжающихся в процессе возбуждения и проведения. Когда приток крови к мозгу прекращается и возникает недостаток кислорода и крови, наступает потеря сознания через 5-10 секунд. Если кровоток не возобновляется в течение нескольких минут, происходит необратимое повреждение головного мозга. Хорошо известно, что при кризах, например при остановке сердца, поражение головного мозга наступает раньше всего и является наиболее решающим в определении степени выздоровления. Отсутствие глюкозы в равной степени разрушительно, но период времени, приводящий к необратимым повреждениям от гипогликемии, больше, поскольку можно использовать другие субстраты.
Различные области мозга имеют разные потребности в энергии, которые связаны с активностью нейронов в этих областях. Измерение количества глюкозы, используемой в минуту в различных областях мозга крысы и обезьяны в нормальном сознании, показывает, что утилизация глюкозы сильно различается по всему мозгу. При этом среднее значение в сером веществе примерно в пять раз больше, чем в белом веществе.
При этом среднее значение в сером веществе примерно в пять раз больше, чем в белом веществе.
Объем кровотока напрямую связан с мозговой активностью. В отдельной группе животных определяли объем притока крови к участкам головного мозга. Результаты показывают, что больше крови притекает к области мозга с высокой метаболической активностью.
Рисунок 11.10 Взаимосвязь между мозговым кровотоком и метаболизмом глюкозы. |
На рис. 11.10 показана превосходная корреляция между количеством потребляемой глюкозы и локальным мозговым кровотоком.
Регуляция притока крови к области головного мозга достигается за счет контроля расширения мозговых сосудов. Расширение кровеносных сосудов контролируется местными факторами, такими как оксид азота (NO), PaCO2, PaO2 и pH. Высокий уровень NO, высокий PaCO2, низкий PaCO2 и низкий pH, возникающие в результате активности мозга, имеют тенденцию расширять кровеносные сосуды и увеличивать кровоток. Скорость производства этих химических веществ зависит от активности и скорости энергетического метаболизма. Следовательно, приток крови к области мозга связан с активностью нейронов в этой области.
Скорость производства этих химических веществ зависит от активности и скорости энергетического метаболизма. Следовательно, приток крови к области мозга связан с активностью нейронов в этой области.
Утилизация глюкозы и визуализация головного мозга. Метаболизм глюкозы является основным источником энергии для мозга. Глюкоза из крови поступает в мозг с помощью транспортного белка Glut-1. Оказавшись внутри клетки мозга, он вступает в гликолитический путь, где превращается в пируват, а затем метаболизируется в цикле Кребса с образованием АТФ. Часть молекул АТФ используется для образования высокоэнергетических молекул фосфокреатина. В условиях аэробного метаболизма глюкоза способна обеспечить мозг достаточным количеством энергии за счет АТФ и фосфокреатина для поддержания нормальной функции. Когда возникает мозговая недостаточность, сначала происходит потеря фосфокреатина, за которой следует истощение АТФ, что обычно сигнализирует о серьезном повреждении мозга.
Депривация глюкозы может привести к нарушению функции мозга.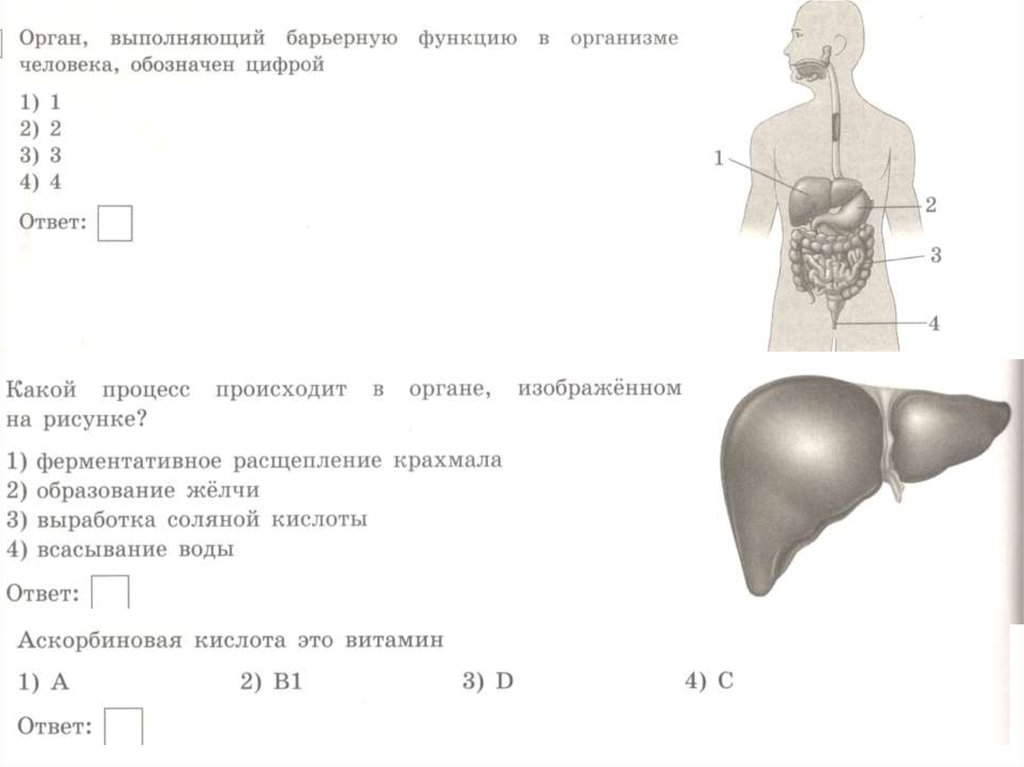 Гипогликемия, которая может возникнуть в результате избыточного инсулина, связана с изменениями психического состояния. Эти изменения могут быть быстро устранены введением глюкозы. В определенных обстоятельствах, например во время голодания, мозг может использовать в качестве субстрата «кетоновые тела» вместо глюкозы. Кетоновые тела, ацетоацетат и D-бета-гидроксибутират образуются в результате катаболизма жирных кислот в печени. Кетоновые тела метаболизируются с образованием ацил-КоА, который вступает в цикл трикарбоновых кислот (ЦТК) с достаточной скоростью для удовлетворения метаболических потребностей мозга.
Гипогликемия, которая может возникнуть в результате избыточного инсулина, связана с изменениями психического состояния. Эти изменения могут быть быстро устранены введением глюкозы. В определенных обстоятельствах, например во время голодания, мозг может использовать в качестве субстрата «кетоновые тела» вместо глюкозы. Кетоновые тела, ацетоацетат и D-бета-гидроксибутират образуются в результате катаболизма жирных кислот в печени. Кетоновые тела метаболизируются с образованием ацил-КоА, который вступает в цикл трикарбоновых кислот (ЦТК) с достаточной скоростью для удовлетворения метаболических потребностей мозга.
Измерение местного использования глюкозы. Местный энергетический обмен сопряжен с локальной функциональной активностью. Для измерения метаболизма глюкозы у экспериментальных животных применяли авторадиографический аналог глюкозы, 2-дезоксиглюкозу (2-ДГ).
Рисунок 11. | Рисунок 11.11b |
Рисунок 11.4 иллюстрирует фундаментальный принцип метода радиоактивной дезоксиглюкозы для измерения локального использования глюкозы мозгом. Утилизация глюкозы начинается с фосфорилирования глюкозы гексокиназой. Образовавшийся глюкозо-6-фосфат не задерживается в тканях. Вместо этого он далее метаболизируется в такие продукты, как CO2 и H3O, которые покидают ткани. 2-дезоксиглюкоза является аналогом глюкозы и транспортируется через гематоэнцефалический барьер с помощью системы переноса глюкозы. Внутри клеток головного мозга 2-дезоксиглюкоза фосфорилируется гексокиназой до дезоксиглюкозо-6-фосфата (ДГ-6-Ф) и не может далее расщепляться до СО2 и Н3О. Вместо этого он задерживается и накапливается в тканях в течение разумного периода времени. Поставив метку на дезоксиглюкозу (такую как [18F] фтор-2-дезокси-D-глюкоза), можно измерить скорость образования меченой дезоксиглюкозо-6-фосфата. Количество 18FDG-6-фосфата можно определить непосредственно с помощью позитронно-эмиссионной томографии (ПЭТ). Метод 2-дезоксиглюкозы был модифицирован для использования человеком с помощью ПЭТ с короткоживущими изотопами, испускающими позитроны, помеченными 2-дезоксиглюкозой.
Поставив метку на дезоксиглюкозу (такую как [18F] фтор-2-дезокси-D-глюкоза), можно измерить скорость образования меченой дезоксиглюкозо-6-фосфата. Количество 18FDG-6-фосфата можно определить непосредственно с помощью позитронно-эмиссионной томографии (ПЭТ). Метод 2-дезоксиглюкозы был модифицирован для использования человеком с помощью ПЭТ с короткоживущими изотопами, испускающими позитроны, помеченными 2-дезоксиглюкозой.
11.6 Функциональная активация энергетического обмена
Рис. 11.12 |
Из-за связи метаболизма с функцией функциональная активация с помощью определенных стимулов приводит к региональному увеличению метаболизма глюкозы в соответствующих мозговых структурах. Движение пальцев и рук увеличивает метаболизм в соответствующих областях мозга. У праворуких добровольцев спонтанная речь увеличивала метаболическую активность в области Брока.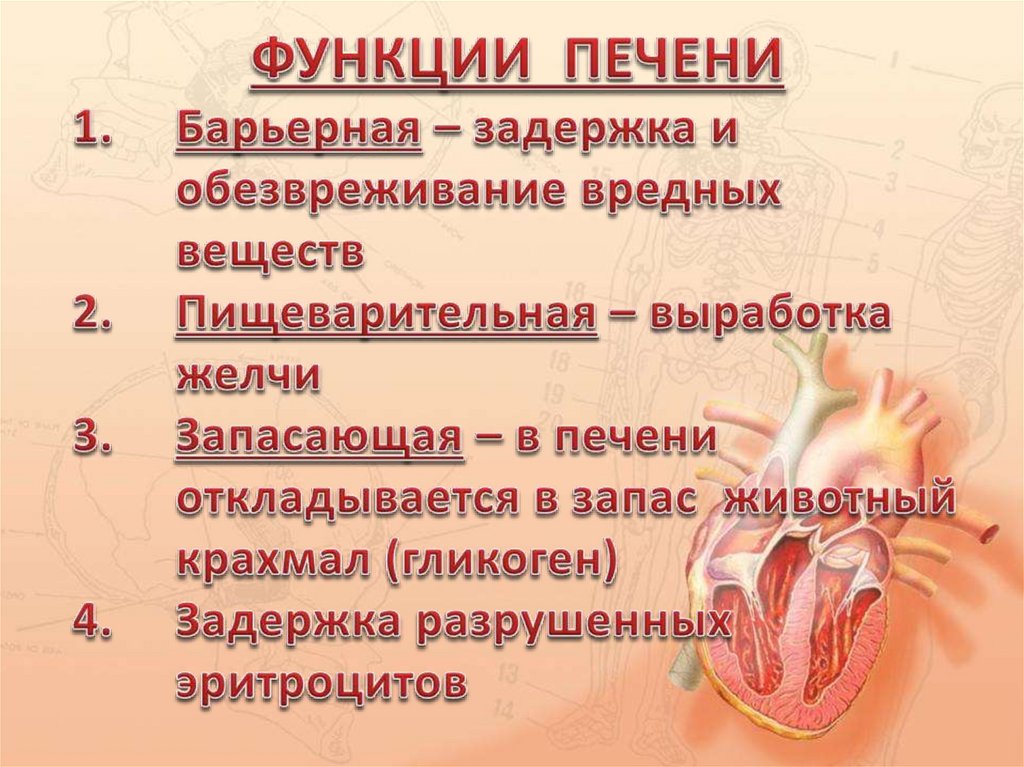 Представление зрительных образов увеличивает утилизацию глюкозы в первичной зрительной коре.
Представление зрительных образов увеличивает утилизацию глюкозы в первичной зрительной коре.
Функциональная МРТ. Вариант МРТ, называемый функциональной МРТ (фМРТ), основан на увеличении притока крови к определенным областям мозга, которое сопровождает активность нейронов. Увеличение кровотока приводит к локальному снижению дезоксигемоглобина из-за меньшей экстракции кислорода. Деоксигемоглобин является парамагнитным и служит источником сигнала в фМРТ. В отличие от ПЭТ, фМРТ использует сигнал, присущий мозгу, и стала предпочтительной технологией для исследования функций мозга.
Рисунок 11.13 |
11.7 Мозговые расстройства и обмен веществ
Судорожные расстройства представляют собой функциональные нарушения мозговой деятельности и приводят к выраженным изменениям метаболизма головного мозга и мозгового кровотока.


 4
4 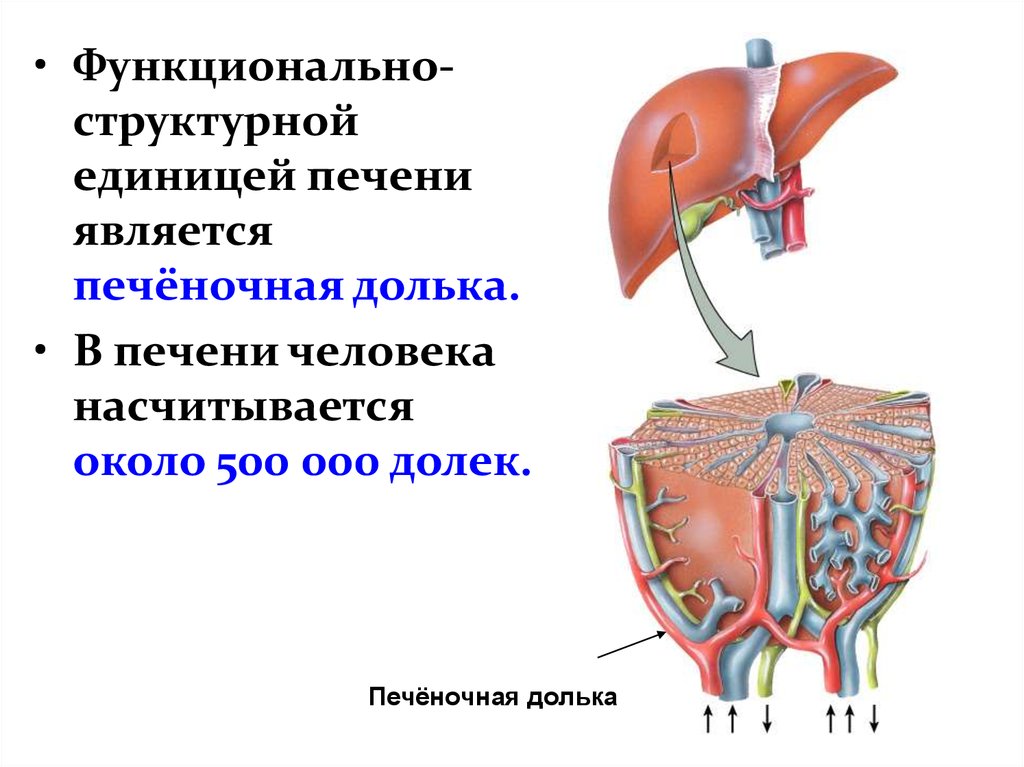 6
6 
 11a
11a
Leave A Comment