ICSC 1653 — ОКСИД НАТРИЯ
ICSC 1653 — ОКСИД НАТРИЯ« back to the search result list(ru)
Chinese — ZHEnglish — ENFinnish — FIFrench — FRGerman — DEHebrew — HEHungarian — HUItalian — ITJapanese — JAKorean — KOPersian — FAPolish — PLPortuguese — PTRussian — RUSpanish — ES
| ОКСИД НАТРИЯ | ICSC: 1653 (Октябрь 2006) |
| CAS #: 1313-59-3 |
| UN #: 1825 |
| EINECS #: 215-208-9 |
| ОСОБЫЕ ОПАСНОСТИ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ТУШЕНИЕ ПОЖАРА | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горючее, но способствует возгоранию других веществ. |
НЕ использовать воду. Использовать сухой порошок, сухой песк. |
| ИЗБЕГАТЬ ЛЮБЫХ КОНТАКТОВ! НЕ ДОПУСКАТЬ ОБРАЗОВАНИЕ ПЫЛИ! ВО ВСЕХ СЛУЧАЯХ ОБРАТИТЬСЯ К ВРАЧУ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРОФИЛАКТИЧЕСКИЕ МЕРЫ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Боли в горле. Кашель. Ощущения жжения. Затрудненное дыхание. Сбивчивое дыхание. | Применять местную вытяжку. Применять средства защиты органов дыхания. | Свежий воздух, покой. Полусидячее положение. Может потребоваться искусственное дыхание. Немедленно обратиться за медицинской помощью. |
| Кожа | Покраснение. Боль. Серьезные ожоги кожи. | Защитные перчатки. Защитная одежда. | Снять загрязненную одежду. Промыть кожу большим количеством воды или принять душ. Обратиться за медицинской помощью. Промыть кожу большим количеством воды или принять душ. Обратиться за медицинской помощью. |
| Глаза | Покраснение. Боль. Ожоги. | Использовать маску для лица или средства защиты глаз в комбинации со средствами защиты органов дыхания если вещество в порошкообразном соостоянии. | Промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно сделать без затруднений). Немедленно обратиться за медицинской помощью. |
| Проглатывание | Боль в горле. Ощущение жжения в горле и груди. Шок или сильная слабость. | Не принимать пищу, напитки и не курить во время работы. | Прополоскать рот. НЕ вызывать рвоту. Обратиться за медицинской помощью. |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
Индивидуальная защита: костюм химической защиты, включая автономный дыхательный аппарат.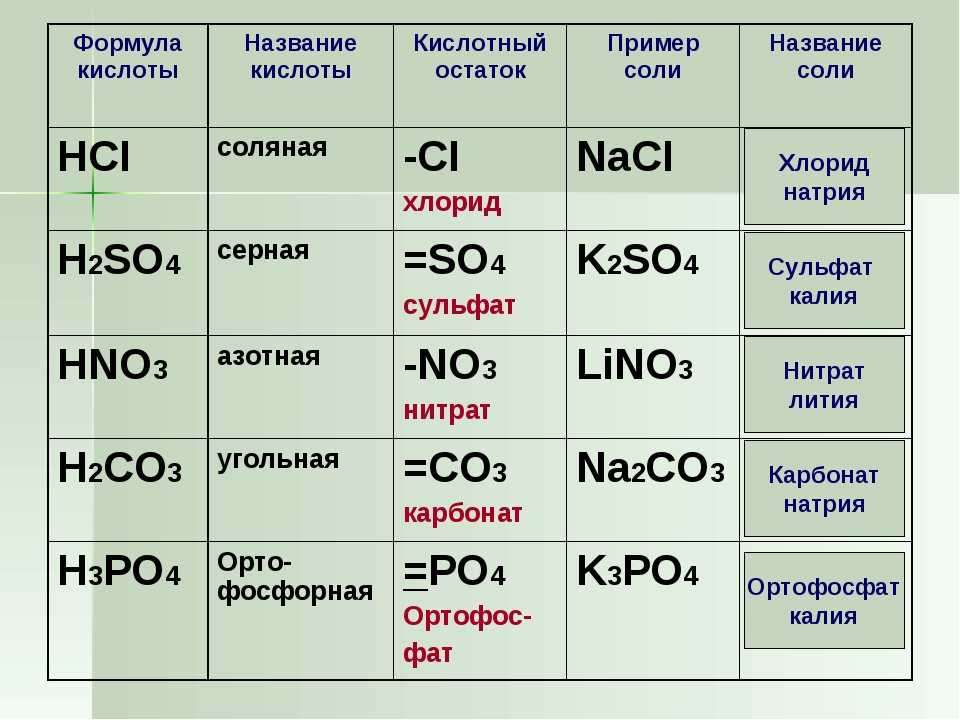 Сухие пластиковыеСмести просыпанное вещество в закрытые контейнеры. Смыть остаток большим количеством воды. Сухие пластиковыеСмести просыпанное вещество в закрытые контейнеры. Смыть остаток большим количеством воды. |
Согласно критериям СГС ООН ОПАСНО Вызывает серьезные ожоги кожи и повреждения глазТранспортировка |
| ХРАНЕНИЕ | |
| Отдельно от сильных кислот и пищевых продуктов и кормов. Хранить сухим. | |
| УПАКОВКА | |
| Не перевозить с продуктами питания и кормами для животных. |
| ОКСИД НАТРИЯ |
ICSC: 1653 |
| ФИЗИЧЕСКИЕ И ХИМИЧЕСКИЕ СВОЙСТВА | |
|---|---|
|
Агрегатное Состояние; Внешний Вид
Физические опасности
Химические опасности
|
Формула: Na2O |
| ВОЗДЕЙСТВИЕ НА ОРГАНИЗМ И ЭФФЕКТЫ ОТ ВОЗДЕЙСТВИЯ | |
|---|---|
|
Пути воздействия
Эффекты от кратковременного воздействия
 Едкое вещество при приеме внутрь. Вдыхание аэрозоля может вызвать отек легких. См Примечания Необходимо медицинское обследование. Едкое вещество при приеме внутрь. Вдыхание аэрозоля может вызвать отек легких. См Примечания Необходимо медицинское обследование.
|
Риск вдыхания
Эффекты от длительного или повторяющегося воздействия
|
| Предельно-допустимые концентрации |
|---|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|
| ПРИМЕЧАНИЯ |
|---|
Бурно реагирует с такими средствами пожаротушения, как вода. Симптомы отека легких часто не проявляются, пока не пройдет несколько часов, и они усугубляются физическими усилиями. Следует рассмотреть возможность немедленного проведения соответствующей ингаляционной терапии врачом или уполномоченным на это лицом. См. карту ICSC 0360. |
| ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ |
|---|
|
Классификация ЕС |
| (ru) | Ни МОТ, ни ВОЗ, ни Европейский Союз не несут ответственности за качество и точность перевода или за возможное использование данной информации. |
Свойства гидроксида натрия и применение вещества в промышленности и быту
Гидроксид натрия является неорганическим токсичным соединением, которое широко применяется при изготовлении различных продуктов ежедневного пользования, в промышленных и бытовых целях.
Основные свойства гидроксида натрия
Наименование неорганического соединения произошло из физических и химических свойств едкого натра, который оказывает сильно разъедающее действие при соприкосновении с различными поверхностями, включая кожу, бумагу, ткани и другие органические вещества. В технических сферах вещество также именуют каустической содой, применение которой распространяется на область быта, промышленность.
Физические свойства гидроксида натрия
По физическим свойствам едкий натр – твердый реагент белого цвета, который плавится при температуре выше 322 градусов. Характеризуется сильной гигроскопичностью. При взаимодействии с воздухом «расплывается» из-за активного поглощения паров воды. При взаимодействии с водой – растворяется, выделяя тепло из-за образования гидратов. Полученный раствор получается мылким.
Химические свойства гидроксида натрия
При взаимодействии с воздухом образует гидраты различного состава, которые при нагревании начинают разлагаться.
Легко вступает в реакции с некоторыми веществами, включая:
- Кислоты.
- Кислотные и амфотерные оксиды и гидроксиды.
- Галогены.
Под воздействием высокой температуры может вступать в реакцию с металлами, а при смешивании с солями – образовывать гидроксиды. В ходе реакции с монооксидом углерода образуется формиат натрия.
Меры безопасности (класс опасности)
Каустик входит в группу пожаробезопасных и не взрывоопасных веществ, но в то же время едким и коррозионно-активным реактивом. Из-за чего веществу был присвоен 2 класс опасности. При взаимодействии с кожными покровами образуется сильнейший ожог, со слизистой носа, глаз — тяжелые заболевания, включая полную потерю зрения. При использовании реагента надевают средства индивидуальной защиты: очки, перчатки и химостойкие костюмы.
Хранение и перевозка
При транспортировке реагента используют II и III группы упаковок. Если же необходима совместная упаковка, используют марки MP15 (II группа упаковки), MP19 (III группа упаковки). Для перевозки используют транспорты 2 или 3 категории.
Если же необходима совместная упаковка, используют марки MP15 (II группа упаковки), MP19 (III группа упаковки). Для перевозки используют транспорты 2 или 3 категории.
Для хранения используют герметичную тару, которую помещают в сухое складское помещение. Рядом с веществом нельзя хранить кислоты, включая органические, легкие металлы и их сплавы.
Применение гидроксида натрия
На производственные и бытовые цели распространяется использование:
- натра едкого чешуированного;
- натра едкого гранулированного;
- диафрагменного твердого;
- ртутного, химического или диафрагменного раствора.
Применение едкого натра распространяется на множество областей:
- Получение бумаги.
- Каустик участвует в получении бумаги и картона, искусственного волокна и древесно-волоконных плит. Также применение распространяется на делигнификацию целлюлозы.
- Изготовление бытовой химии.

- В данной области применения каустическая сода необходима, чтобы провести омыление жиров, которые используются в мыльной продукции, шампунях и других моющих растворах.
- Отрасль химического производства.
- В химии каустик используется с целью нейтрализации действия кислоты или оксидов. Используется в качестве катализатора при проведении химических опытов, анализе для титрования, получении чистых металлов или травлении алюминия. В переработке нефти необходим для получения масел.
- Получение биодизельного топлива.
- В этой области каустик выступает в роли щелочного катализатора, который добавляется к смеси органических масел и спирта.
- Для прочистки инженерных коммуникаций.
- При устранении трубных застоев едкий натр выступает растворителем. Агент расщепляет скопление мусора и обеспечивает его дальнейшее движение по коммуникации.
- В военной сфере.
-
В данной области едкий натр используется, чтобы дегазировать и нейтрализовать действие отравляющих веществ.
 Реагент применяется при сборке изолирующих приборов для дыхания, где едкий натр выступает в роли очистителя воздуха от примесей углекислого газа.
Реагент применяется при сборке изолирующих приборов для дыхания, где едкий натр выступает в роли очистителя воздуха от примесей углекислого газа. - В текстильном производстве.
- В текстильном деле каустик используется для мерсеризации хлопкового и шерстяного сырья. При непродолжительном воздействии едким веществом, растительное волокно становится более прочным, блестящим и шелковистым.
- В поварском деле.
- Использование каустика в приготовлении блюд позволяет быстро очистить овощи и фрукты от кожуры. Также применяется для получения некоторых видов сладостей, напитков и шоколада.
- В косметологических процедурах.
- При помощи каустика удается избавиться от папиллом, бородавок и огрубевших частиц кожи.
- В проявлении фотоснимков.
При проявке фотографий едкий натр ускоряет процесс, что позволяет в разы сократить время на обработку фотоматериалов.
Чтобы купить гидроксид натрия, свяжитесь с нами по телефону или заполните форму на сайте.
Сбалансированное уравнение реакции между оксидом натрия и водой:
Химия Химические реакции Кислотно-основные реакции Кислотно-основные
Маталина С.
спросил 03.08.15
A. Na2O + h3O → 2NaOH
B. Na2O + h3O → 2NaH + O2
C. Na2O + h3O → 2Na + h3O2
D. Na2O + h3O → 2Na + h3 +O2
Откуда мне знать, какой будет реакция?
Подписаться І 2
Подробнее
Отчет
1 ответ эксперта
Лучший Новейшие Самый старыйАвтор: Лучшие новыеСамые старые
Дена А. ответил 03.08.15
Репетитор
4.9 (136)
Бывший заведующий кафедрой химии с более чем 10-летним опытом преподавания
Смотрите таких репетиторов
Смотрите таких репетиторов
ШАГ 1:
Натрий — это щелочной МЕТАЛЛ с зарядом +1.
ОКСИД представляет собой анион с зарядом -2.
Вы должны запомнить заряды (общие степени окисления), глядя на семейства в периодической таблице. (:
Итак, если это Na+1 с O-2, мы пересекаем заряды, чтобы получить индексы. Таким образом, мы получаем Na2O.
ШАГ 2:
Я уверен, вы знаете, что вода – это вода. Итак, мы закончили со стороной реагента: Na2O + h3O
ШАГ 3:
Итак, вот где начинается самое интересное. Вам нужно запомнить различные типы реакций. Первый тип – ЛЮБОЙ ОКСИД МЕТАЛЛА, ДОБАВЛЕННЫЙ В ВОДУ, ДЕЛАЕТ ПРОЧНУЮ ОСНОВУ. В тот момент, когда вы увидели МЕТАЛЛ натрия и анион ОКСИДА, ваш мозг должен был «динь! динь!» (Я предлагаю сделать карточки с различными типами реакций в вашей книге) и вы должны подумать… ЭТО СОСТАВЛЯЕТ ПРОЧНУЮ ОСНОВУ!
ШАГ 4:
Чтобы записать основание, вы кладете Na+1 с анионом ГИДРОКСИДА (ОН-), который также необходимо запомнить.
Итак, Na+ и OH- отменяют свои заряды, и вы просто получаете NaOH.
ШАГ 5:
Мы еще не закончили. Вы должны БАЛАНСИРОВАТЬ последнее уравнение. У нас есть Na2O + h3O —> NaOH. У нас есть 2 натрия, 2 кислорода и 2 водорода на левой стороне, но только по одному на правой стороне. Таким образом, мы должны умножить все правильные виды на коэффициент 2.
КОНЕЧНЫЙ ОТВЕТ:
Na2O + h3O —> 2NaOH
Надеюсь, это поможет!! Я постоянно помогал своим ученикам онлайн.
Голосовать за 3 голос против
Подробнее
Отчет
Все еще ищете помощь? Получите правильный ответ, быстро.
Задайте вопрос бесплатно
Получите бесплатный ответ на быстрый вопрос.
Ответы на большинство вопросов в течение 4 часов.
ИЛИ
Найдите онлайн-репетитора сейчас
Выберите эксперта и встретьтесь онлайн. Никаких пакетов или подписок, платите только за то время, которое вам нужно.
ICSC 1653 — НАТРИЯ ОКСИД
ICSC 1653 — НАТРИЯ ОКСИД| НАТРИЯ ОКСИД | ICSC: 1653 (октябрь 2006 г.) |
| Монооксид натрия Оксид натрия Монооксид натрия | |
| Номер CAS: 1313-59-3 |
| № ООН: 1825 |
| Номер ЕС: 215-208-9 |
| ОСТРЫЕ ОПАСНОСТИ | ПРЕДУПРЕЖДЕНИЕ | ПОЖАРОТУШЕНИЕ | |
|---|---|---|---|
| ПОЖАР И ВЗРЫВ | Не горюч, но усиливает горение других веществ. | НЕТ воды. Используйте сухой порошок, сухой песок. |
| ИЗБЕГАЙТЕ ВСЕХ КОНТАКТОВ! ПРЕДОТВРАТИТЬ РАССЕЯНИЕ ПЫЛИ! ВО ВСЕХ СЛУЧАЯХ ОБРАЩАЙТЕСЬ К ВРАЧУ! | |||
|---|---|---|---|
| СИМПТОМЫ | ПРЕДУПРЕЖДЕНИЕ | ПЕРВАЯ ПОМОЩЬ | |
| Вдыхание | Боль в горле. Кашель. Обжигающее ощущение. Затрудненное дыхание. Одышка. | Используйте местную вытяжку. Используйте защиту органов дыхания. | Свежий воздух, отдых. Полупрямое положение. Может потребоваться искусственное дыхание. Немедленно обратитесь за медицинской помощью. |
| Кожа | Покраснение. Боль. Серьезные ожоги кожи. | Защитные перчатки. Защитная одежда. | Снять загрязненную одежду. Промойте кожу большим количеством воды или примите душ. Немедленно обратитесь за медицинской помощью. Немедленно обратитесь за медицинской помощью. |
| Глаза | Покраснение. Боль. Бернс. | Носите защитную маску или защиту для глаз в сочетании с защитой органов дыхания при попадании порошка. | Промыть большим количеством воды в течение нескольких минут (снять контактные линзы, если это возможно). Немедленно обратитесь за медицинской помощью. |
| Проглатывание | Боль в горле. Ощущение жжения в горле и груди. Шок или коллапс. | Не ешьте, не пейте и не курите во время работы. | Прополоскать рот. Не вызывает рвоту. Немедленно обратитесь за медицинской помощью. |
| ЛИКВИДАЦИЯ УТЕЧЕК | КЛАССИФИКАЦИЯ И МАРКИРОВКА |
|---|---|
Средства индивидуальной защиты: костюм химической защиты, включая автономный дыхательный аппарат. Смести просыпанное вещество в закрытые сухие пластиковые контейнеры. Смойте остатки большим количеством воды. Смести просыпанное вещество в закрытые сухие пластиковые контейнеры. Смойте остатки большим количеством воды. | В соответствии с критериями СГС ООН ОПАСНОСТЬ Вызывает серьезные ожоги кожи и повреждение глаз Транспортировка |
| ХРАНЕНИЕ | |
| Отдельно от сильных кислот, пищевых продуктов и кормов. Сухой. | |
| УПАКОВКА | |
| Не перевозить вместе с пищевыми продуктами и кормами. |
| НАТРИЯ ОКСИД | КМГС: 1653 |
| ФИЗИЧЕСКАЯ И ХИМИЧЕСКАЯ ИНФОРМАЦИЯ | |
|---|---|
Физическое состояние; Внешний вид Физические опасности Химическая опасность | Формула: Na 2 O |
| ВОЗДЕЙСТВИЕ И ВЛИЯНИЕ НА ЗДОРОВЬЕ | |
|---|---|
Пути воздействия Последствия кратковременного воздействия | Риск вдыхания Последствия длительного или многократного воздействия |
| ПРЕДЕЛЫ ВОЗДЕЙСТВИЯ НА РАБОЧЕМ МЕСТЕ |
|---|
| ОКРУЖАЮЩАЯ СРЕДА |
|---|



 Реагент применяется при сборке изолирующих приборов для дыхания, где едкий натр выступает в роли очистителя воздуха от примесей углекислого газа.
Реагент применяется при сборке изолирующих приборов для дыхания, где едкий натр выступает в роли очистителя воздуха от примесей углекислого газа.
 См. Примечания. Показано медицинское наблюдение.
См. Примечания. Показано медицинское наблюдение.
Leave A Comment