Массовая доля нитрата натрия | Задача 2
Задача 2.
При нагревании образца нитрата меди, часть вещества разложилась. При этом выделилось 5,6 л смеси газов. Масса твёрдого остатка составила 26,8г. К этому остатку последовательно добавили 50 мл воды и 10% раствор гидроксида натрия, массой, которая потребовалась для полного осаждения ионов меди.Определите массовую долю нитрата натрия в конечном растворе.
Решение:
При нагревании образца нитрата меди выделяется оксид меди, оксид азота IV и кислород
2Cu(NO3)2 = 2CuO + 4NO2↑ + O2↑
Рассчитаем количество газов, выделившихся при реакции:
5,6л/22/4л/моль = 0, 25 моль.
Из уравнения реакции следует, что на 5 моль смеси выделившихся газов выпадает в осадок 2 моль оксида меди. Исходя из этого, рассчитаем количество и массу выпавшего оксида меди :
5 моль ———— 2 моль
0,25 моль ———х моль х = 0,25
Теперь рассчитаем массу оставшегося нитрата меди в осадке:
mCu(NO3)2 ] = m(образц.) – m(CuO) = 26,8г -8г = 18,8г.
Оставшийся осадок нитрата меди прореагировал с гидроксидом натрия по уравнению:
Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO3
Находим массу гидроксида натрия, потраченного на реакцию:
18,8г хг
Cu(NO3)2 + 2NaOH = Cu(OH)2 + 2NaNO
188г 2 . 40
18,8 . 80
Получим: х = —————— = 8г.
188
Зная массу растворенного вещества и массовую долю раствора, рассчитаем массу 10%-го раствора:
m(NaOH) . 100 8г . 100
m1(р-ра) = ——————- —— = ——————— = 80г.
w1 10
Масса конечного раствора гидроксида натрия равна:
m2(р-ра) = m1(р-ра) + m(h3O) = 80г + 50г = 130г.
Определим массовую долю нитрата натрия в конечном растворе:
w2% = m(NaOH) . 100/ m2(р-ра) = 8г . 100%/130г = 6,15%.
Ответ: 6,15%.
w₁=0,10
m₂=112 г
w₂=0,10
n(H₂SO₄)=m₁w₁/M(H₂SO₄)
n(H₂SO₄)=292*0,10/98=0,30 моль
n(KOH)=m₂w₂/M(KOH)
n(KOH)=112*0,10/56=0,20 моль
мольное соотношение щелочи и кислоты
KOH : H₂SO₄ = 0,20:0,30=1:1,5
KOH + H₂SO₄ = KHSO₄ + H₂O KOH:H₂SO₄ = 1:1
2KOH + H₂SO₄ = K₂SO₄ + 2H₂O KOH:H₂SO₄ = 2:1
серная кислота в избытке, недостаток гидроксида калия (по схеме 1)
m(KHSO₄)=n(KHSO₄)M(KHSO₄)=n(KOH)M(KHSO₄)
m(KHSO₄)=0,20*136=27,2 г
27,2 г гидросульфата калия
SO3- ковалентная полярная, молекулярная крист. решетка,NCl3-ковалентная полярная, молекулярная крист. решетка,ClF3-ковалентная полярная, молекулярная крист. решетка,Br2-ковалентная неполярная, молекулярная крист. решетка,h3O-ковалентная полярная, молекулярная крист. решетка,NaCl-ионная связь, ионная решетка
Если не ошибаюсь, то графит — это углерод.
2Na + 2h3O = 2NaOH + h3
n=0.05 моль V=0.56л
m=0.05*23=1.15 n=0.025моль
Ответ:1.15 г
Задачи на атомистику | CHEMEGE.RU
Задачи на атомистику — это задачи на соотношения частиц (атомов, молекул, ионов и т.д.) в гомогенных и гетерогенных системах (растворах, твердых и газообразных смесях). Это могут быть массовые соотношения (например, массовая доля элемента в смеси), мольные соотношения (например, соотношение числа атомов водорода и кислорода или мольная доля), объемные соотношения (объемная доля и др.).
Похоже, эти задачи станут дебютантами на ЕГЭ по химии-2020.
Ниже я выкладываю задачи на атомистику из реального ЕГЭ по химии 16 июля 2020 года.
Для решения задач на атомистику используются довольно простые идеи. Во-первых, понятие массовой доли. Во-вторых, умение выражать число атомов через число молекул или других структурных единиц.
Например, в молекуле триоксида серы SO3 на 1 молекулу приходится один атом серы и три атома кислорода:
1 молекула SO3 — 1 атом серы, 3 атома кислорода
Несложно пропорцией определить, что на две молекулы триоксида серы будет приходиться два атома серы и шесть атомов кислорода:
2 молекулы SO3 — 2 атома S, 6 атомов О
На 20 молекул триоксида:
20 молекул SO3 — 20 атомов S, 60 атомов О
А вот сколько атомов приходится на х молекуле триоксида? Это также легко определить через пропорцию:
х молекул SO3 — х атомов S, 3х атомов О
Иначе говоря, количество атомов кислорода в молекуле SO3 в три раза больше, чем количество молекул. А количество атомов серы равно количеству молекул триоксида серы. Это простая, но не всегда очевидная идея. То есть индексы в формуле вещества показывают не только, как соотносится количество атомов между собой, но и какое число атомов приходится на 1 молекулу или другую структурную единицу вещества.
Если так соотносится число атомов и молекул, то также будет соотноситься и количество вещества атомов и молекул, выраженное в молях. Потому что 1 моль — это не что иное, как порция, состоящая из одинакового числа данных частиц.
То есть на х моль триоксида серы приходится:
х моль SO3 — х моль атомов S, 3х моль атомов О
Представьте себе, что атомы — это элементы изделия, а молекула состоит из некоторого числа таких деталей. Таким образом, число деталей разного типа всегда больше или равно числа изделий. Получается,
И наоборот, число молекуле триоксида серы в 3 раза меньше, чем число атомов кислорода в составе SO3. И число молекул равно количеству атомов серы.
Например, на х моль атомов серы приходится х моль молекул SO3.
Еще одно понятие, которое пригодится при решении задач на атомистику — молярное соотношение веществ.
Молярное соотношение — это отношение количества одного вещества к количеству другого вещества.
Например, молярное соотношение хлорида натрия и воды в растворе составляет 1 к 20, или 0,05:
n(NaCl)/ n(H2O) = 1/20 = 0,5
Молярное соотношение можно задавать отдельным числом, а можно соотношением:
n(NaCl) : n(H2O) = 1:20
А вот выражать молярное соотношение через проценты нельзя. Это безразмерная величина.
Научиться решать задачи на атомистику не очень сложно. В ЕГЭ по химии атомистика станет, скорее всего, лишь частью более сложной комплексной задачи 34. Но я бы рекомендовал не пытаться сразу решать задачи на атомистику уровня ЕГЭ по химии. Занимаясь в спортзале, вы же не пытаетесь на первой тренировке поднять сразу тяжелую штангу. Точнее, попытаться вы можете, но последствия будут плачевными.
Для начала сделайте разминку возьмите простые задачи, чтобы освоить основные приемы и понять логику решения таких заданий. А после легких задач можно постепенно перейти к более сложным. Именно в таком порядке и расположены задачи в данной подборке «Атомистика», которые позволяют понять, как именно удобно работать с такими заданиями.
Публикую подборку задач, в которых используются идеи атомистики. Все задачи взяты из сборника С.А. Пузакова, В.А. Попкова «Пособие по химии. Вопросы. Упражнения. Задачи». В скобках я привожу нумерацию этих задач в задачнике.
1. (66) В смеси оксида меди (I) и оксида меди (II) на 4 атома меди приходится 3 атома кислорода. Вычислите массовые доли веществ в такой смеси.
Пусть n (количество вещества) (Cu2O) = х моль, n(CuO) = y моль, тогда:
количество вещества атомов меди в первом оксиде n1(Cu) = 2х моль, во втором оксиде: n2(Cu) = у моль
количество вещества атомов кислорода в первом оксиде n1(О) = х моль, во втором оксиде: n2(О) = у моль
общее количество вещества атомов меди: n(Cu) = (2x + y) моль, атомов кислорода: n(O) = (x + y) моль.
По условию задачи их отношение равно как 4 : 3, т. е. (2x + y) / (x + y) = 4 / 3.
Преобразуем приведённое выше равенство, получаем y = 2x.
Выразим через х массы соединений:
m(Cu2O) = n(Cu2O) * M(Cu2O) = (144x) г;
m(CuO) = n(CuO) * M(CuO) = 80 * у = 80 * 2x = (160x) г
Масса смеси двух оксидов будет равна:
m(смеси) = (144x + 160x) г = (304x) г
Теперь рассчитываем массовую долю оксидов в смеси:
ω(Cu2O) = m(Cu2O) / m(смеси) = 144x / 304x = 0.4737 (47.37%)
ω(CuO) = m(CuO) / m(смеси) = 160x / 304x = 0.5263 (52.63%)
Ответ: ω(CuO) = 52,6%, ω(Cu2O) = 47,4%
2. (67) В смеси двух хлоридов железа на 5 атомов железа приходится 13 атомов хлора. Вычислите массовые доли веществ в такой смеси.
Железо образует два устойчивых хлорида: FeCl2 и FeCl3.
Пусть n(FeCl2) = х моль, n(FeCl3) = y моль, тогда:
количество вещества атомов железа в первом хлориде n1(Fe) = х моль, во втором хлориде: n2(Fe) = у моль,
количество вещества атомов хлора в первом хлориде n1(Cl) = 2х моль, во втором хлориде: n2(Сl) = 3у моль,
общее количество вещества атомов железа: n(Fe) = (x + y) моль, атомов хлора: n(Cl) = (2x + 3y) моль.
По условию задачи их отношение равно как 5 : 13, т. е. (x + y) / (2x + 3y) = 5 / 13.
Преобразуя приведённое выше равенство, получаем y = 1,5x.
Выразим через х массы соединений:
m(FeCl2) = n(FeCl2) * M(FeCl2) = (127x) г;
m(FeCl3) = n(FeCl3) * M(FeCl3) = 162,5 * у = 162,5 * 1,5x = (243,75x) г
Масса смеси двух хлоридов будет равна:
m(смеси) = (127x + 243,75x) г = (370,75x) г
Теперь рассчитываем массовую долю хлоридов в смеси:
ω(FeCl2) = m(FeCl2) / m(смеси) = 127x / 370,75x = 0,343 (34,3%)
ω(FeCl3) = m(FeCl3) / m(смеси) = 243,75x / 370,75x = 0,657 (65,7%)
Ответ: ω(FeCl2) = 34,3%, ω(FeCl3) = 65,7%
3. (70) В каком молярном соотношении были смешаны карбид кальция и карбонат кальция, если массовая доля углерода в полученной смеси равна 25%?
Формулы карбида и карбоната кальция: CaC2 и CaCO3.
Пусть n(CaC2) = х моль, n(CaCO3) = y моль, тогда:
количество вещества атомов углерода в карбиде кальция n1(С) = 2х моль, в карбонате: n2(С) = у моль,
общее количество вещества атомов углерода: n(С) = (2x + y) моль.
масса атомов углерода: m(С) = 12(2x + y) г.
Выразим через х массы соединений:
m(CaC2) = n(CaC2) * M(CaC2) = (64x) г;
m(CaCO3) = n(CaCO3) * M(CaCO3) = 100у г
Масса смеси двух веществ будет равна:
m(смеси) = (64x + 100у) г
Теперь записываем выражение для массовой доли атомов углерода в смеси:
ω(C) = m(C) / m(смеси)
0,25 = 12(2x + y) / (64x + 100у)
Преобразуем выражение, выражаем х через у:
х = 1,625у
Это и есть искомое молярное соотношение карбида кальция и карбоната кальция:
n(CaC2)/ n(CaCO3) = х/у = 1,625
Ответ: n(CaC2)/ n(CaCO3) = 1,625
4. (71) В каком молярном соотношении были смешаны гидросульфит натрия и гидросульфид натрия, если массовая доля серы в полученной смеси равна 45%?
Ответ: n(NaHS)/ n(NaHSO3) = 2,18
5. (72) Какую массу сульфата калия следует добавить к 5,5г сульфида калия, чтобы в полученной смеси массовая доля серы стала равной 20%?
Ответ: 31,3 г
6. (73) В смеси нитрата аммония и нитрата свинца (II) массовая доля азота равна 25%. Вычислите массовую долю свинца в этой смеси.
Ответ: 23,6%
7. (74) В смеси нитрата аммония и нитрата бария массовая доля азота равна 30%. Вычислите массовую долю нитрат-ионов в смеси.
Ответ: 71,3%
8. (75) В смеси двух оксидов углерода на 5 атомов углерода приходится 7 атомов кислорода. Вычислите объемную долю более тяжелого оксида в этой смеси
Ответ: φ(СO2) = 40%
9. (619) Через 13,1 г смеси бромида калия и йодида калия, в которой массовая доля брома равна 24,5%, пропустили смесь хлора и брома, в результате чего получилась смесь двух солей, в которой массовая доля брома равна 57%. Вычислите массу смеси галогенов, вступившую в реакцию.
Масса брома в исходной смеси равна:
m(Br) = mсмеси·ω(Br) = 13,1·0,245 = 3,21 г
Количество вещества атомов брома:
n(Br) = m/M = 3,21 г/80 г/моль = 0,04 моль
Количество вещества бромида калия:
n(KBr) = n(Br) = 0,04 моль
Масса этого образца бромида калия:
m(KBr) = n·M = 0.04 моль·119 г/моль = 4,77 г
Масса йодида калия:
m(KI) = m(смеси) — m(KBr) =13,1 — 4,77 = 8,33 г
Количество вещества йодида калия:
n(KI) = m/M = 8,33 г/166 г/моль = 0,05 моль
По условию задачи, смесь йодида калия и бромида калия вступила в реакцию не полностью, но в конечной смеси осталось только две соли. При этом йодид калия, скорее всего, вступил в реакцию полностью, так как иначе конечная смесь будет содержать более двух солей.
Предположим, что сначала прореагируют наиболее активные окислитель и восстановитель — йодид калия и хлор:
2KI + Cl2 = 2KCl + I2
Если весь йодид калия вступил в эту реакцию, то в конечной смеси присутствуют только исходный бромид калия и образовавшийся хлорид калия. Количество хлорида калия:
n(KCl) = n(KI) = 0,05 моль
m(KI) = n·M = 0,05 моль·166 г/моль = 8,3 г
Массовая доля брома в такой смеси:
ω(Br) = m(Br) / m(смеси) = 3,21 г / (8,3 г + 4,77) = 0,2469 или 24,69%, что не соответствует условию задачи.
Следовательно, йодид калия реагирует не только с хлором, но и с бромом:
2KI + Cl2 = 2KCl + I2
2KI + Br2 = 2KBr + I2
Пусть с хлором прореагировало х моль йодида калия, тогда с бромом 0,05-х моль
Тогда образуется х моль хлорида калия и 0,05-х моль бромида калия.
Масса образовавшегося хлорида калия:
m(KCl) = n·M = x моль·74,5 г/моль = 74,5x г
Бромида калия:
m2(KBr) = n·M = (0,05-х) моль·119 г/моль = (5,95 — 119x) г
Масса конечной смеси солей:
mсмеси = mисх(KBr) + m2(KBr) + m(KCl) = 4,77 г + (5,95 — 119x) г + 74.5х = (10,72 — 44,5х) г
Количество атомов брома в конечной смеси:
n(Br) = 0,04 моль + (0,05 — х) моль = (0,09 — х) моль
Масса атомов брома:
m(Br) = n·M = (0,09 — х) моль·80 г/моль = (7,2 — 80х) г
Массовая доля брома в конечной смеси:
ω(Br) = (7,2 — 80х) / (10,72 — 44,5х) = 0,57
Решаем полученное уравнение, находим х:
х = 0,02 моль
Количество вещества и масса хлора, который вступил в первую реакцию:
n(Cl2) = 0,5х = 0,5·0,02 = 0,01 моль
m(Cl2) = n·M = 0,01·71 г/моль = 0,71 г
Количество вещества брома, который вступил во вторую реакцию:
n(Br2) = n·M = 0,5(0,05 — 0,02) моль = 0,015 моль
Масса брома:
m(Br2) = n·M =0,015 моль·160 г/моль = 2,4 г
Масса смеси галогенов, которые прореагировали с йодидом калия:
m(смеси) = m(Cl2) + m(Br2) = 0,71 г + 2,4 г = 3,11 г
Ответ: 3,11 г
10. (620) Через смесь натрия и бромида калия, в которой массовая доля брома равна 60%, пропустили хлор, в результате чего масса брома в смеси солей оказалась в 2 раза меньше, чем в исходной смеси. Вычислите массовую долю брома в полученной смеси солей.
Примем массу исходной смеси за 100 г, тогда масса брома в исходной смеси равна:
m(Br) = mсмеси·ω(Br) = 100·0,6 = 60 г
Количество вещества атомов брома:
n(Br) = m/M = 60 г/80 г/моль = 0,75 моль
Количество вещества бромида калия:
n(KBr) = n(Br) = 0,75 моль
Масса этого образца бромида калия:
m(KBr) = n·M = 0,75 моль·119 г/моль = 89,25 г
Масса натрия:
m(Na) = m(смеси) — m(KBr) =100 — 89,25 = 10,75 г
Количество вещества натрия:
n(Na) = m/M = 10,75 г/23 г/моль = 0,467 моль
Поскольку масса брома в смеси уменьшилась в два раза, в реакцию вступила половина исходного бромида калия, то есть 0,375 моль KBr. При этом натрий прореагировал полностью, так как, по условию, образовалась смесь солей:
2Na + Cl2 = 2NaCl
2KBr + Cl2 = 2KCl + Br2
В первой реакции образовался хлорид натрия:
n(NaCl) = n(Na) = 0,467 моль
m(NaCl) = n·M = 0,467 моль ·58,5 г/моль = 27,32 г
Во второй образовался хлорид калия:
n(KCl) = 0,5·n(KBr) = 0,375 моль
m(KCl) = n·M = 0,375 моль ·74,5 г/моль = 27,94 г
И остался бромид калия:
mост(KBr) = n·M = 0,375 моль ·74,5 г/моль = 44,625 г
В конечной смеси масса брома равна:
mост(Br) = n·M = 0,375 моль ·80 г/моль = 30 г
Масса конечной смеси:
mсм = mост(KBr) + m(KCl) + m(NaCl) = 44,625 г + 27,94 г + 27,32 г = 99,89 г
Массовая доля брома в конечной смеси солей:
ω(Br) = mост(Br)=/mсм = 30 г/99,89 г = 0,30 или 30%
Ответ: ω(Br) = 30%
11. (621) К смеси калия и иодида натрия, в которой массовая доля калия равна 40%, добавили бром, в результате чего масса йода в полученной смеси солей уменьшилась в 5 раз по сравнению с исходной. Вычислите массовую долю йода в полученной смеси солей.
Ответ: 6,08%
12. (827) Аммиак, образовавшийся при гидролизе смеси нитрида кальция и нитрида лития, в которой массовая доля азота равнялась 30%, пропустили через 80 мл бромоводородной кислоты. В результате реакции молярная концентрация кислоты уменьшилась с 2,8 до 1,2 моль/л (изменением объема раствора за счет поглощения газа пренебречь). Вычислите массу исходного образца смеси нитридов.
Ответ: 5,97 г.
13. (828) К 1,59%-му раствору карбоната натрия добавили по каплям 40 г 3,78%-го раствора азотной кислоты; в результате в образовавшемся растворе число атомов азота оказалось в 2 раза больше числа атомов углерода. Вычислите массовые доли веществ в получившемся растворе.
Ответ: 1,28% NaNO3, 0,631 NaHCO3.
14. (855)Через 15 г 9,45%-го раствора азотной кислоты пропустили аммиак; в результате в образовавшемся растворе массовая доля азота оказалась равной 3,5%. Вычислите массовые доли веществ в образовавшемся растворе.
Ответ: 2,82% HNO3, 8,21% NH4NO3.
15. (951) К смеси фосфата натрия, дигидрофосфата натрия и гидрофосфата натрия общей массой 15 г (молярное соотношение солей в порядке перечисления 3:2:1) добавили 100 г 4%-го раствора гидроксида натрия. Установите количественный состав раствора (в массовых долях).
Ответ: w(Na3PO4) = 14,7%, w(NaOH) = 34,3%.
16. (952) К 2 г смеси гидрофосфата калия и дигидрофосфата калия, в которой массовая доля фосфора равна 20%, добавили 20 г 2%-го раствора фосфорной кислоты. Вычислите массовые доли всех веществ в получившемся растворе.
Ответ: w(KH2PO4) = 9,05%, w(K2HPO4) = 1,87%.
17. (992) В смеси карбида алюминия и карбида кальция число атомов алюминия равно числу атомов кальция. При гидролизе этой смеси выделяется 1,12 л (н.у.) смеси газов. Вычислите массу исходной смеси карбидов.
Ответ: 2,86 г
18. (1007) Смесь карбоната стронция и гидрокарбоната аммония общей массой 12 г, в которой масса атомов углерода в 12 раз больше массы атомов водорода, добавили к избытку 10%-го раствора серной кислоты. Вычислите массу выпавшего осадка и объем выделившегося газа (н.у.)
Ответ: 2 л, 13,2 г
19. (1009) Какой объем газа (н.у.) выделится при добавлении к 20 г 20%-го раствора серной кислоты 20 г смеси карбоната калия и гидрокарбоната натрия с одинаковым числом атомов калия и водорода?
Ответ: 0,914 л.
20. (1021) В смеси сульфита кальция и гидрокарбоната кальция число атомов кальция в 6 раз больше числа атомов серы. Вычислите плотность по воздуху газовой смеси, образующейся при обработке этой смеси избытком разбавленного раствора серной кислоты.
Ответ: 1,58
21. (1059) Массовая доля калия в растворе, содержащем силикат калия и сульфат калия, равна 0,909%, а масса серы равна массе кремния. К этому раствору добавили в 4 раза меньшую массу соляной кислоты с массовой долей хлороводорода 1,46%. Вычислите, во сколько раз масса серы оказалась больше массы кремния в образовавшемся растворе.
22. (1162) Смесь натрия с другим щелочным металлом поместили в воду. По окончании реакции воду полностью испарили. Массовая доля кислорода в полученной смеси веществ оказалась равной 50%. Вычислите массовые доли веществ в полученной смеси.
Ответ: w(NaOH) =62,5%, w(LiOH) = 37,5%
23. (1215) В смеси оксида ванадия (V) и оксида ванадия (III) массовая доля кислорода равна 40%. Какое количество вещества алюминия понадобится для полного восстановления ванадия из 100 г этой смеси?
Ответ: 1,67 моль
Задача на атомистику, которую составители ЕГЭ по химии рекомендовали к прорешиванию:
24. Некоторое количество смеси гидрата дигидрофосфата калия и дигидрата гидрофосфата калия с равными массовыми долями веществ растворили в воде, которую взяли в 10 раз больше по массе, чем смеси. Сколько атомов кислорода приходится на один атом фосфора в полученном растворе? (104)
Гидрат дигидрофосфата калия: KH2PO4·H2O
Дигидрат гидрофосфата калия: K2HPO4·2H2O
Пусть количество вещества гидрата дигидрофосфата калия равно х моль, а дигидрата гидрофосфата — у моль.
Масса кристаллогидратов:
m(KH2PO4·H2O) = n·M = 154x г
m(K2HPO4·2H2O) = n·M = 210у г
Поскольку массовые доли кристаллогидратов в исходной смеси равны, массы кристаллогидратов также равны:
m(KH2PO4·H2O) = m(K2HPO4·2H2O)
154х = 210у
Отсюда: х = 1,364у
Масса исходной смеси:
mсм = m(KH2PO4·H2O) + m(K2HPO4·2H2O) = 154x + 210у = 154·1,364у + 210у = 420,056·y г
Количество чистых солей в составе кристаллогидратов:
n(KH2PO4·H2O) = n(KH2PO4) = x моль = 1,36·у моль
n(K2HPO4·2H2O) = n(K2HPO4) = у моль
Масса добавленной воды отличается в 10 раз от массы смеси солей:
m(H2O) = 10mсм = 10·420,056·у = 4200,56у г
Количество вещества добавленной воды:
n(H2O) = 4200,56·у/18 = 233,36·у моль
Определим количество атомов кислорода и фосфора:
в гидрате дигидрофосфата калия KH2PO4·H2O: n1(O) = 5x = 6,82·у моль n(Р) = 1,364·у моль
в дигидрате гидрофосфата калия K2HPO4·2H2O:
n2(O) = 6·у моль = 6·у моль
n(Р) = у моль = у моль
в добавленной воде: n3(O) = 233,36у моль
Общее количество атомов кислорода: n(O) = 233,36у + 6,82у + 6у = 246,18 моль
Атомов фосфора: n(Р) = у + 1,364у = 2,363у моль
Отношение числа атомов кислорода к числу атомов фосфора равно:
246,18х/2,364х ≈ 104
Ответ: n(O)/n(Р) = 104
24. Некоторое количество смеси гидрата дигидрофосфата калия и дигидрата гидрофосфата калия с равными массовыми долями веществ растворили в воде, которую взяли в 10 раз больше по массе, чем смеси. Сколько атомов кислорода приходится на один атом фосфора в полученном растворе? (104)
Гидрат дигидрофосфата калия: KH2PO4·H2O
Дигидрат гидрофосфата калия: K2HPO4·2H2O
Пусть количество вещества гидрата дигидрофосфата калия равно х моль, а дигидрата гидрофосфата — у моль.
Масса кристаллогидратов:
m(KH2PO4·H2O) = n·M = 154x г
m(K2HPO4·2H2O) = n·M = 210у г
Поскольку массовые доли кристаллогидратов в исходной смеси равны, массы кристаллогидратов также равны:
m(KH2PO4·H2O) = m(K2HPO4·2H2O)
154х = 210у
Отсюда: х = 1,364у
Масса исходной смеси:
mсм = m(KH2PO4·H2O) + m(K2HPO4·2H2O) = 154x + 210у = 154·1,364у + 210у = 420,056·y г
Количество чистых солей в составе кристаллогидратов:
n(KH2PO4·H2O) = n(KH2PO4) = x моль = 1,36·у моль
n(K2HPO4·2H2O) = n(K2HPO4) = у моль
Масса добавленной воды отличается в 10 раз от массы смеси солей:
m(H2O) = 10mсм = 10·420,056·у = 4200,56у г
Количество вещества добавленной воды:
n(H2O) = 4200,56·у/18 = 233,36·у моль
Определим количество атомов кислорода и фосфора:
в гидрате дигидрофосфата калия KH2PO4·H2O: n1(O) = 5x = 6,82·у моль n(Р) = 1,364·у моль
в дигидрате гидрофосфата калия K2HPO4·2H2O:
n2(O) = 6·у моль = 6·у моль
n(Р) = у моль = у моль
в добавленной воде: n3(O) = 233,36у моль
Общее количество атомов кислорода: n(O) = 233,36у + 6,82у + 6у = 246,18 моль
Атомов фосфора: n(Р) = у + 1,364у = 2,363у моль
Отношение числа атомов кислорода к числу атомов фосфора равно:
246,18х/2,364х ≈ 104
Ответ: n(O)/n(Р) = 104
1. В смеси оксида магния и фосфида магния массовая доля атомов магния равна 54,4%. Они полностью прореагировала с соляной кислотой массой 365 г 34-% раствора. К полученному раствору добавили раствор фторида калия массой 232 грамма 30-% раствора. Найти массовую долю хлорида калия в конечном растворе.
2. Взяли смесь оксида кальция и карбоната кальция. Массовая доля кальция в смеси 50%. Смесь растворили в 300 г раствора избытка соляной кислоты. Выделившийся газ полностью прореагировал с раствором гидроксида натрия массой 200г и массовой долей 8%. Вычислите массовую долю образовавшейся соли.
3. Взяли смесь Cu и CuO . Массовая доля меди в смеси 96%. Полученную смесь растворили в концентрированной серной кислоте массой 496 г, взятой в избытке. Полученный газ растворили в необходимом количестве раствора гидроксида натрия массой 200 г и массовой долей 10%. Найдите массовую долю соли в растворе после растворения.
4. Смесь из оксида и сульфида алюминия, где массовая доля алюминия 50%, залили 700 г, раствора соляной кислоты, взятой в избытке. Выделившийся газ полностью поглотили 240 г 20% раствора сульфата меди. Вычислите концентрацию соли после того, как залили соляную кислоту.
5. Смесь оксида кальция и карбоната кальция с массовой долей кальция 62,5% растворили в 300 г раствора соляной кислоты. Масса раствора стала 361,6 г. Выделившийся газ пропустили через 80 г 10%-ного раствора гидроксида натрия. Вычислите массовую долю соли в конечном растворе.
Пусть n(CaO) = х моль, n(CaCO3) = y моль, тогда:
количество вещества атомов кальция в оксида n1(Ca) = х моль, в карбонате: n2(Са) = у моль,
общее количество вещества атомов кальция: n(Са) = (x + y) моль.
Масса атомов кальция: m(Ca) = n(Са)·M(Ca) = 40(x + y) г.
Масса оксида кальция: m(CaО) = n(СаО)·M(CaО) = 56x г.
Масса карбоната кальция: m(CaCO3) = n(CaCO3)·M(CaCO3) = 100у г.
Масса смеси: mсм = m(CaО) + m(CaCO3) = (56х + 100у) г
Получаем выражение:
40(x + y)/(56х + 100у) = 0,625
Преобразуя приведённое выше равенство, получаем х = 4,5у.
Далее протекают реакции:
CaO + 2HCl = CaCl2 + H2O
CaCO3 + 2HCl = CaCl2 + CO2 + H2O
Количество образовавшегося углекислого газа n(CO2) = y моль, масса m(CO2) = 44y г.
Запишем уравнение материального баланса для конечного раствора:
mр-ра = m(CaO) + m(CaCO3) + mр-ра(HCl) — m(CO2)
361,6 = 56х + 100у + 300 — 44у
или
61,6 = 56х + 56у
Получаем систему:
х + у = 1,1
х = 4,5у
5,5у = 1,1
у = 0,2 моль, х = 0,9 моль.
Количество углекислого газа: n(CO2) = 0,2 моль, масса m(CO2) = 44·0,2 = 8,8 г.
При взаимодействии углекислого газа с гидроксидом натрия возможно образование средней или кислой соли:
2NaOH + CO2 = Na2CO3 + H2O (1)
NaOH + CO2 = NaHCO3 (2)
Какие продукты образуются, определяется соотношением количества вещества реагентов.
Масса щелочи: m(NaOH) = mр-ра(NaOH) · ω(NaOH) = 80 · 0,1 = 8 г
Количество вещества: n(NaOH) = m(NaOH) / M(NaOH) = 8/40 = 0,2 моль
Соотношение количества вещества реагентов n(NaOH):n(CO2) = 0,2:0,2 = 1:1
Следовательно, протекает только вторая реакция с образованием кислой соли — гидрокарбоната натрия.
n(NaHCO3) = n(CO2) = 0,2 моль
m(NaHCO3) = n(NaHCO3)·M(NaHCO3) = 0,2·84 = 16,8 г
Масса конечного раствора гидрокарбоната:
mр-ра = m(CO2) + mр-ра(NaOH) = 8,8 + 80 = 88,8 г
Массовая доля гидрокарбоната натрия в конечном растворе:
ω(NaHCO3) = m(NaHCO3)/mр-ра = 16,8/88,8 = 0,1892 или 18,92%
Ответ: ω(NaHCO3) = 18,92%
6. Смесь оксида и пероксида натрия, в которой соотношение атомов натрия к атомам кислорода равно 3:2, нагрели с избытком углекислого газа. Полученное вещество растворили в воде. В результате образовалось 600 г раствора. К полученному раствору добавили 229,6 г раствора хлорида железа(III).Найдите массовую долю оксида натрия в исходной смеси, если масса конечного раствора 795 г и массовая доля карбоната натрия в этом растворе 4%.
7. Смесь карбида алюминия и карбида кальция, в которой массовая доля углерода равна 30%, полностью растворили в 547.5 г соляной кислоте. При этом кислота прореагировала без остатка. К образовавшемуся раствору добавили 1260г 8% раствора гидрокарбоната натрия. Найдите массовую долю кислоты в растворе, в котором растворили исходную смесь.
8. В смесь железной окалины и оксида железа(III) добавили 500 г раствора конц. азотной кислоты, причём соотношение атомов железа к атомам кислорода в смеси равно 7:10. Чтобы полностью поглотить выделившийся газ использовали 20 г раствора NaOH с массовой долей 20%.. Найдите массу соли, образовавшейся при добавлении кислоты в смесь.
9. Дана смесь оксида и пероксида бария, в которой число атомов бария относится к числу атомов кислорода как 5:9. Добавили 490 г 20% холодной серной кислоты при этом смесь прореагировала полностью и раствор стал нейтральным. Определить массовую долю воды в полученном растворе.
10. Смесь из оксида лития и нитрида лития с массовой долей атомов лития 56%, смешали с 265 г раствора соляной кислоты с массовой долей 20%. (все вещества полностью прореагировали). После к образовавшемуся раствору добавили 410г 20%- ного фосфата натрия. Найдите массовую долю образовавшегося хлорида натрия.
11. Дан холодный раствор серной кислоты. К нему добавили пероксид бария, при этом вещества прореагировали полностью. В полученном растворе соотношение атомов водорода к кислороду составило 9 к 5. Затем к этому раствору добавили каталитическое количество оксида марганца (IV), в результате масса раствора уменьшилась на 6,4 г. Вычислите массовую долю серной кислоты в исходном растворе.
Холодный раствор серной кислоты реагирует с пероксидом бария без ОВР:
H2SO4 + BaO2 = BaSO4 + H2O2
При этом в растворе присутствует пероксид водорода, а сульфат бария выпадает в осадок.
Пусть n(H2O2) = х моль, n(H2O) = y моль, тогда:
количество вещества атомов водорода в пероксиде n1(H) = 2х моль, в воде: n2(Н) = 2у моль,
количество вещества атомов кислорода в пероксиде n1(О) = 2х моль, в воде: n2(О) = у моль,
общее количество вещества атомов водорода: n(Н) = (2x + 2y) моль,
общее количество вещества атомов кислорода: n(О) = (2x + y) моль.
Получаем соотношение:
(2x + 2y)/(2x + y) = 9/5
Упрощаем его:
у = 8х
При добавлении каталитического количества оксида марганца (IV) пероксид водорода разлагается:
2H2O2 = 2H2O + O2
Пусть весь пероксид водорода разложился, тогда изменение массы раствора равно массе выделившегося газа, то есть массе кислорода:
m(O2) = 6,4 г
n(O2) = m(O2)/M(O2) = 6,4 / 32 = 0,2 моль
Отсюда
n(H2O2) = 2·n(O2) = 2·0,2 = 0,4 моль
х = 0,4 моль
у = 3,2 моль
Отсюда количество вещества серной кислоты с исходном растворе:
n(H2SO4) = n(H2O2) = 0,4 моль
m(H2SO4) = n(H2SO4)·M(H2SO4) = 0,4·98 = 39,2 г
Количество и масса воды не изменялись:
m(H2O) = n(H2O)·M(H2O) = 3,2·18 = 57,6 г
Массовая доля серной кислоты в исходном растворе:
ω(H2SO4) = m(H2SO4)/(m(H2O)+ m(H2SO4)) = 39,2/(39,2 + 57,6) = 0,405 или 40,5%
Ответ: ω(H2SO4) = 40,5%
Массовая доля элемента в соединении
Рассчитать массовую долю элементов в соединении нитрат бария (Ba(NO3)2).
Решение задачи
Вычислим массовую долю элементов в соединении нитрат бария (Ba(NO3)2).
Напомню, что массовая доля элемента в соединении называется число, показывающее какую часть (в долях еденицы или %) составляет масса всех атомов данного элемента, содержащихся в одной молекуле вещества, от общей массы молекулы.
Где:
n – число атомов данного химического элемента в молекуле вещества;
Ar – относительная масса атома данного химического элемента;
Mr – относительная молекулярная масса вещества.
Учитывая данные таблицы Менделеева рассчитаем молярную массу нитрата бария (Ba(NO3)2):
Mr (Ba(NO3)2) = 137 + 2 ⋅ 14 + 2 ⋅ 3 ⋅ 16 = 261.
Рассчитаем массовую долю элемента в соединении бария (Ba):
Рассчитаем массовую долю элемента в соединении азота (N):
Рассчитаем массовую долю элемента в соединении кислорода (O):
Ответ:
массовая доля элемента в соединении бария равна 0,52;
массовая доля элемента в соединении азота равна 0,11;
массовая доля элемента в соединении кислорода равна 0,37.
Определите массовую долю карбоната натрия в растворе, полученном кипячением 150 г 8,4%-ного раствора гидрокарбоната натрия. Какой объем 15,6%-ого раствора хлорида бария (плотностью 1,11 г/мл) прореагирует с полученным карбонатом натрия? Испарением воды можно пренебречь.
Ответ: 5,42 %, 90 мл
Пояснение:
Разложение гидрокарбоната натрия в растворе описывается реакцией:
2NaHCO3 → Na2CO3 + CO2↑ + H2O
Массовая доля растворенного вещества рассчитывается по формуле:
w(в-во)% = m(в-ва)/m(р−ра).100%,
где m(в-ва) – масса растворенного вещества, m(р−ра) – масса раствора).
Вычислим массу растворенного гидрокарбоната натрия (NaHCO3):
M(NaHCO3) = m(р−ра).w(NaHCO3)/100% = 150 г . 8,4%/100% = 12,6 г
ν(NaHCO3) = m(NaHCO3)/M(NaHCO3) = 12,6 г/84 г/моль = 0,15 моль
По уравнению реакции:
ν(Na2CO3) = ν(CO2)= 1/2ν(NaHCO3) = 0,15 моль/2 = 0,075 моль
m(Na2CO3) = M(Na2CO3) . ν(Na2CO3) = 106 г/моль . 0,075 моль = 7,95 г.
m(CO2) = M(CO2) . ν(CO2) = 44 г/моль . 0,075 моль = 3,3 г.
Так как испарением воды можно пренебречь, массу образовавшегося после разложения гидрокарбоната натрия находим, вычитая из массы исходного раствора массу углекислого газа:
m(р−ра) = m(исх.р−ра) — m(CO2) = 150 г – 3,3 г = 146,7 г
Массовая доля карбоната натрия равна:
w(Na2CO3)% = m(Na2CO3)/m(р−ра).100% = 7,95 г/146,7 г.100% = 5,42%
Реакция взаимодействия растворов хлорида бария и карбоната натрия описывается уравнением:
BaCl2 + Na2CO3 → BaCO3↓ + 2NaCl
По уравнению реакции:
ν(BaCl2) = ν(Na2CO3)= 0,075 моль, следовательно
m(BaCl2) = M(BaCl2) . ν(BaCl2) = 208 г/моль . 0,075 моль = 15,6 г
Масса раствора хлорида бария равна:
m(р−ра BaCl2) = m(BaCl2)/w(BaCl2).100% = 15,6 г/15,6%. 100% = 100 г
Объем раствора рассчитывается по формуле:
V(р−ра) = m(р−ра)/ρ(р−ра), где ρ(р−ра) – плотность раствора.
V(р−ра BaCl2) = m(р−ра BaCl2)/ρ(р−ра)
V(р−ра BaCl2) = 100 г/1,11 г/мл = 90 мл
Преобразование молей нитрата натрия в граммы
›› Перевести моль нитрата натрия в грамм
Пожалуйста, включите Javascript использовать конвертер
›› Больше информации от конвертера
Сколько молей нитрата натрия в 1 грамме?
Ответ 0,011765443644878.
Мы предполагаем, что вы конвертируете между моль нитрата натрия и грамм .
Вы можете просмотреть более подробную информацию о каждой единице измерения:
молекулярная масса нитрата натрия или
грамм
Молекулярная формула для нитрата натрия NaNO3.
Базовая единица СИ для количества вещества — моль.
1 моль равен 1 моль нитрата натрия, или 84,99467 грамма.
Обратите внимание, что могут возникнуть ошибки округления, поэтому всегда проверяйте результаты.
Используйте эту страницу, чтобы узнать, как конвертировать моль нитрата натрия в грамм.
Введите свои числа в форме для преобразования единиц!
›› Подобные химические формулы
Обратите внимание, что все формулы чувствительны к регистру.
Вы хотели преобразовать одну из этих похожих формул?
моль NaNO3 до грамма
моль NaNo3 до грамма
›› График быстрой конверсии молей нитрата натрия в граммы
1 моль нитрата натрия в граммах = 84.99467 грамм
2 моля нитрата натрия в граммах = 169,98934 грамма
3 моля нитрата натрия в граммах = 254,98401 грамма
4 моля нитрата натрия в граммах = 339,97868 граммов
5 молей нитрата натрия в граммах = 424,97335 грамма
6 молей нитрата натрия в граммах = 509,96802 грамма
7 молей нитрата натрия в граммах = 594,96269 граммов
8 молей нитрата натрия в граммах = 679,95736 граммов
9 молей нитрата натрия в граммах = 764.95203 грамм
10 молей нитрата натрия в граммах = 849,9467 грамма
›› Хотите другие юниты?
Вы можете сделать обратное преобразование единиц из граммы нитрата натрия в моли или введите другие единицы для преобразования ниже:
›› Общее количество веществ преобразования
моль нитрат натрия в децимол
моль нитрат натрия в киломол
моль нитрат натрия в моль
моль нитрат натрия в сантимол
моль нитрат натрия в молекулу
моль нитрат натрия в атом
моль нитрат натрия в наномол
моль нитрат натрия в пикомол
моль нитрат натрия до микромоль
моль нитрат натрия до миллимоль
›› Подробности расчета молекулярной массы
В химии формула веса — это величина, вычисленная умножением атомного веса (в атомных единицах массы) каждого элемента в химической формуле на число атомов этого элемента, присутствующего в формуле, с последующим сложением всех этих продуктов вместе.
Веса формулы особенно полезны при определении относительных весов реагентов и продуктов в химической реакции. Эти относительные веса, вычисленные по химическому уравнению, иногда называют уравнительными весами.
Если формула, используемая при расчете молярной массы, является молекулярной формулой, вычисленная масса формулы представляет собой молекулярную массу. Массовый процент любого атома или группы атомов в соединении можно рассчитать путем деления общего веса атома (или группы атомов) в формуле на вес формулы и умножения на 100.
Используя химическую формулу соединения и периодическую таблицу элементов, мы можем сложить атомные веса и рассчитать молекулярный вес вещества.
Используемые на этом сайте атомные веса получены от NIST, Национального института стандартов и технологий. Мы используем самые распространенные изотопы. Это как рассчитать молярную массу (среднюю молекулярную массу), которая основана на изотропно взвешенных средних. Это не то же самое, что молекулярная масса, которая является массой одной молекулы четко определенных изотопов.Для объемных стехиометрических расчетов мы обычно определяем молярную массу, которую также можно назвать стандартной атомной массой или средней атомной массой.
Нахождение молярной массы начинается с единиц грамма на моль (г / моль). При расчете молекулярной массы химического соединения он говорит нам, сколько граммов содержится в одном моле этого вещества. Вес формулы — это просто вес в атомных единицах массы всех атомов в данной формуле.
Распространенный запрос на этом сайте — конвертировать грамм в родинки.Чтобы завершить этот расчет, вы должны знать, какое вещество вы пытаетесь преобразовать. Причина в том, что молярная масса вещества влияет на конверсию. Этот сайт объясняет, как найти молярную массу.
›› Метрические преобразования и многое другое
ConvertUnits.com предоставляет онлайн калькулятор преобразования для всех типов единиц измерения. Вы можете найти таблицы преобразования метрик для единиц СИ, а также как английские единицы, валюта и другие данные. Введите в единицу символы, сокращения или полные имена для единиц длины, площадь, масса, давление и др. типы.Примеры включают мм, дюйм, 100 кг, жидкая унция США, 6’3 «, 10 камень 4, куб. см, метров в квадрате, граммы, родинки, футы в секунду и многое другое!
,натрий | Факты, использование и свойства
Натрий (Na) , химический элемент группы щелочных металлов (группа 1 [Ia]) периодической таблицы. Натрий очень мягкий серебристо-белый металл. Натрий является наиболее распространенным щелочным металлом и шестым наиболее распространенным элементом на Земле, составляя 2,8 процента земной коры. В природе он встречается в большом количестве в соединениях, особенно в поваренной соли — хлориде натрия (NaCl), которая образует минерал галит и составляет около 80 процентов растворенных компонентов морской воды.
Encyclopædia Britannica, Inc.Британика Викторина
118 символов и названия периодической таблицы викторины
Au
| атомный номер | 11 |
|---|---|
| атомный вес | 22.9898 |
| температура плавления | 97,81 ° C (208 ° F) |
| температура кипения | 882,9 ° C (1 621 ° F) |
| удельный вес | 0,971 (20 ° C) |
| степени окисления | +1, -1 (редко) |
| электронная конфигурация | 2-8-1 или 1 с 2 2 с 2 2 p 6 3 с 1 |
Свойства и производство
Поскольку натрий чрезвычайно реактивен, он никогда не встречается в свободном состоянии в земной коре.В 1807 году сэр Хэмфри Дэви стал первым, кто получил натрий в его элементарной форме, применив электролиз к конденсированному гидроксиду натрия (NaOH). Натрий является важной составной частью ряда силикатных материалов, таких как полевые шпаты и слюды. В разных частях света имеются огромные залежи каменной соли, а в Чили и Перу имеются залежи нитрата натрия. Содержание натрия в море составляет приблизительно 1,05 процента, что соответствует концентрации приблизительно 3 процентов галогенидов натрия. Натрий был идентифицирован как в атомной, так и в ионной формах в спектрах звезд, включая Солнце и межзвездную среду.Анализ метеоритов показывает, что присутствующий силикатный материал имеет среднее содержание примерно 4,6 атомов натрия на каждые 100 атомов кремния.
сэр Хамфри Дэви сэр Хамфри Дэви, деталь масляной живописи после сэра Томаса Лоуренса; в Национальной портретной галерее в Лондоне. Предоставлено Национальной портретной галереей, ЛондонЛегче воды натрий можно разрезать ножом при комнатной температуре, но при низких температурах он ломкий. Он легко проводит тепло и электричество и в значительной степени проявляет фотоэлектрический эффект (эмиссия электронов при воздействии света).
Натрий, безусловно, самый коммерчески важный щелочной металл. Большинство процессов производства натрия включают электролиз расплавленного хлорида натрия. Недорогой и доступный в количествах цистерн, этот элемент используется для производства присадок к бензину, полимеров, таких как нейлон и синтетический каучук, фармацевтических препаратов и ряда металлов, таких как тантал, титан и кремний. Он также широко используется в качестве теплообменника и в натриевых лампах. Желтый цвет лампы с натриевым паром и пламени натрия (основа аналитического теста на натрий) обозначен двумя яркими линиями в желтой части спектра света.
Лампа натриевая лампа высокого давления. (сверху и по центру) W.H. Родос и Г.С. Вэй в Р. В. Кан и М. Б. Бевер (ред.), Энциклопедия материаловедения и инженерии, Дополнительный том. 3, © 1993 Pergamon Press; (внизу) Дженерал Электрик Получите эксклюзивный доступ к контенту из нашего первого издания 1768 года с вашей подпиской. Подпишитесь сегодняЗначительное использование
Два из самых ранних применений металлического натрия были в производстве цианида натрия и пероксида натрия.Значительные количества были использованы при производстве тетраэтилсвинца в качестве присадки к бензину, рынок, который исчез с появлением неэтилированного бензина. Существенные количества натрия используются в производстве алкилсульфатов натрия в качестве основного ингредиента в синтетических моющих средствах.
Натрий также используется в качестве исходного материала при производстве гидрида натрия (NaH) и борогидрида натрия (NaBH 4 ). Кроме того, натрий используется в производстве красителей и промежуточных продуктов красителей, в синтезе духов и в широком разнообразии органических восстановлений.Он используется при очистке углеводородов и при полимеризации ненасыщенных углеводородов. Во многих органических применениях натрий используется в виде дисперсий в жидких углеводородных средах.
Расплавленный натрий является отличным теплоносителем, и благодаря этому свойству он нашел применение в качестве теплоносителя в жидкометаллических быстрых реакторах-размножителях. Натрий широко используется в металлургии в качестве раскислителя и восстановителя для получения кальция, циркония, титана и других переходных металлов.Коммерческое производство титана включает восстановление тетрахлорида титана (TiCl 4 ) натрием. Продукты металлические Ti и NaCl.
Основные соединения
Натрий обладает высокой реакционной способностью, образуя широкий спектр соединений почти со всеми неорганическими и органическими анионами (отрицательно заряженными ионами). Обычно он имеет степень окисления +1, и его единственный валентный электрон теряется с большой легкостью, образуя бесцветный катион натрия (Na + ). Соединения, которые содержат анион натрия, Na — , также были синтезированы.Основными коммерческими соединениями натрия являются хлорид, карбонат и сульфат.
Наиболее важным и известным соединением натрия является хлорид натрия или поваренная соль NaCl. Большинство других соединений натрия получают прямо или косвенно из хлорида натрия, который встречается в морской воде, в природных рассолах и в виде каменной соли. Большие количества хлорида натрия используются в производстве других тяжелых (промышленных) химических веществ, а также используются непосредственно для удаления льда и снега, для кондиционирования воды и в пищевых продуктах.
натрия хлорид Натрия хлорид. HenningklevjerДругие основные коммерческие применения хлорида натрия включают его использование в производстве хлора и гидроксида натрия путем электролитического разложения и в производстве карбоната натрия (Na 2 CO 3 ) по процессу Сольвея. При электролизе водного раствора хлорида натрия образуются гипохлорит натрия, NaOCl, соединение натрия, кислорода и хлора, которые в больших количествах используются в бытовом хлорном отбеливателе.Гипохлорит натрия также используется в качестве промышленного отбеливателя для бумажной массы и текстиля, для хлорирования воды и в некоторых лекарственных препаратах в качестве антисептика и фунгицида. Это нестабильное соединение, известное только в водном растворе.
Карбонаты содержат карбонат-ион (CO 3 2– ). Бикарбонат натрия, также называемый гидрокарбонатом натрия, или бикарбонат соды, NaHCO 3, является источником углекислого газа и поэтому используется в качестве ингредиента в разрыхлителях, в шипучих солях и напитках, а также в качестве основного компонента сухих химические огнетушители.Его небольшая щелочность делает его полезным для лечения повышенной кислотности желудка или мочи и ацидоза. Он также используется в определенных промышленных процессах, таких как дубление и подготовка шерсти. Карбонат натрия, или кальцинированная сода, Na 2 CO 3 , широко распространен в природе и встречается в составе минеральных вод и твердых минералов: натрона, троны и термонатрита. Большое количество этой щелочной соли используется для изготовления стекла, моющих средств и моющих средств. Карбонат натрия обрабатывают углекислым газом для получения бикарбоната натрия.Моногидратная форма карбоната натрия, Na 2 CO 3 · H 2 O, широко используется в фотографии как составная часть разработчиков.
бикарбонат натрия Бикарбонат натрия (NaHCO3), также известный как пищевая сода или бикарбонат соды. © Geo-grafika / Shutterstock.comСульфат натрия, Na 2 SO 4 , представляет собой белое кристаллическое вещество или порошок, используемый при производстве крафт-бумаги, картона, стекла и моющих средств, а также в качестве сырья для производства различных химических веществ.Его получают либо из месторождений минералов сульфата натрия, мирабилита и затемардита, либо синтетически путем обработки хлорида натрия серной кислотой. Кристаллизованный продукт представляет собой гидрат, Na 2 SO 4 · 10H 2 O, широко известный как глауберова соль. Тиосульфат натрия (гипосульфит натрия), Na 2 S 2 O 3 , используется фотографами для фиксации проявленных негативов и отпечатков; он действует путем растворения части солей серебра, нанесенных на пленку, которые остаются неизменными под воздействием света.
Гидроксид натрия (NaOH) — это коррозийное белое кристаллическое вещество, которое легко впитывает влагу, пока не растворится. Обычно называемая каустическая сода, или щелочь, гидроксид натрия является наиболее широко используемой промышленной щелочью. Это очень коррозийно для животных и растительных тканей. Щелочные растворы, которые образуются при растворении в воде, нейтрализуют кислоты в различных промышленных процессах: при переработке нефти удаляют серную и органическую кислоты; в мыловарении реагирует с жирными кислотами. Растворы NaOH используются при обработке целлюлозы и при производстве многих химических веществ.
Испаритель Испаритель с падающей пленкой для концентрирования растворов едкого натра (гидроксида натрия). Рубен КастельнуовоНитрат натрия, или нитрат соды, NaNO 3 , обычно называют чилийской селитрой, после того, как ее месторождения полезных ископаемых в северной части Чили являются основным источником. Нитрат натрия используется в качестве азотного удобрения и в качестве компонента динамита.
,Формула и структура: Химическая формула нитрата натрия — NaNO 3 . Молекулярная формула NNaO 3 и его молярная масса составляет 84,9947 г / моль. Это натриевая соль азотной кислоты (HNO 3 ), и, следовательно, состоит из катиона натрия (Na + ) и нитрат-аниона (NO 3 — ). Нитрат-ион имеет центральный атом азота, связанный с тремя атомами кислорода через одну двойную связь и две одинарные связи, которые находятся в резонансе друг с другом.
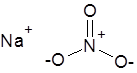
Возникновение: Нитрат натрия встречается в природе в виде крупных минеральных отложений (называемых нитратином) в сухих регионах, особенно в пустынях Южной Америки, поэтому его также называют селитрой Чили / Перу. Месторождения нитрата натрия встречаются в виде нечистой нитратной породы или гравия. Эти природные залежи нитрата натриевой соли являются основным источником этого химического вещества после добычи и очистки.
. Приготовление: нитрат натрия также синтезируется в промышленности для некоторых применений путем взаимодействия азотной кислоты с основанием, таким как карбонат натрия, бикарбонат натрия или гидроксид натрия.
HNO 3 + NaOH → NaNO 3 + H 2 O
Его также получают взаимодействием нитрата аммония с основаниями, поскольку эта реакция является менее экзотермической (с выделением тепла), чем реакция сильного кислотно-сильного основания, описанная выше.
NH 4 NO 3 + NaOH → NaNO 3 + NH 4 OH
Физические свойства: нитрат натрия представляет собой белое кристаллическое вещество с плотностью 2,26 г / мл и температурой плавления 308 ° C. Он существует в виде тригональных или ромбоэдрических кристаллов.
Химические свойства: Нитрат натрия является солью сильной кислоты и, следовательно, полностью диссоциирует в воде на натриевые и нитратные ионы. Это стабильное твердое вещество при комнатной температуре, однако при длительном нагревании оно может взорваться и выделять токсичные пары. Это сильный окислитель и бурно реагирует с сильными восстановителями и легковоспламеняющимися материалами.
Использование: Нитрат натрия используется в качестве пищевого консерванта и заменителя соли. Это также используется в зубных продуктах, взрывчатых веществах, дымовых шашках, удобрениях, очистке сточных вод, материалах для хранения энергии и твердых ракетных топливах.
Воздействие на здоровье / опасности для здоровья: Нитрат натрия является сильным окислителем и может вызвать раздражение кожи и глаз при воздействии. Глотание высоких концентраций нитрата натрия может повредить желудочно-кишечный тракт и вызвать сильную боль в животе, диарею и тошноту.
Молярная масса нитрата натриядля взрывчатого вещества эмульсии
468,00 долларов США — 480,00 долларов США / Тонна | 25 тонн / тонн (мин.Порядок)
- Время выполнения:
Количество (Тонны) 1 — 25 > 25 Est.Время (дни) 14 Торг
- Образцы:

Leave A Comment