Тест по биологии Химический состав клетки
Тест по биологии Химический состав клетки — белки, нуклеиновые кислоты и АТФ 10 класс. Тест включает два варианта, в каждом по 11 заданий.
Вариант 1
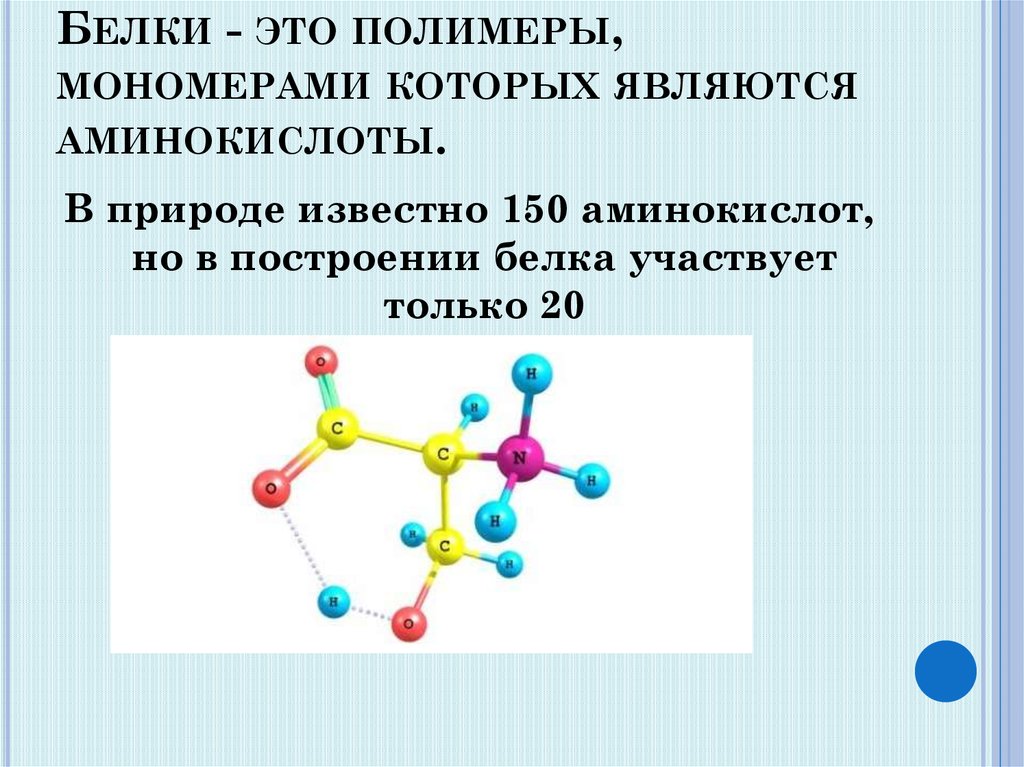
А1. Мономерами белков являются
1) ДНК и рРНК
2) моносахариды
3) аминокислоты
4) нуклеотиды
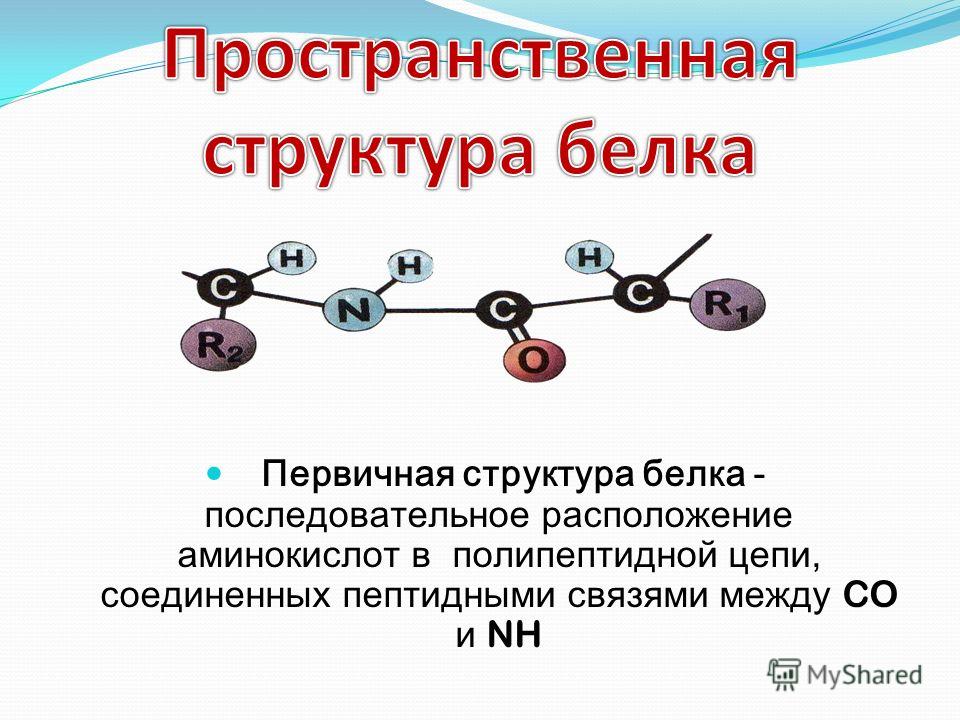
А2. Первичной структурой белка является
1) α-спираль, прошитая водородными связями
2) последовательность аминокислотных остатков в полипептидной цепи
3) взаимное расположение нескольких белковых цепей
4) пространственная конфигурация α-спирали, образованная за счет ковалентных полярных, неполярных и ионных связей
А3. Третичной структурой белковой молекулы является
1) α-спираль, прошитая водородными связями
2) последовательность аминокислотных остатков в полипептидной цепи
3) взаимное расположение нескольких белковых цепей
4) пространственная конфигурация α-спирали, образованная за счет ковалентных полярных, неполярных и ионных связей
А4. Функции ферментов в клетке заключаются в
Функции ферментов в клетке заключаются в
1) транспорте веществ
2) ускорении химических реакций
4) сокращении мышечных волокон
А5. Потеря белком своих природных свойств — это
1) инициация
2) денатурация
3) ренатурация
4) трансляция
А6. Определите молекуле какого вещества принадлежит изображенный на рисунке нуклеотид
1) ДНК
2) РНК
3) АТФ
4) белок
А7. Мономером всех видов РНК является
1) нуклеотид
2) рибоза
3) аминокислота
4) урацил
А8. Молекулы иРНК в отличие от тРНК
1) служат матрицей для синтеза рРНК
2) образуют рибосомы
3) служат матрицей для синтеза белка
4) образуют липиды и углеводы
А9. Универсальным источником энергии для всех реакций, протекающих в клетке, является
1) рРНК
2) АТФ
З) тРНК
4) ДНК
В1. Функциями белков в клетке являются
Функциями белков в клетке являются
1) информационная
2) запасающая, энергетическая
3) транспортная, каталитическая
4) регуляторная, защитная
5) структурная, двигательная
6) передача наследственной информации
В2. Установите соответствие между химическим веществом, его функциями, свойствами и особенностями строения.
ОСОБЕННОСТИ СТРОЕНИЯ И ФУНКЦИИ
А. Является хранителем наследственной информации
В. Содержит пиримидиновое азотистое основание — урацил
Г. Состоит из двух полинуклеотидных цепей, закрученных в спираль
Д. Состоит из одной полинуклеотидной цепи
А. Состоит из нуклеотидов АТГЦ
ВЕЩЕСТВО
1. ДНК
2. иРНК
Запишите выбранные цифры под соответствующими буквами.
Вариант 2
А1. Количество видов аминокислот, входящих в состав белка
1) 60
2) 20
3) 15
4) 10
А2. Вторичной структурой белковой молекулы является
Вторичной структурой белковой молекулы является
1) α-спираль, прошитая водородными связями
2) последовательность аминокислотных остатков в полипептидной цепи
3) взаимное расположение нескольких белковых цепей
4) пространственная конфигурация α-спирали, образованная за счет ковалентных полярных, неполярных и ионных связей
А3. Четвертичной структурой белковой молекулы является
1) α-спираль, прошитая водородными связями
2) последовательность аминокислотных остатков в полипептидной цепи
3) взаимное расположение нескольких белковых цепей
4) пространственная конфигурация α-спирали, образованная за счет ковалентных полярных, неполярных и ионных связей
1) АТФ
2) липиды
3) ферменты
4) углеводы
А5. Белком, увеличивающим скорость химической реакции в клетке, является
1) витамин
2) фермент
3) гормон
4) нуклеотид
А6.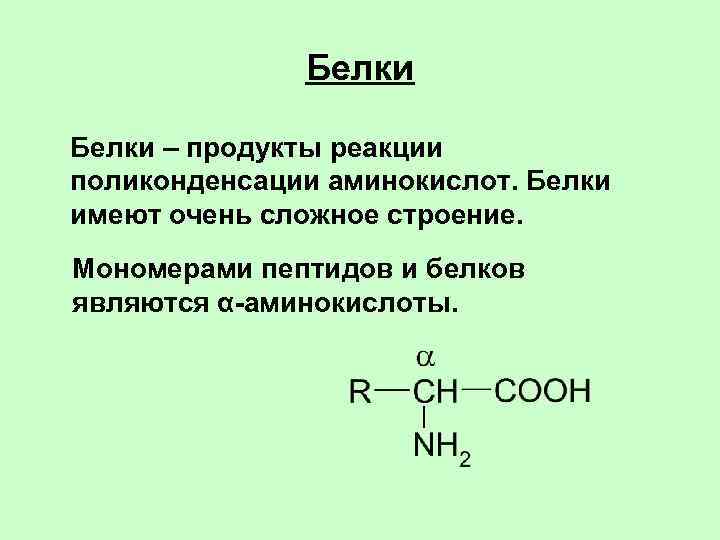 Связь, возникающая между азотистыми основаниями двух комплементарных цепей ДНК
Связь, возникающая между азотистыми основаниями двух комплементарных цепей ДНК
1) ковалентная полярная
2) водородная
3) ковалентная неполярная
4) ионная
А7. Мономером ДНК является
1) нуклеотид
2) дезоксирибоза
3) аминокислота
А8. Определите, молекуле какого вещества принадлежит изображенный на рисунке нуклеотид.
1) ДНК
2) РНК
3) АТФ
4) белок
А9. Синтез АТФ происходит в
1) ядре
2) митохондриях
3) ядрышке
4) рибосомах
В1. Нуклеотид ДНК клетки состоит из
1) рибозы и урацила
2) азотистого основания
3) остатка азотной кислоты
4) дезоксирибозы
5) остатка фосфорной кислоты
6) аминокислоты
В2. Установите соответствие между химическим веществом, его функциями, свойствами и особенностями строения.
ОСОБЕННОСТИ СТРОЕНИЯ И ФУНКЦИИ
А. Состоит из одной полинуклеотидной цепи
 Входит в состав рибосом
Входит в состав рибосомВ. Состоит из нуклеотидов АТГЦ
Г. Состоит из двух полинуклеотидных цепей, закрученных в спираль
Д. Является хранителем наследственной информации
Е. Состоит из нуклеотидов АУГЦ
ВЕЩЕСТВО
1. ДНК
2. иРНК
Запишите выбранные цифры под соответствующими буквами.
Ответы на тест по биологии Химический состав клетки — белки, нуклеиновые кислоты и АТФ 10 класс
Вариант 1
А1-3
А2-2
А3-4
А4-2
А5-2
А6-1
А7-1
А8-3
А9-2
В1. 345
В2. А1 Б2 В2 Г1 Д2 Е1
А1-2
А2-1
А3-3
А4-3
А5-2
А6-2
А7-1
А8-2
А9-2
В1. 245
В2. А2 Б2 В1 Г1 Д1 Е2
PDF версия для печати
Тест Химический состав клетки — белки, нуклеиновые кислоты и АТФ 10 класс
(136 Кб)
Тест по теме «Молекулярная биология» — 4ЕГЭ
59 вопросов.
mb-test.doc
mb-test. pdf
pdf
1. Молекулярная биология изучает:
А протекание биологических процессов на молекулярном уровне;
Б строение клетки;
В морфологическое и физиологическое многообразие бактерий и вирусов.
2. Функции мембран:
А регуляция обмена между клеткой и средой, разделительная функция, рецепторная;
Б транспортная функция, электрическая;
В верны оба варианта ответа.
3. Общая формула аминокислот:
4. Аминокислоты могут проявлять свойства:
А кислот;
Б оснований;
В верны оба варианта ответа.
5. Окончание полипептида, содержащее аминогруппу, называется:
А С – конец;
Б N – конец:
В пептидная связь.
6. Мономерами белков являются:
А нуклеотиды;
Б нуклеосомы;
В аминокислоты.
7. Нуклеотид – это мономер
А белков;
Б нуклеиновых кислот;
В жиров.
8. Простые белки состоят:
А только из нуклеотидов;
Б только из аминокислот;
В из аминокислот и небелковых соединений.
9. Белки, которые растворяются и в воде и в растворе солей, называются:
А альбумины;
Б глобулины;
В фибриллярные белки.
10. В строении белков различают:
А два уровня организации молекулы;
Б три уровня организации молекулы ;
В четыре уровня организации молекулы.
11. Полипептид образуется путем:
А взаимодействия аминогрупп двух соседних аминокислот;
Б взаимодействия аминогруппы одной аминокислоты и карбоксильной группы другой аминокислоты;
В взаимодействия карбоксильных групп двух соседних аминокислот.
12. Степень спирализации белка характеризует:
А первичную структуру белка;
Б вторичную структуру белка;
В третичную структуру белка;
13. Четвертичная структура белка характерна для:
А олигомерных белков;
Б фибриллярных белков;
В глобулярных белков.
14. Белки актин и миозин выполняют функцию:
А транспортную;
Б защитную;
В сократительную.
15. ДНК содержит:
А рибозу, остаток фосфорной кислоты, одно из четырех азотистых оснований: аденин, гуанин, цитозин, тимин;
Б дезоксирибозу, остаток фосфорной кислоты, одно из четырех азотистых оснований: аденин, гуанин, цитозин, тимин;
В дезоксирибозу, остаток фосфорной кислоты, одно из четырех азотистых оснований: аденин, гуанин, цитозин, урацил.
16. Генетический код был открыт:
А Гамовым
Б Гриффитом
В Очоа
17. Специфичность генетического кода состоит в:
А кодировании аминокислот более чем двумя различными триплетами;
Б кодировании каждым триплетом только одной аминокислоты;
В наличии единого кода для всех живущих на земле существ.
18. Вырожденность генетического кода – это:
А кодирование одним триплетом только одной аминокислоты;
Б кодирование одним триплетом одной либо нескольких аминокислот;
В кодирование одной аминокислоты несколькими триплетами.
19. Универсальность генетического кода – это:
А наличие единого кода для всех существ на Земле;
Б кодирование одним триплетом одной либо нескольких аминокислот;
В кодирование одной аминокислоты несколькими триплетами.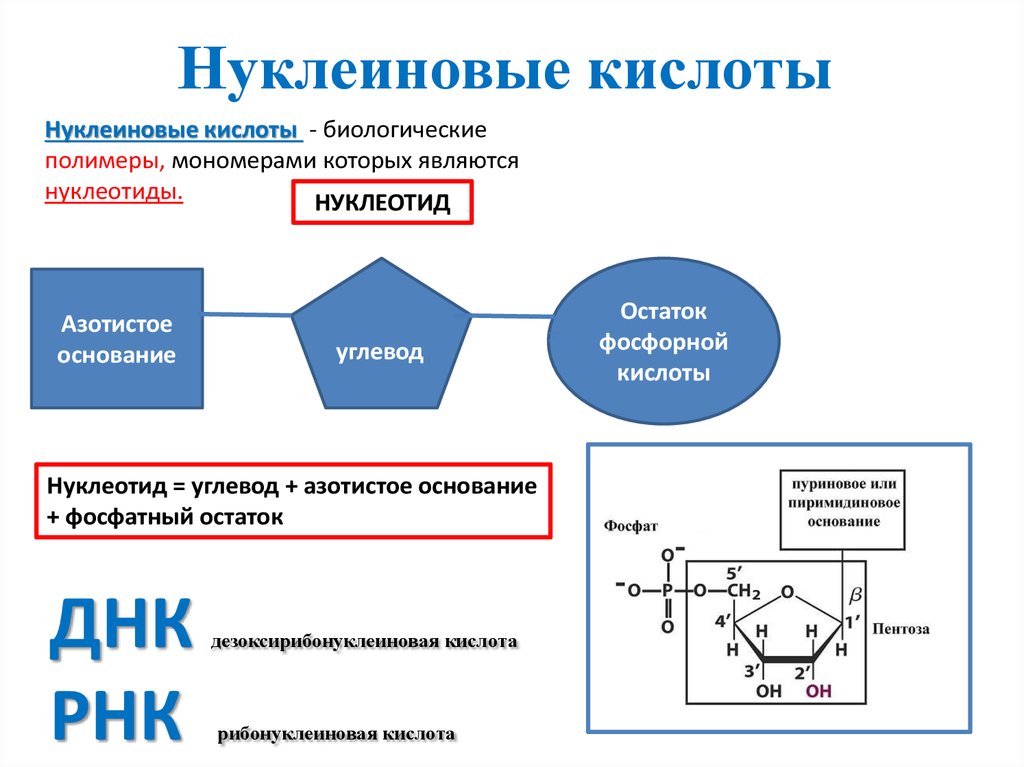
20. Возможных триплетов:
А 64;
Б 28;
В 72,
21. Основания, расположенные комплементарно друг другу:
А А – Т; Г – Ц;
Б А – Ц; Г – Т;
В А – Г; Ц – Т.
22. К первичной структурной организации ДНК относится:
А трехмерная спираль;
Б две комплементарные друг другу антипараллельные полинуклеотидные цепи;
В полинуклеотидная цепь.
23. Вторичная структура ДНК была открыта:
А Натансом и Смитом
Б Уотсоном и Криком
В Эвери, Мак-Леодом и Мак-Карти
24. Сколько уровней организации имеет хроматин:
А три;
Б два;
В четыре.
25. Последовательность организации хроматина в третичной структуре ДНК следующая:
А петли-нуклеосома-соленоид;
Б нуклеосома-соленоид-петли;
В соленоид-петли-нуклеосома.
26. Участок, разделяющий две нуклеосомы, называют:
А соленоид;
Б линкер;
В гистон.
27. РНК в ядре сосредоточено в:
А ядерной оболочке;
Б ядрышке;
В нуклеоплазме.
28. Информация о строении белка передается в цитоплазму:
А матричной РНК;
Б транспортной РНК;
В рибосомной РНК.
29. С рибосомой взаимодействует петля транспортной РНК:
А Дигидроуридиловая
Б Псевдоуридиловая
В Дополнительная
30. Процессинг – это:
А Синтез РНК;
Б Созревание РНК;
В Созревание ДНК.
31. Репликация – это:
А копирование ДНК с образованием 2-х идентичных дочерних молекул;
Б процесс переписывания информации с ДНК на РНК;
В процесс синтеза белка.
32. В репликации ДНК участвует совокупность ферментов и белков. которые образуют:
А репликазу;
Б рестриктазу;
В реплисому.
33. Основной фермент репликации:
А ДНК-полимераза;
Б геликаза;
В лигаза.
34. Начало репликации связано с образованием:
А репликационной вилки и глазка;
Б праймеров;
В фрагментов ДНК на ведущей и отстающей цепи.
35. За расплетение молекулы ДНК ответственен фермент:
А ДНК – полимераза;
Б лигаза;
В геликаза.
36. Механизм репликации ДНК является:
А полуконсервативным;
Б консервативным;
В неконсервативным.
37. Для осуществления процесса репликации в нуклеоплазме необходимо наличие:
А нуклеозидмонофосфатов;
Б нуклеозиддифосфатов;
В нуклеозидтрифосфатов.
38. Синтез дочерних цепей ДНК осуществляется:
А от 5 / конца к 3 / концу;
Б от 3 / конца к 5 / концу;
В на ведущей и отстающей цепях направление синтеза противоположно.
39. Фрагмент Оказаки – это:
А короткий участок отстающей цепи ДНК;
Б длинный участок ведущей цепи ДНК;
В участок материнской цепи ДНК.
40. Репликация ДНК у эукариот протекает:
А быстрее, чем у прокариот;
Б медленнее, чем у прокариот;
В с такой же скоростью, как у прокариот.
41. Транскрипция – это:
А Процесс самокопирования ДНК с образованием двух идентичных дочерних молекул;
Б Процесс переписывания информации, содержащейся в РНК, в форме ДНК.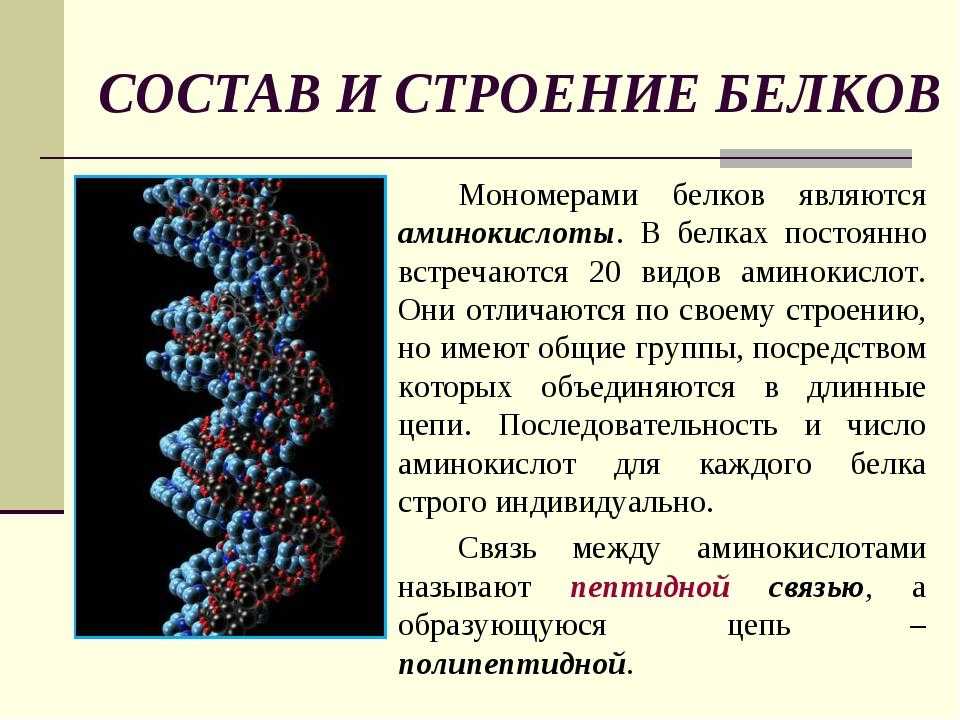
В Процесс переписывания информации, содержащейся в ДНК, в форме РНК.
42. Основной фермент транскрипции:
А ДНК-полимераза;
Б РНК-полимераза;
В рестриктаза.
43. Сходство процессов репликации и транскрипции заключается в том, что:
А синтез дочерних молекул осуществляется в направлении 5′ → 3′;
Б движущая сила – гидролиз пирофосфата;
В верны оба варианта ответа.
44. Отличие процессов репликации и транскрипции:
А при репликации материнская молекула ДНК разрушается, а при транскрипции – сохраняется;
Б для функционирования основного фермента репликации необходимы ионы Mg2+, а транскрипции – Fe2+;
В в активном центре полимеразы транскрипции находятся ионы Zn, а репликации – Li.
45. В процессе транскрипции участвует:
А только одна из двух цепей материнской молекулы ДНК – смысловая;
Б только одна из двух цепей материнской молекулы ДНК – антисмысловая;
В любая из двух цепей материнской молекулы ДНК.
46. Участок ДНК, с которым связывается РНК-полимераза, называется:
А промотор;
Б терминатор;
В транскриптон.
47. В закрытом комплексе РНК-полимеразы и материнской цепи ДНК:
А цепь ДНК расплетена;
Б цепь ДНК не расплетена;
В цепь ДНК разрушена.
48. Кодон инициации – участок цепи, определяющий:
А конец синтеза мРНК;
Б начало транскрипции РНК;
В последовательность нуклеотидов в РНК.
49. Терминация осуществляется в результате:
А замедления движения РНК-полимеразы;
Б ускорения движения РНК-полимеразы;
В сплетения цепей материнской молекулы ДНК.
50. В результате транскрипции образуется:
А только матричная РНК;
Б только транспортная РНК;
В все типы РНК клетки.
51. Синтез белка обозначают термином:
А репликация;
Б транскрипция;
В трансляция;
52. Основной фермент трансляции:
А ДНК-полимераза;
Б аминоацил-тРНК-синтетаза;
В лигаза.
53. При активации аминокислота:
А присоединяется к т РНК;
Б фосфорилируется;
В верны оба варианта ответа
54. Рибосомы в процессе трансляции соединяются в структуру, называемую:
А шероховатая ЭПС;
Б полисома;
В полимер.
55. Кодон инициации кодирует аминокислоту:
А лизин;
Б аспарагин;
В метионин.
56. К аминоацильному участку рибосомы во время трансляции может присоединяться:
А только инициаторная т РНК;
Б все т РНК, несущие аминокислоту;
В все т РНК, несущие аминокислоту, кроме инициаторной.
57. Участок на большой субчастице рибосомы, где локализуется строящийся пептид, называется:
А аминоацильный;
Б пептидильный;
В инициирующий.
58. Процесс элонгации в трансляции – это:
А начало синтеза белка;
Б удлинение полипептидной цепи белка;
В окончание синтеза белка.
59. Изменение последовательности нуклеотидов в ДНК – это:
А хромосомная мутация;
Б генная мутация;
В геномная мутация.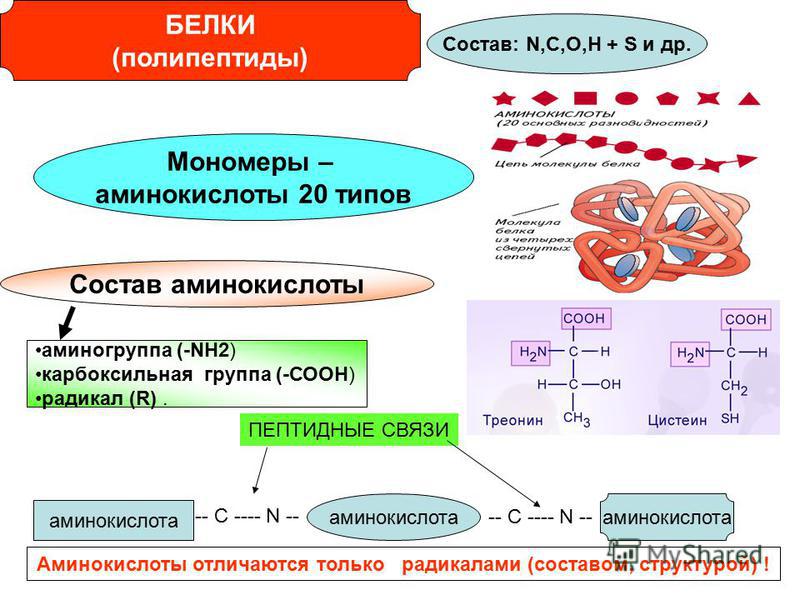
60. Мобильные генетические элементы были открыты:
А Мак-Клинток;
Б Корнбергом;
В Жакобом и Моно.
Ответы
1. А | 31. А
2. В | 32. В
3. В | 33. А
4. В | 34. А
5. Б | 35. В
6. В | 36. А
7. Б | 37. В
8. Б | 38. А
9. Б | 39. А
10. В | 40. Б
11. Б | 41. В
12. Б | 42. Б
13. А | 43. В
14. В | 44. А
15. Б | 45. А
16. А | 46. А
17. Б | 47. Б
18. В | 48. Б
19. А | 49. А
20. А | 50. В
21. А | 51. В
22. В | 52. Б
23. Б | 53. В
24. А | 54. Б
25. Б | 55. В
26. Б | 56. А
27. Б | 57. Б
28. А | 58. Б
29. Б | 59. Б
30. Б | 60. А
Мономерные белки — структура, образование, примеры
Мономерный белок Белки являются жизненно важными веществами для всех живых существ. Они помогают в различных биологических функциях. Вот почему их называют строительными блоками жизни. Они имеют свои уникальные структуры и функции.
Они помогают в различных биологических функциях. Вот почему их называют строительными блоками жизни. Они имеют свои уникальные структуры и функции.
Но знаете ли вы, что они также состоят из более мелких элементов? Как называются эти микроблоки? Почему белки сравнивают с полимерами? Что такое мономеры белков?
Цель этой статьи — дать вам ответы на все эти вопросы. Давайте углубимся в это.
История мономераБудучи студентом, изучающим естественные науки, вы знаете, что многие химические вещества состоят из небольших единиц. Эти маленькие единицы играют жизненно важную роль при рождении пластика. После разработки пластика исследователи начали проявлять большой интерес к этим маленьким единицам. В результате полимеризации и сополимеризации из этих небольших единиц были разработаны различные гибридные структуры.
В период индустриализации органическая химия развивалась относительно быстрыми темпами. Диверсификация структур привела к росту производства нефтехимической продукции.
Термин «мономер» образован путем соединения двух слов «моно» и «мер». Приставка «моно-» означает «один», а суффикс «-мер» означает «часть».
Мономеры, или малые единицы, представляют собой молекулы, которые химически связываются с другими, подобными или отличными молекулами и образуют длинную цепь. В процессе полимеризации они образуют молекулы с длинными повторяющимися цепочками. Эти небольшие единицы могут быть синтетическими или натуральными.
Термин «полимер» используется, когда неопределенное количество мономерных единиц связано с образованием длинной цепи. Проще говоря, полимеры представляют собой сложные структуры из нескольких мономерных звеньев. Если имеется менее 100 мономерных звеньев, химически связанных друг с другом с образованием полимера, такие полимеры называются олигомерами.
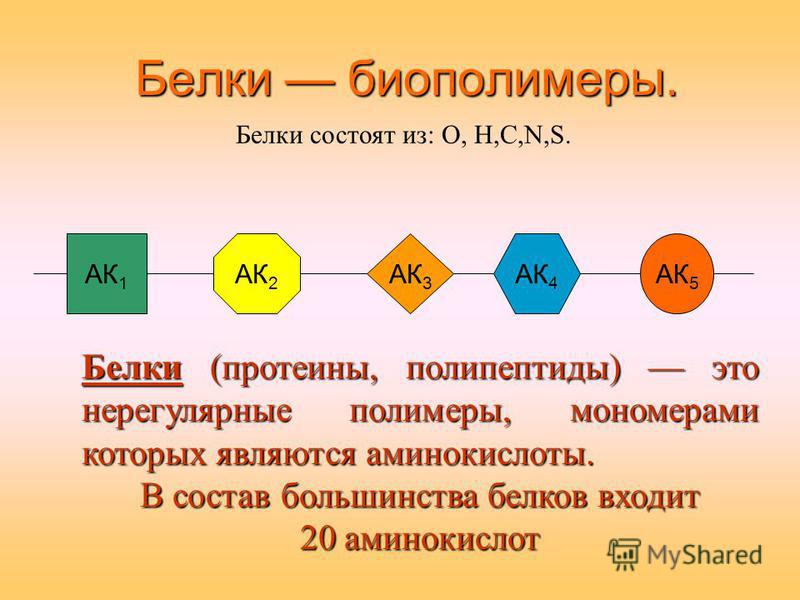
Что такое белки? Полимерные единицы, необходимые для живых существ, называются белками. Белки представляют собой биополимеры, содержащие аминокислоты в качестве мономеров. С химической точки зрения белки представляют собой типы конденсационных полимеров, в которых мономерными единицами являются 𝛼-аминокислоты. Белки образуются путем ковалентной связи таких элементов, как азот, кислород, углерод и водород. В некоторых белках также присутствуют следы серы, йода и фосфора.
Белки представляют собой биополимеры, содержащие аминокислоты в качестве мономеров. С химической точки зрения белки представляют собой типы конденсационных полимеров, в которых мономерными единицами являются 𝛼-аминокислоты. Белки образуются путем ковалентной связи таких элементов, как азот, кислород, углерод и водород. В некоторых белках также присутствуют следы серы, йода и фосфора.
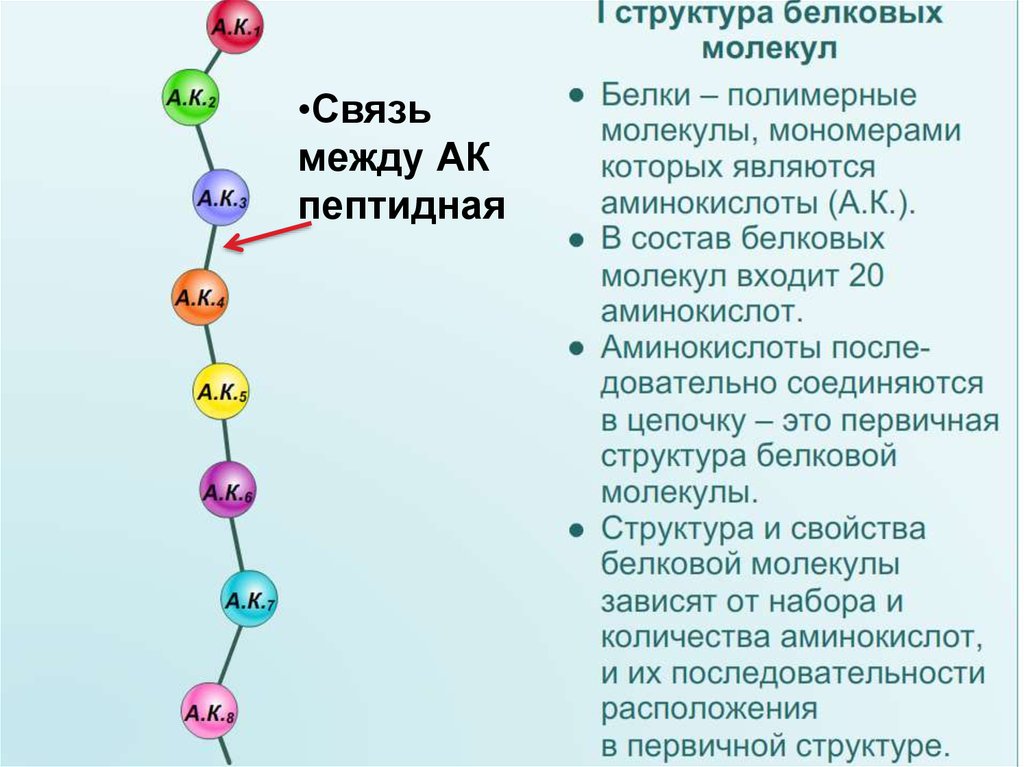
Белки образуются путем связывания нескольких мономерных звеньев. Они содержат одну или несколько полипептидных цепей. Каждая полипептидная цепь образуется путем соединения множества аминокислот с помощью химических связей, называемых пептидными связями. Последовательность аминокислот определяется с помощью гена, кодирующего определенный белок.
После образования полипептидной цепи она превращается в особую трехмерную структуру. Эта структура различна для каждой полипептидной цепи.
Структура белка Структура белка состоит в основном из четырех мономерных белковых структур. Это четвертичные, вторичные, третичные и первичные структуры.
Это четвертичные, вторичные, третичные и первичные структуры.
- Первичная структура: Белки скручены в спирали и свернуты в листы. Аминокислотная последовательность определяет первичную структуру белков.
- Вторичная структура: Водородные связи, соединяющие аминокислоты, определяют вторичную структуру белков. Н-связи могут разорваться только при повышении температуры или кислотных свойств.
- Третичная структура: Атомы серы в аминокислотах тесно связаны пептидной связью.
- Четвертичная структура: В этой структуре отдельные единицы связаны с пространственной дезориентацией.
Ключевой структурной и функциональной единицей полимера является мономер. Эти мономеры являются основными составляющими полимеров. Аминокислоты известны как белковые мономеры. Они присоединяются к большому количеству и соединяются посредством пептидных связей, из которых строятся полипептидные цепи.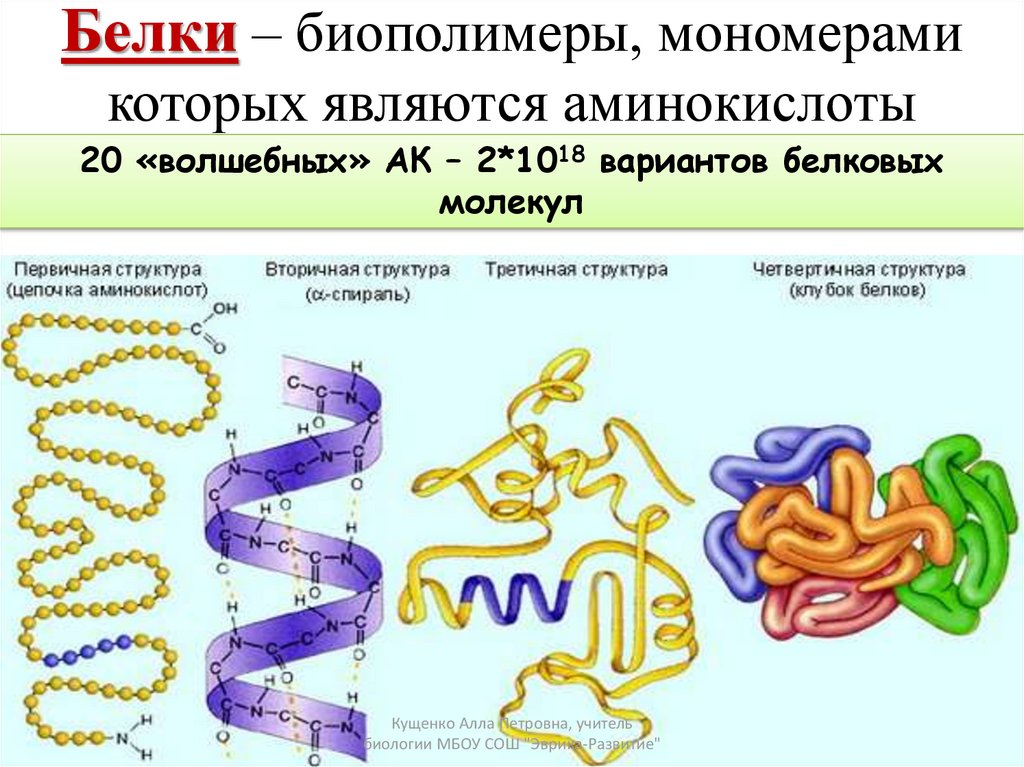 Большие белки образуются при соединении двух или более полипептидных цепей. Последовательность аминокислот определяет функцию и структуру белка.
Большие белки образуются при соединении двух или более полипептидных цепей. Последовательность аминокислот определяет функцию и структуру белка.
Белковые мономеры представляют собой молекулы, которые сливаются с образованием многочисленных белковых комплексов. Полимеры, состоящие из органических мономеров, встречающихся в живых организмах, являются биополимерами. Мономеры делятся на разные классы, такие как спирты, сахара, акрилы, амины и эпоксиды.
Все живые организмы имеют клетки со многими большими молекулами, такими как полисахариды, нуклеиновые кислоты и белки. Эти макромолекулы даже имеют микроструктуры или звенья, которые объединяются в больших количествах. Эти макрокомплексы представляют собой микроструктуры в виде мономеров. Связывание образует макромолекулы или полимеры некоторых мономеров.
Этот мономер связывается с образованием длинной цепочки молекул, что возможно только из-за присутствия углерода и его реакционных свойств. Таким образом, они могут образовывать разные цепочки мономеров белков.
Белки и нуклеиновые кислоты являются основными потребностями всех живых клеток. Элементарными единицами этих мономеров белков являются аминокислоты. Следовательно, будет точнее сказать, что белки состоят из мономеров, называемых аминокислотами. Связывание белковых мономеров происходит за счет полимеризации. Эти составляющие мономеры белков также имеют решающее значение в жизненных процессах.
В результате конструирование белковоподобных полимеров становится понятным при контроле условий и проведении полимеризации аминокислот. Повторяя этот процесс, можно получить несколько сравнительно более простых аминокислот, таких как сахара и нуклеотиды. С помощью этого похожего процесса различные биомолекулы приобретают паттерны.
Строительные блоки или элементарные единицы: Белки Мономеры Белки состоят из некоторых микроединиц. Эти микроединицы обычно известны как мономеры, а в случае белковых мономеров они называются аминокислотами.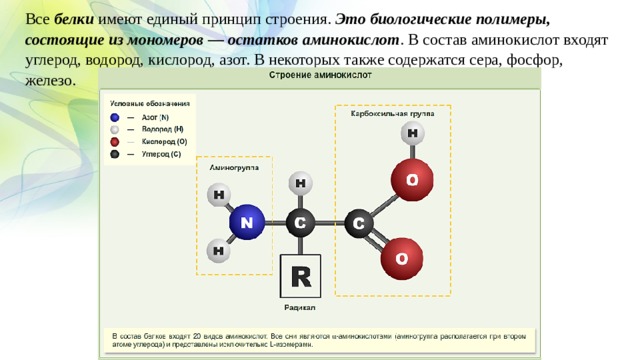
Двадцать различных аминокислот составляют все белки биологической системы в различных последовательностях. Порядок аминокислот, в котором они расположены, называется первичной структурой белка. С химической точки зрения молекула аминокислоты состоит из трех групп: аминогруппы (-Nh3), группы карбоновой кислоты (-COOH) и боковой цепи (группы R). Боковая цепь (группа R) специфична для каждой аминокислоты. Простейшая аминокислота, глицин, содержит атом водорода в группе R.
Кроме того, некоторые другие типы мономеров белков зависят от размера молекул. Обычно эти элементарные единицы классифицируют как незаменимые и несущественные составляющие белков, в зависимости от их потребности. Вы можете быть шокированы, узнав, что около девяноста тысяч композиций или комбинаций белков содержат эти аминокислоты.
Примеры белковых мономеров Всего в живых существах присутствует 20 белковых мономеров. Они подразделяются на два класса: незаменимые белки, которые необходимы для жизни, и несущественные белки, которые не так важны.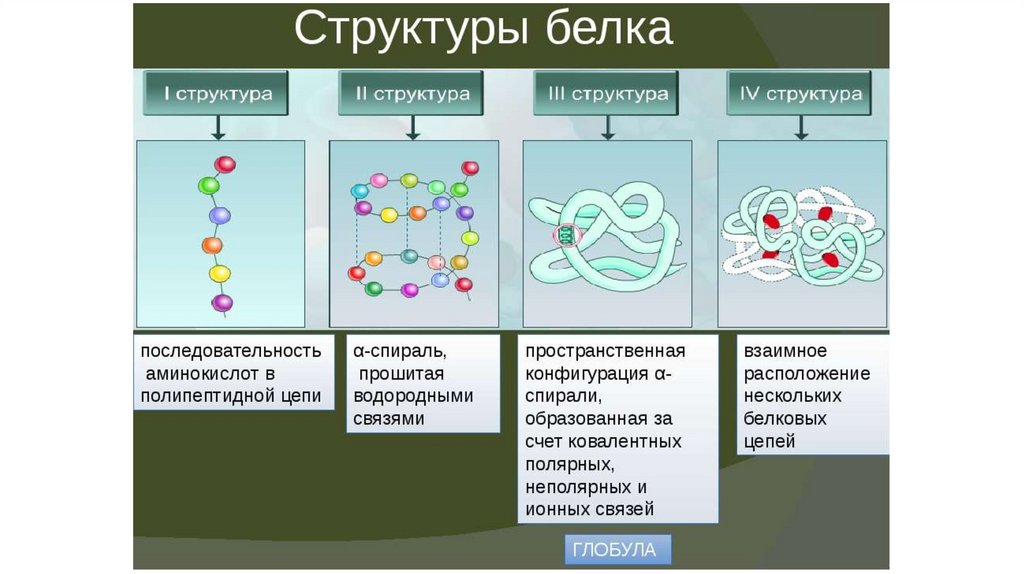
Эти 20 примеров белковых мономеров:
1. Водолюбивый или гидрофильный мономер белка:
- Аспарагин (Asn)
- Глютамин (Gln)
- Лизин (Lys)
- Кислота аспарагиновая (Asp)
- Глутаминовая кислота (Glu)
- Гистидин (Его)
- Аргинин (Arg)
2. Водоотталкивающий или гидрофобный мономер белка:
- Валин (Вал)
- Фенилаланин (Phe)
- Лейцин (лейцин)
- Метионин (метионин)
- Цистеин (Cys)
3. Ни водолюбивый, ни водоотталкивающий мономер белка:
- Глицин (Gly)
- Серин (Серин)
- Тирозин (Tyr)
- Пролин (Pro)
- Аланин (Ала)
- Треонин (Thr)
- Триптофан (Trp)
Проще говоря, мономеры являются строительными блоками белков. В случае белков строительными блоками являются аминокислоты, связанные амидными связями, чтобы соответствовать основной цепи белка (полимеру). Двадцать аминокислотных мономеров используются для построения белков, и каждая из них как группа содержит C, H, O, N, а два содержат S.
В случае белков строительными блоками являются аминокислоты, связанные амидными связями, чтобы соответствовать основной цепи белка (полимеру). Двадцать аминокислотных мономеров используются для построения белков, и каждая из них как группа содержит C, H, O, N, а два содержат S.
Каждый белок имеет разную последовательность аминокислот. Следовательно, «название мономера, из которого состоят белки», будет отличаться от белка к белку. Цепь часто будет иметь большое разнообразие внутри каждого белка вместо повторяющихся аминокислот. Последовательность и состав аминокислотных остатков считаются первичной структурой белка и играют ключевую роль в функционировании белка.
Часто задаваемые вопросы1. Каковы элементарные функции мономера белка в организме человека?
Некоторые важные биологические функции белков приведены ниже:
- Они служат основным структурным материалом для тканей животных.
- Они транспортируют необходимые клетки, такие как кислород, металлы, жирные кислоты, гормоны и т.

- Некоторые белки действуют как ферменты, катализирующие все биологические реакции.
- Некоторые глобулярные белки регулируют метаболические процессы.
- Некоторые белки функционируют как антитела, которые защищают организм от вторжения чужеродных организмов.
2. Что такое незаменимые и заменимые 𝛼-аминокислоты?
Из 20 аминокислот, необходимых для синтеза белка, человеческий организм не может синтезировать только 10. Эти десять аминокислот являются незаменимыми или незаменимыми аминокислотами.
Десять незаменимых аминокислот: валин, метионин, изолейцин, лейцин, фенилаланин, триптофан, треонин, лизин, гистидин и аргинин.
3. Как строение белка связано с его функцией?
Функция белка пропорциональна его структуре. Например, если структура белка волокнистая (например, кератин и коллаген), он ведет себя как структурный белок или защитный белок. Если в структуре аминокислоты есть какая-либо замена, то в этом случае белок денатурируется. Он не выполняет свою надлежащую функцию.
Он не выполняет свою надлежащую функцию.
4. Можно ли классифицировать белки на основе их растворимости и физических свойств?
Белки можно разделить на три категории в зависимости от их растворимости и физических свойств.
Простые белки: Эти белки при гидролизе превращаются в аминокислоты. Например, кератин, эластин, альбумин, коллаген и т. д.
Конъюгированные белки: Эти белки состоят из двух частей, т. е. аминокислот и простетических групп. Например, нуклеопротеины, гемопротеины и др.
Производные белки: Эти белки образуются из нативных белков под действием тепла и химических веществ. Например, денатурированный белок.
Определение, типы и примеры I StudySmarter
Постоянно присутствуют и необходимы для жизни четыре биологические макромолекулы: углеводы, липиды, белки и нуклеиновые кислоты. У этих макромолекул есть одна общая черта: они представляют собой полимеры, состоящие из крошечных одинаковых мономеров.
Далее мы обсудим, что мономеры , как они образуют биологические макромолекулы, и каковы другие примеры мономеров.
Что такое мономер?
Теперь давайте посмотрим на определение мономера.
Мономеры представляют собой простые и идентичные строительные блоки, которые соединяются друг с другом, образуя полимеры.
На рис. 1 показано, как мономеры соединяются вместе, образуя полимеры.
Мономеры соединяются в повторяющиеся субъединицы подобно поезду: каждый вагон представляет собой мономер, а весь поезд, состоящий из множества одинаковых вагонов, соединенных друг с другом, представляет собой полимер.
Мономеры и биологические молекулы
Многие биологически важные молекулы являются макромолекулами. Макромолекулы — это большие молекулы, которые обычно образуются в результате полимеризации более мелких молекул.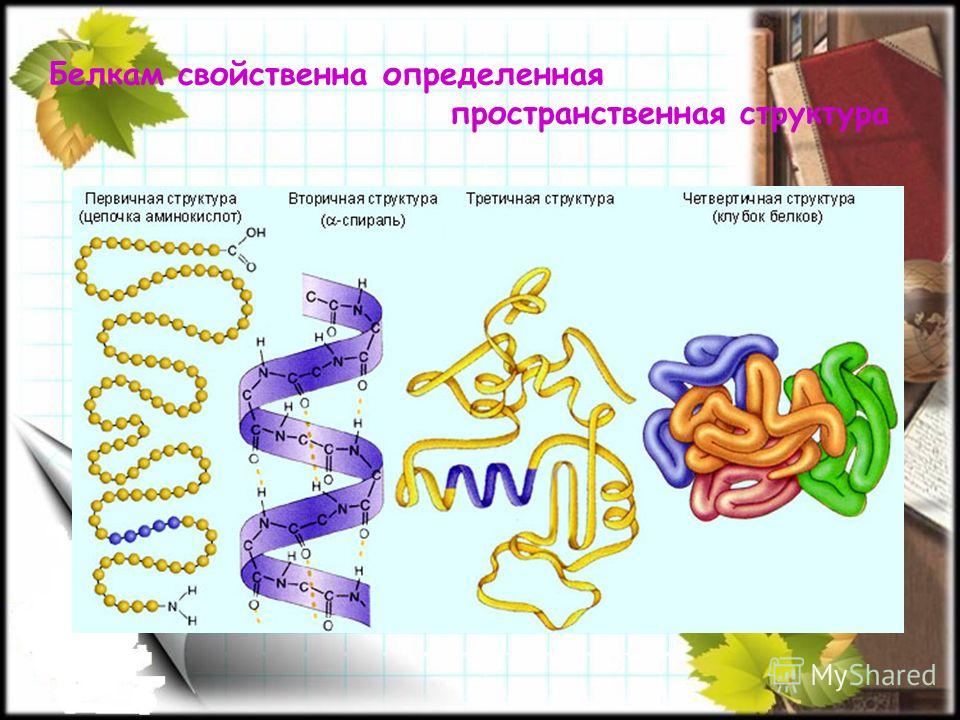 Полимеризация — это процесс, при котором большая молекула, называемая полимером , образуется из комбинации более мелких звеньев, называемых мономерами.
Полимеризация — это процесс, при котором большая молекула, называемая полимером , образуется из комбинации более мелких звеньев, называемых мономерами.
Типы мономеров
Биологические макромолекулы состоят в основном из шести элементов в различных количествах и сочетаниях. Этими элементами являются сера, фосфор, кислород, азот, углерод и водород.
Для образования полимера мономеры соединяются вместе, и в качестве побочного продукта высвобождается молекула воды. Такой процесс называется дегидратационным синтезом .
обезвоживание = потеря воды; синтез = акт соединения
С другой стороны, полимеры можно разрушить, добавив молекулу воды. Такой процесс называется гидролизом .
Существует четыре основных типа макромолекул , которые состоят из соответствующих мономеров:
углеводы — моносахариды
белки — аминокислоты
Ядрат -ядра — нуклеотиды
— жиры и жирные кислоты и Glycerol09
- .
 их мономеры. Мы также приведем несколько соответствующих примеров.
их мономеры. Мы также приведем несколько соответствующих примеров.Углеводы состоят из моносахаридов
Прежде всего, это углеводы.
Углеводы — это молекулы, обеспечивающие энергетическую и структурную поддержку живых организмов. Углеводы состоят из углерода, водорода и кислорода, где соотношение элементов составляет 1 атом углерода: 2 атома водорода: 1 атом кислорода (1C : 2H : 1O)
Углеводы далее подразделяются на моносахариды, дисахариды и полисахариды на основе количество мономеров, содержащихся в макромолекуле.
Моно Сахариды считаются мономерами, из которых состоят углеводы. Примеры моносахаридов включают глюкозу, галактозу и фруктозу.
Ди сахариды состоят из двух моносахаридов . Примеры дисахаридов включают лактозу и сахарозу. Лактоза производится путем сочетания моносахаридов глюкозы и галактозы.
 Обычно он содержится в молоке. Сахароза производится путем сочетания глюкозы и фруктозы. Сахароза — это также причудливый способ сказать столовый сахар.
Обычно он содержится в молоке. Сахароза производится путем сочетания глюкозы и фруктозы. Сахароза — это также причудливый способ сказать столовый сахар.
Вы можете сделать вывод о количестве мономеров в полимере, глядя на префиксы. Моно- означает один; ди- означает два; и поли- означает много. Например, di сахаридов состоят из двух моносахаридов (мономеров).
Примеры полисахаридов включают крахмал и гликоген.
Крахмал состоит из мономеров глюкозы. Избыток глюкозы, вырабатываемой растениями, хранится в различных органах растений, таких как корни и семена. Когда семена прорастают , они используют крахмал, хранящийся в семенах, в качестве источника энергии для зародыша. Это также источник пищи для животных (включая нас, людей!).
Как и крахмал, гликоген также состоит из мономеров глюкозы. Вы можете считать гликоген эквивалентом крахмала, который животные хранят в клетках печени и мышц для получения энергии.

Прорастание относится к совокупности активных метаболических процессов, которые приводят к появлению нового проростка из семени.
Белки состоят из аминокислот
Второй тип макромолекул называется белком .
Белки — это биологические макромолекулы, которые выполняют широкий спектр функций, таких как обеспечение структурной поддержки и действие ферментов, катализирующих биологические реакции.
Белки состоят из мономеров, называемых аминокислота s . Аминокислоты представляют собой молекулы, состоящие из атома углерода, связанного с аминогруппой (NH 2 ), карбоксильной группой (-COOH), атомом водорода и другим атомом или группой, называемой группой R.
Существует 20 распространенных аминокислот, каждая из которых имеет свою R-группу. Аминокислоты имеют различный химический состав (например, кислотность, полярность и т.
 д.) и структуру (спирали, зигзаги и другие формы). Вариации аминокислот в белковых последовательностях приводят к вариациям в функции и структуре белков.
д.) и структуру (спирали, зигзаги и другие формы). Вариации аминокислот в белковых последовательностях приводят к вариациям в функции и структуре белков.Полипептид представляет собой длинную цепь аминокислот, соединенных друг с другом посредством пептидных связей .
Пептидная связь представляет собой химическую связь, образующуюся между двумя молекулами, в которой одна из их карбоксильных групп взаимодействует с аминогруппой другой молекулы, образуя в качестве побочного продукта молекулу воды.
Нуклеиновые кислоты состоят из нуклеотидов
Далее идут нуклеиновые кислоты.
Нуклеиновые кислоты — это молекулы, содержащие генетическую информацию и инструкции для клеточных функций.
Двумя основными формами нуклеиновых кислот являются рибонуклеиновая кислота (РНК) и дезоксирибонуклеиновая кислота (ДНК) .

Нуклеотиды — это мономеры, из которых состоят нуклеиновые кислоты: когда нуклеотиды соединяются вместе, они образуют полинуклеотидные цепи , которые затем образуют сегменты биологических макромолекул, известных как нуклеиновые кислоты. Каждый нуклеотид состоит из трех основных компонентов: азотистого основания, пентозного сахара и фосфатной группы.
Азотистые основания — это органические молекулы с одним или двумя кольцами с атомами азота. И ДНК, и РНК содержат четыре азотистых основания. Аденин, цитозин и гуанин можно найти как в ДНК, так и в РНК. Тимин можно найти только в ДНК, а урацил — только в РНК.
A Пентозный сахар представляет собой молекулу с пятью атомами углерода. В нуклеотидах есть два типа пентозного сахара: рибоза в РНК и дезоксирибоза в ДНК. Что отличает дезоксирибозу от рибозы, так это отсутствие гидроксильной группы (-ОН) на ее 2′-углероде (поэтому она называется «дезоксирибоза»).

Каждый нуклеотид имеет одну или несколько фосфатных групп, присоединенных к сахару пентозе.
Липиды
Наконец, у нас есть липидов . Однако имейте в виду, что липиды не считаются «настоящими полимерами».
Липиды представляют собой группу неполярных биологических макромолекул, включающую жиры, стероиды и фосфолипиды.
Некоторые липиды состоят из жирных кислот и глицерина . Жирные кислоты представляют собой длинные углеводородные цепи с карбоксильной группой на одном конце. Жирные кислоты реагируют с глицерин с образованием глицеридов.
Одна молекула жирной кислоты , присоединенная к молекуле глицерина, образует моноглицерид .
Две молекулы жирных кислот , присоединенные к молекуле глицерина, образуют глицерид ди .

Три молекулы жирных кислот , присоединенные к молекуле глицерина, образуют триглицерид , которые являются основными компонентами жира в организме человека.
Подождите, эти префиксы (моно- и ди-) звучат очень похоже на то, что мы обсуждали ранее в разделе об углеводах. So, why are monosaccharides considered monomers, but not fatty acids and glycerol?
Хотя верно то, что липиды состоят из более мелких единиц (как жирных кислот, так и глицерина), эти единицы не образуют повторяющихся цепей. Обратите внимание, что хотя глицерин всегда один, количество жирных кислот меняется. Таким образом, можно сказать, что в отличие от полимеров липиды содержат цепочку непохожих, неповторяющихся звеньев!
Примеры мономеров
Существует длинный список мономеров, которые можно использовать в качестве примеров для объяснения того, как мономеры уступают место полимерам.
 Вот несколько примеров мономеров, которые помогут вам понять, как работает этот процесс:
Вот несколько примеров мономеров, которые помогут вам понять, как работает этот процесс:Аминокислоты, такие как глутамат, триптофан или аланин. Аминокислоты — это мономеры, из которых строятся белки. Существует 20 различных типов аминокислот, каждая из которых имеет уникальную химическую структуру и боковую цепь. Аминокислоты могут связываться друг с другом через 9Пептид 0003 связывается с с образованием полипептидных цепей, которые затем складываются в функциональные белки.
Нуклеотиды (аденин (A), тимин (T), гуанин (G), цитозин (C) и урацил (U)): нуклеотиды представляют собой мономеры, составляющие нуклеиновых кислот , включая ДНК и РНК. Нуклеотид состоит из молекулы сахара, фосфатной группы и азотистого основания. Нуклеотиды могут соединяться вместе через фосфодиэфирные связи, образуя одну цепь ДНК или РНК.
Моносахариды : моносахариды представляют собой мономеры, из которых состоят углеводы, включая сахара, крахмалы и целлюлозу.
 Моносахариды представляют собой простые сахара, состоящие из одного кольца атомов углерода, к которым присоединены атомы водорода и кислорода. Глюкоза, фруктоза и галактоза — все это примеры моносахаридов. Моносахариды могут соединяться друг с другом через гликозидные связи, образуя более сложные углеводы.
Моносахариды представляют собой простые сахара, состоящие из одного кольца атомов углерода, к которым присоединены атомы водорода и кислорода. Глюкоза, фруктоза и галактоза — все это примеры моносахаридов. Моносахариды могут соединяться друг с другом через гликозидные связи, образуя более сложные углеводы.
Разница между мономерами и полимерами
Мономер представляет собой единицу органической молекулы, которая при соединении с другими мономерами может образовывать полимер. Это означает, что полимеры представляют собой более сложные молекулы по сравнению с мономерами. Полимер состоит из неопределенного количества мономеров. На рисунке 2 ниже показано, как мономеры образуют макромолекулы полимера.
Мономеры
Полимеры / биологические макромолекулы
3 Monosaccharides
Carbohydrates
Amino acids
Proteins
Nucleotides
Nucleic acids
Table 1 .  В этой таблице показаны полимерные биологические макромолекулы и соответствующие им мономеры.
В этой таблице показаны полимерные биологические макромолекулы и соответствующие им мономеры.Также важно отметить, что не все полимеры являются биологическими молекулами. Люди создают и используют искусственные полимеры с 20 9 года.0575-й год.
Примеры искусственных полимеров и их мономеров
Искусственные полимеры представляют собой материалы, созданные людьми путем связывания мономеров. Мы обсудим два примера популярных искусственных полимеров: полиэтилен и поливинилхлорид.
Полиэтилен
Полиэтилен — гибкий, кристаллический и полупрозрачный материал. Вы увидите, что он используется в упаковке, контейнерах, игрушках и даже проводах. На самом деле, это наиболее часто используемый пластик сегодня. Полиэтилен — искусственный полимер, состоящий из этилен мономеры. В одной полиэтиленовой цепи может быть до 10 000 мономерных звеньев!
Поливинилхлорид
Другим часто используемым искусственным полимером является поливинилхлорид (ПВХ).
 Это жесткий материал, который трудно воспламеняется, поэтому его используют в трубах и покрытиях для окон и дверей. Как следует из названия, поливинилхлорид представляет собой полимер, состоящий из мономеров винилхлорида . Винилхлорид — это газ, получаемый при пропускании кислорода, хлористого водорода и этилена через медь, которая действует как катализатор .
Это жесткий материал, который трудно воспламеняется, поэтому его используют в трубах и покрытиях для окон и дверей. Как следует из названия, поливинилхлорид представляет собой полимер, состоящий из мономеров винилхлорида . Винилхлорид — это газ, получаемый при пропускании кислорода, хлористого водорода и этилена через медь, которая действует как катализатор .Катализатор — это любое вещество, которое запускает или ускоряет химическую реакцию, не расходуясь и не изменяясь в процессе.
Мономеры – ключевые выводы
- Мономеры представляют собой простые и идентичные строительные блоки, которые соединяются друг с другом, образуя полимеры.
- Для образования полимера мономеры соединяются вместе, и в качестве побочного продукта выделяется молекула воды. Такой процесс называется дегидратационным синтезом.
- Полимеры можно разложить на мономеры путем добавления молекулы воды. Такой процесс называется гидролизом.


 их мономеры. Мы также приведем несколько соответствующих примеров.
их мономеры. Мы также приведем несколько соответствующих примеров. Обычно он содержится в молоке. Сахароза производится путем сочетания глюкозы и фруктозы. Сахароза — это также причудливый способ сказать столовый сахар.
Обычно он содержится в молоке. Сахароза производится путем сочетания глюкозы и фруктозы. Сахароза — это также причудливый способ сказать столовый сахар.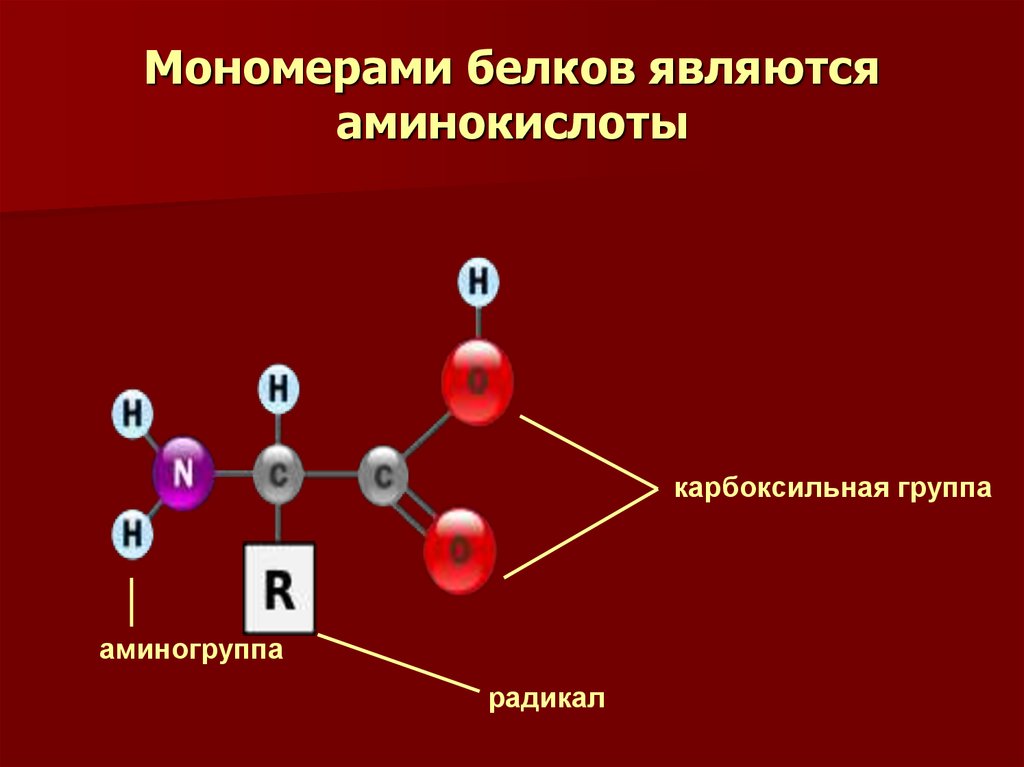
 д.) и структуру (спирали, зигзаги и другие формы). Вариации аминокислот в белковых последовательностях приводят к вариациям в функции и структуре белков.
д.) и структуру (спирали, зигзаги и другие формы). Вариации аминокислот в белковых последовательностях приводят к вариациям в функции и структуре белков.


 Вот несколько примеров мономеров, которые помогут вам понять, как работает этот процесс:
Вот несколько примеров мономеров, которые помогут вам понять, как работает этот процесс: Моносахариды представляют собой простые сахара, состоящие из одного кольца атомов углерода, к которым присоединены атомы водорода и кислорода. Глюкоза, фруктоза и галактоза — все это примеры моносахаридов. Моносахариды могут соединяться друг с другом через гликозидные связи, образуя более сложные углеводы.
Моносахариды представляют собой простые сахара, состоящие из одного кольца атомов углерода, к которым присоединены атомы водорода и кислорода. Глюкоза, фруктоза и галактоза — все это примеры моносахаридов. Моносахариды могут соединяться друг с другом через гликозидные связи, образуя более сложные углеводы. В этой таблице показаны полимерные биологические макромолекулы и соответствующие им мономеры.
В этой таблице показаны полимерные биологические макромолекулы и соответствующие им мономеры.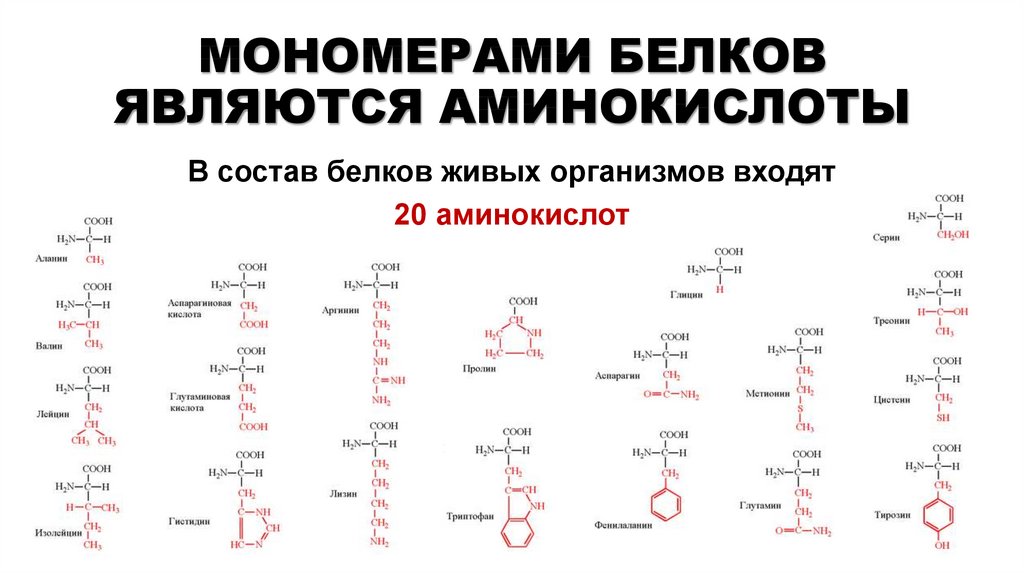 Это жесткий материал, который трудно воспламеняется, поэтому его используют в трубах и покрытиях для окон и дверей. Как следует из названия, поливинилхлорид представляет собой полимер, состоящий из мономеров винилхлорида . Винилхлорид — это газ, получаемый при пропускании кислорода, хлористого водорода и этилена через медь, которая действует как катализатор .
Это жесткий материал, который трудно воспламеняется, поэтому его используют в трубах и покрытиях для окон и дверей. Как следует из названия, поливинилхлорид представляет собой полимер, состоящий из мономеров винилхлорида . Винилхлорид — это газ, получаемый при пропускании кислорода, хлористого водорода и этилена через медь, которая действует как катализатор .
Leave A Comment