Разделение пигментов методом бумажной хроматографии. Разделение пигментов по Краусу
Цель урока: расширить и углубить знания учащихся о способах разделения смесей, изучить химические свойства хлорофилла.
Задачи урока:
Образовательные: помочь детям систематизировать знания о методах разделения смесей, познакомить с химическими свойствами хлорофилла; научить применять знания в жизни.
Развивающие: (формирование и развитие образовательных компетенций):
а) учебно-познавательных: развитие навыков самостоятельной познавательной деятельности; умения ставить познавательную задачу (целеполагание), умения добывать знания, выделять главное, обобщать, делать выводы, проводить самопроверку и самооценку;
б) коммуникативных: навыков работы в паре, взаимодействия с другими людьми, умения ответить на поставленный вопрос;
в) информационных: проводить
материальное и знаковое моделирование, выделять
существенные признаки результата разделения
смесей, извлекать необходимую информацию из
проводимого эксперимента; оформлять и
представлять результаты своей работы.
Воспитательные: Воспитание жизненно необходимых качеств: воспитывать сознательное отношение к учебному труду, самостоятельности, работоспособности каждого для общего результата работы в группе, внимательности в выполнении нового вида деятельности, коллективизма; развивать интерес к знаниям.
Здоровьесберегающие: правила безопасного обращения с веществами.
Структура урока
I. Мотивация
Учитель: Очень – очень давно, еще в 10 в. до н.э.,
на дне Средиземного моря, вблизи Тира –
легендарного города в древней стране Финикии,
воздвигнутого на скале у побережья нынешней
Сирии, – люди ловили улиток – иглянок, так
называемых “багрянок ” вида Murex brandaris. и Murex trunculus,
живущих в водах Средиземного моря, у берегов
Сирии, Греции и Африки.
Сотням рабов приходилось из дня в день нырять за этими улитками в море. Другие рабы выдавливали их, растирали с солью и подвергали дальнейшей переработке, состоявшей из многих операций. Добытое вещество вначале было белым или бледно – желтым, но под действием воздуха и солнечного света постепенно становилось лимонно – желтым, затем зеленым и, наконец, приобретала великолепную фиолетово – красную окраску. Полученный пурпур чудесная краска, напоминавшая пламя, – в течение нескольких веков был самым ценным из всех красителей. Он был тогда символом власти – право носить окрашенные пурпуром одеяния было привилегией правителей и ближайших к ним знатных особ. Правители строго следили за тем, чтобы “императорский” (а позднее “кардинальский”) пурпур не появлялся на одеждах простолюдинов.
Окрашивание только одного квадратного метра
ткани красителем, добытым таким способом, стоило
баснословных средств. Ведь для получения одного
грамма пурпура нужно было обработать десять
тысяч улиток.
Ведь для получения одного
грамма пурпура нужно было обработать десять
тысяч улиток.
За 1500 лет до н. э. финикияне применяли пурпур для окраски тканей, ковров и вели в значительных размерах торговлю пурпуром. Столица Финикийского царства, г. Тир, был в то время основным центром производства пурпуровой краски. Методы ее получения финикияне заимствовали у египтян…
Ребята, скажите, пожалуйста, о чем повествует эта история ?
(Выделять нужные вещества из смесей и использовать их в своих целях люди умели очень давно)
В рассказанной истории ткани организма улиток – иглянок (Murex brandalis) содержали особый пигмент – пурпур. Что означает это слово?
Пигменты (лат. Pigmentum –краска) – это
окрашенные вещества тканей организма. Их
химическая природа различна. Они есть во всех
клетках и выполняют перенос кислорода и
углекислого газа.
Они могут служить светофильтрами, теплоизоляторами, маскировочным материалом, приспосабливая к среде организм тонко и гармонично.
Некоторые пигменты являются провитаминами: желто-оранжевые пигменты растений – каротиноиды и флавоноиды – предшественники витаминов А и Р .
Цвет пигментов зависит от особой группы атомов, поглащающих свет от определенной длины волны в видимой части спектра.
Эта часть молекулы пигмента называется хромофорной. В ней подвижные электроны легко переходят на энергетически более высокую орбиталь . Поэтому пигменты необходимы всюду, где один вид энергии превращается в другой. Животные и растения имеют немало сходно устроенных пигментов.
Хромопротеины – имеют в своем составе
комплекс белка, порфириновые кольца и металл.
Пигмент крови – гемоглобин – содержит в этом кольце атом железа, хлорофилл – магния.
Пигменты животных – меланины – коричневый, черный, желтый – окрашивают кожу, волосы, сетчатку глаза, покровы насекомых.
В мире нет практически чистых веществ, все вещества в своем составе имеют примеси. И все-таки, любые смеси можно разделить. Какие способы разделения веществ вы знаете?
– отстаивание
– фильтрование
– перекристаллизация
– декантация
– хроматография
Слово “хроматография” означает: “хромо” –
цвет, “графо” – пишу. В XIX веке чрезвычайное
интеллектуальное удовлетворение ученым
доставило обнаружение смысла зеленой окраски
растений. Оказывается, растения поглощают свет и
поглощенную энергию используют для синтеза
питательных веществ! Нужно было выделить и
очистить пигменты зеленого листа – хлорофиллы. А
они так близки по свойствам, что разделить их не
удавалось.
Михаил Семёнович Цвет является творцом этого метода анализа, открывшего широчайшие возможности для тонкого химического исследования. В XIX веке чрезвычайное интеллектуальное удовлетворение ученым доставило обнаружение смысла зеленой окраски растений. Оказывается, растения поглощают свет и поглощенную энергию используют для синтеза питательных веществ! Нужно было выделить и очистить пигменты зеленого листа – хлорофиллы. А они так близки по свойствам, что разделить их не удавалось.
Михаил Семенович Цвет бился над задачей
разделения пигментов зеленого листа. Он взял
стеклянную трубку, наполнил ее порошком мела и на
верхний слой налил немного спиртового экстракта
листьев. Экстракт был буро-зеленого цвета, и
такого же цвета стал верхний слой меловой
колонки. А затем Михаил Семенович начал по каплям
лить сверху в трубку с мелом чистый спирт. Капля
за каплей очередная его порция растворяла
пигменты с крупинок мела, передвигаясь вниз по
трубке.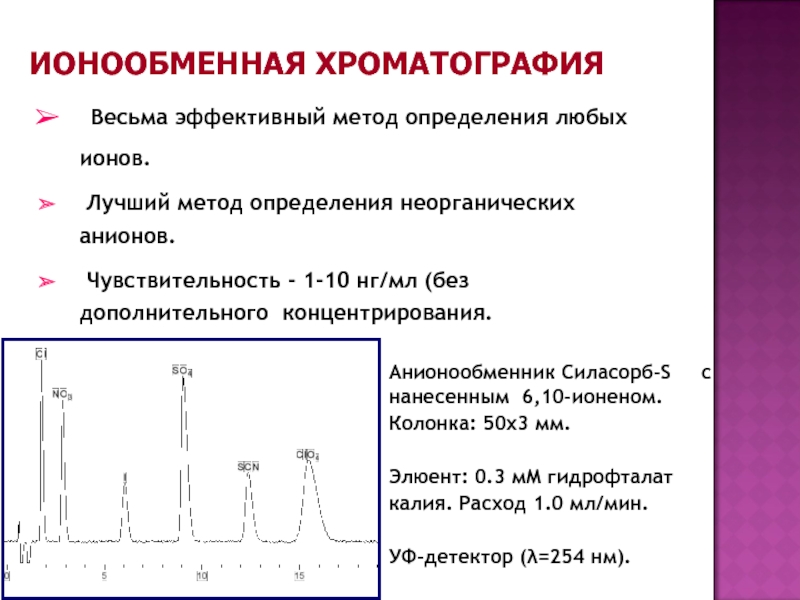
(Трудно удержаться от улыбки: Цвет – хромос, хроматограмма – цветограмма.)
Метод был так странно прост, что большая часть современников или не восприняла это удивительное открытие, или, что еще печальнее, резко восстала против его автора.
Молчание длилось почти 30 лет…
II. Целеполагание
Сегодня, ребята, вам предстоит освоить
два способа разделения пигментов.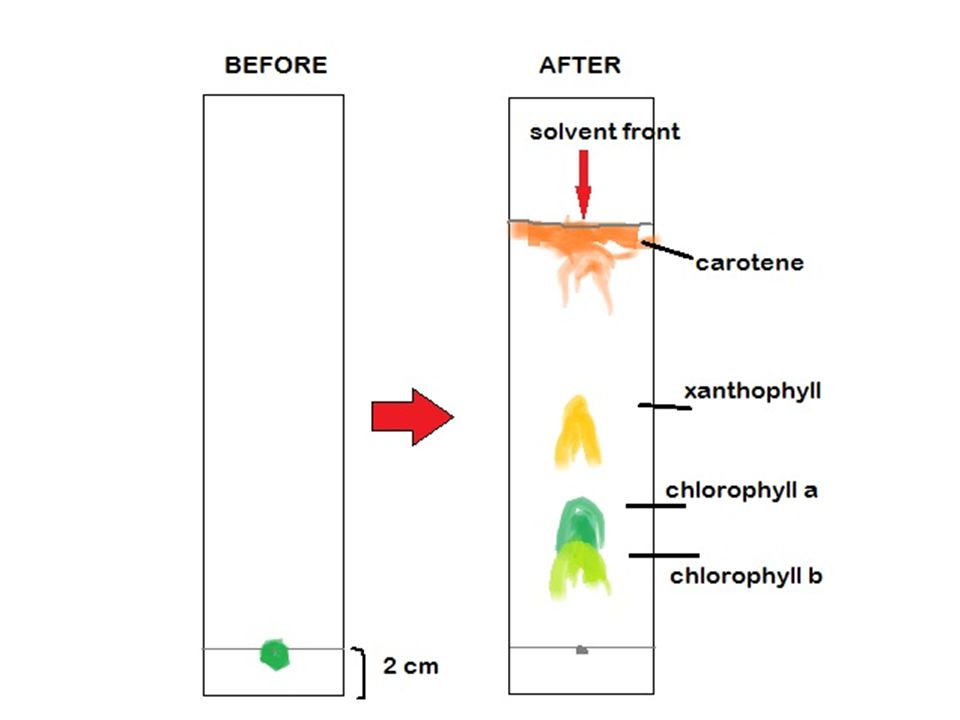 Давайте
представим, что вы сегодня проводите небольшой
научный эксперимент по выделению пигментов из
растений . Но прежде чем вы начнете работу, четко
определите для себя:
Давайте
представим, что вы сегодня проводите небольшой
научный эксперимент по выделению пигментов из
растений . Но прежде чем вы начнете работу, четко
определите для себя:
Расширить и углубить наши представления о пигментах как особых веществах живой клетки, способах разделения смесей, о способах выделения из смеси нужного вещества.
– Кроме того, каждая группа формулирует для себя:
- рабочую гипотезу
- ожидаемый результат
(Ученикам приходилось и ранее делать подобное; если же на уроке учитель впервые дает задание сформулировать гипотезу и предположить результат – этот момент тщательно прорабатывается учителем; учитель поясняет, что такое гипотеза и как ее правильно сформулировать)
Каждой группе после выполнения работы
будет представлено слово для отчета о
выполненной работе и ее результатах.
Учитель:
– Для начала познакомьтесь с инструкцией по выполнению работы, которая находится у вас на рабочем столе. Помните о технике безопасности при работе с химическими реактивами.
III. Работа с инструкционной картой и выполнение практической части урокаАлгоритм работы в группе:
(раздается каждой группе на рабочий стол)
- Внимательно изучи инструктивную карту.
- Обратись к учителю за пояснениями, если что-либо непонятно.
- Сформулируй гипотезу и предположи результат работы.
- Выполни работу.
- На хроматограмме определи типы пигментов и отметь их расположение.
- Составь по работе отчет и пoдготовь выступление.
По всем неясным вопросам, возникающим во время работы не стесняйся обращаться за помощью к учителю !Удачи !
ИНСТРУКЦИЯ ПО ВЫПОЛНЕНИЮ ПРАКТИЧЕСКОЙ РАБОТЫ
(Раздается каждой группе на рабочий стол)
1. РАЗДЕЛЕНИЕ ПИГМЕНТОВ ПО КРАУСУ
РАЗДЕЛЕНИЕ ПИГМЕНТОВ ПО КРАУСУ
“Нет ничего практичнее хорошей теории”
Роберт Кирхгоф, нем. физик
Метод основан на различной растворимости пигментов в спирте и бензине. Сродство пигментов к полярным (спирт, ацетон) и неполярным (бензин) растворителям определяется степенью их полярности.
Ксантофиллы, содержащие две или более полярные группы, хорошо растворимы в спирте, в то время как каротин отличается более высоким сродством к бензину. Фитольный остаток в молекуле хлорофилла представляет собой ее гидрофобную часть и обуславливает возможность взаимодействия молекулы пигмента с бензином. Удаление фитола при омылении хлорофилла увеличивает сродство пигмента к полярным растворителям.
ХОД РАБОТЫ
Убедиться в том, что в спиртовой вытяжке наряду
с хлорофиллом присутствуют жёлтые пигменты,
можно, используя их различную растворимость в
спирте и бензине. Из пигментов группы
каротиноидов в хлоропластах находится
преимущественно жёлто-оранжевый каротин и
золотисто-жёлтый ксантофилл. Все пигменты можно
выделить из листа спиртом, но растворимость
хлорофилла и каротина в бензине выше, чем в
спирте. Ксантофилл в бензине не растворяется.
Из пигментов группы
каротиноидов в хлоропластах находится
преимущественно жёлто-оранжевый каротин и
золотисто-жёлтый ксантофилл. Все пигменты можно
выделить из листа спиртом, но растворимость
хлорофилла и каротина в бензине выше, чем в
спирте. Ксантофилл в бензине не растворяется.
Методика проведения опыта:
В пробирку налейте 2 – 3 мл вытяжки, столько же бензина и 1 – 2 капли воды. Закрыв пальцем пробирку, взболтайте в течение 2 – 3 мин. Через некоторое время жидкость разделится на 2 слоя: бензин, как более легкий, окажется наверху, спирт – внизу. Оба слоя приобрели различную окраску: бензиновый – зеленую, спиртовой – жёлтую. Жёлтый цвет спиртовому раствору придает пигмент ксантофилл. В бензиновом слое находятся 2 пигмента: хлорофилл и каротин, который не заметен из-за интенсивно-зеленого цвета хлорофилла.
Действие щелочи на хлорофилл.
По химическому составу хлорофилл представляет
сложный эфир дикарбоновой кислоты хлорофиллина. Хлорофиллин представляет собой азотосодержащее
металлоорганическое соединение, относящееся к
магний-порфиринам. В центре молекуле хлорофилла
расположен атом магния, который соединён с
четырьмя азотами пиррольных группировок. В
пиррольных группировках хлорофилла имеется
система чередующихся двойных и простых связей.
Это и есть хромофорная группа хлорофилла,
обуславливающая его окраску.
Хлорофиллин представляет собой азотосодержащее
металлоорганическое соединение, относящееся к
магний-порфиринам. В центре молекуле хлорофилла
расположен атом магния, который соединён с
четырьмя азотами пиррольных группировок. В
пиррольных группировках хлорофилла имеется
система чередующихся двойных и простых связей.
Это и есть хромофорная группа хлорофилла,
обуславливающая его окраску.
При взаимодействии сложных эфиров со щелочами (реакция омыления) происходит разрыв сложноэфирных связей с образованием соли данной кислоты и спиртов. В результате реакции омыления образуется соль хлорофиллина и 2 спирта: метиловый и фитол.
Методика выполнения эксперимента:
Налейте в пробирку 2 – 3 мл спиртовой вытяжки
пигментов, добавьте 4 – 5 капель 20%-ного раствора
щелочи и взболтал смесь. Произошла реакция
взаимодействия хлорофилла со щелочью. Цвет
раствора не изменился, так как соли хлорофиллина
имеют зеленую окраску. Затем добавьте бензин,
чтобы общий объем жидкости в пробирке увеличился
в 2 раза, взболтайте и дайте отстояться.
Цвет
раствора не изменился, так как соли хлорофиллина
имеют зеленую окраску. Затем добавьте бензин,
чтобы общий объем жидкости в пробирке увеличился
в 2 раза, взболтайте и дайте отстояться.
Нижний спиртовой слой окрасился в зеленый цвет благодаря присутствию в нём натриевой соли хлорофиллина, которая, в отличие от хлорофилла, в бензине не растворима. Здесь же, в спиртовом слое, находился пигмент ксантофилл, но его окраска маскируется интенсивно зелёным цветом натриевой соли хлорофиллина. Верхний слой бензина окрашен в жёлтый цвет пигментом каротином.
Опыты по разделению пигментов спиртовой вытяжки листа показывают, что она содержит два жёлтых пигмента: каротин и ксантофилл. Количественное соотношение их в растениях примерно равное.
Химические свойства хлорофилла
Наличие магния можно легко обнаружить. Для
этого надо подействовать на спиртовую вытяжку
хлорофилла слабым раствором соляной или
какой-либо другой кислоты. При этом произойдёт
изменение окраски – вытяжка приобретает
жёлто-бурый оттенок. Хлорофилл без магния
получил название феофитина.
При этом произойдёт
изменение окраски – вытяжка приобретает
жёлто-бурый оттенок. Хлорофилл без магния
получил название феофитина.
В молекуле феофитина сравнительно легко ввести обратно какой-нибудь металл и восстановить металлоорганическую связь. Для этого к раствору феофитина прибавляют ацетат меди или ацетат цинка и нагревают. Цинк или медь входят в молекулу хлорофилла, и вытяжка становится опять зелёного цвета.
Методика проведения эксперимента:
- В пробирку со спиртовой вытяжкой хлорофилла добавьте разбавленный раствор соляной кислоты (1:20) до изменения цвета спиртовой вытяжки (бурый оттенок). Образовался феофитин. (Спиртовая вытяжка – 5 мл, соляная кислота – 25 капель). Пробирку необходимо постоянно встряхивать.
- К раствору феофитина, полученному в первом
опыте добавьте кристаллический ацетат цинка 0,1 г
(избыток) и нагрейте на водяной бане в течение 5
минут.
 Раствор приобрел опять зелёное
окрашивание. Образовался хлорофилл.
Раствор приобрел опять зелёное
окрашивание. Образовался хлорофилл.
2. РАЗДЕЛЕНИЕ КРАСИТЕЛЕЙ ИЗ РАСТЕНИЙ МЕТОДОМ БУМАЖНОЙ ХРОМАТОГРАФИИ.
Вначале приготовьте раствор красителя. Для бумажной хроматографии его понадобиться менее 10-15 капель. Достаточно растереть два маленьких листочка и для извлечения из них красящих веществ добавить 2 мл пропанона (ацетона).
Выберем восходящую хроматографию.
Вырежьте из бумаги полоску шириной 1 см. На одном
конце сделайте полоску поуже, чтобы получился
вытянутый “язычок”. Над тем местом, где полоска
начинает сужаться, простым карандашом нанесите
линию старта. На середину этой линии нанесите
одну за другой несколько капель приготовленной
вытяжки хлорофилла. Каждую следующую каплю можно
наносить только после того, как высохнет
предыдущая, и нужно следить, чтобы пятно на
старте не получилось слишком большим. Поэтому
раствор нанесем на бумагу пипеткой с тонко
оттянутым концом. Для ускорения высушивания
можно поместить полоску на нагретый кусок
листового металла или асбеста, либо выдержать ее
в сушильном шкафу. Капли нужно наносить до
образования на линии старта пятна интенсивного
зеленого цвета. Подвесьте полоску бумаги в
пробирке так, чтобы язычок на 1 см был погружен в
растворитель (петролейный эфир, толуол, бензин).
Под действием капиллярных сил растворитель
будет подниматься по бумаге, а вместе с ним будут
подниматься и красители. Но продвигаться по
бумаге они будут с различной скоростью.
Поэтому
раствор нанесем на бумагу пипеткой с тонко
оттянутым концом. Для ускорения высушивания
можно поместить полоску на нагретый кусок
листового металла или асбеста, либо выдержать ее
в сушильном шкафу. Капли нужно наносить до
образования на линии старта пятна интенсивного
зеленого цвета. Подвесьте полоску бумаги в
пробирке так, чтобы язычок на 1 см был погружен в
растворитель (петролейный эфир, толуол, бензин).
Под действием капиллярных сил растворитель
будет подниматься по бумаге, а вместе с ним будут
подниматься и красители. Но продвигаться по
бумаге они будут с различной скоростью.
Медленнее всех поднимается желто-зеленый хлорофилл b, быстрее – ксантофилл и еще быстрее сине-зеленый хлорофилл а. С фронтом растворителя поднимается желтый или оранжевый каротин. После высушивания язычок бумажной полоски погружают в 2Н cоляную кислоту.
IV.
 Обсуждение результатов
эксперимента
Обсуждение результатов
эксперимента
Примерный план отчета
(Раздается каждой группе)
– Что изучалось?
(Постановка проблемы исследования, цели и задачи).
– Как изучалось?
(Описание методов исследования)
– Какие результаты были получены?
(Основные выводы).
После выполнения экспериментальной части работы ребята работают с полученными хроматограммами, находят каждый из пигментов на своей хроматограмме и выступают с отчетами о своей работе. Хроматограммы прилагаются в отчете.
Работая самостоятельно в группах, ребята разработали каждая свою гипотезу, цели и задачи работы, ожидаемый результат.
Так, одна из групп предложила следующее:
Цель: Разделить пигменты методом хроматографии
на бумаге и при помощи двух несмешивающихся
жидкостей.
Задачи:
- Вспомнить все способы разделения смесей.
- Научиться готовить вытяжку из листьев растений.
- Отработать навыки разделения пигментов различными способами.
- Научиться анализировать хромотограммы.
- Отметить на хроматограмме типы пигментов.
- Оценить совершенную работу и полученный результат.
Гипотеза:
Если мы выделим и разделим пигменты растений, то мы установим, какие типы пигментов содержат данные нам растения.
Ожидаемый результат:
Получить хроматограммы с разными типами пигментов.
Следующая группа предложила свой вариант:
Цель: Научиться различным способам разделения пигментов, в частности – при помощи несмешивающихся жидкостей и на специальной хромотографической бумаге.
Задачи:
- Усвоить способ получения вытяжки пигментов из растений.
- Научить распознавать типы пигментов.

- Научиться анализировать хроматограмму.
- Научиться читать хроматограмму.
Гипотеза:
Если мы получим хроматограмму, то, прочитав ее, мы сможем выяснить, какие пигменты есть в растении.
Ожидаемые результаты:
Выделить и получить пигменты, содержащиеся в растении.
V. Рефлексия урока
Учитель задает вопросы ученикам:
– Что вас удивило? Что интересного заметили? Какие вы видите факты?
– Вы смогли выполнить задание? В чем затруднение?
– Вы смогли выполнить задание? Почему не получается? Чем это задание похоже на предыдущее?
– Что вы хотели сделать? Какие знания применили? Задание выполнено?
– Что на уроке было самым интересным?
– Что вызывало затруднения?
– Что у вас вызвало удивление?
– Какие вы выскажите пожелания учителю и друг другу?
– Как вы оцениваете свою работу?
Ребята высказывают свои мнения и пожелания.
Список использованной литературы:
- Энциклопедический словарь юного химика. Москва. «Педагогика». 1990.
- Э. Гроссе. Х. Вайсмантель. Химия для любознательных. Ленинград. «Химия». Ленинградское отделение. 1987 год.
- В.И. Астафуров. Основы химического анализа. Москва. Просвещение. 1983 год.
- А.П.Крешков Основы аналитической химии, – Москва, “Химия”, 1970
- И.И.Грандберг Органическая химия, – Москва, “Дрофа”, 2002
- Н.В.Батурицкая, Т.Д.Фенчук Удивительные опыты с растениями, – Минск, “Народная асвета”, 1991, с. 54 – 61.
- Э.Е.Нифантьев, М.К.Верзилина, О.С.Котлярова Внеклассная работа по химии с использованием хроматографии, – Москва, “Просвещение”, 1983, с.7 – 8.
Презентация
ХРОМАТОГРАФИЯ — ПРОСТОЙ СПОСОБ АНАЛИЗА СЛОЖНЫХ ВЕЩЕСТВ
В 1997 году торжественно отмечалось 125-летие со дня рождения выдающегося
русского химика Михаила Семеновича Цвета, открывшего и впервые применившего
принципиально новый метод исследований — хроматографию. Она стала в наши
дни незаменимым методом разделения и анализа сложных веществ. С ее помощью
удалось, в частности, разобраться в сложностях строения и состава белковых
соединений, получить многие трансурановые элементы периодической системы
Менделеева, разделять и очищать антибиотики, витамины, алкалоиды и гормоны.
Хроматографические явления составляют основу многих природных геохимических
процессов, вроде образования почвы и многих рудных месторождений.
Она стала в наши
дни незаменимым методом разделения и анализа сложных веществ. С ее помощью
удалось, в частности, разобраться в сложностях строения и состава белковых
соединений, получить многие трансурановые элементы периодической системы
Менделеева, разделять и очищать антибиотики, витамины, алкалоиды и гормоны.
Хроматографические явления составляют основу многих природных геохимических
процессов, вроде образования почвы и многих рудных месторождений.
Михаил Семенович Цвет родился 14 мая 1872 года.
Первый опыт по разделению и анализу вещества сложного состава, проделанный Михаилом Семеновичем Цветом в 1903 году, был удивительно простым.
Для исследования сложных химических веществ и соединений применяется целый ряд очень точных физических методов.
Масс-спектроскопия. Исследуемое вещество испаряется при высокой температуре и превращается в поток ионов.
Простейшую хроматограмму можно получить и самому, разделив на листке фильтровальной бумаги смесь разноцветных чернил или анилиновых красок.
Рентгеновская спектроскопия.
Хроматография.
Хроматограмма смеси нескольких сахаров: 1 — рамноза, 2 — ксилоза, 3 — фруктоза, 4 — глюкоза, 5 — сахароза, 6 — мальтоза, 7 — лактоза. Их молекулы различаются по структуре, числу атомов и массе.
Жидкостный хроматограф фирмы «Bruker».
‹
›
Открыть в полном размере
Михаил Семенович Цвет заинтересовался природой хлорофилла, который делает листья зелеными. Роль этого вещества в природе огромна: с его помощью в живом листе световая энергия Солнца превращается в химическую энергию органических соединений.
Профессор Цвет насыпал в стеклянную трубку тонко измельченный порошок
чистого мела, смочил его бензолом, налил сверху немножко раствора хлорофилла,
извлеченного из свежего листа (самый верхний слой порошка, конечно, сразу
окрасился в зеленый цвет), и стал медленно, по каплям подливать в трубочку
с мелом бензол. По мере того как окрашенный слой промывался бензолом, зеленое
колечко вслед за растворителем начало передвигаться вниз по трубке. Потом
(в этом-то и заключалось замечательное открытие Цвета) оно стало постепенно
разделяться. Появилась узкая желтая полоска, она двигалась по трубке наиболее
медленно, ее опередила желто-зеленая полоса, перед которой шла широкая
зелено-синяя полоса, две желтые и в самом низу двигалась еще одна полоса,
тоже желтого цвета. Тщательный анализ показал, что над верхней желтой полоской
располагалась еще одна — бесцветная. Своим опытом Цвет доказал, что хлорофилл
имеет сложное строение, и эта работа легла в основу новой науки.
Потом
(в этом-то и заключалось замечательное открытие Цвета) оно стало постепенно
разделяться. Появилась узкая желтая полоска, она двигалась по трубке наиболее
медленно, ее опередила желто-зеленая полоса, перед которой шла широкая
зелено-синяя полоса, две желтые и в самом низу двигалась еще одна полоса,
тоже желтого цвета. Тщательный анализ показал, что над верхней желтой полоской
располагалась еще одна — бесцветная. Своим опытом Цвет доказал, что хлорофилл
имеет сложное строение, и эта работа легла в основу новой науки.
Компоненты вещества, подобно световым лучам в спектре, расположились друг за другом в столбе порошка в виде окрашенных полос. Это явление было названо хроматограммой, а сам метод исследования — хроматографией, от греческих слов «хроматос» — окраска, «грамма» — считывание и «графия» — запись.
Что же происходило в «хроматографической колонне» — стеклянной трубочке, набитой порошком мела?
Зеленый раствор вытяжки из листьев обесцвечивается, как только приходит
в соприкосновение с порошком мела, а мел становится зеленым. Молекулы всех
соединений, входящих в состав хлорофилла, извлеченного из листа, осаждаются
на поверхности частиц мела. Поглощение растворенно го вещества, паров или
газов поверхностью твердых тел или жидкостью химики называют сорбцией,
а вещества-поглотители — сорбентом. На этом явлении и основаны все хроматографические
методы разделения смесей, сверхтонкой очистки вещества и анализа.
Молекулы всех
соединений, входящих в состав хлорофилла, извлеченного из листа, осаждаются
на поверхности частиц мела. Поглощение растворенно го вещества, паров или
газов поверхностью твердых тел или жидкостью химики называют сорбцией,
а вещества-поглотители — сорбентом. На этом явлении и основаны все хроматографические
методы разделения смесей, сверхтонкой очистки вещества и анализа.
Захваченные поверхностью твердого тела — сорбента молекулы могут переходить обратно в раствор — элюент, снова поглощаться и вновь растворяться, бесчисленное множество раз меняя свое состояние. Между раствором (бензолом в опытах Цвета) и сорбентом (порошком мела) устанавливается равновесие: на поверхности частиц мела находятся почти все молекулы, а в растворе почти совсем нет. Но в этом-то «почти» и заключается сущность хроматографического эффекта.
Немногие молекулы, находящиеся в растворе, увлекаются вниз по трубке
вместе с потоком растворителя. Но по пути они медленно осаждаются вновь
на другие частицы мела, а вместо них переходят в раствор новые молекулы.
Поток растворителя непрерывно поступает сверху в трубку. В верхней части
сорбированного вещества становится все меньше и меньше, в нижней части
— все больше и больше. Постепенно цветная прослойка продвигается в виде
колечек через сорбент вниз по трубке.
Но по пути они медленно осаждаются вновь
на другие частицы мела, а вместо них переходят в раствор новые молекулы.
Поток растворителя непрерывно поступает сверху в трубку. В верхней части
сорбированного вещества становится все меньше и меньше, в нижней части
— все больше и больше. Постепенно цветная прослойка продвигается в виде
колечек через сорбент вниз по трубке.
Молекулы с разным составом или строением осаждаются (сорбируются) на твердой поверхности по-разному. Одни — прикрепляются немного прочнее, другие — несколько слабее. Одни — дольше находятся в связанном состоянии и меньше в растворе; другие — чуть дольше задерживаются в растворе и быстрее увлекаются потоком растворителя.
Поэтому окрашенная смесь различных веществ постепенно разделяется на
составные части. И каждая такая часть сосредотачивается в своем слое. Двигаясь
с разной скоростью вдоль трубки, эти слои расходятся все дальше друг от
друга — образуется хроматограмма.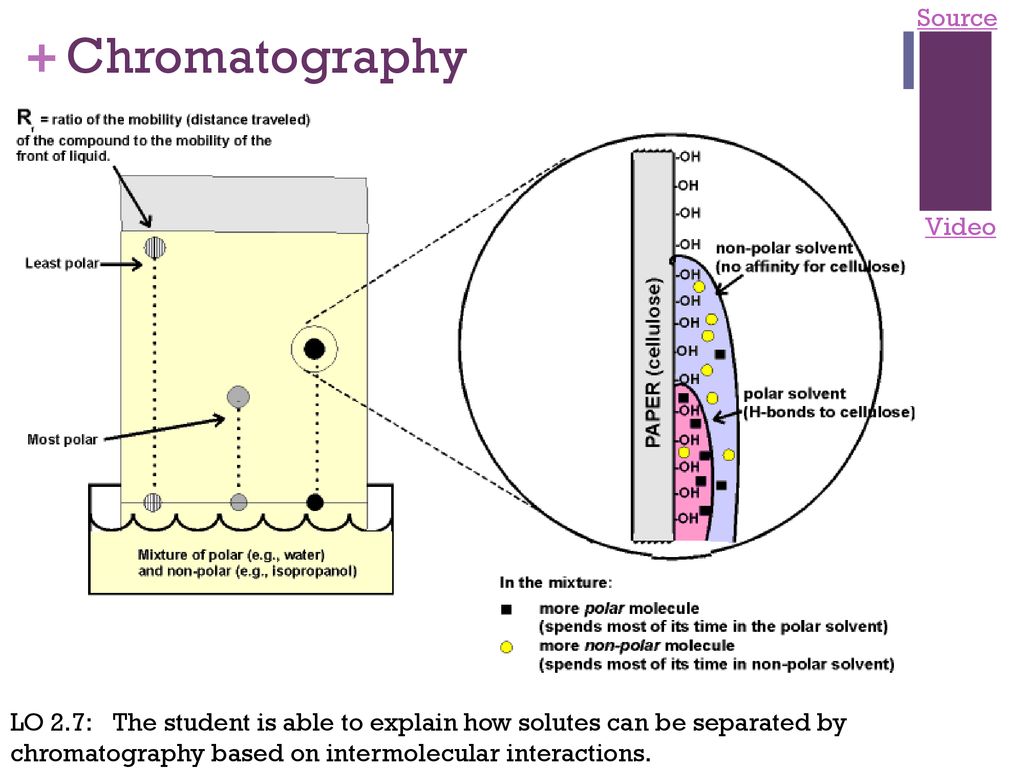 Каждое отдельное цветное кольцо соответствует
какому-то одному химическому соединению.
Каждое отдельное цветное кольцо соответствует
какому-то одному химическому соединению.
Столбик сорбента из трубки можно либо разрезать на слои и получить их отдельно в чистом виде, либо, продолжая промывку бензолом, собирать раствор от каждого цветного слоя отдельно, по мере того как они выходят из колонны с потоком растворителя.
Это напоминает забег на дистанцию спортивных команд в разноцветных костюмах. Те, кто использует для «передышки» на участках дистанции (колонны) меньше времени, окажутся впереди, а кто отдыхал дольше — в середине или позади. Так и растягивается эта цепь «микробегунов» по всей длине колонны. Или другая похожая аналогия: как скорость забега спортсменов зависит от состояния их здоровья и физических возможностей, так и скорость движения компонентов вещества по колонне находится в зависимости от размеров молекул и их химической природы.
Бесцветные вещества обнаруживают, освещая их ультрафиолетом, под действием
которого очень многие соединения флюоресцируют, или «проявляют», обработав
реактивом, который их окрашивает.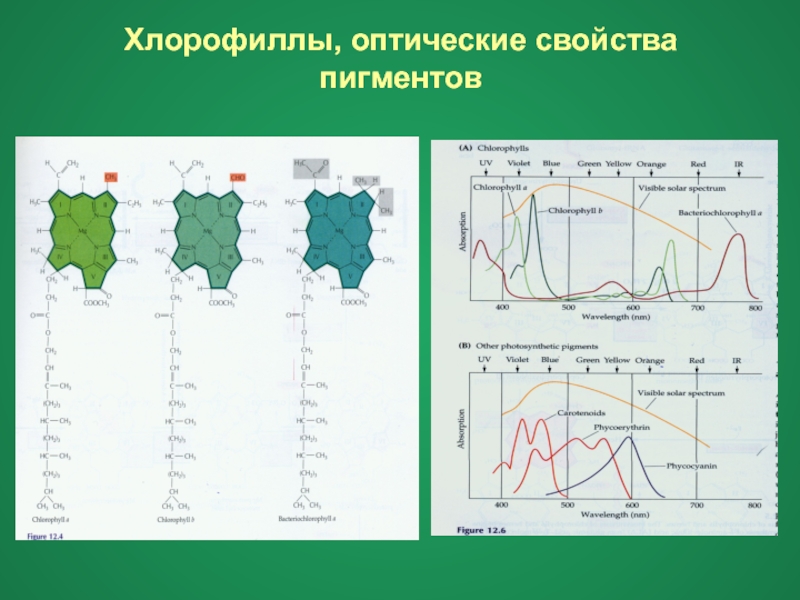
Среди новых методов анализа наиболее часто используется газожидкостная хроматография. Сорбентом в ней служит нелетучая жидкость, которой смочена, например, растертая в порошок керамика (иногда — обыкновенный кирпич), а движущейся средой — любой инертный газ. При помощи этого метода исследуют сложные смеси, содержащие сотни компонетов.
Система их разделения удивительно проста: все происходит в тоненькой
металлической или пластмассовой трубочке диаметром 0,2-0,4 мм. Чтобы достичь
высокой степени разделения, трубочку приходится делать очень длинной. Скажем,
для анализа земляничного аромата (воздуха, окружающего ягоды) потребовалась
колонна длиной 120 метров. Свернутую в спираль трубку помещали в термостат,
температура в котором постепенно повышалась. Это было необходимо для того,
чтобы изучить и те компоненты земляничного запаха, которые ягода выделяет
только в жаркий солнечный день. Через колонну пропускали аргон, облученный
радиоактивным источником. Радиоактивный газ ионизовал органические вещества,
порождая электрический сигнал, который после усиления подавался на записывающее
устройство. Чувствительность такого прибора очень велика и сравнима со
спектральным и масс-спектрометрическим методами анализа: он обнаруживает
одну тысячную часть миллиардной доли грамма вещества (10-12
г). А всего для полного анализа достаточно нескольких миллиграммов смеси.
Радиоактивный газ ионизовал органические вещества,
порождая электрический сигнал, который после усиления подавался на записывающее
устройство. Чувствительность такого прибора очень велика и сравнима со
спектральным и масс-спектрометрическим методами анализа: он обнаруживает
одну тысячную часть миллиардной доли грамма вещества (10-12
г). А всего для полного анализа достаточно нескольких миллиграммов смеси.
Запах свежей земляники оказался очень сложным. Чтобы создать аромат ее спелых ягод, в маленькой «лаборатории» растения синтезируется не менее девяноста шести сложнейших органических душистых соединений.
Чтобы изучить состав нефти, потребовалось сконструировать хроматографическую колонну длиной около полукилометра. На ней удалось не только установить число различных компонентов сырой нефти (их оказалось около шестисот), но и расшифровать формулу каждого из них.
Хроматограммы получают и на бумажных полосках. Такую полоску подвешивают
вертикально и нижний ее конец погружают в сосудик с растворителем. Впитываясь
в бумагу и поднимаясь по ней вверх, растворитель с разной скоростью перемещает
отдельные составные части из смеси. На бумажном листе образуется хроматограмма
— цветные полосы. По их положению и окраске можно определить, что входит
в состав изучаемого вещества. Трудноразделимые смеси часто обрабатывают
дважды, разными растворителями и пропускают в двух взаимно перпендикуляр
ных направлениях, получая двухмерную хроматограмму.
Такую полоску подвешивают
вертикально и нижний ее конец погружают в сосудик с растворителем. Впитываясь
в бумагу и поднимаясь по ней вверх, растворитель с разной скоростью перемещает
отдельные составные части из смеси. На бумажном листе образуется хроматограмма
— цветные полосы. По их положению и окраске можно определить, что входит
в состав изучаемого вещества. Трудноразделимые смеси часто обрабатывают
дважды, разными растворителями и пропускают в двух взаимно перпендикуляр
ных направлениях, получая двухмерную хроматограмму.
Очень похожа на бумажную хроматография в тонком слое. На стеклянную
или пластмассовую пластинку наносят тонкий равномерный слой хорошо измельченного
сорбента. Сам процесс хроматографического разделения идет так же, как и
на бумаге. Тонкослойная хроматография обладает существенными преимуществами:
разделение протекает значительно быстрее, а главное, легче выбрать наиболее
подходящие сорбенты.
Хроматограммы позволили не только понять, из каких составных частей — аминокислот — состоит белок различных живых организмов, но и определить порядок их чередования в молекуле белка. А расшифровав состав табачного дыма, выяснили, что он состоит из сотни различных соединений, в том числе канцерогенных, вызывающих раковые заболевания.
С помощью хроматографии легко устанавливается факт применения спортсменами возбуждающих средств — допингов: достаточно взять на анализ капельку крови, чтобы определить их присутствие.
Еще более перспективен метод ионообменной хроматографии. Он отличается от способа М. С. Цвета тем, что вместо нейтрального сорбента — мела, крахмала, угля — применяются полимерные вещества — ионообменные смолы. Каждая крупинка такого сорбента — как бы гигантская молекула кислоты (смолы-катионита) или основания (смолы-анионита) — вступает в реакцию ионного обмена.
Ионообменные смолы нерастворимы.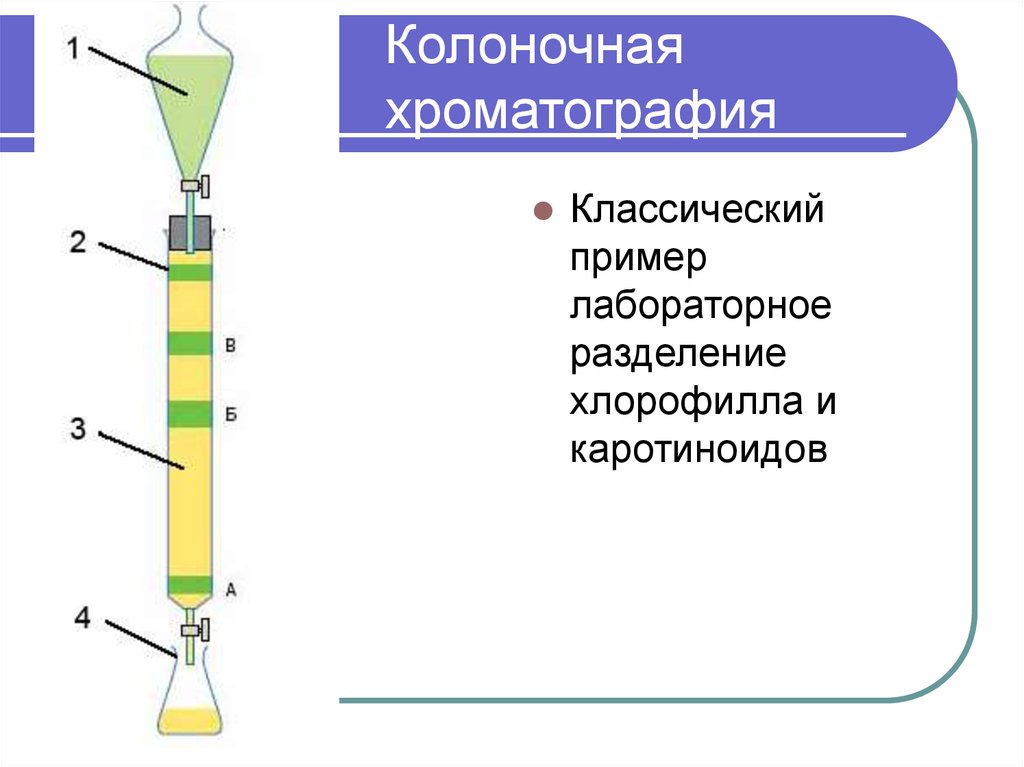 Тонкий порошок такой смолы в хроматографической
колонне поглощает ионы тяжелых металлов из раствора, замещая их на кислоту
или щелочь. Так, например, готовят воду для питания паровых котлов на больших
тепловых электростанциях. Вода очищается от ила и песка и поступает в колонну,
наполненную катионитовой смолой. В ней полностью поглощаются соли кальция
и магния, делающие воду «жесткой», вместо них появляются ионы водорода
— образуется кислота. Подкисленная вода проходит колонну, в которой анионы
образовавшихся кислот нейтрализуются, и получается чистая вода. Ионообменные
смолы превращают даже соленую морскую воду в пресную, пригодную для питья,
и извлекают ценные металлы из промышленных сточных вод.
Тонкий порошок такой смолы в хроматографической
колонне поглощает ионы тяжелых металлов из раствора, замещая их на кислоту
или щелочь. Так, например, готовят воду для питания паровых котлов на больших
тепловых электростанциях. Вода очищается от ила и песка и поступает в колонну,
наполненную катионитовой смолой. В ней полностью поглощаются соли кальция
и магния, делающие воду «жесткой», вместо них появляются ионы водорода
— образуется кислота. Подкисленная вода проходит колонну, в которой анионы
образовавшихся кислот нейтрализуются, и получается чистая вода. Ионообменные
смолы превращают даже соленую морскую воду в пресную, пригодную для питья,
и извлекают ценные металлы из промышленных сточных вод.
На ионообменной колонне смогли разделить смесь изотопов редкоземельных
элементов. Радиоактивность каждой капли раствора, вытекающего из колонны,
измерялась отдельно. Оказалось, что чем выше порядковый номер элемента,
тем быстрее он выходит из колонны при хроматогра фическом разделении. И
чередование элементов удивительным образом точно соответствует их взаимному
положению в периодической системе элементов: америций (№ 95), кюрий (№
96), берклий (№ 97) и калифорний (№ 98).
И
чередование элементов удивительным образом точно соответствует их взаимному
положению в периодической системе элементов: америций (№ 95), кюрий (№
96), берклий (№ 97) и калифорний (№ 98).
Метод, созданный М. С. Цветом 95 лет назад, сегодня применяют во всех областях науки и техники. Он не устарел, и его возможности далеко не исчерпаны.
Физпрактикум
ХРОМАТОГРАММА НА ПРОМОКАШКЕ
Попробуем самостоятельно получить бумажную хроматограмму, разделив на компоненты жидкость сложного состава. Для этого нам понадобится по нескольку капель разноцветных чернил, краски или туши и лист промокательной или фильтровальной бумаги.
Смешаем чернила, получив темную жидкость неопределенного цвета. Нанесем капельку жидкости в центр бумажного листа. Затем точно в середину цветного пятнышка начнем по каплям приливать чистую воду. Каждую каплю нужно вносить только после того, как впитается предыдущая.
Вода играет роль элюэнта, переносящего исследуемое вещество по сорбенту — пористой бумаге. Вещества, входящие в состав смеси, поглощаются бумагой по-разному: одни хорошо удерживаются ею, а другие впитываются медленнее и продолжают некоторое время растекаться вместе с водой. Вскоре по листу бумаги начнет расползаться настоящая красочная хроматограмма: пятно одного цвета в центре, окруженное разноцветными концентрическими кольцами. Так можно получить самые разнообразные, очень красочные узоры.
Вещества, входящие в состав смеси, поглощаются бумагой по-разному: одни хорошо удерживаются ею, а другие впитываются медленнее и продолжают некоторое время растекаться вместе с водой. Вскоре по листу бумаги начнет расползаться настоящая красочная хроматограмма: пятно одного цвета в центре, окруженное разноцветными концентрическими кольцами. Так можно получить самые разнообразные, очень красочные узоры.
Хроматография хлорофилла: Значение | StudySmarter
Когда вы в последний раз ходили в парк, обращали ли вы внимание на цвет листьев? Разные растения имеют немного разную окраску листьев. Некоторые красноватые, а другие темно-зеленоватые. Вы когда-нибудь задумывались, почему это так? Листья содержат уникальные пигменты, которые поглощают свет и используют энергию для фотосинтеза. Различные растения имеют разные пропорции этих пигментов, что придает им особый цвет. В этой статье мы узнаем о хлорофилловая хроматография , метод, используемый для разделения пигментов, содержащихся в растениях.
Что означает хроматография на хлорофилле?
Чтобы понять значение хлорофилловой хроматографии , необходимо сначала понять концепцию хроматографии .
Возможно, вы уже знакомы с этим процессом, но давайте кратко повторим его.
Хроматография — это процесс, в котором различные химические соединения в смеси разделяются на основе определенных свойств.
В этом процессе две основные фазы должны находиться во взаимодействии: подвижная фаза и стационарная фаза . Чтобы начать процесс хроматографии, смесь растворяют в растворителе . Это подвижная фаза , поскольку она может транспортировать растворенные в ней химические соединения через второе вещество , известное как стационарная фаза .
различных компонента смеси обладают другими свойствами, такими как размер , заряд , растворимость и pH , которые заставляют их перемещаться с различными скоростями через стационарную фазу. Следовательно, они вынуждены отделять друг от друга. Конкретные подвижные и неподвижные фазы определяют, будут ли химические вещества двигаться быстрее или медленнее и как они разделяются на основе свойств компонента.
Следовательно, они вынуждены отделять друг от друга. Конкретные подвижные и неподвижные фазы определяют, будут ли химические вещества двигаться быстрее или медленнее и как они разделяются на основе свойств компонента.
Хлорофиллы и каротиноиды
Растения могут использовать солнечную энергию и использовать ее для фиксации двуокиси углерода (CO 2 ) в простых сахаров . Это делается с помощью процесса, с которым вы, возможно, знакомы, фотосинтеза .
Фотосинтез происходит в хлоропластах, находящихся внутри растительных клеток.
Клетки мезофилла в листьях часто имеют наибольшее количество хлоропластов и, следовательно, являются видных фотосинтезирующих клеток в растении. Внутри хлоропластов находится фотосинтетических пигментных белка , задача которых поглощать свет . Эти пигменты являются неотъемлемой частью светозависимой стадии фотосинтеза.
Эти пигменты являются неотъемлемой частью светозависимой стадии фотосинтеза.
Солнечный свет представляет собой смесь электромагнитных волн с разными длинами волн и частотами; видимая часть — всего лишь крошечная часть электромагнитного спектра. Длина волны электромагнитных волн в видимом спектре определяет цвет света .
Эти светопоглощающие пигменты можно разделить на две основные группы в зависимости от цвета света, который они поглощают: c хлорофиллы и c аротеноиды .
Хлорофиллы являются наиболее важными фотосинтетическими пигментами , поглощающими синий и красный свет. Они отражают лучи не синие, а красные, и в результате имеют зеленый цвет .
Есть два хлорофилловых пигмента: хлорофилл a и хлорофилл b . Хлорофилл а имеет голубовато-зеленый пигмент, а хлорофилл b имеет желтовато-зеленый пигмент.
Каротиноиды являются вспомогательными пигментами фотосинтеза, которые помогают поглощать свет, но не так важны, как хлорофиллы. Эти пигменты в основном поглощают фиолетовый светлый, у которого больше энергии.
Каротиноиды состоят из трех пигментов ; желтый ксантофилл, оранжевый каротин и серый феофитин.
Как упоминалось ранее, каждый из этих пигментов поглощает свет с разной длиной волны . Растения в различных средах развили , чтобы сделать различных пропорций этих пигментов к максимальному поглощению света .
Вы, наверное, замечали растения с листьями разного цвета. Некоторые из них слегка красноватые, а другие могут быть темно-зелеными или желто-зелеными.
Метод хлорофилловой хроматографии
Разделение хлорофилла и каротиноидов пигментов проводят с использованием бумажной хроматографии . Этот метод хроматографии называется «бумажной хроматографией», поскольку неподвижной фазы в этом методе представляет собой лист бумаги .
Хроматография — это греческая фраза, объединяющая термины «хром» и «граф», которые вместе означают «цветное письмо». Это связано с тем, что первый метод хроматографии был использован в конце 19 века.ст. для разделения пигментов в смеси.
В бумажной хроматографии растворенных химических соединений разделяются на основе их различной скорости миграции по листам бумаги. Это позволяет идентифицировать растворенных химических вещества на основе их растворимости в определенном растворителе.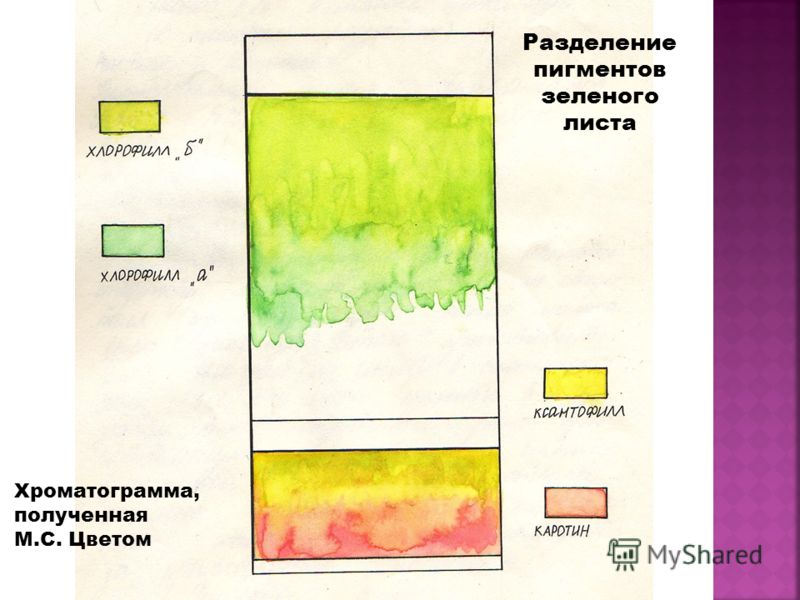 Фотосинтетические пигменты, такие как хлорофилл, каротин и ксантофилл , могут быть разделены методом бумажной хроматографии.
Фотосинтетические пигменты, такие как хлорофилл, каротин и ксантофилл , могут быть разделены методом бумажной хроматографии.
Это недорогой , но эффективный аналитический метод , для которого требуется лишь небольшое количество материала .
Фактор удерживания (Rf) используется в бумажной хроматографии для сравнения и идентификации разделенных химических веществ. Значение Rf соединения равно расстоянию, пройденному на бумаге соединением , деленному на расстояние, пройденное растворителем .
$$Rf=\dfrac{\text{Расстояние, пройденное соединением}}{\text{Расстояние, пройденное растворителем}}$$
Значение \(Rf\) говорит нам о растворимости соединения и размере . Значение l ow Rf означает, что соединение в раз менее растворимо и имеет в больший размер .
Растворитель для хлорофилловой хроматографии
Мы упоминали, что неподвижной фазой в хлорофилловой хроматографии является бумага. А как же подвижная фаза ? Другими словами, какие растворители хлорофилловой хроматографии используются для создания этой фазы?
Некоторые пигменты растворяются в одном растворителе, но не растворяются в другом. Так, смесь растворителей часто используется для получения лучшего разделения пигментных полос. В хлорофилловой хроматографии этанол (C 6 H 2 O) и ацетон (C 3 H 6 O) являются растворителями, обычно используемыми для растворения пигментов .
Если смесь соединений разделить с помощью растворителей, как указано выше, то 9На хроматографической бумаге появятся 0003 различных пятна . Однако чистое соединение покажет только одно пятно — независимо от используемого растворителя.
Процедура хроматографии на хлорофилле
В этом разделе мы рассмотрим, как проводится хроматография на хлорофилле и ее процедура.
Материалы и оборудование
Защитные очки
Пестик и ступка
Бумага для хроматографии или фильтровальная бумага для кофе
A 100ml Beaker
Small capillary tube or a pipette
Pencil
Ruler
Sellotape
A handful of leaves (e.g., spinach leaves)
Ножницы
Этанол
Процедура
Мелко нарезать листья.
Заполните ступку измельченными листьями до глубина около 2 см .
Добавьте в раствор щепотку песка и шесть капель этанола . Песок поможет разрушить листья, а этанол растворит пигменты.

Измельчите ингредиенты не менее трех минут пестиком.
Проведите карандашом линию на расстоянии 3 см от нижней части полоски хроматографической или кофейной фильтровальной бумаги.
Используйте капиллярную трубку или пипетку, чтобы добавить жидкий экстракт из измельченных листьев в центр линии. Держите пятно как можно меньше.
Дайте первой капле высохнуть , прежде чем добавлять другую. Повторяйте этот процесс , пока не добавите пять дополнительных капель раствора, давая каждой высохнуть перед нанесением следующей. Цель состоит в том, чтобы создать на бумаге небольшую область с высокой концентрацией.
Прикрепите бумагу к карандашу с помощью клейкой ленты и поместите ее поверх стакана так, чтобы хроматографическая бумага располагалась вертикально и едва касалась дна стакана.

Добавьте немного этанола в химический стакан так, чтобы этанол достиг бумаги, но все еще находился ниже карандашной линии и пятна.
Удалите бумагу , когда растворитель пройдет вверх по бумаге и останется почти на 2 мм от верха. Затем сразу нарисуйте линию , чтобы отметить расстояние, пройденное растворителем, и , нарисуйте круги вокруг каждой метки пигмента.
Измерьте расстояние между растворителем и каждым пигментом от начальной карандашной линии.
Рассчитайте значение Rf для каждого пигмента.
Пример расчета хлорофилла
Попробуем рассчитать Rf пигментов на хроматографической бумаге. В приведенном ниже примере есть четыре различных пигментных полосы.
Here are the distances travelled by the solvent and the pigments:
| Pigment/solvent | Distance from the origin (cm) |
| Solvent | 9. 9 9 |
| Chlorophyll b | 3.8 |
| Chlorophyll a | 5.3 |
| Xanthophylls | 7.6 |
| Carotenes | 9.7 |
\(\text{Rf for chlorophyll b}=\dfrac{3.8\text{ cm}}{ 9.9\text{ см}}=0,38\)
\(\text{Rf для хлорофилла а}=\dfrac{5,3\text{ см}}{9,9\text{ см}}=0,54\)
\ (\text{Rf для ксантофиллов}=\dfrac{7,6\text{ см}}{9,9\text{ см}}=0,78\)
\(\text{Rf для каротинов}=\dfrac{9,7\text{ см}}{9,9\текст{ см}}=0,98\)
Значение Rf может указывать на растворимость вещества в растворителе и/или размер . Пигменты с малыми значениями Rf либо менее растворимы в растворителе, имеют большие размеры и/или имеют большее сродство к неподвижной фазе (бумаге), чем пигменты с большими значениями Rf.
Хроматография на хлорофилле – основные выводы
- Хроматография – это процесс разделения различных химических соединений в смеси на основе определенных свойств.

- В любом хроматографическом процессе взаимодействуют две фазы: подвижная фаза и неподвижная фаза.
- Фотосинтетические пигменты, содержащиеся в хлоропластах, можно разделить на две основные группы в зависимости от цвета поглощаемого ими света: хлорофиллы и каротиноиды .
- Фактор удерживания (Rf) используется в бумажной хроматографии для сравнения и идентификации разделенных химических веществ. $$Rf=\dfrac{\text{Расстояние, пройденное соединением}}{\text{Расстояние, пройденное растворителем}}$$
Хроматография листьев | Эксперимент | РКЦ Образование
- Пять из пяти
Попробуйте этот практический урок, используя бумажную хроматографию, чтобы разделить и исследовать пигменты в листе
Большинство листьев зеленые из-за хлорофилла. Это вещество играет важную роль в фотосинтезе (процессе, посредством которого растения производят пищу). В этом эксперименте учащиеся исследуют различные пигменты, присутствующие в листе, от хлорофилла до каротинов, используя бумажную хроматографию.
Это вещество играет важную роль в фотосинтезе (процессе, посредством которого растения производят пищу). В этом эксперименте учащиеся исследуют различные пигменты, присутствующие в листе, от хлорофилла до каротинов, используя бумажную хроматографию.
Эксперимент длится около 30 минут и может проводиться в группах из двух или трех студентов.
Оборудование
Аппаратура
- Защита глаз
- Пестик и ступка
- Бумага для хроматографии
- Стакан, 100 см 3
- Маленькая капиллярная трубка (см. примечание 1)
- Карандаш
- Линейка
- Скотч
- Нарезанные листья или листья и ножницы (см. примечание 2)
Химикаты
- Пропанон (ЛЕГКО ВОСПЛАМЕНЯЕМЫЙ, РАЗДРАЖАЮЩИЙ), поставляется в маленькой бутылочке с пипеткой (см. примечание 3)
- Песок
Примечания по оборудованию
- Капиллярная трубка может быть изготовлена в домашних условиях из отрезков обычной стеклянной трубки (диаметр: 3–4 мм) с использованием горелки Бунзена, снабженной распространяющей пламя («рыбий хвост») струей.

- Можно использовать разные листья. Наилучшие результаты получаются от деревьев или кустарников с темно-зелеными листьями, например остролиста.
- Предпочтительно использовать сосковые пипетки, не допускающие разбрызгивания, например, те, которые подходят к флаконам-капельницам с универсальным индикатором.
Примечания по охране труда и технике безопасности
- Прочтите наше стандартное руководство по охране труда и технике безопасности.
- Всегда используйте защитные очки.
- Пропанон, CH 3 COCH 3 (l), (ЛЕГКО ВОСПЛАМЕНЯЕМОЕ, РАЗДРАЖАЮЩЕЕ) – см. CLEAPSS Hazcard HC085A. Пары пропанона ЛЕГКО ВОСПЛАМЕНЯЮТСЯ. Не располагайте поблизости никаких источников воспламенения.
Процедура
- Мелко нарежьте несколько листьев и заполните известковым раствором на глубину около 2 см.
- Добавьте щепотку песка и примерно шесть капель пропанона из сосковой пипетки.
- Растирайте смесь пестиком не менее трех минут.

- На полоске хроматографической бумаги проведите карандашом линию на расстоянии 3 см от низа.
- Используйте тонкую стеклянную трубку, чтобы налить жидкость из экстракта листьев в центр линии. Держите пятно как можно меньше.
- Дайте пятну высохнуть, затем добавьте еще одно пятно сверху. Добавьте еще пять капель раствора, давая каждой высохнуть, прежде чем наносить следующую. Идея состоит в том, чтобы создать очень концентрированное маленькое пятно на бумаге.
- Прикрепите бумагу к карандашу с помощью клейкой ленты так, чтобы при помещении в химический стакан бумага едва касалась основания.
- Поместите не более 10 см 3 пропанона в химический стакан и повесьте бумагу так, чтобы она погрузилась в пропанон. Убедитесь, что уровень пропанона ниже точки.
Источник: Королевское химическое общество
Оборудование, необходимое для использования бумажной хроматографии для разделения различных пигментов в листьях
- Избегайте любых перемещений стакана после начала хроматографии.

- Оставьте эксперимент до тех пор, пока пропанон не впитается почти доверху, а затем удалите бумагу из стакана.
- Отметьте карандашом высоту проникновения пропанона на бумагу и дайте хроматограмме высохнуть.
Учебные заметки
Этот эксперимент работает очень хорошо, если тщательно подготовить пятно на хроматографической бумаге. Она должна быть как можно меньше и как можно более концентрированной. Поощряйте студентов быть терпеливыми и ждать, пока каждое приложение высохнет, прежде чем добавлять следующее.
Должно получиться не менее трех пятен, одно из которых должно быть желтым из-за каротинов.
Степень продвижения любого конкретного компонента вверх по бумаге зависит не только от его растворимости в пропаноне, но и от его притяжения к целлюлозе в хроматографической бумаге. Желтое каротиновое пятно (с более высоким значением RF) имеет тенденцию перемещаться дальше всего вверх по бумаге.
Дополнительная информация
Это ресурс проекта «Практическая химия», разработанного Фондом Наффилда и Королевским химическим обществом.

 Раствор приобрел опять зелёное
окрашивание. Образовался хлорофилл.
Раствор приобрел опять зелёное
окрашивание. Образовался хлорофилл.




Leave A Comment