Самостоятельная работа по графикам зависимости количества теплоты от температуры | Материал для подготовки к ЕГЭ (ГИА) по физике (8 класс) на тему:
Опубликовано 21.08.2017 — 17:35 — Гуденко Елена Викторовна
в сборниках задач нет таких заданий. а в гиа есть. Решим задачи.
Скачать:
| Вложение | Размер |
|---|---|
| графики | 33.5 КБ |
Предварительный просмотр:
Домашнее задание Графики
№1
На рисунке представлен график зависимости температуры твёрдого тела от отданного им количества теплоты. Масса тела 4 кг. Чему равна удельная теплоёмкость вещества этого тела?
№2
На рисунке представлен график зависимости температуры твёрдого тела от полученного им количества теплоты. Чему равна масса нагреваемого тела, если известно, что его удельная теплоёмкость 2500 Дж/(кг ⋅⋅ °С)?
№3
При нагревании и плавлении кристаллического вещества массой 100 г измеряли температуру вещества и количество теплоты, сообщённое веществу. Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
Данные измерений представили в виде таблицы. Считая, что потерями энергии можно пренебречь, определите удельную теплоёмкость вещества в твёрдом состоянии.
Q, кДж | 0 | 2,4 | 4,8 | 7,2 | 9,6 | 12 | 14,4 |
t, °С°С | 50 | 150 | 250 | 250 | 250 | 250 | 300 |
№4 Будущие задачи такие:
Электрический нагреватель за 20 мин доводит до кипения 2,2 кг воды, начальная температура которой 10 °С. Сила тока в нагревателе 7 А, КПД нагревателя равен 45%. Чему равно напряжение в электрической сети?
Сила тока в нагревателе 7 А, КПД нагревателя равен 45%. Чему равно напряжение в электрической сети?
По теме: методические разработки, презентации и конспекты
презентация 8класс Лабораторная работа №1 «Сравнение количеств теплоты при смешивании воды разной температуры»
Презнтация для выполнения лабораторной работы, объясняет порядок выполнения, помогает детям правильно рассчитать количества теплоты и сделать вывод по выполненной работе. Помогает учителю…
Количество теплоты. Единицы количества теплоты. Удельная теплоемкость. Расчет количества теплоты. 8 класс
Количество теплоты. Единицы количества теплоты. Удельная теплоемкость. Расчет количества теплотыЦели урока:Обучающая:ввести понятие количества теплоты, удельной теплоемкости.обосновать зависимос…
Лабораторная работа «Сравнение количеств теплоты при смешивании воды разной температуры»
Бланк лабораторной работы в 8 классе по теме «Сравнение количеств теплоты при смешивании воды разной температуры» (по учебнику Перышкина). ..
..
Контрольная работа по теме «Теплопередача. Количество теплоты» 8 класс
Контрольная работа по теме «Теплопередача. Количество теплоты» для 8 класса составлена на 8 вариантов, по 4 задания. В каждом варианте один качественный вопрос на теплопередачу и три задачи разного ур…
Урок по теме «Количество теплоты. Единицы количества теплоты»
конспект по теме «Количество теплоты. Единицы количества теплоты» + презентация + проверочная работа для программы «Айрен»…
Самостоятельная работа «Компьютерная графика»
Самостоятельная работа «Компьютерная графика"…
Самостоятельная работа «Построение графика квадратичной функции»
Самостоятельная работа предназначена для проверки знаний по теме «Построение графика квадратичной функции"…
Поделиться:
Тепловые явления. Задачи 401-420 Задачи 401-420 |
|
Задача №401    Какое количество теплоты выделится при превращении 400 г воды, имеющей температуру 0°С, в лед. температура которого -10°С? Задача №402    На рисунке представлен график зависимости температуры от полученного количества теплоты для вещества массой 2 кг. Первоначально вещество находилось в твердом состоянии. Определите удельную теплоемкость вещества в твердом состоянии. Задача №403    На диаграмме для двух веществ приведены значения количества теплоты, необходимого для нагревания 1 кг вещества на 10°С и для плавления 100 г вещества, нагретого до температуры плавления. Определите удельную теплоемкость второго вещества. Задача №404    На диаграмме для двух веществ приведены значения количества теплоты, необходимого для нагревания 1 кг вещества на 10°С и для плавления 100 г вещества, нагретого до температуры плавления.  Задача №405    Свинцовое тело при охлаждении на 10 °С выделяет количество теплоты, равное 2600 Дж. Чему равна масса этого тела? Задача №406    На рисунке представлен график зависимости температуры от полученного количества теплоты для вещества массой 1 кг. Первоначально вещество находилось в твердом состоянии. Определите удельную теплоемкость вещества в твердом состоянии    На рисунке представлен график зависимости температуры от времени для процесса нагревания слитка свинца массой 1 кг. Какое количество теплоты получил свинец за 5 мин нагревания? Задача №408    Стальной брусок массой 9,36 кг взятый при температуре 0°С, погрузили в сосуд, содержащий 24 кг воды, температура которой 90°С.  На сколько градусов нагреется брусок к моменту установления теплового равновесия в сосуде? Потерями энергии на нагревание сосуда и окружающего воздуха пренебречь. Ответ округлите до целых. На сколько градусов нагреется брусок к моменту установления теплового равновесия в сосуде? Потерями энергии на нагревание сосуда и окружающего воздуха пренебречь. Ответ округлите до целых.
Задача №409    На рисунке представлен график зависимости температуры от полученного количества теплоты для вещества массой 2 кг. Первоначально вещество находилось в твердом состоянии. Определите удельную теплоту плавления вещества. Ответ выразите в кДж/кг. Задача №410    Какое количество теплоты потребуется, чтобы испарить 200 г воды, взятой при температуре кипения? Задача №411    Стальной брусок погрузили в сосуд, содержащий 20 кг воды, температура которой 90 °С. Какая температура установится в сосуде, если вода при остывании отдала 840 кДж теплоты? Задача №412    Воду массой 1,5 кг доводят до кипения в чайнике мощностью 2 кВт.  имеющем КПД 84%. Сколько времени потребуется на нагревание, если начальная температура воды равна 20°С? имеющем КПД 84%. Сколько времени потребуется на нагревание, если начальная температура воды равна 20°С?
Задача №413    Какое минимальное количество керосина надо сжечь для нагревания 4,6 кг воды от начальной температуры t Задача №414    На рисунке представлен график зависимости температуры твёрдого тела от полученного им количества теплоты. Масса тела — 2 кг. Чему равна удельная теплоёмкость вещества этого тела? Задача №415    Твёрдое тело массой 12 кг помещают в печь мощностью 3 кВт и начинают нагревать. На рисунке изображена зависимость температуры t этого тела от времени нагревания т. Чему равна удельная теплоёмкость вещества тела? Задача №416    Чему равна масса воды, взятой при 10 °С, если при её охлаждении и дальнейшей кристаллизации выделилось количество теплоты 3720 кДж? Задача №417    Твёрдое тело массой 10 кг помещают в печь мощностью 3 кВт и начинают нагревать.  На рисунке изображена зависимость температуры t этого тела от времени нагревания т. Чему равна удельная теплоёмкость вещества тела? На рисунке изображена зависимость температуры t этого тела от времени нагревания т. Чему равна удельная теплоёмкость вещества тела?
Задача №418    Чему равна масса воды, взятой при О °С, если при кристаллизации и последующем её охлаждении до -20 °С выделилось количество теплоты 1860 кДж? Задача №419    Чему равна масса свинца, если при его кристаллизации при температуре плавления и последующего охлаждения до температуры 27 °С выделилось количество теплоты 51200 Дж? Задача №420    Чему равна масса паров спирта, если при их конденсации при температуре кипения и при последующем охлаждении до 28 °С выделяется количество теплоты 20400 Дж? |
Тепло против температуры: в чем сходство и различие? (с графиком)
Люди иногда используют термины тепло и температура взаимозаменяемо. Они связывают тепло со словом горячий и понимают температуру как связанную также с «горячостью» или «холодностью» чего-либо. Возможно, они скажут, что температура в весенний день кажется идеальной, потому что это именно то количество тепла, которое нужно.
Они связывают тепло со словом горячий и понимают температуру как связанную также с «горячостью» или «холодностью» чего-либо. Возможно, они скажут, что температура в весенний день кажется идеальной, потому что это именно то количество тепла, которое нужно.
Однако в физике эти две величины сильно отличаются друг от друга. Они не являются мерами одного и того же, и у них разные единицы измерения, хотя они оба могут помочь вам понять тепловые свойства.
Внутренняя энергия
Чтобы понять теплоту и температуру на фундаментальном уровне, прежде всего важно понять концепцию внутренней энергии. Хотя вы можете быть знакомы с объектами, имеющими кинетическую энергию из-за их движения или потенциальную энергию из-за их положения внутри данного объекта, сами молекулы также могут иметь форму кинетической и потенциальной энергии.
Эта молекулярная кинетическая и потенциальная энергия отличаются от того, что вы можете увидеть, глядя, скажем, на кирпич.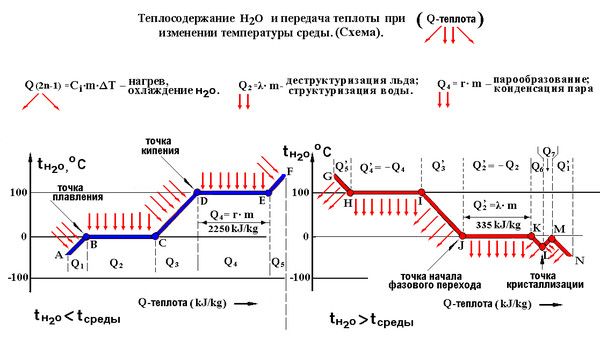 Кирпич, лежащий на земле, кажется неподвижным, и вы можете предположить, что с ним не связана ни кинетическая, ни потенциальная энергия. И действительно, это не так в смысле вашего понимания базовой механики.
Кирпич, лежащий на земле, кажется неподвижным, и вы можете предположить, что с ним не связана ни кинетическая, ни потенциальная энергия. И действительно, это не так в смысле вашего понимания базовой механики.
Но сам кирпич состоит из множества молекул, которые по отдельности совершают различные мелкие движения, невидимые для вас. Молекулы также могут испытывать потенциальную энергию из-за их близости к другим молекулам и сил, действующих между ними. Полная внутренняя энергия этого кирпича есть сумма кинетической и потенциальной энергий самих молекул.
Как вы, наверное, уже знаете, энергия сохраняется. В том случае, если на объект не действуют силы трения или диссипативные силы, механическая энергия также сохраняется. То есть кинетическая энергия может переходить в потенциальную и наоборот, но полная остается постоянной. Однако, когда действует сила, подобная трению, можно заметить, что полная механическая энергия уменьшается. Это потому, что энергия принимала другие формы, такие как звуковая энергия или тепловая энергия.
Когда в холодный день вы потираете руки, вы превращаете механическую энергию в тепловую. То есть кинетическая энергия ваших рук, движущихся друг против друга, изменила форму и стала кинетической энергией молекул в ваших руках относительно друг друга. Среднее значение этой кинетической энергии молекул в ваших руках ученые определяют как температуру.
Определение температуры
Температура – это мера средней кинетической энергии на молекулу вещества. Обратите внимание, что это не то же самое, что внутренняя энергия вещества, поскольку она не включает потенциальную энергию, а также не является мерой общей энергии вещества. Вместо этого это полная кинетическая энергия, деленная на количество молекул. Таким образом, это зависит не от того, сколько чего-то у вас есть (например, от общей внутренней энергии), а скорее от того, сколько кинетической энергии несет средняя молекула в веществе.
Температуру можно измерять во многих различных единицах. Среди них шкала Фаренгейта, которая наиболее распространена в США и некоторых других странах. По шкале Фаренгейта вода замерзает при 32 градусах и кипит при 212. Другой распространенной шкалой является шкала Цельсия, используемая во многих других местах в мире. По этой шкале вода замерзает при 0 градусов и кипит при 100 градусах (что дает довольно четкое представление о том, как была изобретена эта шкала).
Среди них шкала Фаренгейта, которая наиболее распространена в США и некоторых других странах. По шкале Фаренгейта вода замерзает при 32 градусах и кипит при 212. Другой распространенной шкалой является шкала Цельсия, используемая во многих других местах в мире. По этой шкале вода замерзает при 0 градусов и кипит при 100 градусах (что дает довольно четкое представление о том, как была изобретена эта шкала).
Но научным стандартом является шкала Кельвина. В то время как размер приращения по шкале Кельвина такой же, как градус Цельсия, шкала Кельвина начинается с температуры, называемой абсолютным нулем, при которой останавливается все молекулярное движение. Другими словами, он начинается при максимально низкой температуре.
Ноль градусов Цельсия равен 273,15 по шкале Кельвина. Шкала Кельвина является научным стандартом не зря. Предположим, что-то находится при 0 градусов по Цельсию. Что значит сказать, что температура второго объекта в два раза выше? Будет ли этот элемент также равен 0 по Цельсию? Что ж, по шкале Кельвина это понятие не вызывает проблем, и именно потому, что оно начинается с абсолютного нуля.
Определение тепла
Рассмотрим два вещества или объекта при разных температурах. Что это значит? Это означает, что в среднем молекулы одного из веществ (более высокотемпературного) движутся с большей средней кинетической энергией, чем молекулы более низкотемпературного вещества.
Если эти два вещества вступают в контакт, то неудивительно, что энергия начинает усредняться между веществами по мере того, как происходят микроскопические столкновения. Вещество, которое изначально имело более высокую температуру, будет охлаждаться по мере повышения температуры другого вещества, пока они оба не станут одинаковой температуры. Ученые называют это конечное состояние тепловым равновесием .
Тепловая энергия, которая передается от более теплого объекта к более холодному объекту, ученые называют теплом. Тепло – это форма энергии, передаваемая между двумя материалами, находящимися при разных температурах. Тепло всегда переходит от материала с более высокой температурой к материалу с более низкой температурой, пока не будет достигнуто тепловое равновесие.
Поскольку тепло является формой энергии, единицей измерения тепла в системе СИ является джоуль.
Различия между теплотой и температурой
Как вы видели из предыдущих определений, теплота и температура действительно являются двумя разными физическими величинами. Вот лишь некоторые из их отличий:
Они измеряются в разных единицах. Единицей СИ для температуры является кельвин, а единицей СИ для теплоты является джоуль. Кельвин считается базовой единицей, то есть его нельзя разбить на комбинацию других фундаментальных единиц. Джоуль эквивалентен кгм 2 /с 2 .
Отличаются зависимостью от количества молекул. Температура — это мера средней кинетической энергии на молекулу, что означает, что не имеет значения, сколько вещества у вас есть, когда вы говорите о температуре. Однако количество тепловой энергии, которое может передаваться между веществами, очень сильно зависит от того, сколько каждого вещества у вас есть.
Это разные типы переменных. Температура известна как переменная состояния. То есть он определяет состояние, в котором находится вещество или объект. С другой стороны, теплота является переменной процесса. Оно описывает происходящий процесс — в данном случае передачу энергии. Нет смысла говорить о тепле, когда все находится в равновесии.
Они измеряются по-разному. Температура измеряется термометром, который обычно представляет собой устройство, использующее тепловое расширение для изменения показаний на шкале. Тепло, с другой стороны, измеряется калориметром.
Сходства и взаимосвязи между теплом и температурой.
Теплота и температура не совсем не связаны друг с другом, однако:
Обе они являются важными величинами в термодинамике. Изучение тепловой энергии основано на способности измерять температуру, а также на способности отслеживать теплопередачу.
Теплопередача осуществляется за счет разницы температур. Когда два объекта находятся при разных температурах, тепловая энергия будет передаваться от более теплого к более холодному до тех пор, пока не будет достигнуто тепловое равновесие. Таким образом, эти температурные различия являются движущей силой теплопередачи.
Они имеют тенденцию одновременно увеличиваться и уменьшаться. Если в систему добавляется тепло, температура повышается. Если из системы отводится тепло, температура падает. (Одним исключением являются фазовые переходы, и в этом случае тепловая энергия используется для того, чтобы вызвать фазовый переход вместо изменения температуры.)
Они связаны друг с другом уравнением. Тепловая энергия Q связана с изменением температуры ΔT уравнением Q = mcΔT где m — масса вещества и c — его удельная теплоемкость (то есть мера количества тепловой энергии, необходимой для нагревания единицы массы на градус Кельвина для конкретного вещества. )
)
Теплота, температура и полная внутренняя энергия
Внутренняя энергия — это полная внутренняя кинетическая и потенциальная энергия или тепловая энергия в материале. Для идеального газа, в котором потенциальная энергия между молекулами пренебрежимо мала, внутренняя энергия E определяется формулой E = 3/2nRT, где n – количество молей газа и универсальная газовая постоянная R = 8,3145 Дж/мольК.
Связь между внутренней энергией и температурой показывает, что неудивительно, что с повышением температуры увеличивается тепловая энергия. Внутренняя энергия также становится равной 0 при абсолютном 0 градусов Кельвина.
Тепло появляется, когда вы начинаете наблюдать за изменениями внутренней энергии. Первый закон термодинамики дает следующее соотношение:
\Delta E = Q — W
, где Q — теплота, подведенная к системе, а W — работа, выполненная системой.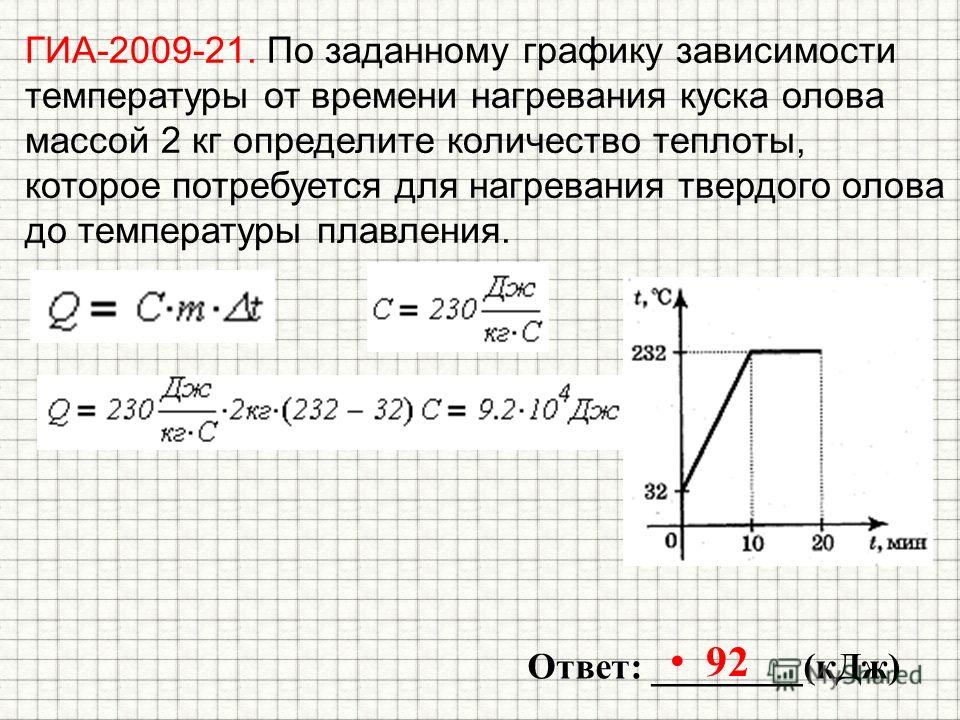 По сути, это утверждение о сохранении энергии. Когда вы добавляете тепловую энергию, внутренняя энергия увеличивается. Если система действует на свое окружение, внутренняя энергия уменьшается.
По сути, это утверждение о сохранении энергии. Когда вы добавляете тепловую энергию, внутренняя энергия увеличивается. Если система действует на свое окружение, внутренняя энергия уменьшается.
Температура как функция тепловой энергии
Как упоминалось ранее, добавление тепловой энергии в систему обычно приводит к соответствующему повышению температуры, если в системе не происходит фазового перехода. Чтобы рассмотреть это более внимательно, рассмотрим глыбу льда, которая начинается ниже точки замерзания, поскольку тепловая энергия добавляется с постоянной скоростью.
Если тепловая энергия непрерывно добавляется, в то время как глыба льда нагревается до замерзания, претерпевает фазовое превращение, становясь водой, а затем продолжает нагреваться до тех пор, пока не достигнет кипения, где претерпевает еще одно фазовое превращение, становясь паром, график температуры по сравнению с теплом будет выглядеть следующим образом:
Пока температура льда ниже точки замерзания, существует линейная зависимость между тепловой энергией и температурой.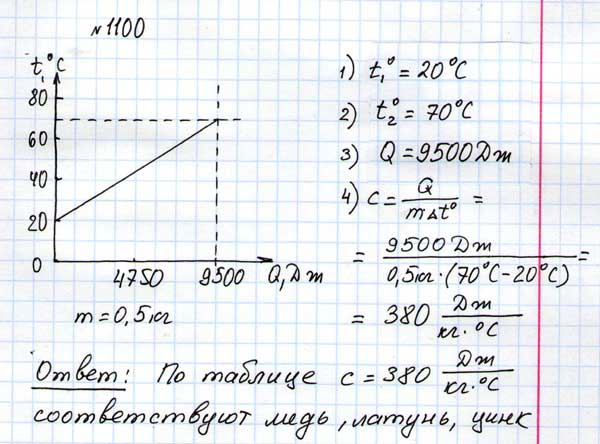 Это неудивительно, как и должно быть, учитывая уравнение Q = mcΔT. Однако, как только лед достигает температуры замерзания, необходимо использовать любую добавленную тепловую энергию, чтобы помочь ему изменить фазу. Температура остается постоянной, несмотря на то, что тепло продолжает добавляться. Уравнение, связывающее тепловую энергию с массой при фазовом переходе из твердого состояния в жидкое, выглядит следующим образом:
Это неудивительно, как и должно быть, учитывая уравнение Q = mcΔT. Однако, как только лед достигает температуры замерзания, необходимо использовать любую добавленную тепловую энергию, чтобы помочь ему изменить фазу. Температура остается постоянной, несмотря на то, что тепло продолжает добавляться. Уравнение, связывающее тепловую энергию с массой при фазовом переходе из твердого состояния в жидкое, выглядит следующим образом:
Q=mL_f
где L f — скрытая теплота плавления — константа, определяющая, сколько энергии требуется на единицу массы для перехода из твердого состояния в жидкое.
Таким образом, пока не добавлено количество теплоты, равное мл f , температура остается постоянной.
После того, как весь лед растаял, температура снова линейно повышается, пока не достигнет точки кипения. Здесь снова происходит фазовый переход, на этот раз из жидкости в газ. Уравнение, связывающее теплоту с массой во время этого фазового перехода, очень похоже:
, где L v — скрытая теплота парообразования — константа, определяющая, сколько энергии требуется на единицу массы для перехода из жидкости в газ. Таким образом, температура снова остается постоянной до тех пор, пока не будет добавлено достаточное количество тепловой энергии. Обратите внимание, что на этот раз он остается постоянным дольше. Это связано с тем, что L v обычно выше, чем L f для вещества.
Таким образом, температура снова остается постоянной до тех пор, пока не будет добавлено достаточное количество тепловой энергии. Обратите внимание, что на этот раз он остается постоянным дольше. Это связано с тем, что L v обычно выше, чем L f для вещества.
Последняя часть графика снова показывает ту же линейную зависимость, что и раньше.
Тепло против температуры — разница и сравнение
Тепло и температура связаны и часто путают. Больше тепла обычно означает более высокую температуру.
Тепло (символ: Q ) — это энергия. Это общее количество энергии (как кинетической, так и потенциальной), которой обладают молекулы в куске материи. Теплота измеряется в джоулях.
Температура (символ: T ) не является энергией. Он относится к средней (кинетической) энергии микроскопических движений одной частицы в системе на одну степень свободы. Измеряется в градусах Кельвина (К), Цельсия (С) или Фаренгейта (F).
При нагревании вещества может произойти одно из двух: температура вещества может повыситься или состояние вещества может измениться.


Leave A Comment