| Массовое числоMass number Массовое число – суммарное число протонов и нейтронов в атомном ядре. См. также
|
Как определить число протонов и нейтронов в атоме? Примеры.
Как определить число нуклонов в ядре атома?
Число нуклонов в ядре атома равно массовому числу атома (относительная атомная масса химического элемента) или сумме протонов и нейтронов.
Как определить число протонов в атоме?
Число протонов в атоме равно заряду его ядра (обозначается как Z) или порядковому номеру элемента в периодической таблице Менделеева.
Как определить число нейтронов в атоме?
Очень просто!
N = A – Z
Где N – число нейтронов, A – атомная масса элемента (в целых числах), Z – заряд ядра атома или порядковый номер атома в периодической таблице Менделеева.
Развернутый ответ
Масса атома складывается из двух величин: масса протонов + масса нейтронов. Дело в том, что масса электронов пренебрежимо мала.
Масса нейтрона = 1,674 927 498 04(95)⋅10⁻²⁷ кг= 1,008 664 915 60(57) а.е.м.
Масса протона = 1,672 621 923 69(51)⋅10⁻²⁷ кг = 1,007276466621(53) а.е.м.
Масса электрона = 9,109383 7015(28)⋅10⁻³¹ кг = 0,000548579909065 а.е.м.
То есть даже 100 электронов дадут в сумме всего 0,0548579909065 а.е.м.
Первоначально Д. И. Менделеев в построении своей периодической таблицы исходил из атомных весов элементов. Однако, дальнейшее развитие науки показало, что свойства химических элементов находятся в прямой зависимости не от атомной массы химического элемента, а от заряда ядра его атома. Таким образом, в периодической таблице химические элементы выстроены в порядке возрастания заряда ядра атома и номер элемента в таблице соответствует заряду его ядра. А заряд ядра равен сумме протонов. То есть № (элемента) = Z (заряд ядра или число протонов).
Остаток массы ядра приходится на нейтроны. Поэтому чтобы определить число нейтронов в атоме нужно всего лишь вычесть из атомной массы число протонов, которое равно заряду ядра или порядковому номеру элемента в таблице Менделеева.
Примеры
Сколько протонов и нейтронов в атоме натрия?
Ar (Na) = 23 а.е.м.
Z (Na) = 11 (протонов)
N = Ar (Na) – Z (Na) = 23 – 11 = 12 (нейтронов)
Ответ: число протонов в атоме натрия равно 11, а число нейтронов в атоме натрия равно 12.
Сколько протонов и нейтронов в атоме фосфора?
Ar (P) = 31 а.е.м.
Z (P) = 15 (протонов)
N = Ar (P) – Z (P) = 31 – 15 = 16 (нейтронов)
Ответ: число протонов в атоме фосфора равно 15, а число нейтронов в атоме фосфора равно 16.
Сколько протонов и нейтронов в атоме золота?
Ar (Au) = 197 а.е.м.
Z (Au) = 79 (протонов)
N = Ar (Au) – Z (Au) = 197 – 79 = 118 (нейтронов)
Ответ: число протонов в атоме золота равно 79, а число нейтронов в атоме золота равно 118.
Сколько протонов и нейтронов в атоме кремния?
Ar (Si) = 28 а.е.м.
Z (Si) = 14 (протонов)
N = Ar (Si) – Z (Si) = 28 – 14 = 14 (нейтронов)
Ответ: число протонов и нейтронов в атоме кремния равно 14.
Сколько протонов и нейтронов в атоме углерода?
Ar (C) = 12 а.е.м.
Z (C) = 6 (протонов)
N = Ar (C) – Z (C) = 12 – 6 = 6 (нейтронов)
Ответ: число протонов и нейтронов в атоме углерода равно 6.
Сколько протонов и нейтронов в атоме калия?
Ar (K) = 39 а.е.м.
Z (K) = 19 (протонов)
N = Ar (K) – Z (K) = 39 – 19 = 20 (нейтронов)
Ответ: число протонов в атоме калия равно 19, а число нейтронов в атоме калия равно 20.
Сколько протонов и нейтронов в атоме железа?
Ar (Fe) = 39 а.е.м.
Z (Fe) = 19 (протонов)
N = Ar (Fe) – Z (Fe) = 56 – 26 = 30 (нейтронов)
Ответ: число протонов в атоме железа равно 19, а число нейтронов в атоме железа равно 30.
Сколько протонов и нейтронов в атоме алюминия?
Ar (Al) = 27 а. е.м.
е.м.
Z (Al) = 13 (протонов)
N = Ar (Al) – Z (Al) = 27 – 13 = 14 (нейтронов)
Ответ: число протонов в атоме алюминия равно 13, а число нейтронов в атоме алюминия равно 14 .
Сколько протонов и нейтронов в атоме фтора?
Ar (F) = 19 а.е.м.
Z (F) = 9 (протонов)
N = Ar (F) – Z (F) = 19 – 9 = 10 (нейтронов)
Ответ: число протонов в атоме фтора равно 9, а число нейтронов в атоме фтора равно 10.
Сколько протонов и нейтронов в атоме хлора?
Ar (Cl) = 35 а.е.м.
Z (Cl) = 17 (протонов)
N = Ar (Cl) – Z (Cl) = 35 – 17 = 18 (нейтронов)
Ответ: число протонов в атоме хлора равно 17, а число нейтронов равно 18.
Сколько протонов и нейтронов в атоме кислорода?
Ar (O) = 16 а.е.м.
Z (O) = 8 (протонов)
N = Ar (O) – Z (O) = 16 – 8 = 8 (нейтронов)
Ответ: число протонов и нейтронов в атоме кислорода равно 8.
Сколько протонов и нейтронов в атоме серы?
Ar (S) = 32 а.е.м.
Z (S) = 16 (протонов)
N = Ar (S) – Z (S) = 32 – 16 = 16 (нейтронов)
Ответ: число протонов и нейтронов в атоме серы равно 16.
Сколько протонов и нейтронов в атоме магния?
Ar (Mg) = 32 а.е.м.
Z (Mg) = 16 (протонов)
N = Ar (Mg) – Z (Mg) = 24 – 12 = 12 (нейтронов)
Ответ: число протонов в атоме магния равно 16, а число нейтронов равно 12.
Сколько протонов и нейтронов в атоме цинка?
Ar (Zn) = 65 а.е.м.
Z (Zn) = 30 (протонов)
N = Ar (Zn) – Z (Zn) = 65 – 30 = 35 (нейтронов)
Ответ: число протонов в атоме цинка равно 30, а число нейтронов в атоме цинка равно 35.
Похожие вопросы:
– Какие атомы имеют одинаковое число нейтронов?
– Как определить общее число электронов в атоме?
Структура атома
Структура атомаАтом и электромагнитное излучение
| Основные Субатомные частицы | Электромагнитный Радиация |
| Свет и другие формы электромагнитного излучения | |
Фундаментальный субатомный Частицы
| Частица | Символ | Оплата | Масса | |
| электрон | и — | -1 | 0,0005486 а. е.м. е.м. | |
| протон | р + | +1 | 1,007276 а.е.м. | |
| нейтрон | нет или | 0 | 1.008665 аму | |
Число протонов, нейтронов и электронов в атоме можно определить из набора простых правила.
- Число протонов в ядре атома равно равно атомному номеру ( Z ).
- Количество электронов в нейтральном атоме равно равно числу протонов.
- Массовое число атома ( M ) равно сумма числа протонов и нейтронов в ядро.
- Число нейтронов равно разности
между массовым числом атома ( M ) и
атомный номер ( Z ).

Примеры: Определим количество протонов, нейтронов, и электроны в следующих изотопах.
| 12 С | 13 С | 14 С | 14 Н |
Различные изотопы элемента идентифицируют, записывая массовое число атома в верхний левый угол символа элемента. 12 С, 13 C и 14 C изотопы углерода ( Z = 6) и, следовательно, содержат шесть протонов. Если атомы нейтральны, они также должны содержать шесть электронов. Единственный разница между этими изотопами в количестве нейтронов в ядре.
12 C: 6 электронов, 6 протонов и 6 нейтронов
13 C: 6 электронов, 6 протонов и 7 нейтронов
14 С: 6 электронов, 6 протонов и 8 нейтронов
Электромагнитный Радиация
Многое из того, что известно о строении электронов
в атоме было получено при изучении взаимодействия
между материей и различными формами электромагнитных
радиация . Электромагнитное излучение имеет некоторые
свойства частицы и волны.
Электромагнитное излучение имеет некоторые
свойства частицы и волны.
Частицы имеют определенную массу и занимают космос. Волны не имеют массы, но несут энергию как они путешествуют по космосу. Помимо их способности несут энергию, волны имеют четыре другие характеристики свойства: скорость, частота, длина волны и амплитуда. Частота ( v ) количество волн (или циклов) на единицу время. Частота волны указывается в единицах циклов. в секунду (с -1 ) или герц (Гц).
Идеализированный рисунок волны на рисунке ниже иллюстрирует определения амплитуды и длины волны. Длина волны ( l ) — наименьшее расстояние между повторяющимися точками на волне. Амплитуда волны — это расстояние между самой высокой (или самой низкой) точкой волны и центр тяжести волны.
Если мы измерим частоту ( v ) волны в циклах
в секунду и длина волны ( l ) в метрах,
Произведение этих двух чисел выражается в метрах на
второй. Произведение частоты ( v ), умноженной на
длина волны ( l ) волны, следовательно, равна скорости ( с )
при котором волна распространяется в пространстве.
Произведение частоты ( v ), умноженной на
длина волны ( l ) волны, следовательно, равна скорости ( с )
при котором волна распространяется в пространстве.
вл = с
Легкие и прочие Формы электромагнитного излучения
Свет — это волна с электрическими и магнитными . компоненты. Следовательно, это форма электромагнитных радиация .
Видимый свет содержит узкую полосу частот и
длины волн в части электромагнитного спектра
которые наши глаза могут обнаружить. Он включает в себя излучение с
длины волн от 400 нм (фиолетовый) до 700 нм (красный).
Поскольку это волна, свет преломляется, когда попадает в стекло.
призма. Когда белый свет фокусируется на призме, световые лучи
с разной длиной волны изгибаются на разную величину и
свет превращается в спектр цветов. Начиная
со стороны спектра, где свет преломляется
наименьший угол, цвета красный, оранжевый, желтый, зеленый,
синий, и фиолетовый.
Начиная
со стороны спектра, где свет преломляется
наименьший угол, цвета красный, оранжевый, желтый, зеленый,
синий, и фиолетовый.
Как видно из следующей диаграммы, энергия переносимый светом, увеличивается по мере того, как мы переходим от красного к синему через видимый спектр.
Поскольку длина волны электромагнитного излучения может быть до 40 м или до 10 -5 нм, видимый спектр составляет лишь малую часть всего диапазона электромагнитного излучения.
Электромагнитный спектр включает радио- и телеволны,
микроволны, инфракрасное излучение, видимый свет, ультрафиолет, рентгеновские лучи,
g-лучи и космические лучи, как показано на рисунке выше. Эти
различные формы излучения движутся со скоростью света
( с ). Однако они различаются по своей частоте и
длины волн. Произведение частоты на
длина волны электромагнитного излучения всегда равна
скорость света.
вл = с
В результате электромагнитное излучение то, что имеет большую длину волны, имеет низкую частоту, а излучение с высокой частотой имеет короткую длину волны.
вопросов и ответов — Как найти количество протонов, электронов и нейтронов в атоме элемента?
Предыдущий вопрос
(Не могли бы вы объяснить плотность?)
Вопросы и ответы
Основной индекс
Следующий вопрос
(Сколько протонов, нейтронов и электронов в атоме?)
Предыдущий вопрос
(Не могли бы вы объяснить плотность?)
Вопросы и ответы Основной индекс
Следующий вопрос
(Сколько протонов, нейтронов и электронов в атоме?)
Вопросы и ответы Основной индекс
Сколько протонов, электронов и нейтронов в атоме криптона, углерода, кислорода, неона, серебра, золота и т.д…?
Чтобы найти количество протонов, электронов и нейтронов в атоме, выполните следующие простые шаги:
Шаг 1. Сбор информации
Сбор информации
Первое, что вам нужно сделать, это найти информацию о вашем элементе. Перейдите в периодическую таблицу элементов и нажмите на свой элемент. Если это упрощает задачу, вы можете выбрать элемент из алфавитного списка.
Используйте Таблицу элементов, чтобы найти атомный номер и атомный вес вашего элемента. Атомный номер — это число, расположенное в верхнем левом углу, а атомный вес — это число, расположенное внизу, как в этом примере для криптона:
Шаг 2 — Число протонов равно…
атомный номер — это количество протонов в атоме элемента. В нашем примере атомный номер криптона равен 36. Это говорит нам о том, что атом криптона имеет в ядре 36 протонов.
Интересно, что каждый атом криптона содержит 36 протонов. Если в атоме нет 36 протонов, он не может быть атомом криптона. Добавление или удаление протонов из ядра атома создает другой элемент. Например, удаление одного протона из атома криптона создает атом брома.
Шаг 3. Число электронов равно…
По определению атомы не имеют общего электрического заряда. Это означает, что должен существовать баланс между положительно заряженными протонами и отрицательно заряженными электронами. Атомов должно быть равное количество протонов и электронов . В нашем примере атом криптона должен содержать 36 электронов, поскольку он содержит 36 протонов.
Электроны особым образом расположены вокруг атомов. Если вам нужно знать, как электроны расположены вокруг атома, взгляните на статью «Как читать таблицу конфигурации электронов?» страница.
Атом может приобретать или терять электроны, становясь так называемым ионом . Ион — это не что иное, как электрически заряженный атом. Добавление или удаление электронов из атома не меняет того, какой это элемент, а только его суммарный заряд.
Например, удаление электрона из атома криптона образует ион криптона, который обычно записывается как Kr + . Знак плюс означает, что это положительно заряженный ион.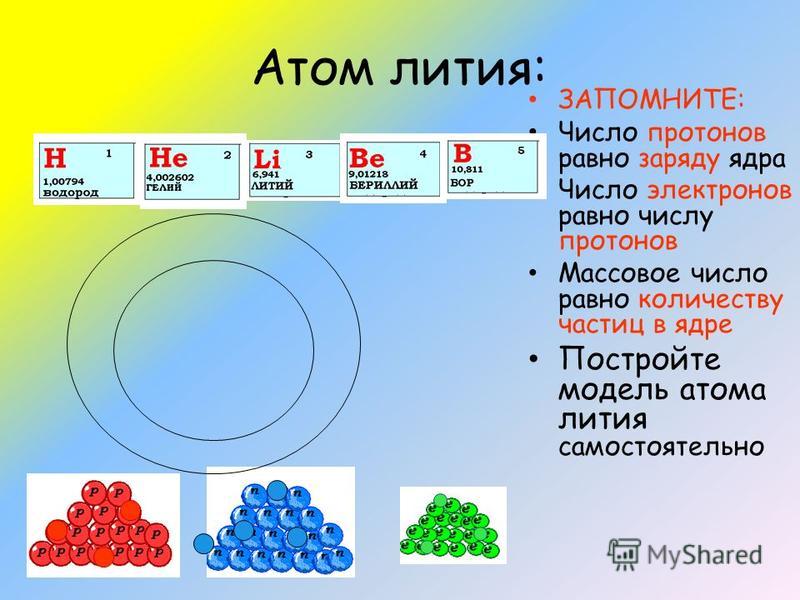 Он заряжен положительно, потому что из атома был удален отрицательно заряженный электрон. Оставшихся 35 электронов было меньше, чем 36 положительно заряженных протонов, что привело к заряду +1.
Он заряжен положительно, потому что из атома был удален отрицательно заряженный электрон. Оставшихся 35 электронов было меньше, чем 36 положительно заряженных протонов, что привело к заряду +1.
Шаг 4. Число нейтронов равно…
Атомный вес в основном является измерением общее число частиц в ядре атома . На самом деле, это не такой чистый срез. Атомный вес на самом деле представляет собой средневзвешенное значение всех встречающихся в природе изотопов элемента по отношению к массе углерода-12. Не понял? Не имеет значения. Все, что вам действительно нужно найти, это то, что называется массовым числом . К сожалению, массовое число не указано в таблице элементов. К счастью, чтобы найти массовое число, все, что вам нужно сделать, это округлить атомный вес до ближайшего целого числа 9.0005 . В нашем примере массовое число криптона равно 84, так как его атомный вес 83,80 округляется до 84.
Массовое число — это количество частиц в ядре атома. Помните, что ядро состоит из протонов и нейтронов. Итак, если мы хотим, мы можем написать:
Помните, что ядро состоит из протонов и нейтронов. Итак, если мы хотим, мы можем написать:
Массовое число = (Количество протонов) + (Количество нейтронов)
Для криптона это уравнение принимает вид:
84 = (Количество протонов) + (Количество нейтронов)
Если бы мы только знали, сколько протонов у криптона, мы могли бы вычислить, сколько у него нейтронов. Подожди… Нам do узнай сколько протонов у криптона! Мы сделали это еще в Шаге 2 ! Атомный номер (36) — это количество протонов в криптоне. Поместив это в уравнение, мы получим:
84 = 36 + (Число нейтронов)
Какое число, добавленное к 36, дает 84? Надеюсь, вы сказали 48. Это количество нейтронов в атоме криптона.
Интересно, что добавление или удаление нейтронов из атома не создает новый элемент. Скорее, он создает более тяжелую или более легкую версию этого элемента. Эти разные версии называются изотопами, и большинство элементов на самом деле представляют собой смесь разных изотопов.

 Боттомоний
Боттомоний Чармоний
Чармоний Как известно атомное
ядро состоит из протонов и нейтронов – элементарных частиц, имеющих очень
близкие массы (≈1.67·10-24 г) и объединяемых термином
“нуклоны”. Если число протонов в ядре обозначить буквой Z, а число нейтронов
— буквой N, то массовое число (или число нуклонов) А = Z + N. Термин “массовое
число” связан с тем, что именно количество нуклонов (протонов и нейтронов)
в ядре практически полностью (с точностью обычно не хуже 1%) определяет
массу атомного ядра и атома. Знание массового числа позволяет оценить массу
ядра и атома. Если известно массовое число, то масса М атома и его ядра
оценивается из следующего соотношения М ≈ А·mN,
где mN — масса нуклона, т.е. протона или нейтрона. Например,
в состав атома алюминия и его ядра входит 27 нуклонов (13 протонов и 14
нейтронов). Его масса ≈ 27·1.67·10-24 г ≈ 4.5·10-23 г. Если необходимо получить массу ядра с большей точностью, то нужно
учесть, что нуклоны в ядре связаны силами ядерного притяжения, и поэтому
в соответствии с соотношением E = mc2 масса ядра уменьшается.
Как известно атомное
ядро состоит из протонов и нейтронов – элементарных частиц, имеющих очень
близкие массы (≈1.67·10-24 г) и объединяемых термином
“нуклоны”. Если число протонов в ядре обозначить буквой Z, а число нейтронов
— буквой N, то массовое число (или число нуклонов) А = Z + N. Термин “массовое
число” связан с тем, что именно количество нуклонов (протонов и нейтронов)
в ядре практически полностью (с точностью обычно не хуже 1%) определяет
массу атомного ядра и атома. Знание массового числа позволяет оценить массу
ядра и атома. Если известно массовое число, то масса М атома и его ядра
оценивается из следующего соотношения М ≈ А·mN,
где mN — масса нуклона, т.е. протона или нейтрона. Например,
в состав атома алюминия и его ядра входит 27 нуклонов (13 протонов и 14
нейтронов). Его масса ≈ 27·1.67·10-24 г ≈ 4.5·10-23 г. Если необходимо получить массу ядра с большей точностью, то нужно
учесть, что нуклоны в ядре связаны силами ядерного притяжения, и поэтому
в соответствии с соотношением E = mc2 масса ядра уменьшается. В массу атома также следует добавить суммарную массу электронов на орбитах
вокруг ядра. Однако все эти поправки не превышают 1%.
В массу атома также следует добавить суммарную массу электронов на орбитах
вокруг ядра. Однако все эти поправки не превышают 1%.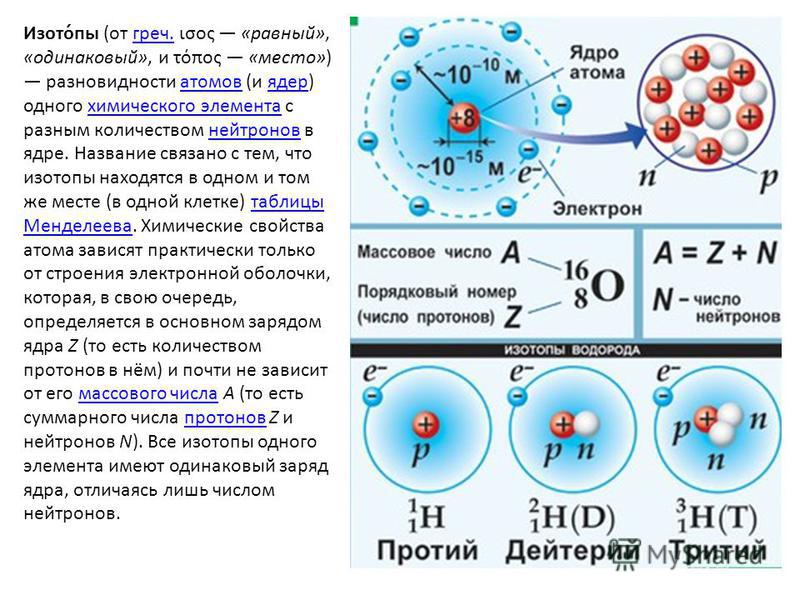
Leave A Comment