Пример 7 функциональных изомеров: с подробными фактами —
В этой статье мы хотим обсудить вещи, связанные с функциональными изомерами, а также подробные факты.
Изомеры — это тип соединений, которые имеют одинаковую молекулярную формулу, но различное распределение атомов в пространстве. . Функциональный изомер — это органическое и неорганическое соединение, имеющее одинаковую формулу, но различную функциональную группу. Функциональный изомер является частью структурного изомера.
Примеры функциональных изомеров приведены ниже:
C2H6OНапример, C2H6O имеет два функциональных изомера. Одним из них является диметиловый эфир (Ch4OCh4), а другим этанол (СН3СН2ОН). В диметиловом эфире функциональной группой является эфир, т.е. связь -COC-. Диметиловый эфир, также известный как метоксиметан. В этаноле функциональной группой является гидроксильная группа, т.е. группа –ОН.
Поскольку два изомера различаются по температуре кипения, эти два изомера можно легко различить. Благодаря наличию ОН-группы в этаноле между молекулами этанола возникает межмолекулярная Н-связь. Для их разделения требуется большое количество энергии, для этого он имеет высокую температуру кипения.
Благодаря наличию ОН-группы в этаноле между молекулами этанола возникает межмолекулярная Н-связь. Для их разделения требуется большое количество энергии, для этого он имеет высокую температуру кипения.
Но в случае диметилового эфира из-за отсутствия ОН-группы между ними не возникает Н-связь, поэтому он имеет более низкую температуру кипения. Поскольку этанол более полярен, чем диметиловый эфир, эти 2 изомера идентифицируются по их полярности. Также этанол способен образовывать межмолекулярную Н-связь с молекулой Н2О, он растворим в воде, а диметиловый эфир не может образовывать Н-связь с водой. Он менее растворим в воде.
Функциональный изомер C2H6OC3H6OC3H6O имеет два функциональных пример изомеров. Один пропаналь (Ch4Ch3CHO), а другой пропанон (Ch4COCh4). В пропанале функциональной группой является –CHO, т.е. альдегид, а в пропаноне функциональной группой является –CO, т.е. кетон. Пропаналь и пропанон можно отличить друг от друга с помощью химической реакции, называемой галоформной реакцией.
когда оба соединения реагируют с NaOH и I2 из-за присутствия атома α-H в пропаноне, он дает желтый осадок CHI3, но пропаналь не дает этого теста из-за отсутствия атома α-H. Реакция нуклеофильного присоединения протекает быстрее с пропаналем, чем с пропаноном, из-за стерического, а также электронного фактора.
Карбонильный углерод менее стерически затруднен и более электрофилен в пропанале, чем в пропаноне. Пропанон имеет более высокую температуру кипения, чем пропанон, потому что в пропаноне карбонильная группа более поляризована, чем у пропаналя. Для этого диполь-дипольная сила притяжения у пропанона выше, чем у пропаналя, а температура кипения у пропанона выше, чем у пропаналя.
Функциональный изомер C3H6OC2h5O2Например, C2h5O2 имеет два функциональных изомера. Один уксусная кислота (Ch4COOH), а другой – метилформиат (HCOOCh4). В уксусной кислоте функциональной группой является кислота, т.е. группа –COOH. В метилформиате функциональным изомером является сложный эфир, т. е. группа –COOR.
е. группа –COOR.
Оба изомера имеют одинаковую молекулярную формулу, но разные функциональные группы и обладают разными физическими и химическими свойствами. По температуре кипения эти 2 изомера можно отличить друг от друга. Уксусная кислота имеет более высокую температуру кипения, чем метилформиат, потому что в уксусной кислоте возникает внутримолекулярная Н-связь, которой нет в метилформиате из-за отсутствия группы –ОН.
По этой причине для отделения молекул уксусной кислоты друг от друга требуется большое количество энергии. Если оба изомера реагируют с NaHCO3 в присутствии небольшого количества тепла, изомер, в котором мы видим вскипание газа CO2, будет уксусной кислотой. С помощью этого химического метода мы можем отличить кислоту от эфира.
Они также могут различаться по значениям дипольного момента. Уксусная кислота имеет более высокое значение дипольного момента, чем метилформиат. Из-за этой более высокой полярности уксусная кислота лучше растворяется в воде, чем метилформиат.
C3H9N существует в виде трех функциональных изомеров. Это пропан-3-амин (Ch2Ch4Ch3Nh3), N-метилэтанамин (Ch3Ch4NHCh3), N,N-диметилметанамин [(Ch4)3N]. Пропан-3-амин 10 амин, N-метилэтанамин 20 амин, N,N-диметилметанамин 30 амин. Все они имеют одинаковую молекулярную формулу, но имеют разные функциональные группы.
Эти три амина отличаются друг от друга реактивом Хинсберга. При взаимодействии с реактивом Хинсберга пропан-1-амин дает сульфонамид, хорошо растворимый в щелочи. N-метилэтанамин также дает нерастворимый в природе сульфонамид. А вот N,N-диметилметанамин не выдерживает этого испытания из-за отсутствия атома H на атоме N, его невозможно нейтрализовать дальше.
Их также можно отличить по температуре кипения. Порядок температур кипения следующий: пропан-1-амин>N-метилэтанамин>N,N-диметилметанамин. Также их растворимость в воде различна. Пропан-1-амин хорошо растворим в природе, а N,N-диметилметанамин наименее растворим в воде и 20 амин лежит между ними.
Пропан-1-амин хорошо растворим в природе, а N,N-диметилметанамин наименее растворим в воде и 20 амин лежит между ними.
Например, C4h20O существует в виде двух функциональных изомеров. Один представляет собой бутан-1-ол (Ch4Ch3Ch3Ch3OH), а другой представляет собой этоксиэтан (Ch4Ch3OCh3Ch4). В бутаноле-1 функциональной группой является группа –ОН, а в этоксиэтане функциональной группой является эфир, т.е. связь –СОС.
Эти два изомера можно отличить друг от друга по разнице их температур кипения. Благодаря наличию группы –ОН между молекулами бутан-1-ола возникает межмолекулярная Н-связь. Поскольку, чтобы отделить их друг от друга, требуется большое количество энергии.
По этой причине он имеет более высокую температуру кипения, чем этоксиэтан, где Н-связь не возникает из-за отсутствия группы –ОН. При взаимодействии двух изомеров с PCl5 бутан-1-ол дает осадок алкилхлорида, тогда как эфир не дает того же самого. Этим химическим методом мы также различаем эти 2 изомера.
Этим химическим методом мы также различаем эти 2 изомера.
Также бутан-1-ол растворим в воде, тогда как этоксиэтан нерастворим в воде. Потому что бутан-1-ол образует Н-связь с водой, а этоксиэтан — нет.
Функциональный изомер C4h20OC4H8O2C4H8O2 имеет 2 примера функциональных изомеров. Один из них — бутановая кислота (Ch4Ch3Ch3COOH), а другой — метилпропионат (Ch4Ch3COOCh4). В бутановой кислоте функциональной группой является кислота, т.е. группа –COOH, а метилпропионат имеет функциональную группу сложного эфира, т.е. группу –COOR.
Поскольку их температура кипения различна, можно выделить 2 изомера по отдельности. Бутановая кислота имеет более высокую температуру кипения, чем метилпропионат. Это связано с наличием внутримолекулярной Н-связи в первом соединении, которая не возникает во втором из-за отсутствия группы –ОН.
Поэтому для разделения молекул бутановой кислоты требуется большое количество энергии, чтобы она имела более высокую температуру кипения, чем метилпропионат. когда 2 изомера реагируют с NaHCO3 при нагревании, бутановая кислота дает вскипание газа CO2, но метилпропионат не дает этого теста.
когда 2 изомера реагируют с NaHCO3 при нагревании, бутановая кислота дает вскипание газа CO2, но метилпропионат не дает этого теста.
Этим химическим методом мы можем различить кислоту и сложный эфир. Бутановая кислота имеет более высокую температуру кипения, чем метилпропионат, из-за более высокой полярность кислоты, чем сложного эфира.
Функциональный изомер C4H8O2C4H8OC4H8O имеет 2 функциональных пример изомеров. Один из них — бутаналь (Ch4Ch3Ch3CHO), а другой — бутанон (Ch4COCh3Ch4). В бутанале функциональная группа –CHO, т.е. альдегид, а бутанон имеет кетоновую функциональную группу, т.е. –CO.
Эти два функциональных изомера можно отличить друг от друга с помощью химической реакции, называемой галоформной реакцией. При взаимодействии обоих изомеров с NaOH и I2 из-за присутствия атома α-H бутанон дает желтый осадок CHI2, а бутаналь не дает этого теста из-за отсутствия атома α-H.
Реакция нуклеофильного присоединения протекает быстрее в бутанале из-за стерического, а также электронного фактора.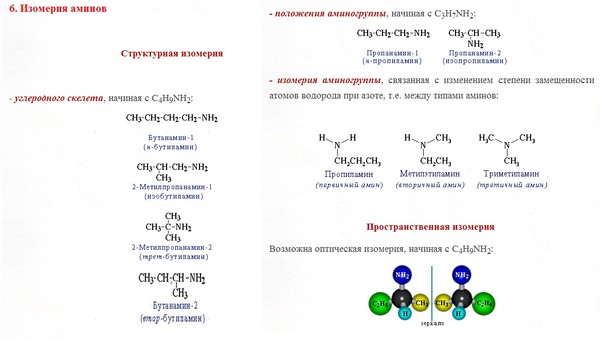 Карбонильный углерод менее стерически затруднен и более электрофилен в бутанале, чем в бутаноне. Бутанон имеет более высокую температуру кипения, чем бутаналь, потому что в бутаноне карбонильная группа более поляризована, чем у бутаналя.
Карбонильный углерод менее стерически затруднен и более электрофилен в бутанале, чем в бутаноне. Бутанон имеет более высокую температуру кипения, чем бутаналь, потому что в бутаноне карбонильная группа более поляризована, чем у бутаналя.
Для этого диполь-дипольная сила притяжения у бутанона выше, чем у бутаналя, а температура кипения у бутанона выше, чем у бутаналя.
Функциональный изомер C4H8O4 stereochemistry
4 stereochemistryAdvertisement
1 of 55
Top clipped slide
Download to read offline
Advertisement
Advertisement
4 stereochemistry
- 4. Введение в стереохимию органических соединений • Основные понятия • Дифференциация соединений • Очень краткий исторический экскурс • Правило последовательности и его применение • E- и Z-диастереомерия • Соединения с несколькими хиральными центрами • Специальные области 174
- Стереохимия является разделом химии, посвященным изучению
расположения в пространстве атомов, составляющих молекулу, а
также их особенностей, ведущих к появлению стереоизомеров.
 ?
Стереохимия – отрасль химии, исследующая простанственное
строение молекул и его влияние на их физические и химические
свойства
Стереохимия:
•Статистическая (конфигурационная) – определение
конфигураций
•Конформационный анализ – внутренная жизнь
молекул в отсутствие химических реакций
•Динамическая – влияние пространственного строения
на направление и скорость реакций
•Теоретическая – математическое описание
?
• Основные понятия Основы стереохимии
175
?
Стереохимия – отрасль химии, исследующая простанственное
строение молекул и его влияние на их физические и химические
свойства
Стереохимия:
•Статистическая (конфигурационная) – определение
конфигураций
•Конформационный анализ – внутренная жизнь
молекул в отсутствие химических реакций
•Динамическая – влияние пространственного строения
на направление и скорость реакций
•Теоретическая – математическое описание
?
• Основные понятия Основы стереохимии
175 - • Очень краткий исторический экскурс 1810-е (?) – Берцелиус, понятие изомера 1840-е – Луи Пастер, расщепление тартратов 1874 – Я. Х. Вант-Гофф, Ж. А. Ле Бель, гипотеза о тетраэдре 1906 – М. А. Розанов, глицериновый альдегид 1951 – Bijvoet (Бейфут/Бейво), первое установление абсолютной конфигурации 1950-е – Д. Бартон, зарождение конформационного анализа 1966 – Р. Кан, К. Ингольд, В. Прелог, правило последовательностей 1969 – Р. Вудворд, Р. Хоффман, стереохимия перициклических реакций Что вам известно о развитии стереохимии в 70-е, 80-е и 90-е годы XX века??? А в XXI веке???!!! Из отзыва Кольбе на статью Вант-Гоффа: «Натурфилософия, побежденная 50 лет назад точным исследованием природы, в настоящее время снова выпущена псевдоестествоиспытателями из клетки, предназначенной для хранения отбросов человеческого ума» Основы стереохимии 176
- 177
- • Дифференциация химических
соединений
1.
 Разный качественный состав
Na2SO4 KNO3
2. Качественный состав одинаков, но:
разный количественный состав
NO NO2
3. Качественный и количественный состав одинаков, но:
разный молекулярный вес
C2h3 C6H6 C8H8
4. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение ИЗОМЕРЫ
C3H6O C3H6O C3H6O (назвать соединения)
5. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение СТЕРЕОИЗОМЕРЫ
Диастереомеры ???< >??? Энантиомеры
6. Что здесь должно быть???
Основы стереохимии
178
Разный качественный состав
Na2SO4 KNO3
2. Качественный состав одинаков, но:
разный количественный состав
NO NO2
3. Качественный и количественный состав одинаков, но:
разный молекулярный вес
C2h3 C6H6 C8H8
4. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение ИЗОМЕРЫ
C3H6O C3H6O C3H6O (назвать соединения)
5. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение СТЕРЕОИЗОМЕРЫ
Диастереомеры ???< >??? Энантиомеры
6. Что здесь должно быть???
Основы стереохимии
178 - • Основные понятия
Изомерами называют соединения, имеющие одинаковый
элементный состав, но различающиеся либо а) характером
последовательности связывания атомов, либо б) их расположением
в пространстве.
Если выполняется а) – структурные изомеры.
Если выполняется б) – стереоизомеры.
Стереоизомеры, которые не могут быть превращены в свои
зеркальные изображения только вращением вокруг связей или
путем смещения, являются хиральными. Пары таких
стереоизомеров называют энантиомерами.

- • Основные понятия Основы стереохимии 180
- • Правило последовательности и его применение С помощью правила последовательности лиганды могут быть расположены в порядке старшинства вокруг центрального атома Тетраэдр Старшинство лигандов (центральный атом не имеет значения, более того, его вообще может не быть): a > b > c > d (по падению старшинства) c d b a a b c d S-форма R-форма b d c a a c b d Основы стереохимии 181
- • Правило последовательности и его применение Вспомогательные правила определения старшинства 1. Больший атомный номер старше меньшего (неподеленная пара имеет «массу» 0) 2. Большее массовое число старше меньшего 3. Z > E 4. r старше, чем s (прохиральные группы) 5. R старше, чем S. M старше, чем P (хиральные группы) Cl Br Ch4 H Cl Ch3Br Ch4 H (R)-1-бромо-1-хлороэтан (S)-1-бромо-2-хлоропропан Основы стереохимии 182
- Тетраэдр, вытянутый в одном направлении
Старшинство лигандов (центральный атом не имеет значения, более
того, его вообще может не быть): a > b и a’ > b’.

- • Правило последовательности и его применение MeH HO2C c a b d OH H N N Cl Br (R)-3-бромо-1-[(2-хлорпиперидинил-1)гидроксиметил]- пиперидин (ВП-1 – вспомогательное правило 1) Назовите Основы стереохимии 184
- • E- и Z-диастереомерия Основы стереохимии 185
- • E- и Z-диастереомерия a b b’ a’ a b a’ b’ a > b, a’ > b’ E Z Me H H Me Me H Me Cl F H Cl F N Me H OH N N Ph Ph N N Ph Ph O E E Z Z Z E Основы стереохимии 186
- • Проекции Фишера (1891) Глицериновый альдегид R/S — ? HOCh3CH(OH)CHO OH OHO OH OHO HHO O OH OHH O OH CHO HHO Ch3OH CHO OHH Ch3OH DL Основы стереохимии 187
- • Проекции Фишера (1891) Fischer projection Fischer, E., Chem. Ber. 1891, 24, 1836 Fischer, E., Chem. Ber. 1891, 24, 2683 Основы стереохимии 188
- • Соединения с 2-мя хиральными центрами Все заместители разные – 4 изомера Основы стереохимии 189
- • Соединения с 2-мя хиральными центрами По два одинаковых – 4 изомера Основы стереохимии 190
- • Соединения с 2-мя хиральными центрами COOH HO H COOH HO H COOH H OH COOH HO H COOH HO H COOH H OH Винная кислота – 3 стереоизомера По три одинаковых – 3 изомера Основы стереохимии 191
- • Соединения с несколькими хиральными центрами COOH HO H HO H HO H HO H COOH Алларовая кислота – сколько стереоизомеров? (ВП-5) Основы стереохимии 192
- • Специальные области
Углеводы Аминокислоты
O
OH
OH
OH
OH
Ch3OH
CHO
OHH
HHO
OHH
OHH
Ch3OH
D-глюкоза,
или….
 ДЗ Назвать по
номенклатуре
β-D-
Глюкопираноза,
или….
ДЗ Назвать по
номенклатуре
COOH
h3N H
R
L-α-аминокислота
Основы стереохимии
193
ДЗ Назвать по
номенклатуре
β-D-
Глюкопираноза,
или….
ДЗ Назвать по
номенклатуре
COOH
h3N H
R
L-α-аминокислота
Основы стереохимии
193 - • Специальные области Стероиды Циклиты HO H Ch4 H H Ch4 H OH 1 2 3 4 5 6 7 810 11 12 13 14 15 16 17 HO OH 5α-андростандиол-3β,16β Циклоалканы, содержащие по одному гидроксилу при каждом из трех или более углеродных атомов в цикле. В случае 1,2,3,4,5,6-циклогексангексаола применяют название инозит Липиды, металлоорганика 1 2 3 4 5 6 Мио- инозит ДЗ. Нарисовать формулы всех инозитов, сколько и какие из них хиральны? Основы стереохимии 194
- • Специальные области Планарная хиральность 4. Основы стереохимии 195
- • Специальные области Гексагелицен Основы стереохимии 196
- Основы конформационного анализа • Основные понятия • Вращение вокруг связей, барьеры вращения • Конфомации этана, пропана и бутана • Алициклы, энергии напряжения • Циклогексан • От одного до шести заместителей в циклогексане • Декалины и стероиды • Циклогексанон и циклогексен • Два слова о пирамидальной инверсии 197
- (Tsukuba, Japan, 1996) Нобелевская премия по химии 1969 198
- • Основные понятия.
 Конформация – разные геометрические (пространственные)
формы, которые молекула может принимать в результате
вращения вокруг простых связей и других внутримолекулярных
движений, проходящих без нарушения целостности молекулы,
т.е. без разрыва химических связей (по Н. С. Зефирову и В. И.
Соколову).
Конформационный анализ – раздел стереохимии, изучающий
конформации молекул, из взаимопревращения и зависимость
физических и химических свойств от конформационных
характеристик
Обычно понятие конформера отождествляют с конформацией,
имеющей минимальную энергию. Явления существования
различных конформеров называют конформационной
изомерией.
Основы стереохимии
199
Конформация – разные геометрические (пространственные)
формы, которые молекула может принимать в результате
вращения вокруг простых связей и других внутримолекулярных
движений, проходящих без нарушения целостности молекулы,
т.е. без разрыва химических связей (по Н. С. Зефирову и В. И.
Соколову).
Конформационный анализ – раздел стереохимии, изучающий
конформации молекул, из взаимопревращения и зависимость
физических и химических свойств от конформационных
характеристик
Обычно понятие конформера отождествляют с конформацией,
имеющей минимальную энергию. Явления существования
различных конформеров называют конформационной
изомерией.
Основы стереохимии
199 - • Вращение вокруг связей, барьеры вращения, проекции Ньюмена H…H = 2.25H…H = 2.55 Основы стереохимии 200
- • Вращение вокруг связей, барьеры вращения Основы стереохимии 201
- • Вращение вокруг связей, барьеры вращения Основы стереохимии 202
- • Вращение вокруг связей, барьеры вращения Основы стереохимии 203
- • Вращение вокруг связей, барьеры
вращения
H
h3C
C
h3
H
H
H
H
H
2.

- • Конформации Взаимодействие Конформация Напряжение Энергия, ккал/моль H – H заслоненная торсионное 1,0 H – Ch4 заслоненная торсионное 1,4 Ch4 – Ch4 заслоненная торсионное и стерическое 3,4 Ch4 – Ch4 гош стерическое 0,9 H H H H H H H H H H H H H H H H H H H H H H H H H H (C12h36) Основы стереохимии 205
- • Вращение вокруг связей, барьеры вращения NMe2 NMe2 92 кДж/моль OMe CO2Me CO2Me OMe C CO2Me O OMe 116 кДж/моль Основы стереохимии 206
- • Алициклы, энергии напряжения Основы стереохимии 207
- • Алициклы, энергии напряжения Основы стереохимии 208
- • Алициклы, энергии напряжения Основы стереохимии 209
- • Конформации алициклов. Основы стереохимии 210
- • Циклогексан. Основы стереохимии 211
- •Циклогексан. Основы стереохимии 212
- • От одного до шести заместителей в циклогексане. Основы стереохимии 213
- • От одного до шести заместителей
в циклогексане.
H
H
H
H
H
H
2.58
H
H
H
H
H
2.
 34
Вырожденный
процесс
K ~ 0.001
Основы стереохимии
214
34
Вырожденный
процесс
K ~ 0.001
Основы стереохимии
214 - • Декалины и стероиды. HO OH ΔG = 51 кДж/моль Транс-декалин Цис-декалин Основы стереохимии 215
- • Циклогексанон и циклогексен. ΔG = 22 кДж/моль (ЦГ — 43) O O 0 13 кДж/моль (ЦГ — 22) Основы стереохимии 216
- • Два слова о пирамидальной инверсии NR3 N Ph N SO2Ph N Me N Cl Me Me Me Me N Me N Me N Me O N Me 47 52 78 100 43 34 65 28 20 – 30 кДж/моль Основы стереохимии 217
- • Устойчивость енолятов: стереохимия Основы стереохимии 218
- • Асимметрическое алкилирование енолятов Перенос хиральности с помощью хелатирования Основы стереохимии 219
- • Стереохимия альдольной реакции Z-енолят: Основы стереохимии 220
- • Стереохимия альдольной реакции Е-енолят: Основы стереохимии 221
- • Хиральные еноляты в альдольной реакции Оксазолидиноны Эванса Основы стереохимии 222
- • Хиральные еноляты в альдольной реакции Основы стереохимии 223
- • Реакция Михаэля: стереохимия Основы стереохимии 224
- • Реакция Михаэля: стереохимия Основы стереохимии 225
- • Правило последовательности и
его применение
OH H
N
N
Br
Br
OH H
N
N
Br
Br
OH H
N
N
Br
Br
OH H
N
N
Br
Br
ДЗ.
 Назвать указанные
соединения
Основы стереохимии
226
Назвать указанные
соединения
Основы стереохимии
226 - Основы стереохимии 227
- Попробуйте объяснить S R Основы стереохимии 228
Advertisement
Число возможных структурных изомеров в ${{\\text{C}}_{\\text{3}}}{{\\text{H}}_{\\text{6}}}\\text{ O}$ являются _______.(A) 9(B) 11(C) 5(D) 3
Ответ
Подтверждено
219,4 тыс.+ просмотров
Подсказка: чтобы найти количество структурных изомеров, возможных для соединения, мы должны сначала узнайте молекулярную структуру и молекулярную формулу этого соединения, а также количество атомов углерода, присутствующих в соединении, которые могут образовывать различные цепи связи. Я приведу все возможные изомеры, включая структуры, которые возможны в ${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}} \text{O}$ молекула.
Полное пошаговое решение :
> Структурные изомеры — это тип изомеров, в которых молекулы с одинаковой молекулярной формулой состоят из различных моделей связей и атомных организаций, которые противоположны стереоизомерам молекулярной связи всегда в одинаковом порядке и только пространственное расположение в них различно. В структурных изомерах мы можем идентифицировать их по характеру связывания. Обычно они имеют одинаковый атомный состав и молекулярный номер, но связаны таким образом, что различаются по функциональным группам. Простым примером структурного изомера могут быть н-бутан и изобутан, где н-бутан представляет собой прямую углеводородную цепь с четырьмя атомами углерода, тогда как изобутан по своей природе является разветвленным.
В структурных изомерах мы можем идентифицировать их по характеру связывания. Обычно они имеют одинаковый атомный состав и молекулярный номер, но связаны таким образом, что различаются по функциональным группам. Простым примером структурного изомера могут быть н-бутан и изобутан, где н-бутан представляет собой прямую углеводородную цепь с четырьмя атомами углерода, тогда как изобутан по своей природе является разветвленным.
> В вопросе указано следующее соединение: ${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}}\text{O} $, который имеет распространенное в ИЮПАК название пропаналь. Соединение, как мы видим, состоит из 3 атомов углерода и 6 атомов водорода, при этом в формуле присутствует функциональная группа кислорода. В нем не хватает двух атомов водорода по сравнению с насыщенным углеводородом. Имеющиеся структуры нуждаются в двойной связи для достижения стабильности. Двойная связь может возникать между двумя атомами углерода или между кислородом и атомом углерода. Это кольцо может быть полностью углеродным с внешним ионом гидроксония. Он также может включать кислород в кольцо. Изомеры ${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}}\text{O}$ включают
Он также может включать кислород в кольцо. Изомеры ${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}}\text{O}$ включают
Как видно из диаграммы, 11 структурных изомеров представляют собой пропаналь, транс-1-пропенол, цис-1-пропенол, ацетон, 2-пропен-2-ол, метилвиниловый эфир, 2-пропен-1-ол. , оксациклобутан, циклопропанол, (S)-1,2-эпоксипропан, (R)-1,2-эпоксипропан.
Отсюда видно, что всего 11 структурных изомеров ${{\text{C}}_{\text{3}}}{{\text{H}}_{\text{6}}}\text {O}$ возможны.
Таким образом, правильным вариантом является Вариант Б.
Примечание: В таких случаях, когда нам нужно указать изомеры, нам всегда нужно проверять молекулярную формулу данного соединения. С помощью молекулярной формулы мы можем сформировать молекулярную структуру и, в зависимости от этой структуры, мы можем проанализировать, является ли соединение оптически активным, состоит ли оно из структурных или функциональных изомеров и т. д.
Дата последнего обновления: 23 апр 2023
•
Всего просмотров: 219. 4k
4k
•
Просмотров сегодня: 4.87k
Недавно обновленные страницы 90 003
Большинство эубактериальных антибиотиков получают из биологии Rhizobium класса 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологии класса 12 А NEET_UG
Какое из следующих утверждений относительно бакуловирусов класса 12 биологии NEET_UG
Канализационные или муниципальные канализационные трубы не должны относиться непосредственно к биологии класса 12 NEET_UG
Очистка сточных вод осуществляется A Микробами B Удобрения класса 12 биологии NEET_UG
Иммобилизация ферментов – это A Превращение активного фермента класса 12 биологии NEET_UG
Большинство эубактериальных антибиотиков получают из A Rhizobium класса 12 биологии NEET_UG 900 03
Биоинсектициды Саламин экстрагированы из 12-го класса биологии NEET_UG
Какое из следующих утверждений относительно бакуловирусов 12-го класса биологии NEET_UG
Канализационные или муниципальные канализационные трубы не должны относиться непосредственно к 12-му классу биологии NEET_UG
Очистка сточных вод осуществляется A Микробами B Удобрения класса 12 биологии NEET_UG
Иммобилизация ферментов – это A Преобразование активного фермента класса 12 биологии NEET_UG
Тенденции сомнений 900 03
Нарисуйте функциональный изомер C3H6O.
- Курс
- NCERT
- Класс 12
- Класс 11
- Класс 10
- Класс 9
- Класс 8 900 70 Класс 7
- Класс 6
- NCERT
- IIT JEE
- Экзамен
- JEE MAINS
- JEE ADVANCED
- X BOARDS 9007 0 XII BOARDS
- NEET
- Neet Предыдущий год (по годам)
- Физика Предыдущий год
- Химия Предыдущий год
- Биология Предыдущий год
- Новый Все образцы работ
- Образцы работ по биологии
- Образцы работ по физике
- Образцы работ по химии
- Скачать в формате PDF 0 Класс 7
- Класс 6
- Экзаменационный уголок
- Онлайн-класс
- Викторина
- Задайте вопрос в Whatsapp
- Поиск Doubtnut
- Английский словарь
- Топперы говорят
- Блог
- О нас
- Карьера
- Скачать
- 90 070 Получить приложение
Вопрос
Обновлено: 15. 05.2021
05.2021
РЕЗОНАНС АНГЛИЙСКИЙ-IUPAC НОМЕНКЛАТУРА И СТРУКТУРА ИЗОМЕРИЯ — Упражнение-2 Часть-2
11 видеоРЕКЛАМА
Текстовое решение
Проверено экспертами
Правильный ответ:
D
Был ли этот ответ полезен?
140
Ab Padhai каро бина объявления ке
Khareedo DN Про и дехо сари видео бина киси объявление ки рукаават ке!
Похожие видео
C3H6O के दो समावयवी हैं। ये किस प्रकार की समावयवता प्रदर्शित करते हैं?
94848678
04:47
C3H6O সংকেতবিশিষ্ট বিভিন্ন কা র্যকরী গ্রুপঘটিত দুটি সাইক্লিক ও দুটি অ্যাসাই ক্লিক আইসােমারের উদাহরণ দাও ।
443048524
05:23
Функциональные изомеры
443912627
52:18
Нарисуйте структуры этих геометрических изомеров.
571113218
Текст Раствор
[«Ацетон и»],[«пропаналь»],[«позиционные изомеры»,[«функциональные изомеры»,[«геометрические изомеры»,[«оптические изомеры»]
583913554
03:09
Изобразите возможные изомеры соединения с молекулярной формулой C_3H_6O и укажите их точечную структуру.
599731162
02:44
Изобразите геометрические изомеры вышеуказанного соединения.
642
Текст Решение
Напишите функциональные изомеры соединения с MF-C_3H_6O.
643223125
03:42
Структурные изомеры, цепные изомеры, изомеры положения, функциональные изомеры
643455892
01:06:38 900 03
Нарисуйте строение изомеров пентана.
643825176
04:55
Изобразите геометрические изомеры бут-2-ена.
644030164
01:02
……………. И ………………… Исправны изомеры.
644035699
02:26
Нарисуйте строение изомеров бутана.
644449329
03:08
Дро-изомеры C4h20
644535682
01:43
Эфир – функциональный изомер спирта: это спирт, не имеющий функционального изомера.
645094426
00:30
РЕКЛАМА
РЕЗОНАНС АНГЛИЙСКАЯ НОМЕНКЛАТУРА ИЮПАК И СТРУКТУРНАЯ ИЗОМЕРИЯ — Упражнение-2 Часть-2
Углеводород (R) имеет шестичленное кольцо, в котором нет ненасыщенных.
 .. 003
.. 003Количество соединений, в которых атом углерода функциональной группы может…
06:51
Нарисуйте функциональный изомер C3H6O .
01:51
Сколько возможно структурно изомерных дибромбутанов.
03:00
Число ациклических структурных изомеров C(5)H(10).
03:20
Сколько всего структурно-изомерных диенов с молекулярным…
02:46
Сколько структурных алкенов формулы C(2)FClBrI возможно:
01: 52
Сколько возможно тетраметилбензола:
02:35
Сколько структурно изомерных циклических изомеров молекулярной формулы C(3…
02:05
Количество структурно-изомерных эфиров с молекулярной формулой C(5H…
04:52
- Ask Unlimited Doubts
- Видеорешения на нескольких языках (включая хинди)
- Видеолекции экспертов
- Бесплатные PDF-файлы (документы за предыдущий год, решения для книг и многое другое)
- Посещение специальных консультационных семинаров для IIT-JEE, NEET и экзаменов Совета
Doubtnut хочет отправлять вам уведомления.

 ?
Стереохимия – отрасль химии, исследующая простанственное
строение молекул и его влияние на их физические и химические
свойства
Стереохимия:
•Статистическая (конфигурационная) – определение
конфигураций
•Конформационный анализ – внутренная жизнь
молекул в отсутствие химических реакций
•Динамическая – влияние пространственного строения
на направление и скорость реакций
•Теоретическая – математическое описание
?
• Основные понятия Основы стереохимии
175
?
Стереохимия – отрасль химии, исследующая простанственное
строение молекул и его влияние на их физические и химические
свойства
Стереохимия:
•Статистическая (конфигурационная) – определение
конфигураций
•Конформационный анализ – внутренная жизнь
молекул в отсутствие химических реакций
•Динамическая – влияние пространственного строения
на направление и скорость реакций
•Теоретическая – математическое описание
?
• Основные понятия Основы стереохимии
175 Разный качественный состав
Na2SO4 KNO3
2. Качественный состав одинаков, но:
разный количественный состав
NO NO2
3. Качественный и количественный состав одинаков, но:
разный молекулярный вес
C2h3 C6H6 C8H8
4. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение ИЗОМЕРЫ
C3H6O C3H6O C3H6O (назвать соединения)
5. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение СТЕРЕОИЗОМЕРЫ
Диастереомеры ???< >??? Энантиомеры
6. Что здесь должно быть???
Основы стереохимии
178
Разный качественный состав
Na2SO4 KNO3
2. Качественный состав одинаков, но:
разный количественный состав
NO NO2
3. Качественный и количественный состав одинаков, но:
разный молекулярный вес
C2h3 C6H6 C8H8
4. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение ИЗОМЕРЫ
C3H6O C3H6O C3H6O (назвать соединения)
5. Качественный и количественный состав и молекулярный вес одинаковы, но:
разное строение СТЕРЕОИЗОМЕРЫ
Диастереомеры ???< >??? Энантиомеры
6. Что здесь должно быть???
Основы стереохимии
178

 ДЗ Назвать по
номенклатуре
β-D-
Глюкопираноза,
или….
ДЗ Назвать по
номенклатуре
COOH
h3N H
R
L-α-аминокислота
Основы стереохимии
193
ДЗ Назвать по
номенклатуре
β-D-
Глюкопираноза,
или….
ДЗ Назвать по
номенклатуре
COOH
h3N H
R
L-α-аминокислота
Основы стереохимии
193 Конформация – разные геометрические (пространственные)
формы, которые молекула может принимать в результате
вращения вокруг простых связей и других внутримолекулярных
движений, проходящих без нарушения целостности молекулы,
т.е. без разрыва химических связей (по Н. С. Зефирову и В. И.
Соколову).
Конформационный анализ – раздел стереохимии, изучающий
конформации молекул, из взаимопревращения и зависимость
физических и химических свойств от конформационных
характеристик
Обычно понятие конформера отождествляют с конформацией,
имеющей минимальную энергию. Явления существования
различных конформеров называют конформационной
изомерией.
Основы стереохимии
199
Конформация – разные геометрические (пространственные)
формы, которые молекула может принимать в результате
вращения вокруг простых связей и других внутримолекулярных
движений, проходящих без нарушения целостности молекулы,
т.е. без разрыва химических связей (по Н. С. Зефирову и В. И.
Соколову).
Конформационный анализ – раздел стереохимии, изучающий
конформации молекул, из взаимопревращения и зависимость
физических и химических свойств от конформационных
характеристик
Обычно понятие конформера отождествляют с конформацией,
имеющей минимальную энергию. Явления существования
различных конформеров называют конформационной
изомерией.
Основы стереохимии
199
 34
Вырожденный
процесс
K ~ 0.001
Основы стереохимии
214
34
Вырожденный
процесс
K ~ 0.001
Основы стереохимии
214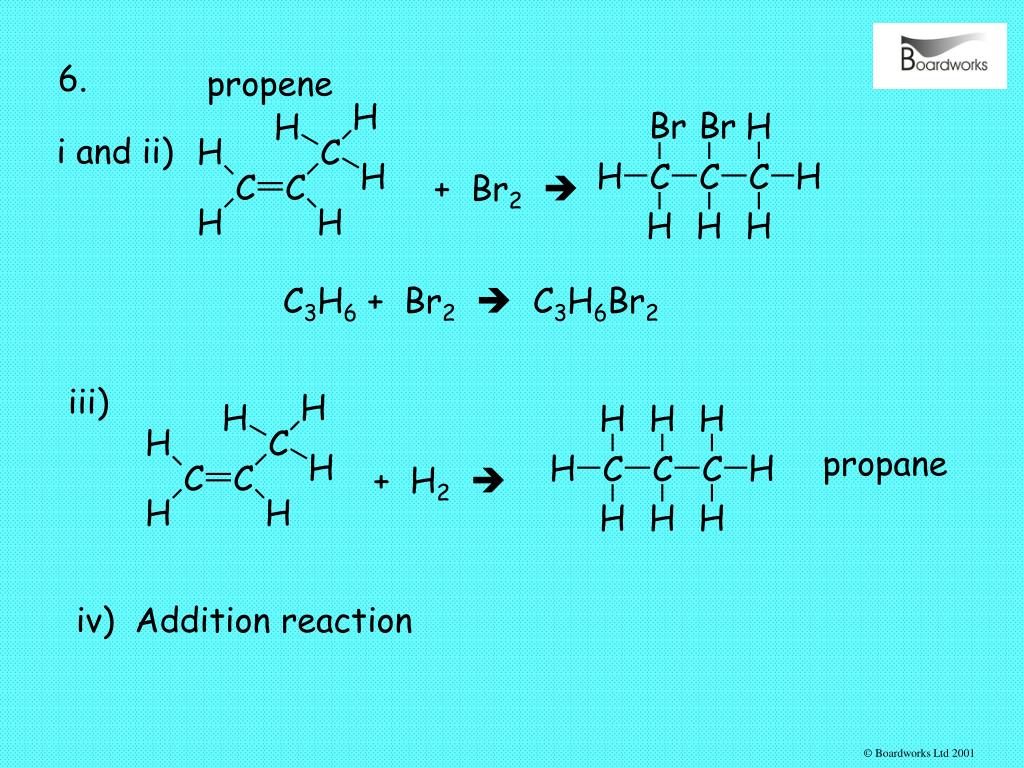 Назвать указанные
соединения
Основы стереохимии
226
Назвать указанные
соединения
Основы стереохимии
226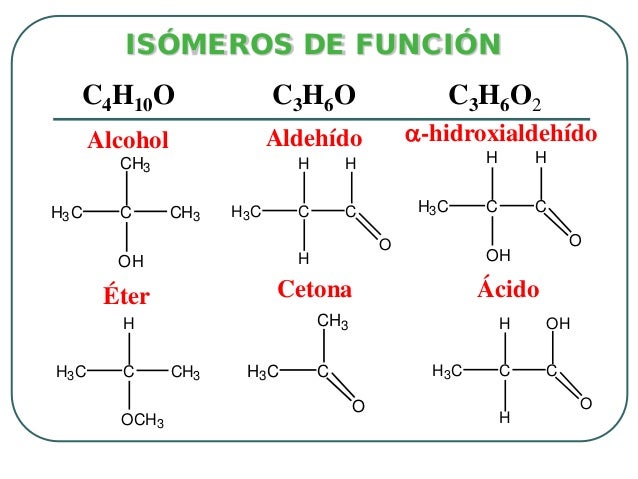 .. 003
.. 003
Leave A Comment