Ресурсы |
|
Версия для слабовидящих
Объявления Уважаемые родители! В разделе Методические материалы размещен список сайтов дистанционного обучения. * * * На очном отделении свободных мест нет. Уважаемые родители! Секретарю и директору школы можно позвонить по тел. +20237485636 с 9.00 до 13.00 (кроме пятницы и субботы). |
Алкадиены, подготовка к ЕГЭ по химии
Алкадиены — непредельные (ненасыщенные) углеводороды, имеющие в молекуле две двойных связи С=С. Каждая такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкадиены также называют диеновыми углеводородами. Первый член гомологического ряда — пропадиен — CH2=C=CH
Номенклатура и изомерия алкадиенов
Названия алкадиенов формируются путем добавления суффикса «диен» к названию алкана с соответствующим числом:
пропадиен, бутадиен, пентадиен и т.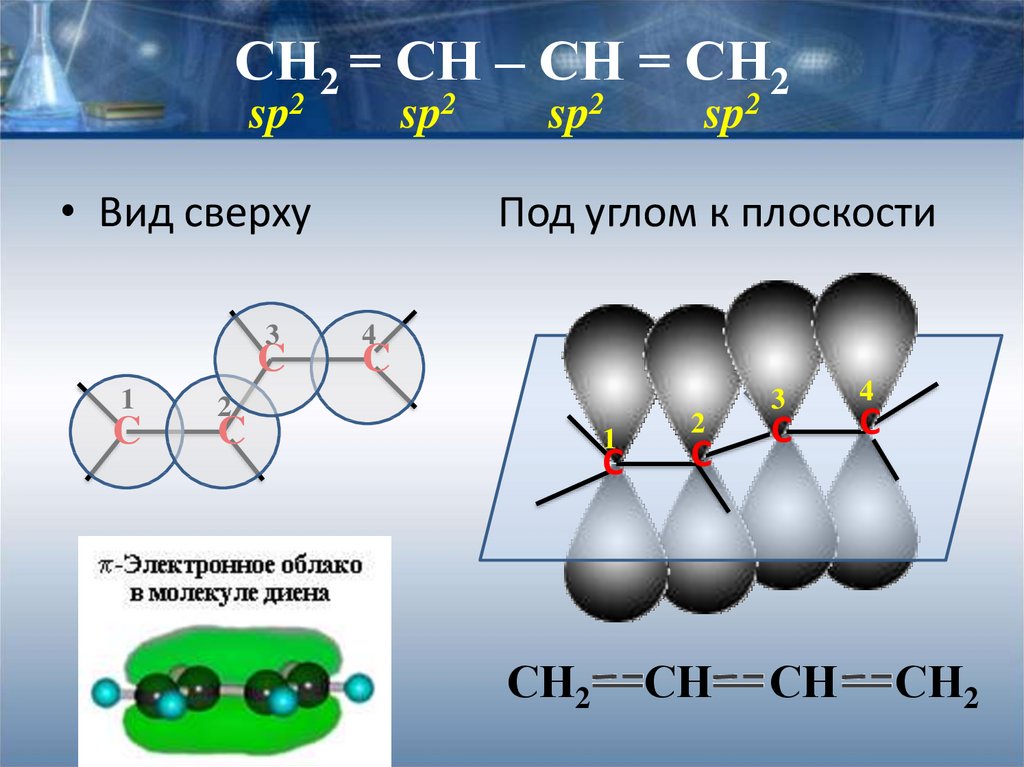 д.
д.
При составления названия алкадиена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойные связи. Нумерация атомов углерода в ней начинается с того края, к которому ближе двойная связь. В конце названия указывают атомы углерода, у которых начинается двойная связь.
Атомы углерода, прилежащие к двойной связи находятся в sp2 гибридизации.
Для алкадиенов характерна изомерия углеродного скелета, положения двойных связей, межклассовая изомерия с алкинами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Также к синтетическим каучукам относится бутадиен-1,3 (дивинил).
Классификация по положению двойных связей
В зависимости от того, как чередуются двойные связи в молекуле алкадиена, они подразделяются на следующие типы:
- Кумулированные двойные связи
- Сопряженные двойные связи
- Изолированные двойные связи
В случае, если две двойные связи прилежат к одному и тому же атому углерода.
Пример — пропадиен-1,2 (аллен) — CH2=C=CH2
В молекуле аллена крайние атомы углерода находятся в состоянии sp2-гибридизации, а центральный атом — sp-гибридизации.
В случае, если две двойные связи разделены одной одинарной связью. В результате такого взаиморасположения в молекулах возникает сопряжение: формируется единое π-электронное облако.
Помните, что сигма-связи (σ-связи) перекрываются вдоль линии плоскости, а пи-связи (π-связи) над и под линией плоскости (линией, соединяющей центры атомов).
Пример — бутадиен-1,3 — CH2=CH-CH=CH2
В случае, если две двойные связи разделены двумя и более одинарными связями.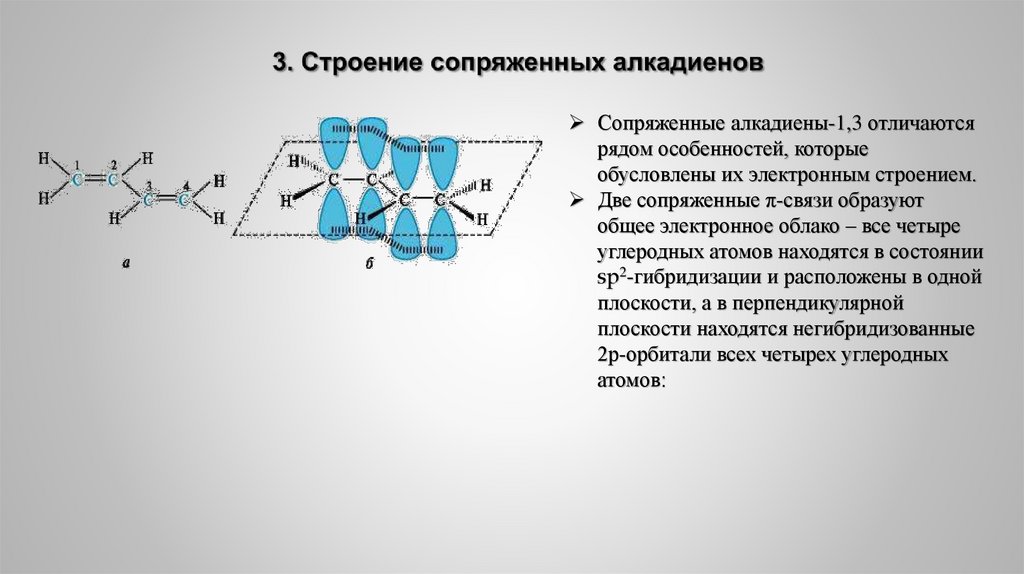
Пример — пентадиен-1,4 — CH2=CH-CH2-CH=CH2
Получение алкадиенов
Алкадиены получают несколькими способами:
- Дегидрогалогенирование дигалогеналканов
- Синтез С.В. Лебедева
- Дегидрирование алканов
В результате реакции молекулы алкана, содержащей два атома галогена, со спиртовым (!) раствором щелочи получается алкадиен. В зависимости от положения галогенов возможны разные варианты.
Отщепление идет по правилу Зайцева: атом водорода отщепляется от соседнего, наименее гидрированного атома углерода.
Сергей Васильевич Лебедев в 1927 году разработал первый промышленный способ получения синтетического каучука из этилового спирта.
2CH3-CH2-OH → (450 °C, кат. ZnO) CH2=CH-CH=CH2 + 2H2O
+ H2
ZnO) CH2=CH-CH=CH2 + 2H2O
+ H2
Каучук занимает важное место в промышленности благодаря своим свойствам: водонепроницаемости, эластичности и способности к электроизоляции. Путем вулканизации из каучука получают резину, используемую повсеместно.
В результате отщепления водорода от молекулы алкана образуются двойные связи. Дегидрирование происходит при повышенной температуре и в присутствии катализатора.
Химические свойства алкадиенов
Алкадиены — ненасыщенные углеводороды, легко вступающие в реакции присоединения. Реакции замещения для них не характерны.
Наличие сопряженных двойных связей увеличивает реакционную способность молекулы и обуславливает необычный механизм некоторых реакций.
- Гидрирование
- Галогенирование
- Гидрогалогенирование
- Окисление
- Полимеризация
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение брома по кратным связям к органическому веществу.
В случае, если двойные связи находятся в сопряжении, выход продуктов во многом зависит от температуры. Например, в ходе галогенирования бутадиена-1,3 при -80°C преимущественно получается продукт 1,2-присоединения, а при +60°C — продукт 1,4-присоединения.
Алкадиены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.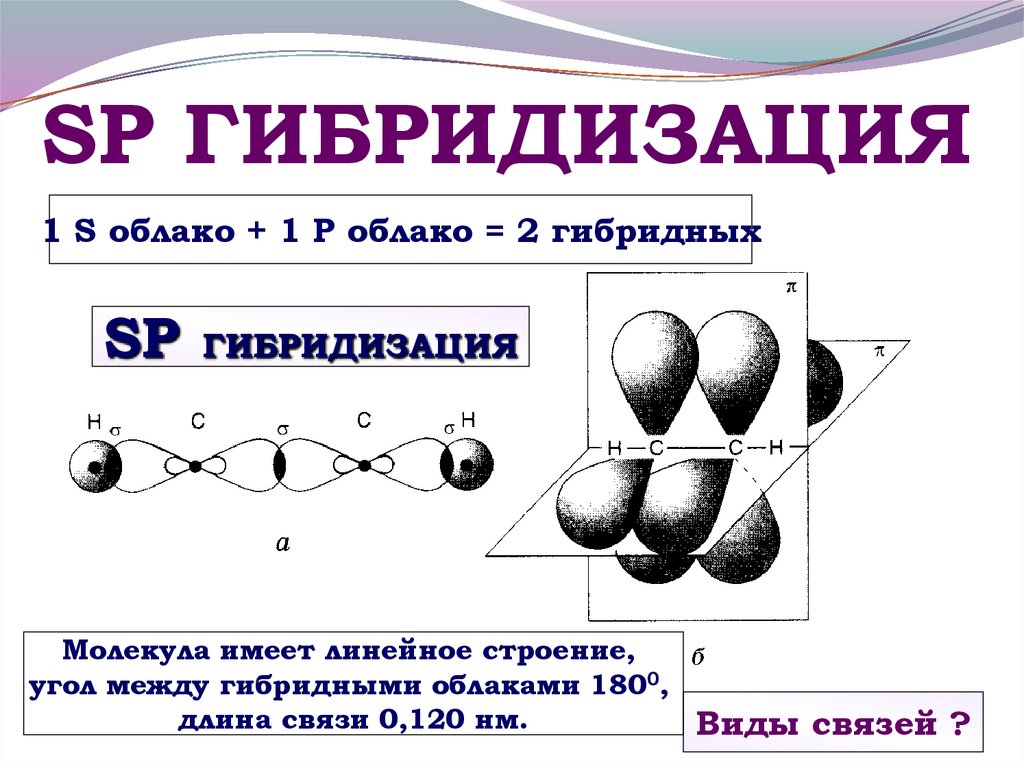
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена — к наименее гидрированному атому углерода.
При горении алкадиены, как и все органические соединения, сгорают с образованием углекислого газа и воды — полное окисление.
2CH2=CH-CH=CH2 + 11O2 → 8CO2 + 6H2O
Полимеризация — цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.
Индекс «n», степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
© Беллевич Юрий Сергеевич 2018-2023
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
Копирование, распространение
(в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов
без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования,
обратитесь, пожалуйста, к Беллевичу Юрию.
2.2: Стабильность сопряженных диенов — молекулярная орбитальная теория
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 418206
Цели
После завершения этого раздела вы сможете
- напишите последовательность реакций, чтобы показать удобный способ получения данного сопряженного диена из алкена, аллилгалогенида, алкилдигалогенида или спирта (диола).

- определяют реагенты, необходимые для получения данного диена из одного из исходных материалов, перечисленных в Задаче 1 выше.
- сравните стабильность сопряженных и несопряженных диенов, используя данные, полученные в результате экспериментов по гидрированию.
- обсуждают связывание в сопряженном диене, таком как 1,3-бутадиен, с точки зрения гибридизации вовлеченных атомов углерода.
- обсудите связь в 1,3-бутадиене с точки зрения теории молекулярных орбиталей и нарисуйте молекулярную орбиталь для этого и подобных соединений.
Ключевые термины
Убедитесь, что вы можете определить и использовать в контексте ключевые термины ниже.
- делокализованные электроны
- узел
Сопряженные и несопряженные диены
Диены представляют собой соединения, содержащие две двойные связи. Эти диены могут быть несопряженными (две двойные связи разделены по крайней мере одной sp 3 гибридизированный атом. Сопряженные диены имеют две двойные связи, разделенные одинарной связью. Сопряженные диены обладают свойствами и реакционной способностью, которые явно отличаются от несопряженных диенов. Определение того, сопряжены ли двойные связи, представляет собой важный навык в органической химии.
Сопряженные диены имеют две двойные связи, разделенные одинарной связью. Сопряженные диены обладают свойствами и реакционной способностью, которые явно отличаются от несопряженных диенов. Определение того, сопряжены ли двойные связи, представляет собой важный навык в органической химии.
Стабильность сопряженных диенов
Известно, что сопряженные диены более стабильны, чем несопряженные диены, о чем свидетельствуют экспериментально определенные теплоты гидрирования. По мере того как алкены становятся более стабильными, они содержат меньше энергии и, следовательно, выделяют меньше тепла при гидрировании. Эксперименты показали, что сопряженные диены имеют более низкую теплоту гидрирования (-226 кДж/моль), чем несопряженные диены (-251 кДж/моль). Используя различия в теплотах гидрирования, можно оценить энергию стабилизации в сопряженных диенах примерно в 25 кДж/моль.
Вот энергетическая диаграмма, сравнивающая различные типы связей с их теплотой гидрирования, чтобы показать относительную стабильность каждой молекулы:
Стабилизация диенов конъюгацией менее драматична, чем ароматическая стабилизация бензола. Тем не менее, аналогичные резонансные и молекулярные орбитальные описания сопряжения могут быть написаны.
Тем не менее, аналогичные резонансные и молекулярные орбитальные описания сопряжения могут быть написаны.
Каждый алкеновый углерод в 1,3-диенах sp 2 гибридизован и, следовательно, имеет один негибридизированный р орбитальный. Четыре орбитали p в 1,3-бутадиене перекрываются, образуя сопряженную систему, которая может быть представлена резонансными формами, показанными ниже. Эта делокализация зарядов стабилизирует сопряженные диены, делая их более стабильными, чем несопряженные диены.
Свидетельство сопряжения в 1,3-диенах проявляется в том, что одинарная связь прочнее и короче (147 пм), чем обычная алкановая связь С-С (154 пм). Резонансный гибрид 1,3-бутадиена показывает, что эта связь содержит значительный характер двойной связи, при этом ее длина связи составляет примерно среднее значение одинарной и двойной связи.
Делокализованную электронную плотность 1,3-диена можно увидеть при просмотре карт электростатического потенциала. В сопряженных диенах наблюдается, что перекрытие пи-электронной плотности (показано красным) ближе друг к другу и делокализовано в сопряженных диенах, тогда как в несопряженных диенах пи-электронная плотность полностью расположена на двойных связях.
В сопряженных диенах наблюдается, что перекрытие пи-электронной плотности (показано красным) ближе друг к другу и делокализовано в сопряженных диенах, тогда как в несопряженных диенах пи-электронная плотность полностью расположена на двойных связях.
Молекулярные орбитали 1,3-диенов
Согласно теории МО, когда двойная связь не сопряжена, два атома 2 p z орбитали объединяются, образуя две pi (π) молекулярных орбиталей , одну низкоэнергетическую π-связывающую орбиталь и одну высокоэнергетическую π-звезду (π*) разрыхляющую молекулярную орбиталь . Иногда они обозначаются на диаграммах МО, подобных приведенной ниже, греческой буквой psi (Ψ) вместо π. В связывающей орбитали Ψ 1 две (+) доли орбиталей 2p z конструктивно взаимодействуют друг с другом, как и две (-) доли. Следовательно, между ядрами на молекулярной орбитали повышена плотность электронов, поэтому она является связывающей орбиталью. В высокоэнергетической разрыхляющей связи Ψ 2 * орбиталь, (+) доля одной 2 p z орбитали деструктивно взаимодействует с (-) долей второй 2 p z орбитали, приводя к узлу между двумя ядрами и общее отвращение. Согласно принципу aufbau , два электрона с двух атомных орбиталей будут спарены на более низкоэнергетической орбитали Ψ 1 , когда молекула находится в основном состоянии.
В высокоэнергетической разрыхляющей связи Ψ 2 * орбиталь, (+) доля одной 2 p z орбитали деструктивно взаимодействует с (-) долей второй 2 p z орбитали, приводя к узлу между двумя ядрами и общее отвращение. Согласно принципу aufbau , два электрона с двух атомных орбиталей будут спарены на более низкоэнергетической орбитали Ψ 1 , когда молекула находится в основном состоянии.
С сопряженным диеном, таким как 1,3-бутадиен, четыре 2p атомные орбитали объединяются, образуя четыре пи молекулярных орбитали с возрастающей энергией. Две связывающие пи-орбитали и две антисвязывающие пи*-орбитали. Комбинация четырех пи молекулярных орбиталей позволяет образовать связывающую молекулярную орбиталь с меньшей энергией, чем у несопряженного алкена. 4 пи-электрона 1,3-бутадиена полностью заполняют связывающие молекулярные орбитали, что придает дополнительную стабильность, связанную с сопряженными двойными связями.
2.2: Stability of Conjugated Dienes-Molecular Orbital Theory распространяется под лицензией CC BY-SA 4.0, авторами, ремиксами и/или кураторами являются Steven Farmer, Dietmar Kennepohl, Layne Morsch, Tim Soderberg, William Reusch и William. Реуш.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.
- Теги
- автор@Дитмар Кеннеполь
- автор@Лейн Морш
- автор@Стивен Фармер
- автор @ Тим Содерберг
- автор@William Reusch
- Конъюгированные диены
- спряжение
- источник[1]-chem-31549
Краткие заметки о стабилизации 1,3-бутадиина и 1,3-бутадиена
Несмотря на то, что бутадиен быстро разлагается в атмосфере, тем не менее он обнаруживается в атмосферном воздухе в городских и пригородных районах в результате частых автомобильных выбросы.
Изомер 1,2-бутадиена, представляющий собой кумулятивный диен со структурой H₂C=C=CHCH3, также известен как бутадиен. Этот аллен не используется ни в одной промышленности.
Производство Извлечение из углеводородов C4Бутадиен создается как побочный продукт процесса парового крекинга, используемого для получения этилена и других алкенов в США, Западной Европе и Японии. Когда алифатические углеводороды смешивают с паром и нагревают до чрезвычайно высоких температур (обычно свыше 900°С) выделяется водород, в результате чего образуется сложная комбинация непредельных углеводородов, в том числе бутадиена. Количество произведенного бутадиена определяется углеводородами, которые используются в качестве сырья. При крекинге легкого сырья, такого как этан, основным продуктом является этилен, но более тяжелое сырье дает более тяжелые олефины, бутадиен и ароматические углеводороды.
Экстрактная перегонка с полярным апротонным растворителем, таким как ацетонитрил, N-метил-2-пирролидон, фурфурол или диметилформамид, используется для отделения бутадиена от других четырехуглеродных углеводородов, полученных при крекинге с водяным паром, из которых он затем отделяется перегонкой .
Нормальный бутан также может быть подвергнут каталитическому дегидрированию с получением бутадиена (н-бутана). В Хьюстоне, штат Техас, в 1957 году открылась первая послевоенная коммерческая фабрика, производившая 65 000 тонн бутадиена в год. До этого компания Rubber Reserve, подразделение правительства США, построила многочисленные заводы в Боргере, штат Техас, Толедо, штат Огайо, и Эль-Сегундо, штат Калифорния, в рамках программы США по производству синтетического каучука, чтобы производить синтетический каучук для войны. усилие. Общая мощность составляла 68 тыс. тонн в год (километрических тонн в год).
Метод Houdry Catadiene, открытый во время Второй мировой войны, в настоящее время используется для коммерческого производства бутадиена из н-бутана. Это требует обработки бутана при высоких температурах над глиноземом и хромом.
Из бутенов Каталитическое дегидрирование типичных бутенов также может давать 1,3-бутадиен. Во время Второй мировой войны программа синтетического каучука США (USSRP) приняла этот подход. Этот метод был намного дешевле, чем использование спирта или н-бутана, но ему приходилось конкурировать с авиационным топливом за доступные молекулы бутена (бутены были в изобилии благодаря каталитическому крекингу). В Батон-Руж и Лейк-Чарльз, штат Луизиана; Хьюстон, Бэйтаун и Порт-Нечес, Техас; и Торранс, Калифорния, СССР построил много заводов. Всего было произведено 275 кмТА в год.
Во время Второй мировой войны программа синтетического каучука США (USSRP) приняла этот подход. Этот метод был намного дешевле, чем использование спирта или н-бутана, но ему приходилось конкурировать с авиационным топливом за доступные молекулы бутена (бутены были в изобилии благодаря каталитическому крекингу). В Батон-Руж и Лейк-Чарльз, штат Луизиана; Хьюстон, Бэйтаун и Порт-Нечес, Техас; и Торранс, Калифорния, СССР построил много заводов. Всего было произведено 275 кмТА в год.
В 1960-х годах компания из Хьюстона, известная как «Петро-Текс», разработала метод окислительного дегидрирования с использованием запатентованного катализатора для получения бутадиена из обычных бутенов. Неизвестно, используется ли этот метод в коммерческих целях.
Для лабораторного использования Поскольку 1,3-бутадиен представляет собой газ, его трудно использовать в лаборатории. Его производство из негазообразных прекурсоров оптимизировано в лаборатории. Его может создать ретро-реакция Дильса-Альдера циклогексена. В лаборатории сульфолен представляет собой полезный твердый хранимый источник 1,3-бутадиена. При нагревании выделяются диен и диоксид серы.
В лаборатории сульфолен представляет собой полезный твердый хранимый источник 1,3-бутадиена. При нагревании выделяются диен и диоксид серы.
Заключение
Большая часть бутадиена используется для производства синтетических каучуков для шин, люверсов и эластичных лент. Полимеризация, процесс, в котором небольшие молекулы (мономеры) соединяются с образованием более крупных, используется для превращения бутадиена в синтетические каучуки (полимеры). Полимеризация бутадиена приводит к полибутадиену, очень мягкому, почти жидкому веществу. Сополимеры создаются путем полимеризации бутадиена и других мономеров, поэтому они более ценны. Полимеризация бутадиена и стирола и/или полимеризация акрилонитрила, такая как акрилонитрил-бутадиен-стирол (ABS), нитрил-бутадиен (NBR) и полимеризация стирол-бутадиен (SBR). В зависимости от соотношений мономеров, используемых при их производстве, эти сополимеры являются прочными и/или эластичными. SBR является наиболее часто используемым веществом в производстве автомобильных шин.


Leave A Comment