Задание 1 ЕГЭ по химии 2023: теория и практика
За это задание ты можешь получить 1 балл. На решение дается около 3 минут. Уровень сложности: базовый.
Средний процент выполнения: 79.2%
Ответом к заданию 1 по химии может быть последовательность цифр, чисел или слов. Порядок записи имеет значение.
Задача 1
1) N 2) S 3) P 4) Se 5) As
Определите, атомы каких из указанных в ряду элементов имеют в возбуждённом состоянии электронную конфигурацию внешнего энергетического уровня ns1np3nd1. Запишите в поле ответа номера выбранных элементов.
Решение
Электронная конфигурация ns1np3nd1 в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 5 электронов, значит нужны элементы из пятой группы главной подгруппы, таких три: азот, фосфор и мышьяк. Однако атом азота не может переходить в возбужденное состояние, так как на втором энергетическом уровне нет d — подуровня, следовательно, ответ: фосфор и мышьяк. {6}$ имеет ксенон Xe, который находится в главной подгруппе VIII группы пятого периода, следовательно, анионы с такой электронной конфигурацией могут образовывать атомы неметаллов, находящихся в пятом периоде, т. е. теллур (ответ — 1) и йод (ответ — 2).
{6}$ имеет ксенон Xe, который находится в главной подгруппе VIII группы пятого периода, следовательно, анионы с такой электронной конфигурацией могут образовывать атомы неметаллов, находящихся в пятом периоде, т. е. теллур (ответ — 1) и йод (ответ — 2).
Вывод: правильные ответы — 1, 2.
Ответ: 12
Показать решение
Бесплатный интенсив
Задача 3
1) Al 2) S 3) P 4) Cr 5) Si
Определите, атомы каких из указанных в ряду элементов в основном состоянии во внешнем слое содержат один неспаренный электрон. Запишите в поле ответа номера выбранных элементов.
Решение
Здесь лучше всего расписать конфигурации атомов, но можно и запомнить, что 1 неспаренный электрон на внешнем уровне имеют атомы элементов 1,3 и 7 групп или атомы элементы с провалом электрона. В 3 группе находится алюминий (
Ответ: 14
Показать решение
Бесплатный интенсив
Задача 4
1) Mg 2) Bi 3) Ba 4) Sr 5) Al
Определите, катионы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня 3s0. 0$ означает, что данный элемент, образующий такой катион, имеет три энергетических уровня, следовательно, в таблице Менделеева находится в III периоде. Из представленных элементов в III периоде находятся Mg и Al.
0$ означает, что данный элемент, образующий такой катион, имеет три энергетических уровня, следовательно, в таблице Менделеева находится в III периоде. Из представленных элементов в III периоде находятся Mg и Al.
Ответ: 12
Показать решение
Бесплатный интенсив
Задача 10
1) Cu 2) Te 3) Se 4) Ag 5) O
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию внешнего энергетического уровня ns1(n–1)d10. Запишите в поле ответа номера выбранных элементов.
Решение
Элементы с такой конфигурацией должны находиться в побочной подгруппе, поскольку заполняется d подуровень ( произошел перескок электрона в связи с устойчивостью полностью заполненного d подуровня), поскольку внешних электронов 1, то группа первая. Ищем элементы I группы побочной подгруппы.
Ответ: 14
Показать решение
Бесплатный интенсив
Задача 11
1) Ti 2) Cl 3) Zr 4) I 5) F
Определите, атомы каких из указанных в ряду элементов имеют электронную конфигурацию энергетического уровня ns2(n–1)d2. 2$ в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 6 электронов, значит нужны элементы из шестой группы главной подгруппы, таких два: сера и селен.
2$ в возбужденном состоянии показывает, что на внешнем слое у атома будет расположено 6 электронов, значит нужны элементы из шестой группы главной подгруппы, таких два: сера и селен.
Ответ: 25
Показать решение
Бесплатный интенсив
Задача 19
1) As 2) Cr 3) Na 4) V 5) Sc
Определите, атомы каких из указанных в ряду элементов имеют 1 неспаренный электрон во внешнем слое в основном состоянии. Запишите в поле ответа номера выбранных элементов.
Решение
Для определения количества неспаренных электронов на внешнем слое нужно представить электронную конфигурацию атома. Атом натрия находится в 3 периоде, поэтому имеет 3 слоя. Всего он имеет 11 электронов, поэтому на последнем слое атом натрия имеет один неспаренный электрон. Атом хрома находится в 4 периоде, он имеет 4 слоя, 3d подуровень заполняется после 4s, но у хрома происходит провал электрона, один электрон с 4s падает на 3d, чтобы быть более энергетически устойчивым, так как в таком случае атом не будет иметь пустых орбиталей на 3d.
Ответ: 23
Показать решение
Бесплатный интенсив
Первое задание в ЕГЭ по химии посвящено электронной конфигурации атома. Для его выполнения дается ряд химических элементов, среди которых нужно выбрать два с одинаковым свойством. Какие могут быть свойства:
- одинаковое число валентных электронов,
- одинаковое количество неспаренных электронов в основном или возбужденном состоянии,
- одна и та же общая электронная конфигурация валентного уровня.
Для правильного выполнения этого задания полезно помнить последовательность заполнения электронами атомных орбиталей, которую легко понять по этому рисунку:
Порядок заполнения электронами атомных орбиталей.
Атом является электронейтральной частицей. Положительный заряд ядра уравновешивается числом отрицательно заряженных электронов, которые движутся в его поле. Заряд ядра атома химического элемента равен его порядковому номеру в периодической системе Д.И. Менделеева. При переходе от одного элемента к следующему заряд ядра увеличивается на единицу. И на единицу возрастает число электронов в атоме. Каждый следующий добавляемый электрон занимает низшую свободную атомную орбиталь.
Заряд ядра атома химического элемента равен его порядковому номеру в периодической системе Д.И. Менделеева. При переходе от одного элемента к следующему заряд ядра увеличивается на единицу. И на единицу возрастает число электронов в атоме. Каждый следующий добавляемый электрон занимает низшую свободную атомную орбиталь.
Краткопериодный вариант периодической системы Д.И. Менделеева
Давайте рассмотрим электронную конфигурацию на примере самого просто атома водорода. Заряд ядра атома водорода +1. Значит, в поле ядра движется 1 электрон, и он занимает самую первую по энергии атомную орбиталь — 1s. Электронная формула атома водорода таким образом записывается:
Электронная формула атома водорода в основном состоянии.
У атома гелия (заряд ядра +2) следующий электрон займет ту же самую s-орбиталь, однако спин у него будет противоположный (стрелка, изображающая электрон, направлена в другую сторону):
Электронная конфигурация атома гелия в основном состоянии.
На этом ёмкость 1 энергетического уровня становится полностью заполненной.
Электронная конфигурация атома лития в основном состоянии.
Правило Хунда: электроны заполняют атомную орбиталь таким образом, чтобы её суммарный спин был максимальным.
Другими словами, при заполнении p, d, f-орбиталей электроны сначала будут занимать квантовые ячейки орбитали по одному, и только потом будут спариваться. По этому поводу можно привести хорошую аналогию: при размещении пассажиров в изначально пустом трамвае, если все люди незнакомы, они будут занимать сначала места по одному, и только когда мест станет не достаточно, незнакомые люди станут занимать места рядом с теми, кто зашел в трамвай раньше. На этом основании запишем электронную конфигурацию атома серы и изобразим распределение электронов по квантовым ячейкам:
Электронная конфигурация атома серы в основном состоянии. Красным цветом показаны электроны валентного уровня.
В образовании химических связей участвуют только электроны внешнего (валентного) энергетического уровня. В атоме серы таким уровнем является третий. На нём расположено шесть электронов, два из которых не спарены.
Число валентных электронов в атоме равно номеру группы (исключения: атомы кобальта и никеля, у них число валентных электронов равно 9 и 10, соответственно).
Особой энергетической устойчивостью обладают наполовину и полностью заполненные орбитали.
Запишем электронную конфигурацию атома хрома. Найдем хром в таблице Менделеева. Его порядковый номер — 24. Это означает, что заряд ядра атома Cr +24, следовательно в поле ядра движется 24 электрона.
Распределим 24 электрона по орбиталям, пользуясь уже известными нам правилами. Помним, что между 4s и 4p-орбиталями заполняется 3d-орбиталь:
Однако, на d-орбитали не хватает одного электрона до наполовину заполненного состояния. А наполовину заполненные орбитали отличаются пониженной энергией. Всё в мире стремится к минимуму энергии; и атом тоже.
Символом в квадратных скобках (у нас это — [Ar]) принято сокращать электронную конфигурацию полностью заполненных невалентных нижних энергетических уровней. У всех благородных газов, которые находятся в 18 группе длиннопериодного варианта периодической системы или в 8 группе краткопериодного, орбитали заполнены полностью, и чтобы не переписывать каждый раз одно и то же пользуются таким способом сокращения записи.
Таким же исключением из правил является атом меди. Ему не хватает одного электрона для полного заполнения 3d-орбитали. И он, как и хром, берет этот электрон с 4-s орбитали:
Именно на тех же основаниях электронная конфигурация молибдена — [Kr] 4d(5)5s(1) (надстрочные индексы указаны в скобках), серебра — [Kr] 4d(10) 5s(1).
Пользуясь информацией, изложенной выше, можно легко вычислить число валентных, внешних и неспаренных электронов в атоме и безошибочно выполнить первое задание ЕГЭ, за которое можно получить 1 первичный балл.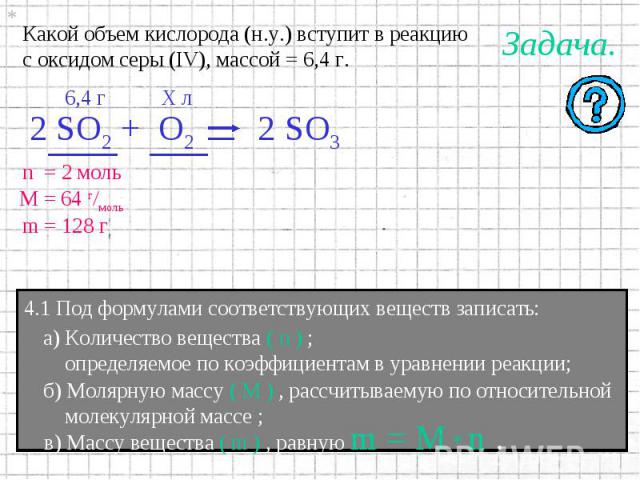
Второе вещество — оксид серы(VI). Это кислотный оксид неметалла в высшей степени окисления. Способен реагировать с веществами основной природы — основаниями и основными оксидами. Растворяется в воде с образованием кислоты. Выбираем ряд под номером 2.
Третье вещество — гидроксид цинка. Это амфотерный гидроксид — проявляет как кислотные, так и основные свойства. Реагирует с кислотами и щелочами. Выбираем ряд под номером 4.
Четвертое вещество — бромид цинка. Это средняя соль. Вступает в реакции ионного обмена с кислотами, солями, основаниями, если в результате образуется осадок, газ или слабый электролит. Следует помнить, что если в результате ионного обмена образуется соль слабого основания и слабой кислоты, то она полностью гидролизуется с образованием этих самых слабого основания и слабой кислоты. Также нужно помнить, что галогениды способны вытеснятся из их солей более активными галогенами. Выбираем ряд под номером 1.
Напоследок поговорим о том, как можно осилить это задание, если всё совсем плохо и не получается найти необходимый ряд веществ. Воспользуемся методом исключения! Если в ряду хоть один реагент точно не реагирует с нашим веществом, то этот ряд можно исключить. Разберем на примере серы из задания выше. Из неметаллов только галогены могут вытеснять менее активные галогены из их солей. Другие неметаллы с солями никогда не реагируют. Таким образом нам точно не подходит ряд 1 (нитрат серебра) и ряд 5 (хлорид бария). Из неметаллов только кислород может реагировать с некоторыми оксидами, значит убираем ряд 2 (оксид бария). Ряд четыре не подходит, потому что бром более сильный неметалл, и сера не вытеснит бром из его кислоты. Остается вариант 3))
Воспользуемся методом исключения! Если в ряду хоть один реагент точно не реагирует с нашим веществом, то этот ряд можно исключить. Разберем на примере серы из задания выше. Из неметаллов только галогены могут вытеснять менее активные галогены из их солей. Другие неметаллы с солями никогда не реагируют. Таким образом нам точно не подходит ряд 1 (нитрат серебра) и ряд 5 (хлорид бария). Из неметаллов только кислород может реагировать с некоторыми оксидами, значит убираем ряд 2 (оксид бария). Ряд четыре не подходит, потому что бром более сильный неметалл, и сера не вытеснит бром из его кислоты. Остается вариант 3))
Какие атомы наиболее распространены во Вселенной?
содержание
Какие самые распространенные атомы во Вселенной?
Наиболее распространены водород и гелий, образовавшиеся в первые 3 минуты Большого взрыва, который является отправной точкой всего сущего. Кислород является третьим наиболее распространенным химическим элементом, за ним следует углерод, который является основой жизни, какой мы ее знаем сегодня.
Какой самый распространенный атом?
Самым распространенным химическим элементом во Вселенной является водород (H). Подсчитано, что он составляет 75% массы всей материи и 93% атомов в космосе.
Каких атомов больше всего в природе?
Начнем с того, что из более чем 90 встречающихся в природе химических элементов только 30 необходимы для живых организмов. Мы можем выделить атомы углерода, кислорода, азота, водорода, серы и фосфора, которые в сумме составляют 99% массы большинства клеток!
Какой самый большой атом во Вселенной?
Какой самый большой атом во Вселенной? Самый большой атом, когда-либо созданный в экспериментальной ситуации, принадлежит Оганессону (Og) и имеет 118 протонов в ядре. На бумаге это благородный газ, то есть: несмотря на то, что он является причудливым человеческим творением, есть некоторый шанс, что он обладает свойствами, подобными свойствам гелия.
Какие 4 основных атома?
Ознакомьтесь с полным обзором четырех типов атомных моделей:
- 1 – Далтон (1803 г.
 )
) - 2 – Томсон (1903 г.)
- 3 – Резерфорд (1911 г.)
- 4 – Бор – 1913.
Каковы 4 основных атома жизни?
Четыре элемента – это кислород, водород, углерод и азот. Прежде чем вы начнете думать, что мы должны плавать со всеми этими атомами кислорода, водорода и азота, помните, что кислород является важной частью воды в нашем организме (h3O).
Сколько атомов в мире?
На самом деле существует приблизительно 133.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000 48 XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX атомов. Там XNUMX нулей.
Что такое человеческий атом?
В организме человека наиболее распространенными атомами, составляющими большинство биологических молекул (белков, углеводов, липидов и нуклеиновых кислот), являются углерод, кислород, азот, водород и фосфор.
Что такое атомы?
Субатомные частицы Сегодня мы знаем, что атомы состоят из субатомных частиц, таких как протоны, нейтроны, электроны, позитроны, кварки, нейтрино и мезоны. В данный момент нас интересуют только фундаментальные субчастицы: протоны, нейтроны и электроны. Протоны — электрически заряженные частицы.
В данный момент нас интересуют только фундаментальные субчастицы: протоны, нейтроны и электроны. Протоны — электрически заряженные частицы.
Какой самый маленький атом в мире?
Среди частиц, имеющих некоторую массу, самой маленькой является нейтрино. «Это может быть 4 x 10–33 грамма», — говорит физик Клаудио Фурукава из USP. Это соответствует одной миллиардной триллионной триллионной части грамма и дает массу в 100 миллионов раз меньше массы протона, которая составляет 1,67 x 10-24 грамма.
Какой самый редкий элемент во Вселенной?
Астат существует только в земной коре в виде радиоактивных изотопов. Общее количество астата в земной коре оценивается менее чем в 32 грамма, что делает его самым редким элементом в мире.
Из скольких атомов состоит тело человека?
Человеческое тело состоит из 7 октиллионов атомов и имеет примерно 10 триллионов клеток. Наиболее распространенными атомами, составляющими большинство биологических молекул (белков, углеводов, липидов и нуклеиновых кислот), являются углерод, кислород, азот, водород и фосфор.
Сколько атомов известно?
Химические элементы состоят из набора атомов, состоящих из одинакового количества протонов в ядре. В настоящее время известно 118 элементов, из них 92 созданы природой и 26 созданы искусственно. Все они представлены в периодической таблице.
Для чего нужен атом?
Атом является фундаментальной единицей материи и наименьшей частицей, способной идентифицировать химический элемент, поскольку он сохраняет его идентичность. Термин атом происходит от греческого и означает неделимый. Он состоит из ядра, содержащего нейтроны и протоны, и электронов, окружающих ядро.
Где находятся атомы?
Структуру атома образуют ядро, состоящее из двух частиц (протонов и нейтронов), и электросфера, в которой находятся электроны. Атомы — это бесконечно малые частицы, из которых состоит вся материя во Вселенной.
Как долго живет атом?
10 35 лет — это среднее время жизни атома, по данным американского астронома Мартина Риса.
Сколько атомов в 1 ячейке?
Это зависит от размера ячейки, не все ячейки имеют одинаковый размер. Но это число приблизительно равно 7 квадриллионам атомов на клетку, если мы возьмем общее количество атомов в теле и разделим его на общее количество клеток в человеческом теле.
Кто открыл атом?
Первыми мыслителями-философами, рассматривавшими эту идею, были: Левкип и Демокрит, причем Левкипп был первым, кто предположил, что все состоит (вся вселенная) из неделимых частиц, называемых атомами.
Что меньше кварка?
Следовательно, кварки и электроны — самые маленькие из известных нам объектов.
Нельзя что-то трогать?
Ответ прост: никогда, ни при каких обстоятельствах мы по-настоящему не прикасаемся к другим вещам или людям. Когда мы подходим очень близко к телу, у нас появляется ощущение прикосновения к нему. Но внутри происходит так называемое электрическое отталкивание.
Когда мы подходим очень близко к телу, у нас появляется ощущение прикосновения к нему. Но внутри происходит так называемое электрическое отталкивание.
Что такое мельчайшая частица вещества?
Это неделимая единица материи.
Атом – это частица, образованная материей, которая не может быть разделена. Этот компонент состоит из нейтронов, протонов и электронов и имеет в качестве своей основной характеристики при изучении химии, являясь самой маленькой видимой частицей, существующей в природе.
Правда ли, что мы состоим из атомов?
Но фундаментальным аспектом являются атомы, из которых состоит наше тело. По сути, мы состоим всего из четырех типов частиц, которые существовали большую часть времени в истории Вселенной. Это может быть немного сокращено.
Каковы первые элементы Вселенной?
Водород, гелий и литий, самые легкие элементы периодической таблицы, образовались первыми во Вселенной. Теоретические и наблюдательные данные указывают на образование этих элементов в первые три минуты после Большого взрыва, физического события, ответственного за создание Вселенной 13.8 миллиарда лет назад.
Теоретические и наблюдательные данные указывают на образование этих элементов в первые три минуты после Большого взрыва, физического события, ответственного за создание Вселенной 13.8 миллиарда лет назад.
Как назывался атом до того, как он получил это имя?
Модель атома стала известна как бильярдный шар, потому что в то время атом характеризовался как сферическая, массивная и неразрушимая единица, подобная бильярдному шару.
Какие три типа атомов существуют?
По атомному подобию атомы можно разделить на изотопы, изобары, изотоны и изоэлектроны.
- Изотопы: это классификация атомных видов, которые могут иметь различную массу.
- Изобары: разные атомы, имеющие одинаковое массовое число.
Во всем ли есть атом?
Все происходит из материи, а материя состоит из атомов. Об атомном ядре известно, что оно состоит из протонов и нейтронов, на самом деле эта теория существует с 1932 года, уже тогда отстаивалась идея неделимости атома, получившая название фундаментальной частицы.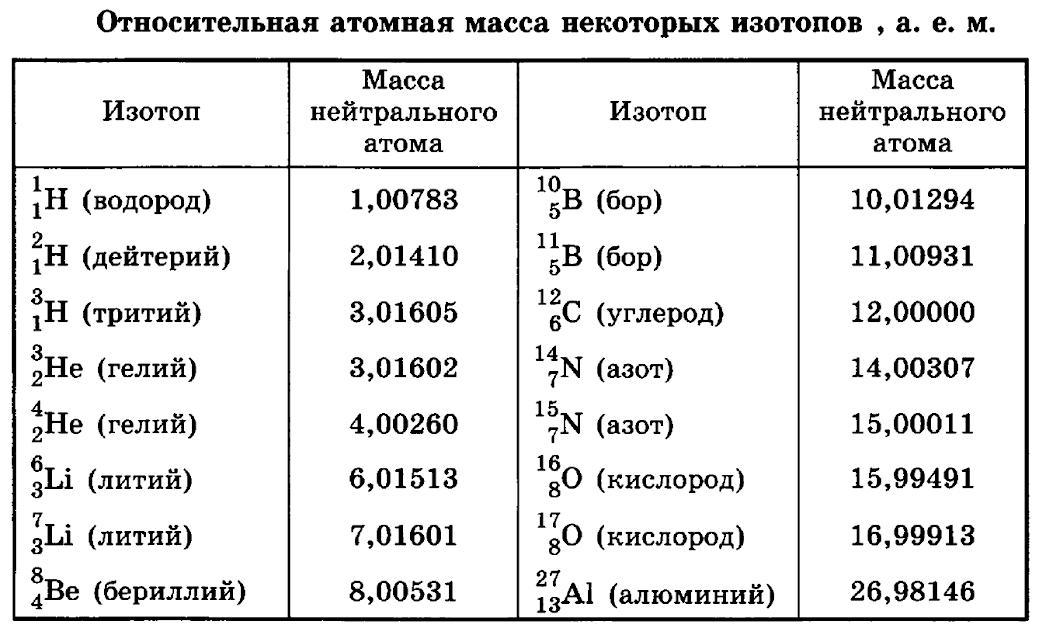
Что такое атомы Приведите примеры?
Атом представляет собой структуру (состоящую из протона, нейтрона, электрона, ядра, уровней, подуровней и орбиталей), образующую материю. Атом — это название, данное образующемуся из материи (всему, что занимает пространство и имеет массу). Это название предложили греческие философы Демокрит и Левкипп.
Можно ли разбить атом?
Ядерное деление в ядерной физике — это расщепление ядра нестабильного атома на два меньших ядра путем бомбардировки его частицами, такими как нейтроны. Изотопы, образующиеся при расщеплении, имеют одинаковую массу, но обычно имеют соотношение масс 3:2.
Какой самый старый атом во Вселенной?
Отвечать. Теория Биг-Бена очень расплывчата, но предполагается, что самым старым атомом является водород.
Что такое кварк?
Протоны и нейтроны, находящиеся вместе в ядре атома, могут быть фрагментированы на еще более мелкие частицы. Эти частицы называются кварками. Насколько нам известно, существует по крайней мере шесть различных видов кварков, обнаруженных в ходе экспериментов, проведенных на больших ускорителях частиц.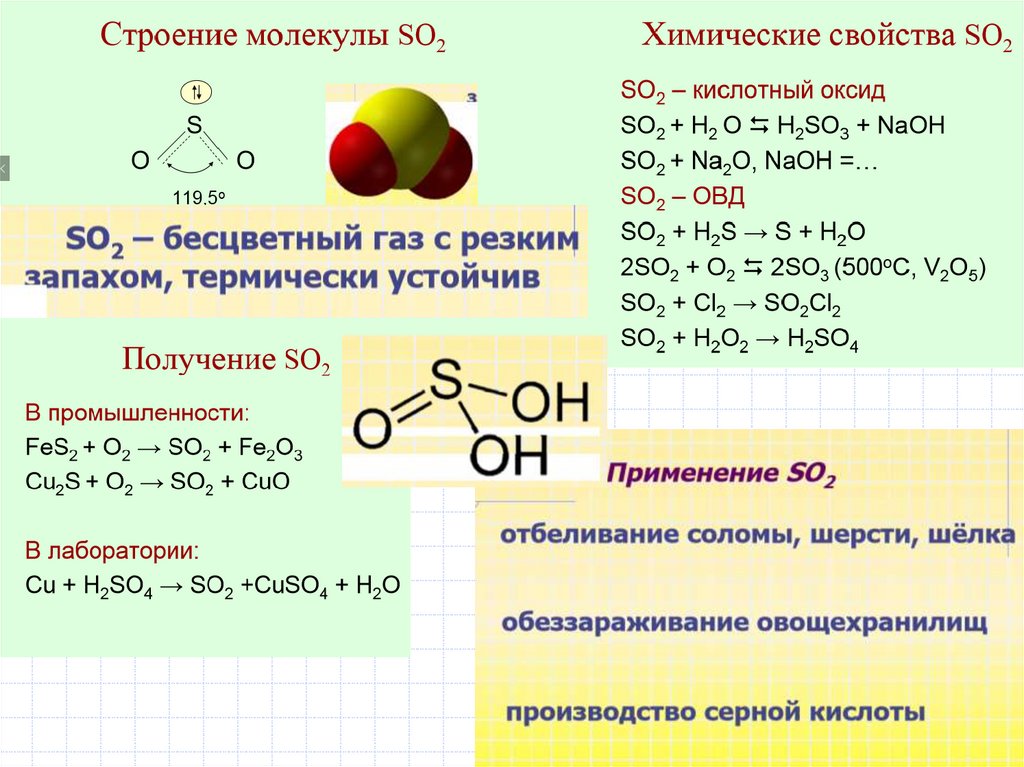
Какой самый слабый элемент?
Многие фанаты выбирают между управлением водой, землей или огнем. Однако многие не выбирают воздушную стихию, которую некоторые считают самой слабой.
Какой самый важный элемент во Вселенной?
Водород, основной химический элемент во Вселенной
Это наиболее присутствующий элемент во Вселенной, составляющий 75% элементарной массы всего, что существует, он считается самым важным топливом для формирования и поддержания звезд, включая астро-короля, Солнце.
Какой самый негативный элемент?
Таким образом, наиболее электроотрицательным элементом является фтор (4,0), а наименее электроотрицательным — цезий (0,7).
Какая часть тела не имеет материи?
Какая часть тела не имеет материи? Ответ: Только вакуум.
Какая самая большая клетка в организме человека?
Половые клетки
Самой большой клеткой человека является яйцеклетка, женская половая гамета.
Сколько атомов у Солнца?
Сколько примерно атомов водорода на Солнце? Ответ: число атомов водорода nH будет равно 1,19. 82 атомов в наблюдаемой Вселенной. Чтобы поместить это в контексте, это 10.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000 XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX
82 атомов в наблюдаемой Вселенной. Чтобы поместить это в контексте, это 10.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000 XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX
Каковы основные типы атомов?
В этом смысле выделяют четыре основных типа атомов: изотопы, изобары, изотоны и изоэлектроны.
Сколько атомов во Вселенной?
На самом деле существует приблизительно 133.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000.000 XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX XNUMX атомов.
Сколько атомов известно в настоящее время?
Химические элементы состоят из набора атомов, состоящих из одинакового количества протонов в ядре. В настоящее время известно 118 элементов, из них 92 созданы природой и 26 созданы искусственно. Все они представлены в периодической таблице.
Which statements are consistent with Dalton’s atomic theory as it…
Recent Channels
- General Chemistry
Chemistry
- General Chemistry
- Organic Chemistry
- Analytical Chemistry
- GOB Chemistry
- Biochemistry
Биология
- Общая биология
- Микробиология
- Анатомия и физиология
- Генетика
- Cell Biology
Math
- College Algebra
- Trigonometry
- Precalculus
Physics
- Physics
Business
- Microeconomics
- Macroeconomics
- Financial Accounting
Social Sciences
- Psychology
Начните вводить текст, затем используйте стрелки вверх и вниз, чтобы выбрать вариант из списка.
- 2. Атомы и элементы
- Атомная теория
Проблема
Соответствующее решение
2 м
Воспроизведите видео:
Привет всем, кто отвечает на этот вопрос, нам нужно определить утверждение, которое следует за атомной теорией Дальтона, и объяснить, почему утверждение А. утверждает, что утверждение вода утверждает, что вода образуется при соединении водорода с кислородом в соотношении 1-2. соотношение. Мы хотим напомнить, что атомы соединяются в целочисленных отношениях. Таким образом, мы бы сказали, что это утверждение противоречит теории Дальтона. Таким образом, мы бы исключили вариант А. Вариант Б утверждает, что медь может быть получена из атомов железа. Мы хотим напомнить, что вы не можете делать такие вещи, вы не можете сделать атомы одного элемента из другого. Следовательно, это несовместимо с атомной теорией Дальтона. Таким образом, мы можем исключить вариант Б. Переходя к утверждению, вы увидите, что все атомы цинка имеют одинаковую массу и свойства. И поэтому мы бы вспомнили, что неважно, сколько атомов цинка у нас в молекуле. Это утверждение согласуется с теорией Дальтона, потому что атомы данного элемента имеют одинаковую массу и свойства. Так что это в точности из атомной теории Дальтона, и мы согласны с выбором C. Так что мы можем определенно сказать, что это непротиворечиво. Переходим к варианту D. У нас атомы углерода и азота имеют разные физические свойства, но имеют одинаковые химические свойства. И это утверждение полностью противоречит утверждениям. См. утверждение C. Соответствует теории Дальтона. Тогда утверждение D. Определенно снова будет несовместимым, атомы данного элемента имеют одинаковую массу и другие свойства. Таким образом, мы бы исключили вариант D. Таким образом, единственным правильным выбором для завершения этого примера является вариант C. Все атомы данного элемента, например цинка, будут иметь одинаковую массу и другие сходные свойства. Так что это соответствует атомной теории Дальтона, и это завершит этот пример как наш окончательный ответ.
И поэтому мы бы вспомнили, что неважно, сколько атомов цинка у нас в молекуле. Это утверждение согласуется с теорией Дальтона, потому что атомы данного элемента имеют одинаковую массу и свойства. Так что это в точности из атомной теории Дальтона, и мы согласны с выбором C. Так что мы можем определенно сказать, что это непротиворечиво. Переходим к варианту D. У нас атомы углерода и азота имеют разные физические свойства, но имеют одинаковые химические свойства. И это утверждение полностью противоречит утверждениям. См. утверждение C. Соответствует теории Дальтона. Тогда утверждение D. Определенно снова будет несовместимым, атомы данного элемента имеют одинаковую массу и другие свойства. Таким образом, мы бы исключили вариант D. Таким образом, единственным правильным выбором для завершения этого примера является вариант C. Все атомы данного элемента, например цинка, будут иметь одинаковую массу и другие сходные свойства. Так что это соответствует атомной теории Дальтона, и это завершит этот пример как наш окончательный ответ. Если у вас есть какие-либо вопросы, пожалуйста, оставьте их ниже, и я увижу всех в следующем практическом видео.
Если у вас есть какие-либо вопросы, пожалуйста, оставьте их ниже, и я увижу всех в следующем практическом видео.
Связанные видео
Связанная практика
История атомной теории
от профессора Дейва объясняет
150views
Атомная теория материи
от Pearson
74Views
.
by CrashCourse
286views
Atomic Theory
by Jules Bruno
158views
Урок 6 — Атомная теория вещества, часть 1 (Chemistry Tutor)
по математике и науке
115просмотров
Атомная теория Дальтона | Don’t Memorize
by Don’t Memorize
123views
Развитие атомной теории: введение
by JFR Science
134views
Атомная теория | Материя | Физика | FuseSchool
от FuseSchool — Global Education
146views
Atomic Theory Example 1
by Jules Bruno
103views
Видео с вопросами: Расчет общего числа атомов в комплексах элемента
Стенограмма видео
Сколько атомов кислорода присутствует в формуле 10SO2?
Напомним, что химическая формула определяется как выражение химических символов и числовых индексов, которое представляет собой состав одной единицы соединения. Переписывая формулу, приведенную в вопросе, мы имеем соединение SO2, где химический символ S указывает на присутствие элемента серы, а химический символ O указывает на присутствие элемента кислорода. Оба химических символа можно найти в периодической таблице.
Переписывая формулу, приведенную в вопросе, мы имеем соединение SO2, где химический символ S указывает на присутствие элемента серы, а химический символ O указывает на присутствие элемента кислорода. Оба химических символа можно найти в периодической таблице.
Химический символ кислорода и химический символ серы можно найти в группе 16, при этом химический символ кислорода присутствует во втором периоде, а химический символ серы в третьем периоде таблицы Менделеева. Если мы посмотрим на нижние индексы для каждого химического символа в формуле, то сначала заметим, что для серы не показан нижний индекс. Это связано с тем, что правилом написания химических формул является то, что значения нижнего индекса, равные единице, подразумеваются, но не записываются в химической формуле. Другими словами, когда в данной химической формуле присутствует один атом любого элемента, значение нижнего индекса номер один не отображается, а отображается только химический символ.
Таким образом, в случае с атомом серы в этой химической формуле, несмотря на то, что в представленной формуле нет нижнего индекса, согласно правилу, на самом деле подразумевается число один, что означает наличие одного атома серы в одной молекуле это соединение. Что касается атома кислорода, нижний индекс два указывает на наличие двух атомов кислорода в одной молекуле этого соединения.
Что касается атома кислорода, нижний индекс два указывает на наличие двух атомов кислорода в одной молекуле этого соединения.
Это также можно наблюдать на чертеже шаростержневой модели молекулы SO2, которая изображает один центральный атом серы, связанный с двумя атомами кислорода. Основываясь на этой информации, может возникнуть соблазн ответить на вопрос «Сколько атомов кислорода в формуле 10SO2?» два атома кислорода из-за нижнего индекса два справа от химического символа кислорода. Однако в данном случае это было бы неверно, поскольку в этой формуле содержится еще одна информация, которую мы еще не обсудили.
Цифра 10 в начале формулы называется коэффициентом. Коэффициенты появляются перед химической формулой и указывают количество дискретных единиц. Или, в данном конкретном случае, это число указывает на количество молекул SO2, что означает, что в этой формуле 10 молекул SO2. Чтобы решить эту проблему, давайте начнем с перечисления информации, которую мы узнали о формуле.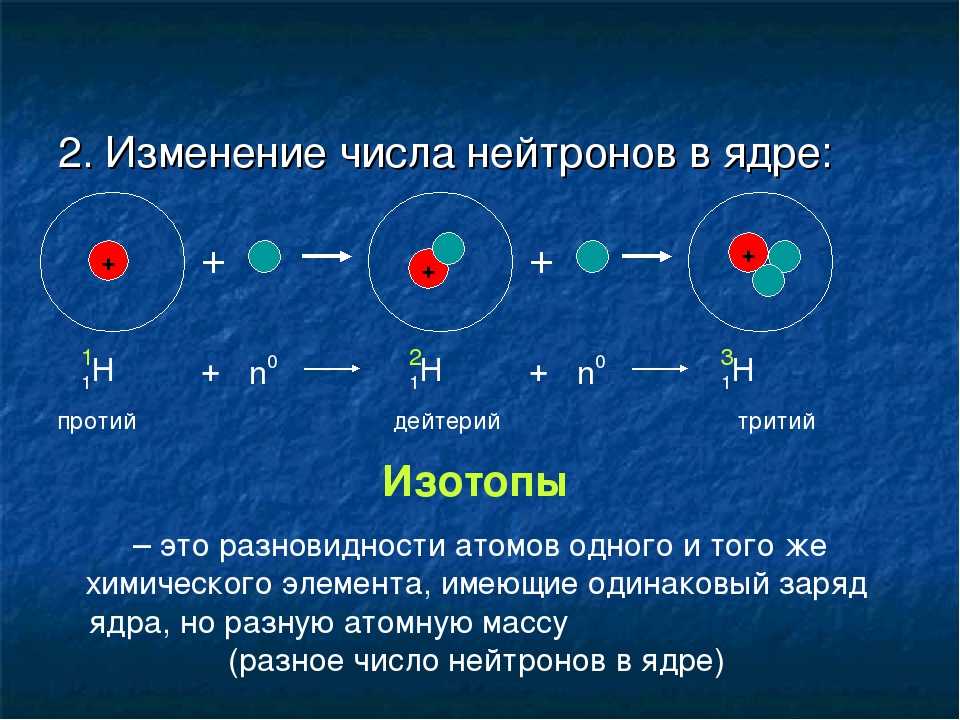 Коэффициент номер 10 перед молекулой SO2 указывает на наличие 10 молекул SO2. Поскольку вопрос сосредоточен на количестве атомов кислорода, мы запишем, что в одной молекуле SO2 содержится два атома кислорода.
Коэффициент номер 10 перед молекулой SO2 указывает на наличие 10 молекул SO2. Поскольку вопрос сосредоточен на количестве атомов кислорода, мы запишем, что в одной молекуле SO2 содержится два атома кислорода.
Теперь мы можем переписать эти две части информации в виде дробей, чтобы найти общее количество атомов кислорода в формуле. Когда информация записывается как таковая, она позволяет сокращать единицы молекул SO2, что означает, что мы остаемся с единицами атомов кислорода, что соответствует тому, что задает вопрос. Если мы закончим алгебраическую функцию, умножив два числа в верхней части дробей и разделив это произведение на все числа в нижней части дробей, мы обнаружим, что в формуле 10SO2 содержится 20 атомов кислорода.
Другим способом решения этой проблемы было бы распределение коэффициента 10 на подразумеваемый нижний индекс один справа от химического символа серы и на нижний индекс два справа от химического символа кислорода. Умножив коэффициент 10 на индекс два, мы получим тот же ответ: 20 атомов кислорода в 10 молекулах SO2.

 )
)
Leave A Comment