Курс подготовки к ЕГЭ по химии
Полный курс подготовки к ЕГЭ по химии-2023. Здесь приведена теория по каждому заданию в соответствии с спецификацией и кодификатором ЕГЭ по химии. Учебные материалы и теория, необходимые для подготовки к ЕГЭ по химии.
Вы можете поддержать работу сайта, разработку новых материалов и тестов. Донаты принимаются через форму:
Обратите внимание! Форма выше — это не оплата курса по химии, это форма для сбора донатов на работу сайта)
| 1 | ТЕОРЕТИЧЕСКИЕ ОСНОВЫ ХИМИИ | |
| | 1.1. | Современные представления о строении атома |
1. | Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояния атомов Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами) | |
| 1.2 | Периодический закон и Периодическая система химических элементов Д.И. Менделеева | |
| 1.2.1. | Закономерности изменения свойств элементов и их соединений по периодам и группам Тренировочные тесты в формате ЕГЭ по теме «Периодический закон» (задание 2 ЕГЭ по химии) ( с ответами) | |
| 1.2.2. | Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов. | |
| 1.2.3. | Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов Д. И. Менделеева и особенностям строения их атомов И. Менделеева и особенностям строения их атомов | |
| 1.2.4. | Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов | |
| | Химическая связь и строение вещества | |
| 1.3.1 | Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь Тренировочные тесты в формате ЕГЭ по теме «Химические связи» (задание 4 ЕГЭ по химии) ( с ответами) | |
| 1.3.2. | Электроотрицательность. Степень окисления и валентность химических элементов Тренировочные тесты в формате ЕГЭ по теме «Степень окисления и валентность» (задание 3 ЕГЭ по химии) ( с ответами) | |
| 1.3.3. | Вещества молекулярного и немолекулярного строения. | |
| 1.4. | Химическая реакция | |
| 1.4.1. | Классификация химических реакций в неорганической и органической химии Тренировочные тесты в формате ЕГЭ по теме «Классификация реакций» ( с ответами) | |
| 1.4.2. | Тепловой эффект химической реакции. Термохимические уравнения | |
| 1.4.3. | Скорость реакции, ее зависимость от различных факторов | |
| 1.4.4. | Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» ( с ответами) | |
| 1.4.5. | Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты Сильные и слабые электролиты | |
| 1.4.6. | Реакции ионного обмена | |
| 1.4.7. | Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная Тренировочные тесты в формате ЕГЭ по теме «Гидролиз» (с ответами) | |
| 1.4.8. | Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее Тренировочные тесты в формате ЕГЭ по теме «Окислительно-восстановительные реакции» (задание 19 ЕГЭ по химии) ( с ответами) | |
| 1.4.9. | Электролиз расплавов и растворов (солей, щелочей, кислот) Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 20 ЕГЭ по химии) ( с ответами) | |
| 1.4.10. | Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии | |
| 2 | НЕОРГАНИЧЕСКАЯ ХИМИЯ | |
| 2.1. | Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная) Номенклатура неорганических веществ (тривиальная и международная)Тренировочные тесты в формате ЕГЭ по теме «Классификация неорганических веществ» (задание 5 ЕГЭ по химии) ( с ответами) | |
| 2.2. | Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа) | |
| 2.3. | Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния | |
| 2.4. | Характерные химические свойства оксидов: основных, амфотерных, кислотных | |
| 2.5. | Характерные химические свойства оснований и амфотерных гидроксидов | |
| 2.6. | Характерные химические свойства кислот | |
| 2.7. | Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка) | |
| 2.8. | Взаимосвязь различных классов неорганических веществ | |
 | ОРГАНИЧЕСКАЯ ХИМИЯ | |
| 3.1. | Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах Тренировочные тесты в формате ЕГЭ по теме «Теория строения орг. соединений» ( с ответами) | |
| 3.2. | Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа | |
| 3.3. | Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная) | |
| 3.4. | Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола) | |
| 3.5. | Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола.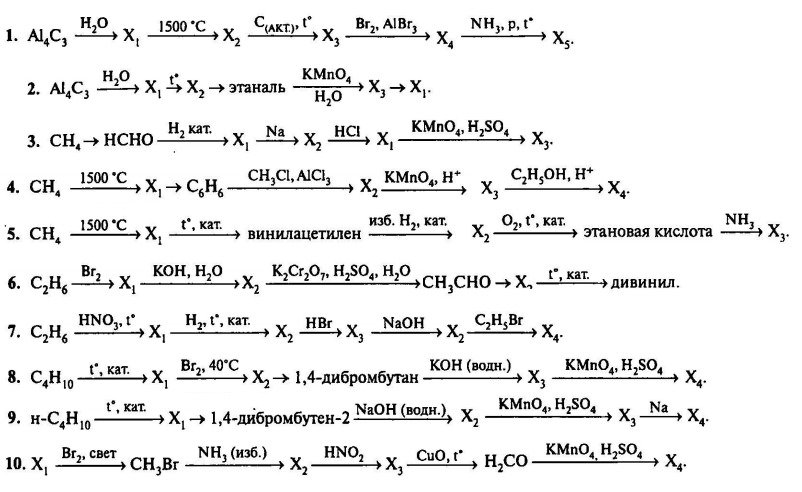 | |
| 3.6. | Характерные химические свойства альдегидов, карбоновых кислот, сложных эфиров | |
| 3.7. | Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот | |
| 3.8. | Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды) | |
| 3.9. | Взаимосвязь органических соединений | |
| 4. | МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ | |
| 4.1. | Экспериментальные основы химии | |
| 4.1.1. | Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии | |
4. 1.2. 1.2. | Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ | |
| 4.1.3. | Определение характера среды водных растворов веществ. Индикаторы | |
| 4.1.4. | Качественные реакции на неорганические вещества и ионы | |
| 4.1.5. | Качественные реакции органических соединений | |
| 4.1.6. | Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений | |
| 4.1.7. | Основные способы получения углеводородов (в лаборатории): алканов, алкенов, алкинов, циклоалканов, алкадиенов, аренов | |
| 4.1.8. | Основные способы получения органических кислородсодержащие соединений (в лаборатории): спиртов, альдегидов и кетонов, карбоновых кислот | |
| 4.2.1. | Понятие о металлургии: общие способы получения металлов | |
| 4.2.2. | Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия Химическое загрязнение окружающей среды и его последствия | |
| 4.2.3. | Природные источники углеводородов, их переработка | |
| 4.2.4. | Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки | |
| 4.3. | Расчеты по химическим формулам и уравнениям реакций | |
| 4.3.1. | Расчеты с использованием понятия «массовая доля вещества в растворе» | |
| 4.3.2. | Расчеты объемных отношений газов при химических реакциях | |
| 4.3.3. | Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ | |
| 4.3.4. | Расчеты теплового эффекта реакции | |
| 4.3.5. | Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси) | |
4. 3.6. 3.6. | Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества | |
| 4.3.7. | Установление молекулярной и структурной формулы вещества | |
| 4.3.8. | Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного | |
| 4.3.9. | Расчеты массовой доли (массы) химического соединения в смеси |
1.1.1. Строение электронных оболочек атомов элементов первых четырех периодов: s-, p- и d-элементы. Электронная конфигурация атомов и ионов. Основное и возбужденное состояния атомов
Тренировочные тесты в формате ЕГЭ по теме «Строение атома» (задание 1 ЕГЭ по химии) ( с ответами)
1.2. Периодический закон и Периодическая система химических элементов Д.И. Менделеева
Тренировочные тесты в формате ЕГЭ по теме «Периодический закон» (задание 2 ЕГЭ по химии) ( с ответами)
1. 2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
2.1. Закономерности изменения свойств элементов и их соединений по периодам и группам
1.2.2. Общая характеристика металлов IА–IIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов.
1.2.3. Характеристика переходных элементов (меди, цинка, хрома, железа) по их положению в Периодической системе химических элементов Д.И. Менделеева и особенностям строения их атомов
1.2.4. Общая характеристика неметаллов IVА–VIIА групп в связи с их положением в Периодической системе химических элементов Д.И. Менделеева и особенностями строения их атомов
1.3. Химическая связь и строение вещества
1.3.1. Ковалентная химическая связь, ее разновидности и механизмы образования. Характеристики ковалентной связи (полярность и энергия связи). Ионная связь. Металлическая связь. Водородная связь
Тренировочные тесты в формате ЕГЭ по теме «Химические связи» (задание 4 ЕГЭ по химии) ( с ответами)
1.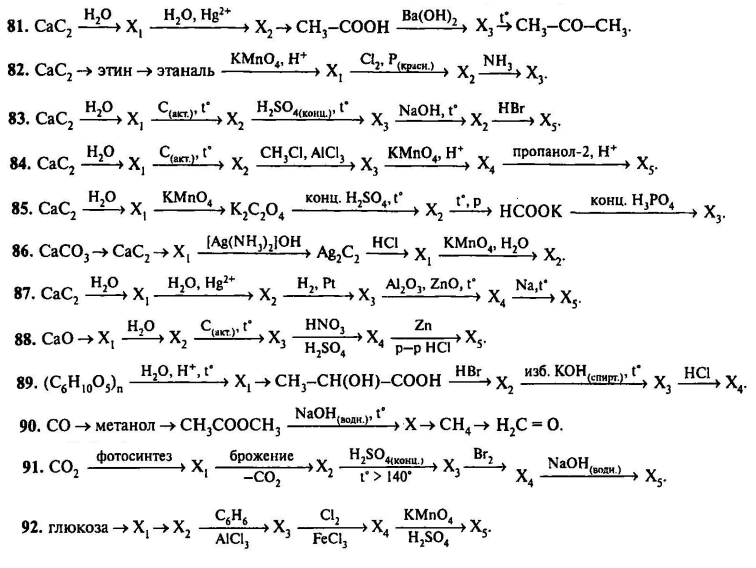 3.2. Электроотрицательность. Степень окисления и валентность химических элементов
3.2. Электроотрицательность. Степень окисления и валентность химических элементов
Тренировочные тесты в формате ЕГЭ по теме «Степень окисления и валентность» (задание 3 ЕГЭ по химии) ( с ответами)
1.3.3. Вещества молекулярного и немолекулярного строения. Тип кристаллической решетки. Зависимость свойств веществ от их состава и строения
1.4. Химическая реакция
1.4.1. Классификация химических реакций в неорганической и органической химии
1.4.2. Тепловой эффект химической реакции. Термохимические уравнения
1.4.3. Скорость реакции, ее зависимость от различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Скорость реакции» (задание 20 ЕГЭ по химии) ( с ответами)
1.4.4. Обратимые и необратимые химические реакции. Химическое равновесие. Смещение химического равновесия под действием различных факторов
Тренировочные тесты в формате ЕГЭ по теме «Химическое равновесие реакции» (задание 24 ЕГЭ по химии) ( с ответами)
1. 4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты
4.5. Электролитическая диссоциация электролитов в водных растворах. Сильные и слабые электролиты
1.4.6. Реакции ионного обмена
1.4.7. Гидролиз солей. Среда водных растворов: кислая, нейтральная, щелочная
Тренировочные тесты в формате ЕГЭ по теме «Гидролиз» (задание 23 ЕГЭ по химии) ( с ответами)
1.4.8. Реакции окислительно-восстановительные. Коррозия металлов и способы защиты от нее
Тренировочные тесты в формате ЕГЭ по теме «Окислительно-восстановительные реакции» (задание 21 ЕГЭ по химии) ( с ответами)
1.4.9. Электролиз расплавов и растворов (солей, щелочей, кислот)
Тренировочные тесты в формате ЕГЭ по теме «Электролиз» (задание 22 ЕГЭ по химии) ( с ответами)
1.4.10. Ионный (правило В.В. Марковникова) и радикальный механизмы реакций в органической химии
2. НЕОРГАНИЧЕСКАЯ ХИМИЯ
2.1. Классификация неорганических веществ. Номенклатура неорганических веществ (тривиальная и международная)
Тренировочные тесты в формате ЕГЭ по теме «Классификация неорганических веществ» (задание 5 ЕГЭ по химии) ( с ответами)
2.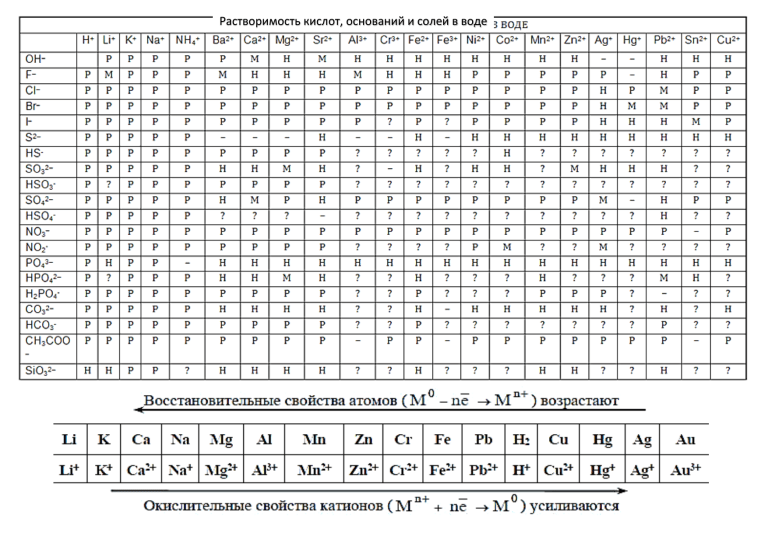 2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа)
2. Характерные химические свойства простых веществ – металлов: щелочных, щелочноземельных, магния, алюминия; переходных металлов (меди, цинка, хрома, железа)
2.3. Характерные химические свойства простых веществ – неметаллов: водорода, галогенов, кислорода, серы, азота, фосфора, углерода, кремния
2.4. Характерные химические свойства оксидов: основных, амфотерных, кислотных
2.5. Характерные химические свойства оснований и амфотерных гидроксидов
2.6. Характерные химические свойства кислот
2.7. Характерные химические свойства солей: средних, кислых, основных; комплексных (на примере соединений алюминия и цинка)
2.8. Взаимосвязь различных классов неорганических веществ
3. ОРГАНИЧЕСКАЯ ХИМИЯ
3.1. Теория строения органических соединений: гомология и изомерия (структурная и пространственная). Взаимное влияние атомов в молекулах
3.2. Типы связей в молекулах органических веществ. Гибридизация атомных орбиталей углерода. Радикал. Функциональная группа
Радикал. Функциональная группа
3.3. Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)
3.4. Характерные химические свойства углеводородов: алканов, циклоалканов, алкенов, диенов, алкинов, ароматических углеводородов (бензола и гомологов бензола, стирола)
3.5. Характерные химические свойства предельных одноатомных и многоатомных спиртов, фенола.
3.6. Характерные химические свойства альдегидов, карбоновых кислот, сложных эфиров
3.7. Характерные химические свойства азотсодержащих органических соединений: аминов и аминокислот. Важнейшие способы получения аминов и аминокислот
3.8. Биологически важные вещества: жиры, белки, углеводы (моносахариды, дисахариды, полисахариды)
3.9. Взаимосвязь органических соединений
4. МЕТОДЫ ПОЗНАНИЯ В ХИМИИ. ХИМИЯ И ЖИЗНЬ
4.1. Экспериментальные основы химии
4.1.1. Правила работы в лаборатории. Лабораторная посуда и оборудование. Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии
Правила безопасности при работе с едкими, горючими и токсичными веществами, средствами бытовой химии
4.1.2. Научные методы исследования химических веществ и превращений. Методы разделения смесей и очистки веществ
4.1.3. Определение характера среды водных растворов веществ. Индикаторы
4.1.4. Качественные реакции на неорганические вещества и ионы
4.1.5. Качественные реакции органических соединений
4.1.6. Основные способы получения (в лаборатории) конкретных веществ, относящихся к изученным классам неорганических соединений
4.1.7. Основные способы получения углеводородов (в лаборатории): алканов, алкенов, алкинов, циклоалканов, алкадиенов, аренов
4.1.8. Основные способы получения органических кислородсодержащие соединений (в лаборатории): спиртов, альдегидов и кетонов, карбоновых кислот
4.2.1. Понятие о металлургии: общие способы получения металлов
4.2.2. Общие научные принципы химического производства (на примере промышленного получения аммиака, серной кислоты, метанола). Химическое загрязнение окружающей среды и его последствия
Химическое загрязнение окружающей среды и его последствия
4.2.3. Природные источники углеводородов, их переработка
4.2.4. Высокомолекулярные соединения. Реакции полимеризации и поликонденсации. Полимеры. Пластмассы, волокна, каучуки
4.3. Расчеты по химическим формулам и уравнениям реакций
4.3.1. Расчеты с использованием понятия «массовая доля вещества в растворе»
4.3.2. Расчеты объемных отношений газов при химических реакциях
4.3.3. Расчеты массы вещества или объема газов по известному количеству вещества, массе или объему одного из участвующих в реакции веществ
4.3.4. Расчеты теплового эффекта реакции
4.3.5. Расчеты массы (объема, количества вещества) продуктов реакции, если одно из веществ дано в избытке (имеет примеси)
4.3.6. Расчеты массы (объема, количества вещества) продукта реакции, если одно из веществ дано в виде раствора с определенной массовой долей растворенного вещества
4.3.7. Установление молекулярной и структурной формулы вещества
4. 3.8. Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного
3.8. Расчеты массовой или объемной доли выхода продукта реакции от теоретически возможного
4.3.9. Расчеты массовой доли (массы) химического соединения в смеси
Курс подготовки к ЕГЭ или ОГЭ (ГИА) по химии:
Общая химия
Часть 1. Строение вещества
1. Строение атома. Электронные формулы атомов
2. Периодический закон
3. Строение молекул. Типы химических связей. Основные характеристики ковалентной связи. Межмолекулярные связи
4. Строение вещества (кристаллические решетки). Основные физические свойства различных кристаллов
5. Степень окисления и валентность химических элементов.
Часть 2. Основы неорганической химии
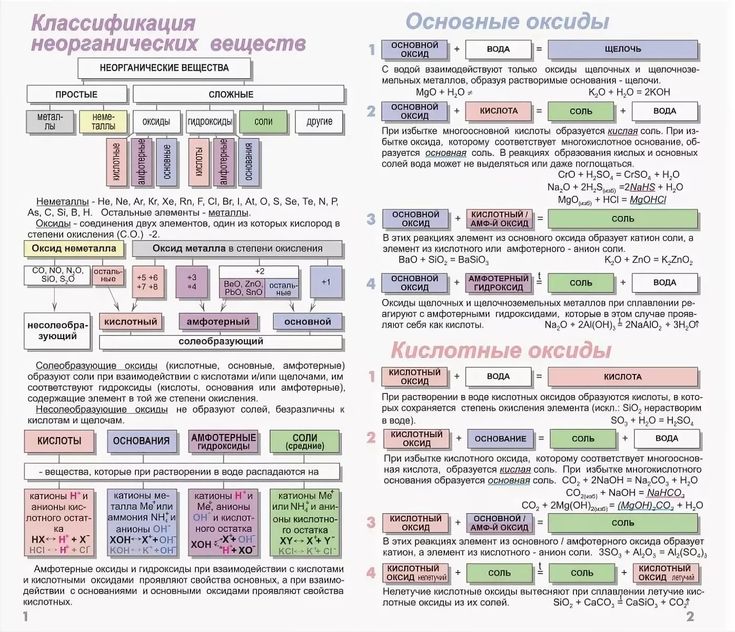
1. Классификация неорганических веществ
2. Номенклатура неорганических веществ
3. Способы получения оксидов
4. Химические свойства основных оксидов
5. Химические свойства кислотных оксидов
6. Химические свойства амфотерных оксидов
7. Химические свойства и способы получения кислот
Химические свойства и способы получения кислот
8. Химические свойства и способы получения солей
9. Химические свойства и способы получения оснований
10. Взаимосвязь основных классов неорганических веществ
11. Бинарные соединения — гидриды.
12. Реакции разложения в неорганической химии
Часть 3. Физико-химия растворов:
1. Понятие о растворах, растворимость
2. Теория электролитической диссоциации
3. Реакции ионного обмена
4. Гидролиз.
Часть 4. Окислительно-восстановительные реакции
1. Окислительно-восстановительные реакции.
2. Электролиз солей. Электролиз солей карбоновых кислот. Коррозия.
Часть 5. Особенности работы в лаборатории
Часть 6. Химические реакции. Закономерности их протекания
1. Классификация химических реакций.
2. Кинетика (скорость) химических реакций и ее зависимость от разных факторов.
3. Термодинамика химических реакций: химическое равновесие и его смещение.
Органическая химия
1. Теория строения органических веществ. Классификация органических веществ. Гомологи и изомеры. Виды изомерии.
2. Алканы: химические и физические свойства, строение, получение, изомерия.
3. Алкены: химические и физические свойства, строение, получение, изомерия.
4. Алкины: химические и физические свойства, строение, получение, изомерия.
5. Алкадиены: химические и физические свойства, строение, получение, изомерия.
6. Арены: химические и физические свойства, строение, получение, изомерия.
7. Циклоалканы: химические и физические свойства, строение, получение, изомерия.
8. Спирты: химические и физические свойства, строение, изомерия и способы получения. Фенолы: химические свойства, способы получения, строение и изомерия.
9. Альдегиды и кетоны: химические и физические свойства, строение и изомерия, получение.
10. Карбоновые кислоты: химические и физические свойства, строение, номенклатура и изомерия, способы получения.
11. Сложные эфиры: химические и физические свойства, строение, получение, изомерия.
12. Жиры: химические и физические свойства, строение, получение.
13. Углеводы: химические и физические свойства, строение, получение.
14. Амины: химические и физические свойства, строение, получение, изомерия.
15. Аминокислоты: химические и физические свойства, строение, получение, изомерия.
16. Белки: химические и физические свойства, строение и получение.
17. Взаимосвязь разных классов органических веществ.
18. Качественные реакции в органической химии.
Характерные реакции в органической химии:
Реакция Дюма Электролиз солей карбоновых кислот Пиролиз метана Реакция Вагнера
Химия элементов
Часть 1. Химия щелочных металлов и их соединений. Пероксиды щелочных металлов. Гидроксиды щелочных металлов.
Химия щелочных металлов и их соединений. Пероксиды щелочных металлов. Гидроксиды щелочных металлов.
Часть 2. Химия щелочноземельных металлов. Оксиды щелочноземельных металлов. Гидроксиды щелочноземельных металлов.
Часть 3. Химия алюминия и его соединений. Оксид алюминия. Гидроксид алюминия. Соли алюминия.
Часть 4. Химия углерода. Оксид углерода (II) и оксид углерода (IV). Угольная кислота и ее соли (карбонаты и гидрокарбонаты).
Часть 5. Химия кремния. Оксид кремния (IV). Кремниевая кислота. Силан. Силикаты.
Часть 6. Химия азота и его соединений. Оксиды азота. Аммиак. Нитриды. Азотная кислота и азотистая кислота. Нитраты.
Часть 7. Химия фосфора и его соединений. Фосфин. Фосфиды металлов. Оксиды фосфора III и V. Фосфорные кислоты и их соли (фосфаты, гидрофосфаты и дигидрофосфаты, пирофосфаты и метафосфаты). Фосфористая кислота.
Часть 8. Химия кислорода и его соединений.
Часть 9. Химия серы и ее соединений. Сероводород и сульфиды. Оксиды серы – сернистый газ и серный ангидрид. Серная кислота и ее свойства. Сернистая кислота. Особенности химии сульфатов и сульфитов.
Серная кислота и ее свойства. Сернистая кислота. Особенности химии сульфатов и сульфитов.
Часть 10. Химия галогенов и их соединений.
Часть 11. Химия d-элементов: железа, хрома, цинка, меди.
Часть 12. Химия водорода и его соединений.
Задачи: базовый блок
1. Атомно -молекулярное учение
2. Способы выражения концентрации в растворах: массовая доля, растворимость, молярная концентрация.
3. Расчеты по уравнению реакции
4. Задачи на избыток-недостаток
5. Задачи на примеси
6. Задачи на выход
Задачи повышенной сложности
1. Задачи на электролиз
2. Задачи на кристаллогидраты
3. Задачи на пластинки
4. Задачи на порции
5. Неполное разложение
6. Задачи на альтернативные реакции (кислые/средние соли, амфотерность)
7. Задачи на атомистику
8. Задачи на смеси и сплавы
9. Задачи на растворимость
Диагностические и тренировочные работы
Все реальные варианты КИМ ЕГЭ по химии
Тренировочная работа по химии в формате ЕГЭ 26 октября 2017 года
Тренировочная работа по химии для 11 классов 30 ноября 2017 года
Досрочный ЕГЭ по химии 25. 03.2019
03.2019
Видеоопыты
Видеоопыты по общей и неорганической химии
Видеоопыты по органической химии
Понравилось это:
Нравится Загрузка…
Теория и практика по химии
12 сентября 2019
В закладки
Обсудить
Жалоба
TG 4ЕГЭ
Химия
В этой статье собраны ссылки на самые важные материалы.
При проверке тестов не забывайте заглядывать в комментарии к постам: там можно найти ответы на интересные вопросы или информацию об опечатках, если они были.
Хэштеги
#vopros_1_ege@chem4you и #vopros_1_ege@chem4you— теория и практика к №1 ЕГЭ
#vopros_2_ege_Dacuk_Stepenin и #vopros_2_ege@chem4you— теория и практика к №2 ЕГЭ
#vopros_3_ege_Dacuk_Stepenin — теория и практика к №3 ЕГЭ
#vopros_4_ege_Dacuk_Stepenin — теория и практика к №4 ЕГЭ
#vopros_5_ege_Dacuk_Stepenin — теория и практика к №5 ЕГЭ
#vopros_6_ege_Dacuk_Stepenin — теория и практика к №6 ЕГЭ
#vopros_7_ege_Dacuk_Stepenin — теория и практика к №7 ЕГЭ
#vopros_10_ege_Dacuk_Stepenin — теория и практика к №10 ЕГЭ
#vopros_19_ege_Dacuk_Stepenin — теория и практика к №19 ЕГЭ
#vopros_25_ege_Dacuk_Stepenin — теория и практика к №25 ЕГЭ
#vopros_27_ege_Dacuk_Stepenin — задачи №27
#vopros_28_ege_Dacuk_Stepenin — задачи №28
#vopros_29_ege_Dacuk_Stepenin — задачи №29
#vopros_30_ege_Dacuk_Stepenin — теория и практика к №30 ЕГЭ
#vopros_31_ege_Dacuk_Stepenin — теория и практика к №31 ЕГЭ
#task@chem4you — задания-опросы на разные темы
#neorg_Dacuk_Stepenin — полезности по неорганике
#test_Dacuk_Stepenin — подборки тестов
#infographic_Dacuk_Stepenin — схемы и иллюстрации
Тренировочные варианты ЕГЭ
В 2019/2020 году тренировочные варианты выходят раз в две недели. По средам выкладываем задания, по субботам — ответы.
По средам выкладываем задания, по субботам — ответы.
2020 — #kim2020@chem4you
2019 — https://vk.com/topic-52582503_39485203
34 задача ЕГЭ
- На пластинку
- На олеум
- На электролиз
- Про лишние данные в задачах
- Задачи с редкими реакциями
- Кристаллогидраты
- Растворимость
- Нестандартные задачи на растворы (актуальный файл в комментариях)
- Тренажер «Какая реакция идет первой»
ОВР-МАРАФОН
- Видео + тесты «Степень окисления»
- Видео + тесты «Окислитель и восстановитель»
- Статья про азотную кислоту
- Статья про серную кислоту
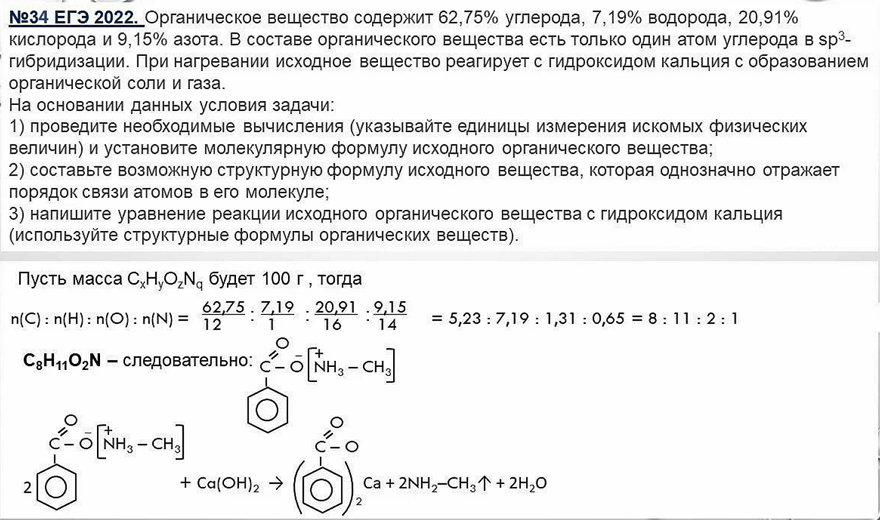
35 задача ЕГЭ
Сказка про медведей, которые формулу выводили — https://vk.com/wall-52582503_669
Тренируем округления — https://vk.com/wall-52582503_684
Просто подборка — https://vk.com/wall-52582503_945
Задачи с азотом — https://vk.com/wall-52582503_959
Полимеры и мономеры — https://vk. com/wall-52582503_1219
com/wall-52582503_1219
Свойства основных классов веществ
Кислые и основные соли — https://vk.com/wall-52582503_3338
Тренажер «Свойства кислот, получение солей» — https://vk.com/wall-52582503_2723
Всякое полезное
Допущения на ЕГЭ — https://vk.com/wall-52582503_3304
Ошибки во втором задании ЕГЭ — https://vk.com/wall-52582503_2887
Коварный иодоводород — https://vk.com/wall-52582503_2879
Чего нет в таблице растворимости: Cu(+) — https://vk.com/wall-52582503_3499
Суровые сульфиды — https://vk.com/wall-52582503_3368
Соответствие кислотный оксид — кислота — https://vk.com/wall-52582503_3568
Шпаргалка по металлам — https://vk.com/wall-52582503_3442
Реакция Вюрца — https://vk.com/wall-52582503_3591
Шпаргалка по пероксидам — https://vk.com/wall-52582503_3655
Реакции декарбоксилирования — https://vk.com/wall-52582503_3675
Важное про оформление и задания ЕГЭ — https://vk. com/@chem4you-faq-ege
com/@chem4you-faq-ege
Шпаргалка по циклоалканам — https://vk.com/wall-52582503_3697
Опасные места в таблице растворимости -https://vk.com/wall-52582503_3622
Качественная реакция на галогенсодержащую органику — https://vk.com/wall-52582503_3942
Растворение и среда раствора — https://vk.com/wall-52582503_4091
Гидроксид меди (II) и органика — https://vk.com/wall-52582503_3815
Сила кислот — https://vk.com/wall-52582503_3750
ОВР в органике — https://vk.com/wall-52582503_4172
Гидролиз в органике — https://vk.com/wall-52582503_4281
Расстановка коэффициентов в реакции горения — https://vk.com/wall-52582503_4106
Откуда взялись гомологические формулы — https://vk.com/wall-52582503_4124
ОВР в органике в нейтральной среде — https://vk.com/wall-52582503_4222
Базовые задачи
Массовая доля элемента в веществе, часть 1 — https://vk.com/wall-52582503_15
Массовая доля элемента в веществе, часть 2 — https://vk. com/wall-52582503_16
com/wall-52582503_16
Массовая доля вещества в растворе — https://vk.com/wall-52582503_18
Задачи на избыток и недостаток — https://vk.com/wall-52582503_70
Тесты по органике
Алканы, алкены, циклы, диены, алкины — https://vk.com/wall-52582503_3897
Арены — https://vk.com/wall-52582503_4048
Спирты, фенолы — https://vk.com/wall-52582503_4297
Альдегиды, кетоны — https://vk.com/wall-52582503_4534
Карбоновые кислоты, сложные эфиры — https://vk.com/wall-52582503_5271
Химия элементов
Таблица по свойствам неметаллов — https://vk.com/wall-52582503_2685
Прошлые статьи по химии и вопросы по темам
Выберите свой уровень:
A LevelASIBGCSEIGCSEInternational A LevelInternational ASO LevelPre U
Не знаете, с чего начать, когда дело доходит до пересмотра курса химии? Благодаря этим ресурсам по пересмотру вы будете точно знать, на чем сосредоточиться и как структурировать свой пересмотр, чтобы вы могли быть готовы к экзамену в кратчайшие сроки.
Здесь вы найдете четкие примечания к повторению, прошлые работы по химии, типичные экзаменационные вопросы, полностью объясненные типовые ответы и многое другое.
Просто выберите свой квалификационный уровень ((I)GCSE, A Level, IB) и экзаменационную комиссию ниже, и погрузитесь во все, что вам нужно, чтобы учиться умнее, а не усерднее.
AQA Уровень A Химия
Примечания к пересмотруТематические вопросыПрошлые документы Тематические вопросыПрошлые докладыCIE Уровень A Химия
Примечания к пересмотруТематические вопросыПрошлые докладыТеория и альтернатива практическим темам ВопросыПрошлые доклады Тематические вопросы0012 OCR A Уровень химии Пересмотр NoteStopic Вопросы. Вопросы: Вопросы папстопических вопросовAQA как химия
Пересмотр. QuestionsDP IB Chemistry: HL
Revision Notes Topic Questions Practice Paper QuestionsDP IB Chemistry: SL
Пересмотр вопросов NoteStopic Вопросы Practice ВопросыAQA GCSE Chemistry
Ревизия NoteStopic Вопросы Paper Paperspast Paper ВОПРОСЫAQA GCSE Chemistry: Комбинированная наука
РЕССИОН НЕОБХОД Заметки о пересмотреТематические вопросыПрошлые работыOCR Gateway GCSE Chemistry
Заметки о пересмотреТематические вопросыПрошлые работыПрошлые работы Тематические вопросыOCR Gateway GCSE Chemistry: Комбинированная наука
Пересмотр NoteStopic ВопросыCIE IGCSE Chemistry
Пересмотр NoteStopic Вопросы Paperspast Paper Topic Вопросы и альтернатива практической тематической тематикеEdexcel IGCSE Chemistry
NotesteStic Papestopic Papersciste 9001 ED ED ED ED ED ED EDEXCES 900SCESCE 900SCESCES 900SCESE 900SCESE 900SCESE 900SCESE 900SCESE 9001.
Edexcel IGCSE Chemistry: Double Science
Примечания к изменениям Предыдущие статьиТематические вопросыEdexcel International A Level Chemistry
Пересмотр NoteStopic Вопросы Поспространения папстопических вопросовEdexcel International As Chemistry
Revision NotesCIE o Уровень Химия
Прошние папскорости.Компания
Быстрые ссылки
Mocks 2019 – Chemistry PLC
10 апреля 2019 г. Mr B Clayton
Это разбивка всего содержания, которое будет в вашей экзаменационной работе AP2 1 и охватывает все темы раздела химии. Используйте это, свои книги, карточки и все ресурсы в классе Google, чтобы определить свои сильные стороны и области, над которыми вам нужно поработать при подготовке к экзамену.








Leave A Comment