Энергетический обмен — что это, определение и ответ
Энергетический обмен (диссимиляция, катаболизм) – это совокупность химических реакций постепенного распада органических соединений, сопровождающихся высвобождением энергии, часть которой расходуется на синтез АТФ.
Синтез АТФ происходит в клетках всех организмов в процессе фосфорилирования, т. е. присоединения остатка фосфорной кислоты к АДФ (аденозиндифосфату). Энергия для фосфорилирования АДФ образуется в ходе энергетического обмена.
В зависимости от среды обитания диссимиляция может протекать в два или три этапа.
У большинства живых организмов – аэробов, живущих в кислородной среде, – в ходе диссимиляции осуществляется три этапа: подготовительный, бескислородный, кислородный.
У анаэробов, обитающих в среде, лишенной кислорода, или у аэробов при его недостатке, диссимиляция протекает лишь в два первых этапа с образованием промежуточных органических соединений, еще богатых энергией.

Рисунок – распад и синтез АТФ
Этапы энергетического обмена
Рассмотрим энергетический обмен в многоклеточном организме (например, человеческом) и в одноклеточном (например, клетке простейшего).
Первый этап – подготовительный.
В желудочно-кишечном тракте многоклеточных организмов он осуществляется пищеварительными ферментами.
У одноклеточных – ферментами лизосом.
На первом этапе происходит расщепление белков до аминокислот, жиров до глицерина и жирных кислот, полисахаридов до моносахаридов, нуклеиновых кислот до нуклеотидов. Этот процесс называется пищеварением. Вся энергия на этом этапе рассеивается в виде тепла.
Второй этап – бескислородный (гликолиз).
С6Н12O6 + 2АДФ + 2Ф → 2С3Н4O3 + 2АТФ.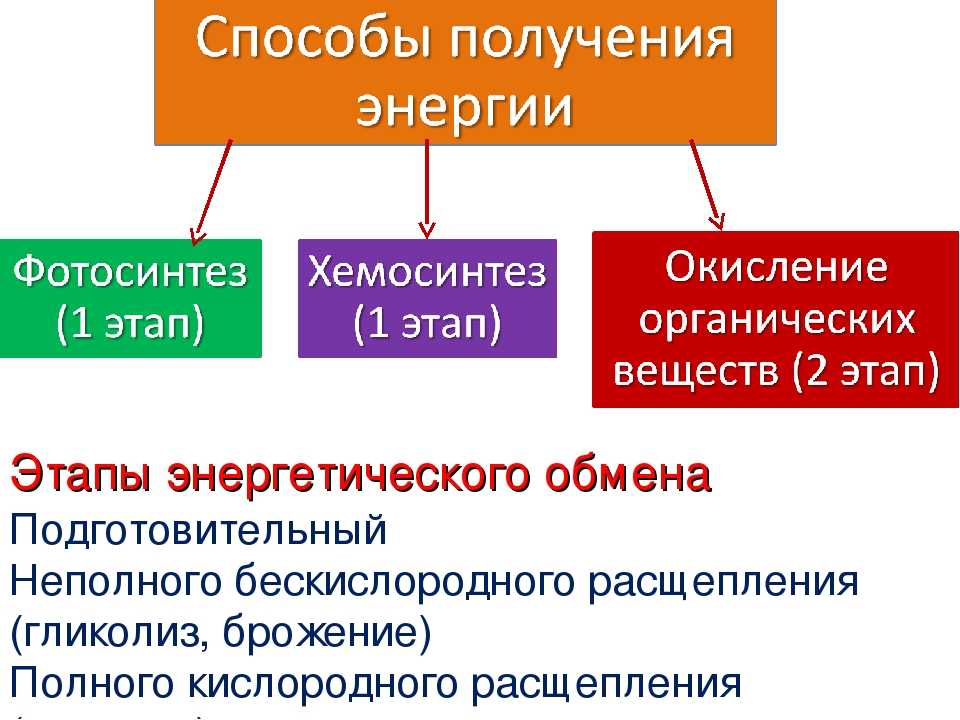
Остальная энергия рассеивается в виде тепла.
Энергии, накопленной при гликолизе, слишком мало для организмов, использующих кислород для своего дыхания. Вот почему в мышцах животных, в том числе и у человека, при больших нагрузках и нехватке кислорода образуется молочная кислота (С3Н6O3), которая накапливается в виде лактата. Появляется боль в мышцах. У нетренированных людей это происходит быстрее, чем у людей тренированных
Третий этап – кислородный.
Состоит из двух последовательных процессов – цикла Кребса, названного по имени Нобелевского лауреата Ганса Кребса, и окислительного фосфорилирования.
Его смысл заключается в том, что при кислородном дыхании пируват окисляется до окончательных продуктов – углекислого газа и воды, а энергия, выделяющаяся при окислении, запасается в виде 36 молекул АТФ. (34 молекулы в цикле Кребса и 2 молекулы в ходе окислительного фосфорилирования).

Энергия распада органических соединений обеспечивает реакции их синтеза в пластическом обмене.
Эволюционно кислородный этап возник после накопления в атмосфере достаточного количества молекулярного кислорода и появления аэробных организмов.
Окислительное фосфорилирование, или клеточное дыхание.
Происходит на внутренних мембранах митохондрий, в которые встроены молекулы-переносчики электронов и ферментные комплексы АТФ-синтазы.
Молекулы-переносчики транспортируют электроны к молекулярному кислороду. Часть энергии рассеивается в виде тепла, а часть расходуется на образование АТФ.
Суммарная реакция энергетического обмена:
С6Н12O6 + 6O2 → 6СO2 + 6Н2O + 38АТФ.
Бескислородный и кислородный этапы энергетического обмена
Для удобства запоминания, используйте таблицу с этапами энергетического обмена.
30. Этапы энергетического обмена в клетке. Анаэробный этап. Брожение.
Первый этап— подготовительный. Пища поступает в организм животных и человека в виде сложных высокомолекулярных соединений. Прежде чем поступить в клетки и ткани, эти вещества должны разрушиться до низкомолекулярных, более доступных для клеточного усвоения веществ. На первом этапе происходит гидролитическое расщепление органических веществ, идущее при участии воды. Оно протекает под действием ферментов в пищеварительном тракте многоклеточных животных, в пищеварительных вакуолях одноклеточных, а на клеточном уровне — в лизосомах.
Второй этап осуществляется на клеточном уровне при
отсутствии кислорода. Он протекает в
цитоплазме клетки. Рассмотрим расщепление
глюкозы, как одного из ключевых веществ
обмена в клетке. Все остальные органические
вещества (жирные кислоты, глицерин,
аминокислоты) на разных этапах втягиваются
в процессы ее превращения. Бескислородное
расщепление глюкозы называется гликолизом.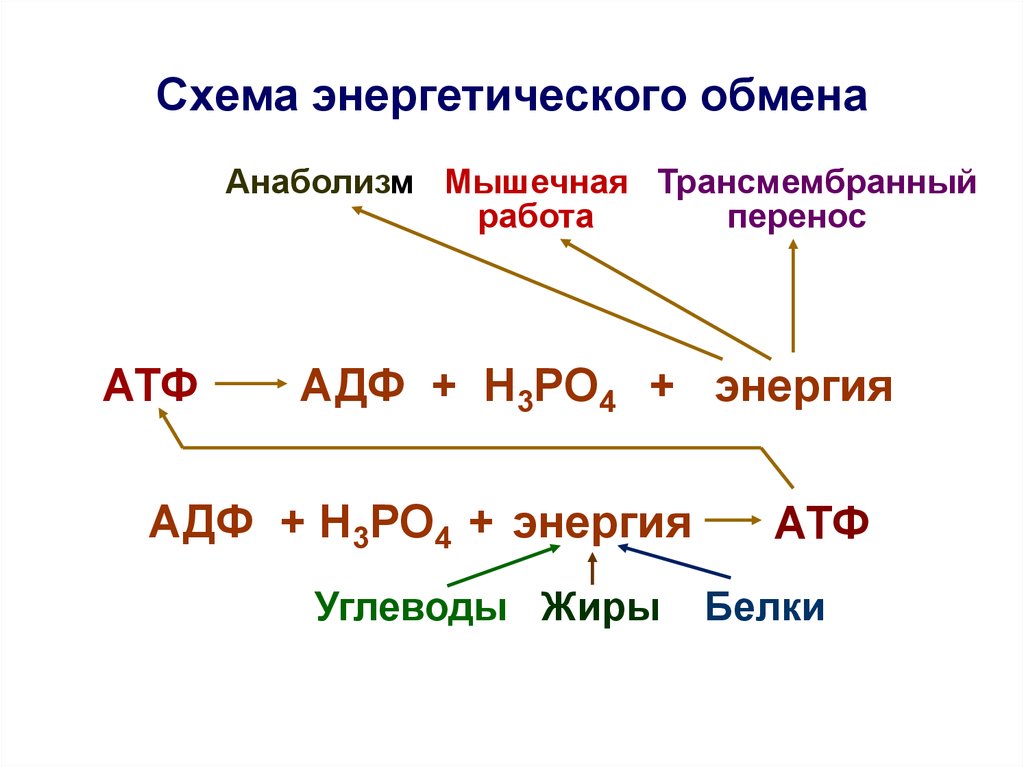
Третий этап — биологическое окисление, или дыхание. Этот этап протекает только в присутствии кислорода и иначе называется кислородным. Он протекает в митохондриях.
Начальные этапы окисления углеводов происходят в цитозоле и не требуют участия кислорода, поэтому эта стадия процесса называется анаэробным окислением, или гликолизом. Главным субстратом окисления при анаэробном получении энергии служат гексозы и в первую очередь глюкоза. Процесс гликолиза включает 9 последовательных ферментативных реакций, в результате которых молекула глюкозы превращается в две молекулы пирувата. В ходе некоторых из этих реакций происходит восстановление НАД+ до НАДН и перенос неорганического фосфата на АДФ с образованием высокоэнергетической связи АТФ. В глюкозе количество потенциальной энергии, заключенной в связях между атомами С, Н и О, составляет около 680 ккал на 1 моль. Эта энергия освобождается при полном окислении глюкозы: С6Н12О6+6О2=6Н2О+6СО2+680ккал.
В процессе гликолиза происходит неполное
окисление субстрата. В результате него
глюкоза распадается до триоз, при этом
тратятся 2 молекулы АТФ и синтезируются
4 молекулы АТФ, так что в конечном
результате клетка получает всего 2
молекулы АТФ. В энергетическом отношении
этот процесс малоэффективен, поэтому
из 680 ккал, заключающихся в связях 1 моля
глюкозы, освобождается менее 10% энергии.
Несмотря на низкий энергетический
выход, анаэробное окисление, гликолиз,
широко используется в живой природе.
Эритроциты млекопитающих, например,
получают всю необходимую им энергию за
счет гликолиза, так как у них нет
митохондрий. Конечные продукты гликолиза
— триозы, в первую очередь пировиноградная
кислота, все еще несут большое количество
химической энергии и вовлекаются в
дальнейшее окисление, происходящее в
самих митохондриях.
В результате него
глюкоза распадается до триоз, при этом
тратятся 2 молекулы АТФ и синтезируются
4 молекулы АТФ, так что в конечном
результате клетка получает всего 2
молекулы АТФ. В энергетическом отношении
этот процесс малоэффективен, поэтому
из 680 ккал, заключающихся в связях 1 моля
глюкозы, освобождается менее 10% энергии.
Несмотря на низкий энергетический
выход, анаэробное окисление, гликолиз,
широко используется в живой природе.
Эритроциты млекопитающих, например,
получают всю необходимую им энергию за
счет гликолиза, так как у них нет
митохондрий. Конечные продукты гликолиза
— триозы, в первую очередь пировиноградная
кислота, все еще несут большое количество
химической энергии и вовлекаются в
дальнейшее окисление, происходящее в
самих митохондриях.
Про этапы см. 30 вопрос.
Окислительные процессы в митохондриях
связаны с окислительным циклом
трикарбоновых кислот и с дыхательной
цепью переноса электронов. Они начинаются
после образования в матриксе достаточного
количества ацетил-КоА из пирувата и
жирных кислот.
Главная функция цикла
лимонной кислоты-окисление ацетата,
который включается в цикл в форме молекул
ацетил-КоА. Цикл начинается взаимодействия
ацетил-КоА с оксалоацетатом, что приводит
к образованию цитрата. Далее в ходе семи
последовательных ферментативных реакций
два атома углерода удаляются в виде
углекислого газа, и в конце концов
регенерируется оксалоацетат. Каждый
оборот цикла дает две молекулы углекислого
газа, который диффундирует из митохондрий
и покидает клетку. Энергия, высвобождающаяся
при окислении химических связей лимонной
кислоты, потребляется в цикле трикарбоновых
кислот несколькими способами.
Окислительное фосфорилирование связано
с переносом электронов от НАДН и ФАДН
по дыхательной цепи к молекулярному
кислороду и использованием энергии для
синтеза АТФ. Эти процессы протекают на
внутренней мембране митохондрий, в
которой находятся белки-переносчики
дыхательной цепи и комплексы АТФ-синтетазы.
Дыхательная цепь внутренней
мембраны митохондрий содержит три
главных ферментных комплекса, участвующих
в переносеэлектронов
с НАДН на кислород. Первый,
НАДН-дегидрогеназный, комплекспринимает электроны от HAДH
и переносит их во второй комплекс-комплекс
цитохромов b-с,
который переносит их на цитохромоксидазный
комплекс, передающий электроны на
кислород, в результате чего образуется
вода. На этом процесс окисления
заканчивается (конечными продуктами
окисления исходного субстрата являются
углекислый газ и вода). Перенос электронов
по дыхательнойцепи
происходит с участием убихинона и
цитохрома с-мобильных переносчиков,
передвигающихся в мембране от одного
комплекса к другому и обратно. Переносчики
электронов расположены и дыхательной
цепи таким образом, что каждый последующий
комплекс обладает большим сродством к
электронам, чем предыдущий. Электроны
перемещаются от одного комплекса к
другому, пока не перейдут на кислород,
имеющий наибольшее сродство к электрону.
Перенос электронов сопровождается их
переходом на более низкие энергетические
уровни и выделением энергии.
Преобразование энергии
окислительных реакций в энергию АТФ
происходит на внутренней митохондриальной
мембране в результате хемиосмоса. При
достижении определенной разности
потенциалов (220 мВ) белковый комплекс
АТФ-синтетазы начинает транспортировать
протоны обратно в матрикс и при этом
превращает одну форму энергии в другую:
образует АТФ из АДФ и неорганического
фосфата. АТФ-синтетаза состоит из двух
основных частей: мембранного компонента
F0,
осуществляющего транспорт протонов
через мембрану, и сопрягающего фактора
F1,
осуществляющего синтез АТФ.
Окислительные процессы в митохондриях и фосфорилирование АДФ можно разобщить, сняв разность потенциалов на митохондриальной мембране, сделав в ней диффузионные каналы, а также механическим нарушением, либо с помощью различных химических соединений. Перенос электронов и окисление субстрата будут продолжаться, но синтеза АТФ не будет. Разобщение метаболических процессов окисления и фосфорилирования приводит к образованию значительного количества тепла вместо накопления энергии в форме макроэргических соединений.
Суммарное уравнение: С6Н12О6 + 6О2 → 6СО2 + 6Н2О + 38АТФ + Q
32. Гипотеза
эволюционного происхождения митохондрий,
хлоропластов, ядра, ЭПР. Возникновение клеточной
организации в ходе эволюции. (нет) Теорию
эндосимбиотического происхождения
хлоропластов впервые предложил в 1883
годуАндреас
Шимпер, показавший
их саморепликацию внутри клетки.
А. С. Фаминцин и О. В. Баранецкий-о
двойственной природе лишайников
— комплекса гриба и водоросли. К. С. Мережковский в
1905 году предложил само название
«симбиогенез», впервые детально
сформулировал теорию и даже создал на
её основе новую систему органического
мира.
Фаминцин в 1907 году, опираясь
на работы Шимпера, также пришёл к выводу,
что хлоропласты являются симбионтами,
как и водоросли в составе лишайников.
В
В. Баранецкий-о
двойственной природе лишайников
— комплекса гриба и водоросли. К. С. Мережковский в
1905 году предложил само название
«симбиогенез», впервые детально
сформулировал теорию и даже создал на
её основе новую систему органического
мира.
Фаминцин в 1907 году, опираясь
на работы Шимпера, также пришёл к выводу,
что хлоропласты являются симбионтами,
как и водоросли в составе лишайников.
В
Митохндрии — это потомки аэробных бактерий (прокариот),поселившихся некогда в предковой эукариотической клетке и «научившимися» жить в ней в качестве симбионтов.Пластиды, подобно митохондриям, имеют свои собственные прокариотические ДНК и рибосомы. По-видимому, хлоропласты произошли от фотосинтезирующих бактерий, поселившихся в своё время в гетеротрофных клетках протистов, превратив их в автотрофные водоросли.
Доказательства Митохондрии и пластиды:•
имеют две полностью замкнутые мембраны. При этом внешняя сходна с мембранами вакуолей,
внутренняя — бактерий.•
размножаются бинарным
делением (причём
делятся иногда независимо от деления клетки)• генетический
материал — кольцевая ДНК,
не связанная с гистонами (ДНКмитохондрий и пластид ближе
к ДНК бактерий, чем к ядерной ДНК эукариот)•
имеют свой аппарат синтеза
белка— рибосомы и
др.
При этом внешняя сходна с мембранами вакуолей,
внутренняя — бактерий.•
размножаются бинарным
делением (причём
делятся иногда независимо от деления клетки)• генетический
материал — кольцевая ДНК,
не связанная с гистонами (ДНКмитохондрий и пластид ближе
к ДНК бактерий, чем к ядерной ДНК эукариот)•
имеют свой аппарат синтеза
белка— рибосомы и
др.
Смешение у эукариот многих свойств,
характерных для архей и бактерий,
позволило предположить симбиотическое
происхождение ядра от
метаногенной архебактерии, внедрившейся
в клетку миксобактерии. В последнее десятилетие сформировалась
также гипотеза вирусного
эукариогенеза (англ.viral
eukaryogenesis). В её основании лежит ряд
сходств устройства генетического
аппарата эукариот и вирусов: линейное
строение ДНК, её тесное взаимодействие
с белками и др. Было показано
сходство ДНК-полимеразы эукариот
и поксивирусов,
что сделало именно их предков основными
кандидатами на роль ядра.
4.1: Обзор метаболизма — Медицина LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 5979
Развитие навыков
- Кратко опишите, как получается и используется энергия из дающих энергию нутриентов, а также как и где она сохраняется в организме для дальнейшего использования.
- Объясните роль энергии в процессе построения тканей и органов.
В различных главах этого текста мы исследовали метаболизм углеводов, липидов и белков. В следующем разделе мы соберем эту информацию, чтобы получить четкое представление о важности метаболизма в питании человека.
Метаболизм определяется как сумма всех химических реакций, необходимых для поддержания клеточной функции и, следовательно, жизни организма. Метаболизм классифицируется либо как катаболизм, относящийся ко всем метаболическим процессам, связанным с распадом молекул, либо к анаболизму, который включает все метаболические процессы, участвующие в построении более крупных молекул. Как правило, катаболические процессы высвобождают энергию, а анаболические процессы потребляют энергию. Общими целями метаболизма являются передача энергии и транспорт веществ. Энергия из пищевых макроэлементов преобразуется в клеточную энергию, которая используется для выполнения клеточной работы. Метаболизм превращает макроэлементы в вещества, которые клетка может использовать для роста и размножения, а также в отходы.
Метаболизм классифицируется либо как катаболизм, относящийся ко всем метаболическим процессам, связанным с распадом молекул, либо к анаболизму, который включает все метаболические процессы, участвующие в построении более крупных молекул. Как правило, катаболические процессы высвобождают энергию, а анаболические процессы потребляют энергию. Общими целями метаболизма являются передача энергии и транспорт веществ. Энергия из пищевых макроэлементов преобразуется в клеточную энергию, которая используется для выполнения клеточной работы. Метаболизм превращает макроэлементы в вещества, которые клетка может использовать для роста и размножения, а также в отходы.
В главе 5 вы узнали, что ферменты — это белки и что их задача — катализировать химические реакции. (Напомним, что слово «катализирует» означает ускорение химической реакции и снижение энергии, необходимой для завершения химической реакции, при этом катализатор не расходуется в ходе реакции.) Без ферментов химические реакции не происходили бы с достаточно высокой скоростью и потребляют слишком много энергии для существования жизни. Метаболический путь представляет собой серию ферментативных реакций, которые превращают исходный материал (известный как субстрат) в промежуточные продукты, которые являются субстратами для следующих ферментативных реакций в пути, пока, наконец, не будет синтезирован конечный продукт в результате последней ферментативной реакции. в пути. Некоторые метаболические пути сложны и включают множество ферментативных реакций, а другие включают лишь несколько химических реакций.
Метаболический путь представляет собой серию ферментативных реакций, которые превращают исходный материал (известный как субстрат) в промежуточные продукты, которые являются субстратами для следующих ферментативных реакций в пути, пока, наконец, не будет синтезирован конечный продукт в результате последней ферментативной реакции. в пути. Некоторые метаболические пути сложны и включают множество ферментативных реакций, а другие включают лишь несколько химических реакций.
Для обеспечения клеточной эффективности метаболические пути, участвующие в катаболизме и анаболизме, регулируются в соответствии с энергетическим статусом, гормонами и уровнями субстрата и конечного продукта. Согласованное регулирование метаболических путей предотвращает неэффективное построение клетками молекулы, когда она уже доступна. Точно так же, как было бы неэффективно строить стену одновременно с ее разрушением, для клетки метаболически неэффективно синтезировать жирные кислоты и одновременно разрушать их.
Катаболизм пищевых молекул начинается при попадании пищи в рот, так как фермент слюнной амилазы инициирует расщепление углеводов. Весь процесс пищеварения превращает большие полимеры в пище в мономеры, которые могут быть абсорбированы. Углеводы расщепляются до моносахаридов, липиды – до жирных кислот, а белки – до аминокислот. Эти мономеры всасываются в кровоток либо напрямую, как в случае с моносахаридами и аминокислотами, либо переупаковываются в клетках кишечника для транспорта непрямым путем через лимфатические сосуды, как в случае с жирными кислотами и другими жирорастворимыми молекулами. После всасывания кровь переносит питательные вещества к клеткам. Клетки, которым требуется энергия или строительные блоки, поглощают питательные вещества из крови и перерабатывают их катаболическим или анаболическим путем. Системам органов тела требуется топливо и строительные блоки для выполнения многих функций организма, таких как пищеварение, всасывание, дыхание, перекачка крови, транспортировка питательных веществ и отходов, поддержание температуры тела и создание новых клеток.
Энергетический метаболизм более конкретно относится к метаболическим путям, которые высвобождают или сохраняют энергию. Некоторые из них являются катаболическими путями, такими как гликолиз (расщепление глюкозы), β-окисление (расщепление жирных кислот) и катаболизм аминокислот. Другие являются анаболическими путями и включают те, которые участвуют в хранении избыточной энергии (например, гликогеноз) и синтезе триглицеридов (липогенез). В таблице \(\PageIndex{1}\) приведены некоторые катаболические и анаболические пути и их функции в энергетическом обмене.
| Катаболические пути | Функция | Анаболические пути | Функция |
|---|---|---|---|
| Гликолиз | Распад глюкозы | Глюконеогенез | Синтез глюкозы |
| Гликогенолиз | Распад гликогена | Гликогенез | Синтезировать гликоген |
| β-окисление | Расщепление жирных кислот | Липогенез | Синтез триглицеридов |
| Протеолиз | Расщепление белка до аминокислот | Синтез аминокислот | Синтезировать аминокислоты |
Катаболизм: распад
Когда уровень энергии высокий, клетки строят молекулы, а когда уровень энергии низкий, инициируются катаболические пути для производства энергии. Глюкоза является предпочтительным источником энергии для большинства тканей, но жирные кислоты и аминокислоты также могут катаболизироваться в молекулу клеточной энергии АТФ. Катаболизм питательных веществ в энергию можно разделить на три стадии, каждая из которых включает отдельные метаболические пути. Три стадии распада питательных веществ позволяют клеткам переоценить свои потребности в энергии, поскольку конечные продукты каждого пути могут быть либо переработаны в энергию, либо направлены на анаболические пути. Кроме того, промежуточные продукты метаболических путей иногда могут быть перенаправлены на анаболические пути после удовлетворения клеточных энергетических потребностей. Три стадии распада питательных веществ следующие:
Глюкоза является предпочтительным источником энергии для большинства тканей, но жирные кислоты и аминокислоты также могут катаболизироваться в молекулу клеточной энергии АТФ. Катаболизм питательных веществ в энергию можно разделить на три стадии, каждая из которых включает отдельные метаболические пути. Три стадии распада питательных веществ позволяют клеткам переоценить свои потребности в энергии, поскольку конечные продукты каждого пути могут быть либо переработаны в энергию, либо направлены на анаболические пути. Кроме того, промежуточные продукты метаболических путей иногда могут быть перенаправлены на анаболические пути после удовлетворения клеточных энергетических потребностей. Три стадии распада питательных веществ следующие:
- Стадия 1: Гликолиз глюкозы, β-окисление жирных кислот или катаболизм аминокислот
- Стадия 2: Цикл лимонной кислоты (или цикл Кребса)
- Стадия 3: Цепь переноса электронов и синтез АТФ
Расщепление глюкозы начинается с гликолиза, который представляет собой десятиэтапный метаболический путь, дающий две молекулы АТФ на молекулу глюкозы; гликолиз происходит в цитозоле и не требует кислорода. Помимо АТФ, конечными продуктами гликолиза являются две трехуглеродные молекулы, называемые пируватом. Пируват имеет несколько метаболических судеб. Во-первых, при недостатке кислорода он превращается в лактат, а затем направляется в печень. Во-вторых, если кислорода достаточно и клетка нуждается в энергии, она направляется в митохондрии и входит в цикл лимонной кислоты (или цикл Кори, или цикл Кребса), или, в-третьих, она может быть преобразована в другие молекулы (анаболизм).
Помимо АТФ, конечными продуктами гликолиза являются две трехуглеродные молекулы, называемые пируватом. Пируват имеет несколько метаболических судеб. Во-первых, при недостатке кислорода он превращается в лактат, а затем направляется в печень. Во-вторых, если кислорода достаточно и клетка нуждается в энергии, она направляется в митохондрии и входит в цикл лимонной кислоты (или цикл Кори, или цикл Кребса), или, в-третьих, она может быть преобразована в другие молекулы (анаболизм).
Пируват, который транспортируется в митохондрии, отщепляет один из своих атомов углерода с образованием ацетил-КоА. Ацетил-КоА, двухуглеродная молекула, общая для метаболизма глюкозы, липидов и белков, вступает во вторую стадию энергетического обмена, цикл лимонной кислоты. Это необратимый процесс. Расщепление жирных кислот начинается с катаболического пути, известного как β-окисление, которое происходит в митохондриях. В этом катаболическом пути четыре ферментативных этапа последовательно удаляют двухуглеродные молекулы из длинных цепей жирных кислот, давая молекулы ацетил-КоА. В случае аминокислот после удаления азота (дезаминирования) из аминокислоты оставшийся углеродный скелет может быть ферментативно преобразован в ацетил-КоА или какой-либо другой промежуточный продукт цикла лимонной кислоты.
В случае аминокислот после удаления азота (дезаминирования) из аминокислоты оставшийся углеродный скелет может быть ферментативно преобразован в ацетил-КоА или какой-либо другой промежуточный продукт цикла лимонной кислоты.
В лимонной кислоте циклический ацетил-КоА соединен с четырехуглеродной молекулой. В этом многоэтапном пути два атома углерода теряются при образовании двух молекул углекислого газа. Энергия, полученная от разрыва химических связей в цикле лимонной кислоты, трансформируется в еще две молекулы АТФ (или их эквиваленты) и высокоэнергетические электроны, переносимые молекулами никотинамидадениндинуклеотида (НАДН) и флавинадениндинуклеотида (ФАДН). 2 ). НАДН и ФАДН 2 переносят электроны (водород) на внутреннюю мембрану митохондрий, где происходит третий этап синтеза энергии, так называемая электронтранспортная цепь. В этом метаболическом пути происходит последовательный перенос электронов между несколькими белками и синтез АТФ. Также образуется вода.
Весь процесс катаболизма питательных веществ химически подобен горению, так как молекулы углерода сгорают с образованием углекислого газа, воды и тепла. Однако многие химические реакции при катаболизме питательных веществ замедляют распад молекул углерода, так что большая часть энергии может быть захвачена, а не преобразована в тепло и свет. Эффективность полного катаболизма питательных веществ составляет от 30 до 40 процентов, поэтому часть энергии высвобождается в виде тепла. Тепло является жизненно важным продуктом катаболизма питательных веществ и участвует в поддержании температуры тела. Если бы клетки были слишком эффективны в преобразовании энергии питательных веществ в АТФ, люди не дотянули бы до следующего приема пищи, так как они умерли бы от переохлаждения.
Мы измеряем энергию в калориях, которые представляют собой количество энергии, выделяемой для нагревания одного грамма воды на один градус Цельсия. Пищевые калории измеряются в ккал или калориях или 1000 калорий. При сгорании углеводы дают 4 ккал/г; белок дает 4 ккал/г; жир дает 9 ккал/г; а алкоголь дает 7 ккал/г.
При сгорании углеводы дают 4 ккал/г; белок дает 4 ккал/г; жир дает 9 ккал/г; а алкоголь дает 7 ккал/г.
Некоторые аминокислоты удаляют азот и затем поступают в цикл лимонной кислоты для производства энергии. Азот включается в мочевину, а затем удаляется с мочой. Углеродный скелет превращается в пируват или напрямую поступает в цикл лимонной кислоты. Эти аминокислоты называются глюконеогенными, потому что они могут быть использованы для производства глюкозы. Аминокислоты, которые дезаминируются и превращаются в ацетил-КоА, называются кетогенными аминокислотами и никогда не могут стать глюкозой.
Жирные кислоты никогда не могут быть превращены в глюкозу, но являются источником энергии. Они расщепляются на двухуглеродные единицы в процессе, называемом бета-окислением, и входят в цикл лимонной кислоты в виде ацетил-КоА. В присутствии глюкозы эти две углеродные единицы входят в цикл лимонной кислоты и сжигаются для получения энергии (АТФ) и производства побочного продукта CO 2 . Если глюкозы мало, образуются кетоны. Кетоновые тела можно сжигать для получения энергии. Мозг может использовать кетоны.
Если глюкозы мало, образуются кетоны. Кетоновые тела можно сжигать для получения энергии. Мозг может использовать кетоны.
Анаболизм: Здание
Энергия, высвобождаемая катаболическими путями, приводит в действие анаболические пути в построении макромолекул, таких как белки РНК и ДНК, и даже целых новых клеток и тканей. Анаболические пути необходимы для создания новой ткани, такой как мышцы, после длительных упражнений или ремоделирования костной ткани, процесса, включающего как катаболические, так и анаболические пути. Анаболические пути также создают молекулы для хранения энергии, такие как гликоген и триглицериды. Промежуточные продукты катаболических путей энергетического метаболизма иногда отвлекаются от производства АТФ и вместо этого используются в качестве строительных блоков. Это происходит, когда клетка находится в положительном энергетическом балансе. Например, промежуточный продукт цикла лимонной кислоты, α-кетоглутарат, может быть анаболически преобразован в глутамат аминокислот или глутамин, если они необходимы. Напомним, что человеческий организм способен синтезировать одиннадцать из двадцати аминокислот, входящих в состав белков. Все метаболические пути синтеза аминокислот ингибируются конкретной аминокислотой, которая является конечным продуктом данного пути. Таким образом, если в клетке достаточно глютамина, она отключает его синтез.
Напомним, что человеческий организм способен синтезировать одиннадцать из двадцати аминокислот, входящих в состав белков. Все метаболические пути синтеза аминокислот ингибируются конкретной аминокислотой, которая является конечным продуктом данного пути. Таким образом, если в клетке достаточно глютамина, она отключает его синтез.
Анаболические пути регулируются их конечными продуктами, но еще в большей степени энергетическим состоянием клетки. Когда энергии достаточно, более крупные молекулы, такие как белок, РНК и ДНК, будут строиться по мере необходимости. В качестве альтернативы, когда энергии недостаточно, белки и другие молекулы будут разрушаться и катаболизироваться для высвобождения энергии. Драматический пример этого наблюдается у детей с маразмом. Эти дети имеют серьезные нарушения функций организма, часто заканчивающиеся смертью от инфекции. Детям с маразмом не хватает калорий и белка, которые необходимы для выработки энергии и построения макромолекул. Отрицательно-энергетический баланс у детей с маразмом приводит к распаду мышечной ткани и тканей других органов в попытках организма выжить. Значительное уменьшение мышечной ткани делает детей с маразмом истощенными или «мышечно истощенными».
Значительное уменьшение мышечной ткани делает детей с маразмом истощенными или «мышечно истощенными».
Рисунок \(\PageIndex{2}\): Метаболический путь глюконеогенеза
В гораздо менее тяжелом примере у человека также наблюдается отрицательный энергетический баланс между приемами пищи. В это время уровень глюкозы в крови начинает падать. Чтобы восстановить уровень глюкозы в крови до нормального уровня, стимулируется анаболический путь, называемый глюконеогенезом. Глюконеогенез — это процесс образования молекул глюкозы из определенных аминокислот, происходящий главным образом в печени (рис. \(\PageIndex{2}\)). Печень экспортирует синтезированную глюкозу в кровь для использования другими тканями.
Аккумулятор энергии
Напротив, в состоянии «сытости» (когда уровень энергии высок) дополнительная энергия из питательных веществ будет храниться. Глюкоза может запасаться только в мышечной и печеночной тканях. В этих тканях он хранится в виде гликогена, высокоразветвленной макромолекулы, состоящей из тысяч мономеров глюкозы, соединенных химическими связями. Мономеры глюкозы соединяются вместе анаболическим путем, называемым гликогенезом. На каждую запасенную молекулу глюкозы расходуется одна молекула АТФ. Следовательно, для хранения энергии требуется энергия. Уровень гликогена быстро достигает своего физиологического предела, и когда это происходит, избыток глюкозы превращается в жир. Клетка с положительным энергетическим балансом обнаруживает высокую концентрацию АТФ, а также ацетил-КоА, вырабатываемых катаболическими путями. В ответ отключается катаболизм и включается синтез триглицеридов, происходящий анаболическим путем, называемым липогенезом. Новообразованные триглицериды транспортируются в жировые клетки, называемые адипоцитами. Жир является лучшей альтернативой гликогену для хранения энергии, поскольку он более компактен (на единицу энергии) и, в отличие от гликогена, организм не запасает воду вместе с жиром. Вода имеет значительный вес, и повышенные запасы гликогена, которые сопровождаются водой, резко увеличивают массу тела. Когда тело находится в положительном энергетическом балансе, избыток углеводов, липидов и белков метаболизируется в жир.
Мономеры глюкозы соединяются вместе анаболическим путем, называемым гликогенезом. На каждую запасенную молекулу глюкозы расходуется одна молекула АТФ. Следовательно, для хранения энергии требуется энергия. Уровень гликогена быстро достигает своего физиологического предела, и когда это происходит, избыток глюкозы превращается в жир. Клетка с положительным энергетическим балансом обнаруживает высокую концентрацию АТФ, а также ацетил-КоА, вырабатываемых катаболическими путями. В ответ отключается катаболизм и включается синтез триглицеридов, происходящий анаболическим путем, называемым липогенезом. Новообразованные триглицериды транспортируются в жировые клетки, называемые адипоцитами. Жир является лучшей альтернативой гликогену для хранения энергии, поскольку он более компактен (на единицу энергии) и, в отличие от гликогена, организм не запасает воду вместе с жиром. Вода имеет значительный вес, и повышенные запасы гликогена, которые сопровождаются водой, резко увеличивают массу тела. Когда тело находится в положительном энергетическом балансе, избыток углеводов, липидов и белков метаболизируется в жир.
Ключевые выводы
- Общими целями метаболизма являются передача энергии и транспорт веществ. Метаболизм определяется как сумма всех химических реакций, необходимых для поддержания клеточной функции, и подразделяется либо на катаболизм (относится ко всем метаболическим процессам, связанным с распадом молекул), либо к анаболизму (который включает все метаболические процессы, участвующие в построении более крупных молекул). Как правило, катаболические процессы высвобождают энергию, а анаболические процессы потребляют энергию.
- Метаболический путь представляет собой серию ферментативных стадий, которые превращают субстрат (исходный материал) в промежуточные продукты, которые являются субстратами для протекающих ферментативных реакций до тех пор, пока в результате последней ферментативной реакции в пути не будет синтезирован конечный продукт.
- Системам органов тела требуется топливо и строительные блоки для переваривания, поглощения, дыхания, перекачки крови, транспортировки питательных веществ и отходов, поддержания температуры тела и создания новых клеток среди множества других функций.

- Когда уровень энергии высок, клетки строят молекулы, а когда уровень энергии низкий, катаболические пути стимулируются для высвобождения энергии.
- Энергия, высвобождаемая катаболическими путями, приводит в действие анаболические пути в построении более крупных макромолекул.
- В «сытом» состоянии (когда уровень энергии высок) дополнительное питательное топливо будет храниться в виде гликогена или триглицеридов.
Начало обсуждения
- Обсудите практичность хранения энергии в ранних человеческих цивилизациях и последствия этих метаболических процессов в современном мире. Вернитесь к истории индейцев пима в главе 1 «Питание и вы» и к концепции «бережливого гена».
- Может ли человек с избыточным весом винить в своем избыточном весе более медленный обмен веществ?
4.1: Обзор метаболизма распространяется под лицензией CC BY-NC-SA 3.0 и был создан, изменен и/или курирован LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 3,0
- Показать оглавление
- нет
- Теги
Метаболическая энергия — Клетка
Многие задачи, которые должна выполнять клетка, такие как движение и синтез макромолекул, требуют энергии. Таким образом, большая часть клеточной активности посвящена получению энергии из окружающей среды и использованию этой энергии для запуска энергозатратных реакций. Хотя ферменты контролируют скорость практически всех химических реакций внутри клетки, ферментативный катализ не влияет на положение равновесия химических реакций. Законы термодинамики управляют химическими равновесиями и определяют энергетически выгодное направление всех химических реакций. Многие реакции, которые должны протекать внутри клеток, энергетически невыгодны и поэтому могут протекать только за счет дополнительных затрат энергии. Следовательно, клетки должны постоянно расходовать энергию, полученную из окружающей среды. Генерация и использование метаболической энергии, таким образом, являются фундаментальными для всей клеточной биологии.
Таким образом, большая часть клеточной активности посвящена получению энергии из окружающей среды и использованию этой энергии для запуска энергозатратных реакций. Хотя ферменты контролируют скорость практически всех химических реакций внутри клетки, ферментативный катализ не влияет на положение равновесия химических реакций. Законы термодинамики управляют химическими равновесиями и определяют энергетически выгодное направление всех химических реакций. Многие реакции, которые должны протекать внутри клеток, энергетически невыгодны и поэтому могут протекать только за счет дополнительных затрат энергии. Следовательно, клетки должны постоянно расходовать энергию, полученную из окружающей среды. Генерация и использование метаболической энергии, таким образом, являются фундаментальными для всей клеточной биологии.
Свободная энергия и АТФ
Энергетика биохимических реакций лучше всего описывается в терминах термодинамической функции, называемой свободной энергией Гиббса ( G ) , названной в честь Джозайи Уилларда Гиббса.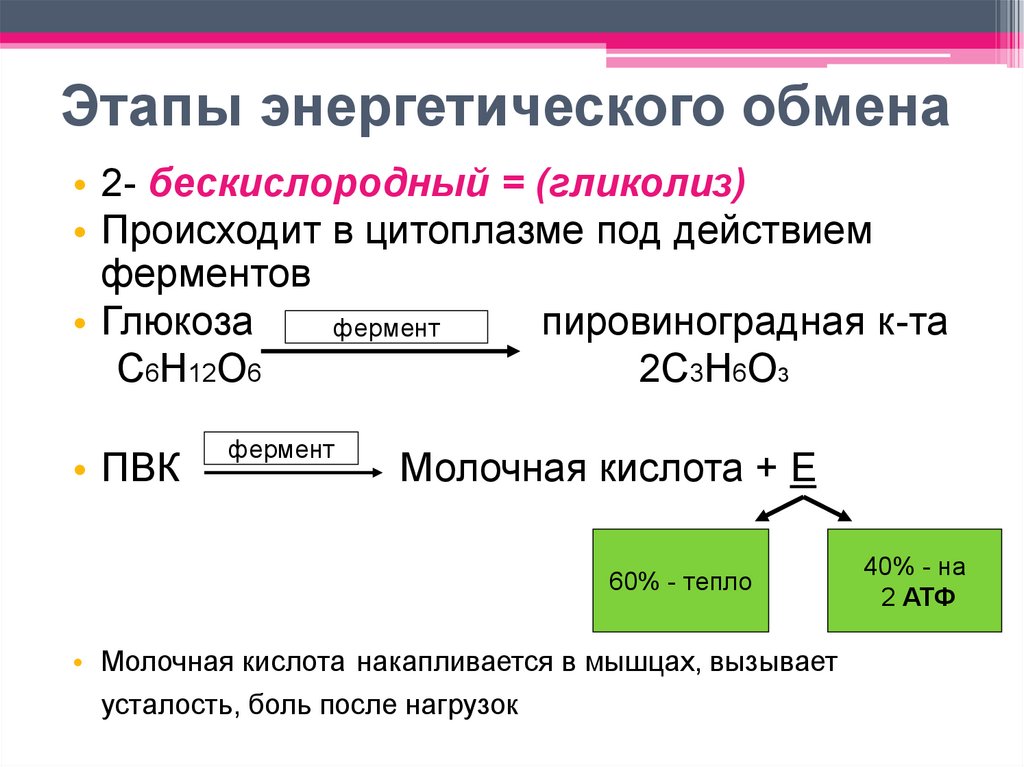 Изменение свободной энергии (Δ G ) реакции сочетает в себе эффекты изменений энтальпии (тепло, которое выделяется или поглощается во время химической реакции) и энтропии (степень беспорядка в результате реакции), чтобы предсказать, будет ли или реакция не является энергетически выгодной. Все химические реакции самопроизвольно протекают в энергетически выгодном направлении, сопровождаясь уменьшением свободной энергии (Δ Г < 0). Например, рассмотрим гипотетическую реакцию, в которой А превращается в В:
Изменение свободной энергии (Δ G ) реакции сочетает в себе эффекты изменений энтальпии (тепло, которое выделяется или поглощается во время химической реакции) и энтропии (степень беспорядка в результате реакции), чтобы предсказать, будет ли или реакция не является энергетически выгодной. Все химические реакции самопроизвольно протекают в энергетически выгодном направлении, сопровождаясь уменьшением свободной энергии (Δ Г < 0). Например, рассмотрим гипотетическую реакцию, в которой А превращается в В:
Если Δ G < 0, эта реакция будет протекать в прямом направлении, как написано. Однако если Δ G > 0, реакция пойдет в обратном направлении и В превратится в А.
Δ G реакции определяется не только внутренними свойствами реагентов и продуктов, но и также их концентрациями и другими условиями реакции (например, температурой). Таким образом, полезно определить изменение свободной энергии реакции в стандартных условиях. (Стандартные условия считаются 1- M концентрация всех реагентов и продуктов и давление 1 атм). Стандартное изменение свободной энергии (Δ G °) реакции напрямую связано с положением ее равновесия, поскольку фактическое Δ G является функцией как Δ G° , так и концентраций реагентов и продуктов. Например, рассмотрим реакцию
Стандартное изменение свободной энергии (Δ G °) реакции напрямую связано с положением ее равновесия, поскольку фактическое Δ G является функцией как Δ G° , так и концентраций реагентов и продуктов. Например, рассмотрим реакцию
. Изменение свободной энергии можно записать следующим образом:
, где R — газовая постоянная, а T — абсолютная температура.
В равновесии Δ G = 0 и реакция не протекает ни в одном направлении. Таким образом, константа равновесия реакции ( K = [B]/[A] в равновесии) напрямую связана с Δ G ° приведенным выше уравнением, которое можно выразить следующим образом:
или
. Если фактическое отношение [B]/[A] больше равновесного соотношения ( K ), Δ G > 0 и реакция протекает в обратном направлении (превращение B в A). С другой стороны, если отношение [B]/[A] меньше равновесного отношения, Δ G < 0, и A превращается в B.
Стандартное изменение свободной энергии (Δ G °) реакции, таким образом, определяет ее химическое равновесие и предсказывает, в каком направлении будет протекать реакция при любом заданном наборе условий. . Для биохимических реакций стандартное изменение свободной энергии обычно выражается как Δ G° ′, что представляет собой стандартное изменение свободной энергии реакции в водном растворе при pH = 7, что примерно соответствует условиям внутри клетки.
. Для биохимических реакций стандартное изменение свободной энергии обычно выражается как Δ G° ′, что представляет собой стандартное изменение свободной энергии реакции в водном растворе при pH = 7, что примерно соответствует условиям внутри клетки.
Многие биологические реакции (например, синтез макромолекул) термодинамически неблагоприятны (Δ G > 0) в клеточных условиях. Для протекания таких реакций требуется дополнительный источник энергии. Например, рассмотрим реакцию
Превращение А в В энергетически невыгодно, поэтому реакция протекает в обратном, а не прямом направлении. Однако реакцию можно запустить в прямом направлении, соединив превращение А в В с энергетически выгодной реакцией, такой как:
Если эти две реакции объединить, то сопряженная реакция может быть записана следующим образом:
Δ G объединенной реакции представляет собой сумму изменений свободной энергии ее отдельных компонентов, поэтому сопряженная реакция энергетически выгодна. и будет действовать как написано. Таким образом, энергетически невыгодное превращение А в В обусловлено его присоединением ко второй реакции, связанной с большим уменьшением свободной энергии. Ферменты отвечают за проведение таких связанных реакций скоординированным образом.
и будет действовать как написано. Таким образом, энергетически невыгодное превращение А в В обусловлено его присоединением ко второй реакции, связанной с большим уменьшением свободной энергии. Ферменты отвечают за проведение таких связанных реакций скоординированным образом.
Клетка использует этот основной механизм для управления многими энергетически неблагоприятными реакциями, которые должны происходить в биологических системах. Аденозин-5′-трифосфат (АТФ) играет центральную роль в этом процессе, выступая в качестве хранилища свободной энергии внутри клетки (). Связи между фосфатами в АТФ известны как высокоэнергетические связи, поскольку их гидролиз сопровождается относительно большим уменьшением свободной энергии. В самих химических связях нет ничего особенного; их называют высокоэнергетическими связями только потому, что при их гидролизе внутри клетки высвобождается большое количество свободной энергии. При гидролизе АТФ до АДФ плюс фосфат (P i ), Δ G °′= -7,3 ккал/моль. Напомним, однако, что Δ G °′ относится к «стандартным условиям», в которых концентрации всех продуктов и реагентов составляют 1 M . Фактические внутриклеточные концентрации P i составляют примерно 10 -2 M, , а внутриклеточные концентрации АТФ выше, чем АДФ. Эти различия между внутриклеточными концентрациями и концентрациями в стандартном состоянии благоприятствуют гидролизу АТФ, поэтому для гидролиза АТФ внутри клетки Δ G составляет примерно -12 ккал/моль.
Напомним, однако, что Δ G °′ относится к «стандартным условиям», в которых концентрации всех продуктов и реагентов составляют 1 M . Фактические внутриклеточные концентрации P i составляют примерно 10 -2 M, , а внутриклеточные концентрации АТФ выше, чем АДФ. Эти различия между внутриклеточными концентрациями и концентрациями в стандартном состоянии благоприятствуют гидролизу АТФ, поэтому для гидролиза АТФ внутри клетки Δ G составляет примерно -12 ккал/моль.
Рисунок 2.31
АТФ как хранилище свободной энергии. Связи между фосфатными группами АТФ называются высокоэнергетическими связями, поскольку их гидролиз приводит к значительному уменьшению свободной энергии. АТФ может гидролизоваться либо до АДФ плюс фосфатная группа (HPO 4 2-), либо до АМФ (подробнее…)
В качестве альтернативы АТФ может гидролизоваться до АМФ плюс пирофосфат (PP i ) . Эта реакция дает примерно такое же количество свободной энергии, как гидролиз АТФ в АДФ. Однако пирофосфат, полученный в результате этой реакции, затем сам быстро гидролизуется с Δ G аналогичен гидролизу АТФ. Таким образом, общее изменение свободной энергии в результате гидролиза АТФ в АМФ примерно в два раза больше, чем при гидролизе АТФ в АДФ. Для сравнения, связь между сахаром и фосфатной группой AMP не обладает высокой энергией, а типична для ковалентных связей; для гидролиза АМП Δ G °′= -3,3 ккал/моль.
Однако пирофосфат, полученный в результате этой реакции, затем сам быстро гидролизуется с Δ G аналогичен гидролизу АТФ. Таким образом, общее изменение свободной энергии в результате гидролиза АТФ в АМФ примерно в два раза больше, чем при гидролизе АТФ в АДФ. Для сравнения, связь между сахаром и фосфатной группой AMP не обладает высокой энергией, а типична для ковалентных связей; для гидролиза АМП Δ G °′= -3,3 ккал/моль.
Из-за сопутствующего снижения свободной энергии гидролиз АТФ можно использовать для запуска других энергозатратных реакций внутри клетки. Например, первой реакцией гликолиза (обсуждаемой в следующем разделе) является превращение глюкозы в глюкозо-6-фосфат. Реакцию можно записать следующим образом:
Поскольку эта реакция энергетически невыгодна, как написано (Δ G °′= +3,3 ккал/моль), она должна идти в прямом направлении за счет гидролиза АТФ (Δ G °′= -7,3 ккал/моль). /моль):
Комбинированная реакция может быть записана следующим образом:
Изменение свободной энергии для этой реакции представляет собой сумму изменений свободной энергии для отдельных реакций, поэтому для сопряженной реакции Δ G °′ = -4,0 ккал/моль, что способствует образованию глюкозо-6-фосфата.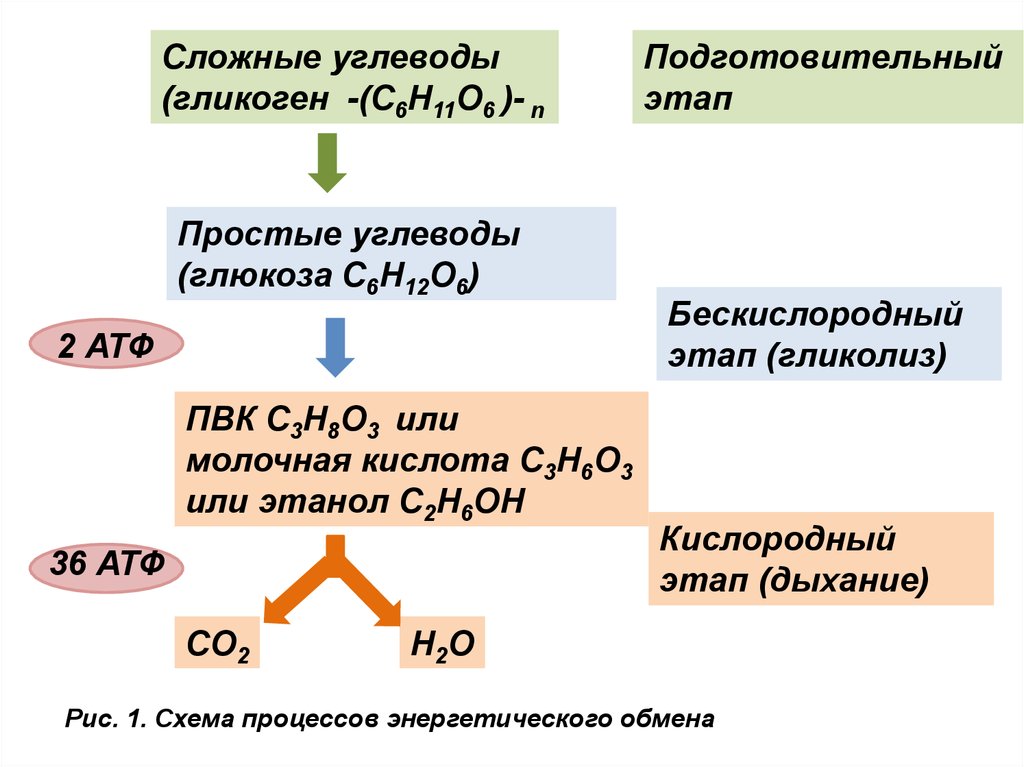
Другие молекулы, в том числе другие нуклеозидтрифосфаты (например, GTP), также имеют высокоэнергетические связи и могут использоваться в качестве АТФ для запуска энергозатратных реакций. Однако для большинства реакций АТФ обеспечивает свободную энергию. Таким образом, реакции с выделением энергии внутри клетки связаны с синтезом АТФ, тогда как реакции, требующие энергии, связаны с гидролизом АТФ. Таким образом, высокоэнергетические связи АТФ играют центральную роль в клеточном метаболизме, выступая в качестве полезной формы хранения свободной энергии.
Генерация АТФ из глюкозы
Расщепление углеводов, особенно глюкозы, является основным источником клеточной энергии. Полный окислительный распад глюкозы до CO 2 и H 2 O можно записать следующим образом:
Реакция дает большое количество свободной энергии: Δ G °′= -686 ккал/моль. Чтобы использовать эту свободную энергию в пригодной для использования форме, глюкоза окисляется внутри клеток в несколько этапов, связанных с синтезом АТФ.
Гликолиз, начальная стадия распада глюкозы, характерен практически для всех клеток. Гликолиз происходит в отсутствие кислорода и может обеспечить всю метаболическую энергию анаэробных организмов. Однако в аэробных клетках гликолиз является лишь первой стадией деградации глюкозы.
Реакции гликолиза приводят к расщеплению глюкозы до пирувата с чистым приростом двух молекул АТФ (). Начальные реакции в пути фактически потребляют энергию, используя АТФ для фосфорилирования глюкозы до глюкозо-6-фосфата, а затем фруктозо-6-фосфата до фруктозо-1,6-бисфосфата. Ферменты, катализирующие эти две реакции, — гексокиназа и фосфофруктокиназа соответственно — являются важными регуляторными точками гликолитического пути. Ключевым элементом контроля является фосфофруктокиназа, которая ингибируется высоким уровнем АТФ. Ингибирование фосфофруктокиназы приводит к накоплению глюкозо-6-фосфата, который, в свою очередь, ингибирует гексокиназу. Таким образом, когда клетка имеет достаточный запас метаболической энергии в виде АТФ, расщепление глюкозы подавляется.
Рисунок 2.32
Реакции гликолиза. Глюкоза расщепляется до пирувата с образованием двух молекул АТФ и НАДН. В анаэробных условиях НАДН повторно окисляется путем превращения пирувата в этанол или лактат. В аэробных условиях (подробнее…)
Реакции, следующие за образованием фруктозо-1,6-бисфосфата, составляют часть гликолитического пути, производящую энергию. Расщепление фруктозо-1,6-бисфосфата дает две молекулы трехуглеродного сахара глицеральдегид-3-фосфата, который окисляется до 1,3-бисфосфоглицерата. Фосфатная группа этого соединения имеет очень высокую свободную энергию гидролиза (Δ G °′= -11,5 ккал/моль), поэтому он используется в следующей реакции гликолиза для запуска синтеза АТФ из АДФ. Продукт этой реакции, 3-фосфоглицерат, затем превращается в фосфоенолпируват, второй высокоэнергетический промежуточный продукт гликолиза. При гидролизе высокоэнергетического фосфата фосфоенолпирувата Δ G °′ = -14,6 ккал/моль его превращение в пируват сопряжено с синтезом АТФ.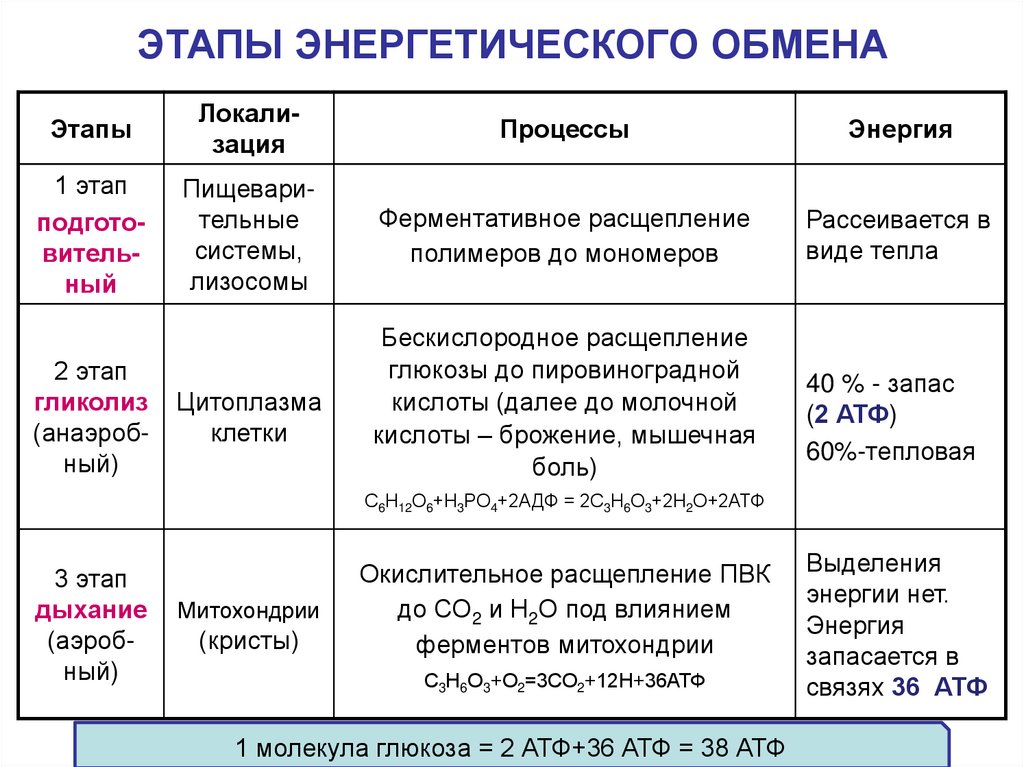 Таким образом, каждая молекула глицеральдегид-3-фосфата, превращенная в пируват, связана с образованием двух молекул АТФ; всего из каждой исходной молекулы глюкозы синтезируется четыре АТФ. Поскольку для инициации начальных реакций требовалось две АТФ, чистый выигрыш от гликолиза составляет две молекулы АТФ.
Таким образом, каждая молекула глицеральдегид-3-фосфата, превращенная в пируват, связана с образованием двух молекул АТФ; всего из каждой исходной молекулы глюкозы синтезируется четыре АТФ. Поскольку для инициации начальных реакций требовалось две АТФ, чистый выигрыш от гликолиза составляет две молекулы АТФ.
Помимо производства АТФ, гликолиз превращает две молекулы кофермента НАД + в НАДН. В этой реакции NAD + действует как окислитель, который принимает электроны от глицеральдегид-3-фосфата. НАДН, образующийся в виде продукта, должен быть рециркулирован, выступая в качестве донора электронов для других окислительно-восстановительных реакций внутри клетки. В анаэробных условиях НАДН, образующийся при гликолизе, реокисляется до НАД + путем превращения пирувата в лактат или этанол. Однако в аэробных организмах NADH служит дополнительным источником энергии, отдавая свои электроны в цепь переноса электронов, где они в конечном итоге используются для восстановления O 2 до H 2 O в сочетании с образованием дополнительного АТФ.
В эукариотических клетках гликолиз происходит в цитозоле. Затем пируват транспортируется в митохондрии, где его полное окисление до CO 2 и H 2 O дает большую часть АТФ, образующегося при распаде глюкозы. Следующим этапом метаболизма пирувата является его окислительное декарбоксилирование в присутствии кофермента А (КоА) , служащего переносчиком ацильных групп в различных метаболических реакциях (). Один углерод пирувата выделяется в виде CO 2 , а оставшиеся два атома углерода присоединяются к КоА с образованием ацетил-КоА. При этом одна молекула НАД + восстанавливается до НАДН.
Рисунок 2.33
Окислительное декарбоксилирование пирувата. Пируват превращается в CO 2 и ацетил-КоА, при этом образуется одна молекула НАДН. Коэнзим А (КоА-SH) является основным переносчиком активированных ацильных групп в различных реакциях.
Ацетил-КоА, образующийся в результате этой реакции, вступает в цикл лимонной кислоты или цикл Кребса (), который является центральным путем окислительного метаболизма.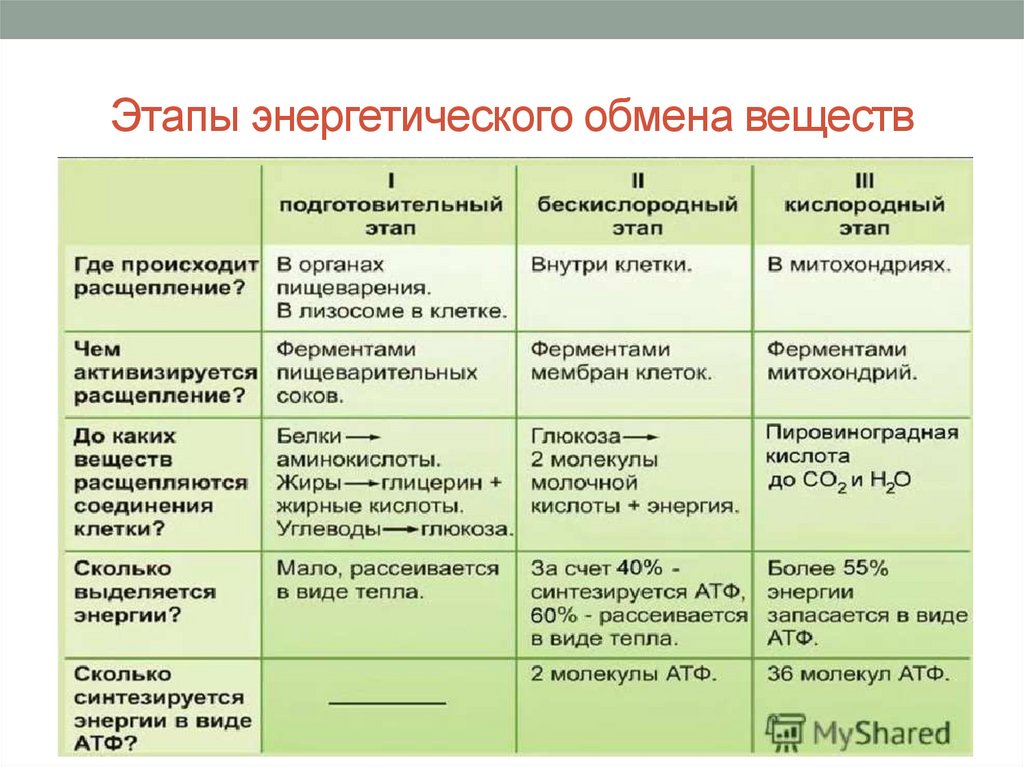 Двухуглеродная ацетильная группа объединяется с оксалоацетатом (четыре атома углерода) с образованием цитрата (шесть атомов углерода). Через восемь дальнейших реакций два атома углерода цитрата полностью окисляются до CO 2 и регенерируют оксалоацетат. Во время цикла в ГТФ образуется одна высокоэнергетическая фосфатная связь, которая используется непосредственно для запуска синтеза одной молекулы АТФ. Кроме того, каждый оборот цикла дает три молекулы НАДН и одну молекулу восстановленного флавинадениндинуклеотида ( ФАДН 2 ), который является еще одним переносчиком электронов в окислительно-восстановительных реакциях.
Двухуглеродная ацетильная группа объединяется с оксалоацетатом (четыре атома углерода) с образованием цитрата (шесть атомов углерода). Через восемь дальнейших реакций два атома углерода цитрата полностью окисляются до CO 2 и регенерируют оксалоацетат. Во время цикла в ГТФ образуется одна высокоэнергетическая фосфатная связь, которая используется непосредственно для запуска синтеза одной молекулы АТФ. Кроме того, каждый оборот цикла дает три молекулы НАДН и одну молекулу восстановленного флавинадениндинуклеотида ( ФАДН 2 ), который является еще одним переносчиком электронов в окислительно-восстановительных реакциях.
Рисунок 2.34
Цикл лимонной кислоты. Двухуглеродная ацетильная группа переносится от ацетил-КоА к оксалоацетату с образованием цитрата. Затем два атома углерода цитрата окисляются до CO 2 и регенерируют оксалоацетат. Каждый оборот цикла дает одну молекулу ГТФ, три (подробнее…)
Цикл лимонной кислоты завершает окисление глюкозы до шести молекул СО 2 .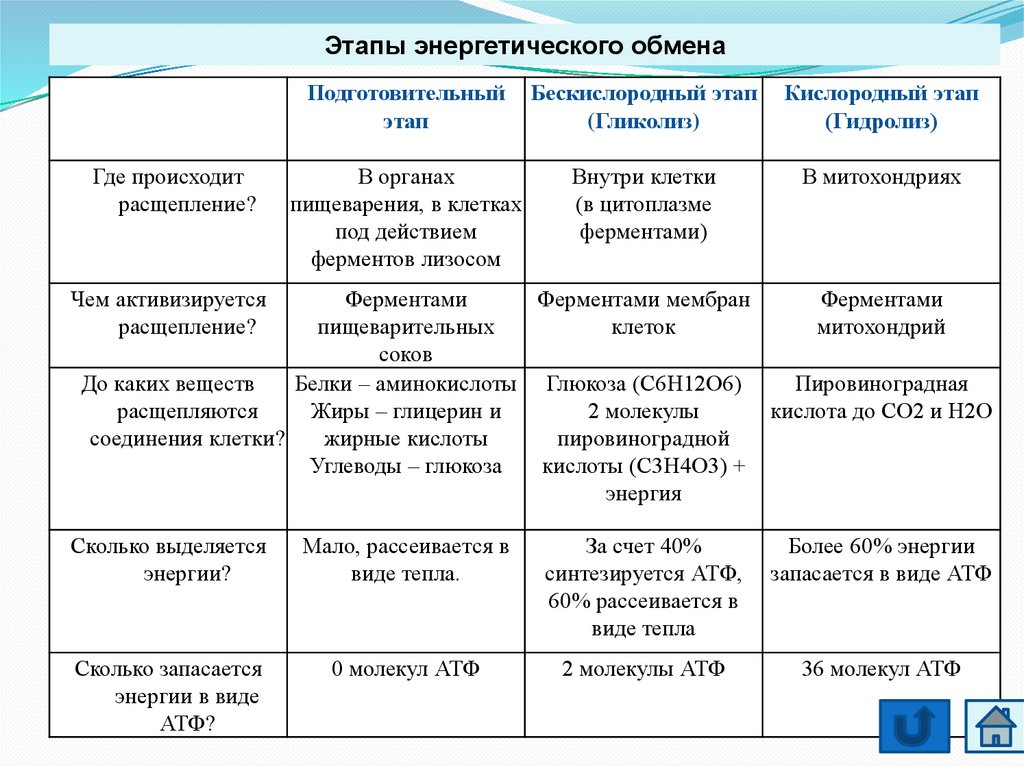 Непосредственно из каждой молекулы глюкозы получается четыре молекулы АТФ — две из гликолиза и две из цикла лимонной кислоты (по одной на каждую молекулу пирувата). Кроме того, десять молекул НАДН (две от гликолиза, две от превращения пирувата в ацетил-КоА и шесть от цикла лимонной кислоты) и две молекулы ФАДН 2 формируются. Оставшаяся энергия, полученная при расщеплении глюкозы, поступает от повторного окисления НАДН и ФАДН 2 , при этом их электроны передаются по цепи переноса электронов, чтобы (в конечном итоге) восстановить O 2 до H 2 O.
Непосредственно из каждой молекулы глюкозы получается четыре молекулы АТФ — две из гликолиза и две из цикла лимонной кислоты (по одной на каждую молекулу пирувата). Кроме того, десять молекул НАДН (две от гликолиза, две от превращения пирувата в ацетил-КоА и шесть от цикла лимонной кислоты) и две молекулы ФАДН 2 формируются. Оставшаяся энергия, полученная при расщеплении глюкозы, поступает от повторного окисления НАДН и ФАДН 2 , при этом их электроны передаются по цепи переноса электронов, чтобы (в конечном итоге) восстановить O 2 до H 2 O.
Во время окислительного фосфорилирования электроны НАДН и ФАДН 2 объединяются с О 2 , а энергия, высвобождаемая в процессе, управляет синтезом АТФ из АДФ. Перенос электронов от НАДН к О 2 высвобождает большое количество свободной энергии: Δ G °′= -52,5 ккал/моль на каждую пару переданных электронов. Чтобы эту энергию можно было собрать в пригодной для использования форме, процесс происходит постепенно путем прохождения электронов через ряд носителей, которые составляют цепь переноса электронов ().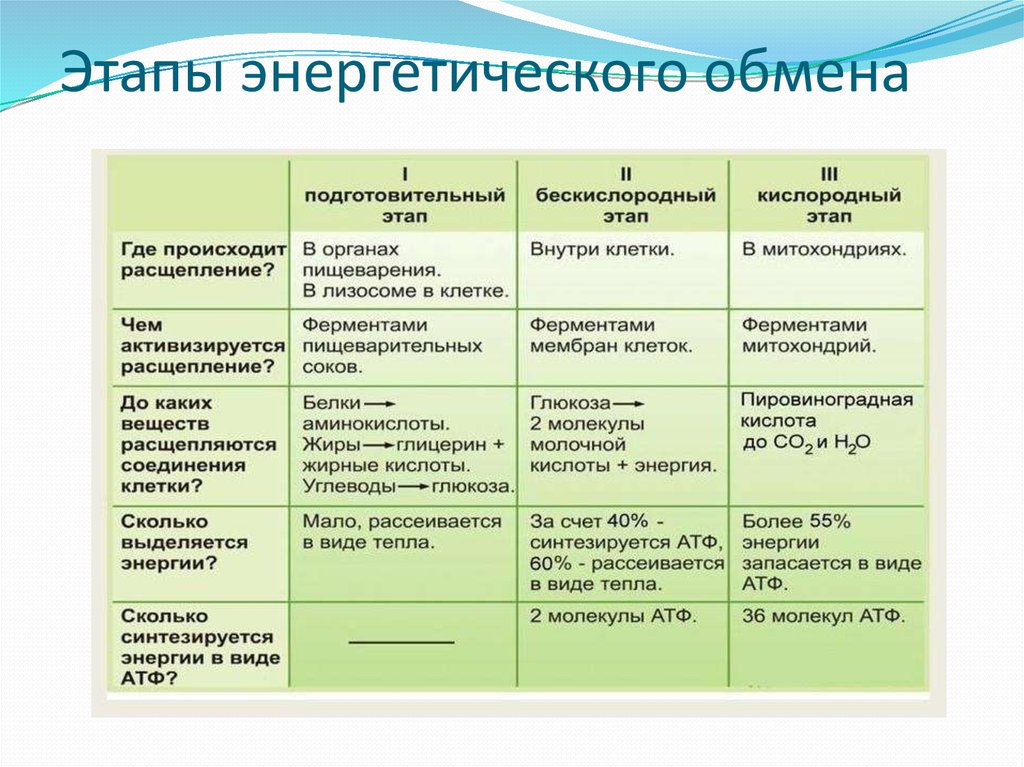 Компоненты электрон-транспортной цепи расположены во внутренней митохондриальной мембране эукариотических клеток, а окислительное фосфорилирование более подробно рассматривается при обсуждении митохондрий в главе 10. У аэробных бактерий, которые используют сопоставимую систему, компоненты электрон-транспортной цепи расположены в плазматической мембране. В любом случае перенос электронов от NADH к O 2 дает достаточно энергии для синтеза примерно трех молекул АТФ. Электроны от FADH 2 входят в электронтранспортную цепь на более низком энергетическом уровне, поэтому их переход к O 2 дает меньше полезной свободной энергии, всего две молекулы АТФ.
Компоненты электрон-транспортной цепи расположены во внутренней митохондриальной мембране эукариотических клеток, а окислительное фосфорилирование более подробно рассматривается при обсуждении митохондрий в главе 10. У аэробных бактерий, которые используют сопоставимую систему, компоненты электрон-транспортной цепи расположены в плазматической мембране. В любом случае перенос электронов от NADH к O 2 дает достаточно энергии для синтеза примерно трех молекул АТФ. Электроны от FADH 2 входят в электронтранспортную цепь на более низком энергетическом уровне, поэтому их переход к O 2 дает меньше полезной свободной энергии, всего две молекулы АТФ.
Рисунок 2.35
Цепь переноса электронов. Электроны от НАДН и ФАДН 2 переносятся на О 2 через ряд переносчиков, организованных в четыре белковых комплекса в митохондриальной мембране. Свободная энергия, полученная в результате реакций переноса электронов в комплексах (подробнее.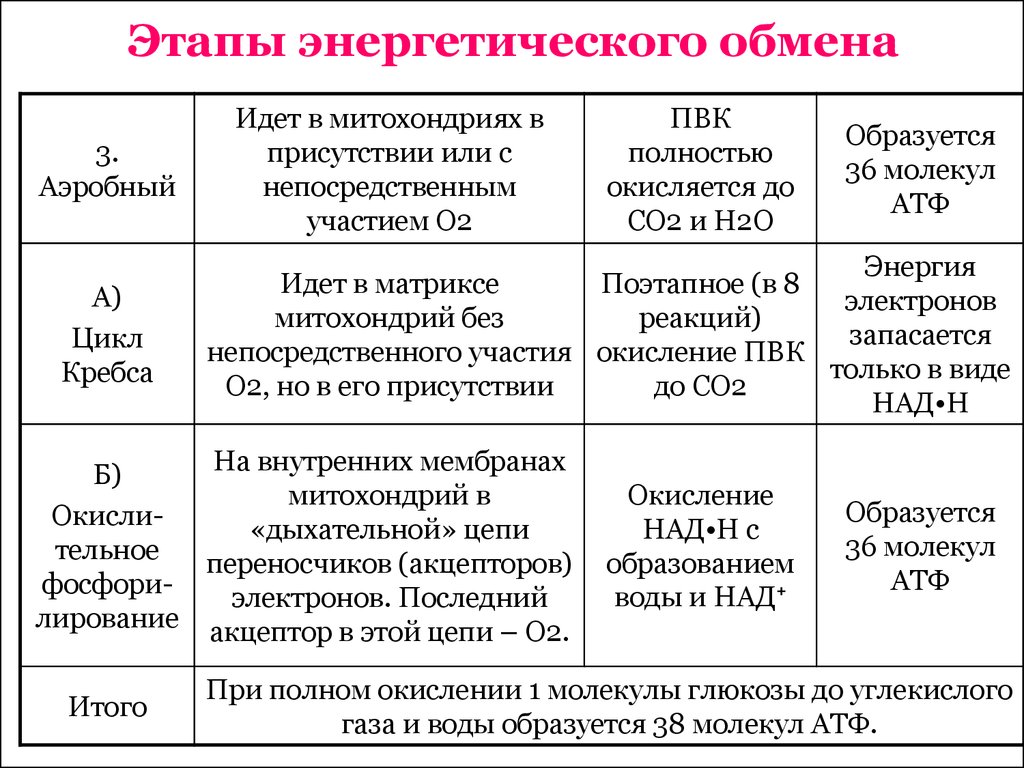 ..)
..)
Теперь можно рассчитать общий выход АТФ при окислении глюкозы. Чистая выгода от гликолиза составляет две молекулы АТФ и две молекулы НАДН. Превращение пирувата в ацетил-КоА и его метаболизм в цикле лимонной кислоты дает две дополнительные молекулы АТФ, восемь молекул НАДН и две молекулы ФАДН 2 . Если предположить, что три молекулы АТФ образуются в результате окисления каждой НАДН и две из каждой ФАДН 2 , общий выход составляет 38 молекул АТФ на молекулу глюкозы. Однако в некоторых клетках этот выход ниже, потому что две молекулы НАДН, образующиеся в результате гликолиза в цитозоле, не могут напрямую проникать в митохондрии. Вместо этого их электроны должны быть перенесены в митохондрию через челночную систему. В зависимости от используемой системы этот перенос может привести к попаданию этих электронов в электрон-транспортную цепь на уровне FADH 9.0134 2 . В таких случаях две молекулы НАДН, полученные в результате гликолиза, дают две, а не три молекулы АТФ, что снижает общий выход до 36, а не 38 АТФ на молекулу глюкозы.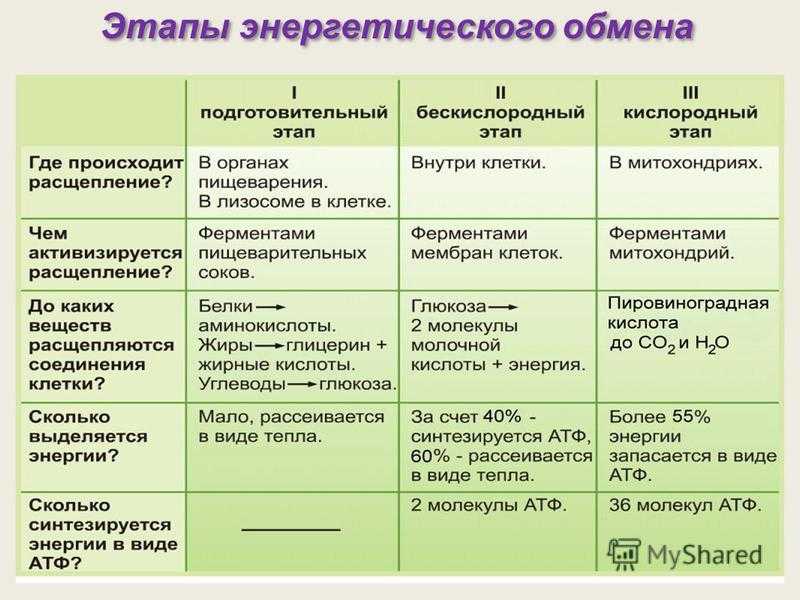
Получение энергии из других органических молекул
Энергия в форме АТФ может быть получена в результате распада других органических молекул, при этом центральную роль снова играют пути, участвующие в деградации глюкозы. Нуклеотиды, например, могут расщепляться до сахаров, которые затем вступают в гликолитический путь, а аминокислоты расщепляются посредством цикла лимонной кислоты. Две основные формы хранения энергии в клетках, полисахариды и липиды, также могут расщепляться с образованием АТФ. Полисахариды расщепляются на свободные сахара, которые затем метаболизируются, как обсуждалось в предыдущем разделе. Однако липиды представляют собой еще более эффективную молекулу для накопления энергии. Поскольку липиды более восстановлены, чем углеводы, и состоят в основном из углеводородных цепей, их окисление дает значительно больше энергии на массу исходного материала.
Жиры (триацилглицеролы) являются основной формой хранения липидов. Первым шагом в их утилизации является их расщепление до глицерина и свободных жирных кислот. Каждая жирная кислота присоединяется к коферменту А, образуя жирный ацил-КоА за счет одной молекулы АТФ (10). Затем жирные кислоты расщепляются в ступенчатом окислительном процессе, по два атома углерода за раз, давая ацетил-КоА плюс жирный ацил-КоА, более короткий на одну двухуглеродную единицу. Каждый цикл окисления также дает одну молекулу НАДН и одну молекулу ФАДН 9.0134 2 . Затем ацетил-КоА входит в цикл лимонной кислоты, и расщепление остатка жирной кислоты продолжается таким же образом.
Каждая жирная кислота присоединяется к коферменту А, образуя жирный ацил-КоА за счет одной молекулы АТФ (10). Затем жирные кислоты расщепляются в ступенчатом окислительном процессе, по два атома углерода за раз, давая ацетил-КоА плюс жирный ацил-КоА, более короткий на одну двухуглеродную единицу. Каждый цикл окисления также дает одну молекулу НАДН и одну молекулу ФАДН 9.0134 2 . Затем ацетил-КоА входит в цикл лимонной кислоты, и расщепление остатка жирной кислоты продолжается таким же образом.
Рисунок 2.36
Окисление жирных кислот. Жирная кислота (например, пальмитат насыщенной 16-углеродной жирной кислоты) первоначально присоединяется к коферменту А за счет одной молекулы АТФ. Затем окисление жирной кислоты происходит путем поэтапного удаления двухуглеродных единиц в виде ацетила (подробнее…)
Таким образом, расщепление 16-углеродной жирной кислоты дает семь молекул НАДН, семь молекул ФАДН 2 и восемь ацетил-КоА. С точки зрения образования АТФ этот выход соответствует 21 молекуле АТФ, полученной из НАДН (3 × 7), 14 молекул АТФ из ФАДН 2 (2 × 7) и 96 из ацетил-КоА (8 × 12).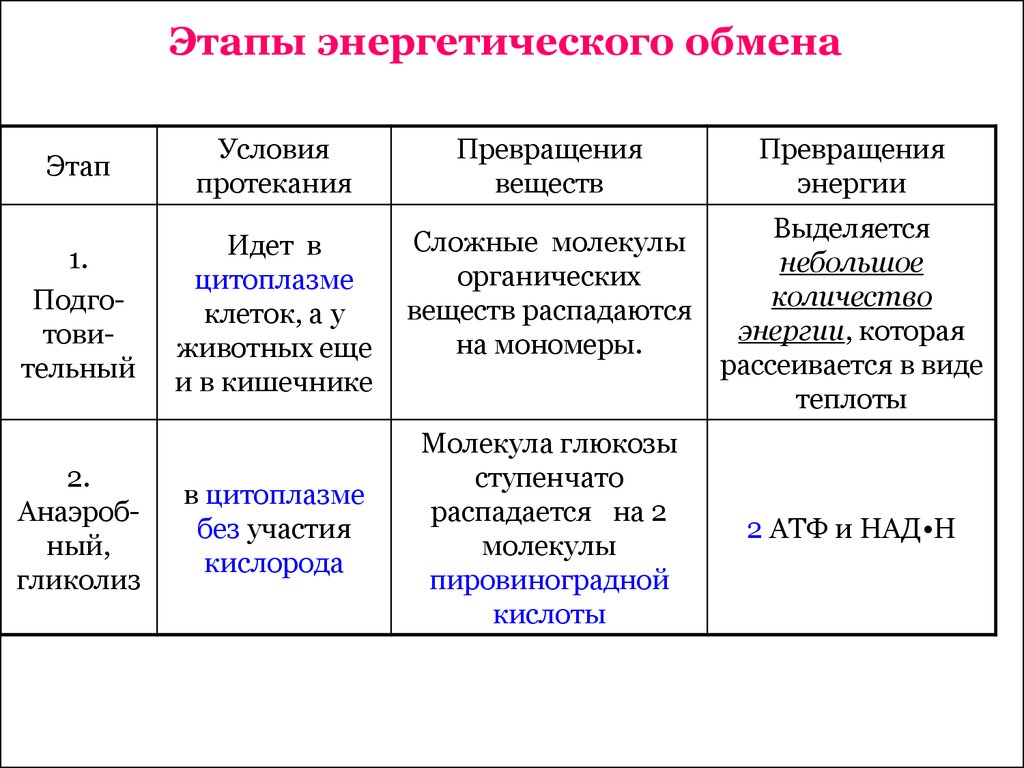 Поскольку для запуска процесса использовалась одна АТФ, чистый прирост составляет 130 АТФ на молекулу 16-углеродной жирной кислоты. Сравните этот выход с чистым приростом 38 АТФ на молекулу глюкозы. Поскольку молекулярная масса насыщенной 16-углеродной жирной кислоты равна 256, а молекулярная масса глюкозы — 180, выход АТФ примерно в 2,5 раза выше на грамм жирной кислоты — отсюда преимущество липидов перед полисахаридами в качестве молекул-аккумуляторов энергии.
Поскольку для запуска процесса использовалась одна АТФ, чистый прирост составляет 130 АТФ на молекулу 16-углеродной жирной кислоты. Сравните этот выход с чистым приростом 38 АТФ на молекулу глюкозы. Поскольку молекулярная масса насыщенной 16-углеродной жирной кислоты равна 256, а молекулярная масса глюкозы — 180, выход АТФ примерно в 2,5 раза выше на грамм жирной кислоты — отсюда преимущество липидов перед полисахаридами в качестве молекул-аккумуляторов энергии.
Фотосинтез
Производство энергии в результате окисления углеводов и липидов основано на разложении предварительно образованных органических соединений. Энергия, необходимая для синтеза этих соединений, в конечном итоге получается из солнечного света, который собирается и используется растениями и фотосинтезирующими бактериями для запуска синтеза углеводов. Преобразуя энергию солнечного света в полезную форму химической энергии, фотосинтез является источником практически всей метаболической энергии в биологических системах.
Общее уравнение фотосинтеза можно записать следующим образом:
Однако этот процесс намного сложнее и проходит в две отдельные стадии. В первом, называемом световыми реакциями, энергия, поглощаемая солнечным светом, приводит к синтезу АТФ и НАДФН (кофермента, сходного с НАДН), сопряженному с окислением H 2 O в O 2 . АТФ и НАДФН, образующиеся в результате световых реакций, управляют синтезом углеводов из CO 2 и H 2 9.0135 O во втором наборе реакций, называемых темновыми реакциями , потому что они не требуют солнечного света. В эукариотических клетках как световые, так и темновые реакции протекают в хлоропластах.
Фотосинтетические пигменты улавливают энергию солнечного света, поглощая фотоны. Поглощение света этими пигментами заставляет электрон перемещаться со своей нормальной молекулярной орбитали на орбиту с более высокой энергией, таким образом преобразуя энергию солнечного света в химическую энергию. В растениях наиболее распространенными фотосинтетическими пигментами являются хлорофиллы (), которые вместе поглощают видимый свет всех длин волн, кроме зеленого. Дополнительные пигменты поглощают свет с другими длинами волн, поэтому практически весь спектр видимого света может быть захвачен и использован для фотосинтеза.
В растениях наиболее распространенными фотосинтетическими пигментами являются хлорофиллы (), которые вместе поглощают видимый свет всех длин волн, кроме зеленого. Дополнительные пигменты поглощают свет с другими длинами волн, поэтому практически весь спектр видимого света может быть захвачен и использован для фотосинтеза.
Рисунок 2.37
Строение хлорофилла. Хлорофиллы состоят из порфириновых кольцевых структур, связанных с углеводородными хвостами. Хлорофиллы а и b отличаются одной функциональной группой в порфириновом кольце.
Энергия, полученная при поглощении света, используется для преобразования H 2 O в O 2 (). Высокоэнергетические электроны, полученные в результате этого процесса, затем попадают в цепь переноса электронов, в которой их перенос через ряд переносчиков связан с синтезом АТФ. Кроме того, эти высокоэнергетические электроны восстанавливают НАДФ + в НАДФН.
Рис. 2.38
Световые реакции фотосинтеза. Энергия солнечного света используется для разделения H 2 O на O 2 . Высокоэнергетические электроны, полученные в результате этого процесса, затем транспортируются через ряд носителей и используются для преобразования НАДФ + в НАДФН. Энергия, полученная из электрона (подробнее…)
Энергия солнечного света используется для разделения H 2 O на O 2 . Высокоэнергетические электроны, полученные в результате этого процесса, затем транспортируются через ряд носителей и используются для преобразования НАДФ + в НАДФН. Энергия, полученная из электрона (подробнее…)
В реакциях в темноте АТФ и НАДФН, образующиеся в реакциях со светом, управляют синтезом углеводов из CO 2 и H 2 O. Одна молекула CO 2 за раз добавляется в цикл реакций, известный как цикл Кальвина в честь его первооткрывателя Мелвина Кальвина, который приводит к образованию углеводов (). В целом цикл Кальвина потребляет 18 молекул АТФ и 12 молекул НАДФН на каждую синтезированную молекулу глюкозы. Для превращения каждой молекулы НАДФ + в НАДФН необходимо два электрона, поэтому 24 электрона должны пройти через цепь переноса электронов, чтобы образовать достаточное количество НАДФН для синтеза одной молекулы глюкозы.




Leave A Comment