АТФ — аденозинтрифосфорная кислота.
Тема: АТФ – аденозинтрифосфорная кислота
Цель: познакомиться с особенностями строения и функциями АТФ.
Изучение нового материала
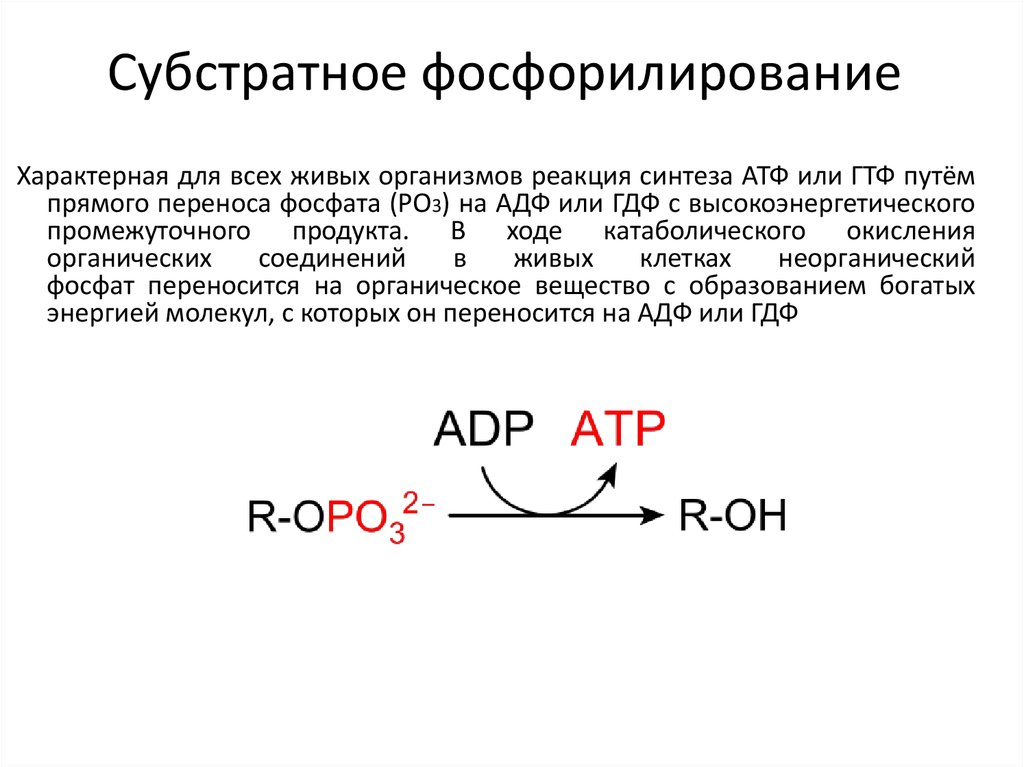
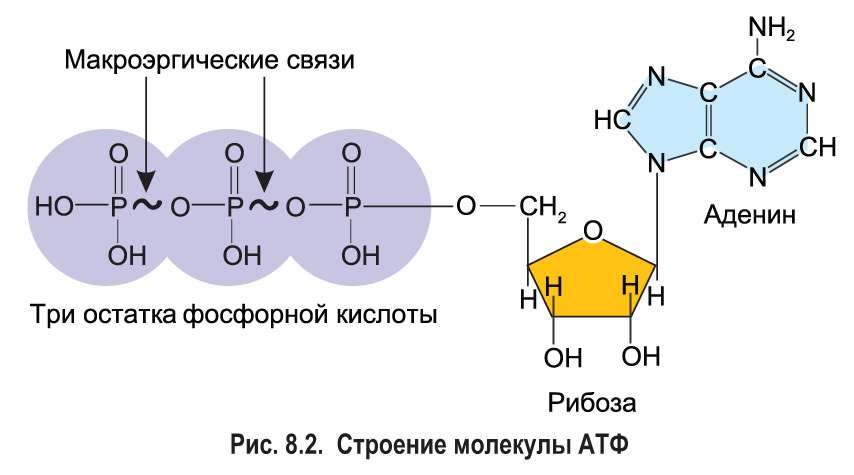
АТФ (аденозинтрифосфорная кислота) – сложное органическое соединение, содержащее две макроэргические (богатые энергией) связи.
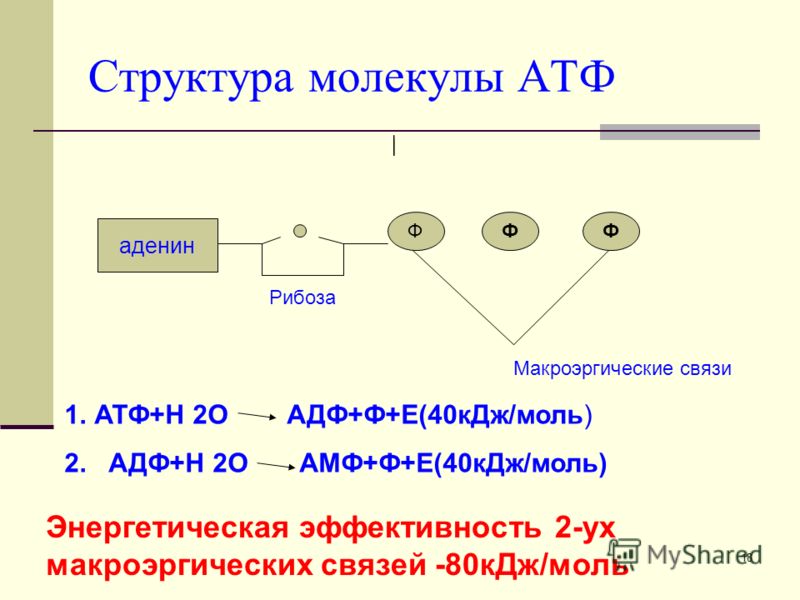
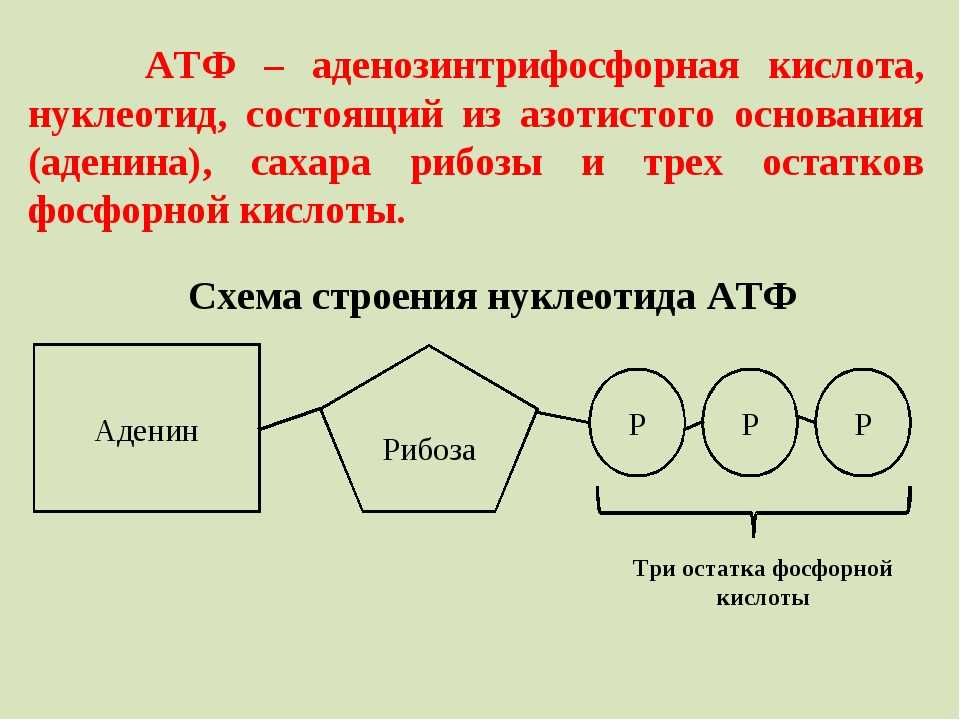
Представлена одним нуклеотидом, состоящим из азотистого основания аденина, углевода рибозы (пентоза) и (в отличие от нуклеотидов ДНК и РНК) трех остатков фосфорной кислоты.
При отделении одного остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту), если отделяется еще один остаток фосфорной кислоты, то АДФ переходит в АМФ (аденозинмонофосфорную кислоту), что бывает крайне редко.
АТФ→АДФ+Ф+Е
АДФ→АМФ+Ф+Е
Место отделившегося остатка фосфорной кислоты занимает молекула воды.
Отделение каждого остатка фосфорной кислоты происходит с помощью ферментов, при этом выделяется 40 кДж (а при разрыве обычных ковалентных связей – около 12 кДж) энергии. Именно поэтому эти связи называют макроэргическими. В молекуле АТФ две макроэргические связи.
При синтезе АТФ, наоборот, поглощается большое количество энергии. У всех организмов АТФ синтезируется на внутренней мембране митохондрий в процессе кислородного (III) этапа диссимиляции (катаболизма), поэтому их называют энергетическими станциями клетки.
Молекулы АТФ, покидая митохондрии, попадают в гиалоплазму, участвуют в различных процессах жизнедеятельности клетки и возвращаются в виде АДФ и Ф.
У зеленых растений, кроме митохондрий, АТФ синтезируется в хлоропластах в процессе световой стадии фотосинтеза (фотофосформирование).
Во всех клетках АТФ аккумулирует энергию, которая расходуется по мере надобности там, где в клетке происходят процессы с затратой энергии.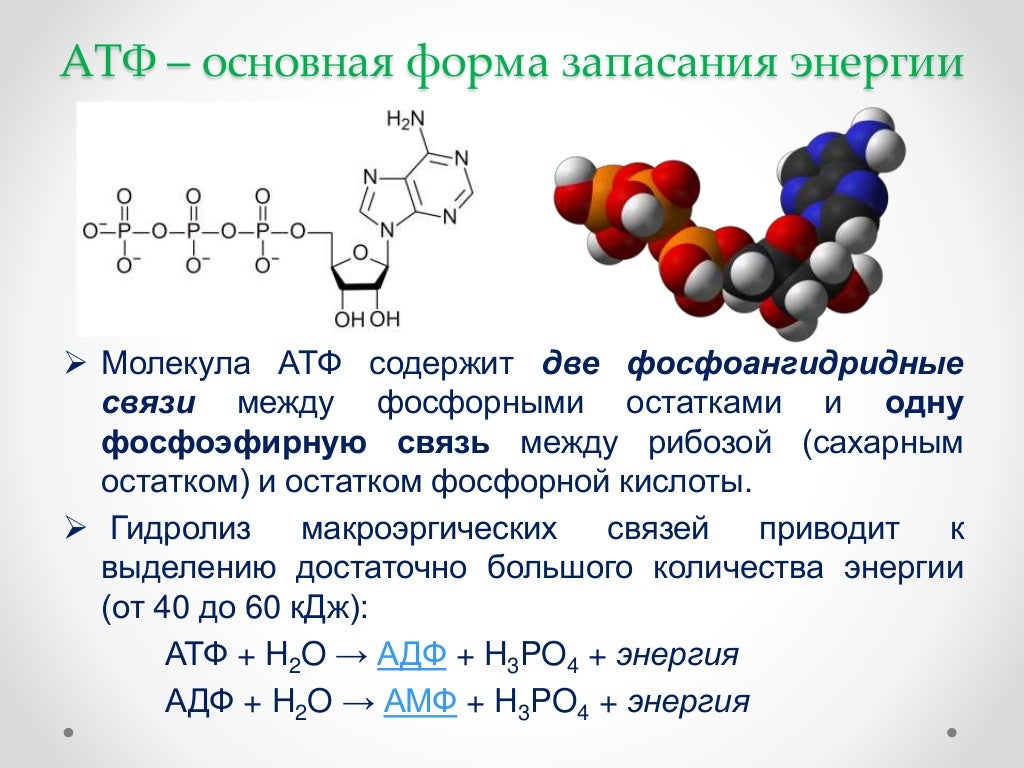
Наибольшее количество АТФ потребляет мышечная ткань.
Закрепление
Вопрос:
Какие особенности строения определяют основную функцию АТФ?
Обобщение
Вывод: значение АТФ в жизни клетки велико, она играет центральную роль в клеточных превращениях энергии.
Домашнее задание:
Выучить конспект.
Дополнительный материал
АМФ – аденозинмонофосфорная кислота — входит в состав всех РНК.
Остатки фосфорной кислоты отщепляются из состава АТФ под действием фермента АТФазы.
Контрольная работа
Тема: АТФ
1. Какова структура молекулы АТФ?
1) биополимер; 2) нуклеотид; 3) мономер.
2. Какие соединения входят в состав АТФ?
Какие соединения входят в состав АТФ?
1) азотистое основание аденин; 2) углевод рибоза;
3) три молекулы фосфорной кислоты; 4) глицерин; 5) аминокислота.
3. В каких органеллах синтезируется АТФ в растительной клетке?
1) рибосомы; 2) митохондрии; 3) хлоропласты.
4. В каких органеллах синтезируется АТФ в животной клетке?
1) рибосомы; 2) митохондрии; 3) хлоропласты.
5. В результате какого процесса, происходящего в митохондриях, синтезируется АТФ?
1) фотосинтез; 2) дыхание; 3) биосинтез белков.
6. С каким процессом связан синтез АТФ в хлоропластах?
1) световая фаза фотосинтеза; 2) темновая фаза фотосинтеза;
3) биосинтез белков.
7. Что служит источником энергии при синтезе АТФ в митохондриях?
1) органические соединения; 2) теплота; 3) свет.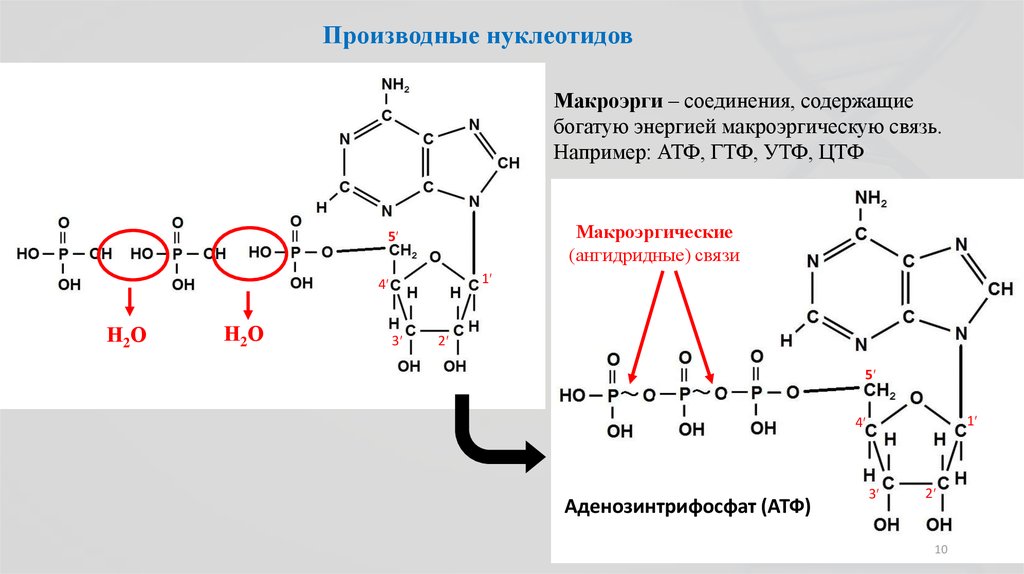
8. Что служит источником энергии при синтезе АТФ в хлоропластах?
1) органические соединения; 2) теплота; 3) свет.
9. Где происходит синтез АТФ в митохондриях?
1) на наружной мембране; 2) на кристах.
10. Где происходит расщепление АТФ?
1) на наружной мембране; 2) на кристах; 3) в цитоплазме.
11. Сколько энергии заключено в АТФ?
1) 40 кДж; 2) 80 кДж; 3) 0 кДж.
12. Сколько энергии заключено в АДФ?
1) 40 кДж; 2) 80 кДж; 3) 0 кДж.
13. Сколько энергии заключено в АМФ?
1) 40 кДж; 2) 80 кДж; 3) 0 кДж.
Ответы:
1-2
2-1,2,3
3-2,3
4-2
5-2
6-1
7-1
8-3
9-2
10-3
11-2
12-1
13-3
Макроэргические соединения | это.
 .. Что такое Макроэргические соединения? I Макроэрги́ческие соедине́ния (греч. makros большой + ergon работа, действие; синоним: высокоэргические соединения, высокоэнергетические соединения)
.. Что такое Макроэргические соединения? I Макроэрги́ческие соедине́ния (греч. makros большой + ergon работа, действие; синоним: высокоэргические соединения, высокоэнергетические соединения)группа природных веществ, молекулы которых содержат богатые энергией, или макроэргические, связи; присутствуют во всех живых клетках и участвуют в накоплении и превращении энергии. Разрыв макроэргических связей в молекулах М.с. сопровождается выделением энергии, используемой для биосинтеза и транспорта веществ, мышечного сокращения, пищеварения и других процессов жизнедеятельности организма.
Все известные М.с. содержат фосфорильную (—РО3Н2) или ацильную
группы и могут быть описаны формулой Х—Y, где Х — атом азота, кислорода, серы или углерода, а Y — атом фосфора или углерода. Реакционная способность М.с. связана с повышенным сродством к электрону атома Y, что обусловливает высокую свободную энергию гидролиза М.с., составляющую 6—14 ккал/моль.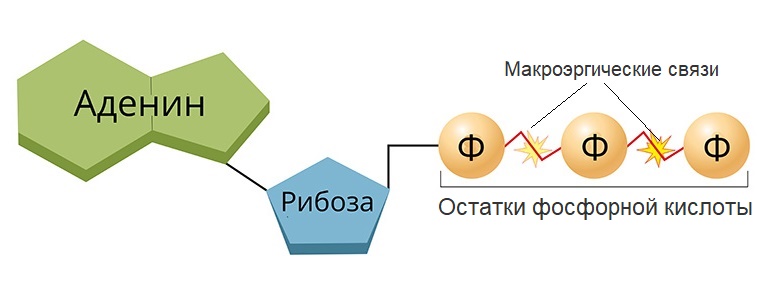
Важной группой соединений, в которую входят М.с., являются аденозинфосфорные, или адениловые, кислоты — нуклеозиды, содержащие аденин, рибозу и остатки фосфорной кислоты (см. рис.).
Наиболее значительное из них — аденозинтрифосфорная кислота (аденозинтрифосфат, АТФ).
АТФ представляет собой аденозинфосфорную кислоту, содержащую 3 остатка фосфорной кислоты (или фосфатных остатка), служит универсальным переносчиком и основным аккумулятором химической энергии в живых клетках, кофермент многих ферментов (см. Коферменты). АТФ не единственное биологически активное соединение, содержащее пирофосфатные связи. Некоторые фосфорилированные соединения по количеству энергии, заключенной в таких связях, не отличаются от АТФ. Однако дифосфаты таких соединений не могут заменить аденозиндифосфорную кислоту в тех процессах, которые ведут к синтезу АТФ, а их трифосфаты не могут заменить АТФ в последующих процессах энергетического обмена, в которых АТФ используется как донор энергии, необходимой для протекания биосинтетических реакций.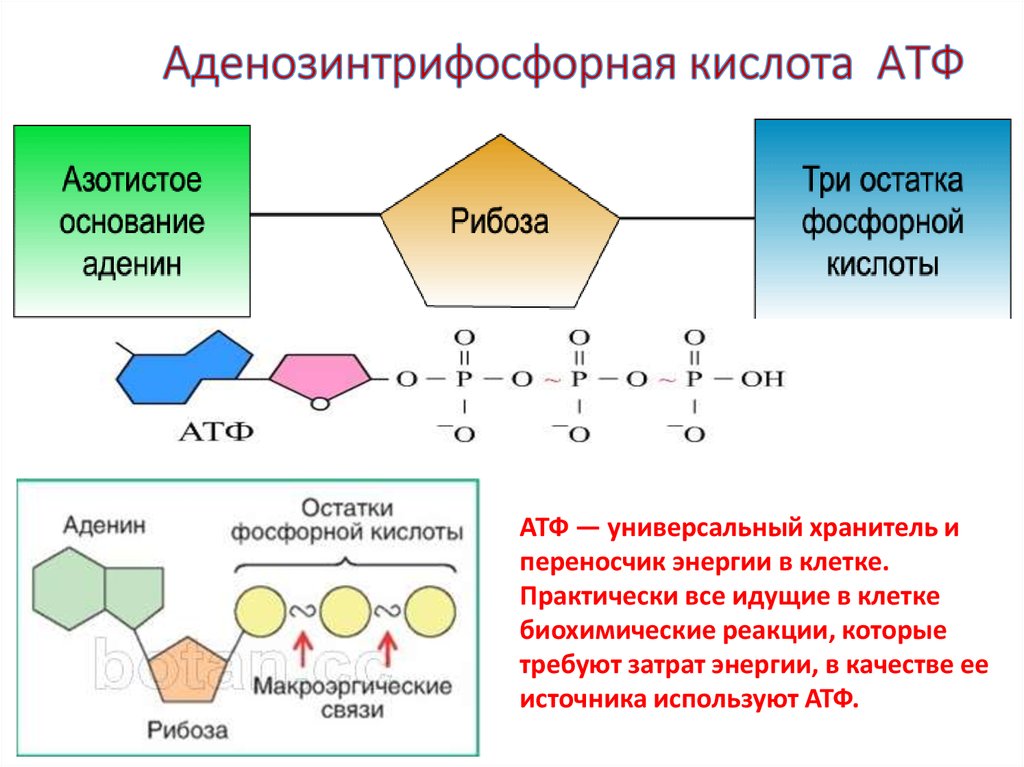
В отдельных биосинтетических реакциях непосредственным источником энергии служат не АТФ, а некоторые другие трифосфонуклеотиды. Однако их нельзя считать первичным источником энергии, поскольку сами они образуются в результате переноса фосфатной или пирофосфатной группы от АТФ. Это справедливо и для вещества другого типа, приспособленного для запасания энергии, — креатинфосфата (см. Креатинин). Макроэргическими в молекуле АТФ являются две пирофосфатные связи: между α- и β- и между β- и γ-фосфатными остатками. При гидролизе концевой пирофосфатной связи освобождается 8,4 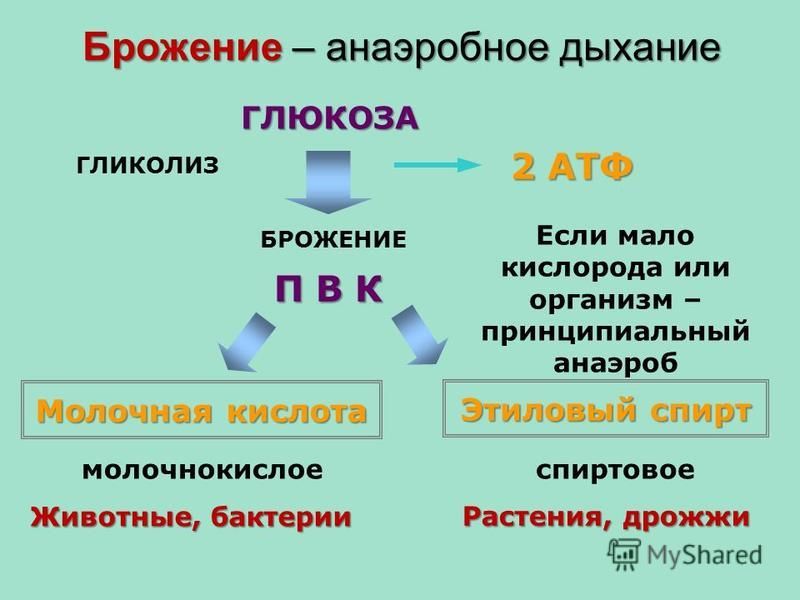
Отщепление фосфатных остатков от молекул АТФ происходит при участии аденозинтрифосфатаз (АТФ-аз) — ферментов класса гидролаз, широко распространенных в клетках всех организмов и обеспечивающих использование энергии АТФ для осуществления различных процессов жизнедеятельности. Группа транспортных АТФ-аз осуществляет активный перенос ионов, аминокислот, нуклеотидов, Сахаров и других веществ через биологические мембраны, создание и поддержание градиентов концентраций ионов (ионных градиентов) по обе стороны биологических мембран. Активный транспорт ионов, обеспечиваемый за счет энергии гидролиза АТФ, лежит в основе биоэнергетики (Биоэнергетика) клетки, процессов клеточного возбуждения, поступления в клетку и выведения веществ из клетки и организма, К важнейшим транспортным АТФ-азам, обеспечивающим перенос ионов при гидролизе АТФ, относятся Н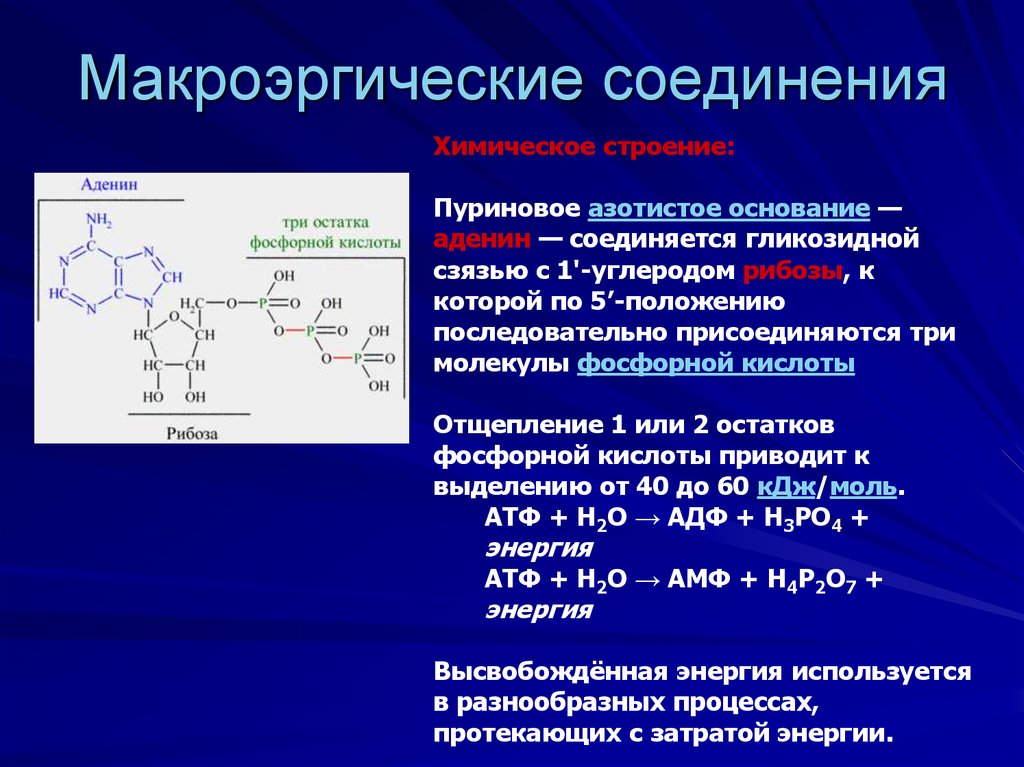 В результате осуществляемого этими ферментами транспорта ионов против градиента их концентраций на мембране генерируется разность электрических потенциалов. Нарушение функционирования транспортных АТФ-аз (например, выключение АТФ-аз в условиях гипоксии в отсутствие АТФ) ведет к развитию многих патологических состояний. Известны лекарственные средства (например, сердечные гликозиды), регулирующие активность этих ферментов.
В результате осуществляемого этими ферментами транспорта ионов против градиента их концентраций на мембране генерируется разность электрических потенциалов. Нарушение функционирования транспортных АТФ-аз (например, выключение АТФ-аз в условиях гипоксии в отсутствие АТФ) ведет к развитию многих патологических состояний. Известны лекарственные средства (например, сердечные гликозиды), регулирующие активность этих ферментов.
Расщепление АТФ может сопровождаться не только переносом фосфорильной группы на молекулу-акцептор, как это происходит в реакциях, катализируемых киназами (Киназы)
АТФ образуется из аденозиндифосфорной кислоты (АДФ) в результате окислительного фосфорилирования при переносе электронов в митохондриальной электронпереносящей цепи (см. Дыхание тканевое, Обмен веществ и энергии) или в результате фосфорилирования на уровне субстрата (см.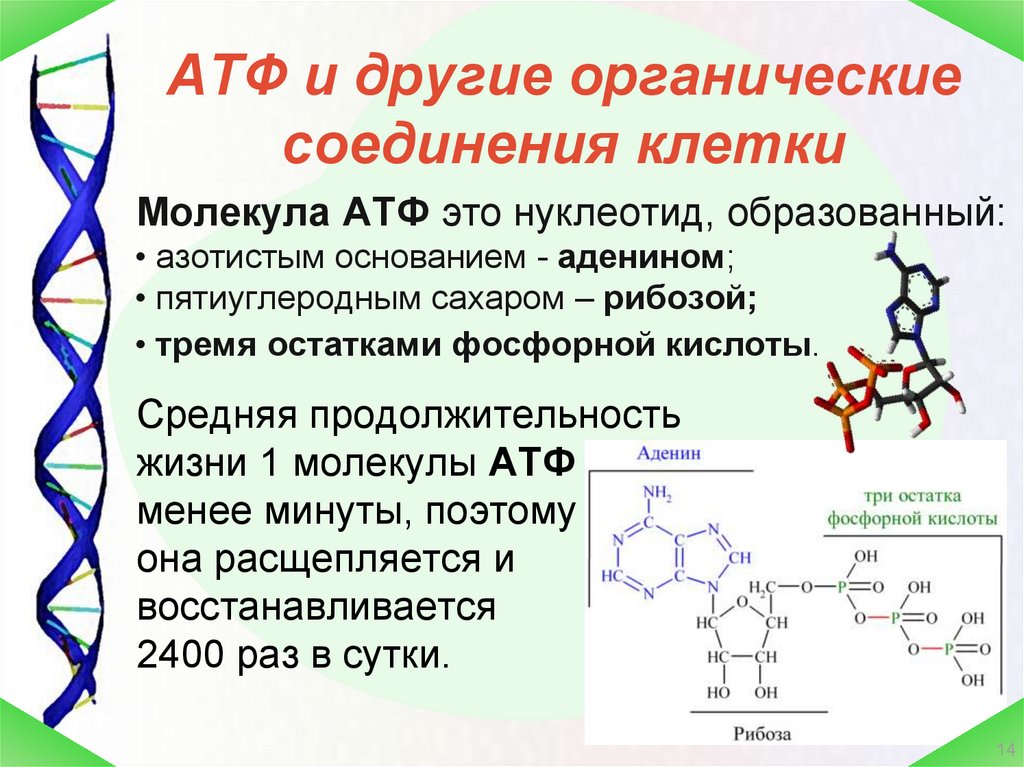
Важным макроэргическим соединением, участвующим в ресинтезе АТФ в мышечной ткани, является содержащийся в скелетных мышцах всех позвоночных животных креатин-фосфат — фосфорилированное производное креатина, или β-метилгуанидинуксусной кислоты (см. Креатинин)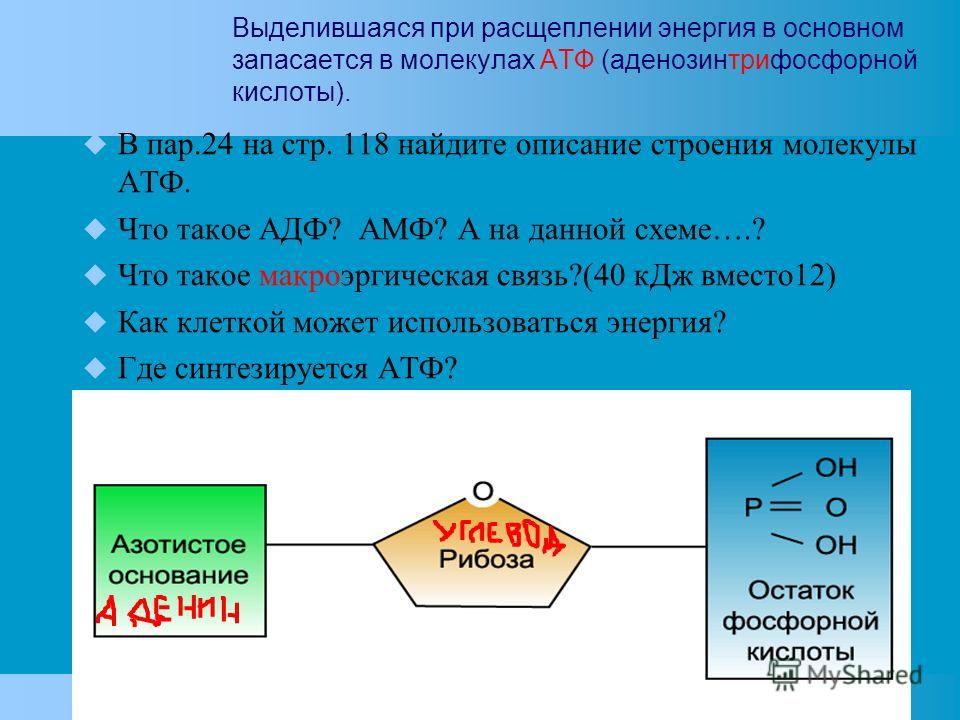
Наряду с АТФ к макроэргическим соединениям относятся и другие нуклеозидтрифосфорные кислоты: гуанозинтрифосфат (ГТФ), уридинтрифосфат (УТФ), инозинтрифосфат (ИТФ) и тимидинтрифосфат (ТТФ), играющие роль поставщиков энергии в различных биосинтетических процессах и взаимопревращениях углеводов, липидов, а также соответствующие нуклеозиддифосфорные кислоты, пирофосфорная и полифосфорная кислоты (см. Фосфор)
Библиогр.: Брода Э. Эволюция биоэнергетических процессов, пер. с англ., М., 1978: Певзнер Л. Основы биоэнергетики, пер. с англ., М., 1977; Рэкер Э. Биоэнергетические механизмы, пер. с англ., М., 1979; Скулачев В.П. Трансформация энергии в биомембранах, М., 1972.
Макроэргические соединения.
II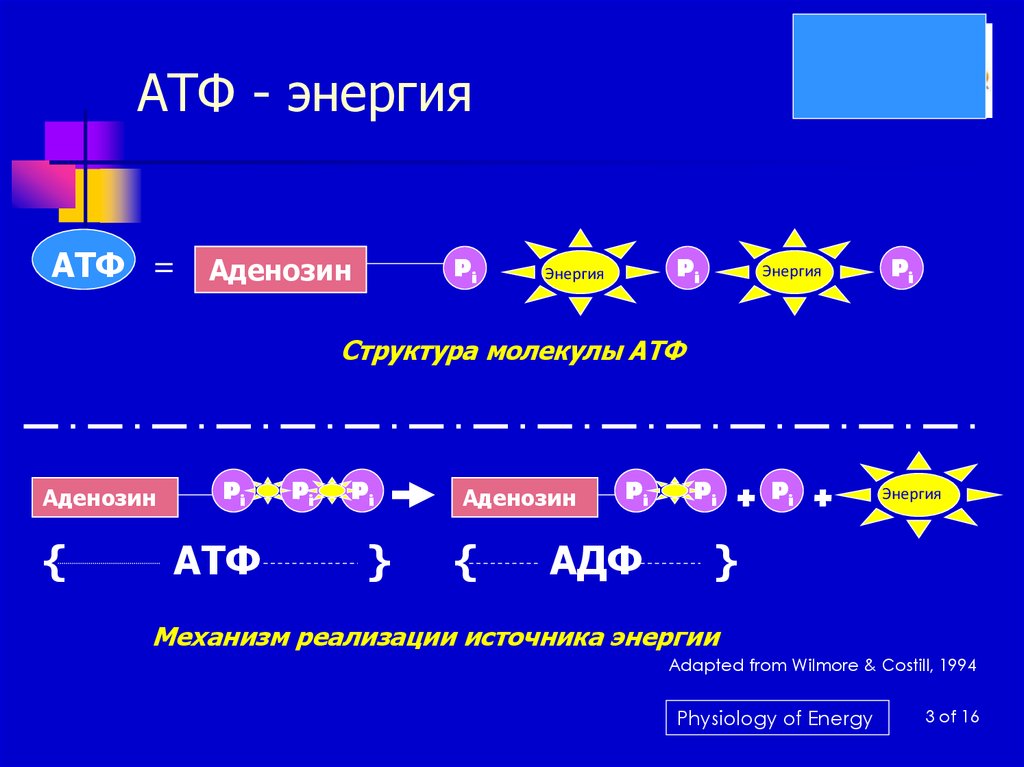 высокоэргические соединения)
высокоэргические соединения)органические соединения, расщепление которых сопровождается выделением большого количества свободной энергии; в М. с. аккумулируется энергия, расходуемая организмом в процессе своей жизнедеятельности.
1. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг.
АТФ/АДФ — Химия LibreTexts
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 376
Аденозин-5′-трифосфат (АТФ) состоит из аденинового кольца, сахара рибозы и трех фосфатных групп. АТФ часто используется для передачи энергии в клетке. АТФ-синтаза производит АТФ из АДФ или AMP + P
АТФ часто используется для передачи энергии в клетке. АТФ-синтаза производит АТФ из АДФ или AMP + P
Введение
АТФ представляет собой нестабильную молекулу, которая гидролизуется до АДФ и неорганического фосфата, когда находится в равновесии с водой. Высокая энергия этой молекулы обусловлена двумя высокоэнергетическими фосфатными связями. Связи между молекулами фосфатов называются фосфоангидридными связями. Они богаты энергией и имеют ΔG -30,5 кДж/моль.
Рисунок 1: Структура молекулы АТФ и молекулы АДФ соответственно. Адениновое кольцо находится вверху и связано с сахаром рибозой, который связан с фосфатными группами.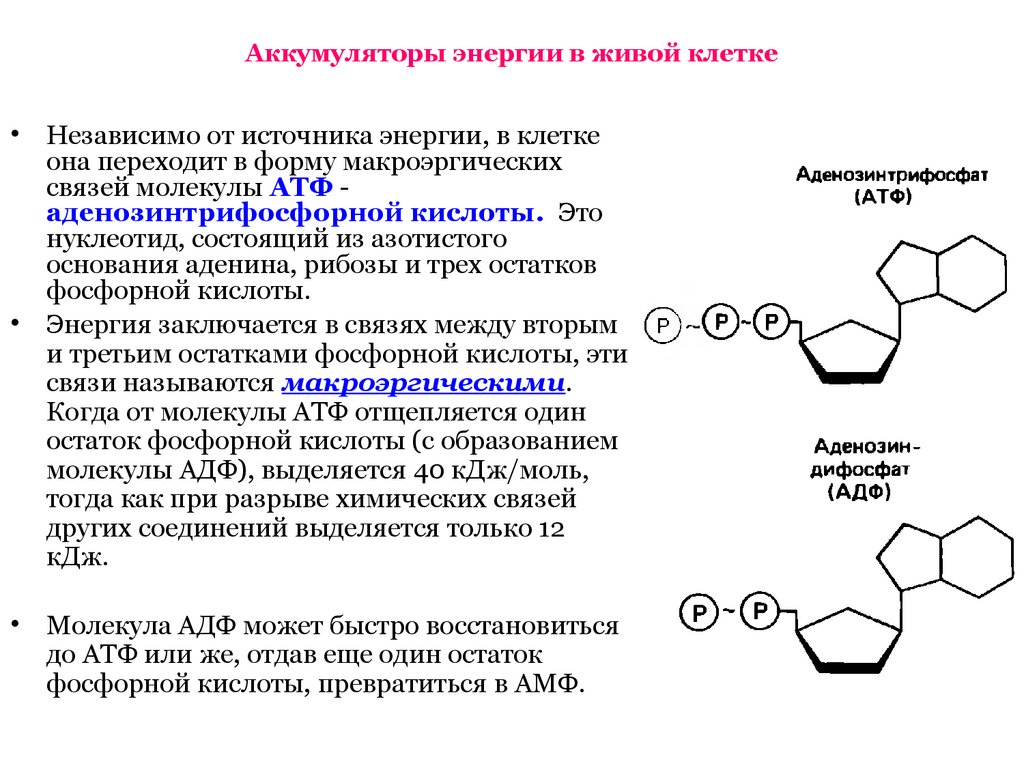 Используется с разрешения Wikipedia Commons.
Используется с разрешения Wikipedia Commons.Гидролиз АТФ
Удаление или добавление одной фосфатной группы взаимопревращает АТФ в АДФ или АДФ в АМФ. При разрыве одной фосфоангидридной связи выделяется 7,3 ккал/моль энергии.
\[\ce{АТФ + H_2O \rightarrow АДФ + P_{i}} \tag{ΔG = -30,5 кДж/моль}\]
\[\ce{АТФ + H_2O \rightarrow AMP + 2 P_{i } } \tag{ΔG = -61 кДж/моль}\] 9{+}} \nonumber\]
Почему гидролиз АТФ является экзергонической реакцией?
- Энтропия, то есть уровень беспорядка, АДФ больше, чем АТФ. Следовательно, из-за термодинамики реакция происходит самопроизвольно, потому что она хочет быть на более высоком уровне энтропии. Кроме того, свободная энергия Гиббса АТФ выше, чем у АДФ. Естественно, молекулы хотят находиться в более низком энергетическом состоянии, поэтому равновесие смещается в сторону АДФ.
- Электростатическое отталкивание четырех отрицательных зарядов атомов кислорода молекулы АТФ. Естественно, одноименные заряды отталкиваются, а противоположные притягиваются.
 Следовательно, если есть четыре отрицательных заряда в непосредственной близости друг от друга, они естественным образом будут отталкиваться друг от друга. Это делает АТФ относительно нестабильной молекулой, потому что при возможности она захочет отдать свои фосфатные группы, чтобы стать более стабильной молекулой.
Следовательно, если есть четыре отрицательных заряда в непосредственной близости друг от друга, они естественным образом будут отталкиваться друг от друга. Это делает АТФ относительно нестабильной молекулой, потому что при возможности она захочет отдать свои фосфатные группы, чтобы стать более стабильной молекулой. - Резонансная стабилизация АДФ и Р и больше, чем у АТФ. Молекулы кислорода АДФ делят электроны. Эти электроны постоянно перемещаются между атомами кислорода, создавая эффект, называемый резонансом. Это стабилизирует ADP. В АТФ резонанса не бывает; следовательно, это более нестабильная молекула.
- Существует большая степень сольватации P i , H + и АДФ по сравнению с АТФ. Это означает, что АТФ легче потерять одну из своих фосфатных групп. Но требуется большое количество воды, чтобы заставить АДФ потерять один из своих фосфатов.
АТФ в клетке
АТФ является основным переносчиком энергии для большинства энергозатратных реакций, протекающих в клетке.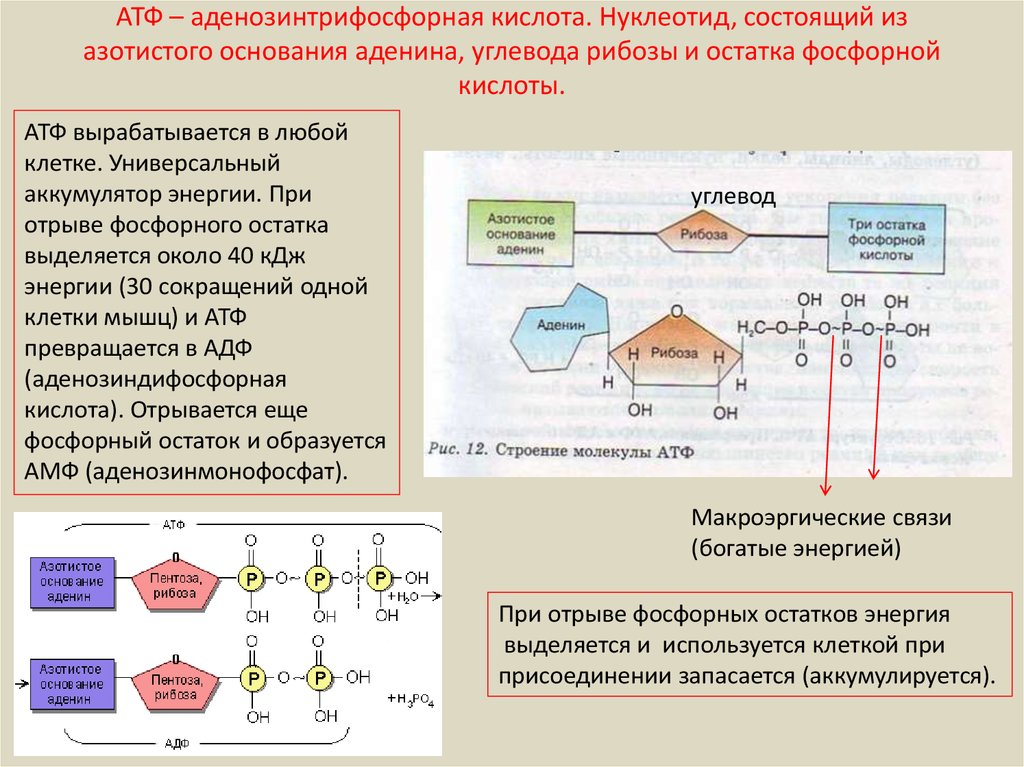 Непрерывный синтез АТФ и его немедленное использование приводит к тому, что АТФ имеет очень высокую скорость оборота. Это означает, что АДФ очень быстро синтезируется в АТФ и наоборот. Например, требуется всего несколько секунд, чтобы половина молекул АТФ в клетке превратилась в АДФ, который использовался для управления эндергоническими (неспонтанными) реакциями, а затем снова превратился в АТФ с помощью экзергонических (самопроизвольных) реакций.
Непрерывный синтез АТФ и его немедленное использование приводит к тому, что АТФ имеет очень высокую скорость оборота. Это означает, что АДФ очень быстро синтезируется в АТФ и наоборот. Например, требуется всего несколько секунд, чтобы половина молекул АТФ в клетке превратилась в АДФ, который использовался для управления эндергоническими (неспонтанными) реакциями, а затем снова превратился в АТФ с помощью экзергонических (самопроизвольных) реакций.
АТФ используется во многих клеточных процессах, таких как гликолиз, фотосинтез, бета-окисление, анаэробное дыхание, активный транспорт через клеточные мембраны (как в цепи переноса электронов) и синтез макромолекул, таких как ДНК.
Ссылки
- Зубай, Джеффри. Биохимия. Нью-Йорк: издательство Macmillan Publishing Company, 1988. .
Проблемы
- В каком процессе клеточного дыхания образуется больше всего АТФ?
- Правда или ложь: АТФ может использоваться для регуляции определенных ферментов.

- Из одной молекулы глюкозы сколько молекул АТФ получится?
- Где находится АТФ-синтаза?
- Верно или неверно: АТФ образуется в результате фосфорилирования на уровне субстрата.
Ответы
- Цепь переноса электронов
- Правда
- 32–34 молекулы АТФ
- Расположен во внутренней митохондриальной мембране.
- Правда
Авторы и ссылки
- Тиффани Луи, Калифорнийский университет, Дэвис.
ATP/ADP распространяется под лицензией CC BY-NC-SA 4.0 и был создан, изменен и/или курирован LibreTexts.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Глава
- Лицензия
- CC BY-NC-SA
- Версия лицензии
- 4,0
- Показать страницу TOC
- № на стр.

- Теги
- АТП
- гидролиз
Соединения, богатые энергией; классификация; биологическое значение АТФ и циклического АМФ: Pharmaguideline
В клетке химические связи могут использоваться для хранения энергии, но не все химические связи обладают одинаковой энергией.
В клетке химические связи могут использоваться для хранения энергии, но не все химические связи обладают одинаковой энергией. Разорванная химическая связь может высвободить большее количество энергии, чем другие. Молекула фосфата состоит из трех атомов кислорода, присоединенных к одному атому фосфора (PO3). Он образует фосфатные связи с другими молекулами, когда они связаны вместе. Когда вы разрываете эту связь, высвобождается огромное количество энергии.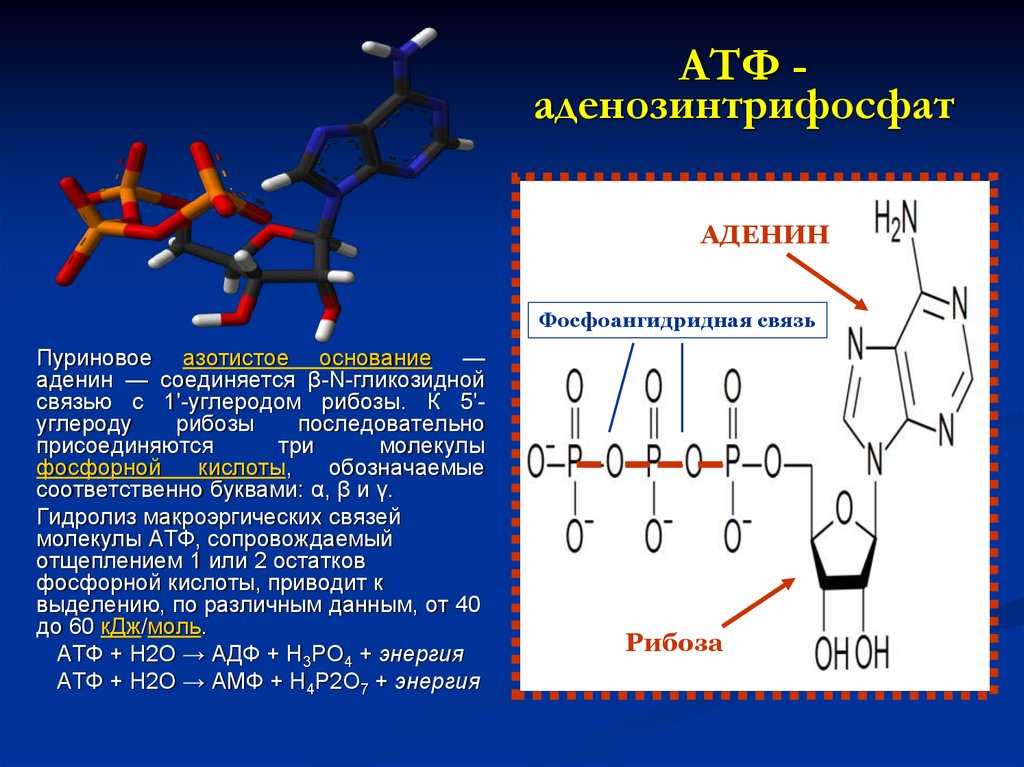 Эти молекулы сами состоят из богатых энергией соединений. Клетки используют эти богатые энергией соединения в качестве топлива для биохимических реакций, требующих энергии. Молекулы, полученные из кофермента А, являются еще одним важным источником энергии. Например, ацетил-КоА имеет богатую серой тиоэфирную связь, а не фосфатную связь, поэтому он обеспечивает энергию. Энергии требуется ровно столько, чтобы образовать фосфатную связь в АТФ при расщеплении ацетил-КоА. Несмотря на то, что эти молекулы необходимы для всех типов метаболизма, они особенно важны для микробов, которые полагаются на анаэробный метаболизм (ферментацию), протекающий без доступа кислорода.
Эти молекулы сами состоят из богатых энергией соединений. Клетки используют эти богатые энергией соединения в качестве топлива для биохимических реакций, требующих энергии. Молекулы, полученные из кофермента А, являются еще одним важным источником энергии. Например, ацетил-КоА имеет богатую серой тиоэфирную связь, а не фосфатную связь, поэтому он обеспечивает энергию. Энергии требуется ровно столько, чтобы образовать фосфатную связь в АТФ при расщеплении ацетил-КоА. Несмотря на то, что эти молекулы необходимы для всех типов метаболизма, они особенно важны для микробов, которые полагаются на анаэробный метаболизм (ферментацию), протекающий без доступа кислорода.
Классификация соединений, богатых энергией
Всего существует 5 типов
Фосфоангидриды — В фосфорной кислоте две молекулы соединяются, образуя соединение, называемое фосфоангидридами. Пример. В АТФ встречаются такие виды связей. Молекулярная структура АТФ состоит из двух высокоэнергетических молекул дифосфата (фосфоангидридные связи).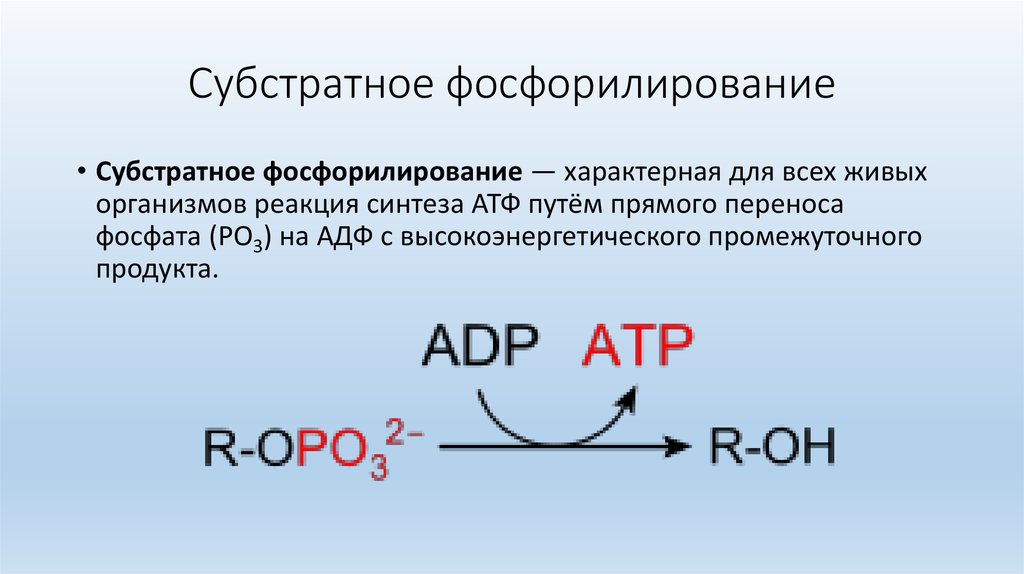 Связь сложного эфира фосфорной кислоты между рибозой и фосфатом не такая энергоемкая, как связь сложного эфира фосфорной кислоты. В большинстве эндергонических реакций АТФ служит основным непосредственным источником свободной энергии. Пример — транспорт, мышечные сокращения и передача нервных импульсов. Протеосинтез и глюконеогенез зависят от ГТФ (гуанидинтрифосфата) в качестве источника энергии. Кроме того, UTP (трифосфат уридина) и CTP (трифосфат цитидина) являются источниками энергии, которые используются организмом для получения энергии из сахаридов и липидов.
Связь сложного эфира фосфорной кислоты между рибозой и фосфатом не такая энергоемкая, как связь сложного эфира фосфорной кислоты. В большинстве эндергонических реакций АТФ служит основным непосредственным источником свободной энергии. Пример — транспорт, мышечные сокращения и передача нервных импульсов. Протеосинтез и глюконеогенез зависят от ГТФ (гуанидинтрифосфата) в качестве источника энергии. Кроме того, UTP (трифосфат уридина) и CTP (трифосфат цитидина) являются источниками энергии, которые используются организмом для получения энергии из сахаридов и липидов.
Енолфосфатная связь — Существует полоса очень высокой энергии, которая высвобождает 61 кДж/моль при гидролизе. Во время ингликолиза глюкозы фосфоенолпируват образует такую же связь, что и фосфоенолпируват.
Ацилфосфатная связь — При гидролизе эта связь дает 49 кДж/моль энергии. Этот тип связи возникает при ингликолизе 1-3 бисфосфоглицератов
Гуанидинфосфат — При присоединении фосфата к гуанидину образуется гуанидинфосфат. При гидролизе продукт высвобождает около 43 килоджоулей энергии. ФХ содержит тот же тип связи, что и фосфокреатин. Это вещество содержится в мышечных клетках и действует как запас энергии в тканях.
При гидролизе продукт высвобождает около 43 килоджоулей энергии. ФХ содержит тот же тип связи, что и фосфокреатин. Это вещество содержится в мышечных клетках и действует как запас энергии в тканях.
Тиоэфирная связь — В тиоэфирной связи нет богатого энергией фосфата, поэтому она не содержит много энергии. Ацетил-ко-А содержит этот тип связи.
Биологическое значение АТФ
Наиболее распространенным источником энергии для клеток является АТФ. Аденозинтрифосфат (АТФ) состоит из углерода, азота, водорода, кислорода и фосфора. В реакциях, когда АТФ подвергается гидролизу, выделяется большое количество энергии, поскольку она содержит нестабильные высокоэнергетические связи. Поскольку фермент удаляет фосфатную группу из АТФ с образованием АДФ, он генерирует значительное количество энергии, которая может использоваться клеткой для различных метаболических процессов. Белки, а также другие макромолекулы могут быть синтезированы с его помощью. При удалении второй фосфатной группы из АТФ образуется аденозинмонофосфат (АМФ), а также дополнительное выделение энергии. АМФ и АДФ добавляются обратно к фосфату с образованием АТФ, когда организму не требуется энергия, которая при необходимости гидролизуется. Следовательно, АТФ служит эффективным источником энергии для клеточных путей.
При удалении второй фосфатной группы из АТФ образуется аденозинмонофосфат (АМФ), а также дополнительное выделение энергии. АМФ и АДФ добавляются обратно к фосфату с образованием АТФ, когда организму не требуется энергия, которая при необходимости гидролизуется. Следовательно, АТФ служит эффективным источником энергии для клеточных путей.
Циклический АМФ
Циклический АМФ играет ключевую роль в действии гормонов благодаря действию адреналина. Гормон «бей или беги» вырабатывается надпочечниками в ответ на стресс. В результате действия гормона повышается артериальное давление, а глюкоза расщепляется для получения энергии. Физическая активность помогает людям справляться с трудностями ситуации. В ответ организм демонстрирует высокое кровяное давление, учащенное сердцебиение и сухость во рту. За эти ответы ответственны биохимические реакции. Адреналин остается вне клеток на связанных с мембраной рецепторах, когда он связывается с ними. Аденилатциклаза производит циклический АМФ, вторичный мессенджер.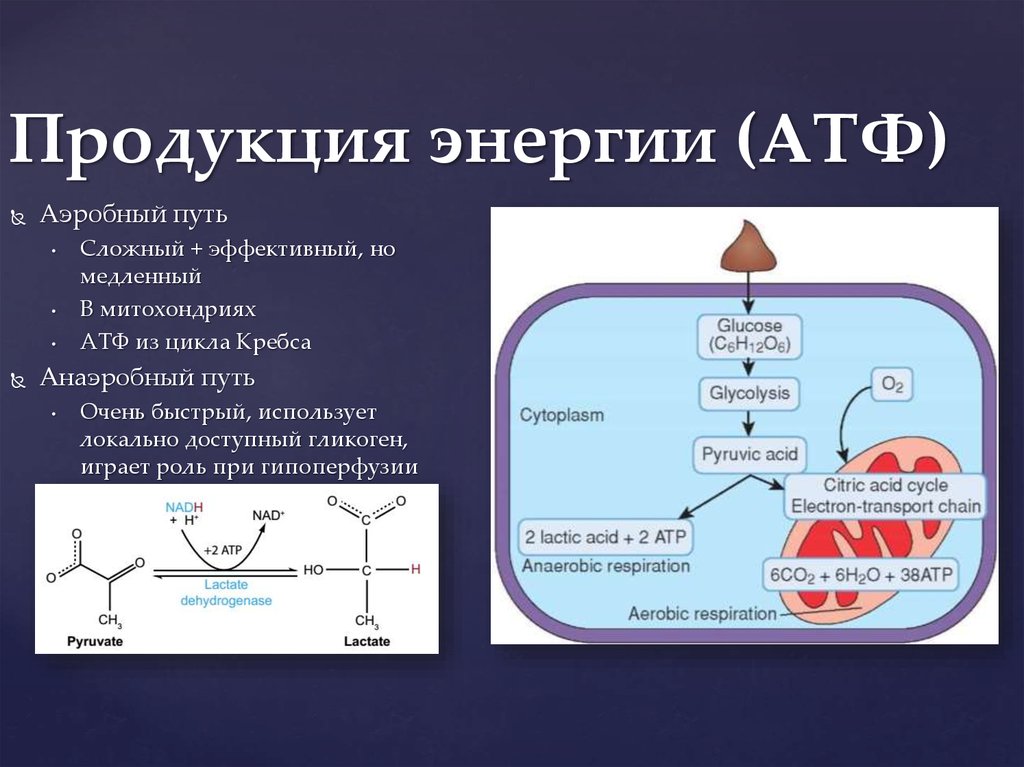
Ферментная система аденилатциклазы состоит из двух компонентов. Он катализирует аденилатциклазу, когда он связан с рецептором, связанным с гормоном, и когда с ним связывается и активируется регуляторный белок, стимулирующий G-белок (белок, связывающий гуанилатные нуклеотиды). В качестве посредника между рецептором и синтезом циклического АМФ важную роль играет G-белок. От гуанилатного нуклеотида, связанного с G-белками, зависит, активны они или неактивны. G-белок связывается с GDP, когда он неактивен. Как только G-белок становится активным, GTP связывается с ним. В G-белках GTP превращается в GDP за счет внутренней активности GTPase. G-белок становится неактивным после гидролиза GTP. G-белки цикличны:
- Гормоны связываются с рецепторами.
- Рецепторы, связывающие гормоны, связываются с G-белками, в результате чего ГТФ замещает ГДФ.
- Аденилатциклаза взаимодействует с GTP-связанным G-белком.
- При гидролизе GTP G-белок возвращается в основное состояние.

Различные G-белки могут увеличивать или уменьшать продукцию циклического АМФ путем стимуляции или ингибирования аденилатциклазы.
Например, циклический АМФ не влияет на гликогенфосфорилазу и гликогенсинтазу. Вместо этого циклический АМФ стимулирует активность протеинкиназы, что в конечном итоге вызывает реакцию в клетках. Фосфат переносится от АТФ к гликогенфосфорилазе и гликогенфосфорилазе через циклические АМП, которые связываются с протеинкиназой А. Затем гликоген-1-фосфат образуется из гликогена с помощью активной гликогенфосфорилазы. Затем мышцы могут использовать этот источник энергии.
Невозможно вечно держать ячейку включенной. Они должны на что-то реагировать. Каждый шаг можно отменить. Протеинфосфатаза гидролизует фосфат из белка, начиная с целевого белка. Фермент фосфодиэстераза гидролизует циклический АМФ. Гидролиз GTP G-белком может иметь решающее значение для модуляции. Аденилатциклаза после стимуляции возвращается в нестимулированное состояние.

 Следовательно, если есть четыре отрицательных заряда в непосредственной близости друг от друга, они естественным образом будут отталкиваться друг от друга. Это делает АТФ относительно нестабильной молекулой, потому что при возможности она захочет отдать свои фосфатные группы, чтобы стать более стабильной молекулой.
Следовательно, если есть четыре отрицательных заряда в непосредственной близости друг от друга, они естественным образом будут отталкиваться друг от друга. Это делает АТФ относительно нестабильной молекулой, потому что при возможности она захочет отдать свои фосфатные группы, чтобы стать более стабильной молекулой.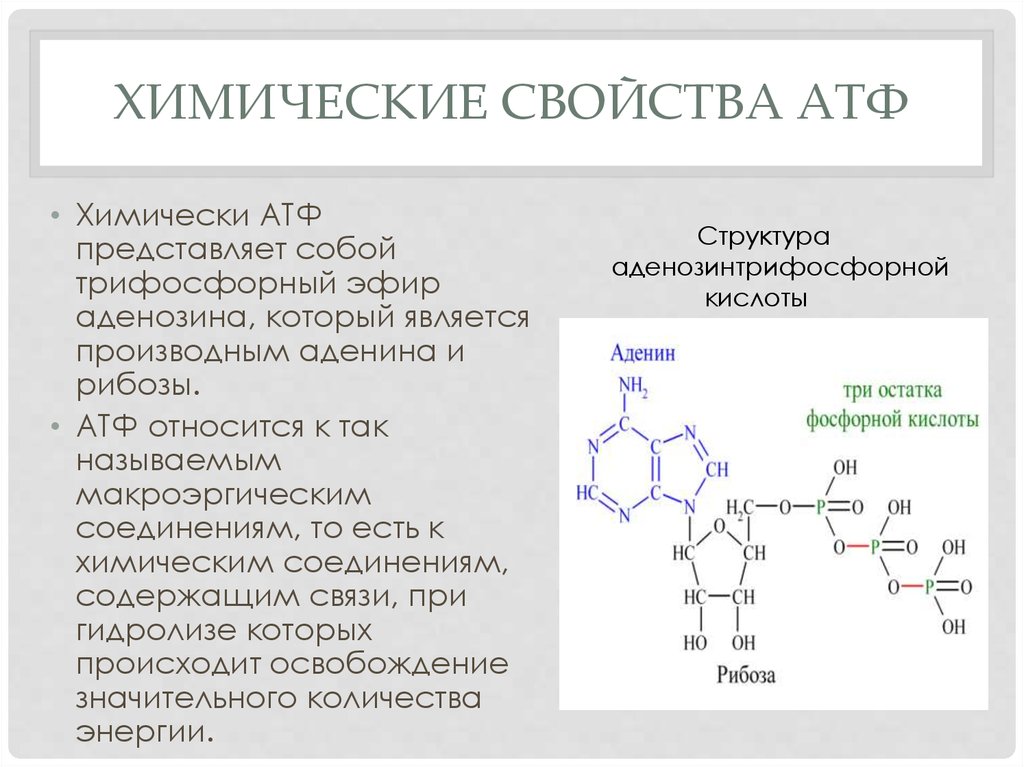

Leave A Comment