Подготовка к ЕГЭ по химии самостоятельно на 100 баллов
Автор статьи Ирина Борисовна Юдина, преподаватель Образовательной компании «ЕГЭ-Студия».
Можно ли подготовиться к ЕГЭ по химии самостоятельно?
Если вы блестяще знаете школьную программу, не на “5”, а на “10”,
Если вы понимаете всё-всё досконально,
Если, кроме школьных учебников, вы занимаетесь по специальным книгам для самостоятельной подготовки к ЕГЭ по химии —
вы вполне справитесь без репетиторов!
Однако учеников, которые могут самостоятельно подготовиться к ЕГЭ по химии, — единицы.
Если вы занимаетесь с репетитором — вам намного проще готовиться. В этом случае успех более вероятен.
Почему же большинству тех, кто сдает ЕГЭ по химии, нужен репетитор?
— во-первых, репетитор по химии знает, что именно нужно для ЕГЭ. В школьном учебнике материала много, и хотя ЕГЭ по химии – это экзамен по школьной программе, акценты в нем расставлены совсем иначе.
— во-вторых, репетитор по химии — это человек, которому хватает знаний и квалификации реально оценить ваш уровень.
Внимание. В задачах ЕГЭ по химии возможна ситуация, когда ошибочные рассуждения случайно приводят к верному ответу. Если вы самостоятельно готовитесь к ЕГЭ по химии — будьте внимательны! Ищите способы реально оценить свой уровень.
— в-третьих, репетитор по химии может найти и предоставить все необходимые материалы в сжатом виде и добиться их полного понимания учеником. Он подбирает нужные задачи. Ученик сам не может этого сделать — потому что еще не разобрался в химии на должном уровне.
Для тех, кто все-таки решил готовиться к ЕГЭ по химии самостоятельно, я рекомендую свою книгу “Химия. Авторский курс подготовки к ЕГЭ”. Рекомендую также книгу Н. Е. Кузьменко, В. В. Еремина, В. А. Попкова «Начала химии». Там даже больше материала, чем необходимо для сдачи ЕГЭ, но это необходимо для глубокого понимания. В химии есть разделы, которые в ЕГЭ не входят, но если ты с ними знаком, то намного лучше понимаешь происходящее. Например, это квантовые числа и строение атома, это механизмы реакций в органической химии.
В химии есть разделы, которые в ЕГЭ не входят, но если ты с ними знаком, то намного лучше понимаешь происходящее. Например, это квантовые числа и строение атома, это механизмы реакций в органической химии.
Я могу рекомендовать также учебники Н. С. Ахметова, Б. В. Некрасова, Н. Л. Глинки по общей и неорганической химии. Это, конечно, для углублённой подготовки, и там материала больше, чем необходимо для сдачи ЕГЭ.
Готовиться к ЕГЭ по химии самостоятельно совсем не просто. Химия — это многообразие фактов, которые мы пытаемся описать, заметив некоторые закономерности. “Выпадающие точки” мы называем исключениями. И возможно, что лет через 200 ученые скажут: «Бедные древние ученые XXI века, как много они не знали, как они глубоко заблуждались!» Так мы сейчас говорим про ученых XVIII — XIX века.
Какие исключения могут встретиться в ЕГЭ? Я как репетитор это знаю, а ученик не знает. Я могу сказать своему ученику, что исключений нужно знать всего пять, и это с запасом. И так в любой теме!
Но и это не всё. Оказывается, разные, одинаково авторитетные учебники, могут друг другу противоречить! Особенно в теме «Химические реакции».
Оказывается, разные, одинаково авторитетные учебники, могут друг другу противоречить! Особенно в теме «Химические реакции».
В органической химии не бывает стопроцентного выхода реакции. В реальности то, что мы называем реакцией в органической химии, — это несколько параллельных процессов, с получением разных продуктов. И какие-то из них считаются основными процессами, а другие побочными, и разные авторы расходятся во мнении.
Репетиторы много лет анализируют варианты ЕГЭ, изучают критерии и знают, что именно требуется в ЕГЭ. Но ученик может этого не знать!
Даже тестовая часть ЕГЭ по химии очень непроста. Например, в задании пять вариантов ответов. Нужно из них выбрать три и еще расположить их в определенном порядке! Сможете ли вы сделать это, готовясь к ЕГЭ по химии самостоятельно? Выбор за вами!
Спасибо за то, что пользуйтесь нашими статьями.
Информация на странице «Подготовка к ЕГЭ по Химии самостоятельно» подготовлена нашими редакторами специально, чтобы помочь вам в освоении предмета и подготовке к ЕГЭ и ОГЭ. Чтобы успешно сдать нужные и поступить в высшее учебное заведение или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из разделов нашего сайта.
Чтобы успешно сдать нужные и поступить в высшее учебное заведение или техникум нужно использовать все инструменты: учеба, контрольные, олимпиады, онлайн-лекции, видеоуроки, сборники заданий.
Также вы можете воспользоваться другими материалами из разделов нашего сайта.
Публикация обновлена: 09.03.2023
Как подготовиться к ЕГЭ по химии — план
Подготовка к ЕГЭ по химии
Как проходит ЕГЭ по химии в 2023 году
На ЕГЭ по химии, как и в случае с большинством других предметов, ученик 11 класса должен будет справиться с 2 частями экзамена:
Чтобы решить все 34 задания единого государственного экзамена, у ученика будет 210 минут. За это время нужно будет успеть ответить на вопросы обеих частей, подготовить полное решение для задач 2-й части и перенести ответы в бланк.
Кстати, в отличие от ОГЭ, на ЕГЭ по химии не будет задания-эксперимента.
| Уровень сложности заданий на ЕГЭ по химии | |
|---|---|
| Базовая | 17 |
| Повышенная | 11 |
| Высокая | 6 |
Если вы хотите больше узнать об особенностях экзамена и подготовки к нему, советуем заглянуть в раздел «Демоверсии, спецификации, кодификаторы» сайта ФИПИ. Там вы найдете всю актуальную информацию о ЕГЭ по химии и методические рекомендации. Все это поможет распланировать подготовку к экзамену так, чтобы сдать его на 100 баллов.
Изменения в ЕГЭ по химии
По сравнению с 2022 годом экзамен по химии немного изменится. Вот список нововведений:
Немного поменялось условие задания 23, в котором нужно рассчитать концентрацию веществ.

Задания 33 и 34 поменялись местами.
Задания 9, 12 и 16 теперь станут повышенной сложности.
Полезные подарки для родителей
В колесе фортуны — гарантированные призы, которые помогут наладить учебный процесс и выстроить отношения с ребёнком!
Как хорошо сдать ЕГЭ по химии: разбор сложных задач
Как мы узнали из таблицы в предыдущем разделе, экзамен по химии — один из самых сложных. На 34 задания в нем приходится целых 11 повышенной сложности и 6 — высокой. Но если вы хотите поступить в вуз мечты, советуем научиться их решать так, чтобы не упустить ни одного балла. А потому предлагаем начать подготовку прямо сейчас и вместе разобрать несколько таких задач.
Задание 7
Это задание проверяет буквально все ваши знания в области неорганической химии.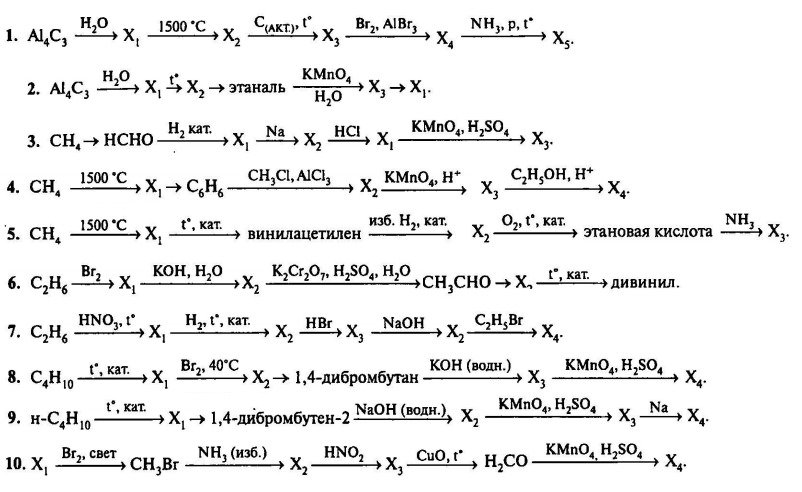 Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Здесь нужно знать как химические свойства простых соединений, так и химические свойства сложных соединений. Давайте разберем одно из таких заданий, чтобы понять, как их решать, чтобы сдать ЕГЭ по химии.
Установите соответствие между веществом и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Вещество | Реагенты |
|---|---|
| А) S | 1) AgNO3, K3PO4, Cl2 |
| Б) SO3 | 2) BaO, NaOH, H2O |
| В) Zn(OH)2 | 3) H2, Cl2, O2 |
| Г) ZnBr2 | 4) HBr, LiOH, CH3COOH (p-p) |
| 5) H3PO4 (p-p), BaCl2, CuO |
Решение:
Вариант под буквой А — простое вещество, сера.
 Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.Вещество под буквой Б — кислотный оксид. Кислотные оксиды не реагируют с кислотами, поэтому смело вычеркиваем варианты, где присутствует хоть одна кислота. Остаются варианты № 1–3. Реагенты под цифрой 3 тоже можем вычеркнуть, так как кислотный оксид уже в своей максимальной степени окисления и дальше взаимодействовать с кислородом не может. Остаются варианты № 1 и № 2. Оксид серы (VI) может реагировать с основным оксидом с образованием соли, со щелочью с образованием соли и воды, и с водой, при этом образуя кислоту. Выбираем № 2.
Амфотерный нерастворимый в воде гидроксид цинка может взаимодействовать только с теми, что способны его растворить. Единственно верный вариант под № 4, где указаны кислоты и щелочь.
При взаимодействии соли с другими сложными веществами надо помнить про три признака протекания химической реакции: выпадения осадка, выделение газа и образование малодиссоциирующего вещества — воды.
 Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Ответ: 3241.
Задание 15
Это задание Единого государственного экзамена проверит ваши знания химических свойств органических соединений. Чтобы справиться с ним, нужно по записанным словами реагирующим веществам составить уравнение реакции и выбрать из перечня один из получившихся продуктов. Давайте рассмотрим на примере, как решать такую задачу.
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| Реагирующие вещества | Продукт взаимодействия |
|---|---|
| А) уксусная кислота и сульфид калия | пропионат калия |
| Б) муравьиная кислота и гидроксид калия | этилат калия |
| В) муравьиный альдегид и гидроксид меди (II) при нагревании | формиат меди (II) |
| Г) этанол и калий | формиат калия |
| ацетат калия | |
| углекислый газ |
Решение:
Органические кислоты могут реагировать с солями, если те имеют летучий анион.
 В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.Муравьиная кислота проявляет свойства неорганической кислоты и может взаимодействовать с щелочами с образованием соли и воды. Соль муравьиной кислоты — формиат. Правильный ответ № 4.
Под буквой В описана качественная реакция на альдегиды с образованием соответствующей кислоты, оксида меди (I) и воды. Исключение — муравьиный альдегид. Он окисляется до углекислого газа, а остальные продукты реакции те же. Соответственно, правильный ответ № 6.
Калий как активный металл может замещать протон водорода в гидроксогруппе у спиртов с образованием алкоголята. Правильный ответ: № 2.
Ответ: 5462.
Задание 16
Это задание всё так же проверяет ваши знания по химическим свойствам и, как следствие, умение записывать превращения в рамках органической химии. Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Однако оно усложняется тем, что теперь вам самим нужно подобрать такой реактив, чтобы произошло уже известное превращение. Давайте попробуем решить один из вариантов такой задачи вместе — это повысит ваши шансы сдать ЕГЭ на 100 баллов.
Задана схема превращений веществ:
Определите, какие из указанных веществ являются веществами х и у:
2-бромбутан;
этаналь;
этен;
метилпропан;
хлорэтан.
Решение:
Посмотрим, что случилось с известными нам веществами.
У спирта исчезла ОН-группа, затем что-то произошло, и углеродная цепочка увеличилась вдвое. Мы помним, что когда цепочка увеличивается вдвое, то, скорее всего, это реакция Вюрца.
 А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.Бутан подвергают нагреванию с использованием катализатора. Нужно помнить, что в таких условиях проводится изомеризация алканов. Из бутана получается метилпропан. Ответ: № 4.
Ответ: 54.
Задание 26
Теперь разберем задачи, которые заканчивают тестовую часть ЕГЭ по химии. Рассмотрим условие одной из них на нахождение массы соли, которую необходимо добавить для получения раствора с новой заданной массовой долей.
Вычислите массу нитрата калия (в граммах), которую следует растворить в 160 г раствора с массовой долей этой соли 10% для получения раствора с массовой долей 12%. Ответ округлите до десятых.
Чтобы решить эту задачу, вспомним основную формулу нахождения массовой доли:
Найдем массу изначально растворенного нитрата калия в растворе, выразив из формулы выше:
подставим значения:
Чтобы увеличить массовую долю соли в растворе, необходимо ее добавить еще.
 Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:Далее в дело вступает чистая математика. Разделим обе части уравнения на 100%:
По пропорции перемножим крест-накрест:
0,12 * (160 + X) = 16 + X.
Раскроем скобки:
19,2 + 0,12Х = 16 + Х.
Приведем подобные: с Х в одну сторону, без Х — в другую:
3,2 = 0,88Х.
Найдем Х:
Масса нитрата калия, которую необходимо добавить для увеличения массовой доли раствора до 12%, равна 3,6 граммам.
Ответ: 3,6.
Задание 28
Эта задача может встретиться на экзамене в нескольких вариантах. Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
Давайте разберем один из них — задание на нахождение доли выхода продукта реакции.
В результате реакции тримеризации ацетилена объемом 26,88 л (н.у) получили 24,96 г бензола. Вычислите массовую долю выхода продукта реакции от теоретически возможного.
Решение:
Для начала напишем формулу, по которой считается доля выхода продукта:
Как определить, какая масса практическая, а какая — теоретическая? Значения, которые даются после слова «получили», — это практическая масса. Та, которая получилась в результате проведения химической реакции в реальных условиях. Масса теоретическая — та, которую рассчитывают из уравнения реакции, зная массу исходных реагентов.
Напишем уравнение химической реакции тримеризации ацетилена:
Найдем количество вещества ацетилена:
подставим значения:
Перейдем на количество вещества бензола, получаемого из ацетилена:
Зная количество вещества бензола, найдем его массу:
подставим значения:
m = 0,4 * 78 = 31,2 грамма.

Масса, рассчитываемая по уравнению реакции, является теоретической. Масса практическая дана нам по условию. Подставим полученные данные по массам в формулу для нахождения доли выхода продукта реакции:
Доля выхода бензола из данного объема ацетилена составляет 80%.
Ответ: 80.
Как оценивают готовые работы на ЕГЭ по химии
1-я часть
В 1-й части Единого государственного экзамена по химии задания 1–5, 9–13, 16–21, 25–28 оценивают 1 баллом, если вы запишете верный ответ по эталону. При этом в заданиях 1, 3, 4, 11, 12, 13, 17 и 18 ответ — это ряд цифр. То, в каком порядке вы их запишете, не влияет на оценку. Например, если в задании верны варианты под номерами 1 и 4, их можно записать как 14 или как 41. И в обоих случаях ответ засчитают как верный.
За правильные ответы в заданиях 6, 7, 8, 14, 15, 22, 23 и 24 можно получить по 2 балла. Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
Если ваш ответ отличается от эталона на один символ, его оценят в 1 балл. Во всех остальных случаях задание считают выполненным неверно и ставят 0 баллов.
2-я часть
В этой части нужно записать не только ответ, но и решение. А значит, и оценивать такие задания будут сразу по нескольким критериям. Зато за верный ответ в некоторых вопросах можно получить больше баллов, чем за любое задание 1-й части. Максимум — 5 баллов. А теперь давайте разберемся, как именно их будут оценивать.
| Задание № 29 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества и записал уравнение химической реакции, составил электронный баланс, указал окислитель и восстановитель | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 30 | Баллы |
|---|---|
| Ответ верный и полный: ученик выбрал вещества, записал все нужные уравнения реакции | 2 |
| Есть только один верный элемент ответа | 1 |
| Все элементы ответа записаны неверно | 0 |
| Максимальный балл | 2 |
| Задание № 31 | Баллы |
|---|---|
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 4 |
| Задание № 32 | Баллы |
|---|---|
| Правильно записаны 5 уравнений реакции | 5 |
| Правильно записаны 4 уравнения реакции | 4 |
| Правильно записаны 3 уравнения реакции | 3 |
| Правильно записаны 2 уравнения реакции | 2 |
| Правильно записано 1 уравнение реакции | 1 |
| Все уравнения реакции записаны неверно | 0 |
| Максимальный балл | 5 |
| Задание № 33 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 3 элемента | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 3 |
| Задание № 34 | Баллы |
|---|---|
| Ответ верный и полный, записаны все 4 элемента | 4 |
| Правильно записаны только 3 элемента ответа | 3 |
| Правильно записаны только 2 элемента ответа | 2 |
| Правильно записан только 1 элемент ответа | 1 |
| Все элемента ответа записаны неверно | 0 |
| Максимальный балл | 4 |
Как сдать ЕГЭ по химии на 3, 4 и 5
Мы уже познакомились с критериями, по которым будут оценивать работы на ЕГЭ. А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
А теперь давайте разберемся, сколько баллов нужно получить для оценок 3, 4 или 5. Официально ЕГЭ не оценивают по пятибалльной системе с 2008 года. Если вам так проще оценить свои знания, их можно перевести. Но это будет лишь примерный перевод.
Будьте внимательны: баллы из таблиц выше — первичные, а требования к абитуриентам на поступление выражены в тестовых. Чтобы понять, сколько заданий точно нужно решить, чтобы поступить, надо перевести баллы из одной системы в другую. Это можно сделать по таблице ниже.
| Первичные баллы | Тестовые баллы | Оценка |
|---|---|---|
| <11 | <36 | 2 |
| 11–25 | 36–55 | 3 |
| 26–38 | 56–72 | 4 |
| 39–56 | 73–100 | 5 |
6 рекомендаций, как подготовиться к ЕГЭ по химии
Единый государственный экзамен — это ответственная задача, от результатов подготовки к которой иногда многое зависит. Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
Чтобы немного облегчить для вас этот путь, мы собрали 6 простых, но рабочих советов от наших преподавателей. Следуйте им и тогда сможете подготовиться к экзамену по химии как можно лучше.
Узнайте все о структуре ЕГЭ и научитесь работать с КИМами.
Начинайте готовиться заранее. Но если получилось так, что осталось мало времени, составьте новый экспресс-план с помощью вашего преподавателя.
Ведите календарь подготовки к экзамену. Отмечайте на нем запланированные темы, разные методики, занятия у репетитора, пробные ЕГЭ и самоподготовку.
Распределяйте время на темы, исходя из ваших знаний. Больше учите то, что «западает», остальное — повторяйте.
Советуйтесь с учителем. Это может быть ваш преподаватель по химии или репетитор. Круто, если он сможет поделиться с вами опытом подготовки к ЕГЭ.

Заботьтесь о своем здоровье, не забывайте отдыхать, не лишайте себя живого общения. Все это может сказаться на вашем самочувствии, а значит, и баллах тоже.
Если вы хотите сдать ЕГЭ по химии на 100 баллов, советуем тщательно продумать, как вы будете готовиться к нему. Лучший из них — совмещать самостоятельную работу и дополнительные занятия.
На курсах подготовки к ЕГЭ по химии в Skysmart школьники отрабатывают все типы задач и разбирают критерии оценок. Для каждого из них мы составляем индивидуальный план, который приведет к нужным баллам. Он учитывает уровень знаний ученика и время до экзамена, что позволяет «выжать» максимум из подготовки. А еще мы рассказываем о ЕГЭ без «страшилок» и прикрас, чтобы школьник точно знал, что его ждет на экзамене. Ждем на первом бесплатном занятии!
Полное руководство по экзамену AP по химии
Тимоти Пек 9 AP Guides,Standardized Tests
Экзамен AP по химии является одним из наиболее распространенных экзаменов, сдаваемых как самостоятельными, так и зачисленными студентами. В 2019 году примерно 150 000 из более чем 5 миллионов студентов, сдавших экзамены AP, сдали экзамен AP по химии. Если вы заинтересованы в сдаче экзамена AP Chemistry, независимо от того, посещали ли вы класс или занимались самостоятельно, прочитайте разбивку теста и советы CollegeVine о том, как лучше всего подготовиться к нему.
Когда проводится экзамен по химии?
Экзамены AP 2020 были переведены на онлайн-экзамены из-за коронавируса. Узнайте об этих изменениях в нашем сообщении Как коронавирус влияет на экзамены AP ?
Об экзамене AP по химии
Курс AP по химии направлен на развитие ваших продвинутых навыков исследования и рассуждения, таких как разработка плана сбора данных, анализ данных, применение математических процедур и установление связей между понятиями в разных областях. Поскольку база научных знаний так быстро расширяется благодаря открытиям и исследованиям, курс AP Chemistry, как и AP Biology, фокусируется на вашем овладении устойчивыми концептуальными представлениями в этой области и конкретным содержанием, которое их поддерживает.
Поскольку база научных знаний так быстро расширяется благодаря открытиям и исследованиям, курс AP Chemistry, как и AP Biology, фокусируется на вашем овладении устойчивыми концептуальными представлениями в этой области и конкретным содержанием, которое их поддерживает.
Предпосылками для сдачи AP Chemistry являются алгебра II и общий курс химии в средней школе. Если вы не посещали эти курсы до поступления или самостоятельного обучения, вы вряд ли будете готовы к уровню мышления, необходимому для успешной сдачи экзамена AP по химии.
Экзамен AP Chemistry состоит из двух основных компонентов: научная практика и содержание курса. Научная практика — это навыки, необходимые для того, чтобы мыслить как химик, в то время как содержание курса охватывает абстрактные понятия или темы, которые являются основой курса. Содержание курса далее разбито на «Большие идеи».
Экзамен AP по химии состоит из шести научных практик:
| Навыки | Описание | Процент от Оценка за экзамен (раздел с несколькими вариантами ответов) | Процент от Экзаменационный балл (раздел свободного ответа) |
| Модели и изображения | Описать модели и представления, в том числе в разных масштабах | 8%-12% | 2%–4% |
| Вопрос и метод | Определение научных вопросов и методов | 8%-12% | 10%-16% |
| Представление данных и явлений | Создание представлений или моделей химических явления | 8%-16% | |
| Анализ модели | Анализировать и интерпретировать модели и представления на по одной шкале или по нескольким шкалам | 23%-30% | 23%-30% |
| Математические процедуры | Решение задач с использованием математических соотношений | 35%-42% | 43%53% |
| Аргументация | Разработайте объяснение или научный аргумент | 8%-12% | 15%-24% |
Экзамен AP Chemistry включает четыре основные идеи:
| Навык | Описание |
| Масштаб, пропорции и количество | Понимание значения макроскопического и атомарного масштаба, а также отношения между величинами в одном масштабе и в разных масштабах |
| Структура и свойства | Использование наблюдаемых свойств для вывода об аспектах структуры и взаимодействий атомов и молекул |
| Трансформации | Понимание деталей трансформаций, происходящих как на акроскопическом, так и на атомарном уровне |
| Энергия | Роль энергетики в характеристике и контроле химических систем |
Во время сдачи экзамена AP по химии вы можете использовать научный калькулятор только в разделе бесплатных ответов. Вам также будет предоставлен список уравнений и формул и копия периодической таблицы. Полный список рекомендаций по использованию калькуляторов и приемлемых моделей можно найти в Правилах использования калькуляторов College Board. Копию списка уравнений и формул, представленных на экзамене, можно найти в приложении к официальному курсу AP Chemistry и описанию экзамена.
Вам также будет предоставлен список уравнений и формул и копия периодической таблицы. Полный список рекомендаций по использованию калькуляторов и приемлемых моделей можно найти в Правилах использования калькуляторов College Board. Копию списка уравнений и формул, представленных на экзамене, можно найти в приложении к официальному курсу AP Chemistry и описанию экзамена.
Содержание курса AP Chemistry
Курс AP Chemistry состоит из девяти разделов. Ниже приведена рекомендуемая последовательность блоков из College Board, а также процентное соотношение каждого блока в разделе с несколькими вариантами ответов экзамена AP по химии.
| Химический блок AP | Описание | Процент баллов за экзамен (раздел с несколькими вариантами ответов) |
| Атомная структура и свойства | Узнайте о составе атомов и о том, как ученые измеряют и классифицируют эти молекулярные строительные блоки | 7%–9% |
| Молекулярная и ионная структура соединения и свойства | Откройте для себя диапазон химических связей и то, как их структура может влиять на свойства созданных молекул | 7%–9% |
| Межмолекулярные силы и свойства | Узнайте, как атомы объединяются для создания твердых тел, жидкостей и газов, и как субатомные силы управляют свойствами всего вокруг вас | 18%–22% |
| Химические реакции | Узнайте, как различать физические и химические процессы, а также как измерять и выражать химические реакции с помощью химических уравнений | 7%–9% |
| Кинетика | Изучение различных методов наблюдения за изменениями, происходящими во время химической реакции, и за эффектами ряда реакций | 7%–9% |
| Термодинамика | Узнайте об изменениях энергии в химических реакциях и о том, как передача энергии может изменить физические свойства вещества | 7%–9% |
| Принципы равновесия | Изобразите, как химические реакции изменяются с течением времени, что заставляет вещества достигать равновесия и как системы реагируют, когда это равновесие нарушается | 7%–9% |
| Кислоты и основания | Узнайте больше о pH, качествах и свойствах кислот и оснований, а также о том, как они взаимодействуют в химических реакциях | 11%–15% |
| Приложения термодинамики | Введение в концепцию «термодинамической благоприятности» реакций, что означает вероятность их протекания с учетом изменения энергии и факторов окружающей среды | 7%–9% |
Содержание экзамена по химии AP
Экзамен AP по химии — один из самых продолжительных экзаменов AP, его продолжительность составляет три часа пятнадцать минут. Он состоит из двух разделов: первый раздел содержит вопросы с несколькими вариантами ответов, а второй раздел состоит из вопросов со свободным ответом.
Он состоит из двух разделов: первый раздел содержит вопросы с несколькими вариантами ответов, а второй раздел состоит из вопросов со свободным ответом.
Раздел 1. Множественный выбор
1 час 30 минут | 60 вопросов | 50% баллов
Первый раздел экзамена AP по химии содержит 60 вопросов с несколькими вариантами ответов — как в наборах, так и по отдельности — которые у вас есть 90 минут на ответ. Чтобы получить высокие баллы за этот раздел экзамена, учащиеся должны уметь:
- Объяснять, анализировать и интерпретировать модели и представления химических свойств или явлений
- Разработка экспериментов и процедур для проверки прогноза или теории
- Использование математических отношений для решения задач
- Использовать доказательства и/или рассуждения, чтобы сделать или обосновать научное утверждение и поддержать его
Пример отдельного вопроса с несколькими вариантами ответов:
Ответ: C
Образец набора вопросов с несколькими выборами:
Ответы-7: B, 8: D
Раздел 2: бесплатный ответ
1 час 45 минуты | 7 вопросов | 50% баллов
Раздел экзамена AP по химии со свободными ответами состоит из трех длинных эссе (каждое оценивается в 10 баллов) и четырех кратких ответов (каждое оценивается в четыре балла). Вам разрешено использовать научный или графический калькулятор на протяжении всей части экзамена, где можно дать свободный ответ. (Калькулятор с четырьмя функциями разрешен, но не рекомендуется.) Вы сами должны планировать свое время на этот раздел, так как инспектор напомнит вам об оставшемся времени, но не будет заставлять вас переходить к следующему вопросу в любая точка.
Вам разрешено использовать научный или графический калькулятор на протяжении всей части экзамена, где можно дать свободный ответ. (Калькулятор с четырьмя функциями разрешен, но не рекомендуется.) Вы сами должны планировать свое время на этот раздел, так как инспектор напомнит вам об оставшемся времени, но не будет заставлять вас переходить к следующему вопросу в любая точка.
Пример длинного вопроса эссе:
Пример вопроса о коротком ответе:
AP Chemistry Distribution, средний балл и скорость прохождения

 Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3.
Как правило, простые вещества взаимодействуют с другими простыми веществами, значительно реже со сложными веществами. Под это описание подходит вариант № 3. Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей.
Под это описание подходит вариант под № 1. Но как же хлор? Дело в том, что вышестоящие в группе галогены способны вытеснить нижестоящие из их солей. В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5.
В результате взаимодействия образуется соль уксусной кислоты и сероводород (летучее соединение). Соль, которая образована в таких условиях, — ацетат калия. Это вещество № 5. А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено.
А в неё вступают только галогеналканы. Ищем нужный нам вариант. Он находится под номером 5. Первое вещество найдено. Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:
Но мы не знаем сколько, поэтому примем массу добавляемой соли за Х и подставим в исходную формулу нахождения массовой доли с учетом новых значений:

 В 2019 году 55,6% учащихся, сдавших экзамен AP Chemistry, получили оценку 3 и выше. Из них только 11,5% студентов получили наивысший балл 5, а еще 16,6% получили 4 балла. Чуть более четверти всех испытуемых получили 3 балла, что в значительной степени способствовало успешной сдаче экзамена. Примерно четверть студентов получили на экзамене 2 балла, а 21,4% испытуемых набрали 1 балл.
В 2019 году 55,6% учащихся, сдавших экзамен AP Chemistry, получили оценку 3 и выше. Из них только 11,5% студентов получили наивысший балл 5, а еще 16,6% получили 4 балла. Чуть более четверти всех испытуемых получили 3 балла, что в значительной степени способствовало успешной сдаче экзамена. Примерно четверть студентов получили на экзамене 2 балла, а 21,4% испытуемых набрали 1 балл.

 Принстонское обозрение Cracking the AP Chemistry Exam, 2020 Premium Edition: 5 практических тестов + полный обзор содержания содержит подробное руководство по экзамену, хотя его иногда критикуют за длинные описания содержания. Другим хорошим выбором является ускоренный курс по химии AP, для экзамена 2020 года, книга + онлайн: получите более высокий балл за меньшее время (ускоренный курс Advanced Placement (AP)), третье издание , который содержит более краткое изложение содержания и часто хвалят за конкретные советы по учебе.
Принстонское обозрение Cracking the AP Chemistry Exam, 2020 Premium Edition: 5 практических тестов + полный обзор содержания содержит подробное руководство по экзамену, хотя его иногда критикуют за длинные описания содержания. Другим хорошим выбором является ускоренный курс по химии AP, для экзамена 2020 года, книга + онлайн: получите более высокий балл за меньшее время (ускоренный курс Advanced Placement (AP)), третье издание , который содержит более краткое изложение содержания и часто хвалят за конкретные советы по учебе. Обязательно прочитайте отзывы, прежде чем выбрать один из них — их качество сильно различается. У Varsity Tutors есть приложение AP Chemistry, которое получило высокую оценку.
Обязательно прочитайте отзывы, прежде чем выбрать один из них — их качество сильно различается. У Varsity Tutors есть приложение AP Chemistry, которое получило высокую оценку.
 Подчеркните каждую часть вопроса, обведите глагол задачи и отмечайте их по мере написания. Многие студенты теряют баллы, просто забывая включить одну часть вопроса, состоящего из нескольких частей.
Подчеркните каждую часть вопроса, обведите глагол задачи и отмечайте их по мере написания. Многие студенты теряют баллы, просто забывая включить одну часть вопроса, состоящего из нескольких частей.
 Зарегистрируйтесь сегодня в своей учетной записи CollegeVine и получите преимущество в своем путешествии в колледж!
Зарегистрируйтесь сегодня в своей учетной записи CollegeVine и получите преимущество в своем путешествии в колледж!  На обоих участках у вас будет доступ к периодической таблице элементов, а также к диаграмме, в которой перечислены любые формулы и константы, которые могут вам понадобиться для ваших расчетов.
На обоих участках у вас будет доступ к периодической таблице элементов, а также к диаграмме, в которой перечислены любые формулы и константы, которые могут вам понадобиться для ваших расчетов.
Leave A Comment