Хлоруксусной кислоты глицин
Какую массу глицина можно получить из 200г технической хлоруксусной кислоты, содержащей 2% примесей?
Сколько грамм глицина можно получить из 160г хлоруксусной кислоты
Реакция: Ch3Cl-COOH + Nh4 = HCl + Ch3(Nh3)-COOH
n(Ch3Cl-COOH) = m/M = 160 г/94,5 г/моль = 1,69 моль
m(глиц.) теор = n*M = 1,69 моль*75 г/моль = 127 г
m(глиц) практ = m(теор) *B = 127 г*0,65 = 82,5 г
Уксусный альдегид уксусная кислота хлоруксусная. Аминоуксусная кислота солянокислый глицин соль . Бутан этан хлорэтан бутан изобутан.
Решить цепочку C-Ch5-C2H6-C2h5-спирт-альдегид-кислота-хлоруксусная кислота-глицин
C + 2h3= Ch5
Ch5+Cl2=Ch4Cl+HCl
Ch4Cl+2Na+ClCh4=C2H6+2NaCl
C2H6= C2h5+h3
C2h5+h3O= C2H5OH + Q
C2H5OH + CuO = Ch4COH +h3O + Cu
Ch4COH + [O] —-> Ch4COOH
Ch4COOH + Cl2 = Ch3ClCOOH
хз)
Синтезируют ГЛИЦИН из хлоруксусной кислоты и Nh4. В спектре ЯМР в D2О химический сдвиг протонов группы СН2 составляет 3,55 м. д. Внутр. соль ГЛИЦИН называют бетаином.
д. Внутр. соль ГЛИЦИН называют бетаином.
Как из хлоруксусной кислоты получить глицин?Подскажите пожалуйста формулу))
Проще синтезировать его из мыла
Установленные закономерности изменения диэлектрических характеристик водных растворов хлоруксусной кислоты и глицина в зависимости от состава.
Из 90г хлоруксусной кислоты получили 40г глицина. Каков выход продукта?
4/9
Как из уксусной кислоты получить глицин?. Оценка рыночной стоимости недвижимогокачестве медикаменты глицин реакция получения глицина из хлоруксусной кислоты?
Уксусная кислота >хлоруксусная кислота >глицин
C2H5OH- А — Б — В — Г. Что В и какие идут реакцит? Заранее спасибо.
Этанол ->А этаналь-> Б уксусная или этановая кислота-> В хлоруксусная кислота->Г аминоуксусная или глицин
Получают необходимо соединение в промышленных масштабах в результате взаимодействия хлоруксусной кислоты с аммиаком. В сфере производства продуктов питания глицин…
Глицин+соляная кислота, Аланин +гидроксид натрия, хлоруксусная кислота+аммиак
Химия
Http://www. interneturok.ru/
interneturok.ru/
СПОСОБ ПОЛУЧЕНИЯ ГЛИЦИНА аммонолизом монохлоруксусной кислоты при 40 — 70oС в присутствии гексаметилентетрамина в среде метанола, содержащего 10% воды…
2) С6Н12О6—>2С2Н5ОН + 2СО2 в присутствии фермента, как катализатора
3) бензол получается при дегидратации циклогексана
С6Н12 —->С6Н6 + 3Н2
Помогите пожалуйста составить уравнения реакций
Связи, конечно, потрясающие! Но я попроще предложу:
1) Ch4Ch4 + Cl2 (УФ-свет) = HCl + Ch4Ch3Cl (хлорэтан)
2) Сh4Ch3Cl + KOH = KCl + C3Ch3OH (этанол)
3) Сh4Ch3OH + CuO (t) = Cu + h3O + Ch4CHO (этаналь)
4) Ch4CHO + Ag2O (t) = 2Ag + Ch4COOH (уксусная кислота)
5) Ch4COOH + Сl2 (УФ-свет) = HCl + Ch3ClCOOH (хлоруксусная кислота)
6) Ch3ClCOOH + Nh4 = HCl + Nh3Ch3COOH (аминоуксусная кислота, или глицин)
7) 2Nh3Ch3COOH ——> Nh3Ch3CO-NHCh3COOH (дипептид, глицилглицин)
Синтезируют глицин из хлоруксусной кислоты и Nh4. Глицин входит в состав многих белков и биологически активных соединений.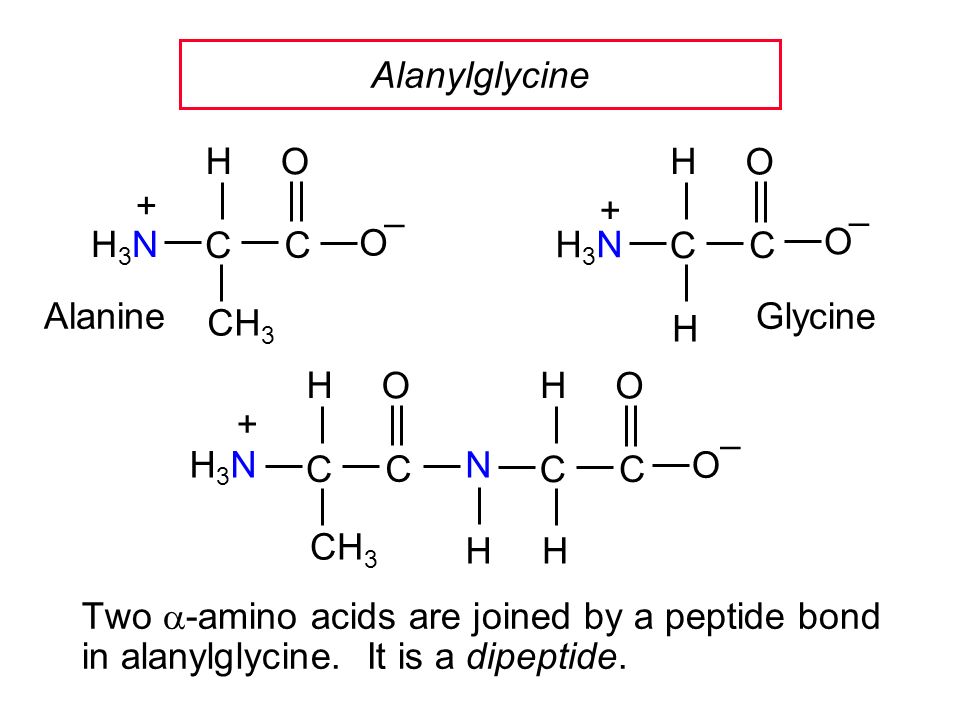
Помогите пож) как из этилена получить аминоуксусную кислоту? реакцию надо)
Выпей его-и вся реакция внутри пройдет)) ) Хорошо)))
Глицин и его соли образуют комплексные соединения со многими неорганическими солями.Синтезируют глицин из хлоруксусной кислоты и Nh4.
Реакция хлоруксусной кислоты с аммиаком
Условия никакие не нужны, просто смотря какие реагенты и в каком виде прибавляете и какой продукт реакции нужно получить. Хлоруксусная к-та имеет два центра для реакции — хлор и карбоксильную кислотную группу… Если аммиак будете приливать в виде водного раствора (то есть в виде гидроксида), то работать будет карбоксильная группа и получаться в качестве продукта реакции хлорацетат аммония:
Cl-Ch3-COOH+Nh5OH = Cl-Ch3-COONh5+h3O
Для того чтобы заставить работать другой центр к-ты — хлор и получить аминоуксусную к-ту (глицин), то кристаллическую хлоруксусную к-ту растворяют в безводном инертном растворителе (типа этанола, ацетонитрила, формамида, диметилацетамида) и пропускают через этот раствор сухой аммиак в виде газа из баллона.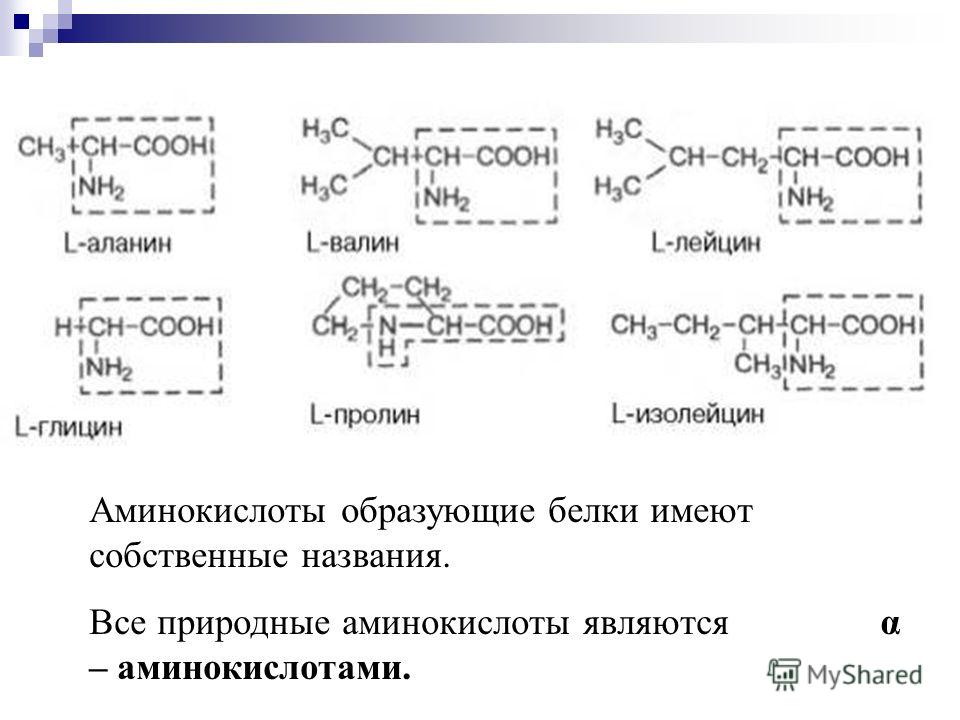 .. В качестве катализатора полезно добавить несколько капель триэтиламина в качестве акцептора HCl и реакция уже идет:
.. В качестве катализатора полезно добавить несколько капель триэтиламина в качестве акцептора HCl и реакция уже идет:
ClCh3COOH + Nh4 = Nh3Ch3COOH+HCl
Р-ция хлоруксусной монохлоруксусной кислоты с анилином — пром. метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин Ch4NHCh3COONa…
А какая кислота сильнее?) какая кислота сильнее? Уксусная, хлороуксусная, аминоуксусная или бромоуксусная?)
Вопрос химикам….пожалуйста, помогите!!!!
A — Ch3ClCOOH, хлорэтановая кислота, B — Ch3Nh3COOH, аминоуксусная или глицин, C — Nh5ClCh3COOH — соляно-кислый глицин, не знаю ка назвать по-другому.
Хлорирование прекращают, когда проба сырой хлоруксусной кислоты будет.Реакцией с аммиаком получают глицин, с метиламином — саркозин
Оба правы
Подскажите пожалуйста,как из хлоруксусной кис-ты получить аминоуксусную?
С аммиаком зафигачь и получишь аминоуксусную к-ту и хлороводород.
Как Глицин, Glycine and its sodium salt, Аминоуксусная кислота, Iconyl, АминоэтановаяНо также его можно получать химически путем взаимодействия хлоруксусной кислоты с.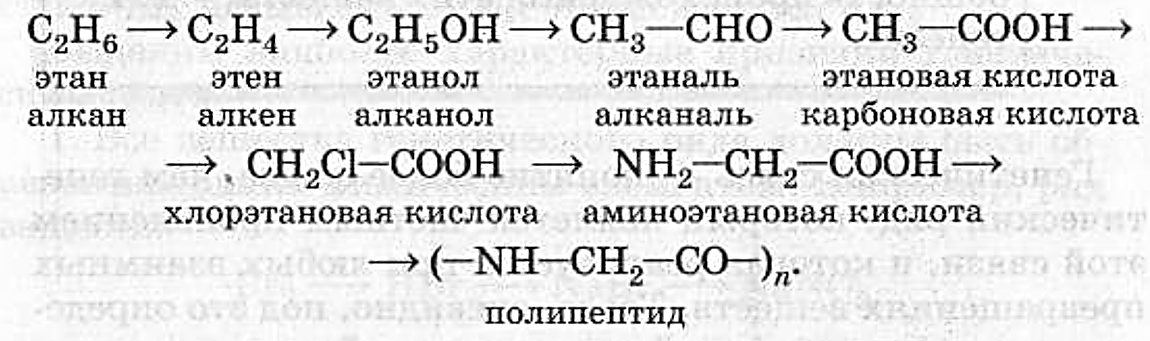 ..
..
При взаимодействии с аммиаком происходят такие реакции:
ClCh3COOH + Nh4 ——> ClCh3COONh5,
ClCh3COONh5 + 2 Nh4 ——> h3NCh3COONh5 + Nh5Cl,
Подкислением полученного раствора глицината аммония можно получить глицин (аминоуксусную кислоту) :
h3NCh3COONh5 + HCl ——> h3NCh3COOH + Nh5Cl.
Как получить глицин (распишите по-понятнее я же школота)?
В аптеке продается.
Получают необходимо соединение в промышленных масштабах в результате взаимодействия хлоруксусной кислоты с аммиаком. В сфере производства продуктов питания глицин…
Реакцией хлоруксусной кислоты с аммиаком.
Как из хлорэтановой кислоты получить аланин?
Вообще, получают из альфахлопропионовой кислоты. (1-хлорэпропановой) Вы не ошиблись?
Расчет реакции получения аминоуксусной кислоты из хлоруксусной кислоты.Глицин аминоуксусная кислота, аминоэтановая кислота простейшая алифатическая.
Да легко вааааааааришь варишь а потом в -50с градусов потом ещё 15 на +100повари
Этановая кислота — это, вроде, уксусная.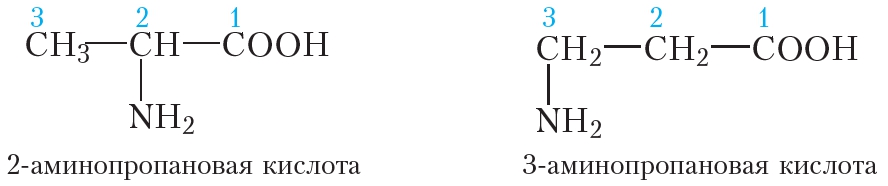 Из хлоруксусной легко получается аминоуксусная (гликокол, глицин). Можно, конечно, и углеродную цепь наращивать, но это представляет чисто теоретический интерес.
Из хлоруксусной легко получается аминоуксусная (гликокол, глицин). Можно, конечно, и углеродную цепь наращивать, но это представляет чисто теоретический интерес.
При синтетическим получении аланина Вы столкнетесь с проблемой рацемизации: природный аланин — L-изомер, в результате синтеза Вы почти наверняка получите рацемат — симесь равных количеств D- и L-изомеров. Разделение оптических изомеров (обычно с использованием ферментов) — задача вполне разрешимая, но не тривиальная.
Весь вопрос — для чего Вам аланин понадобился? Его, причем оптически активный (L-изомер), не проблема приобрести готовый — в промышленности, насколько я знаю, его получают микробиологическим путем, а для продуктов биологического происхождения проблема оптической активности не возникает.
Реакция получения глицина из уксусной кислоты
Напишите уравнения реакций получения глицина из этилена.
Получение глицерина из карбоната кальция Получить из карбоната кальция: а) глицин б) тротил в) фенолят калия
Гг
Хлоруксусные кислоты — типичные представители галогенкарбоновых кислот.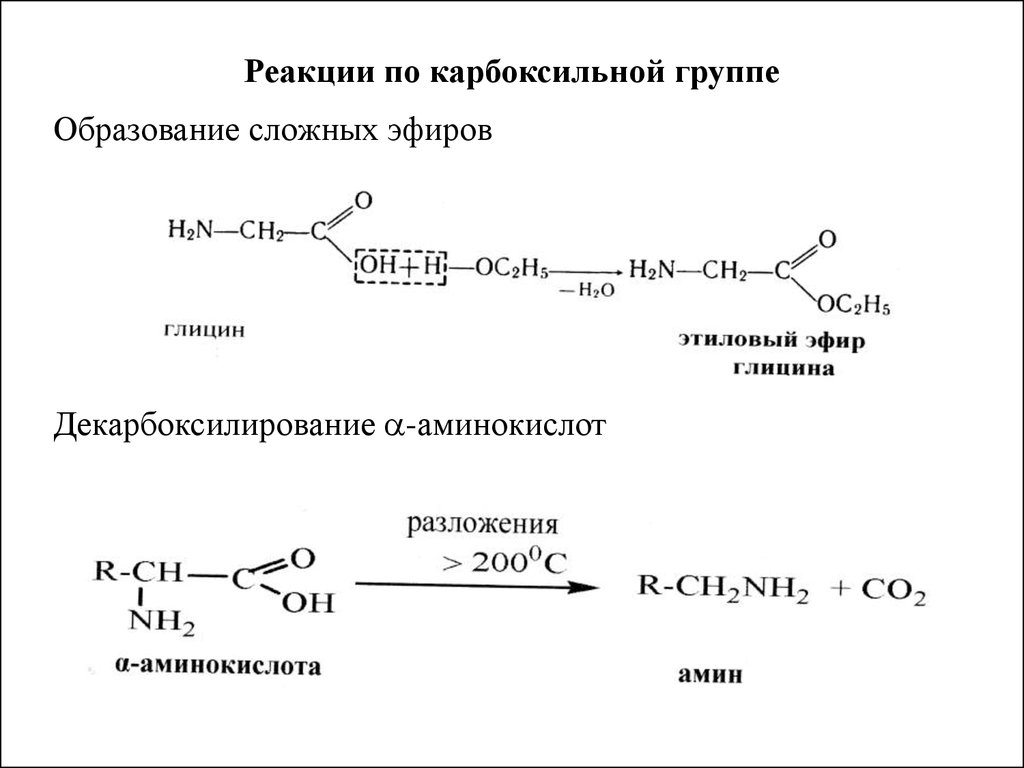 с анилином — пром. метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин…
с анилином — пром. метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин…
Как из этанола получить глицин? напишите уравнение пжл!!!
Химики, помогите….
Ch4COOH + CI2 = Ch4COOCI + HCI
(A)
Ch4COOCI + Nh4 = Ch4CONh3 + HCI + h3O
(B)
Ch4CONh3 + HCI = Ch4COCI + Nh4 + h3!
(C)
ТЫ ИХ ТОКА УРОВНЯЙ! А ТО, голову ломать не о4 охото.
Кислоту аминоуксусную кислоту, глицин следующим путем при присоединении к этилену воды вПри взаимодействии уксусной кислоты с хлором образуется хлоруксусная кислота
А теперь как будет на самом деле :
Ch4COOH + Cl2 == ClCh3COOH ( это хлоруксусная кислота ) + HCl
ClCh3COOH + 2Nh4 == h3NCh3COOH ( это аминоуксусная кислота, или глицин ) + Nh5Cl
h3NСh3COOH + HCl == [h4NCh3COOH]+ Cl- ( эта штуковина будет называться хлорид карбоксиметиламмония )
Получение глицина хлоруксусной кислоты
Какую массу глицина можно получить из 200г технической хлоруксусной кислоты, содержащей 2% примесей?
Сколько грамм глицина можно получить из 160г хлоруксусной кислоты
Реакция: Ch3Cl-COOH + Nh4 = HCl + Ch3(Nh3)-COOH
n(Ch3Cl-COOH) = m/M = 160 г/94,5 г/моль = 1,69 моль
m(глиц.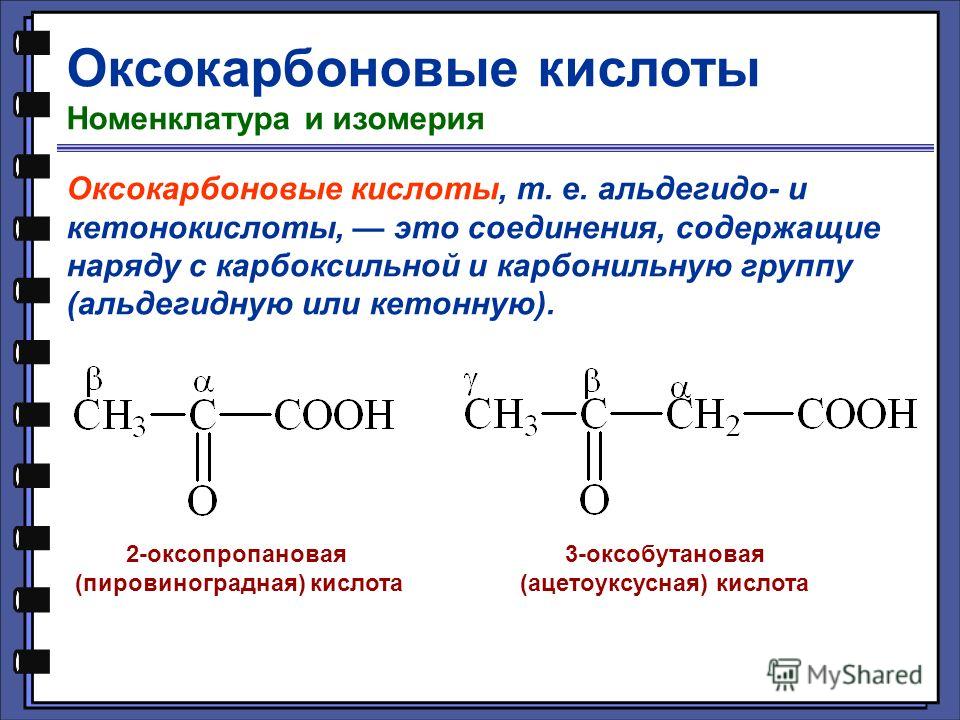 ) теор = n*M = 1,69 моль*75 г/моль = 127 г
) теор = n*M = 1,69 моль*75 г/моль = 127 г
m(глиц) практ = m(теор) *B = 127 г*0,65 = 82,5 г
Хлоруксусные кислоты — типичные представители галогенкарбоновых кислот.Р-ция С1СН2СООН с анилином — пром. метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин Ch4NHCh3COONa, с щелочной целлюлозой…
Решить цепочку C-Ch5-C2H6-C2h5-спирт-альдегид-кислота-хлоруксусная кислота-глицин
C + 2h3= Ch5
Ch5+Cl2=Ch4Cl+HCl
Ch4Cl+2Na+ClCh4=C2H6+2NaCl
C2H6= C2h5+h3
C2h5+h3O= C2H5OH + Q
C2H5OH + CuO = Ch4COH +h3O + Cu
Ch4COH + [O] —-> Ch4COOH
Ch4COOH + Cl2 = Ch3ClCOOH
хз)
Хлоруксусные кислоты — типичные представители галогенкарбоновых кислот.Р-ция С1СН2СООН с анилином — пром. метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин Ch4NHCh3COONa, с щелочной целлюлозой…
Реакция получения глицина из уксусной кислоты
Как из хлоруксусной кислоты получить глицин?Подскажите пожалуйста формулу))
Проще синтезировать его из мыла
Р-ция С1СН2СООН с анилином — пром.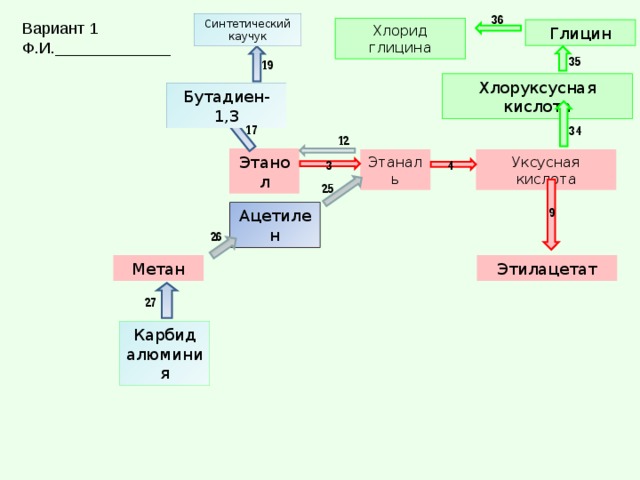 метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин Ch4NHCh3COONa, с щелочной целлюлозойТабл. 2. — СВОЙСТВА НЕКОТОРЫХ ПРОИЗВОДНЫХ ХЛОРУКСУСНЫХ КИСЛОТ.
метод получения индиго, р-цией с Nh4 получают глицин, с метиламином — саркозин Ch4NHCh3COONa, с щелочной целлюлозойТабл. 2. — СВОЙСТВА НЕКОТОРЫХ ПРОИЗВОДНЫХ ХЛОРУКСУСНЫХ КИСЛОТ.
Из 90г хлоруксусной кислоты получили 40г глицина. Каков выход продукта?
4/9
Аминоуксусная кислота, хлоруксусная кислота, аммиак, уксусный альдегид.Одноосновные карбоновые кислоты. Интерактивные задачи по химии. Кислородсодержащие органические соединения.
Уксусная кислота >хлоруксусная кислота >глицин
C2H5OH- А — Б — В — Г. Что В и какие идут реакцит? Заранее спасибо.
Этанол ->А этаналь-> Б уксусная или этановая кислота-> В хлоруксусная кислота->Г аминоуксусная или глицин
Получение уксусной кислоты из этанола осуществляют, окисляя его кислородом.Третий этап взаимодействие хлоруксусной кислоты с аммиаком. Ch3ClCOOH 2Nh4 Nh3 Ch3COOH Nh5Cl.
Химия
Http://www.interneturok.ru/
Из 45 г уксусной кислоты была получена хлоруксусная кислота, которая затем была превращена в аминоуксусную.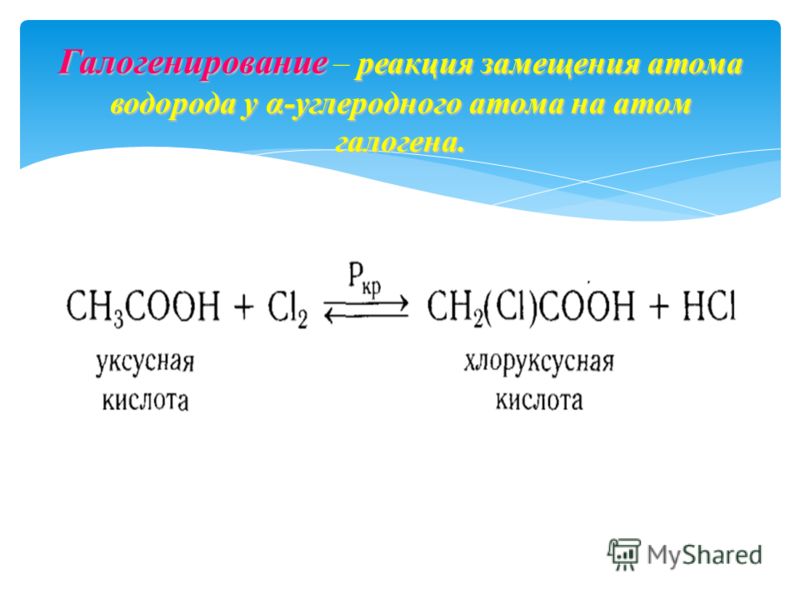 Глицин аминоуксусная кислота, аминоэтановая кислота простейшая алифатическая. 1 получение 2 биологическая роль 3 в медицине 4 в…
Глицин аминоуксусная кислота, аминоэтановая кислота простейшая алифатическая. 1 получение 2 биологическая роль 3 в медицине 4 в…
2) С6Н12О6—>2С2Н5ОН + 2СО2 в присутствии фермента, как катализатора
3) бензол получается при дегидратации циклогексана
С6Н12 —->С6Н6 + 3Н2
Помогите пожалуйста составить уравнения реакций
Связи, конечно, потрясающие! Но я попроще предложу:
1) Ch4Ch4 + Cl2 (УФ-свет) = HCl + Ch4Ch3Cl (хлорэтан)
2) Сh4Ch3Cl + KOH = KCl + C3Ch3OH (этанол)
3) Сh4Ch3OH + CuO (t) = Cu + h3O + Ch4CHO (этаналь)
4) Ch4CHO + Ag2O (t) = 2Ag + Ch4COOH (уксусная кислота)
5) Ch4COOH + Сl2 (УФ-свет) = HCl + Ch3ClCOOH (хлоруксусная кислота)
6) Ch3ClCOOH + Nh4 = HCl + Nh3Ch3COOH (аминоуксусная кислота, или глицин)
7) 2Nh3Ch3COOH ——> Nh3Ch3CO-NHCh3COOH (дипептид, глицилглицин)
Аминоуксусная кислота реагирует с каждым из двух веществ HCl, KOH NaCl, Nh4 C2H5OH CO2, HNO3.Аминоуксусную кислоту можно получить в одну стадию из кислоты уксусной пропионовой 2-хлорпропионовой хлоруксусной.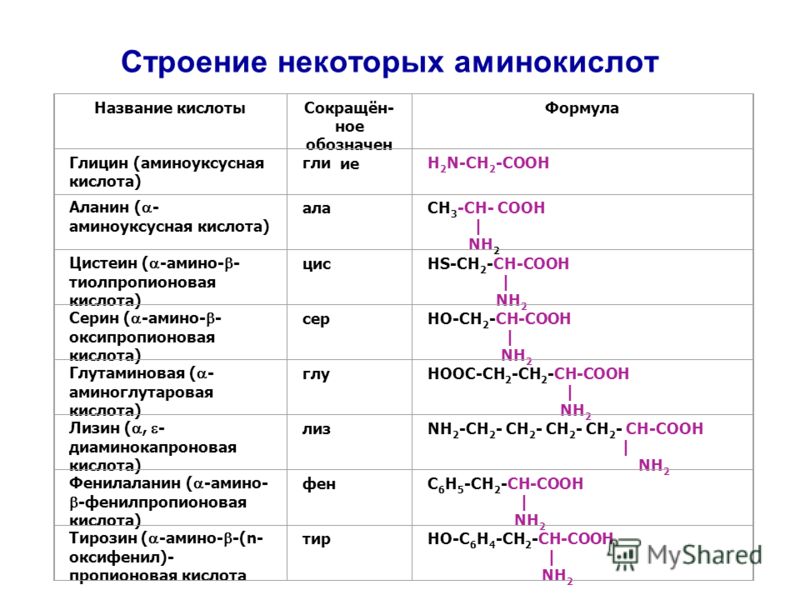
Помогите пож) как из этилена получить аминоуксусную кислоту? реакцию надо)
Выпей его-и вся реакция внутри пройдет)) ) Хорошо)))
Результаты измерений диэлектрических характеристик водных растворов хлоруксусной кислоты и глицина в широком интервале концентраций при температурах 20,40 и 60 С на частоте 6 ГГц
Реакция хлоруксусной кислоты с аммиаком
Условия никакие не нужны, просто смотря какие реагенты и в каком виде прибавляете и какой продукт реакции нужно получить. Хлоруксусная к-та имеет два центра для реакции — хлор и карбоксильную кислотную группу… Если аммиак будете приливать в виде водного раствора (то есть в виде гидроксида), то работать будет карбоксильная группа и получаться в качестве продукта реакции хлорацетат аммония:
Cl-Ch3-COOH+Nh5OH = Cl-Ch3-COONh5+h3O
Для того чтобы заставить работать другой центр к-ты — хлор и получить аминоуксусную к-ту (глицин), то кристаллическую хлоруксусную к-ту растворяют в безводном инертном растворителе (типа этанола, ацетонитрила, формамида, диметилацетамида) и пропускают через этот раствор сухой аммиак в виде газа из баллона.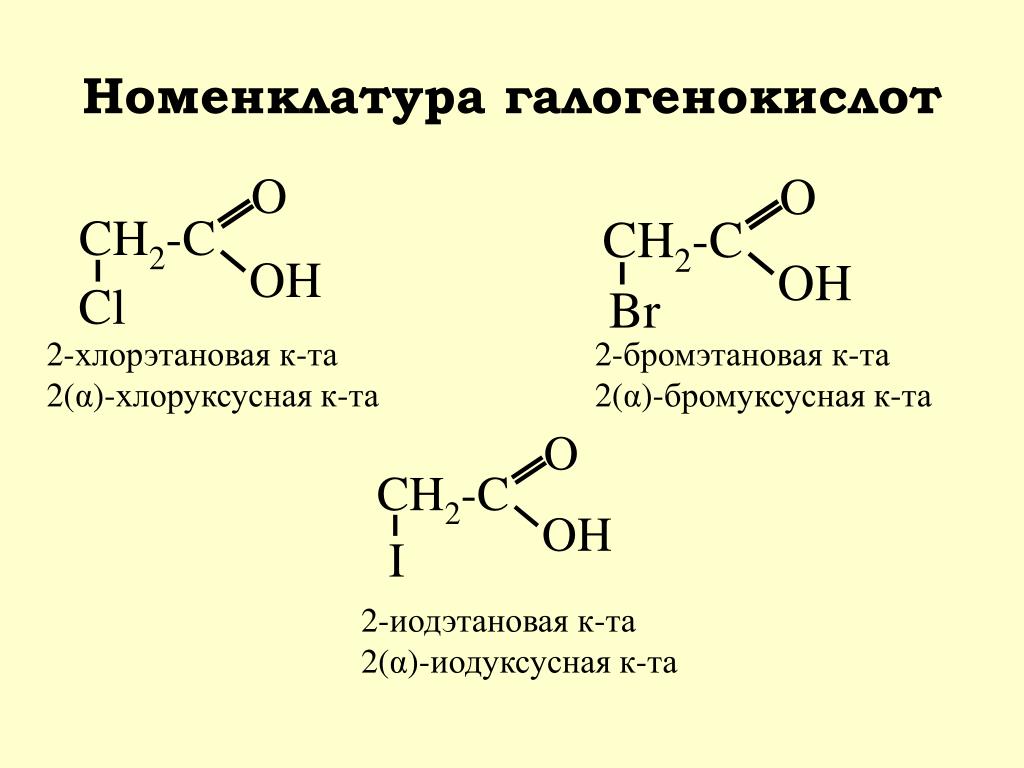 .. В качестве катализатора полезно добавить несколько капель триэтиламина в качестве акцептора HCl и реакция уже идет:
.. В качестве катализатора полезно добавить несколько капель триэтиламина в качестве акцептора HCl и реакция уже идет:
ClCh3COOH + Nh4 = Nh3Ch3COOH+HCl
А получение аминоуксусной кислоты глицина из хлоруксусной под действием аммиака. б получение дикаптола лекарственное средство, применяемое для лечения острых и и хронических отравлений соединениями тяжелых металлов …
А какая кислота сильнее?) какая кислота сильнее? Уксусная, хлороуксусная, аминоуксусная или бромоуксусная?)
Вопрос химикам….пожалуйста, помогите!!!!
A — Ch3ClCOOH, хлорэтановая кислота, B — Ch3Nh3COOH, аминоуксусная или глицин, C — Nh5ClCh3COOH — соляно-кислый глицин, не знаю ка назвать по-другому.
6. Из уксусной кислоты массой 27 г получили хлоруксусную кислоту, выход которой составляет 60%.Может ли иметь указанный сложный эфир изомеры? 10. Сколько граммов глицина потратится на получение 46,62 г глицилфенилаланина?
Оба правы
Подскажите пожалуйста,как из хлоруксусной кис-ты получить аминоуксусную?
С аммиаком зафигачь и получишь аминоуксусную к-ту и хлороводород.
Как из хлоруксусной кислоты получить аминоуксусную нужно уравнение реакции составить. Ребят, помогите!!Cl-Ch3-COOH 2Nh4 gt Nh3-Ch3-COOH Nh5Cl. 1-хлоруксусная к-та 1- аминоуксусная к-та хлорид аммония.
При взаимодействии с аммиаком происходят такие реакции:
ClCh3COOH + Nh4 ——> ClCh3COONh5,
ClCh3COONh5 + 2 Nh4 ——> h3NCh3COONh5 + Nh5Cl,
Подкислением полученного раствора глицината аммония можно получить глицин (аминоуксусную кислоту) :
h3NCh3COONh5 + HCl ——> h3NCh3COOH + Nh5Cl.
Как получить глицин (распишите по-понятнее я же школота)?
В аптеке продается.
Одноосновные карбоновые кислоты. Интерактивные задачи по химии. Кислородсодержащие органические соединения.
Реакцией хлоруксусной кислоты с аммиаком.
Как из хлорэтановой кислоты получить аланин?
Вообще, получают из альфахлопропионовой кислоты. (1-хлорэпропановой) Вы не ошиблись?
5. Описанный способ успешно применяют для получения хлоруксусной кислоты в больших количествах.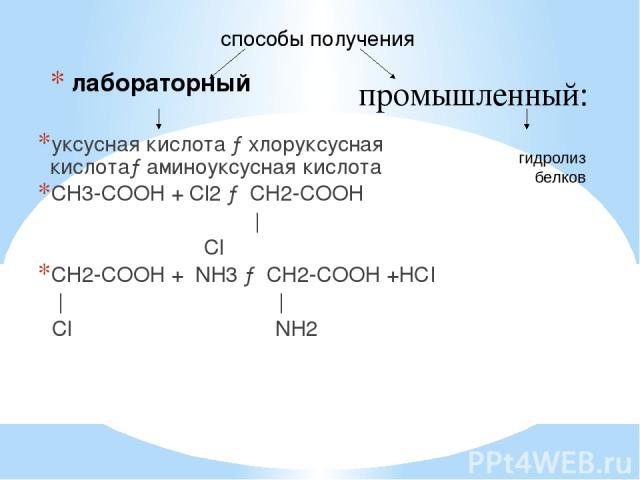 Реакция с анилином — промышленный способ получения индиго, реакцией с аммиаком получают глицин, с метиламином — саркозин, с щелочной целлюлозой…
Реакция с анилином — промышленный способ получения индиго, реакцией с аммиаком получают глицин, с метиламином — саркозин, с щелочной целлюлозой…
Да легко вааааааааришь варишь а потом в -50с градусов потом ещё 15 на +100повари
Этановая кислота — это, вроде, уксусная. Из хлоруксусной легко получается аминоуксусная (гликокол, глицин). Можно, конечно, и углеродную цепь наращивать, но это представляет чисто теоретический интерес.
При синтетическим получении аланина Вы столкнетесь с проблемой рацемизации: природный аланин — L-изомер, в результате синтеза Вы почти наверняка получите рацемат — симесь равных количеств D- и L-изомеров. Разделение оптических изомеров (обычно с использованием ферментов) — задача вполне разрешимая, но не тривиальная.
Весь вопрос — для чего Вам аланин понадобился? Его, причем оптически активный (L-изомер), не проблема приобрести готовый — в промышленности, насколько я знаю, его получают микробиологическим путем, а для продуктов биологического происхождения проблема оптической активности не возникает.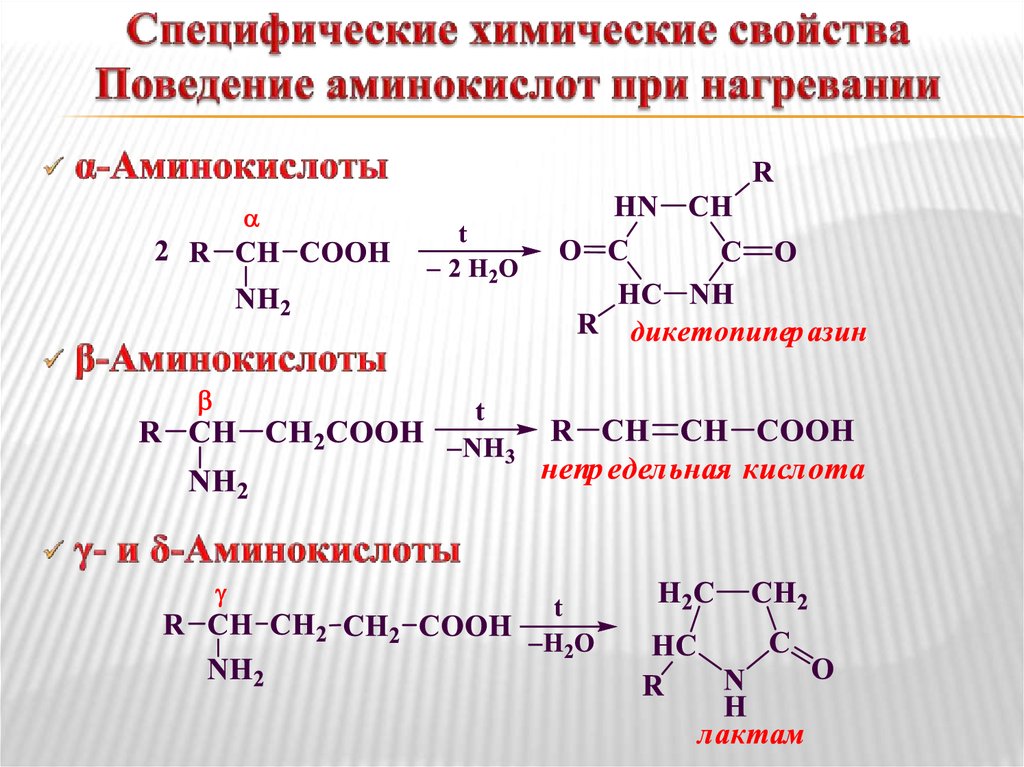
Напишите уравнения реакций получения глицина из этилена.
Получение глицерина из карбоната кальция Получить из карбоната кальция: а) глицин б) тротил в) фенолят калия
Гг
Next Группа цифр в записи числа 5 букв кажется начинается на р Математическое действие 8 букв Отрезок координатного луча 9 букв . 2 thoughts on реакция получения глицина из хлоруксусной кислоты???
Как из этанола получить глицин? напишите уравнение пжл!!!
Химики, помогите….
Ch4COOH + CI2 = Ch4COOCI + HCI
(A)
Ch4COOCI + Nh4 = Ch4CONh3 + HCI + h3O
(B)
Ch4CONh3 + HCI = Ch4COCI + Nh4 + h3!
(C)
ТЫ ИХ ТОКА УРОВНЯЙ! А ТО, голову ломать не о4 охото.
При действии на трихлорэтилен водного раствора серной кислоты образуется хлоруксусная кислота c.56 .Получение глицина гликокола . Оставляют стоять при комнатной температуре на 48 час. раствор 189 г хлоруксусной кислоты в 8 л водного раствора аммиака…
А теперь как будет на самом деле :
Ch4COOH + Cl2 == ClCh3COOH ( это хлоруксусная кислота ) + HCl
ClCh3COOH + 2Nh4 == h3NCh3COOH ( это аминоуксусная кислота, или глицин ) + Nh5Cl
h3NСh3COOH + HCl == [h4NCh3COOH]+ Cl- ( эта штуковина будет называться хлорид карбоксиметиламмония )
В цепи превращений СН4 → А → уксусный альдегид (+ Ag2O)→ Б (+ Cl2)→ В (+ Nh4)→ Х
1) 2Ch5(t) —> 3Н2 + HC ≡ CH ацетилен
2) HC ≡ CH + h3O (t, Hg2+) —> Ch4-CHO (этаналь, уксусный альдегид)
3) Ch4CHO + Ag2O (t) —> 2Ag + Ch4COOH (уксусная кислота)
4) Ch4COOH + Сl2 (уф-свет) —> HCl + Ch3Cl-COOH (хлоруксусная кислота)
5) CHСlCOOH + Nh4—> HCl + Ch3Nh3COOH (аминоуксусная кислота, глицин)
Кислота хлоруксусная кислота аминоуксусная кислота.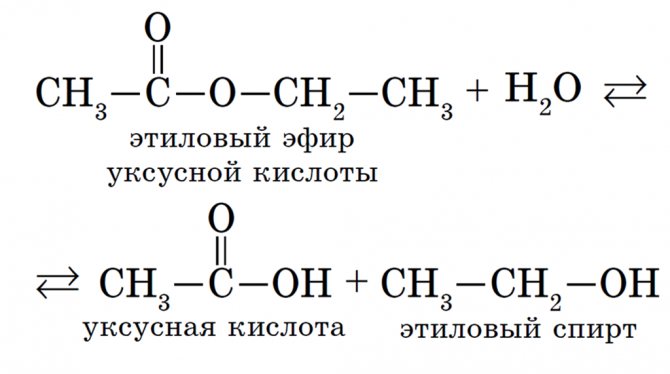 Рассчитайте, сколько граммов 40 -го раствора этилового спирта можно получить из 5 моль глюкозы.Re получение хлоруксусной кислоты из глицина.
Рассчитайте, сколько граммов 40 -го раствора этилового спирта можно получить из 5 моль глюкозы.Re получение хлоруксусной кислоты из глицина.
Получение глицина хлоруксусной кислотызарегистрироваться либо войти на сайт под своим именем.
Патент США на способ получения производных глицина и их применение. Патент (Патент № 6,663,764, выдан 16 декабря 2003 г.) получение производных глицина, свободных от органически связанных ионов галогена и/или галогенида. Настоящее изобретение также относится к применению таких производных глицина в косметических препаратах.
ПРЕДПОСЫЛКИ ИЗОБРЕТЕНИЯ
Производные глицина, такие как бетаины, известны как мягкие и совместимые вещества, которые обычно могут использоваться в больших количествах для приготовления косметических препаратов для очистки и ухода за кожей и волосами.
В предшествующем уровне техники производные глицина обычно получают реакцией третичных аминов с избытком монохлоруксусной кислоты в щелочном водном растворе при повышенной температуре.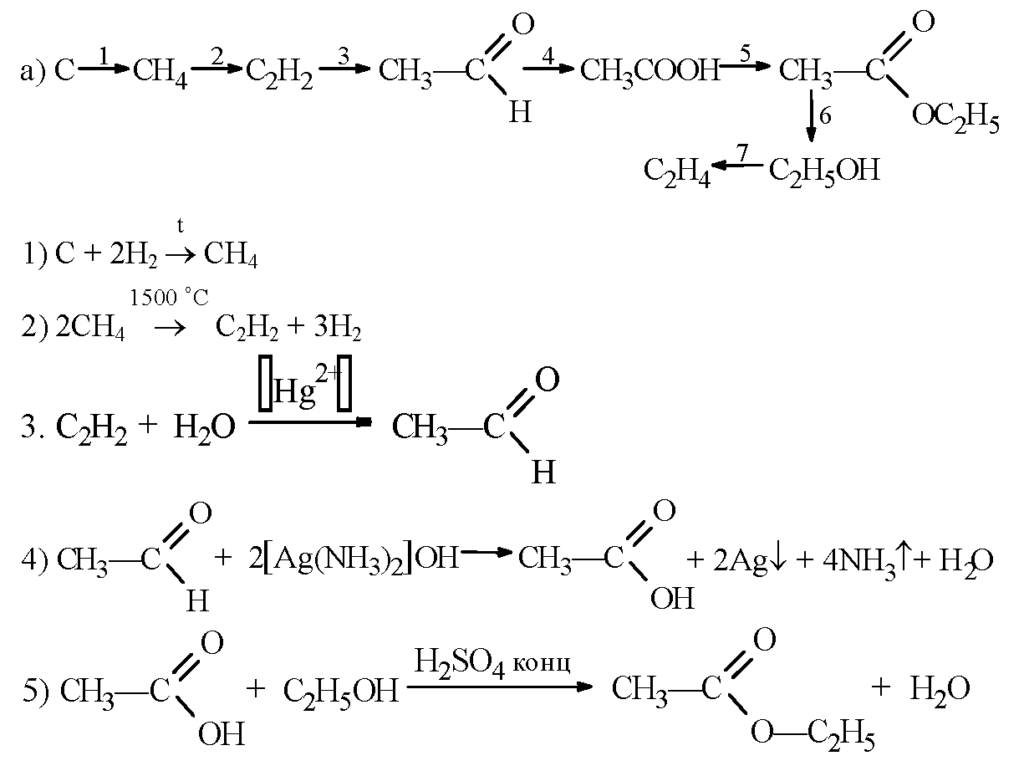
В прошлом были предприняты большие усилия для получения производных глицина, свободных от примесей, которые могут вызывать раздражение кожи или нежелательны по другим токсикологическим и физиологическим причинам.
К ним относятся, в частности, остаточные количества соединений, содержащих органически связанный хлор, возникающих в результате процесса, таких как монохлоруксусная кислота (МХУ) и, в частности, дихлоруксусная кислота (ДХУ) или ее соли, которые вводятся в конечный продукт с использованием хлоруксусной кислоты.
Попытки уменьшить содержание этих соединений за счет увеличения времени реакции или увеличения pH не привели к значительному снижению образования примесей. Использование pH выше примерно 10, особенно при повышенных температурах около или выше 100°C, влечет за собой риск усиления разложения (DE-B-2926 479, ЕР-В-0 557 835). DE-A-3939264 относится к способу снижения остаточного содержания свободного алкилирующего агента в водных растворах амфотерных или цвиттер-ионных поверхностно-активных веществ, отличающемуся тем, что растворы подвергают последующей обработке аммиаком, аминокислотой, содержащей от 2 до 8 атомов углерода.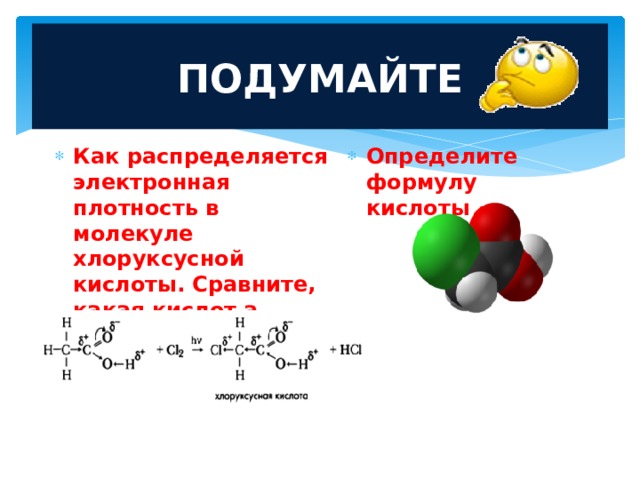
Кроме того, реакционные смеси содержат большое количество ионов хлорида в форме их солей щелочных металлов или аммония. По этой причине эти реакционные смеси предшествующего уровня техники имеют связанные с ними дополнительные недостатки, такие как увеличение вязкости конечного продукта и ухудшение низкотемпературной стабильности составов. Кроме того, реакционные смеси предшествующего уровня техники не могут быть составлены с рядом дополнительных активных ингредиентов.
Кроме того, из-за содержания ионов хлора известные реакционные смеси слишком агрессивны для очистки чувствительных к коррозии металлических подложек, которые используются, в частности, в электронной промышленности.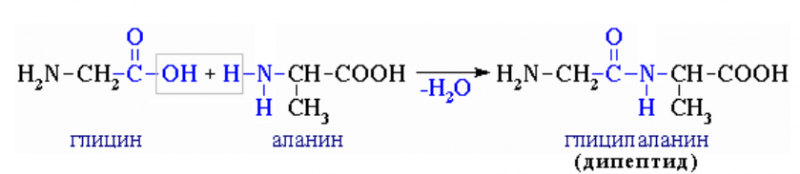
Поэтому был предпринят ряд попыток удалить эти соли, например, путем экстракции растворителем, как описано в JP-A-759981984, или электродиализом в соответствии с EP-A-0 269 940. Помимо тот факт, что полное удаление ионов хлора невозможно, эти способы предшествующего уровня техники сложны и экономически невыгодны из-за необходимости дополнительных стадий.
Существует также множество процессов, позволяющих окислять спирты до карбоновых кислот. Помимо классических процессов окисления в лабораторных масштабах с помощью оксидов тяжелых металлов. (например, KMnO4), известны процессы, которые могут осуществляться в промышленных масштабах, такие как окисление NO2 (патент США № 5,856,470), нитрилоксидами (патент США № 5,179,218), кислородом с катализом благородным металлом (DE-3929063) или электрохимически (EP-A-0199413, DE-A-3443303).
Из работ H. J. Schäfer (Overview: Topics in Current Chemistry, 1987, 142, 102–129) известно, что первичные спирты можно окислить электролизом в щелочном растворе с использованием анодов, покрытых гидроксидом оксида никеля NiO(OH) и стальные катоды с получением соответствующих карбоновых кислот с теоретическим выходом от 46 до 99%.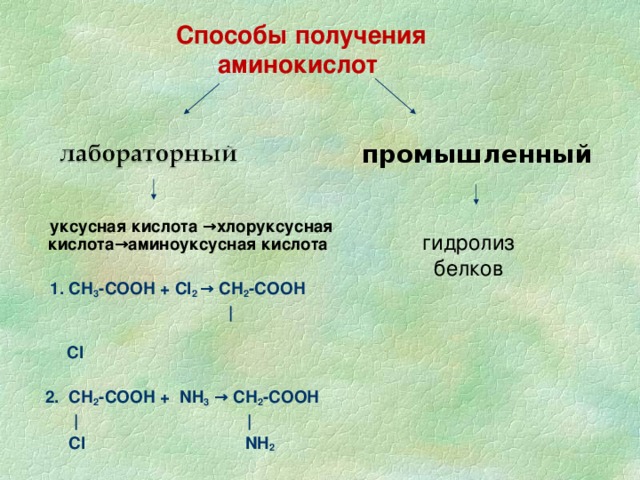 Окисление происходит главным образом с помощью непрямого анодного процесса, в котором спирт окисляется гидроксидом оксида никеля с трехвалентным никелем с образованием карбоновой кислоты, при этом NiO(OH) восстанавливается до оксида никеля или гидроксида никеля с двухвалентным никелем. В результате удаления электронов на аноде двухвалентный никель снова превращается в трехвалентный никель.
Окисление происходит главным образом с помощью непрямого анодного процесса, в котором спирт окисляется гидроксидом оксида никеля с трехвалентным никелем с образованием карбоновой кислоты, при этом NiO(OH) восстанавливается до оксида никеля или гидроксида никеля с двухвалентным никелем. В результате удаления электронов на аноде двухвалентный никель снова превращается в трехвалентный никель.
Электрохимическое окисление спиртов, связанных с четвертичным положительно заряженным азотом через этиленовую группу, не описано в работе HJ Schäfer.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
В попытке преодолеть недостатки предшествующего уровня техники и предложить способ, позволяющий получать производные глицина, свободные от органически связанных ионов галогенов и/или галогенидов, в настоящее время установлено, что эта цель может быть достигнута путем окисления четвертичных аминоспиртов. Удивительно, но четвертичный положительно заряженный азот не мешает процессу окисления, и не могут быть обнаружены ни продукты окисления азота, такие как N-оксиды, ни продукты разложения по Гофману.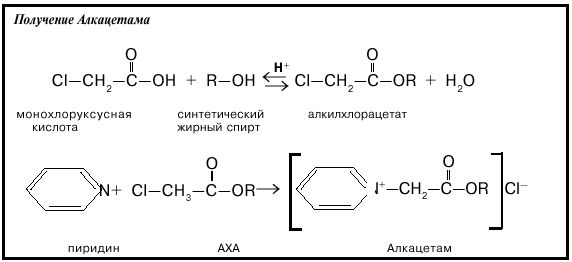
Окисление четвертичного аминоспирта до соответствующего производного глицина может быть осуществлено в настоящем изобретении электрохимическим окислением в водном щелочном растворе с использованием никелевых электродов с покрытием.
Таким образом, настоящее изобретение предлагает способ получения производных глицина путем окисления соединений -гидроксиэтиламмония электролизом водного щелочного раствора, который включает проведение окисления с использованием анодов, покрытых гидроксидом оксида никеля.
Способ по изобретению отличается исключительной экологичностью, так как не образуются вредные для окружающей среды побочные продукты и можно избежать использования высокотоксичной хлоруксусной кислоты. Кроме того, продукт, не содержащий неорганического хлора, получается напрямую, что позволяет избежать технически сложного отделения ионов хлора.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Как указано выше, настоящее изобретение обеспечивает способ получения производных глицина электрохимическим окислением гидроксильных групп соединений -гидроксиэтиламмония, присутствующих в водном щелочном растворе, т.е. электролите, с получением соответствующие кислоты.
При использовании электрохимического процесса по настоящему изобретению теоретические выходы без исключения превышают 80%. Электролиз по настоящему изобретению в принципе осуществляется таким образом, что водный электролит подвергается электролизу на электродах, покрытых гидроксидом оксида никеля. Покрытие электродов может быть выполнено обычными способами, такими как, например, способ, предложенный Х. Й. Шефером. В принципе, слой Ni(OH)2 катодно осаждается из раствора соли Ni на следующем аноде, а затем анодно преобразуется в щелочном растворе в NiO(OH) (J. Kaulen, H.J. Schäfer, Tetrahedron, 19).82, 38, 3299).
Помимо металлического никеля, анодные материалы, которые должны быть покрыты NiO(OH), включают любой материал, к которому может прилипать активированный слой гидроксида оксида никеля, такой как, например, монель, нержавеющая сталь, графит или стеклоуглерод .
Электролизер, используемый в настоящем изобретении, может состоять из любого материала, стойкого к электролиту и реагентам, такого как щелочестойкое стекло, фарфор, полиэтилен, резина или нержавеющая сталь.
Тип элемента, используемый в настоящем изобретении, может быть разделенным или неразделенным, последний предпочтительнее, поскольку не следует опасаться снижения желаемого продукта электролиза.
Способ согласно настоящему изобретению может осуществляться непрерывно или периодически, причем предпочтение отдается периодическому способу. В этой процедуре система электролиза состоит из водного раствора соединения -гидроксиэтиламмония с рН предпочтительно более 12. На щелочность растворов обычно влияют гидроксиды щелочных металлов (предпочтительно NaOH и КОН).
Предпочтительное содержание соединения -гидроксиэтиламмония, присутствующего в щелочном растворе, составляет от 1 до 30% по весу, предпочтительно от 20 до 30% по весу.
Температура электролиза, используемая в настоящем изобретении, обычно составляет от 20 до 80°С, предпочтительно около 70°С. количество, предпочтительно в 1,5-3 раза превышающее количество электроэнергии.
Когда электролиз завершен, электролизованный раствор доводят до pH примерно от 6 до 7, например, с помощью фосфорной кислоты, и концентрируют путем выпаривания. Кроме того, остаток можно необязательно экстрагировать из электролизованного раствора подходящим растворителем. Спирты (этанол, изопропанол), например, подходят для этой цели. Полученный экстракт освобождается от растворителя и дает чистые бетаины.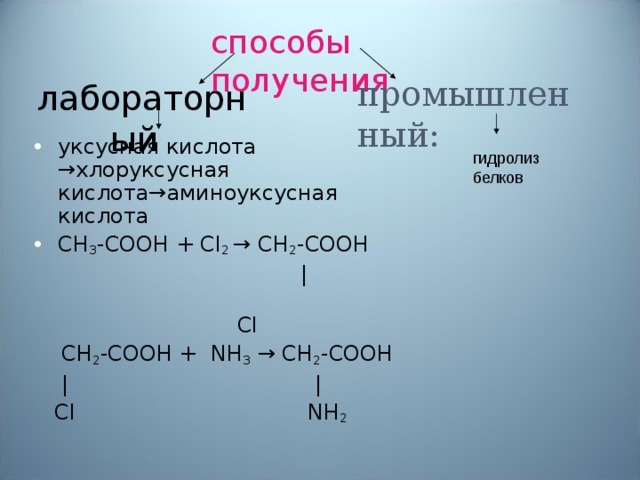
Экстракция необходима только в том случае, если целью является получение бессолевых бетаинов. Однако соли, возникающие при синтезе, обычно не представляют проблемы, а это означает, что можно обойтись без экстракции.
Соединения -гидроксиэтиламмония, совместно используемые в соответствии с настоящим изобретением, могут быть получены способами, известными в данной области, путем взаимодействия аминов с этиленоксидом в кислом растворе (EP-A-0 098 802). Соединения
-гидроксиэтиламмония, которые можно использовать в настоящем изобретении, включают все соединения, которые содержат по меньшей мере одну четвертичную аминогруппу и по меньшей мере одну группу ОН, предпочтительно формулы (I) и/или (II) и/или ( III)
где
каждый R независимо друг от друга может быть алкильным радикалом, имеющим от 1 до 3 атомов углерода, и/или -Ch3-Ch3-OH;
n, m, o могут принимать значения от 1 до 5, предпочтительно от 1 до 3, в частности 1; и
R1 представляет собой алкильный радикал, необязательно содержащий гетероатомы, в частности атомы кислорода и/или азота, или радикал Ra-(C(O)-NH-(Ch3)q)r-, где q=1-6, предпочтительно 2 или 3, а r=0 или 1.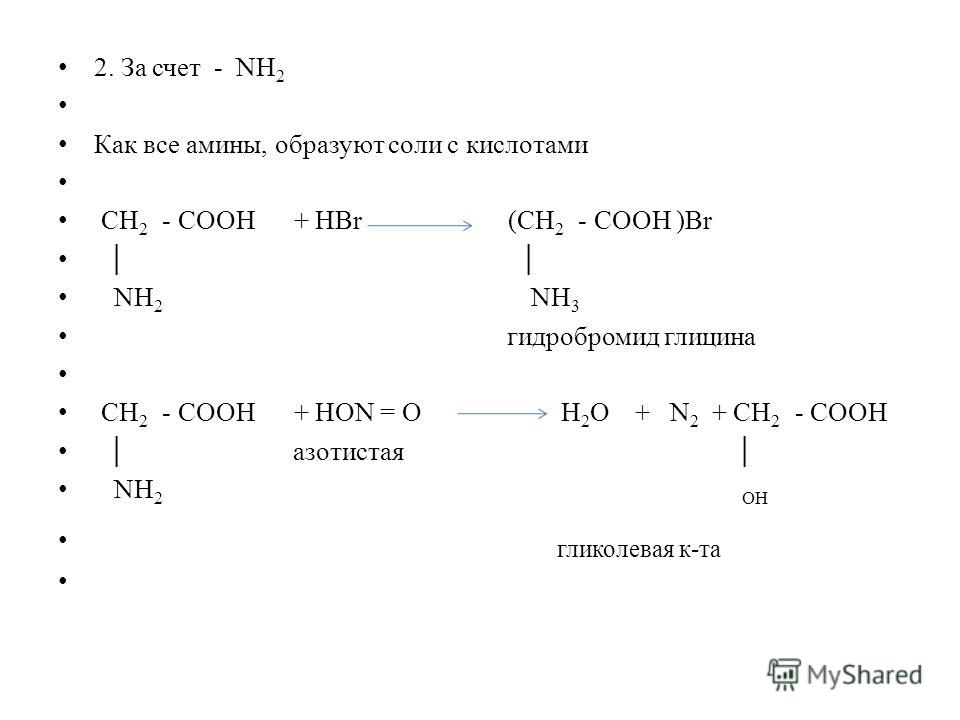
Согласно настоящему изобретению предпочтение отдается соединениям, в которых свободные валентности общей формулы (I) связаны с радикалом Ra-C(O)-NH -(Ch3)3, где Ra может быть необязательно замещенным алкильным или алкенильным радикалом, имеющим от 7 до 21 атомов углерода, или необязательно замещенным алкильным или алкенильным радикалом, имеющим от 1 до 22 атомов углерода, предпочтительно, имеющим от 7 до 17 атомов углерода, и радикалы R независимо друг от друга могут быть алкильными радикалами, имеющими от 1 до 3 атомов углерода; или, если r=0, Ra может быть алкильным или алкенильным радикалом, имеющим от 8 до 22 атомов углерода; валентности общих формул (I)-(III) связаны с необязательно замещенным алкильным или алкенильным радикалом, имеющим от 1 до 22 атомов углерода, предпочтительно, имеющим от 8 до 18 атомов углерода, или с радикалом Ra-C(O)-[NH -(Ch3)z]y-, где Ra имеет указанное выше значение, а z, y, независимо друг от друга, могут быть числами от 1 до 3.
Радикал Ra предпочтительно получают из природных жирных кислот, таких как, например, каприловая кислота, каприновая кислота, 2-этилгексановая кислота, лауриновая кислота, миристиновая кислота, пальмитиновая кислота, пальмитолеиновая кислота, изостеариновая кислота, стеариновая кислота, гидроксистеариновая кислота (рицинолеиновая кислота), дигидроксистеариновая кислота, олеиновая кислота, линолевая кислота, петроселиновая кислота, элаидиновая кислота, арахиновая кислота, бегеновая кислота, эруковая кислота и гадолеиновая кислота, а также технические смеси, которые образуются при расщеплении под давлением натуральных жиров и масла, такие как олеиновая кислота, линолевая кислота, линоленовая кислота и, в частности, жирная кислота рапсового масла, жирная кислота соевого масла, жирная кислота подсолнечного масла, жирная кислота таллового масла.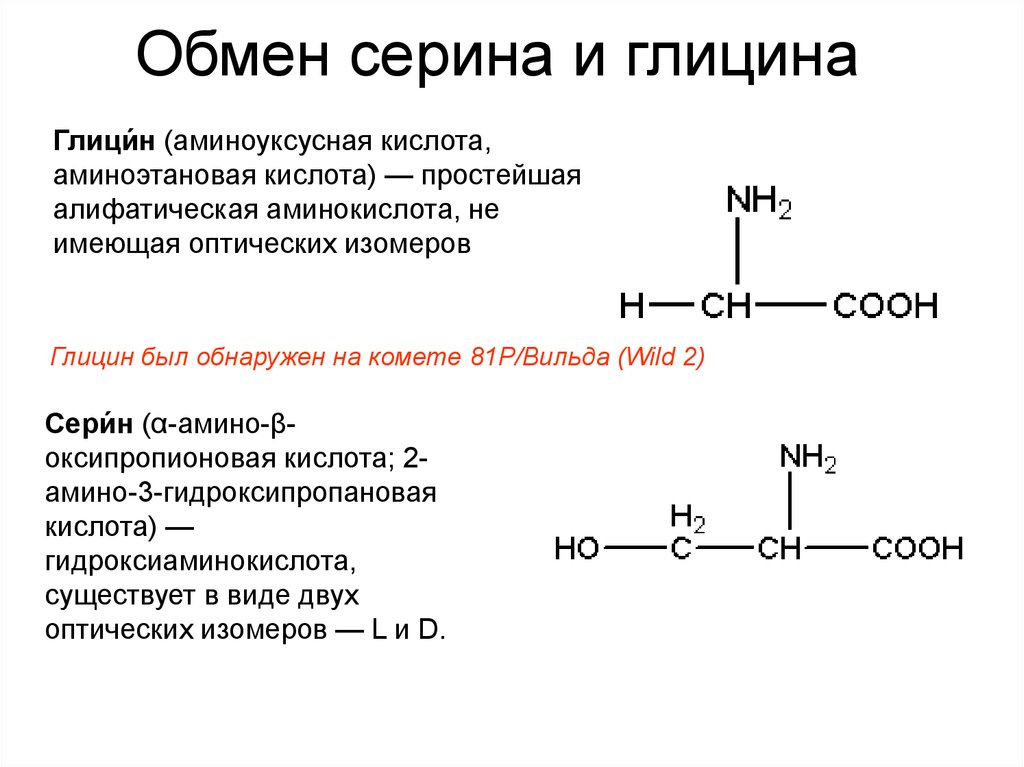 Все жирные кислоты с одинаковым распределением цепей являются подходящими и поэтому могут использоваться в настоящем изобретении.
Все жирные кислоты с одинаковым распределением цепей являются подходящими и поэтому могут использоваться в настоящем изобретении.
Содержание ненасыщенных фракций в этих жирных кислотах или сложных эфирах жирных кислот, при необходимости, доводится известными процессами каталитического гидрирования до желаемого йодного числа или достигается путем смешивания полностью гидрогенизированных жирных компонентов с негидрогенизированными жирными компонентами.
Йодное число, которое является мерой средней степени насыщения жирной кислоты, представляет собой количество йода, поглощаемого 100 г соединения для насыщения двойных связей.
Предпочтение отдается использованию частично гидрогенизированных С8/18-жирных кислот кокосового масла и пальмового масла, жирных кислот рапсового масла, жирных кислот подсолнечного масла, жирных кислот соевого масла и жирных кислот таллового масла с йодными числами в диапазоне примерно от 80 до 150 и, в частности, С8/18-кокосовые жирные кислоты технического качества, и в этом случае в некоторых случаях может быть выгодным выбор цис/транс-изомеров, таких как обогащенные элаидиновой кислотой фракции С16/18-жирных кислот. Вышеупомянутые соединения являются коммерчески доступными продуктами и поставляются различными компаниями под их соответствующими торговыми названиями.
Вышеупомянутые соединения являются коммерчески доступными продуктами и поставляются различными компаниями под их соответствующими торговыми названиями.
Соединения общих формул (I)-(III), используемые в настоящем изобретении, подвергают электрохимическому окислению с получением соответствующих кислот, как описано ниже.
Следующие примеры приведены для иллюстрации способа изобретения, а также некоторых преимуществ, которые могут быть получены при его использовании.
ПРИМЕР 1
150 мл 27%-ного раствора 2-гидроксиэтил(диметил)-3-ундецилкарбоксамидопропиламмония×0,5 ч3PO4-, содержащего 4,2 г NaOH, подвергали электролизу в течение 7 ч при силе тока 2,0 А в стеклянной кювете вместимостью 150 мл с обратным холодильником на сетчатом электроде (60,5 см2, никелевая сетка, покрытая NiO(OH)) и катоде (цилиндр, внутренний диаметр, Ø 1,7 см, высота 7 см, нержавеющая сталь). Во время этого электролиза рН увеличился до 8-9.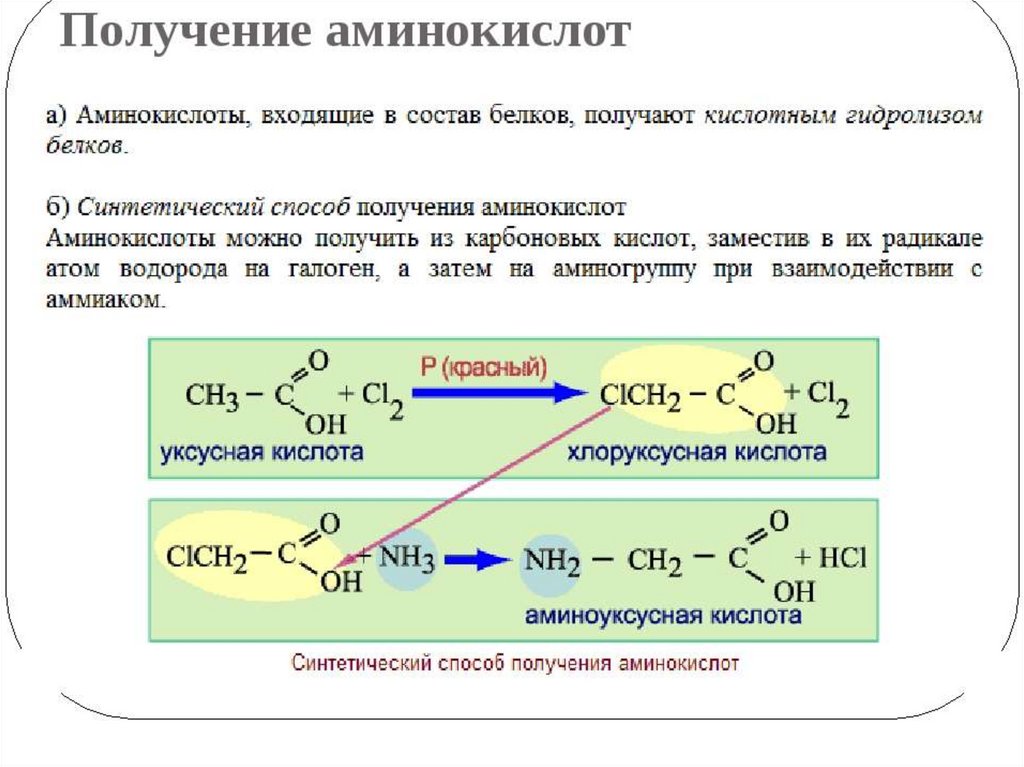 в течение 5 ч и добавляли 4 мл насыщенного раствора NaOH. Затем силу тока доводили до 1,0 А и проводили электролиз еще в течение 7 часов. По истечении этого времени раствор снова имел pH от 8 до 9, и снова добавляли 4 мл насыщенного раствора NaOH. Затем устанавливали силу тока 0,5 А и проводили электролиз еще в течение 7,5 часов. Полученный раствор имел pH от 8 до 9. Мониторинг реакции осуществляли с помощью TL-хроматографии и масс-спектрометрии ESI.
в течение 5 ч и добавляли 4 мл насыщенного раствора NaOH. Затем силу тока доводили до 1,0 А и проводили электролиз еще в течение 7 часов. По истечении этого времени раствор снова имел pH от 8 до 9, и снова добавляли 4 мл насыщенного раствора NaOH. Затем устанавливали силу тока 0,5 А и проводили электролиз еще в течение 7,5 часов. Полученный раствор имел pH от 8 до 9. Мониторинг реакции осуществляли с помощью TL-хроматографии и масс-спектрометрии ESI.
Продукт электролиза доводили до рН от 6 до 7 с помощью фосфорной кислоты и концентрировали выпариванием. Остаток экстрагировали изопропанолом и полученный экстракт освобождали от растворителя. В качестве продукта получали желто-коричневое твердое вещество.
Анализ
Выход: 23,3 г (91% от теории)
13C-ЯМР (100 МГц, CDCl3): &dgr;=13,67 (Ch4), от 22,24 до 31,48 (Ch3), 35,86 и 35,87 (Ch3CONH и CONH ), 50,32 (N+(Ch4)2), 62,12 (Ch3N+), 63,98 (N+Ch3COO-) 167,09 (COO-), 174,06 (CONH) м.д.
ПРИМЕР 2
Эксперимент проводили аналогично примеру 1.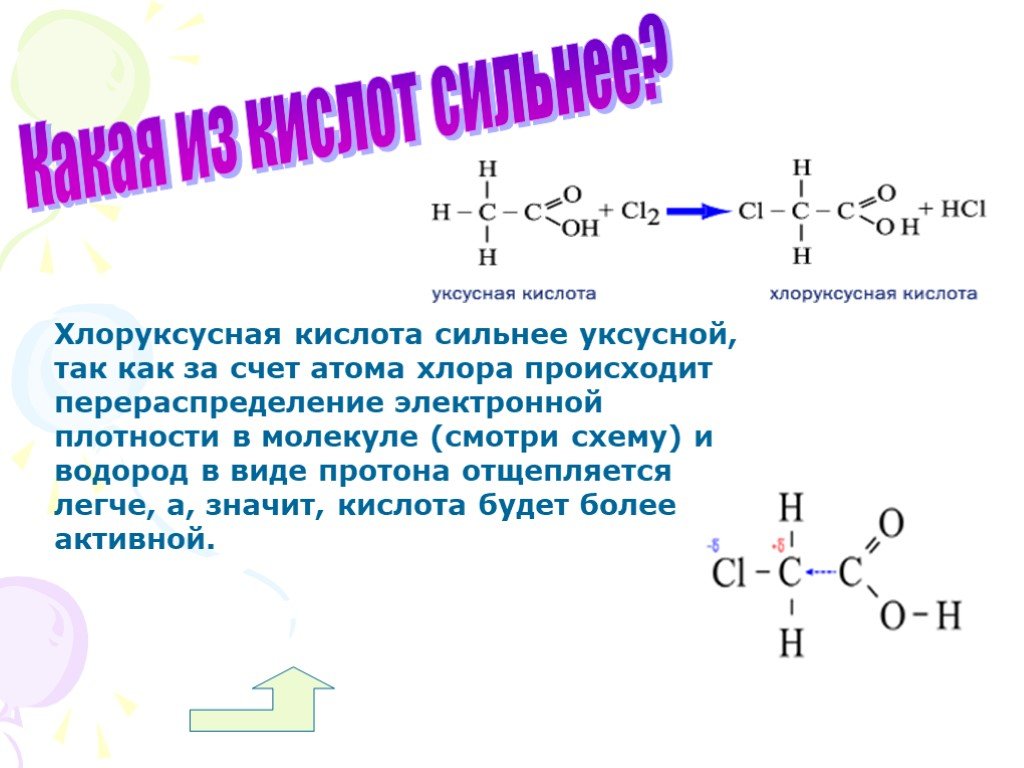 В отличие от примера 1 в качестве исходного материала использовали 2-гидроксиэтил(диметил)-3-ундецилкарбоксамидопропиламмоний×0,5 C2O4H-. При окислении оксалат окислялся до СО2, который в щелочной среде реагирует с образованием карбоната, и только затем аммонийный спирт окисляется до соответствующего производного глицина. В начале к раствору добавляли соответственно большее количество требуемого NaOH.
В отличие от примера 1 в качестве исходного материала использовали 2-гидроксиэтил(диметил)-3-ундецилкарбоксамидопропиламмоний×0,5 C2O4H-. При окислении оксалат окислялся до СО2, который в щелочной среде реагирует с образованием карбоната, и только затем аммонийный спирт окисляется до соответствующего производного глицина. В начале к раствору добавляли соответственно большее количество требуемого NaOH.
Анализ
Выход: 20,28 г (82% от теории)
13C-ЯМР (100 МГц, CDCl3): &dgr;=13,39 (Ch4), от 21,95 до 31,18 (Ch3), 35,55 (шир., Ch3CONH и CONHCh3) ), 50,15 (N+(Ch4)2), 61,77 (Ch3N+), 63,73 (N+Ch3COO-), 165,81 (COO-), 173,65 (CONH) м.д.
ПРИМЕР 3
Опыт проводили аналогично примеру 1. В отличие от примера 1 использовали 105 мл 2,7%-ного раствора аммиачной смеси (в пересчете на фракцию жирных кислот кокосового ореха), в состав которой в качестве основного компонент 2-гидроксиэтил(диметил)-3-ундецилкарбоксамидопропиламмоний×0,5 ч3PO4- подвергали электролизу в течение 3 ч при 2,0 А.
Анализ
Выход: 2,35 г (96% от теории)
13C-ЯМР (100 МГц, CDCl3): &dgr;=13,69 (Ch4), от 22,24 до 31,48 (Ch3), 35,84 и 35,87 (Ch3CONH и CONH ), 50,41 (N+(Ch4)2), 62,23 (Ch3N+), 64,31 (N+Ch3COO-), 166,14 (COO-), 173,93 (CONH) м.д.
МС (ESI): m/e=365 (M++Na, 100%).
Хотя настоящее изобретение было конкретно показано и описано в отношении его предпочтительных вариантов осуществления, специалистам в данной области должно быть понятно, что вышеуказанные и другие изменения в формах и деталях могут быть сделаны без отклонения от сущности и объема настоящего изобретения. настоящее изобретение. Таким образом, предполагается, что настоящее изобретение не ограничивается точными формами и деталями, описанными и проиллюстрированными, а попадает в объем настоящей заявки.
Монохлоруксусная кислота
Монохлоруксусная кислота (MCA)
Ведущая технология, обеспечивающая качество и надежность
Качество и универсальность в глобальном масштабе
Мы являемся крупнейшим в мире производителем MCA и ее натриевой соли, SMCA с мощностью более 250000 тонн в год по всему миру.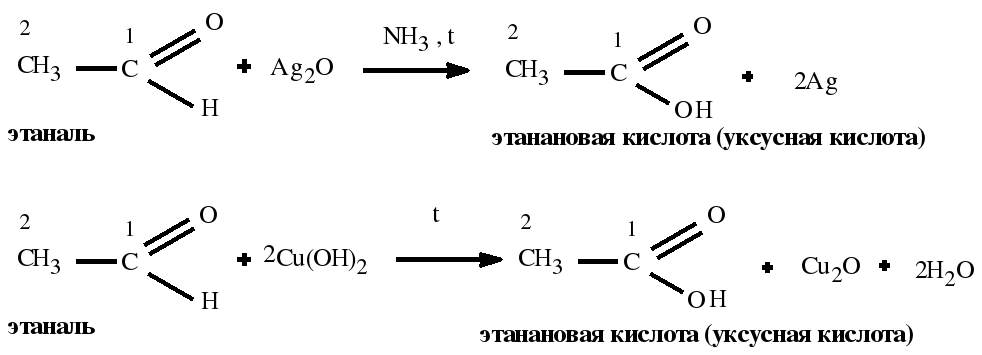 Являясь вашим глобальным местным поставщиком (S)MCA, поддерживающим существующие цепочки поставок на зрелых рынках, и идеально подходящим для поддержки вашего роста на развивающихся рынках.
Являясь вашим глобальным местным поставщиком (S)MCA, поддерживающим существующие цепочки поставок на зрелых рынках, и идеально подходящим для поддержки вашего роста на развивающихся рынках.
MCA (твердые и жидкие), SMCA, а также производные (ECA и MeCA) доступны в упаковках различных размеров и качества из нашей глобальной производственной сети. Узнайте больше о наших предложениях в Интернете или свяжитесь с нами, чтобы найти то, что соответствует вашим требованиям.
Избранные товары
Монохлоруксусная кислота
МСА 80% р-р. в воде
Монохлоруксусная кислота для использования в качестве основного сырья для различных продуктов, таких как карбоксиметилцеллюлоза, клеи, фармацевтические препараты и химикаты для защиты растений.
Читать далееМонохлоруксусная кислота
Хлопья МСА
Эти хлопья монохлоруксусной кислоты представляют собой белое кристаллическое вещество с характерным запахом. Он используется в качестве основного сырья для различных продуктов, таких как карбоксиметилцеллюлоза, клеи, фармацевтические препараты и химикаты для защиты растений.
Он используется в качестве основного сырья для различных продуктов, таких как карбоксиметилцеллюлоза, клеи, фармацевтические препараты и химикаты для защиты растений.
Монохлоруксусная кислота
Гранулы SMCA
Это твердое вещество монохлоруксусной кислоты поставляется в виде белых гранул. Он используется в качестве основного сырья для различных продуктов, таких как карбоксиметилцеллюлоза, клеи, фармацевтические препараты и химикаты для защиты растений.
Читать далееМонохлоруксусная кислота
порошок SMCA
Монохлоруксусная кислота для использования в качестве основного сырья для различных продуктов, таких как карбоксиметилцеллюлоза, клеи, фармацевтические препараты и химикаты для защиты растений.
Читать далееИскать все продукты MCA
Чистые руки защищают от инфекций
Чтобы правильно помыть руки, нужно столько же времени, сколько дважды спеть «Happy Birthday».
Свяжитесь с нами!
Для получения дополнительной информации о наших Монохлоруксусная кислота (MCA) , свяжитесь с нашими специалистами. Мы с нетерпением ждем ответа от вас.
Тип запроса Выберите тип запроса *Запросить информацию о продуктеЗапросить техническую помощьЗапросить паспорта безопасностиЗапросить образецЗапросить цену
Имя
Фамилия
Электронная почта
Компания
Страна
Please select your country *AfghanistanÅland IslandsAlbaniaAlgeriaAmerican SamoaAndorraAngolaAnguillaAntigua and BarbudaArgentinaArmeniaArubaAsia (Federated States of)AustraliaAustriaAzerbaijanBahamasBahrainBangladeshBarbadosBelarusBelgiumBelizeBeninBermudaBhutanBolivia (Plurinational State of)Bonaire, Sint Eustatius and SabaBosnia and HerzegovinaBotswanaBouvet IslandBrazilBritish Indian Ocean TerritoryBrunei DarussalamBulgariaBurkina FasoBurundiCambodiaCameroonCanadaCayman IslandsCentral African RepublicChadChileChinaChristmas islandCocos (Keeling) IslandsColombiaComorosCongoCongo (Democratic Republic of the)Cook IslandsCosta RicaCôte d’IvoireCroatiaCubaCuraçaoCyprusCzech RepublicDenmarkDjiboutiDominicaDominican RepublicEcuadorEgyptEl SalvadorEquatorial GuineaEritreaEstoniaEthiopiaFalkland Islands (Malvinas)Faroe IslandsFijiFinlandFranceFrench AsiaFrench GuianaFrench PolynesiaFrench Southern TerritoriesGabonGambiaGeorgiaGermanyGhanaGibraltarGreeceGreenlandGrenadaGuadeloupeGuamGuatemal aGuernseyGuineaGuinea-BissauGuyanaHaitiHeard Island and McDonald IslandsHoly SeeHondurasHong KongHungaryIcelandIndiaIndonesiaIran (Islamic Republic of)IraqIrelandIsle of ManIsraelItalyJamaicaJapanJerseyJordanKazakhstanKenyaKiribatiKorea (Democratic People’s Republic of)Korea (Republic of)KuwaitKyrgyzstanLao People’s Democratic RepublicLatviaLebanonLesothoLiberiaLibyaLiechtensteinLithuaniaLuxembourgMacaoMacedonia (the former Yugoslav Republic of)MadagascarMalawiMalaysiaMaldivesMaliMaltaMarshall IslandsMartiniqueMauritaniaMauritiusMayotteMexicoMicronesia (Federated States of)Moldova (Republic of )MonacoMongoliaMontenegroMontserratMoroccoMozambiqueMyanmarNamibiaNauruNepalNetherlandsNew CaledoniaNew ZealandNicaraguaNigerNigeriaNiueNorfolk IslandNorthern Mariana IslandsNorwayOmanPakistanPalauPalestine, State ofPanamaPapua New GuineaParaguayPeruPhilippinesPitcairnPolandPortugalPuerto RicoQatarRéunionRomaniaRussian FederationRwandaSaint BarthélemySaint Helena, Ascension and Tristan da CunhaSai nt Kitts and NevisSaint LuciaSaint Martin (French part)Saint Pierre and MiquelonSaint Vincent and the GrenadinesSamoaSan MarinoSao Tome and PrincipeSaudi ArabiaSenegalSerbiaSeychellesSierra LeoneSingaporeSint Maarten (Dutch part)SlovakiaSloveniaSolomon IslandsSomaliaSouth AfricaSouth Georgia and the South Sandwich IslandsSouth SudanSpainSri LankaSudanSurinameSvalbard and Jan MayenSwazilandSwedenSwitzerlandSyrian Arab RepublicTaiwan, Province of ChinaTajikistanTanzania, United Republic ofThailandTimor-LesteTogoTokelauTongaTrinidad and TobagoTunisiaTurkeyTurkmenistanTurks and Caicos IslandsTuvaluUgandaUkraineUnited Arab EmiratesUnited Kingdom of Great Britain and Northern IrelandUnited States Minor Outlying IslandsUnited States of AmericaUruguayUzbekistanVanuatuVenezuela (Bolivarian Republic of)Viet NamVirgin Islands (British)Virgin Islands (U.

Leave A Comment