ПОЛ (перекисное окисление липидов)
Исследование, направленное на выявление в образце крови продуктов перекисного окисления липидов и их активности в целях оценки роли данных веществ в реакциях окислительного повреждения клеток организма (так называемого окислительного стресса).
Синонимы русские
Перекисное окисление липидов; оценка окислительного повреждения (окислительного стресса).
Синонимы английские
Lipid peroxidation; assessment of oxidative damage (oxidative stress).
Метод исследования
Спектрофотометрия.
Единицы измерения
Мкмоль/л (микромоль на литр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Детям в возрасте до 1 года не принимать пищу в течение 30-40 минут до исследования.
- Не принимать пищу в течение 2-3 часов до исследования, можно пить чистую негазированную воду.

- Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Перекисное окисление липидов – это химический процесс, каскад реакций превращения липидов (поступающих с пищей или синтезированных в организме) с участием свободных радикалов – активных заряженных молекул. Так как липиды — компоненты мембран всех клеток организма, реакции перекисного окисления могут приводить к нарушению их структуры и повреждению клетки, что является одним из механизмов патогенеза ряда заболеваний.
Реакции ПОЛ постоянно происходят в организме в норме в определенной степени, которая не должна превышаться во избежание их повреждающего действия. Перекисное окисление липидов играет важную роль для процесса апоптоза, регулирования структуры мембран и их функций (презентация рецепторов, работа ионных каналов, высвобождение биологически активных веществ, передача сигналов между клетками и т.д.).
Чрезмерная активность ПОЛ может приводить к разрушению мембраны клетки, проникновению или выходу из нее веществ, которых не должно быть в норме, что ведет к нарушению жизнедеятельности клеток (их преждевременное старение, разрушение, измененные функции передачи веществ, связывания ферментов и рецепторов).
В организме в роли ингибирующего фактора (т.е. сдерживающего реакции ПОЛ) выступает антиоксидантная система. Таким образом, патологические реакции перекисного окисления липидов могут быть как при чрезмерной активности самих этих процессов, так и при недостаточности работы антиоксидантной системы.
Исследование позволяет оценить количественно, насколько активно протекают реакции ПОЛ в организме и насколько с ними справляются собственные защитные системы организма. Такой анализ продуктов перекисного окисления липидов играет важную роль в определении связи их повреждающего действия с возникновением, развитием или прогрессированием того или иного заболевания. Исследование проводится методом спектрофотометрии, основанным на изучении физико-химических свойств веществ, в частности их спектров поглощения.
Таким образом, анализ продуктов реакций ПОЛ позволяет понять механизмы развития серьезных заболеваний, определить так называемый маркер окислительного стресса организма. При своевременно выявленном нарушении есть возможность оптимально подобрать лечение и предотвратить развитие заболевания, его прогрессирование, направить его течение по более благоприятному варианту. Следует отметить, что интерпретация результата осуществляется только врачом с учетом всех имеющихся данных анамнеза и других методов диагностики.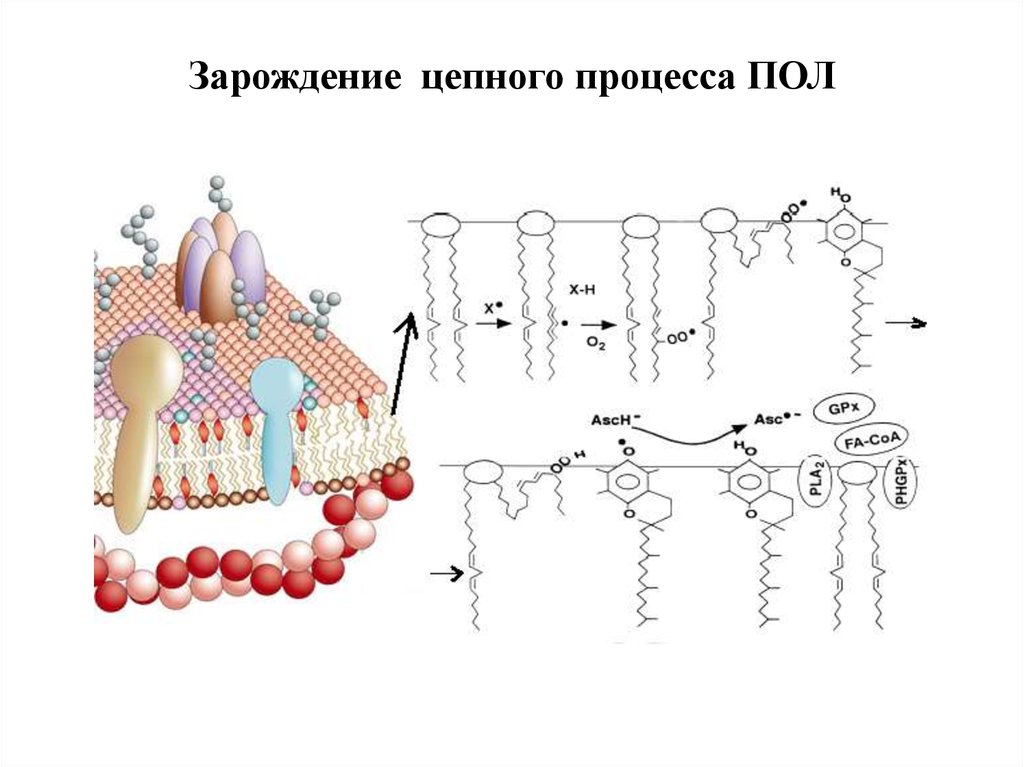
Для чего используется исследование?
- Для диагностики оксидативного стресса и степени интоксикации организма вследствие повышенной активности реакций перекисного окисления липидов.
- Для выявления дефицита антиоксидантной системы и оценки риска заболеваний, ассоциированных с ее недостатком (заболевания сердечно-сосудистой системы, иммунодефициты, доброкачественные и злокачественные опухоли, гормональные нарушения, аутоиммунные заболевания, воспалительные процессы и др.).
- Для выявления генетических форм дефицита ферментов.
Когда назначается исследование?
- При заболеваниях сердечно-сосудистой системы (атеросклеротическое повреждение сосудов, ишемическая болезнь сердца, гипертоническая болезнь).
- При метаболических заболеваниях (в первую очередь, при сахарном диабете).
- При предраковых заболеваниях и злокачественных новообразованиях.
- При заболеваниях дыхательной системы (ХОБЛ, бронхиальная астма).

- При поражении ЦНС (болезнь Паркинсона, болезнь Альцгеймера, ОНМК, энцефалопатии).
- При аутоиммунных заболеваниях (ревматоидный артрит, системная красная волчанка, диффузная склеродермия).
- При бесплодии и привычном невынашивании беременности.
- При хронических инфекциях и воспалительных процессах.
- При подозрении на врождённый дефицит ферментов.
Что означают результаты?
Референсные значения: 2.2 – 4.8 мкмоль/л.
При повышении результата относительно референсного диапазона можно рассматривать процесс перекисного окисления липидов как фактор развития или прогрессирования какого-либо патологического процесса. Это позволяет подбирать терапию, исходя из патогенетического процесса, т.е. механизма развития патологии, что делает ее наиболее оптимальной.
Также рекомендуется
- Клинический анализ крови: общий анализ, лейкоцитарная формула, СОЭ (с микроскопией мазка крови при выявлении патологических изменений)
- Базовые биохимические показатели
Кто назначает исследование?
Терапевт, врач общей практики, кардиолог, эндокринолог, онколог, пульмонолог, токсиколог, нутрициолог.
Литература
- Halliwell B, Chirico S. Lipid peroxidation: its mechanism, measurement, and significance. Am J Clin Nutr. 1993 May; 57.
- Ramana KV, Srivastava S, Singhal SS. Lipid peroxidation products in human health and disease 2014. Oxid Med Cell Longev. 2014;2014:162414.
- Niki E. Lipid peroxidation products as oxidative stress biomarkers. Biofactors. 2008;34(2):171-80.
- Gaschler MM, Stockwell BR. Lipid peroxidation in cell death. Biochem Biophys Res Commun. 2017 Jan 15; 482(3):419-425.
Холестерин
Холестерин — это вещество, необходимое организму для строительства клеточных мембран, синтеза желчных кислот, выработки гормонов и витамина D. С химической точки зрения холестерин является жироподобным веществом — липидом (от греческого «lipid» — жир).
 Являясь жироподобным веществом, нерастворимым в воде, он переносится по кровеносным сосудам только в составе комплексов с белками – хиломикронов и липопротеидов. Главными переносчиками холестерина в организме являются липопротеиды. Липопротеиды (белково-липидные комплексы) различаются по размеру, плотности и содержанию липидов.
Являясь жироподобным веществом, нерастворимым в воде, он переносится по кровеносным сосудам только в составе комплексов с белками – хиломикронов и липопротеидов. Главными переносчиками холестерина в организме являются липопротеиды. Липопротеиды (белково-липидные комплексы) различаются по размеру, плотности и содержанию липидов.По плотности липопротеиды разделяются на следующие классы:
• липопротеиды очень низкой плотности (ЛПОНП)
• липопротеиды промежуточной плотности (ЛППП)
• липопротеиды низкой плотности (ЛПНП)
• липопротеиды высокой плотности (ЛПВП)
Соотношение жиров (липидов) и белков в липопротеидах различно. Минимальное количество белка содержится в хиломикронах. Возрастание плотности липопротеидов характеризуется увеличением содержания в них белкового компонента, как показано в таблице.
Процентный состав липопротеидов плазмы крови
(G.R. Thompson, 1991)
| Тип | Липиды | Белки |
| Хиломикроны | 98–99% | 1–2% |
| ЛПОНП | 90% | 10% |
| ЛППП | 82% | 18% |
| ЛПНП | 75% | 25% |
Липопротеиды различаются по их роли в развитии атеросклероза.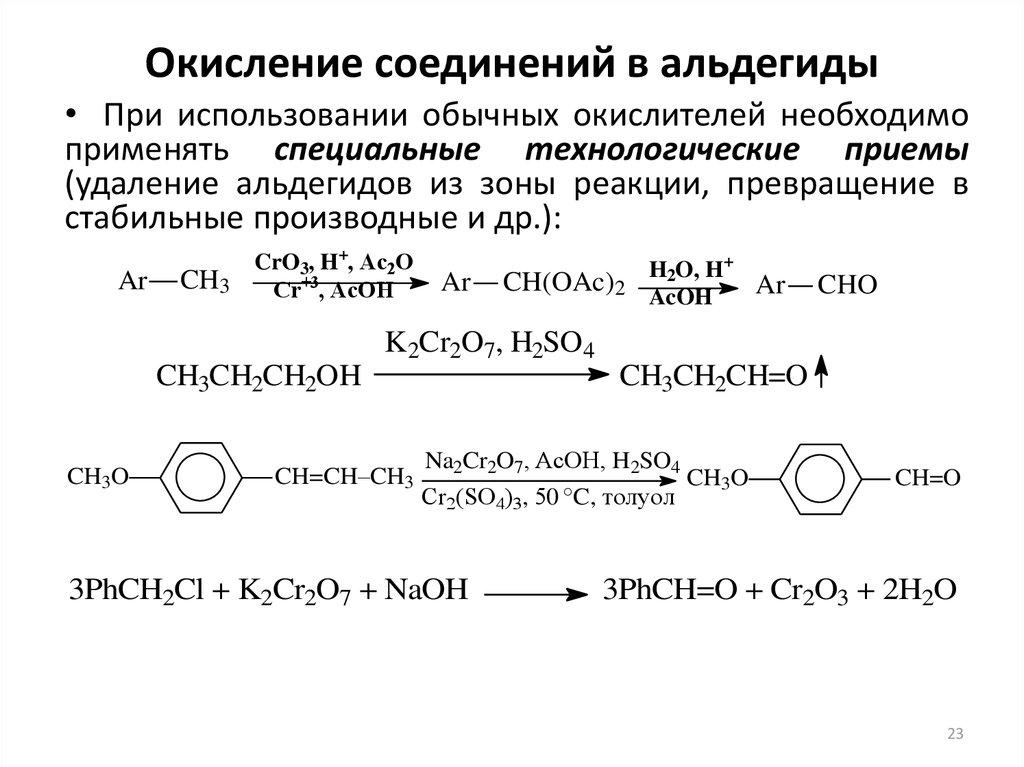 Так, липопротеиды низкой и очень низкой плотности считаются атерогенными (способствующими развитию атеросклероза), а содержащийся в них холестерин называют «плохим» холестерином. ЛПОНП и ЛПНП транспортируют холестерин из печени в клетки и ткани организма.
Так, липопротеиды низкой и очень низкой плотности считаются атерогенными (способствующими развитию атеросклероза), а содержащийся в них холестерин называют «плохим» холестерином. ЛПОНП и ЛПНП транспортируют холестерин из печени в клетки и ткани организма.
Липопротеиды высокой плотности (ЛПВП), напротив, считаются антиатерогенными (препятствующими развитию атеросклероза), а содержащийся в них холестерин называют «хорошим» холестерином. Липопротеиды высокой плотности (ЛПВП) за рубежом называют «полицейскими атеросклероза». Антиатерогенное действие ЛПВП проявляется благодаря их способности захватывать холестерин, выводить его из клеток, тканей, в том числе стенок артерий, и транспортировать обратно в печень.
В организме имеется три субстрата (или «пула»), где находится холестерин. Это плазма крови, печень, вернее — клетки печени (гепатоциты), и клетки других органов. Холестерин, находящийся в печени, находится в динамическом равновесии с холестерином плазмы крови. В зависимости от активности печеночных клеток количество (концентрация) холестерина плазмы крови может существенно меняться.
Содержание достаточного для организма количества холестерина поддерживается его постоянным синтезом
в клетках печени. Холестерин, образующийся в клетках печени, называют эндогенным холестерином. Холестерин также поступает в организм с пищей. Это так называемый экзогенный холестерин. Если экзогенного холестерина доставляется в печень много, то при нормальном обмене ограничивается синтез эндогенного холестерина.
Как уже отмечалось холестерин жироподобным веществом, нерастворимым в воде, он переносится по кровеносным сосудам только в составе комплексов с белками. Эти белково-липидные комплексы (ЛПОНП, ЛППП, ЛПНП и ЛПВП) также образуются в печени и затем поступают в кровоток.
Помимо перечисленных соединений в печени образуется еще один вид жиров, ассоциированных с риском развития атеросклероза. Это триглицериды. Они транспортируются к мышцам, накапливаются там, и при необходимости расщепляются, становясь источником энергии.
Обмен холестерина
Свободный холестерин подвергается окислению в печени и органах, синтезирующих стероидные гормоны (надпочечники, семенники, яичники, плацента). Это единственный процесс необратимого выведения холестерина из мембран и липопротеидных комплексов.
Это единственный процесс необратимого выведения холестерина из мембран и липопротеидных комплексов.
Ежедневно на синтез стероидных гормонов расходуется 2–4% от общего количества холестерина. В гепатоцитах 60–80% холестерина окисляется до желчных кислот, которые в составе желчи выделяются в просвет тонкой кишки и участвуют в пищеварении (эмульгирование жиров).
Вместе с желчными кислотами в тонкую кишку попадает небольшое количество свободного холестерина, который частично удаляется с каловыми массами, а оставшаяся часть его растворяется и вместе с желчными кислотами и фосфолипидами всасывается стенками тонкой кишки. Желчные кислоты обеспечивают разложение жиров на составные части (эмульгирование жиров). После выполнения этой функции 70–80% оставшихся желчных кислот всасывается в конечном отделе тонкой кишки (подвздошной кишке) и поступает по системе воротной вены в печень. Здесь стоит отметить, что желчные кислоты имеют еще одну функцию: они являются важнейшим стимулятором поддержания нормальной работы (моторики) кишечника.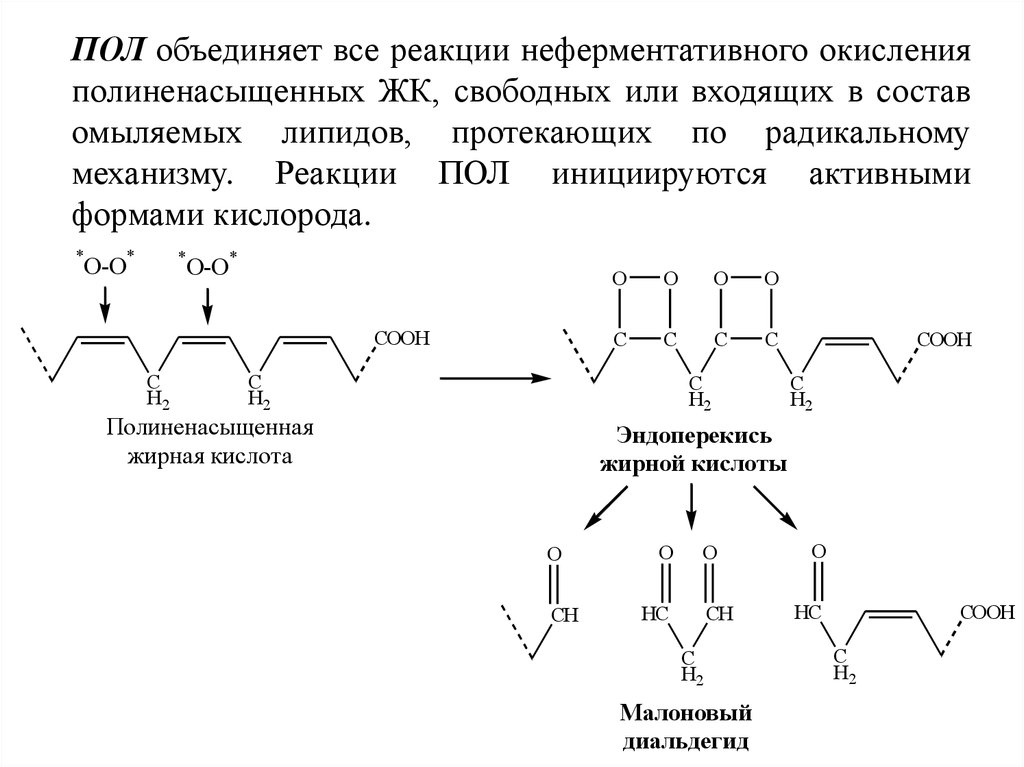
Схематично обмен холестерина можно представить так. Печень нагружает жиром липопротеиды очень низкой плотности (ЛПОНП), которые потом путешествуют по кровеносным сосудам, разгружая жир. Частично «разгрузившиеся» ЛПОНП становятся липопротеидами низкой плотности (ЛПНП).
Липопротеиды низкой плотности (ЛПНП), главные переносчики холестерина при их движении по кровеносным сосудам, могут прилипать
к стенкам сосудов, сужая их внутренний просвет.
Липопротеиды высокой плотности (ЛПВП) освобождают прилипшие к стенке сосуда частицы ЛПНП с холестерином и несут их обратно в печень, где частицы ЛПНП снова нагружаются холестерином и превращаются в ЛПОНП, либо распадаются и выводятся из организма.
При активном потреблении жирной пищи и нарушениях жирового обмена печень вырабатывает избыточное количество липопротеидов очень низкой плотности (ЛПОНП) и низкой плотности (ЛПНП). При наличии повреждений эндотелия и отсутствии достаточного количества липопротеидов высокой плотности (ЛПВП), частицы липопротеидов низкой плотности (ЛПНП) с холестерином начинают «прилипать» к стенкам сосудов. Постепенно развивается сужение сосудов, т. е. атеросклероз, а следом все неприятности: стенокардия, инфаркт, инсульт и другие осложнения атеросклероза.
Постепенно развивается сужение сосудов, т. е. атеросклероз, а следом все неприятности: стенокардия, инфаркт, инсульт и другие осложнения атеросклероза.
Для чего определяют индекс атерогенности?
Для оценки выраженности атерогенных (способствующих развитию атеросклероза) свойств плазмы крови и степени риска развития клинических проявлений атеросклероза используются формулы, позволяющие рассчитать индекс атерогенности (ИА) по соотношению атерогенных и антиатерогенных фракций липопротеидов. Существует множество способов для вычисления индекса атерогенности.
Один из наиболее распространенных в мире – определение индекса атерогенности, как соотношения общего холестерина (ОХС) к холестерину ЛПВП (ОХС/ХС ЛПВП). Он свидетельствует об атерогенности липидного спектра крови при уровне > 5.
В России широко используют другое соотношение, называемое индексом атерогенности А. Н. Климова. Это отношение суммы холестерина атерогенных липопротеидов низкой плотности (ХС ЛПНП) и очень низкой плотности (ХС ЛПОНП) к холестерину антиатерогенных липопротеидов высокой плотности (ХС ЛПВП).
Индекс атерогенности (А.Н. Климова)= ХС ЛПНП + ХС ЛПОНП / ХС ЛПВП = ОХС – ХС ЛПВП / ХС ЛПВП
Обе формулы приведены потому, что они одинаковы. Дело в том, что общий холестерин (ОХС) состоит из ХС ЛПНП, ХС ЛПОНП и ХС ЛПВП.
Лабораториям в поликлинике или больнице для простоты вычисления индекса атерогенности достаточно определить в крови пациента уровни общего холестерина и холестерина ЛПВП. Если от уровня общего холестерина отнять показатель ХС ЛПВП, то получим сумму холестерина атерогенных липопротеидов – ЛПНП и ЛПОНП.
Нормальное значение индекса атерогенности А.Н. Климова — 3,0–4,0. Значение индекса атерогенности выше 4,0 указывает на высокий риск развития атеросклероза или возможность его прогрессирования вплоть до развития серьезных осложнений.
Высокий уровень холестерина – ключевой фактор риска атеросклероза
Еще в начале ХХ века петербургский ученый, основатель холестериновой теории атеросклероза Н. Н. Аничков говорил: «без высокого уровня холестерина в крови не бывает атеросклероза». С этим согласно большинство отечественных и зарубежных исследователей.
Н. Аничков говорил: «без высокого уровня холестерина в крови не бывает атеросклероза». С этим согласно большинство отечественных и зарубежных исследователей.
С начала прошлого века была установлена связь атеросклероза с повышенным содержанием в крови холестерина — химического соединения, необходимого для жизнедеятельности человеческого организма. В первую очередь, как уже отмечалось, он необходим как строительный материал для клеточных мембран. Кроме формирования каркаса клеток, организм использует холестерин для синтеза многих жизненно необходимых веществ, например, гормонов (кортикостероидов, андрогенов, эстрогенов и др.) и витаминов.
Таким образом, с одной стороны — жизнь без холестерина невозможна, с другой стороны — холестерин является едва ли не главной угрозой для современного человека. Это противоречие кажущееся, так как исследователями было установлено, что ответственным за возникновение и развитие атеросклероза является не сам холестерин, а повышенный уровень ряда его соединений с белками – ЛПОНП и ЛПНП в сочетании с пониженным уровнем ЛПВП.
К сожалению, люди, сами того не замечая, способствуют развитию атеросклероза. Как уже отмечалось ранее, еще в раннем детском возрасте на стенках сосудов могут образовываться жировые (или липидные) пятна. Если уровень холестерина в крови нормальный, то жировые пятна со временем исчезают и атеросклеротические бляшки не образуются. Но в условиях повышенного уровня холестерина, вернее холестерина ЛПОНП и ЛПНП, человек подвергается повышенному риску развития грозного по своему прогнозу заболевания. А если он еще и курит, имеет избыточный вес и повышенное артериальное давление, то риск развития атеросклероза возрастает в несколько раз. Все перечисленные факторы могут приводить к повреждению эндотелия (внутренней выстилки) сосудов, где начинается процесс образования атеросклеротических бляшек. Поэтому так важно знать пути профилактики и основы лечения «болезни века».
Риск развития осложнений атеросклероза особенно высок при тяжелых врожденных нарушениях липидного обмена, которые передаются по наследству и которыми, как правило, страдают все близкие родственники. Такие случаи принято относить к семейной гиперхолестеринемии, вызываемой наследственным дефектом рецепторов липопротеидов низкой плотности. Ген локализуется в 19-й хромосоме.
Различают гомозиготную и гетерозиготную семейную гиперхолестеринемию. При гетерозиготной гиперхолестеринемии общий холестерин бывает выше нормативных показателей в 2–3 раза, а при гомозиготной гиперхолестеринемии – в 4–6 и более раз. Оба эти состояния — предвестники раннего развития клинических проявлений атеросклероза в виде ишемической болезни сердца и даже — инфаркта миокарда.
Мы лечили семнадцатилетнюю (!) девушку, страдавшую тяжелой формой ишемической болезни сердца. У ее родителей также наблюдалось ранее развитие атеросклероза. Отец перенес инфаркт миокарда в 29 лет, мать была оперирована по поводу ишемической болезни сердца в 35 лет и в 40 лет — по поводу ишемической болезни головного мозга.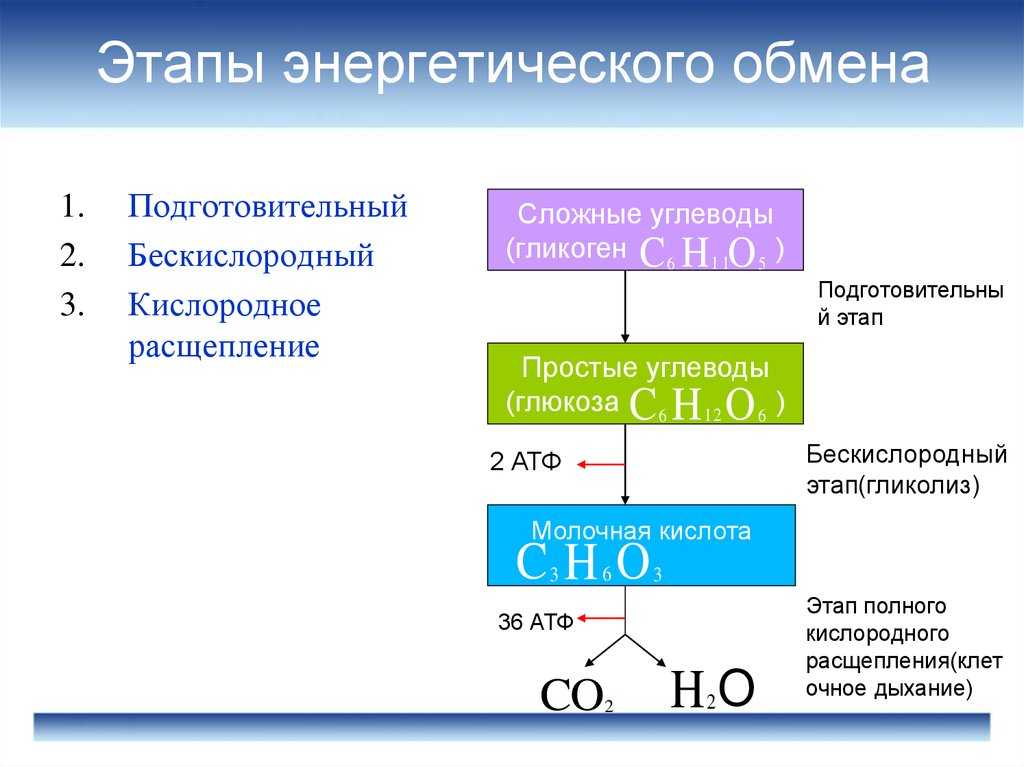
В предисловии к монографии, посвященной хирургической коррекции нарушений жирового обмена, изданной в 1987 г., академик А. Н. Климов пишет о девочке с гомозиготной семейной гиперхолестеринемией, которая в 6-летнем возрасте перенесла инфаркт миокарда, имея цифры холестерина плазмы крови в 10 раз превышающие нормальные.
При наследственной гиперхолестеринемии степень риска развития в молодом возрасте ишемической болезни сердца в 20 раз выше, чем у людей, имеющих нормальный липидный спектр крови.
Каким же образом нарушается липидный обмен при наследственной гиперхолестеринемии? В результате мутаций генов нарушается обмен липопротеидов низкой плотности – самых атерогенных липопротеидов. Этот механизм открыли во второй половине ХХ века американские ученые Браун и Гольдштейн, за что получили Нобелевскую премию. Как они выяснили, на поверхности большинства клеток организма имеются особые молекулы белка, называемые «рецепторами». Их задача — забирать из тока крови не все липопротеиды, а только липопротеиды низкой плотности (ЛПНП), богатые холестерином, и отправлять их внутрь клетки. Освободившись от холестерина, рецепторы возвращаются обратно на ее поверхность. Так как холестерина внутри клетки становится много, то угнетается его синтез самой клеткой и значит — уменьшается количество рецепторов к липопротеидам низкой плотности, находящихся на мембране. В течение суток эти рецепторы захватывают из плазмы крови до 1 г холестерина. Такой захват рецепторами липопротеидов низкой плотности обеспечивает нормальный уровень холестерина в крови, препятствуя развитию атеросклероза. Недостаток таких рецепторов находится в основе наследственной семейной гиперхолестеринемии.
Их задача — забирать из тока крови не все липопротеиды, а только липопротеиды низкой плотности (ЛПНП), богатые холестерином, и отправлять их внутрь клетки. Освободившись от холестерина, рецепторы возвращаются обратно на ее поверхность. Так как холестерина внутри клетки становится много, то угнетается его синтез самой клеткой и значит — уменьшается количество рецепторов к липопротеидам низкой плотности, находящихся на мембране. В течение суток эти рецепторы захватывают из плазмы крови до 1 г холестерина. Такой захват рецепторами липопротеидов низкой плотности обеспечивает нормальный уровень холестерина в крови, препятствуя развитию атеросклероза. Недостаток таких рецепторов находится в основе наследственной семейной гиперхолестеринемии.
Мы не будем останавливаться очень подробно на механизме различных видов семейной гиперхолестеринемии, но отметим, что существует 5 типов мутаций, при которых рецепторы к липопротеидам низкой плотности не работают.
Частота гетерозиготной семейной гиперхолестеринемии составляет 1:500, гомозиготной семейной гиперхолестеринемии — 1: 1 000 000 жителей нашей планеты, и люди, имеющие их, обязательно заболевают атеросклерозом, даже если соблюдают низкохолестериновую диету. Чтобы в молодом возрасте не возникли тяжелейшие клинические проявления атеросклероза (например, инфаркт миокарда и другие), они обречены на пожизненный прием лекарственных препаратов, нормализующих липидный обмен.
Чтобы в молодом возрасте не возникли тяжелейшие клинические проявления атеросклероза (например, инфаркт миокарда и другие), они обречены на пожизненный прием лекарственных препаратов, нормализующих липидный обмен.
Таким образом, в основе развития атеросклероза лежат процессы, связанные с нарушением жирового (липидного) обмена. Они проявляются различным соотношением липидов и липопротеидов и называются дислипидемиями.
Наиболее часто встречаются дислипидемии, обусловленные нарушением синтеза и замедлением распада липидов, снижением активности мембранных транспортных систем, обеспечивающих перенос холестерина и триглицеридов из клетки.
Различают первичные и вторичные дислипидемии. Первичные дислипидемии — это самостоятельные нарушения процессов синтеза и распада липопротеидов, связанные как с особенностями образа жизни, так и с генетически обусловленными метаболическими дефектами. Вторичные дислипидемии возникают на фоне различных заболеваний, в том числе гормональных (гипотиреоз, беременность), метаболических (сахарный диабет, ожирение, подагра), почечных (нефротический синдром, хроническая почечная недостаточность), токсикозависимостей (алкоголь).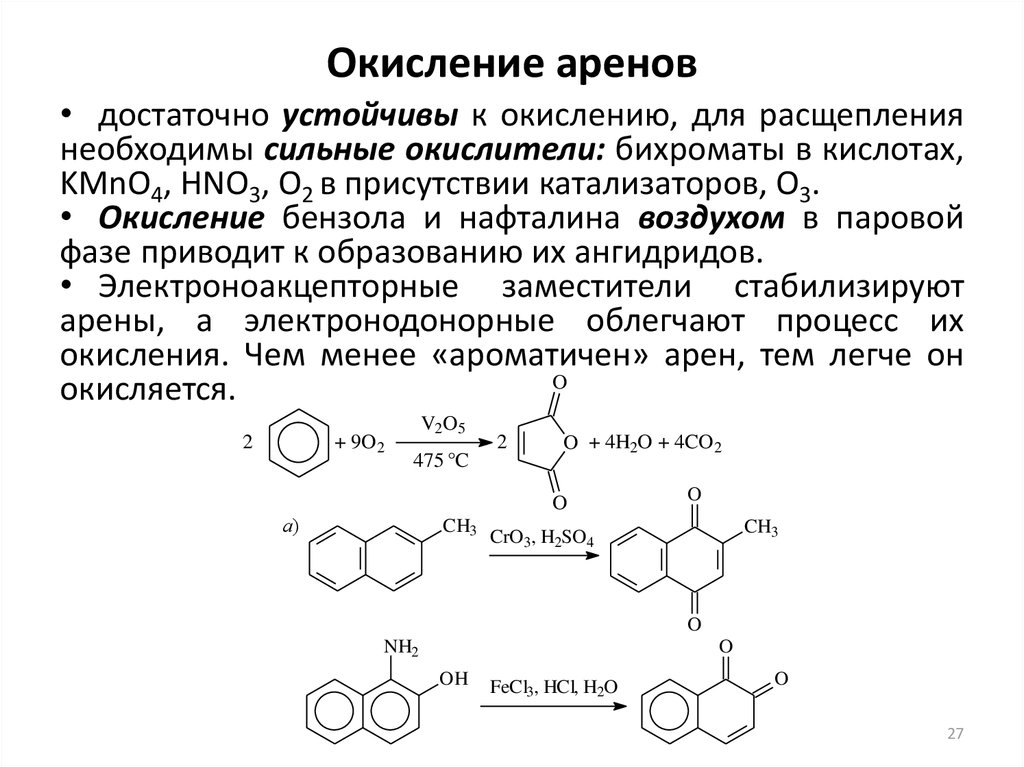
Какой уровень холестерина считается нормальным?
Первым шагом в соблюдении правил по снижению уровня холестерина является проверка его содержания в крови. Анализ на содержание холестерина в крови выполняется практически во всех поликлиниках и больницах бесплатно или за небольшую плату.
Анализ крови на содержание в ней холестерина обычно не требует предварительной подготовки, но выполняется это исследование натощак, через 10 часов после последнего приема пищи. Берется небольшое количество крови, которое исследуется сразу же экспресс-методом или посылается в лабораторию. Если исследование проводится экспересс-методом, то ответ выдается сразу же. Если выполняется развернутый анализ (липидограмма), кровь отсылается в лабораторию, и ответ может быть готов на следующий день или через день.
Запомните уровень своего холестерина и его компонентов.
Самый простой анализ – это определение уровня общего холестерина.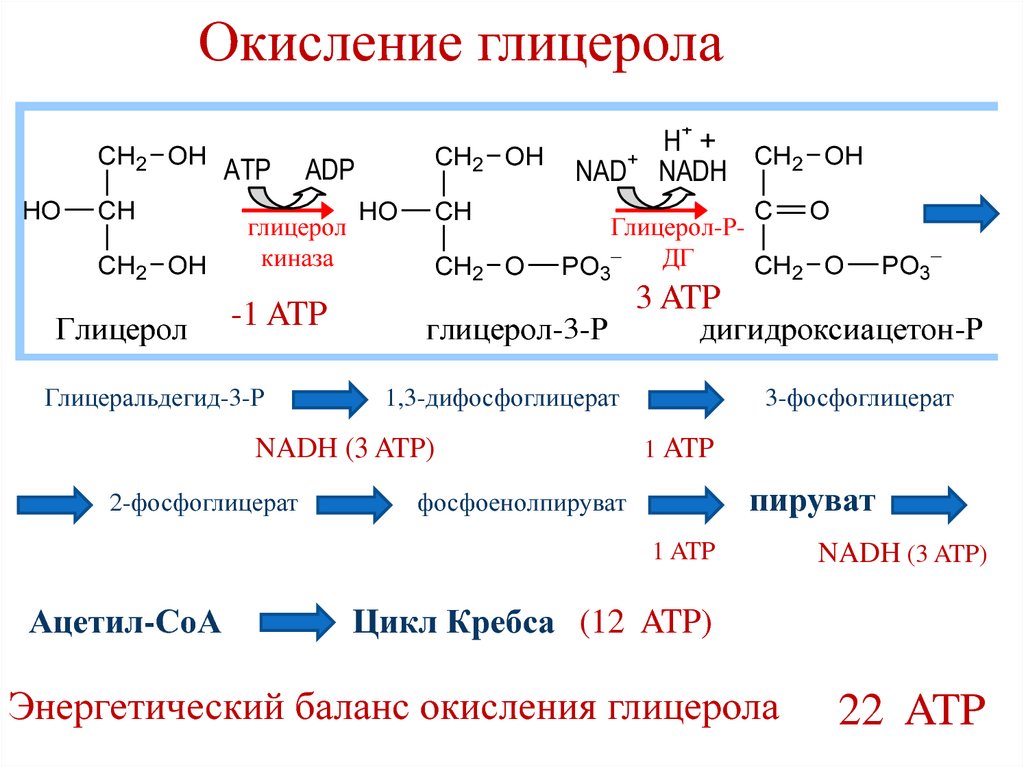 Общий холестерин (ОХС) складывается из холестерина липопротеидов низкой плотности (ЛПНП), липопротеидов очень низкой плотности (ЛПОНП) и липопротеидов высокой плотности (ЛПВП):
Общий холестерин (ОХС) складывается из холестерина липопротеидов низкой плотности (ЛПНП), липопротеидов очень низкой плотности (ЛПОНП) и липопротеидов высокой плотности (ЛПВП):
ОХС = ХС ЛПНП + ХС ЛПОНП + ХС ЛПВП
Поговорим о нормативах липидного спектра крови. Количество холестерина и липопротеидов измеряется в миллимолях на литр (ммоль/л) или в миллиграмм на децилитр (мг/дл). Какой уровень показателей липидного спектра считается нормальным?
Нормативы разные для здоровых людей, имеющих низкий риск сердечно-сосудистых заболеваний, и больных сердечно-сосудистыми заболеваниями.
Итак, нормативы липидного спектра крови для здоровых людей:
Общий холестерин (ОХС) < 5,0 ммоль/л (< 190 мг/дл)
Холестерин ЛПНП (ХС ЛПНП) < 3,0 ммоль/л (< 115 мг/дл)
Холестерин ЛПВП (ХС ЛПВП) > 1,0 ммоль/л (> 40 мг/дл) у мужчин
Холестерин ЛПВП (ХС ЛПВП) > 1,2 ммоль/л (> 45 мг/дл) у женщин
Триглицериды (ТГ) < 1,7 ммоль/л (< 150 мг/дл)
Нормативы липидного спектра крови для больных ишемической болезнью сердца и больных диабетом:
Общий холестерин (ОХС) < 4,5 ммоль/л (< 175 мг/дл)
Холестерин ЛПНП (ХС ЛПНП) < 1,8 ммоль/л (< 70 мг/дл)
Холестерин ЛПВП (ХС ЛПВП) > 1,0 ммоль/л (> 40 мг/дл) у мужчин
Холестерин ЛПВП (ХС ЛПВП) > 1,2 ммоль/л (> 45 мг/дл) у женщин
Триглицериды (ТГ) < 1,7 ммоль/л (< 150 мг/дл)
Если у пациента выявлена гиперхолестеринемия, принято определять ее степень выраженности.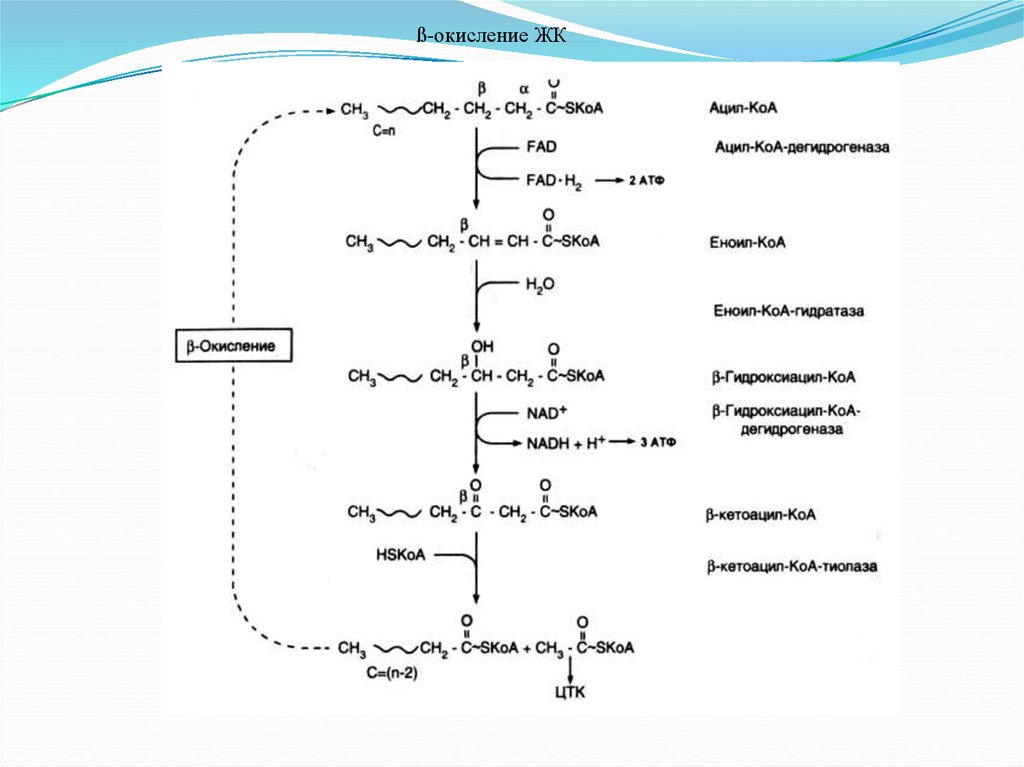 Различают 3 степени гиперхолестеринемии:
Различают 3 степени гиперхолестеринемии:
• легкая гиперхолестеринемия при уровне общего холестерина (ОХС) крови 5,0 < ОХС < 6,5 ммоль/л (190 < ОХС < 250 мг/дл)
• умеренная гиперхолестеринемия при 6,5 < ОХС < 7,8 ммоль/л (250 < ОХС < 300 мг/дл)
• выраженная гиперхолестеринемия при уровне ОХС > 7,8 ммоль/л (ОХС > 300 мг/дл)
Процесс окисления жиров и масел
Окисление жиров является одной из основных причин порчи пищевых продуктов наряду с действием микроорганизмов. Это приводит к изменению аромата и вкуса, цвета, потере некоторых питательных веществ и образованию потенциально вредных веществ, что приводит к сокращению срока годности пищевых продуктов . Этот процесс имеет важные экономические последствия, поскольку продукт становится непригодным для употребления в пищу .
Окислительный процесс жиров вызывает снижение питательной способности пищевых продуктов за счет разрушения жирорастворимых витаминов и разложения полиненасыщенных кислот.
Безопасность пищевых продуктов также может быть затронута, поскольку продукты окисления могут представлять токсичность, некоторые летучие продукты, пероксиды, оксикислоты и т. д. использование антиоксидантных веществ . Для этого сосредоточимся на процессе окисления жиров и основных факторах, влияющих на окисление жиров.
Основная форма окисления липидов происходит посредством свободнорадикальной реакции продолжения цепи , в которой пероксиды и гидропероксиды образуются из жирных кислот и кислорода, что известно как процесс самоокисления . Эти соединения довольно нестабильны, поэтому их можно разрушить, что приведет к образованию большего количества свободных радикалов и возникновению цепной реакции.
Исторически считалось, что добавление кислорода к молекуле жирной кислоты приводит к образованию четырехатомного кольца в качестве основного продукта реакции. Эта молекула называется «пероксид».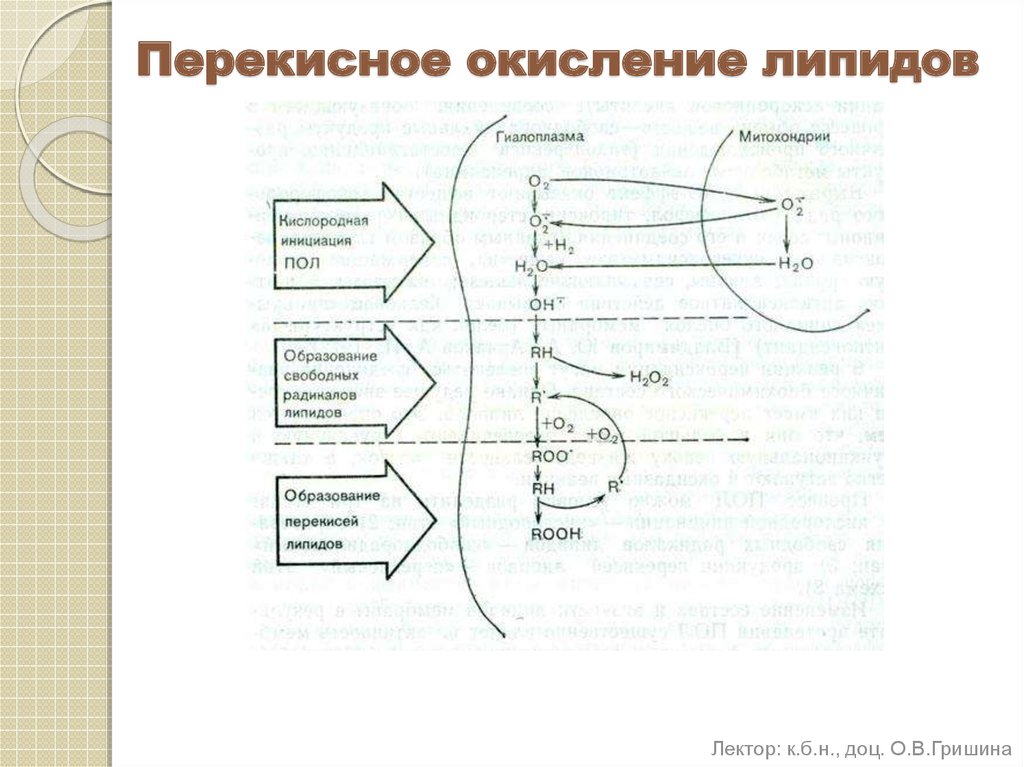 Однако на самом деле образуется гидропероксид из-за присоединения кислорода к альфа-углероду двойной связи. Несмотря на это, ошибочное представление до сих пор сохраняется и пероксиды по-прежнему относятся к продуктам распада жира.
Однако на самом деле образуется гидропероксид из-за присоединения кислорода к альфа-углероду двойной связи. Несмотря на это, ошибочное представление до сих пор сохраняется и пероксиды по-прежнему относятся к продуктам распада жира.
Самоокисление – это необратимый процесс окисления жиров . Полностью избежать его невозможно, но его можно отсрочить за счет добавления антиоксидантов .
Процесс окисления жировМеханизм окисления состоит из трех фаз :
- Индукция : инициаторами обычно являются энергия (свет, тепло и т. д.), следы тяжелых металлов и радикалов пероксиды, вызывающие образование активных свободных радикалов. Действие энергии вызывает разложение жирной кислоты на свободный радикал и ион водорода.
- Размножение : при окислении свободных радикалов в сочетании с другими жирными кислотами образуются гидропероксиды и другие свободные радикалы, которые вновь вступают в цепь окисления.
 С другой стороны, гидропероксиды с выделением энергии образуют оксидрильные группы и окисленную форму свободных радикалов, которые вместе с другими жирными кислотами приводят к образованию большего количества гидропероксидов и новых свободных радикалов. Наконец, оксидрильные группы вместе с другими жирными кислотами высвобождают воду и новые свободные радикалы, подвергающиеся новому окислению.
С другой стороны, гидропероксиды с выделением энергии образуют оксидрильные группы и окисленную форму свободных радикалов, которые вместе с другими жирными кислотами приводят к образованию большего количества гидропероксидов и новых свободных радикалов. Наконец, оксидрильные группы вместе с другими жирными кислотами высвобождают воду и новые свободные радикалы, подвергающиеся новому окислению. - Конец : количество реактивных соединений огромно и они начинают взаимодействовать друг с другом. Концентрация перекисных радикалов падает по мере стабилизации образования продуктов распада. Учитывая стабильность продуктов, возникающих в реакциях обрыва, окислительная активность прекращается. На автоокисление жиров по-прежнему влияют свободные радикалы, а также воздействие температуры и света. Образование новых цепей способствует ускорению общей реакции, кроме того, реакционная способность повышается в присутствии некоторых металлов, таких как медь и железо.
После полного разрушения жирных кислот образуются вторичные продукты окисления , которые ответственны за возникновение прогорклости .
Чтобы задержать или предотвратить окисление жиров и прогорклость пищевых продуктов, необходимо знать ч способ предотвращения образования первых свободных радикалов или первых гидропероксидов , так как это может быть достигнуто только на первой стадии окислительный процесс, во время инициации. Наоборот, как только окислительный процесс достигает фазы распространения, этот процесс больше не может быть задержан или остановлен.
Вас может заинтересовать: Физические свойства масел и жиров
9000 3 Факторы, влияющие на окисление
Факторы, влияющие на окисление, могут быть внутренними и/или внешними по отношению к продукты питания , то есть они могут относиться к продукту и применяемой технологии. Некоторые из наиболее важных из них перечислены ниже (д-р Паукар Пеначо, Ухудшение состояния агропромышленных продуктов, 2014 г. ):
):
- Температура : скорость самоокисления увеличивается с температурой. Он может влиять не только на скорость автоокисления, но и на механизмы реакции.
- Светлый : жирные кислоты и их пероксиды представляют собой бесцветные вещества, не поглощающие видимый свет. Таким образом, если нет дополнительного сенсибилизатора, можно предположить, что влияние видимого света на автоокисление не имеет большего значения. Однако ультрафиолетовый свет сильно поглощается ненасыщенными соединениями.
- Кислород : скорость самоокисления увеличивается с увеличением давления кислорода, пока не достигнет постоянной скорости реакции.
- Влажность : влияние активности воды на скорость окисления липидов очень сложное. Прогорклость быстро развивается как при очень высоком, так и при очень низком уровне влажности. Максимальная стабильность наблюдается при промежуточных уровнях влажности, соответствующих значениям монослоя (защитное действие воды в виде монослоя).

- Ионизирующее излучение : одним из наиболее заметных эффектов высокоэнергетического облучения пищевых продуктов является заметное повышение восприимчивости к окислительному прогорклости.
- Катализаторы : ионы тяжелых металлов являются мощными катализаторами окисления липидов, уменьшают индукционный период и увеличивают скорость реакции.
В заключение укажем, что для ингибирования, снижения или задержки окисления липидов необходимо воздействовать на один или несколько факторов, способствующих его развитию .
В широком смысле он считается антиоксидантом любым веществом или процессом действия, помогающим ограничить скорость и/или расширение окислительных процессов . В соответствии с этой концепцией можно было бы рассмотреть три типа антиоксидантов в зависимости от механизма их действия. Первые два типа связаны с добавлением химических соединений, а третий обязан своим действием модификациям определенных факторов в пище и/или при ее обработке.
В следующих статьях мы подробно проанализируем классификацию и действие антиоксидантов для использования в пищевых продуктах .
Загрузите нашу электронную книгу и узнайте, как выбрать идеальный антиоксидант для вашего продукта !
СКАЧАТЬ ЭЛЕКТРОННУЮ КНИГУ
Окисление липидов в пищевых системах
LO ● + Fe 2+ + H + 90 152 —→ LOH + Fe 3+
Трехвалентное железо (Fe3+ ) Уравнения (3) и (4) образуют комплексы с тиоцианатом, а поглощение при 500 нм определяет количество гидропероксида, присутствующего в образце [9] . Конечное количество окисленного Fe2+ зависит от природы растворителя и количества присутствующего LOOH. Однако количество окисленного двухвалентного железа зависит от количества LOOH, присутствующего в образце, при одинаковых условиях растворения. Метод тиоцианата железа проще йодометрического, а двухвалентное железо менее чувствительно к кислороду, чем йодид [10] . Этот метод также успешно использовался для определения уровней окисления липидов в пищевых продуктах, приготовленных из насекомых 9.0151 [11] [12] . Этот метод является простым, быстрым и чувствительным и чувствителен к гидропероксидам моно- и полиненасыщенных жирных кислот (ПНЖК).
Этот метод также успешно использовался для определения уровней окисления липидов в пищевых продуктах, приготовленных из насекомых 9.0151 [11] [12] . Этот метод является простым, быстрым и чувствительным и чувствителен к гидропероксидам моно- и полиненасыщенных жирных кислот (ПНЖК).
2.1.2. Анализ сопряженных диенов
Автоокисление представляет собой цепную реакцию полиненасыщенных жирных кислот. Когда атом водорода отрывается от ПНЖК реактивным кислородом (например, гидроксильным радикалом), двойная связь, соседствующая с лишенным кислорода углеродом, перемещается к другой двойной связи и образует сопряженные диены, что стабилизирует молекулу [4] . В присутствии кислорода пероксильный радикал ПНЖК превращает свободный радикал в новую ПНЖК, и она становится гидропероксидом с конъюгированной формой ПНЖК. Таким образом, анализ сопряженного диена представляет степень окисления на ранней стадии. Сопряженные диены поглощают при 233 нм и, таким образом, могут быть оценены путем регистрации увеличения поглощения экстрагированных липидов при длине волны 90–151 [13] 90–152 .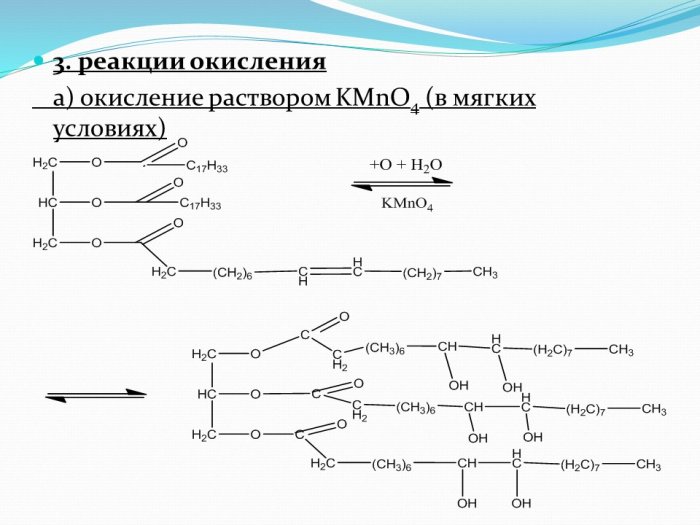 Этот метод прост и определяет все сопряженные формы диенов в липидах на ранней стадии окисления липидов. Результаты диеновой конъюгации хорошо согласуются с перекисным и йодным числами [14] . Однако пик диеновой конъюгации отчетлив при 233 нм, выделяется только в полностью пероксидированных липидах, а в частично пероксидированных липидах пик становится нечетким из-за неперекисного липида и экстрагированных примесей 90–151 [6] 90–152 .
Этот метод прост и определяет все сопряженные формы диенов в липидах на ранней стадии окисления липидов. Результаты диеновой конъюгации хорошо согласуются с перекисным и йодным числами [14] . Однако пик диеновой конъюгации отчетлив при 233 нм, выделяется только в полностью пероксидированных липидах, а в частично пероксидированных липидах пик становится нечетким из-за неперекисного липида и экстрагированных примесей 90–151 [6] 90–152 .
2.2. Прямые методы определения вторичных продуктов окисления
Несмотря на простоту определения степени окисления с использованием первичных соединений, во время окисления образуется большое количество вторичных (деградированных) продуктов. Многие методы применяются на основе продуктов вторичного разложения, но в этом обзоре обсуждаются наиболее распространенные методы для пищевых продуктов растительного и животного происхождения.
2.2.1. Метод реактивных веществ с тиобарбитуровой кислотой (TBARS)
Анализ тиобарбитуровых реактивных веществ (ТБАРС) является одним из самых популярных методов определения окисления липидов в мясных и рыбных продуктах. Малоновый альдегид (МА) — альдегид, образующийся при расщеплении ненасыщенных жирных кислот [15] [16] [17] . Одна молекула МА реагирует с двумя молекулами тиобарбитуровой кислоты при нагревании в кислом растворе с образованием уникального соединения основания Шиффа, дающего розовую окраску, а окраска может быть измерена с помощью видимого (при 532–535 нм) или флуоресцентного (возбуждение 515 нм, эмиссия 553 нм) спектрофотометры [16] [17] .
Малоновый альдегид (МА) — альдегид, образующийся при расщеплении ненасыщенных жирных кислот [15] [16] [17] . Одна молекула МА реагирует с двумя молекулами тиобарбитуровой кислоты при нагревании в кислом растворе с образованием уникального соединения основания Шиффа, дающего розовую окраску, а окраска может быть измерена с помощью видимого (при 532–535 нм) или флуоресцентного (возбуждение 515 нм, эмиссия 553 нм) спектрофотометры [16] [17] .
Абсорбционная спектрометрия
Образование хромогена в результате реакции тиобарбитуровой кислоты (ТБК) и МА показано на Рис. 2 [18] . Скорость реакции зависит от концентрации ТБК, pH и используемой температуры [19] . МА можно экстрагировать перегонкой или раствором кислоты перед реакцией с TBA [20] . ТВА добавляют к гомогенату образца для реакции с МА в образце [6] [21] напрямую.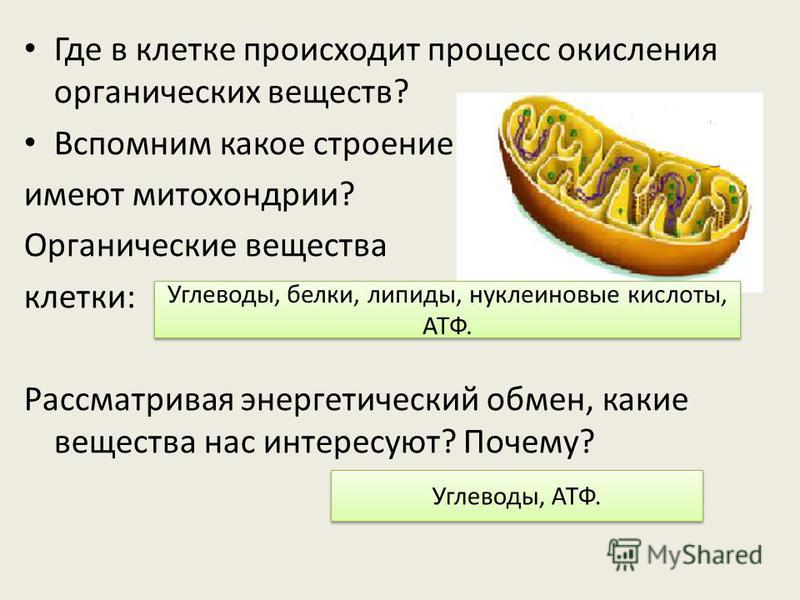 Метод дистилляции обычно используется для сырых, вяленых и вареных мясных продуктов, но это трудоемкий метод. В этом методе МА экстрагируют трихлоруксусной кислотой (ТХУ) с контролируемой скоростью, собирают дистиллят, вводят в реакцию с ТВА и измеряют оптическую плотность с помощью спектрофотометра [22] . Кислотная экстракция используется в основном для образцов сырого и вареного мяса и рыбы, в которых используется 7,5% ТХУ, с последующей фильтрацией и реакцией с ТБА на кипящей водяной бане в течение 30–40 мин [17] . Этот метод также использовался для определения окисления липидов в пищевых продуктах на основе насекомых [11] [12] . В методе прямой реакции два объема раствора ТБК/ТХК (15% ТХУ/20 мМ ТБК) добавляют к одному объему гомогената образца и проводят реакцию при температуре кипения в течение 15 мин. Окраску супернатанта собирают после центрифугирования и измеряют оптическую плотность с помощью спектрофотометра при 532 нм. Количественное определение МА в мясе проводится с использованием стандартной кривой и выражается в мг МДА/кг пищи [23] [24] .
Метод дистилляции обычно используется для сырых, вяленых и вареных мясных продуктов, но это трудоемкий метод. В этом методе МА экстрагируют трихлоруксусной кислотой (ТХУ) с контролируемой скоростью, собирают дистиллят, вводят в реакцию с ТВА и измеряют оптическую плотность с помощью спектрофотометра [22] . Кислотная экстракция используется в основном для образцов сырого и вареного мяса и рыбы, в которых используется 7,5% ТХУ, с последующей фильтрацией и реакцией с ТБА на кипящей водяной бане в течение 30–40 мин [17] . Этот метод также использовался для определения окисления липидов в пищевых продуктах на основе насекомых [11] [12] . В методе прямой реакции два объема раствора ТБК/ТХК (15% ТХУ/20 мМ ТБК) добавляют к одному объему гомогената образца и проводят реакцию при температуре кипения в течение 15 мин. Окраску супернатанта собирают после центрифугирования и измеряют оптическую плотность с помощью спектрофотометра при 532 нм. Количественное определение МА в мясе проводится с использованием стандартной кривой и выражается в мг МДА/кг пищи [23] [24] . Метод TBARS является легким, простым, недорогим и воспроизводимым, а его значения хорошо коррелируют с сенсорными свойствами конечного продукта. Однако ТБК может реагировать с другими окисленными соединениями в пищевом продукте и давать ложноположительные результаты [19] [16] [25] . Нитриты, используемые в вяленых мясных продуктах, могут вступать в реакцию с МА в кислых условиях и имеют более низкие значения в вяленых мясных продуктах. Следовательно, добавление сульфаниламида необходимо как для методов дистилляции, так и для методов экстракции [15] [16] . Образование желтого или оранжевого хромогена является еще одним недостатком этого теста и в основном связано с реакцией сахаров (сахарозы, глюкозы и фруктозы), водорастворимых белков, пептидов и свободных аминокислот, таких как Lys и Arg, в мясе. и мясные продукты с TBA. Помимо углеводов, пигменты фенилпропаноидного типа также могут проявлять поглощение при 532 нм, что приводит к завышению оценки окисления [19] .
Метод TBARS является легким, простым, недорогим и воспроизводимым, а его значения хорошо коррелируют с сенсорными свойствами конечного продукта. Однако ТБК может реагировать с другими окисленными соединениями в пищевом продукте и давать ложноположительные результаты [19] [16] [25] . Нитриты, используемые в вяленых мясных продуктах, могут вступать в реакцию с МА в кислых условиях и имеют более низкие значения в вяленых мясных продуктах. Следовательно, добавление сульфаниламида необходимо как для методов дистилляции, так и для методов экстракции [15] [16] . Образование желтого или оранжевого хромогена является еще одним недостатком этого теста и в основном связано с реакцией сахаров (сахарозы, глюкозы и фруктозы), водорастворимых белков, пептидов и свободных аминокислот, таких как Lys и Arg, в мясе. и мясные продукты с TBA. Помимо углеводов, пигменты фенилпропаноидного типа также могут проявлять поглощение при 532 нм, что приводит к завышению оценки окисления [19] .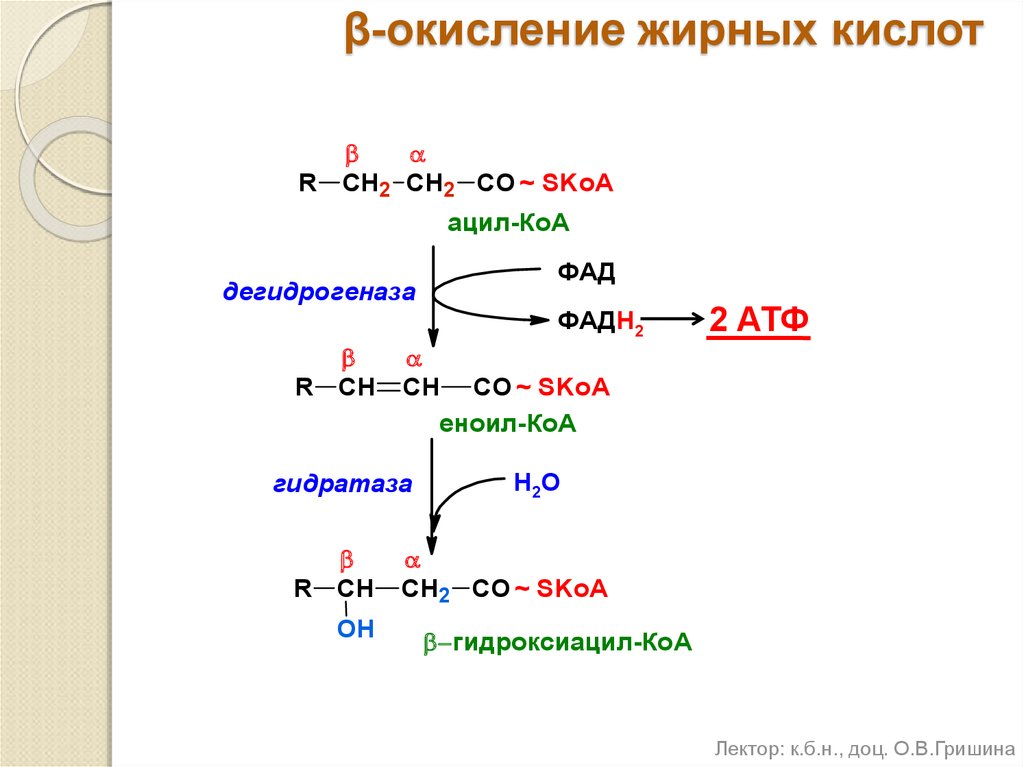 МДА также может быть преобразован в другие органические соединения при хранении в рыбе и рыбных продуктах, что приводит к низкому значению МДА [26] . Таким образом, метод TBARS непригоден для определения уровня окисления пищевых продуктов с высоким содержанием углеводов и яичного желтка.
МДА также может быть преобразован в другие органические соединения при хранении в рыбе и рыбных продуктах, что приводит к низкому значению МДА [26] . Таким образом, метод TBARS непригоден для определения уровня окисления пищевых продуктов с высоким содержанием углеводов и яичного желтка.
Рисунок 2. Формирование хромофора во время анализа TBARS.
Флуорометрическая спектрометрия
Флуорометрическое измерение TBARS началось с наблюдения Bernheim et al. [27] , который обнаружил, что при окислении ненасыщенных жирных кислот образуются 3 атома углерода, предположительно МА, которые реагируют с ТБК и дают красный пигмент [27] . Однако многие компоненты пищевых продуктов, такие как аминокислоты, белки и углеводы, могут реагировать с TBA [28] [29] . Yagi модифицировал флуорометрический метод TBARS для определения уровня перекиси в сыворотке или плазме с помощью флуорометра. Он собрал водорастворимые TBARS в образцах сыворотки или плазмы путем осаждения белков и продуктов окисления липидов в кислых условиях. Затем осадок собирали, суспендировали в дистиллированной воде и реагировали с ТВА при 95°С в течение 1 часа. Продукты реакции экстрагировали н-бутанолом и измеряли интенсивность флуоресценции при 553 нм с возбуждением при 515 нм [30] . Флюорометрический метод Яги обладал большей чувствительностью, чем спектрофотометрический метод, но не подходил для мяса. Так, Джо и Ан [15] дополнительно модифицировали метод Яги для использования в мясе. Они непосредственно добавляли ТВА к мясным гомогенатам в кислых условиях, а затем подвергали их реакции при 90 °C в течение 15 минут, экстрагировали прореагировавшие продукты окисления липидов, используя смесь н-бутанола и пиридина, а затем измеряли интенсивность флуоресценции при 550 нм с помощью 520 нм. возбуждение нм. Флюорометрические методы показали высокую чувствительность при незначительном влиянии мясных компонентов [15] .
Он собрал водорастворимые TBARS в образцах сыворотки или плазмы путем осаждения белков и продуктов окисления липидов в кислых условиях. Затем осадок собирали, суспендировали в дистиллированной воде и реагировали с ТВА при 95°С в течение 1 часа. Продукты реакции экстрагировали н-бутанолом и измеряли интенсивность флуоресценции при 553 нм с возбуждением при 515 нм [30] . Флюорометрический метод Яги обладал большей чувствительностью, чем спектрофотометрический метод, но не подходил для мяса. Так, Джо и Ан [15] дополнительно модифицировали метод Яги для использования в мясе. Они непосредственно добавляли ТВА к мясным гомогенатам в кислых условиях, а затем подвергали их реакции при 90 °C в течение 15 минут, экстрагировали прореагировавшие продукты окисления липидов, используя смесь н-бутанола и пиридина, а затем измеряли интенсивность флуоресценции при 550 нм с помощью 520 нм. возбуждение нм. Флюорометрические методы показали высокую чувствительность при незначительном влиянии мясных компонентов [15] . Для сравнения, флуорометрические методы Яги, Джо и Ана более чувствительны, чем обычные спектрофотометрические методы, и подходят для образцов с низким уровнем TBARS, таких как сыворотка крови и образцы свежего мяса [15] [30] .
Для сравнения, флуорометрические методы Яги, Джо и Ана более чувствительны, чем обычные спектрофотометрические методы, и подходят для образцов с низким уровнем TBARS, таких как сыворотка крови и образцы свежего мяса [15] [30] .
2.2.2. Хроматографические методы
Поскольку традиционные методы TBARS обладают недостаточной специфичностью и чувствительностью, были разработаны альтернативные аналитические подходы. Хроматографические методы разработаны для определения первичных и вторичных продуктов окисления, присутствующих в пищевых продуктах. Какуда и др. [31] разработали метод ВЭЖХ для оценки количества МА в водных дистиллятах куриного мяса. Они обнаружили, что ВЭЖХ более чувствительна, чем спектрофотометрические методы, при оценке продуктов окисления липидов в водных дистиллятах кур. Гидропероксиды и малоновый альдегид, первичные и вторичные продукты окисления в пищевых продуктах, также можно сначала экстрагировать в кислых условиях, а затем определить продукты окисления с помощью ВЭЖХ [32] . Метод прост, чувствительность выше по сравнению с другими методами, но занимает много времени. Идентификацию и количественную оценку продукта можно легко выполнить, если блок ВЭЖХ соединен с масс-спектрометром [19] [16] [32] [33] . Недавно была разработана комплексная двумерная жидкостная хроматография (ЖХ × ЖХ) для определения продуктов окисления липидов с использованием детектора светорассеяния (ELSD). Этот метод позволяет определять как полярные, так и неполярные продукты окисления липидов. Однако подготовка образца для метода ВЭЖХ [33] сложна, время анализа одного образца велико, а стоимость оборудования высока. Поэтому промышленное применение этого метода ограничено.
Метод прост, чувствительность выше по сравнению с другими методами, но занимает много времени. Идентификацию и количественную оценку продукта можно легко выполнить, если блок ВЭЖХ соединен с масс-спектрометром [19] [16] [32] [33] . Недавно была разработана комплексная двумерная жидкостная хроматография (ЖХ × ЖХ) для определения продуктов окисления липидов с использованием детектора светорассеяния (ELSD). Этот метод позволяет определять как полярные, так и неполярные продукты окисления липидов. Однако подготовка образца для метода ВЭЖХ [33] сложна, время анализа одного образца велико, а стоимость оборудования высока. Поэтому промышленное применение этого метода ограничено.
Газовая хроматография с масс-спектрометрией — еще один метод, используемый для определения продуктов окисления липидов в пищевых продуктах. Конкретные маркерные соединения, такие как гексаналь и общие альдегиды, были наиболее успешно используемыми летучими соединениями для определения степени окисления в различных пищевых продуктах, включая мясо, молоко, сушеные и растительные продукты, с использованием GC-MS [23]. . Кроме того, типичные конечные продукты окисления липидов, такие как альдегиды, кетоны, углеводороды и спирты, которые реагировали с ТВА, используются для определения степени окисления с помощью ГХ-МС [24] . Ан и др. [34] показали, что количества пропаналя, пентаналя, гексаналя, 1-пентанола и общего количества летучих веществ сильно коррелировали (p < 0,01) со значениями TBARS приготовленного мяса, но гексаналь и общее количество летучих веществ представляли степень окисления липидов. лучше, чем любые отдельные летучие соединения в вареном мясе. Метод ГХ также является чувствительным методом, но стоимость оборудования высока, а анализ требует много времени [19] [34] [35] Таким образом, обычные спектрофотометрические методы TBARS по-прежнему предпочтительнее хроматографических методов из-за их простоты.
. Кроме того, типичные конечные продукты окисления липидов, такие как альдегиды, кетоны, углеводороды и спирты, которые реагировали с ТВА, используются для определения степени окисления с помощью ГХ-МС [24] . Ан и др. [34] показали, что количества пропаналя, пентаналя, гексаналя, 1-пентанола и общего количества летучих веществ сильно коррелировали (p < 0,01) со значениями TBARS приготовленного мяса, но гексаналь и общее количество летучих веществ представляли степень окисления липидов. лучше, чем любые отдельные летучие соединения в вареном мясе. Метод ГХ также является чувствительным методом, но стоимость оборудования высока, а анализ требует много времени [19] [34] [35] Таким образом, обычные спектрофотометрические методы TBARS по-прежнему предпочтительнее хроматографических методов из-за их простоты.
2.3. Косвенные методы, используемые для обнаружения вторичных продуктов окисления
2.
 3.1. Флуорометрический метод
3.1. Флуорометрический метод Флуорометрический метод является косвенным методом, широко используемым для определения уровня окисления липидов в сырой рыбе, мясных продуктах и субпродуктах животного происхождения, таких как кровь [36] [26] . Его также можно использовать с растительными маслами, богатыми полиненасыщенными жирными кислотами (ПНЖК) [37] [38] . Кроме того, флуорометрический метод использовался для определения окисления липидов в продуктах с низким содержанием влаги, таких как крупы 9.0151 [39] . Во флуорометрическом методе МА превращается в тетраметоксипропан, что устраняет ложные показания флуоресценции витамина А, никотинамидадениндинуклеотида (НАДН), белков и аминокислот. Таким образом, этот метод больше подходит для богатых белком пищевых продуктов с большим количеством ионных и ковалентных связей, таких как рыба [40] . Наиболее распространенный метод включает экстракцию липидов с использованием растворителя хлороформ-метанол-вода. Собранный органический слой смешивают с сульфатом натрия и фильтруют. Затем смесь сушат газообразным азотом при температуре не выше 35°С. Эквивалент МА в липидных экстрактах измеряют путем взаимодействия с ТБК. В экстракционный растворитель добавляют БГТ и измеряют вторичные продукты реакции окисления липидов по возбуждению флуоресценции (360 нм) и эмиссии (440 нм) водного и органического слоев, содержащих хлороформ и метанол (2:1) [37] [38] . Полученная флуоресценция надежна и чувствительна к обнаружению липидов и водорастворимых гидропероксидов в образцах мяса и рыбы [41] . Чувствительность этого метода выше, чем у абсорбционных спектрофотометрических методов (метод TBARS), он воспроизводим, прост и требует небольшого количества образца для определения уровня окисления в мясе и мясных продуктах.
Собранный органический слой смешивают с сульфатом натрия и фильтруют. Затем смесь сушат газообразным азотом при температуре не выше 35°С. Эквивалент МА в липидных экстрактах измеряют путем взаимодействия с ТБК. В экстракционный растворитель добавляют БГТ и измеряют вторичные продукты реакции окисления липидов по возбуждению флуоресценции (360 нм) и эмиссии (440 нм) водного и органического слоев, содержащих хлороформ и метанол (2:1) [37] [38] . Полученная флуоресценция надежна и чувствительна к обнаружению липидов и водорастворимых гидропероксидов в образцах мяса и рыбы [41] . Чувствительность этого метода выше, чем у абсорбционных спектрофотометрических методов (метод TBARS), он воспроизводим, прост и требует небольшого количества образца для определения уровня окисления в мясе и мясных продуктах.
Липофусцин обычно используется в качестве флуоресцентного маркера, но некоторые другие маркеры, такие как 1,4-дигидропиридины и 1-пальмитоил-2-((2-(4-(6-фенилтранс-1,3,5-гексатриенил)- фенил)-этил)-карбонил)-sn-глицеро-3-фосфохолин (ДФХ-ФХ), дифенил-1-пиренилфосфин (ДФФП) также используются в качестве нового типа флуоресцентных соединений в пищевых продуктах. Эти маркеры растворяют в смеси хлороформ/метанол и растворители удаляют с помощью азота. Высушенный образец смешивают с фосфатным буфером и наблюдают за ходом реакции при 430 нм (возбуждение при 354 нм) при 37 °С с помощью флуориметра 9.0151 [41] . С этими маркерами обработка изображений представлена как новый метод определения уровня окисления в пищевых продуктах [40] [41] .
Эти маркеры растворяют в смеси хлороформ/метанол и растворители удаляют с помощью азота. Высушенный образец смешивают с фосфатным буфером и наблюдают за ходом реакции при 430 нм (возбуждение при 354 нм) при 37 °С с помощью флуориметра 9.0151 [41] . С этими маркерами обработка изображений представлена как новый метод определения уровня окисления в пищевых продуктах [40] [41] .
2.3.2. Сенсорный анализ
Сенсорная оценка вызывает, измеряет, анализирует и интерпретирует реакцию человека на свойства пищевых материалов. Обученный или неподготовленный эксперт может определить органолептические характеристики, такие как запах, аромат и вкус пищевого продукта [42] . Органолептическая оценка считается важным методом, поскольку она напрямую интерпретирует уровень окисления в пищевом продукте [43] [44] [45] . В практической ситуации эта оценка выполняется полевыми панелями, потребительскими панелями, панелями профилирования свободного выбора, панелями анализа количественного описания и экспертными панелями, особенно в отношении продуктов с низким содержанием влаги, таких как злаки [39] [42] [46] . Органолептическая оценка экономически эффективна и проста и может применяться ко всем продуктам растительного и животного происхождения в жидкой, полутвердой и твердой формах. Тем не менее, органолептический анализ показывает высокие региональные различия и низкую повторяемость из-за личных предпочтений и опыта, культурного происхождения, возраста и пола участников, а также времени проведения оценки. Поэтому рекомендуется органолептический, наряду с химическим и инструментальным, анализ. Как обсуждалось выше, существует множество методов определения степени окисления липидов в пищевых продуктах, но один метод не может подойти для всех пищевых продуктов. Таким образом, выбор правильного и эффективного метода для конкретной пищи имеет важное значение.
Органолептическая оценка экономически эффективна и проста и может применяться ко всем продуктам растительного и животного происхождения в жидкой, полутвердой и твердой формах. Тем не менее, органолептический анализ показывает высокие региональные различия и низкую повторяемость из-за личных предпочтений и опыта, культурного происхождения, возраста и пола участников, а также времени проведения оценки. Поэтому рекомендуется органолептический, наряду с химическим и инструментальным, анализ. Как обсуждалось выше, существует множество методов определения степени окисления липидов в пищевых продуктах, но один метод не может подойти для всех пищевых продуктов. Таким образом, выбор правильного и эффективного метода для конкретной пищи имеет важное значение.
2.4. Методы обнаружения первичных и вторичных продуктов окисления
p-анизидиновый тест (p-AV) и общий индекс окисления (TOTOX) — два распространенных метода, используемых для определения окисления липидов в пищевых продуктах, особенно пищевых маслах. Тесты на п-анизидин и ТОТОКС определяют как первичные, так и вторичные продукты окисления в масле [47] . Однако в тесте на анизидин в качестве основных маркеров окисления используются альдегиды, такие как 2-алкенали и 2,4-алкадинали, а уровень образующегося анизидина измеряется с помощью УФ-спектрофотометра при 350 нм [47] [48] .
Тесты на п-анизидин и ТОТОКС определяют как первичные, так и вторичные продукты окисления в масле [47] . Однако в тесте на анизидин в качестве основных маркеров окисления используются альдегиды, такие как 2-алкенали и 2,4-алкадинали, а уровень образующегося анизидина измеряется с помощью УФ-спектрофотометра при 350 нм [47] [48] .
TOTOX указывает общую степень окисления и может дать хорошее объяснение конечного качества пищевого масла. Он рассчитывается по следующему уравнению:
TOTOX = п-анизидиновое число + 2 пероксидное число.
Методы p-AV и TOTOX просты, требуют меньше технических знаний и обычно используются для определения качества масел, содержащих EPA/DHA, и готовых продуктов [48] [49] . Однако p-AV не подходит для определения окисления в маслах, богатых омега-3, с интенсивным цветом или специфическими ароматизаторами, добавленными к конечному маслу [49] . В таблице 1 представлены сводные данные о методах окисления липидов с их принципами, применением, преимуществами и недостатками каждого метода.
Таблица 1. Краткое изложение общих методов, используемых при окислении липидов.


 С другой стороны, гидропероксиды с выделением энергии образуют оксидрильные группы и окисленную форму свободных радикалов, которые вместе с другими жирными кислотами приводят к образованию большего количества гидропероксидов и новых свободных радикалов. Наконец, оксидрильные группы вместе с другими жирными кислотами высвобождают воду и новые свободные радикалы, подвергающиеся новому окислению.
С другой стороны, гидропероксиды с выделением энергии образуют оксидрильные группы и окисленную форму свободных радикалов, которые вместе с другими жирными кислотами приводят к образованию большего количества гидропероксидов и новых свободных радикалов. Наконец, оксидрильные группы вместе с другими жирными кислотами высвобождают воду и новые свободные радикалы, подвергающиеся новому окислению.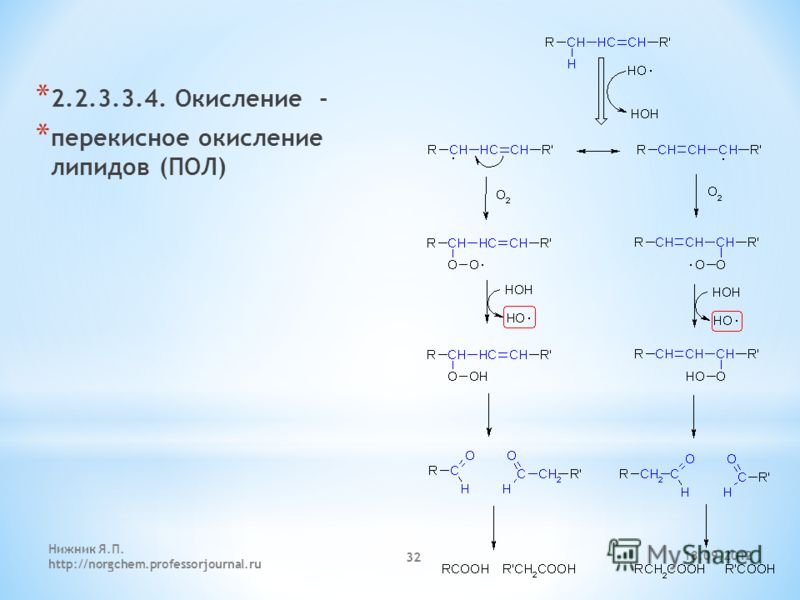
Leave A Comment