Контрольна робота «Теплові явища»
Контрольная работа по теме «Тепловые явления»
Вариант
1 (1,5 балла). На сколько изменится внутренняя энергия куска олова массой 2 кг, если его нагреть на 1оС?
2 (1,5 балла). Сколько нужно сжечь газа, чтобы выделилось 115 000 кДж теплоты?
3 (2 балла). В алюминиевый калориметр массой 140 г налили 250 г воды при температуре 15оС. После того, как брусок из свинца массой 100 г нагретый до 100оС поместили в калориметр с водой, там установилась температура 16оС. Составить уравнение теплового баланса и определить удельную теплоёмкость свинца.
4 (3 балла). Сколько спирта надо сжечь, чтобы изменить температуру воды массой 2 кг от 14оС до 50оС, если вся теплота, выделенная спиртом, пойдёт на нагревание воды.
5 (4 балла). На керогазе нагрели 3 кг воды от 25оС до 100оС.
Контрольная работа по теме «Тепловые явления»
Вариант
1 (1,5 балла). Какова масса железной детали, если на её нагревание от 20оС до 200оС пошло 20,7 кДж теплоты?
2 (1,5 балла). Сколько спирта надо сжечь, чтобы получить 45 000 кДж теплоты?
3 (2 балла). Вода массой 150 г, налитая в латунный калориметр массой 200 г, имеет температуру 12оС. Найти температуру, которая установится в калориметре, если в воду опустить железную гирю массой 0,5 кг, нагретую до 100
4 (3 балла). Сколько воды, взятой при температуре 14оС, можно на-греть до 50оС, сжигая спирт массой 30 г и считая, что вся выделяемая при горении спирта энергия идёт на нагревание воды.
5 (4 балла). В медном сосуде массой 0,5 кг нагревают 2л воды, взятой при температуре 10оС. До какой температуры можно нагреть воду за счёт сжигания 50 г спирта? КПД считать равным 50%.
До какой температуры можно нагреть воду за счёт сжигания 50 г спирта? КПД считать равным 50%.
Контрольная работа по теме «Тепловые явления»
Вариант
1 (1,5 балла). На сколько градусов повысилась температура 4 л воды, если она получила количество теплоты, равное 168 кДж?
2 (1,5 балла). Какая масса каменного угля была сожжена в печи, если при этом выделилось 60 МДж теплоты?
3 (2 балла). Стальное изделие закалялось нагреванием до температуры 700оС с последующим опусканием в масло массой 2 кг, взятое при температуре 10оС. При этом масло нагрелось до температуры 40оС. Найти массу стального изделия, если изделие охладилось на 30оС при переносе. Удельная теплоёмкость масла 2100 Дж/(кг·К).
4 (3 балла). Сколько дров необходимо сжечь для того, чтобы нагреть 50 л воды в железном котле массой 10 кг от 15
5 (4 балла). На примусе с КПД 40% необходимо вскипятить 4л воды, начальная температура которой 20оС, в алюминиевой кастрюле массой 2 кг. Определить расход керосина на нагревание воды и кастрюли.
Контрольная работа по теме «Тепловые явления»
Вариант
1 (1,5 балла). Какое количество теплоты необходимо для нагревания латунной гири массой 200 г от 20оС до 28оС?
2 (1,5 балла
3 (2 балла). Чтобы охладить деталь из меди, имеющую температуру 100оС, её погрузили в 420 г воды с температурой 15оС. Определите массу детали, если известно, что в процессе теплообмена вода нагрелась на 18оС.
4 (3 балла). На сколько изменится температура воды объёмом 100 л, если считать, что вся теплота, выделяемая при сжигании древесного угля массой 0,5 кг, пойдёт на нагревание воды?
5 (4 балла). Сколько процентов теплоты полезно использовано, если на спиртовке нагрели 400 г воды от 20о
Сколько процентов теплоты полезно использовано, если на спиртовке нагрели 400 г воды от 20о
Задачи на расчет количества теплоты
Вы можете изучить и скачать доклад-презентацию на тему Задачи на расчет количества теплоты. Презентация на заданную тему содержит 13 слайдов. Для просмотра воспользуйтесь проигрывателем, если материал оказался полезным для Вас — поделитесь им с друзьями с помощью социальных кнопок и добавьте наш сайт презентаций в закладки!
Презентации» Физика» Презентация Задачи на расчет количества теплоты
Слайды и текст этой презентации
Слайд 1
Описание слайда:
Задачи на расчет количества теплоты
Слайд 2
Описание слайда:
Условие
В алюминиевый калориметр массой 45 г, содержащий 100 г воды при температуре 20°С, поместили чугунную гирю массой 50 г, предварительно нагретую до 100°С. Какая температура установится в калориметре?
Какая температура установится в калориметре?
Слайд 3
Описание слайда:
Условие В алюминиевый калориметр массой 45 г, содержащий 100 г воды при температуре 20°С, поместили чугунную гирю массой 50 г, предварительно нагретую до 100°С. Какая температура установится в калориметре?
Слайд 4
Описание слайда:
Условие В алюминиевый калориметр массой 45 г, содержащий 100 г воды при температуре 20°С, поместили чугунную гирю массой 50 г, предварительно нагретую до 100°С. Какая температура установится в калориметре?
Слайд 5
Описание слайда:
Условие
В алюминиевый калориметр массой 45 г,
содержащий 100 г воды при температуре 20°С,
поместили чугунную гирю массой 50 г,
предварительно нагретую до 100°С.
Слайд 6
Описание слайда:
Какие тепловые процессы происходят в задаче? Назовите процессы, которые происходят с каждым из этих тел
Слайд 7
Описание слайда:
Слайд 8
Описание слайда:
Обсуждение
Слайд 9
Описание слайда:
Решение
Слайд 10
Описание слайда:
Решение
Описание слайда:
Решение
Слайд 12
Описание слайда:
Решение
Слайд 13
Описание слайда:
Ответ
Tags Задачи на расчет количества теплоты
Похожие презентации
Презентация успешно отправлена!
Ошибка! Введите корректный Email!
Конечная температура после помещения теплого металла в более холодную воду
Конечная температура после помещения теплого металла в более холодную водуКогда теплый металл помещают в более холодную воду, какой получается конечная температура?
Перейти к расчету конечной температуры при смешивании металла и воды: задачи 1 — 15
Перейти к расчету конечной температуры при смешивании двух проб воды
Назад в меню термохимии
Эти задачи точно такие же, как смешивание двух количеств воды, за одним небольшим исключением: удельные теплоемкости в двух частях уравнения будут разными. Удельная теплоемкость воды останется на уровне 4,184, но значение для металла будет другим. Эти значения сведены в таблицы, а списки выбранных значений есть в большинстве учебников.
Удельная теплоемкость воды останется на уровне 4,184, но значение для металла будет другим. Эти значения сведены в таблицы, а списки выбранных значений есть в большинстве учебников.
Пример #1: Определите конечную температуру, когда кусок железа массой 25,0 г при температуре 85,0 °C помещают в 75,0 г воды при температуре 20,0 °C.
Сначала обсуждение, потом решение. Простите меня, если пункты кажутся очевидными:
а) Более холодная вода будет нагреваться (к ней «притекает» тепловая энергия). Более нагретый металл остынет (из него «вытекает» тепловая энергия).
b) Вся смесь будет иметь температуру ЖЕ . Это очень, очень важно.
c) Энергия, которая «вытекла» (из более теплой воды), равна энергии, которая «втекла» (в более холодную воду)
Ключ решения номер один: Начнем с того, что назовем конечную, конечную температуру «x». Имейте в виду, что И утюг, и вода будут нагреваться до температуры, которую мы называем «х». Кроме того, убедитесь, что вы понимаете, что «x», который мы используем, ЯВЛЯЕТСЯ НЕ Δt, а ОКОНЧАТЕЛЬНОЙ температурой. Это то, для чего мы решаем.
Кроме того, убедитесь, что вы понимаете, что «x», который мы используем, ЯВЛЯЕТСЯ НЕ Δt, а ОКОНЧАТЕЛЬНОЙ температурой. Это то, для чего мы решаем.
Более нагретое железо понижается с 85,0 до х, значит, его Δt равно 85,0 минус х. Более холодная вода нагревается, поэтому ее Δt равно x минус 20,0.
Последний абзац может немного сбить с толку, поэтому давайте сравним его с числовой строкой:
Чтобы вычислить абсолютное расстояние, это большее значение минус меньшее значение, поэтому от 85,0 до х равно 85,0 минус х, а расстояние от х до 20,0 равно х минус 20,0
Ключевое решение номер два: количество энергии, выходящее из теплой воды, равно количеству энергии, выходящей из холодной воды. Это означает:
q потеря = q усиление
Таким образом, путем подстановки имеем:
(25,0) (85,0 — х)(0,45) = (75,0) (х — 20,0) (4,184)
Найдите х
Обратите внимание на использование удельной теплоты сгорания железа. Это 0,45 Дж на грамм-градус Цельсия.
Это 0,45 Дж на грамм-градус Цельсия.
Учитывая, что 75/25 = 3, получаем:
38,25 — 0,45х = 12,552х — 251,04
тогда
13,002x = 289,29
Ответ
22,25 °С
, если вы не слишком придирчивы к значащим цифрам.
Обратите внимание, что температура железа немного падает, в то время как вода перемещается всего на несколько (в данном случае 2,25) градусов. Это типичная ситуация в этом типе проблемы.
Пример #2: Определите конечную температуру, когда 10,0 г алюминия при 130,0 °C смешиваются с 200,0 г воды при 25,0 °C.
Техника расчета не отличается от Примера №1. Обратите внимание, начальная температура металла выше точки кипения воды. В действительности образец может испарить незначительное количество воды, но мы будем считать, что это не так для расчетов.
Решение:
1) Настройте числа:
q алюминий = q вода(10) (130 − x) (0,901) = (200,0 )(x − 25) (4,18)
2) Заметив, что 200/10 = 20, получаю:
117,13 — 0,901х = 83,6х — 2090х = 26,12 °С.
Имейте в виду, что «x» соответствует конечной температуре, а НЕ Δt.
Также я решил эту проблему с 4.18. Выполнение этого с 4.184 дает немного другой ответ. Убедитесь, что вы согласовали со своим учителем значения различных констант, которые он/она хочет, чтобы вы использовали.
Пример №3: Определите конечную температуру, когда 20,0 г ртути при 165,0 °C смешиваются с 200,0 г воды при 60,0 °C. (C p для Hg = 0,14 Дж на грамм-градус Цельсия.)
Мы проигнорируем тот факт, что ртуть жидкая. он не растворяется в воде.
Решение:
(20,0) (165,0 — х) (0,14) = (200,0) (х — 60,0) (4,18)Заметив, что 200/20 = 10, я получаю:
23,1 — 0,14х = 41,8х — 2508
41,94х = 2531,1
х = 60,35 °С
Обратите внимание, что вода перемещается только на 0,35 градуса. Имейте в виду, что существует большое количество воды по сравнению с ртутью, И что для перемещения воды на один градус требуется гораздо больше энергии, чем для того же количества ртути, перемещаемого на один градус.
Пример №4: 10,0 г воды имеют температуру 59,0 °C. Если в калориметр поместить 3,00 г золота при температуре 15,2 °С, какова будет конечная температура воды в калориметре? (Удельная теплоемкость золота составляет 0,128 Дж/г°С.)
Решение:
1) Настройте следующее:
q вода = q золото(10,0) (59,0 − x) (4,184) = (3,00) (x − 15,2) (0,128)
2) Алгебра:
2468,56 — 41,84х = 0,384х — 5,836842,224х = 2474,3968
х = 58,6 °С
Обратите внимание, что в этом случае вода остывает, а золото нагревается. Это противоположно самой распространенной задаче этого типа, но методика решения та же.
Пример №5: 105,0 мл H 2 O изначально имеет комнатную температуру (22,0 °C). Охлажденный стальной стержень (2,00°С) помещают в воду. Если конечная температура системы 21,5 °С, какова масса стального стержня? (удельная теплоемкость воды = 4,184 Дж/г °C; удельная теплоемкость стали = 0,452 Дж/г °C)
Решение:
(105,0 г) (0,5 °C) (4,184 Дж °C -1 г -1 ) = (x) (19,5 °C) (0,452 Дж °C -1 г -1 )х = 24,9 г
Пример #6: Кольцо из чистого золота и кольцо из чистого серебра имеют общую массу 15,0 г.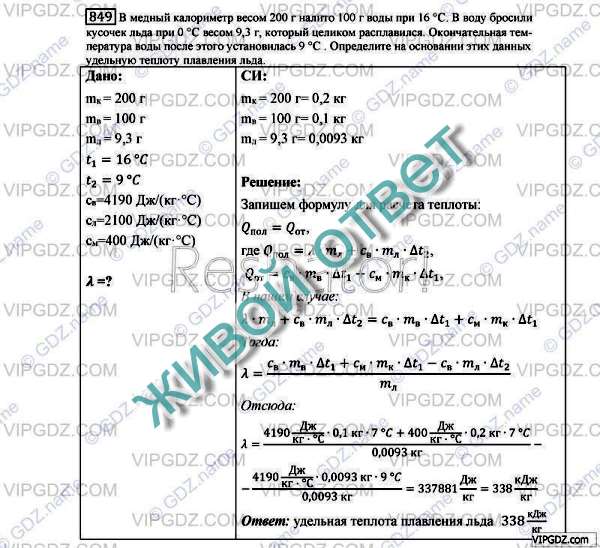 Два кольца нагревают до 62,4°С и опускают в 13,6 мл воды при 22,1°С. Когда достигается равновесие, температура воды составляет 23,9 °С. (Примите плотность воды 0,998 г/мл.)
Два кольца нагревают до 62,4°С и опускают в 13,6 мл воды при 22,1°С. Когда достигается равновесие, температура воды составляет 23,9 °С. (Примите плотность воды 0,998 г/мл.)
(а) Какова масса золотого кольца?
(b) Какова масса серебряного кольца?
Комментарий: теплотворная способность доступна во многих местах в Интернете и в учебниках. Вот пример.
Решение:
1) Основное используемое уравнение:
Полученное или потерянное тепло = (масса) (изменение температуры) (удельная теплоемкость)В более компактной форме: q = (m) (Δt) (C p )
Ниже будут использованы три из них.
2) Две массы, связанные с золотым и серебряным кольцами:
Пусть y = граммы золота
Следовательно, 15,0 − y = грамм серебра
3) Масса воды:
13,6 мл x 0,998 г/мл = 13,5728 г
4) Тепло, получаемое водой:
q = (13,5728 г) x (1,8 °C) (4,184 Дж г¯ 1 °C¯ 1 )кв = 102,2195 Дж
1,8 получается следующим образом: 23,9 − 22,1
5) Когда золотое кольцо и серебряное кольцо остывают, они высвобождают энергию, которая в сумме составляет 102,2195 Дж. Сумма может быть выражена следующим образом:
Сумма может быть выражена следующим образом:
(у) (38,5 °С) (0,129 Дж г¯ 1 °С¯ 1 ) + (15 − у) (38,5 °С) (0,235 Дж г¯ 1 °С¯ 1 ) = 102,2195 ДжПомните, изменение на 1 °C равно изменению на 1 K. Это означает, что 0,129 Дж·г¯ 1 °C¯ 1 — это то же самое, что 0,129 Дж·г¯ 1 К¯ 1
38,5 было получено таким же образом, как и 1,8 чуть выше.
6) Алгебра!
4,9665г + (15 — г) (9,0475) = 102,21954,9665г + 135,7125 – 9,0475г = 102,2195
-4,081г = -33,493
г = 8,21 г золота
15,0 − 8,21 = 6,79г Ag
Пример №7: Кольцо массой 8,352 грамма сделано из золота и серебра. Когда кольцо было нагрето до 94,52 °С, а затем брошено в 13,40 г воды при 20,00 °С, температура воды после достижения теплового равновесия составила 22,00 °С. Какова массовая доля золота и серебра в кольце?
Решение:
Теплота, выделяемая серебром, плюс теплота, выделяемая золотом, равняется теплоте, поглощаемой водой.Установите массу серебра равной «x». Это означает, что масса золота равна 8,352 минус x.
(x) (72,52 °C) (0,235 Дж/г °C) + (8,352 − x) (72,52 °C) (0,129 Дж/г °C) = (13,40 г) (2,00 °C) (4,184 Дж /г °С)
72,52 получается из 94,52 минус 22,00
17,0422х + (8,352 — х) (9,35508) = 112,1312
17,0422х + 78,13362816 — 9,35508х = 112,1312
7,68712x = 33,99757184
х = 4,422667 г
массовых процентов золота: (4,422667 / 8,352) * 100 = 52,95%
Массовая доля серебра: 100,00 − 52,95 = 47,05%
Пример #8: Кубик льда весом 74,0 г при температуре -12,0 °C помещают на блок меди массой 10,5 кг при температуре 23,0 °C, и вся система изолируется от окружающей среды. Через несколько минут лед растаял, и температура системы достигла равновесия. Рассчитайте конечную температуру системы.
Комментарий: не указана ни одна из соответствующих констант. Вам придется искать правильные значения, если вы столкнулись с такой проблемой. Если вы изучите свои источники информации, вы можете обнаружить, что они немного отличаются от значений, которые я использую. Это обычное дело. Многие из используемых значений были определены экспериментально, и разные источники часто содержат немного отличающиеся значения.
Если вы изучите свои источники информации, вы можете обнаружить, что они немного отличаются от значений, которые я использую. Это обычное дело. Многие из используемых значений были определены экспериментально, и разные источники часто содержат немного отличающиеся значения.
Решение:
1) Лед изменяется с −12 до 0:
q = (74,0 г) (12,0 °C) (2,06 Дж/г °C) = 1829,28 Дж
2) Лед тает:
q = (74,0 г / 18,0 г/моль) (6,02) = 24,7489 кДж
3) Жидкая вода подвергается неизвестному повышению температуры до конечного значения x
q = (74,0 г) (x — 0) (4,184 Дж/г°C) = 309,616x
4) Медь теряет тепло и падает до конечного значения x:
q = (10500 г) (23,0 − x) (0,385 Дж/г°C)
5) Количество тепла, отдаваемое медью, равно количеству тепла, полученному водой:
(10500) (23,0 — х) (0,385) = 1829,28 + 24748,9 + 309,616хОбратите внимание, что кДж от таяния льда используется как Дж, а не кДж.
Масса меди выражается в граммах, а не в кг.
(23,0 — х) (4042,5) = 26578,18 + 309,616х
92977,5 — 4042,5х = 26578,18 + 309,616х
66399,32 = 4352,116х
х = 15,2568 °С
x = 15,2 °C (до трех цифр, я следовал правилу округления до 5)
Пример #9: Сколько граммов воды можно нагреть с 25,0 °С до 35,0 °С за счет тепла, выделяемого 85,0 г железа, которое охлаждается с 85,0 °С до 35,0 °С? Удельная теплоемкость железа 0,450 Дж/г °С.
Решение:
1) Сколько тепла теряет утюг?
изменение температуры —> 85,0 °C − 35,0 0 °C = 50,0 °Cq = (масса) (изменение температуры) (удельная теплоемкость)
q = (85,0 г) (50,0 °С) (0,450 Дж/г °С)
q = 1912,5 Дж
2) Предположим, что все 1912,5 Дж идут на нагрев воды:
q = (масса) (изменение температуры) (удельная теплоемкость)1912,5 Дж = (х) (10,0 °С) (4,184 Дж/г °С)
х = 45,7 г
Обратите внимание, что удельная теплоемкость жидкой воды в тексте задачи не приводится.
3) Эту задачу можно было бы решить, приравняв два уравнения и решив относительно «x»:
(85,0 г) (50,0 °C) (0,450 Дж/г °C) = (x) (10,0 °C) (4,184 Дж/г °C)
Пример #10: Найдите массу жидкости H 2 O при 100,0 °C, которую можно вскипятить в газообразное H 2 O при 100,0 °C блоком алюминия массой 130,0 г при температуре 402,0 °C? Предположим, что алюминий способен кипятить воду до тех пор, пока ее температура не упадет ниже 100,0 °С. Теплоемкость алюминия равна 0,900 Дж г¯ 1 °С¯ 1 , а теплота парообразования воды при 100 °С составляет 40,65 кДж моль¯ 1
Решение:
1) Теплота, которую Al может потерять при переходе от начальной к конечной температуре:
q = m Δt C pq = (130.) г (302,0 °С) (0,900 Дж г¯ 1 °С¯ 1 ) = 35334 Дж = 35,334 кДж
Для испарения воды доступно 35,334 кДж тепла.
2) Используйте 35,334 кДж и теплоту парообразования воды для вычисления молей, а затем массу испарившейся воды:
q = (ΔH) (моль)35,334 кДж = (40,65 кДж/моль) (х)
х = 0,869225 молей H 2 O
масса H 2 O = (0,869225 моль) (18,015 г/моль) = 15,659г
Три сига инжира, это 15,6 г
Бонус Пример: 250-граммовый образец металла нагревают до температуры 98,0 °C. Его помещают в 100 г воды в латунный калориметрический стакан с латунной мешалкой. Общая масса чашки и мешалки составляет 50,0 грамм. Начальная температура воды, мешалки и калориметра 20,0 °С. Конечная равновесная температура системы составляет 30,0 °С. Чему равна удельная теплоемкость металлического образца? (Удельная теплоёмкость латуни 0,0920 кал г¯ 1 C¯ 1 .)
Решение:
1) Количество тепла, выделяемого образцом металла, поглощается (а) водой и (б) латунным калориметром и мешалкой. Какое количество теплоты было захвачено водой?
Какое количество теплоты было захвачено водой?
q = m Δt C pq = (100, г) (10,0 °C) (1,00 г кал. г¯ 1 C¯ 1 )
кв = 1000 кал
Примечание: 1,00 г кал/г¯ 1 C¯ 1 – удельная теплоемкость жидкой воды.
2) Сколько тепла поглотил латунный калориметр и мешалка?
q = m Δt C pq = (50,0 г) (10,0 °C) (0,092 кал г¯ 1 C¯ 1 )
q = 54,28 кал
3) Суммарное тепло, выделяемое металлическим образцом:
1000 кал + 54,28 кал = 1054,28 кал
4) Определите удельную теплоемкость металлического образца:
q = m Δt C p1054,28 кал = (250, г) (68,0 °C) (C p )
C p = 0,062 г кал г¯ 1 C¯ 1
Перейти к расчету конечной температуры при смешивании металла и воды задач 1 — 15
Перейти к расчету конечной температуры при смешивании двух проб воды
Назад в меню термохимии
Когда 45 г металла при 100°C бросают в ледяной калориметр, наблюдается уменьшение объема льда на 0,4596×10−6 м3.
 Чему равна удельная теплоемкость металла? (L=336×103 Дж/кг и относительная плотность льда =0,917)
Чему равна удельная теплоемкость металла? (L=336×103 Дж/кг и относительная плотность льда =0,917)Вопрос
Обновлено: 07.09.2019
NN GHOSH-КАЛОРИМЕТРИЯ-Все вопросы
20 видеоРЕКЛАМА
Текст Решение
9 Ответ 0 NA 5 0 Правильный ответ 90 0004 Ответить
Шаг за шагом пошаговое решение от экспертов, которое поможет вам избавиться от сомнений и получить отличные оценки на экзаменах.
Ab Padhai каро бина объявления ке
Khareedo DN Pro и дехо сари видео бина киси объявление ки rukaavat ке!
Похожие видео
Небольшое количество воды массой m при температуре θ (в ∘C) выливается на большую массу льда M, находящегося в точке плавления. Если с — удельная теплоемкость воды, L — удельная теплоемкость воды, а L — удельная скрытая теплота плавления льда, то масса расплавленного льда равна
11749502
при 0∘С. В калориметр опускают 50 г металла при 100°С. Установлено, что при достижении теплового равновесия объем содержимого калориметра уменьшается на 0,5×10–6 м3. Вычислите удельную теплоемкость металла. Изменением объема металла пренебречь. Удельная скрытая теплота плавления льда составляет L=300×103 Дж/кг, а его относительная плотность равна 0,9..
Установлено, что при достижении теплового равновесия объем содержимого калориметра уменьшается на 0,5×10–6 м3. Вычислите удельную теплоемкость металла. Изменением объема металла пренебречь. Удельная скрытая теплота плавления льда составляет L=300×103 Дж/кг, а его относительная плотность равна 0,9..
15085696
При температуре воздуха -10∘C лед на большом мелководном озере увеличивается на 1 см за 12 минут. Найдите теплопроводность льда. (Плотность льда = 900 кгм-3 и L = 330×103 Дж кг-1)
15634998
Сферический железный шар помещают на большой кусок сухого льда при температуре 0°C. Мяч погружается в лед до половины. Какой была температура утюга?
(Плотность железа =7,7×103кгм3, Плотность льда =920кгм-3 Удельная теплоемкость железа =504Джкг-1К-1, Удельная скрытая теплота плавления льда =336×103Джкг-1) 9(1) )
17686445
1 кг льда при 0°C сжимается при таянии на 91×10−6 м3. Твердое вещество массой 40 г, брошенное при температуре 60°С в ледяной калориметр, вызывает изменение объема на 0273×10-6 м3.
(Удельная теплота плавления льда =336×103 Дж/кг. Рассчитать удельную теплоемкость твердого тела. изменение температуры при погружении в него 10×10-3 кг металла при температуре 100 ∘ С. Относительная плотность льда 0,917. Найдите удельную теплоемкость металла.
17686451
Калориметр содержит лед. Определить теплоемкость калориметра, если для нагревания его вместе с содержимым от 270 К до 270 К требуется 2,1 кДж теплоты, а для повышения его температуры с 272 К до 274 К требуется 69,72 кДж теплоты.
(л льда =336×103 Джкг-1, удельная теплоемкость льда =2100кг-1К-1)
17686466
Термостойкий конверт содержит 100 г льда при температуре 1∘C. Он сжат до 1200 атм. Найдите массу растаявшего льда, если температура плавления льда понизится на 1°С при повышении давления на 138 атм.
(л льда =336×103 Джкг-1 и удельная теплоемкость льда =2100Джкг-1К-1)
17686467
Текст Решение
Сосуд площадью 1 м2, изготовленный из медного листа толщиной 5 мм, наполнен тающего льда и погружен в воду при температуре 100∘C.


 Масса меди выражается в граммах, а не в кг.
Масса меди выражается в граммах, а не в кг.

Leave A Comment