4. Синтез жиров
Синтезируются жиры из глицерина и жирных кислот.
Глицерин в организме возникает при распаде жира (пищевого и собственного), а также легко образуются из углеводов.
Жирные кислоты синтезируются из ацетилкофермента А. Ацетилкофермент А – универсальный метаболит. Для его синтеза необходимы водород и энергия АТФ. Водород же получается из НАДФ.Н2. В организме синтезируются только насыщенные и мононасыщенные (имеющие одну двойную связь) жирные кислоты. Жирные кислоты, имеющие две и более двойных связей в молекуле, называемые полинасыщенные, в организме не синтезируются и должны поступать с пищей. Для синтеза жира могут быть использованы жирные кислоты – продукты гидролиза пищевого и собственного жиров.
Все участники синтеза жира должны быть в активном виде: глицерин в форме
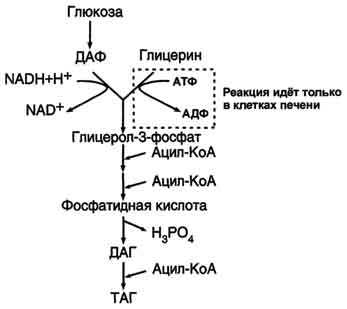
Следует отметить, что глицерин и жирные кислоты могут быть получены из углеводов. Поэтому при избыточном потреблении их на фоне малоподвижного образа жизни развивается ожирение.
ДАФ –дигидроацетонфосфат,
ДАГ – диацилглицерин.
ТАГ – триацилглицерол.
Общая характеристика липопротеинов.
Все типы липопротеинов имеют сходное строение – гидрофобное ядро и гидрофильный слой на поверхности. Гидрофильный слой образован белками, которые называют апопротеинами,и амфифильными молекулами липидов – фосфолипидами и холестеролом. Гидрофильные группы этих молекул обращены к водной фазе, а гидрофобные части – к гидрофобному ядру липопротеина, в котором находятся транспортируемые липиды.
Апопротеины выполняют несколько функций:
• формируют структуру липопротеинов;
• взаимодействуют с рецепторами на поверхности клеток и таким образом определяют, какими тканями будет захватываться данный тип липопротеинов;
• служат ферментами или активаторами ферментов, действующих на липопротеины.
Липопротеины. В организме синтезируются следующие типы липопротеинов: хиломикроны (ХМ), липопротеины очень низкой плотности (ЛПОНП), липопротеины промежуточной плотности (ЛППП), липопротеины низкой плотности (ЛПНП) и липопротеины высокой плотности (ЛПВП).Каждый из типов ЛП образуется в разных тканях и транспортирует определѐнные липиды. Например, ХМ транспортируют экзогенные (пищевые жиры) из кишечника в ткани, поэтому триацилглицеролы составляют до 85% массы этих частиц.
Свойства липопротеинов. ЛП хорошо растворимы в крови, неопалесцируют, так как имеют небольшой размер иотрицательный зарядна
поверхности. Некоторые ЛП легко проходят через стенки капилляров кровеносных сосудов и доставляют липиды к клеткам. Большой размер ХМ не позволяет им проникать через стенки капилляров, поэтому из клеток кишечника они сначала попадают в лимфатическую систему и потом через главный грудной проток вливаются в кровь вместе с лимфой. Судьба жирных кислот, глицерола и остаточных хиломикронов. В результате действия ЛП-липазы на жиры ХМ образуются жирные кислоты и глицерол. Основная масса жирных кислот проникает в ткани. В жировой ткани в абсорбтивный период жирные кислоты депонируются в виде триацилглицеролов, в сердечной мышце и работающих скелетных мышцах используются как источник энергии. Другой продукт гидролиза жиров, глицерол, растворим в крови, транспортируется в печень, где в абсорбтивный период может быть использован для синтеза жиров.
Гиперхиломикронемия, гипертриглицеронемия.После приѐма пищи, содержащей жиры, развивается физиологическая гипертриглицеронемия и, соответственно, гиперхиломикронемия, которая может продолжаться до нескольких часов.Скорость удаления ХМ из кровотока зависит от:
• активности ЛП-липазы;
• присутствия ЛПВП, поставляющих апопротеины С-II и Е для ХМ;
• активности переноса апоС-II и апоЕ на ХМ.
Генетические дефекты любого из белков, участвующих в метаболизме ХМ, приводят к развитию семейной гиперхиломикронемии – гиперлипопротеинемии типа I.
Содержание жиров в пищевых продуктах.Жиры как запасные вещества находятся в соединительной ткани животных и рыб, в жировой ткани, подкожной клетчатке, печени и костях, а также в семенах растений и иногда в мякоти плодов.
В растениях одного и того же вида состав и свойства жира могут колебаться в зависимости от климатических условий произрастания. Содержание и качество жиров в животном сырье также зависит от породы, возраста, степени упитанности, пола, сезона года и т.д.
Жиры широко используют, при производстве многих пищевых продуктов, они обладают высокой калорийностью и пищевой ценностью, вызывают длительное чувство насыщения. Жиры являются важными вкусовыми и структурными компонентами в процессе приготовления пищевых продуктов, оказывают значительное влияние на внешний вид пищи. При жарке жир играет роль среды, передающей тепло.
Данные о содержании жиров в некоторых продуктах
Название продукта | Примерное содержа-ние жиров в пищевых продуктах, % на сырую массу | Название продукта | Примерное содержа-ние жиров в пищевых продуктах, % на сырую массу |
Семена: | Хлеб ржаной | 1,20 | |
Подсолнечника | 35-55 | Овощи свежие | 0,1-0,5 |
Конопли | 31-38 | Плоды свежие | 0,2-0,4 |
Мака | 40 | Говядина | 3,8-25,0 |
Какао-бобы | 55 | Свинина | 6,3-41,3 |
Орехи арахиса | 40-55 | Баранина | 5,8-33,6 |
Орехи грецкие (ядра) | 58-74 | Рыба | 0,4-20 |
Хлебные злаки: | Молоко коровье | 3,2-4,5 | |
Пшеница | 2,3 | Масло сливочное | 61,5-82,5 |
Рожь | 2,0 | Маргарин | 82,5 |
Овес | 6,2 | Яйца | 12,1 |
В жирах, полученных из растительных и животных тканей, кроме глицеридов, могут находиться свободные жирные кислоты, фосфатиды, стеролы, пигменты, витамины, вкусовые и ароматические вещества, ферменты, белки и др., которые влияют на качество и свойства жиров. На вкус и запах жиров также оказывают влияние вещества, образующиеся в жирах при хранении (альдегиды, кетоны, перекисные и другие соединения).
Жиры в организм человека должны постоянно поступать с пищей. Потребность в жирах зависит от возраста, характера работы, климатических условий и других факторов, но в среднем в сутки взрослому человеку необходимо от 80 до 100 г жиров. В суточном рационе должно быть примерно 70 % животных и 30 % растительных жиров.
studfiles.net
Синтез жиров в клетке осуществляется в
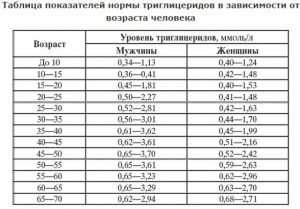
Первичная гипертриглицеридемия — что это такое? Так называется повышение уровня триглицеридов в крови, которое обнаруживается у 5% жителей нашей планеты. Наиболее распространено заболевание у пожилых людей. Триглицериды — жироподобные вещества, откладывающиеся в подкожной клетчатке. Часть их входит в состав крови и обеспечивает ткани необходимой энергией. Если жиры, поступающие с пищей, не успевают преобразовываться в энергию, организм превращает их в запасы. Уровень триглицеридов в крови возрастает, что может нанести вред. Анализ крови на эти вещества используется для оценки риска атеросклероза.
При гипертриглицеридемии повышается концентрация липопротеидов низкой плотности. Они оседают на сосудистых стенках, способствуя развитию атеросклероза и онкологических заболеваний. Длительное течение гипертриглицеридемии может привести к инсульту или инфаркту. Процесс считается необратимым, ведь жиры снижают тонус стенок и уменьшают просвет артерии, препятствуя притоку крови к тканям.
 Обследование необходимо в том случае, если при проведении общего анализа крови было обнаружено какое-либо отклонение. Определение уровня триглицеридов может проводиться как отдельно, так и в сочетании с тестом на общий холестерин. Этот анализ входит в состав липидограммы. Последнюю нужно сдавать каждому взрослому человеку не реже 1 раза в 5 лет. Концентрацией триглицеридов в собственной крови должны интересоваться люди, страдающие сахарным диабетом, ведь количество липопротеидов низкой плотности повышается одновременно с уровнем глюкозы. В группу риска входят люди, имеющие другие хронические заболевания.
Обследование необходимо в том случае, если при проведении общего анализа крови было обнаружено какое-либо отклонение. Определение уровня триглицеридов может проводиться как отдельно, так и в сочетании с тестом на общий холестерин. Этот анализ входит в состав липидограммы. Последнюю нужно сдавать каждому взрослому человеку не реже 1 раза в 5 лет. Концентрацией триглицеридов в собственной крови должны интересоваться люди, страдающие сахарным диабетом, ведь количество липопротеидов низкой плотности повышается одновременно с уровнем глюкозы. В группу риска входят люди, имеющие другие хронические заболевания.
Если у ближайших родственников пациента были обнаружены патологии сердечно-сосудистой системы, первый анализ он должен сдать в 2–10 лет. Посетить специалиста необходимо при появлении признаков нарушения функций внутренних органов. Так как при гипертриглицеридемии повышается уровень жиров в крови, на результат анализа влияет множество факторов, к его сдаче необходимо подготовиться основательно.
Количество триглицеридов в крови остается увеличенным в течение нескольких часов после еды или употребления алкоголя, поэтому на момент сдачи анализов с последнего приема пищи должно пройти более 8 часов. Показатели крови могут изменяться в течение дня и месяца. Поэтому однократное проведение анализа считается неинформативным.
Классификация триглицеридемии осуществляется на основании типа соединений, количество которых в организме увеличивается. Жироподобные вещества, поступающие в организм человека с пищей, называются экзогенными. Эндогенными считаются соединения, образующиеся в результате обмена. Эндогенная триглицеридемия диагностируется при повышении уровня нейтральных жиров из-за метаболических нарушений. Экзогенные формы характеризуются увеличением количества вещества из-за неправильного питания.
Гипертриглицеридемия протекает бессимптомно, поэтому поставить диагноз без проведения исследования невозможно. Косвенными признаками можно считать:
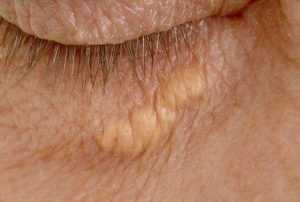 На лице пациента появляются прыщи, имеющие жировое содержимое. Однако такие симптомы могут появляться и при некоторых других заболеваниях.
На лице пациента появляются прыщи, имеющие жировое содержимое. Однако такие симптомы могут появляться и при некоторых других заболеваниях.
При отсутствии лечения гипертриглицеридемия приводит к развитию:
Наиболее опасным осложнением считается панкреатит — воспаление поджелудочной железы. Острая форма патологии сопровождается:
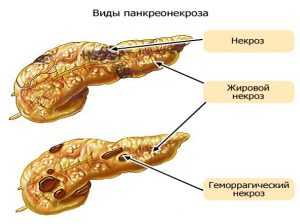 При панкреатите происходит панкреонекроз — омертвение тканей части или всего органа.
При панкреатите происходит панкреонекроз — омертвение тканей части или всего органа.
Часто повышенный уровень триглицеридов в крови обнаруживается у пациентов, предпочитающих жирную пищу; у беременных женщин; у людей, проходящих гормональную терапию. Рассмотрим, как лечить это заболевание.
Лечение подразумевает применение лекарственных препаратов и изменение режима питания. Медикаментозная терапия проводится при тяжелых формах гипертриглицеридемии и начинается с минимальных доз. Наиболее часто назначаются:
 Они блокируют производство триглицеридов в организме и замедляют усвоение поступающих извне веществ. При неэффективности лечения дозу препарата увеличивают либо лекарство заменяют.
Они блокируют производство триглицеридов в организме и замедляют усвоение поступающих извне веществ. При неэффективности лечения дозу препарата увеличивают либо лекарство заменяют.
Диета является важной частью немедикаментозного лечения. Суточный рацион должен содержать не более 1400 ккал, с помощью такого питания пациент может быстро избавиться от лишнего веса. Питаться необходимо небольшими порциями, 4–5 раз в день. Нельзя принимать пищу в вечернее и ночное время. Ограничить рекомендуется потребление макаронных и хлебобулочных изделий. Полностью отказываются от:
Даже сладкие фрукты рекомендуется исключить. Обогатить рацион клетчаткой можно за счет бобовых.
Рыбу необходимо употреблять не реже 3 раз в неделю. От жирных соусов и майонеза рекомендуется отказаться, допускается введение в рацион оливкового масла. Количество потребляемой в сутки соли снижают до 3 г. Лечебные диеты, умеренные физические нагрузки в течение 2 месяцев способствуют снижению уровня триглицеридов в 2 раза.
При значительном повышении концентрации жиров в организме следует обратиться к врачу.
Первичная гипертриглицеридемия — что это такое? Так называется повышение уровня триглицеридов в крови, которое обнаруживается у 5% жителей нашей планеты. Наиболее распространено заболевание у пожилых людей. Триглицериды — жироподобные вещества, откладывающиеся в подкожной клетчатке. Часть их входит в состав крови и обеспечивает ткани необходимой энергией. Если жиры, поступающие с пищей, не успевают преобразовываться в энергию, организм превращает их в запасы. Уровень триглицеридов в крови возрастает, что может нанести вред. Анализ крови на эти вещества используется для оценки риска атеросклероза.
Нормой считается уровень, не превышающий 150 мг/дл. Его повышение до 300 мг/дл считается показателем нарушений в режиме питания и наличия ожирения 1 степени. Если этот показатель значительно превышает 300 мг/дл, речь идет об опасных патологических состояниях, требующих незамедлительного лечения.
При гипертриглицеридемии повышается концентрация липопротеидов низкой плотности. Они оседают на сосудистых стенках, способствуя развитию атеросклероза и онкологических заболеваний. Длительное течение гипертриглицеридемии может привести к инсульту или инфаркту. Процесс считается необратимым, ведь жиры снижают тонус стенок и уменьшают просвет артерии, препятствуя притоку крови к тканям.
Когда нужно делать анализ?
 Обследование необходимо в том случае, если при проведении общего анализа крови было обнаружено какое-либо отклонение. Определение уровня триглицеридов может проводиться как отдельно, так и в сочетании с тестом на общий холестерин. Этот анализ входит в состав липидограммы. Последнюю нужно сдавать каждому взрослому человеку не реже 1 раза в 5 лет. Концентрацией триглицеридов в собственной крови должны интересоваться люди, страдающие сахарным диабетом, ведь количество липопротеидов низкой плотности повышается одновременно с уровнем глюкозы. В группу риска входят люди, имеющие другие хронические заболевания.
Обследование необходимо в том случае, если при проведении общего анализа крови было обнаружено какое-либо отклонение. Определение уровня триглицеридов может проводиться как отдельно, так и в сочетании с тестом на общий холестерин. Этот анализ входит в состав липидограммы. Последнюю нужно сдавать каждому взрослому человеку не реже 1 раза в 5 лет. Концентрацией триглицеридов в собственной крови должны интересоваться люди, страдающие сахарным диабетом, ведь количество липопротеидов низкой плотности повышается одновременно с уровнем глюкозы. В группу риска входят люди, имеющие другие хронические заболевания.
Если у ближайших родственников пациента были обнаружены патологии сердечно-сосудистой системы, первый анализ он должен сдать в 2–10 лет. Посетить специалиста необходимо при появлении признаков нарушения функций внутренних органов. Так как при гипертриглицеридемии повышается уровень жиров в крови, на результат анализа влияет множество факторов, к его сдаче необходимо подготовиться основательно.
Количество триглицеридов в крови остается увеличенным в течение нескольких часов после еды или употребления алкоголя, поэтому на момент сдачи анализов с последнего приема пищи должно пройти более 8 часов. Показатели крови могут изменяться в течение дня и месяца. Поэтому однократное проведение анализа считается неинформативным.
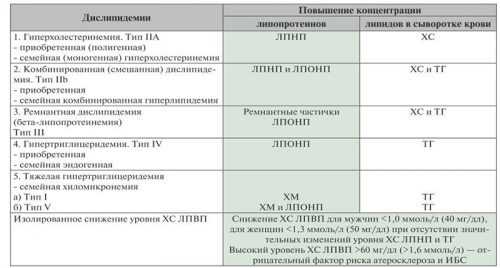
Классификация триглицеридемии осуществляется на основании типа соединений, количество которых в организме увеличивается. Жироподобные вещества, поступающие в организм человека с пищей, называются экзогенными. Эндогенными считаются соединения, образующиеся в результате обмена. Эндогенная триглицеридемия диагностируется при повышении уровня нейтральных жиров из-за метаболических нарушений. Экзогенные формы характеризуются увеличением количества вещества из-за неправильного питания.
Причины и симптомы
Гипертриглицеридемия протекает бессимптомно, поэтому поставить диагноз без проведения исследования невозможно. Косвенными признаками можно считать:
- снижение остроты зрения;
- тяжесть в правом подреберье;
- раздражительность;
- головные боли;
- гепатомегалию.
 На лице пациента появляются прыщи, имеющие жировое содержимое. Однако такие симптомы могут появляться и при некоторых других заболеваниях.
На лице пациента появляются прыщи, имеющие жировое содержимое. Однако такие симптомы могут появляться и при некоторых других заболеваниях.
При отсутствии лечения гипертриглицеридемия приводит к развитию:
- ожирения;
- атеросклероза;
- цирроза печени;
- сахарного диабета.
Наиболее опасным осложнением считается панкреатит — воспаление поджелудочной железы. Острая форма патологии сопровождается:
- болями в эпигастральной области;
- тошнотой и рвотой;
- отсутствием аппетита;
- высокой температурой;
- истощением организма.
 При панкреатите происходит панкреонекроз — омертвение тканей части или всего органа.
При панкреатите происходит панкреонекроз — омертвение тканей части или всего органа.
Основные причины гипертриглицеридемии:
- пожилой возраст;
- гипертония;
- наличие хронических заболеваний эндокринной системы;
- алкоголизм.
Часто повышенный уровень триглицеридов в крови обнаруживается у пациентов, предпочитающих жирную пищу; у беременных женщин; у людей, проходящих гормональную терапию. Рассмотрим, как лечить это заболевание.
Терапевтические мероприятия
Лечение подразумевает применение лекарственных препаратов и изменение режима питания. Медикаментозная терапия проводится при тяжелых формах гипертриглицеридемии и начинается с минимальных доз. Наиболее часто назначаются:
- никотиновая кислота;
- фибраты;
- рыбий жир.
 Они блокируют производство триглицеридов в организме и замедляют усвоение поступающих извне веществ. При неэффективности лечения дозу препарата увеличивают либо лекарство заменяют.
Они блокируют производство триглицеридов в организме и замедляют усвоение поступающих извне веществ. При неэффективности лечения дозу препарата увеличивают либо лекарство заменяют.
Диета является важной частью немедикаментозного лечения. Суточный рацион должен содержать не более 1400 ккал, с помощью такого питания пациент может быстро избавиться от лишнего веса. Питаться необходимо небольшими порциями, 4–5 раз в день. Нельзя принимать пищу в вечернее и ночное время. Ограничить рекомендуется потребление макаронных и хлебобулочных изделий. Полностью отказываются от:
- кондитерских изделий;
- мороженого;
- меда;
- варенья;
- газированных напитков.
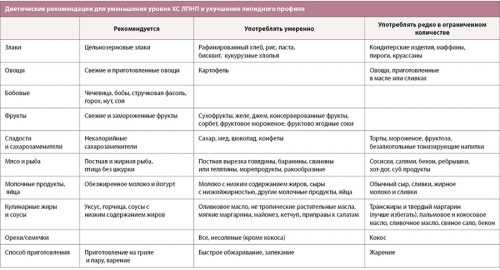
Даже сладкие фрукты рекомендуется исключить. Обогатить рацион клетчаткой можно за счет бобовых.
Рыбу необходимо употреблять не реже 3 раз в неделю. От жирных соусов и майонеза рекомендуется отказаться, допускается введение в рацион оливкового масла. Количество потребляемой в сутки соли снижают до 3 г. Лечебные диеты, умеренные физические нагрузки в течение 2 месяцев способствуют снижению уровня триглицеридов в 2 раза.
При значительном повышении концентрации жиров в организме следует обратиться к врачу.
НАШИ ЧИТАТЕЛИ РЕКОМЕНДУЮТ!
Для снижения холестерина наши читатели успешно используют Aterol. Видя, такую популярность этого средства мы решили предложить его и вашему вниманию.
Подробнее здесь…
Липоевая кислота при повышенном холестерине: как принимать?
- Стабилизирует уровень сахара надолго
- Восстанавливает выработку инсулина поджелудочной железой
Узнать больше…
Липоевая кислота — биоактивное соединение, которое ранее относилось к группе витаминоподобных соединений. В настоящий момент большинство исследователей это соединение относят к витаминам, имеющим лекарственные свойства.
Липоевая кислота также в фармакологии носит названия лапамид, тиоктовая кислота, парааминобензойная кислота, альфа-липоевая кислота, витамин N и берлитион.
Общепризнанным международным названием этого соединения является тиоктовая кислота.
На основании этого соединения фармакологическая промышленность выпускает медицинские препараты такие, как, например, Берлитион, Тиоктацид и Липоевая кислота.
Липоевая кислота является важнейшим элементом в цепочке метаболизма жиров в организме. При достаточном количестве этого компонента в организме человека снижается количество холестерина.
Тиоктовая кислота, способствуя снижению уровня холестерина в крови, препятствует развитию осложнений, возникающих при развитии сахарного диабета на фоне избыточного веса тела.
Избыточный вес тела чаще всего сопровождается повышенным содержанием холестерина. Липоевая кислота при холестерине способствует его снижению, что предотвращает развитие нарушений в работе сердца, сосудистой и нервной системы.
Наличие достаточного количества этого соединения в организме способствует предотвращению развития инсультов и инфарктов, при их появлении сглаживает последствия таких осложнений.
Благодаря дополнительному приему этого биоактивного соединения происходит более полное и более быстрое восстановление организма после возникновения инсульта, а степень пареза и ухудшения выполнения своих функций нервной тканью головного мозга значительно снижается.
Физические свойства липоевой кислоты
Липоевая кислота по физическим характеристикам является кристаллическим порошком, который имеет желтоватую окраску. Это соединение имеет горький вкус и специфический запах. Кристаллическое соединение слаборастворимо в воде и отлично растворяется в спиртах. В воде растворяется очень хорошо натриевая соль липоевой кислоты. Это свойство соли липоевой кислоты обуславливает применение этого соединения, а не чистой липоевой кислоты.
Это соединение применяется при изготовлении различных медпрепаратов и разных БАДов.
Это соединение оказывает на человека сильное антиоксидантное воздействие на организм. Поступление этого соединения в организм позволяет поддерживать на должном уровне жизненные силы организма.
Благодаря наличию антиоксидантных свойств это соединение способствует связыванию и выведению из организма различных типов свободных радикалов. У витамина N имеется четко выраженная способность связывать и выводить из организма человека токсических для него компоненты и ионы тяжелых металлов.
Помимо этого липоевая кислота способствует нормализации функционирования ткани печени. Достаточное количество этого соединения в организме предотвращает развитие повреждений печеночной ткани при возникновении и развитии хронических недугов, таких как гепатит и цирроз.
Препараты, имеющие в своем составе липоевую кислоту, обладают четко выраженными гепапротекторными свойствами.
Биохимические свойства липоевой кислоты
Липоевая кислота способна оказывать инсулиноподобное действие, что позволяет использовать препараты, содержащие это соединение для замещения инсулина при возникновении его недостатка в случае развития в организме сахарного диабета.
Благодаря наличию этого свойства препараты с содержанием витамина N позволяют на начальных стадиях развития сахарного диабета обеспечивать глюкозой клетки периферических тканей организма. Это приводит к снижению показателя содержания сахаров в плазме крови. Препараты, в состав которых входит витамин, способны благодаря наличию своих свойств усиливать действие инсулина и устраняют возможное глюкозное голодание.
Такое состояние является частым явлением при развитии в организме сахарного диабета второго типа.
Благодаря усилению проницаемости клеток периферических тканей для глюкозы все метаболические процессы в клетках начинают протекать значительно быстрее и более полно. Это обусловлено тем, что глюкоза в клетке является главным источником энергии.
Липоевая кислота благодаря наличию у нее таких специфических свойств, препараты, содержащие это соединение, часто применяются в процессе проведения терапии инсулиннезависимого типа сахарного диабета.
За счет нормализации функционирования различных органов, происходит улучшение общего состояния организма.
Благодаря наличию антиоксидантных свойств соединение способствует восстановлению структуры и функционирования нервной ткани.
При применении этого соединения происходит улучшение большинства функций организма.
Витамин представляет собой естественный метаболит, который образуется в организме человека и способствует нормализации функционирования органов и их систем.
Поступление липоевой кислоты в организм в достаточном количестве способствует снижению уровня холестерина в организме.
Поступление тиоктовой кислоты в организм человека
В нормальном состоянии это биоактивное соединение поступает в организм человека из продуктов питания, которые являются богатыми на содержание этого соединения.
Помимо этого это активное вещество способно синтезироваться организмом самостоятельно, поэтому липоевая кислота не относится к числу незаменимых соединений.
Следует заметить, что с возрастом, а также при некоторых серьезных нарушениях в организме синтез этого химвещества сможет значительно снижаться в организме. Это приводит к тому, что человек, страдающий некоторыми видами заболеваний, вынужден принимать для компенсации недостатка витамина N в организме специальные медпрепараты, позволяющие восполнить недостаток.
Вторым вариантом компенсации недостатка витамина является корректировка рациона питания с целью потребления большего количества продуктов, в которых имеется повышенное содержание липоевой кислоты. Для снижения холестерина в организме при сахарном диабете рекомендуется употреблять большое количество продуктов богатых на содержание липоевой кислоты. Это снижает вероятность развития осложнений и уменьшает степень развития ожирения, которое является сопутствующим осложнением при сахарном диабете второго типа.
Липоевая кислота содержится в наибольшем количестве в следующих продуктах питания:
- бананы;
- бобовые – горох, фасоль;
- мясо говядины;
- печень говядины;
- грибы;
- дрожжи;
- любые сорта капусты;
- зелень – шпинат, петрушка, укроп, базилик;
- лук;
- молоко и молочные продукты;
- почки;
- рис;
- перец;
- сердце;
- яйца.
Другие продукты, которые не указаны в этом перечне также имеют в своем составе это биоактивное соединение, но его содержание является очень небольшим.
Нормой потребления для нормального функционирования организма человека считается 25-50 мг соединения в сутки. Беременные и кормящие матери должны потреблять альфа-липоевой кислоты около 75 мг в сутки, а дети до 15 лет от 12,5 до 25 мг в сутки.
В случае наличия в организме больного заболеваний печени почек или сердца, нарушающих их функционирование норма потребления этого соединения возрастает до 75 мг в сутки для взрослого человека. Этот показатель не зависит от возраста.
Это связано с тем, что при наличии недугов происходит более быстрое расходование биоактивного соединения в организме.
Избыток и дефицит витамина N в организме
Четко выраженных признаков или специфических симптомов недостатка витамина в организме на сегодня не выявлено.
Это связано с тем, что этот компонент метаболизма человеческого организма самостоятельно может синтезироваться клетками и всегда присутствует хотя бы в небольшом количестве.
При недостаточном количестве этого соединения в организме человека могут развиваться некоторые нарушения.
Основными нарушениями, выявляемыми в случае наличия дефицита липоевой кислоты, являются следующие:
- Появление частых неврологических симптомов, которые проявляются в виде головокружений, болевых ощущений в области головы, развитии полиневритов и диабетической невропатии.
- Нарушения в функционировании ткани печени, приводящие к развитию жирового гепатоза и нарушениям процессов желчеобразования.
- Развитие атеросклеротических процессов в сосудистой системе.
- Развитие метаболического ацидоза.
- Появление мышечных спазмов.
- Развитие миокардиодистрофии.
Избытка витамина N в организме не возникает. Это связано с тем, что любые излишки этого соединения, поступающие в организм с продуктами или принимаемыми БАДами, очень быстро выводятся из него. При этом в случае возникновения избытка витамина он не успевает оказать на организм существенного негативного влияния до своего выведения.
В редких случаях при наличии нарушений в процессах выведения наблюдается развитие гипервитаминоза. Такая ситуация может быть характерна для случаев длительного применения препаратов с высоким содержанием липоевой кислоты в дозировках превышающих рекомендуемые.
Переизбыток витамина в организме проявляется появлением изжоги, повышенной кислотности желудочного сока, появлением болевых ощущений в подложечной области. Гипервитаминоз может также проявляться в виде возникновения аллергических реакций на кожных покровах тела.
Препараты и БАДы липоевой кислоты, показания к применению
В настоящий момент осуществляется выпуск лекарственных препаратов и БАДов, которые содержат этот витамин.
Лекарственные средства предназначены для проведения медикаментозной терапии при возникновении различных заболеваний связанных с недостатком липоевой кислоты.
БАДы рекомендуются для применения в целях профилактики возникновения нарушений в работе организма.
Применение лекарственных средств, в состав которых входит липоевая кислота, осуществляется чаще всего при выявлении у пациента следующих заболеваний:
- различных форм нейропатии;
- нарушений в работе печени;
- нарушений в работе сердечно-сосудистой системы.
Лекарственные препараты выпускаются в виде капсул таблеток и раствор для проведения инъекций.
БАДы выпускаются только в форме капсул и таблеток.
Наиболее распространенными медпрепаратами, содержащими липоевую кислоту, являются следующие:
- Берлитион. Выпускается в виде таблеток и концентрата для приготовления растворов для внутривенных инъекций.
- Липамид. Препарат выпускается в форме таблеток.
- Липоевая кислота. Препарат реализуется в форме таблеток и раствора для осуществления внутримышечных инъекций.
- Липотиоксон – средство для приготовления растворов предназначенных для внутривенных инъекций.
- Нейролипон. Препарат производится в виде капсул для перорального применения и концентрата для приготовления раствора для проведения внутривенных инъекций.
- Тиогамма – производится в форме таблеток и концентрата. Предназначенного для приготовления раствора.
- Тиоктовая кислота – медсредство производится в форме таблеток.
В качестве компонента липоевая кислота входит в следующие БАДы:
- Антиоксидант от NSP;
- Альфа-липоевая кислота от DHC;
- Альфа-липоевая кислота от Солгар;
- Альфа Д3 – Тева;
- Гастрофилин Плюс;
- Нутрикоэнзим Q10 с альфа-липоевой кислотой от Солгар.
Липоевая кислота входит в состав поливитаминных комплексов:
- Алфавит Диабет.
- Алфавит Эффект.
- Компливит Диабет.
- Компливит Сияние.
Применяется липоевая кислота с профилактической целью или в качестве компонента при проведении комплексной терапии разных заболеваний. В качестве профилактической меры рекомендуется использовать БАДы и поливитаминные комплексы. Суточный прием липоевой кислоты при применении БАДов должен составлять 25-50 мг. При проведении комплексной терапии заболеваний дозировка принимаемой липоевой кислоты может составлять до 600 мг в сутки.
О пользе липоевой кислоты для диабетика расскажет видео в этой статье.
- Стабилизирует уровень сахара надолго
- Восстанавливает выработку инсулина поджелудочной железой
Узнать больше…
krov.holesterin-lechenie.ru
Синтез жиров
Синтезируются жиры из глицерина и жирных кислот.
Глицерин в организме возникает при распаде жира (пищевого и собственного), а также легко образуются из углеводов.
Жирные кислоты синтезируются из ацетилкофермента А. Ацетилкофермент А – универсальный метаболит. Для его синтеза необходимы водород и энергия АТФ. Водород же получается из НАДФ.Н2. В организме синтезируются только насыщенные и мононасыщенные (имеющие одну двойную связь) жирные кислоты. Жирные кислоты, имеющие две и более двойных связей в молекуле, называемые полинасыщенные, в организме не синтезируются и должны поступать с пищей. Для синтеза жира могут быть использованы жирные кислоты – продукты гидролиза пищевого и собственного жиров.
Все участники синтеза жира должны быть в активном виде: глицерин в форме глицерофосфата, а жирные кислоты в форме ацетилкофермента А. Синтез жира осуществляется в цитоплазме клеток (преимущественно жировой ткани, печени, тонкой кишки). Пути синтеза жиров представлены в схеме.
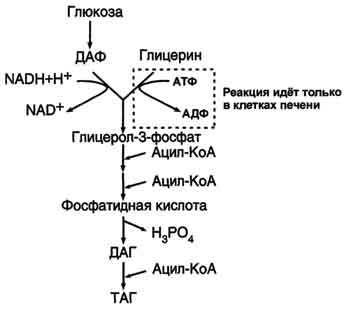
Следует отметить, что глицерин и жирные кислоты могут быть получены из углеводов. Поэтому при избыточном потреблении их на фоне малоподвижного образа жизни развивается ожирение.
Строение и обмен нуклеиновых кислот.
1.Строение мононуклеотидов.
2. Строение нуклеиновых кислот.
3. Переваривание нуклеиновых кислот. Катаболизм.
4. Синтез нуклеотидов.
5. Синтез нуклеиновых кислот.
Строение мононуклеотидов.
По своему строению нуклеиновые кислоты являются полинуклеотидами, состоящими из мононуклеотидов или нуклеотидов.
Нуклеотид сложное органическое соединение, состоящее из трех частей: азотистого основания, углевода и остатков фосфорной кислоты.
Азотистые основания — это гетероциклические органические соединения, относящиеся к двум классам – пурины и пиримидины. Из пуринов в состав нуклеиновых кислот входят аденин и гуанин
А из пиримидинов цитозин, тимин(ДНК) и урацил(РНК) .
Углеводом, входящим в состав нуклеотидов может быть рибоза (РНК) и дезоксирибоза (ДНК)
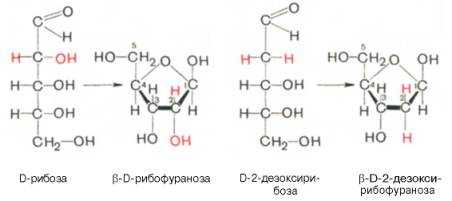
Азотистое основание, связанное с углеводом называется нуклеозидом.
Фосфорная кислота присоединяется эфирной связью к пятому атому углерода рибозы или дезоксирибозы. Нуклеотиды, входящие в состав нуклеиновых кислот имеют один остаток фосфорной кислоты и называются мононуклеотидами. Однако в клетке встречаются ди- и тринуклеотиды.
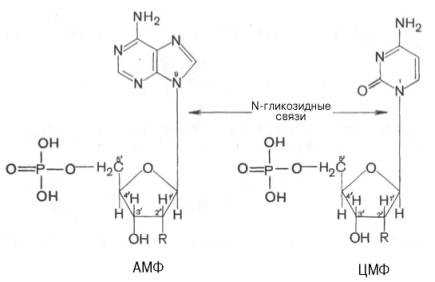
Например, нуклеотид, состоящий из аденина, рибозы и одного остатка фосфорной кислоты называется аденозинмонофосфат или АМФ, а из цитозина и одного остатка фосфорной кислоты цитозинмонофосфат или ЦМФ.
Строение нуклеиновых кислот.
С точки зрения химии нуклеиновые кислоты – нерегулярные полимеры, состоящие из довольно сложно устроенных мономеров, называемых нуклеотидами.
Нуклеиновых кислот в клетках встречается два класса – ДНК и РНК. ДНК – дезоксирибонуклеиновая кислота, а РНК – рибонуклеиновая кислота.
Структура ДНК очень сложна и своеобразна. Каждый нуклеотид, из которого состоит ДНК, состоит из остатков сахара дезоксирибозы, остатка фосфорной кислоты и азотистого основания. Азотистых оснований четыре разновидности: аденин, гуанин, цитозин, и тимин. Нуклеотиды соединены в длинные цепи с помощью фосфорно-диэфирных связей.
В 1953 году исследователи Джеймс Уотсон и Френсис Крик предложили модель, которая объясняла строение молекулы ДНК. Согласно их теории ДНК состоит из двух спиральных цепей, соединенных водородными связями. Азотистые основания обеих цепей находятся внутри спирали и образуют водородные связи. Эти связи соединяют цепи ДНК не случайным образом, а по принципу комплементарности или соответствия. Суть этого принципа в следующем, если в одной цепи стоит тимин, то в противоположной цепи, ему соответствует аденин, а против гуанина всегда стоит цитозин. Это значит, что при удвоении ДНК на каждой из её цепей может быть достроена другая, и вместо одной молекулы получатся сразу две.
Принцип комплементарности лежит в основе всех процессов связанных с реализацией генетической информации: репликации ДНК (удвоения ДНК), транскрипции(синтеза РНК на ДНК матрицах), и трансляции(биосинтеза белка на основе матриц РНК).
На схемах ниже продемонстрирована структура ДНК и принцип комплементарности.
studfiles.net
1) Регуляция синтеза жиров.
1.Триглицериды синтезируются вклетках различных органов и тканей в качестве резервных питательных веществ, однако их синтез с наибольшей интенсивностью протекает в клетках печени и в клетках жировой ткани. Для синтеза необходимы высшие жирные кислоты и глицерол. Высшие жирные кислоты или поступают в клетки из плазмы крови, или же синтезируются в них из ацетил-КоА. Глицерол может поступать в клетки из плазмы крови, однако основным источником глицерола для синтеза триглицеридов и фосфолипидов в клетках служит фосфодигидроксиацетон — промежуточный продукт расщепления глюкозы.
Высшие жирные кислоты участвуют в биосинтезе триглицеридов в виде своих активированных производных — ацил-КоА. Необходимый для синтеза 3-фосфоглицерол образуется или путем восстановления фосфодигидроксиацетона ( реакция катализируется глицеральдегид-3-фосфатдегидрогеназой за счет обратимости ее действия ), или за счет фосфорилирования свободного глицерола (реакция катализируется АТФ-зависимой глицеролкиназой).
После образования 3-фосфоглицерола за счет двух последовательных реакций ацилирования образуется фосфатидная кислота. От нее гидролитическим путем отщепляется остаток фосфорной кислоты с образованием диглицерида, а затем с помощью еще одной реакции ацилирования завершается синтез триацилглицерина.
Синтез резервных триацилглицеринов идет в основном в период абсорбции продуктов пищеварения и поступления их во внутреннюю среду организма. В постабсорбционном периоде идет мобилизация резервных триглицеридов. Они расщепляются в клетках под действием ферментов липаз.
2 вопрос. Мобилизация жиров из жировой ткани
Адипоциты (место депонирования жиров) располагаются в основном под кожей, образуя подкожный жировой слой, и в брюшной полости, образуя большой и.малый сальники. Мобилизация жиров, т.е. гидролиз до глицерола и жирных кислот, происходит в постабсорбтивный период, при голодании и активной физической работе. Гидролиз внутриклеточного жира осуществляется под действием фермента гормончувствительной липазы — ТАГ-липазы. Этот фермент отщепляет одну жирную кислоту у первого углеродного атома глицерола с образованием диацилглицерола, а затем другие липазы гидролизуют его до глицерола и жирных кислот, которые поступают в кровь. Глицерол как водорастворимое вещество транспортируется кровью в свободном виде, а жирные кислоты (гидрофобные молекулы) в комплексе с белком плазмы — альбумином.
Вопрос№3
Регуляция процессов синтеза и «мобилизации» триглицеридов, их биологическая роль.
Какой процесс будет преобладать:
В абсорбированный период при увеличении соотношения инсулин/глюкагон в печени активируется синтез жиров.
В жировой ткани
индуцируется синтез ЛП-липазы в адипоцитах и осуществляется ее экспонирование на поверхность эндотелия → увеличивается поступление жирных кислот (жк) в адипоциты.
инсулин активирует белки-переносчики глюкогзы-ГЛЮТ-4
поступление глюкозы в адипоциты и гликолиз активируются.
(в результате) образуются все необходимые компоненты для синтеза жк: глицерол-3-фосфат, активные формы жк
В печени
инсулин, действуя на различные механизмы, активирует ферменты путем дефосфолирирования и индуцирует их синтез.
увеличивается активность и синтез ферментов ─ регуляторные ферменты гликолиза :пировутдегидрогеназный комплекс, ферменты, участвующие в синтезе жк из ацнтил-КоА ─ участвующих в превращении части глюкозы в жиры.
(результат) увеличение синтеза жиров и секреция их в кровь в составе ЛПОНП.
ЛПОНП доставляют жиры в капилляры жировой ткани, где действие ЛП-липазы обеспечивает быстрое поступление жк в адипоциты, где они депонируются в составе триацилглицеринов.
Биологическое значение:
— запасание жиров в жировой ткани – основная форма депонирования источников энергии в организме человека.
2) Регуляция мобилизации жиров.
Стимулируется:
глюкагоном и адреналином
в меньшей степени другими гормонами: соматотропином,кортизолом
В постабсорбированный период:
при голодании глюкагон, действуя на адипоциты через аденилциклазную систему
активирует протеинкиназуА
которая фосфолирирует → активирует гормончувствительную липазу
что инициирует липолиз
и выделение жк и глицерина в кровь.
1. при физической нагрузке адреналин, который действует на аденилциклазную систему через:
Ɓ-рецепторы (адренергичнские), которые при выскокой концентрации в крови приводят к липолитическому действию.
А-рецепторы, которые связаны с ингибирущим G-белком, который инактивирует аденилциклазную систему, при низких концентрациях в крови –антилиполитическое действие.

4. В крови триацилглицеролы, входящие в состав зрелых хиломикронов, гидролизуются ферментом липопротеинлипазой. ЛП-липаза связана с гепарансульфатом (гетерополисахоридом), находящимся на поверхности эндотелиальных клеток, выстилающих стенки кровеносных сосудов. ЛП-липаза гидролизует молекулы жиров до 3 молекул ЖК. На поверхности ХМ различают 2 фактора, необходимых для активности ЛП-липазы – АпоС-II и фосфолипиды. АпоС-II активирует этот фермент, а фосфолипаза участвует в связывание этого фермента с поверхностью ХМ.
ЛП-липазы синтезируются в разных клетках многих тканей, но они все отличаются по значению. Поэтому гидролиз ЛП-липазы происходит в абсорбированный период. ЖК поступают в адипоциты и используются для синтеза жиров. В постабсорбированном состоянии, когда количество жиров в крови снижается, ЛП-липаза продолжает синтезировать жиры в составе ЛПОНП, которые присутствуют в крови в небольшом количестве, и ЖК используются в этой ткани как источник энергии. Даже при низкой концентрации жиров в крови.
studfiles.net
Синтез углеводов из жиров
Поиск ЛекцийПроцесс синтеза углеводов из жиров можно представить общей схемой:
Рисунок 7 – Общая схема синтеза углеводов из жиров
Один из основных продуктов расщепления липидов – глицерин – легко используется в синтезе углеводов через образование глицеральдегид-3-фосфата и его вступление в глюнеогенез. У растений и микроорганизмов столь же легко используется на синтез углеводов и другой важный продукт расщепления липидов– жирные кислоты (ацетил-КоА), через глиоксилатный цикл.
Но общая схема не отражает всех биохимических процессов, происходящих в результате образования углеводов из жиров.
Поэтому рассмотрим все этапы данного процесса.
Схема синтеза углеводов и жиров более полно представлена на рисунке 8 и происходит в ряд этапов.
1 этап. Гидролитическое расщепление жира под действием фермента липазы на глицерин и высшие жирные кислоты (см. п.1.2). Продукты гидролиза должны, пройдя ряд превращений, превратиться в глюкозу.
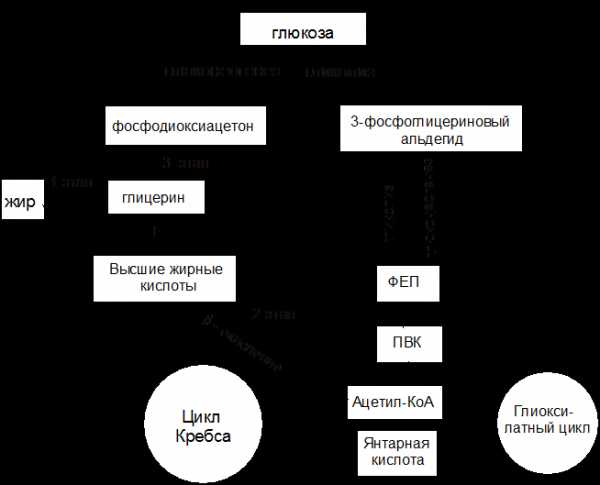
Рисунок 8 – Схема биосинтеза углеводов из жиров
2 этап. Превращение высших жирных кислот в глюкозу. Высшие жирные кислоты, которые образовались в результате гидролиза жира, разрушаются преимущественно путем b-окисления (этот процесс был рассмотрен ранее в разделе 1.2 пункт 1.2.2). Окончательным продуктом этого процесса является ацетил-КоА.
Глиоксилатный цикл
Растения, некоторые бактерии и грибы могут использовать ацетил-КоА не только в цикле Кребса, но и в цикле, получившим название глиоксилатного. Этот цикл играет важную роль в качестве связующего звена в метаболизме жиров и углеводов.
Особенно интенсивно глиоксилатный цикл функционирует в особых клеточных органеллах–глиоксисомах – при прорастании семян масличных растений. При этом происходит превращение жира в углеводы, необходимые для развития проростка семени. Этот процесс функционирует до тех пор, пока у проростка не разовьется способность к фотосинтезу. Когда в конце прорастания запасной жир истощается, глиоксисомы в клетке исчезают.
Глиоксилатный путь специфичен только для растений и бактерий, у животных организмов он отсутствует. Возможность функционирования глиоксилатного цикла связана с тем, что растения и бактерии способны синтезировать такие ферменты, как изоцитратлиаза и малатсинтаза, которые вместе с некоторыми ферментами цикла Кребса участвуют в глиоксилатном цикле.
Схема окисления ацетил-КоА по глиоксилатному пути показана на рисунке 9.
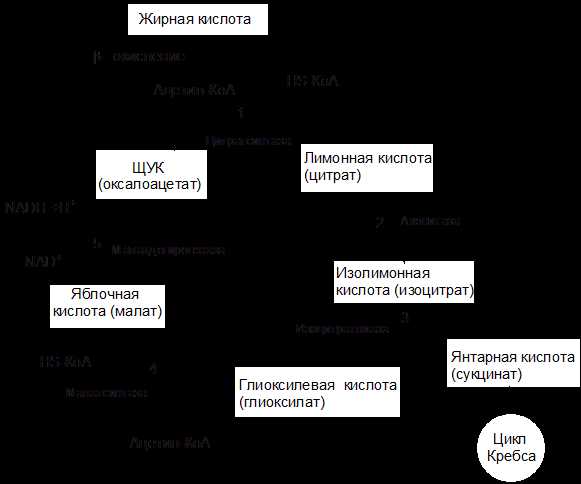
Рисунок 9 – Схема глиоксилатного цикла
Две начальные реакции (1 и 2) глиоксилатного цикла идентичны таковым цикла трикарбоновых кислот. В первой реакции (1) ацетил-КоА конденсируется с оксалоацетатом под действием цитратсинтазы, с образованием цитрата. Во второй реакции цитрат изомеризуется в изоцитрат при участии аконитатгидратазы. Следующие реакции, специфичные для глиоксилатного цикла, катализируются специальными ферментами. В третьей реакции изоцитрат под действием изоцитратлиазы расщепляется на глиоксилевую кислоту и янтарную кислоту:
В ходе четвертой реакции, катализируемой малатсинтазой, глиоксилат конденсируется с ацетил-КоА (второй молекулой ацетил-КоА, вступающей в глиоксилатный цикл) с образованием яблочной кислоты (малат):
Затем в пятой реакции малат окисляется до оксалоацетата. Эта реакция идентична конечной реакции цикла трикарбоновых кислот; она же является конечной реакцией глиоксилатного цикла, т.к. образовавшийся оксалоацетат вновь конденсируется с новой молекулой ацетил-КоА, начиная тем самым новый оборот цикла.
Образовавшаяся в третьей реакции глиоксилатного цикла янтарная кислота не используется этим циклом, а подвергается дальнейшим превращениям.
Рекомендуемые страницы:
poisk-ru.ru
Синтез жиров — стр. 5
3.3. Синтез жиров
Синтезируются жиры из глицерина и жирных кислот. Глицерин в организме возникает при распаде жира (пищевого или собственного), а также легко образуется из углеводов. Жирные кислоты синтезируются из ацетилкофермента А — универсального метаболита организма. Для этого синтеза еще необходимы водород (в форме НАДФН2) и энергия АТФ. В организме синтезируются только насыщенные и мононенасыщенные (имеющие одну двойную связь) жирные кислоты. Кислоты, содержащие две и более двойных связей в своей молекуле (полиненасыщенные), в организме не синтезируются и должны поступать с пищей. Для синтеза жира также могут быть использованы жирные кислоты — продукты гидролиза пищевого и собственного жиров.
Все участники синтеза жира должны быть в активном виде: глицерин в форме глицерофосфата, а жирные кислоты в форме ацилко-фермента А. Синтез жира осуществляется в цитоплазме клеток (преимущественно жировой ткани, печени, тонкой кишки) и протекает по следующей схеме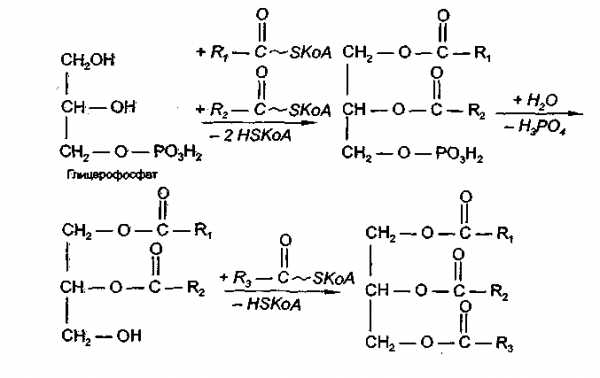
Следует подчеркнуть, что глицерин и жирные кислоты могут быть получены углеводов. Поэтому при избыточном потреблении углеводов на фоне малоподвижного образа жизни развивается ожирение.
Лекция 4. Обмен белков
4.1. Катаболизм белков
Белки, входящие в состав клеток организма, также подвергаются постоянному распаду под влиянием внутриклеточных протеолитических ферментов, называемых внутриклеточными протеиназами или катепсинами. Эти ферменты локализованы в специальных внутриклеточных органоидах – лизосомах. Под действием катепсинов белки организма также превращаются в аминокислоты. (Важно отметить, что распад как пищевых, так и собственных белков организма приводит к образованию одних и тех же 20 видов аминокислот.) В сутки расщепляется примерно 200 г белков организма. Поэтому в течение суток в организме появляется около 300 г свободных аминокислот.
4.2. Синтез белков
Большая часть аминокислот используется для синтеза белков. Синтез белков происходит при обязательном участии нуклеиновых кислот.
Первый этап синтеза белка — транскрипция — осуществляется в клеточном ядре с использованием ДНК как источника генетической информации. Генетическая информация обусловливает порядок расположения аминокислот в полипептидных цепях синтезируемого белка. Эта информация закодирована последовательностью азотистых оснований в молекуле ДНК. Каждая аминокислота кодируется сочетанием трех азотистых оснований, называемым кодоном, или триплетом. Участок молекулы ДНК, содержащий информацию об определенном белке, получил название «ген». На этом участке ДНК во время транскрипции по принципу комплементарности синтезируется информационная РНК (иРНК). Эта нуклеиновая кислота представляет собой копию соответствующего гена. Образовавшаяся иРНК выходит из ядра и поступает в цитоплазму. Аналогичным образом на ДНК как на матрице происходит синтез рибосомных (рРНК) и транспортных (тРНК).
В ходе второго этапа – рекогниции (распознавания), протекающего в цитоплазме, аминокислоты избирательно связываются со своими переносчиками — транспортными РНК(тРНК). Молекула каждой тРНК представляет собой короткую полинуклеотидную цепь, содержащую примерно 80 нуклеотидов и частично закрученную в двойную спираль, что приводит к возникновению конфигурации «изогнутого клеверного листа». На одном конце полинуклеотидной цепи у всех тРНК находится нуклеотид, содержащий аденин. К этому концу молекулы тРНК присоединяется аминокислота. Петля, противоположная месту присоединения аминокислоты, содержит антикодон, состоящий из трех азотистых оснований и предназначенный для последующего связывания с комплементарным кодоном иРНК. Одна из боковых петель молекулы тРНК обеспечивает присоединение тРНК к ферменту, участвующему в рекогниции, а другая, боковая, петля необходима для присоединения тРНК к рибосоме на следующем этапе синтеза белка.
На этом этапе в качестве источника энергии используется молекула АТФ. В результате рекогниции образуется комплекс аминокислота-тРНК. В связи с этим второй этап синтеза белка называют активацией аминокислот.
Третий этап синтеза белка — трансляция — происходит на рибосомах. Каждая рибосома состоит из двух частей — большой и малой субчастиц. По химическому составу обе субчастицы состоят из рРНК и белков. Рибосомы способны легко распадаться на субчастицы, которые снова могут соединяться друг с другом, образуя рибосому. Трансляция начинается с диссоциации рибосомы на субчастицы, которые сразу же присоединяются к начальной части молекулы иРНК, поступающей из ядра. При этом между субчастицами остается пространство (так называемый туннель), где располагается небольшой участок иРНК. Затем к образовавшемуся комплексу рибосома — иРНК присоединяются тРНК, связанные с аминокислотами. Присоединение тРНК к этому комплексу происходит путем связывания одной из боковых петлей тРНК с рибосомой и связывания антикодона тРНК с комплементарным ему кодоном иРНК, находящимся в туннеле между субчастицами рибосомы. Одновременно к комплексу рибосома — иРНК могут присоединиться только две тРНК с аминокислотами.
Благодаря специфическому связыванию антикодонов тРНК с кодонами иРНК, к участку молекулы иРНК, находящемуся в туннеле, присоединяются только молекулы тех тРНК, у которых антикодоны комплементарны кодонам иРНК. Поэтому эти тРНК доставляют в рибосомы только строго определенные аминокислоты. Далее аминокислоты соединяются друг с другом пептидной связью и образуется дипептид, который связан с одной из тРНК. После этого рибосома передвигается вдоль иРНК ровно на один кодон (это перемещение рибосомы называется траислокацией).
В результате транслокации свободная (без аминокислоты) тРНК отщепляется от рибосомы, а в зоне туннеля появляется новый кодон, к которому присоединяется по принципу комплементарности еще одна тРНК с аминокислотой, соответствующей этому кодону. Доставленная аминокислота соединяется с ранее образовавшимся дипептидом, что приводит к удлинению пептидной цепи. Далее следуют новые транслокации, поступление на рибосому новых тРНК с аминокислотами и дальнейшее удлинение пептидной цепи.
Таким образом порядок включения аминокислот в синтезируемый белок определяется последовательностью кодонов в иРНК. Завершается синтез полипептидной цепи при поступлении в туннель особого кодона, который не кодирует аминокислоты и к которому не может присоединиться ни одна тРНК. Такие кодоны называются терминирующими.
В итоге за счет описанных трех этапов синтезируются полипептиды, т. е. формируется первичная структура белка. Высшие (пространственные) структуры (вторичная, третичная, четвертичная) возникают самопроизвольно.
Синтез белков — процесс энергоемкий. Для включения в молекулу синтезируемого белка только одной аминокислоты требуется не менее трех молекул АТФ.
4.3. Метаболизм аминокислот
Помимо синтеза белков аминокислоты еще используются для синтеза различных небелковых соединений, имеющих важное биологическое значение. Часть аминокислот подвергается распаду и превращается в конечные продукты: С02, Н20 и NН3 Распад начинается с реакций, общих для большинства аминокислот.
К ним относятся:
а) декарбоксилирование — отщепление от аминокислот карбоксильной группы в виде углекислого газа:
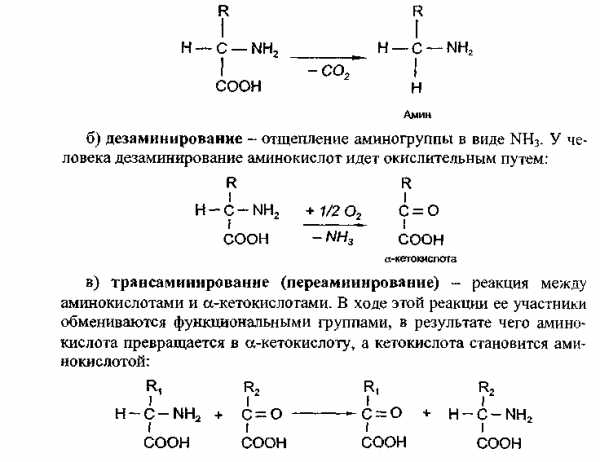
Трансаминированию подвергаются все аминокислоты. В этой реакции участвует кофермент — фосфопиридоксаль, для образования которого необходим витамин В6 — пиридоксин.
Трансаминирование — это главное превращение аминокислот в организме, так как его скорость значительно выше, чем у реакций декар-боксилирования и дезаминирования.
Трансаминирование выполняет две основные функции:
а) за счет трансаминирования одни аминокислоты могут превращаться в другие. При этом общее количество аминокислот не меняется, но изменяется соотношение между ними. С пищей в организм посту пают чужеродные белки, у которых аминокислоты находятся в иных пропорциях по сравнению с белками организма. Путем трансаминирования происходит корректировка аминокислотного состава организма.
б) является составной частью косвенного (непрямого) дезаминирования аминокислот — процесса, с которого начинается распад большинства аминокислот.
На первой стадии этого процесса аминокислоты вступают в реакцию трансаминирования с α-кетоглутаровой кислотой. Аминокислоты при этом превращаются в α-кетокислоты, а α-кетоглутаровая кислота переходит в глутаминовую кислоту (аминокислота).
На второй стадии появившаяся глутаминовая кислота подвергается дезаминированию, от нее отщепляется NН3 и снова образуется α-кетоглутаровая кислота. Образовавшиеся α-кетокислоты далее подвергаются глубокому распаду и превращаются в конечные продукты С02 и Н20. Для каждой из 20 кетокислоr (их образуется столько же, сколько имеется видов аминокислот) имеются свои специфические пути распада. Однако при распаде некоторых аминокислот в качестве промежуточного продукта образуется пировиноградная кислота, из которой возможен синтез глюкозы. Поэтому аминокислоты, из которых возникают такие кетокислоты, получили название глюкогенные. Другие же кетокислоты при своем распаде не образуют пирувата. Промежуточным продуктом у них является ацетилкофермент А, из которого невозможно получить глюкозу, но зато могут синтезироваться кетоновые тела. Аминокислоты, соответствующие таким кетокислотам, называются кетогенные.
Второй продукт косвенного дезаминирования аминокислот — аммиак. Для организма аммиак является высокотоксичным. Поэтому в организме имеются молекулярные механизмы его обезвреживания. По мере образования NН3 связывается во всех тканях с глутаминовой кислотой с образованием глутамина. Это временное обезвреживание аммиака. С током крови глутамин поступает в печень, где распадается опять на глутаминовую кислоту и NНз. Образовавшаяся глутаминовая кислота с кровью снова поступает в органы для обезвреживания новых порций аммиака. Освободившийся аммиак, а также углекислый газ в печени используются для синтеза мочевины.
Синтез мочевины — циклический, многостадийный процесс, потребляющий большое количество энергии. В синтезе мочевины очень важное участие принимает аминокислота орнитин. Эта аминокислота не входит в состав белков. Образуется орнитин из другой аминокислоты — аргинина, который присутствует в белках. В связи с важной ролью орнитина синтез мочевины получил название орнитиновый цикл.
Впроцессе синтеза к орнитину присоединяются две молекулы аммиака и молекула углекислого газа, и орнитин превращается в аргинин, от которого сразу же отщепляется мочевина, и вновь образуется орнитин. Наряду с орнитином и аргинином в образовании мочевины еще участвуют аминокислоты: глутамин и аспарагиновая кислота. Глутамин является поставщиком аммиака, а аспарагиновая кислота его переносчиком.
Синтез мочевины — это окончательное обезвреживание аммиака. Из печени с кровью мочевина поступает в почки и выделяется с мочой. В сутки образуется 20-35 г мочевины. Выделение мочевины с мочой характеризует скорость распада белков в организме.
Раздел 3. Биохимия мышечной ткани
Лекция 5. Биохимия мышц
5.1. Клеточное строение мышечного волокна
У животных и человека имеются два основных типа мышц: поперечно-полосатые и гладкие. Поперечно-полосатые мышцы прикрепляются к костям, т. е. к скелету, и поэтому еще называются скелетными. Поперечно-полосатые мышечные волокна составляют также основу сердечной мышцы – миокарда, хотя имеются определенные различия в строении миокарда и скелетных мышц. Гладкие мышцы образуют мускулатуру стенок кровеносных сосудов, кишечника, пронизывают ткани внутренних органов и кожу.
Каждая поперечно-полосатая мышца состоит из нескольких тысяч волокон, объединенных соединительнотканными прослойками и такой же оболочкой — фасцией. Мышечные волокна (миоциты) представляют собою сильно вытянутые многоядерные клетки крупного размера длиной до 2-3 см, а в некоторых мышцах даже более 10 см. Толщина мышечных клеток около 0,1-0,2 мм.
Как и любая клетка, миоцит содержит такие обязательные органоиды, как ядра, митохондрии, рибосомы, цитоплазматическую сеть и клеточную оболочку. Особенностью миоцитов, отличающих их от других клеток, является наличие сократительных элементов — миофибрилл.
Ядра окружены оболочкой — нуклеолеммой и состоят в основном из нуклеопротеидов. В ядре содержится генетическая информация для синтеза белков.
Рибосомы — внутриклеточные образования, являющиеся по химическому составу нуклеопротеидами. На рибосомах происходит синтез белков.
Митохондрии — микроскопические пузырьки размером до 2-3 мкм, окруженные двойной мембраной. В митохондриях протекает окисление углеводов, жиров и аминокислот до углекислого газа и воды с использованием молекулярного кислорода (кислорода воздуха). За счет энергии, выделяющейся при окислении, в митохондриях осуществляется синтез АТФ. В тренированных мышцах митохондрии многочисленны и располагаются вдоль миофибрилл.
Цитоплазматическая сеть (саркоплазматическая сеть, саркоплаз-матический ретикулум) состоит из трубочек, канальцев и пузырьков, образованных мембранами и соединенных друг с другом. Саркоплазматическая сеть с помощью особых трубочек, называемых Т-системой, связана с оболочкой мышечной клетки — сарколеммой. Особо следует выделить в саркоплазматической сети пузырьки, называемые цистернами и содержащие в большой концентрации ионы кальция. В цистернах содержание ионов Са2+ примерно в тысячу раз выше, чем в цитозоле. Такой высокий градиент концентрации ионов кальция возникает вследствие функционирования фермента — кальциевой аденозинтри-фосфатазы (кальциевая АТФаза), встроенного в стенку цистерны. Этот фермент катализирует гидролиз АТФ и за счет выделяющейся при этом энергии обеспечивает перенос ионов кальция вовнутрь цистерн. Такой Механизм транспорта ионов кальция образно называется кальциевым насосом, или кальциевой помпой.
Цитоплазма (цитозоль, саркоплазма) занимает внутреннее пространство миоцитов и представляет собой коллоидный раствор, содержащий белки, гликоген, жировые капли и другие включения. На долю белков саркоплазмы приходится 25-30% от всех белков мышц. Среди саркоплазматических белков имеются активные ферменты. К ним в первую очередь следует отнести ферменты гликолиза, расщепляющие гликоген или глюкозу до пировиноградной или молочной кислоты. Еще один важный фермент саркоплазмы — креатинкиназа, участвующий в энергообеспечении мышечной работы. Особого внимания заслуживает белок саркоплазмы миоглобин, который по строению идентичен одной из субъединиц белка крови – гемоглобина. Состоит миоглобин из одного полипептида и одного гема. Функция миоглобина заключается в связывании молекулярного кислорода. Благодаря этому белку в мышечной ткани создается определенный запас кислорода. В последние годы установлена еще одна функция миоглобина — это перенос 02 от сарколеммы к мышечным митохондриям.
Кроме белков в саркоплазме имеются небелковые азотсодержащие вещества. Их называют, в отличие от белков, экстрактивными веществами, так как они легко экстрагируются водой. Среди них — адениловые нуклеотиды АТФ, АДФ, АМФ и другие нуклеотиды, причем преобладает АТФ. Концентрация АТФ в покое примерно 4-5 ммоль/кг. К экстрактивным веществам также относятся креатинфосфат, его предшественник — креатин и продукт необратимого распада креатинфосфата — креатинин. В покое концентрация креатинфосфата обычно 15-25 ммоль/кг. Из аминокислот в большом количестве имеются глутаминовая кислота и глутамин.
Основной углевод мышечной ткани — гликоген. Концентрация гликогена колеблется в пределах 0,2-3%. Свободная глюкоза в саркоплазме содержится в очень малой концентрации — имеются лишь ее следы. В процессе мышечной работы в саркоплазме происходит накопление продуктов углеводного обмена — лактата и пирувата.
Протоплазматический жир связан с белками и имеется в концентрации 1%. Запасной жир накапливается в мышцах, тренируемых на выносливость.
5.2. Структура сарколеммы
Каждое мышечное волокно окружено клеточной оболочкой — сарколеммой. Сарколемма представляет собою лилопротеидную мембрану толщиной около 10 нм. Снаружи сарколемма окружена сетью из переплетенных нитей белка коллагена. При мышечном сокращении в коллагеновой оболочке возникают упругие силы, за счет которых при расслаблении мышечное волокно растягивается и возвращается в исходное состояние. К сарколемме подходят окончания двигательных нервов. Место контакта нервного окончания с сарколеммой называется нервно-мышечный синапс, или концевая нервная пластинка.
Сократительные элементы — миофибриллы — занимают большую часть объема мышечных клеток, их диаметр около 1 мкм. В нетренированных мышцах миофибриллы расположены рассеянно, а в тренированных они сгруппированы в пучки, называемые полями Конгейма.
5.3. Строение анизотропных и изотропных дисков
Микроскопическое изучение строения миофибрилл показало, что они состоят из чередующихся светлых и темных участков, или дисков. В мышечных клетках миофибриллы располагаются таким образом, что светлые и темные участки рядом расположенных миофибрилл совпадают, что создает видимую под микроскопом поперечную исчерченность всего мышечного волокна. Было обнаружено, что миофибриллы являются сложными структурами, построенными, в свою очередь, из большого числа мышечных нитей (протофибрилл, или филаментов) двух типов — толстых и тонких. Толстые нити имеют диаметр 15 нм, тонкие — 7 нм.
Состоят же миофибриллы из чередующихся пучков параллельно расположенных толстых и тонких нитей, которые концами заходят друг в друга. Участок миофибриллы, состоящий из толстых нитей и находящихся между ними концов тонких нитей, обладает двойным лучепреломлением. При микроскопии этот участок задерживает видимый свет или поток электронов (при использовании электронного микроскопа) и поэтому кажется темным. Такие участки получили название анизотропные, или темные, диски (А-диски).
Светлые участки миофибрилл состоят из центральных частей тонких нитей. Они сравнительно легко пропускают лучи света или поток электронов, так как не обладают двойным лучепреломлением и называются изотропными, или светлыми, дисками (I-диски). В середине пучка тонких нитей поперечно располагается тонкая пластинка из белка, которая фиксирует положение мышечных нитей в пространстве. Эта пластинка хорошо видна под микроскопом в виде линии, идущей поперек I-диска, и названа Z-пластинкой.
Участок миофибриллы между соседними 2-линиями получил название саркомер. Его длина 2,5-3 мкм. Каждая миофибрилла состоит из нескольких сотен саркомеров (до 1000).
5.4. Строение и свойства сократительных белков
Изучение химического состава миофибрилл показало, что толстые и тонкие нити состоят только из белков.
Толстые нити состоят из белка миозина. Миозин — белок с молекулярной массой около 500 кДа, содержащий две очень длинные полипептидные цепи. Эти цепи образуют двойную спираль, но на одном конце эти нити расходятся и формируют шаровидное образование — глобулярную головку. Поэтому в молекуле миозина различают две части — глобулярную головку и хвост. В состав толстой нити входит около 300 миозиновых молекул, а на поперечном срезе толстой нити обнаруживается 18 молекул миозина. Миозиновые молекулы в толстых нитях переплетаются своими хвостами, а их головки выступают из толстой нити по правильной спирали. В головках миозина имеются два важных участка (центра). Один из них катализирует гидролитическое расщепление АТФ, т. е. соответствует активному центру фермента. АТФазная активность миозина впервые обнаружена отечественными биохимиками Энгельгардтом и Любимовой. Второй участок головки миозина обеспечивает во время мышечного сокращения связь толстых нитей с белком тонких нитей — актином.
Тонкие нити состоят из трех белков: актина, тропонина и тропомиозина.
Основной белок тонких нитей — актин. Актин — глобулярный белок с молекулярной массой 42 кДа. Этот белок обладает двумя важнейшими свойствами. Во-первых, проявляет высокую способность к полимеризации с образованием длинных цепей, называемых фибриллярным актином (можно сравнить с нитью бус). Во-вторых, как уже отмечалось, актин может соединяться с миозиновыми головками, что приводит к образованию между тонкими и толстыми нитями поперечных мостиков, или спаек.
Основой тонкой нити является двойная спираль из двух цепей фибриллярного актина, содержащая около 300 молекул глобулярного актина (как бы две нити бус, закрученные в двойную спираль, каждая бусинка соответствует глобулярному актину).
Еще один белок тонких нитей – тропомиозин – также имеет форму двойной спирали, но эта спираль образована полипептидными цепями и по размеру гораздо меньше двойной спирали актина. Тропомиозин располагается в желобке двойной спирали фибриллярного актина.
Третий белок тонких нитей – тропонин — присоединяется к тропомиозину и фиксирует его положение в желобке актина, при котором блокируется взаимодействие миозиновых головок с молекулами глобулярного актина тонких нитей.
5.5. Механизм мышечного сокращения
Мышечное сокращение является сложным механохимическим процессом, в ходе которого происходит преобразование химической энергии гидролитического расщепления АТФ в механическую работу, совершаемую мышцей.
В настоящее время этот механизм еще полностью не раскрыт. Но достоверно известно следующее:
Источником энергии, необходимой для мышечной работы является АТФ.
Гидролиз АТФ, сопровождающийся выделением энергии, катализируется миозином, который, как уже отмечалось, обладает ферментативной активностью.
Пусковым механизмом мышечного сокращения является повышение концентрации ионов Са в саркоплазме миоцитов, вызываемое двигательным нервным импульсом.
Во время мышечного сокращения между толстыми и тонкими нитями миофибрилл возникают поперечные мостики, или спайки.
Во время мышечного сокращения происходит скольжение тонких нитей вдоль толстых, что приводит к укорочению миофибрилл и всего мышечного волокна в целом.
Имеется много гипотез, пытающихся объяснить молекулярный механизм мышечного сокращения. Наиболее обоснованной в настоящее время является гипотеза «весельной лодки», или «гребная» гипотеза X. Хаксли. В упрощенном виде ее суть заключается в следующем.
В мышце, находящейся в состоянии покоя, толстые и тонкие нити миофибрилл друг с другом не соединены, так как участки связывания на молекулах актина закрыты молекулами тропомиозина.
Мышечное сокращение происходит под воздействием двигательного нервного импульса, представляющего собой волну повышенной мембранной проницаемости, распространяющуюся по нервному волокну.
Эта волна повышенной проницаемости передается через нервно-мышечный синапс на Т-систему саркоплазматической сети и в конечном счете достигает цистерн, содержащих ионы кальция в большой концентрации. В результате значительного повышения проницаемости стенки цистерн ионы кальция выходят из цистерн и их концентрация в саркоплазме за очень короткое время (около 3 мс) возрастает в 1000 раз. Ионы кальция, находясь в высокой концентрации, присоединяются к белку тонких нитей — тропонину — и меняют его пространственную форму (конформацию). Изменение конформации тропонина, в свою очередь, приводит к тому, что молекулы тропомиозина смещаются вдоль желобка фибриллярного актина, составляющего основу тонких нитей, и освобождают тот участок актиновых молекул, который предназначен для связывания с миозиновыми головками. В результате этого между миозином и актином (т. е. между толстыми и тонкими нитями) возникает поперечный мостик, расположенный под углом 90°. Поскольку в толстые и тонкие нити входит большое число молекул миозина и актина (около 300 в каждую), то между мышечными нитями образуется довольно большое количество поперечных мостиков, или спаек. Образование связи между актином и миозином сопровождается повышением АТФазной активности последнего, в результате чего происходит гидролиз АТФ:
АТФ + Н20 АДФ + Н3Р04 + энергия
За счет энергии, выделяющейся при расщеплении АТФ, миозиновая головка, подобно шарниру или веслу лодки, поворачивается и мостик между толстыми и тонкими нитями оказывается под углом 45°, что приводит к скольжению мышечных нитей навстречу друг другу. Совершив поворот, мостики между толстыми и тонкими нитями разрываются. АТФазная активность миозина вследствие этого резко снижается, и гидролиз АТФ прекращается. Но если двигательный нервный импульс продолжает поступать в мышцу и в саркоплазме сохраняется высокая концентрация ионов кальция, поперечные мостики вновь образуются, АТФазная активность миозина возрастает и снова происходит гидролиз новых порций АТФ, дающий энергию для поворота поперечных мостиков с последующим их разрывом. Это ведет к дальнейшему движению толстых и тонких нитей навстречу друг другу и укорочению миофибрилл и мышечного волокна.
В результате многократного образования, поворота и разрыва мостиков мышца может максимально сократиться, при этом тонкие нити наслаиваются друг на друга (иногда могут переплетаться), а толстые нити упираются в Z-пластинку. Каждый цикл сокращения (образование, поворот и разрыв мостика) требует расходования одной молекулы АТФ в качестве источника энергии. Учитывая, что во всей мышце во время ее сокращения возникает огромнейшее количество поперечных мостиков, затраты АТФ на энергообеспечение мышечной деятельности очень велики.
textarchive.ru

Leave A Comment