Фотосинтез | Молекулярная биология
Фотосинтез — это преобразование энергии света в энергию химических связей органических соединений.
Фотосинтез характерен для растений, в том числе всех водорослей, ряда прокариот, в том числе цианобактерий, некоторых одноклеточных эукариот.
В большинстве случаев при фотосинтезе в качестве побочного продукта образуется кислород (O2). Однако это не всегда так, поскольку существует несколько разных путей фотосинтеза. В случае выделения кислорода его источником является вода, от которой на нужды фотосинтеза отщепляются атомы водорода.
Фотосинтез состоит из множества реакций, в которых участвуют различные пигменты, ферменты, коферменты и др. Основными пигментами являются хлорофиллы, кроме них — каротиноиды и фикобилины.
В природе распространены два пути фотосинтеза растений: C3 и С4. У других организмов есть своя специфика реакций. Все, что объединяет эти разные процессы под термином «фотосинтез», – во всех них в общей сложности происходит преобразование энергии фотонов в химическую связь.
Выделяют две фазы фотосинтеза — световую и темновую. Первая зависит от светового излучения (hν), которое необходимо для протекания реакций. Темновая фаза является светонезависимой.
У растений фотосинтез протекает в хлоропластах. В результате всех реакций образуются первичные органические вещества, из которых потом синтезируются углеводы, аминокислоты, жирные кислоты и др. Обычно суммарную реакцию фотосинтеза пишут в отношении
6CO2 + 6H2O → C6H12O6 + 6O2
Атомы кислорода, входящие в молекулу O2, берутся не из углекислого газа, а из воды. Углекислый газ – источник углерода, что более важно. Благодаря его связыванию у растений появляется возможность синтеза органики.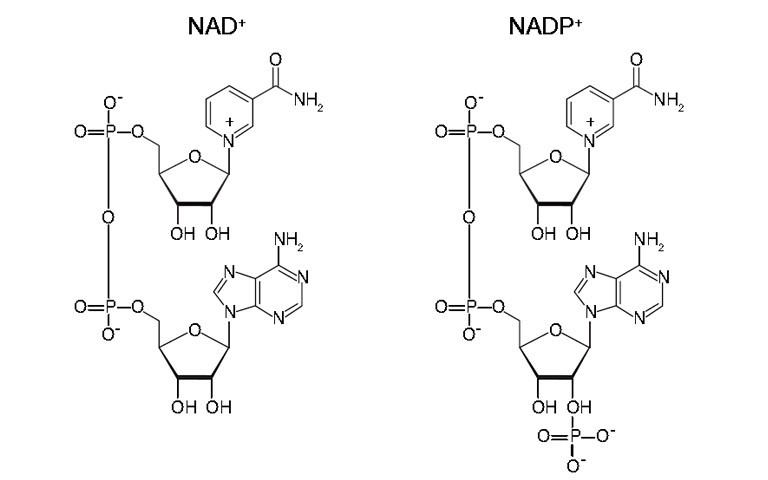
Представленная выше химическая реакция есть обобщенная и суммарная. Она далека от сути процесса. Так глюкоза не образуется из шести отдельных молекул углекислоты. Связывание CO
Для прокариот характерны свои особенности фотосинтеза. Так у бактерий главный пигмент — бактериохлорофилл, и не выделяется кислород, так как водород берется не из воды, а часто из сероводорода или других веществ. У сине-зеленых водорослей основным пигментом является хлорофилл, и при фотосинтезе выделяется кислород.
Световая фаза фотосинтеза
В световой фазе фотосинтеза происходит синтез АТФ и НАДФ·H2 за счет лучистой энергии.

Электроны в конечном итоге оказываются у кофермента НАДФ, который, заряжаясь отрицательно, притягивает к себе часть протонов и превращается в НАДФ·H2. Также накопление протонов по одну сторону тилакоидной мембраны и электронов по другую создает электрохимический градиент, потенциал которого используется ферментом АТФ-синтетазой для синтеза АТФ из АДФ и фосфорной кислоты.
Главными пигментами фотосинтеза являются различные хлорофиллы. Их молекулы улавливают излучение определенных, отчасти разных спектров света. При этом некоторые электроны молекул хлорофилла переходят на более высокий энергетический уровень. Это неустойчивое состояние, и по-идее электроны путем того же излучения должны отдать в пространство полученную из вне энергию и вернуться на прежний уровень. Однако в фотосинтезирующих клетках возбужденные электроны захватываются акцепторами и с постепенным уменьшением своей энергии передаются по цепи переносчиков.
На мембранах тилакоидов существуют два типа фотосистем, испускающих электроны при действия света.
Электроны фотосистемы I, пройдя по цепи переносчиков, восстанавливают НАДФ.
Энергия электронов, оторвавшихся от фотосистемы II, используется для синтеза АТФ. А сами электроны фотосистемы II заполняют электронные дырки фотосистемы I.
Дырки второй фотосистемы заполняются электронами, образующимися в результате
Примерное суммарное уравнение световой фазы фотосинтеза:
H2O + НАДФ + 2АДФ + 2Ф → ½O2 + НАДФ · H2 + 2АТФ
Циклический транспорт электронов
Выше описана так называемый нецикличная световая фаза фотосинтеза.
Фотофосфорилирование и окислительное фосфорилирование
Световую фазу фотосинтеза можно сравнить с этапом клеточного дыхания — окислительным фосфорилированием, которое протекает на кристах митохондрий. Там тоже происходит синтез АТФ за счет передачи электронов и протонов по цепи переносчиков. Однако в случае фотосинтеза энергия запасается в АТФ не для нужд клетки, а в основном для потребностей темновой фазы фотосинтеза. И если при дыхании первоначальным источником энергии служат органические вещества, то при фотосинтезе – солнечный свет. Синтез АТФ при фотосинтезе называется 
Темновая фаза фотосинтеза
Впервые темновую фазу фотосинтеза подробно изучили Кальвин, Бенсон, Бэссем. Открытый ими цикл реакций в последствии был назван циклом Кальвина, или C3-фотосинтезом. У определенных групп растений наблюдается видоизмененный путь фотосинтеза – C
В темновых реакциях фотосинтеза происходит фиксация CO2. Темновая фаза протекает в строме хлоропласта.
Восстановление CO2 происходит за счет энергии АТФ и восстановительной силы НАДФ·H2, образующихся в световых реакциях. Без них фиксации углерода не происходит. Поэтому хотя темновая фаза напрямую не зависит от света, но обычно также протекает на свету.
Цикл Кальвина
Первая реакция темновой фазы – присоединение CO2 (карбоксилирование) к 1,5-рибулезобифосфату (рибулезо-1,5-дифосфат) – 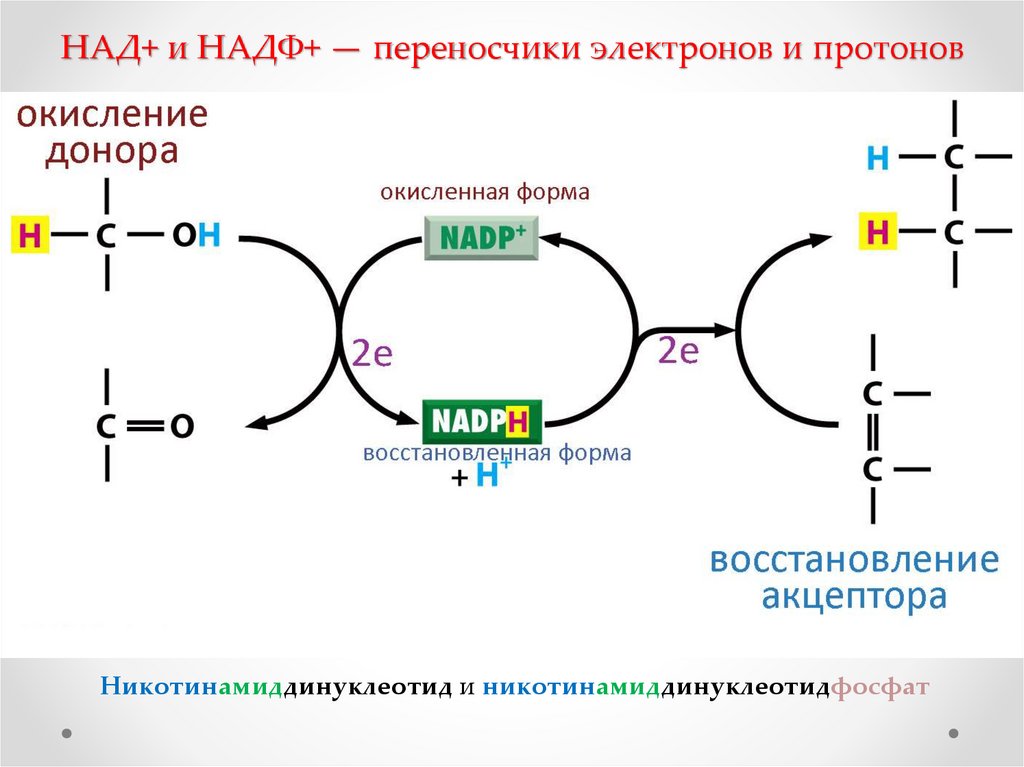 Последний представляет собой дважды фосфорилированную рибозу. Данную реакцию катализирует фермент рибулезо-1,5-дифосфаткарбоксилаза, также называемый рубиско.
Последний представляет собой дважды фосфорилированную рибозу. Данную реакцию катализирует фермент рибулезо-1,5-дифосфаткарбоксилаза, также называемый рубиско.
В результате карбоксилирования образуется неустойчивое шестиуглеродное соединение, которое в результате гидролиза распадается на две трехуглеродные молекулы фосфоглицериновой кислоты (ФГК) – первый продукт фотосинтеза. ФГК также называют фосфоглицератом.
РиБФ + CO2 + H2O → 2ФГК
ФГК содержит три атома углерода, один из которых входит в состав кислотной карбоксильной группы (-COOH):
Из ФГК образуется трехуглеродный сахар (глицеральдегидфосфат) триозофосфат (ТФ), включающий уже альдегидную группу (-CHO):
ФГК (3-кислота) → ТФ (3-сахар)
На данную реакцию затрачивается энергия АТФ и восстановительная сила НАДФ · H2. ТФ — первый углевод фотосинтеза.
После этого большая часть триозофосфата затрачивается на регенерацию рибулозобифосфата (РиБФ), который снова используется для связывания CO2.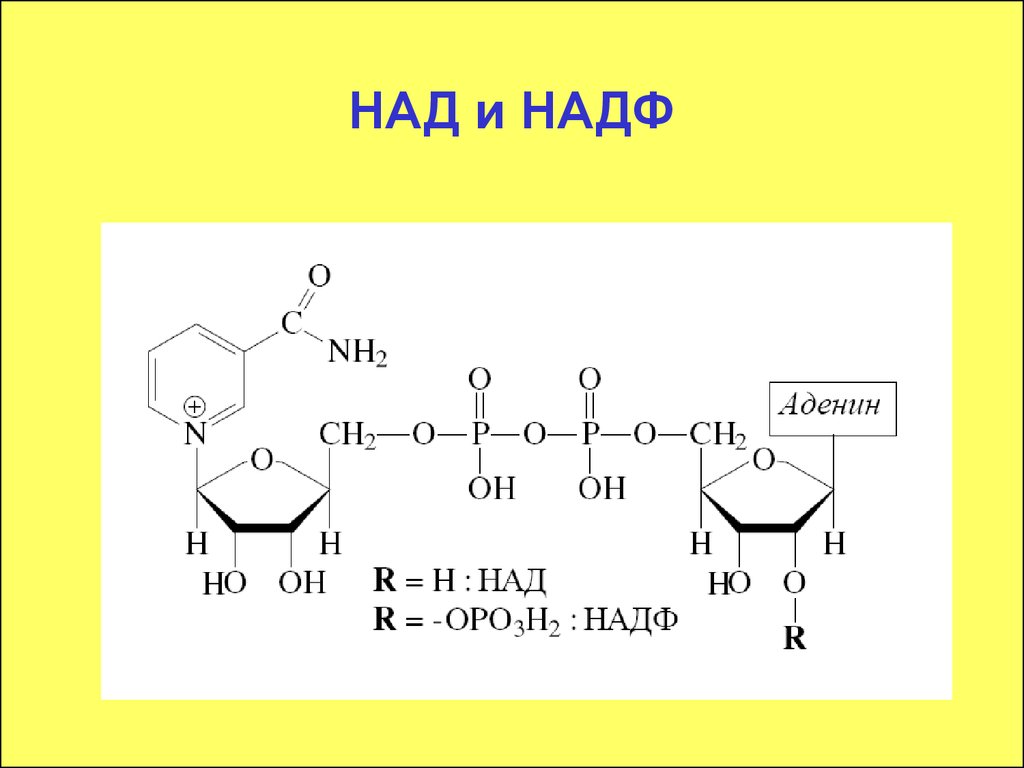 Регенерация включает в себя ряд идущих с затратой АТФ реакций, в которых участвуют сахарофосфаты с количеством атомов углерода от 3 до 7.
Регенерация включает в себя ряд идущих с затратой АТФ реакций, в которых участвуют сахарофосфаты с количеством атомов углерода от 3 до 7.
В таком круговороте РиБФ и заключается цикл Кальвина.
Из цикла Кальвина выходит меньшая часть образовавшегося в нем ТФ. В перерасчете на 6 связанных молекул углекислого газа выход составляет 2 молекулы триозофосфата. Суммарная реакция цикла с входными и выходными продуктами:
6CO2 + 6H2O → 2ТФ
При этом в связывании участвую 6 молекул РиБФ и образуется 12 молекул ФГК, которые превращаются в 12 ТФ, из которых 10 молекул остаются в цикле и преобразуются в 6 молекул РиБФ. Поскольку ТФ — это трехуглеродный сахар, а РиБФ — пятиуглеродный, то в отношении атомов углерода имеем: 10 * 3 = 6 * 5. Количество атомов углерода, обеспечивающих цикл не изменяется, весь необходимый РиБФ регенерируется. А шесть вошедших в цикл молекул углекислоты затрачиваются на образование двух выходящих из цикла молекул триозофосфата.
На цикл Кальвина в расчете на 6 связанных молекул CO2 затрачивается 18 молекул АТФ и 12 молекул НАДФ · H2, которые были синтезированы в реакциях световой фазы фотосинтеза.
Расчет ведется на две выходящие из цикла молекулы триозофосфата, так как образующаяся в последствии молекула глюкозы, включает 6 атомов углерода.
Триозофосфат (ТФ) — конечный продукт цикла Кальвина, но его сложно назвать конечным продуктом фотосинтеза, так как он почти не накапливается, а, вступая в реакции с другими веществами, превращается в глюкозу, сахарозу, крахмал, жиры, жирные кислоты, аминокислоты. Кроме ТФ важную роль играет ФГК. Однако подобные реакции происходят не только у фотосинтезирующих организмов. В этом смысле темновая фаза фотосинтеза – это то же самое, что цикл Кальвина.
Из ФГК путем ступенчатого ферментативного катализа образуется шестиуглеродный сахар фруктозо-6-фосфат, который превращается в глюкозу.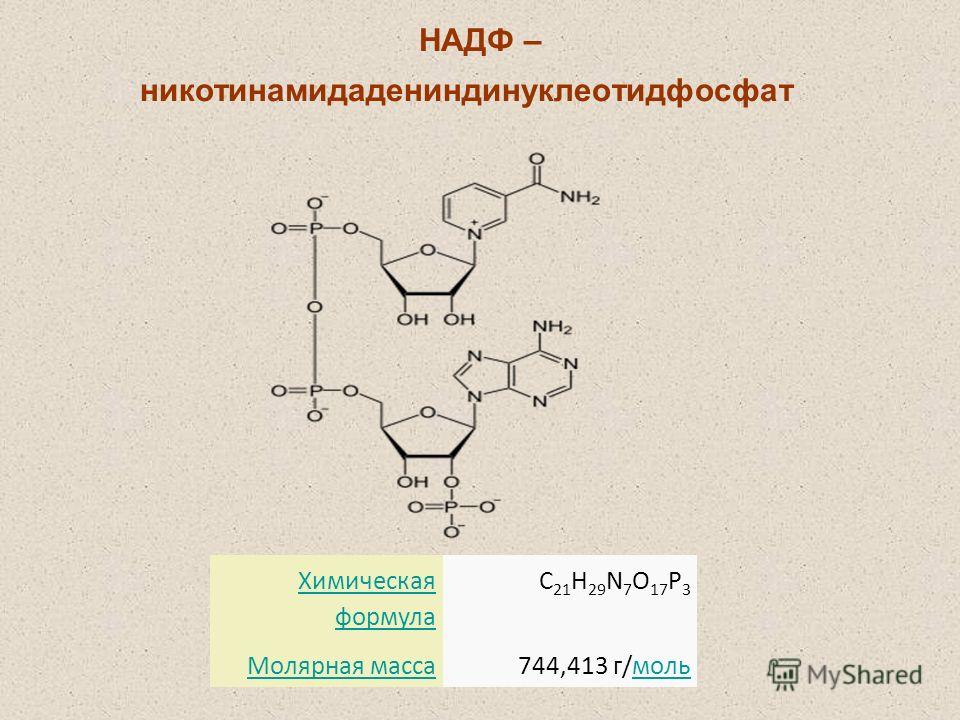 В растениях глюкоза может полимеризоваться в крахмал и целлюлозу. Синтез углеводов похож на процесс обратный гликолизу.
В растениях глюкоза может полимеризоваться в крахмал и целлюлозу. Синтез углеводов похож на процесс обратный гликолизу.
Фотодыхание
Кислород подавляет фотосинтез. Чем больше O2 в окружающей среде, тем менее эффективен процесс связывания CO2. Дело в том, что фермент рибулозобифосфат-карбоксилаза (рубиско) может реагировать не только с углекислым газом, но и кислородом. В этом случае темновые реакции несколько иные.
Содержащая пять атомов углерода молекула рибулозобифосфата реагирует уже не с CO2, а с O2. В результате чего образуются по одной молекуле фосфогликолата (C2) и фосфоглицериновой кислоты (C3), а не две ФГК как обычно.
Фосфогликолат — это фосфогликолевая кислота. От нее сразу отщепляется фосфатная группа, и она превращается в гликолевую кислоту (гликолат). Для его «утилизации» снова нужен кислород. Поэтому чем больше в атмосфере кислорода, тем больше он будет стимулировать фотодыхание и тем больше растению будет требоваться кислорода, чтобы избавиться от продуктов реакции.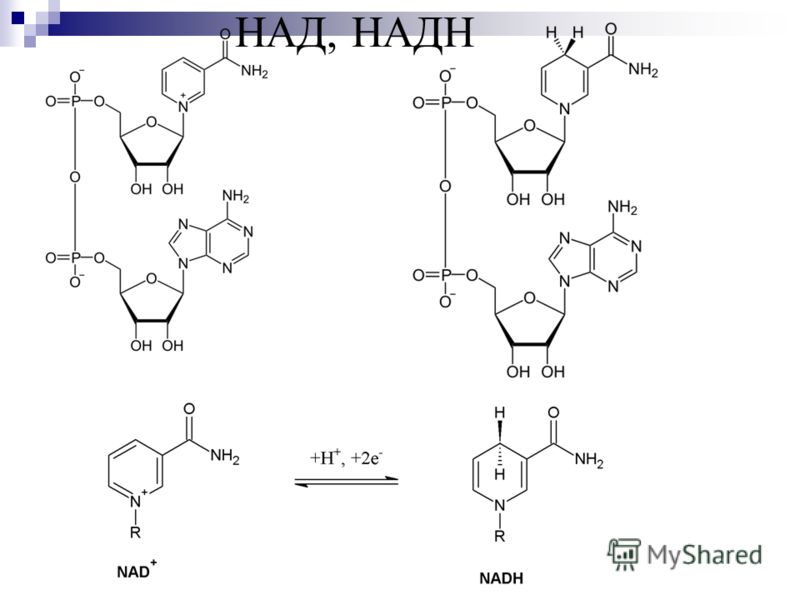
Фотодыхание — это зависимое от света потребление кислорода и выделение углекислого газа. То есть обмен газов происходит как при дыхании, но протекает в хлоропластах и зависит от светового излучения. От света фотодыхание зависит лишь потому, что рибулозобифосфат образуется только при фотосинтезе.
При фотодыхании происходит возврат атомов углерода из гликолата в цикл Кальвина в виде фосфоглицериновой кислоты (фосфоглицерата).
2 Гликолат (С2) → 2 Глиоксилат (С2) →2 Глицин (C2) — CO2 → Серин (C3) →Гидроксипируват (C3) → Глицерат (C3) → ФГК (C3)
Как видно, возврат происходит не полный, так как один атом углерода теряется при превращении двух молекул глицина в одну молекулу аминокислоты серина, при этом выделяется углекислый газ.
Кислород необходим на стадиях превращения гликолата в глиоксилат и глицина в серин.
Превращения гликолата в глиоксилат, а затем в глицин происходят в пероксисомах, синтез серина в митохондриях. Серин снова поступает в пероксисомы, где из него сначала получается гидрооксипируват, а затем глицерат. Глицерат уже поступает в хлоропласты, где из него синтезируется ФГК.
Серин снова поступает в пероксисомы, где из него сначала получается гидрооксипируват, а затем глицерат. Глицерат уже поступает в хлоропласты, где из него синтезируется ФГК.
Фотодыхание характерно в основном для растений с C3-типом фотосинтеза. Его можно считать вредным, так как энергия бесполезно тратится на превращения гликолата в ФГК. Видимо фотодыхание возникло из-за того, что древние растения были не готовы к большому количеству кислорода в атмосфере. Изначально их эволюция шла в атмосфере богатой углекислым газом, и именно он в основном захватывал реакционный центр фермента рубиско.
C
4-фотосинтез, или цикл Хэтча-СлэкаЕсли при C3-фотосинтезе первым продуктом темновой фазы является фосфоглицериновая кислота, включающая три атома углерода, то при C4-пути первыми продуктами являются кислоты, содержащие четыре атома углерода: яблочная, щавелевоуксусная, аспарагиновая.
С4-фотосинтез наблюдается у многих тропических растений, например, сахарного тростника, кукурузы.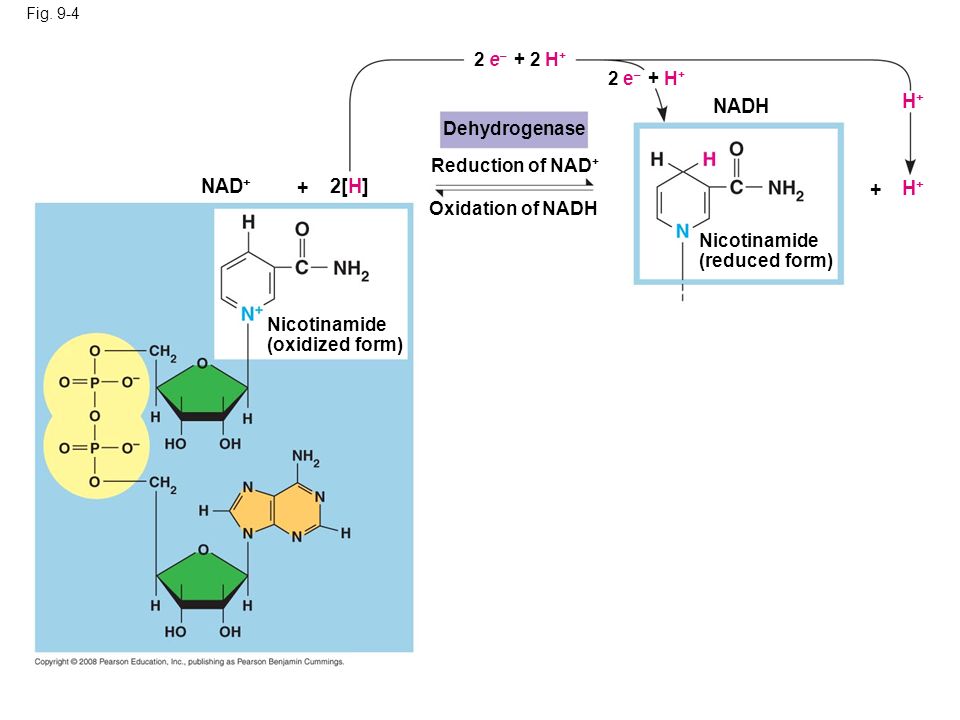
С4-растения эффективнее поглощают оксид углерода, у них почти не выражено фотодыхание.
Растения, в которых темновая фаза фотосинтеза протекает по C4-пути, имеют особое строение листа. В нем проводящие пучки окружены двойным слоем клеток. Внутренний слой — обкладка проводящего пучка. Наружный слой — клетки мезофилла. Хлоропласты клеток слоев отличаются друг от друга.
Для мезофильных хлоропласт характерны крупные граны, высокая активность фотосистем, отсутствие фермента РиБФ-карбоксилазы (рубиско) и крахмала. То есть хлоропласты этих клеток адаптированы преимущественно для световой фазы фотосинтеза.
В хлоропластах клеток проводящего пучка граны почти не развиты, зато высока концентрация РиБФ-карбоксилазы. Эти хлоропласты адаптированы для темновой фазы фотосинтеза.
Углекислый газ сначала попадает в клетки мезофилла, связывается с органическими кислотами, в таком виде транспортируется в клетки обкладки, освобождается и далее связывается также, как у C3-растений. То есть C4-путь дополняет, а не заменяет C3.
То есть C4-путь дополняет, а не заменяет C3.
В мезофилле CO2 присоединяется к фосфоенолпирувату (ФЕП) с образованием оксалоацетата (кислота), включающего четыре атома углерода:
Реакция происходит при участии фермента ФЕП-карбоксилазы, обладающего более высоким сродством к CO2, чем рубиско. К тому же ФЕП-карбоксилаза не взаимодействует с кислородом, а значит не затрачивается на фотодыхание. Таким образом, преимущество C4-фотосинтеза заключается в более эффективной фиксации углекислоты, увеличению ее концентрации в клетках обкладки и следовательно более эффективной работе РиБФ-карбоксилазы, которая почти не расходуется на фотодыхание.
Оксалоацетат превращается в 4-х углеродную дикарбоновую кислоту (малат или аспартат), которая транспортируется в хлоропласты клеток обкладки проводящих пучков. Здесь кислота декарбоксилируется (отнятие CO2), окисляется (отнятие водорода) и превращается в пируват.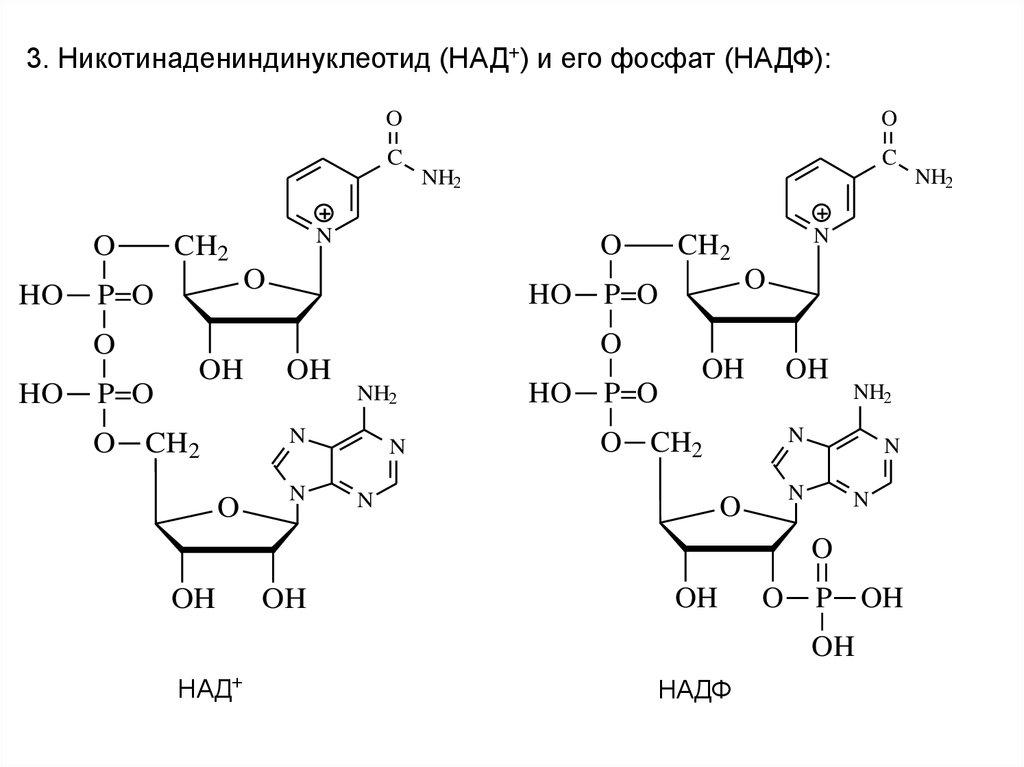 Водород восстанавливает НАДФ. Пируват возвращается в мезофилл, где из него регенерируется ФЕП с затратой АТФ.
Водород восстанавливает НАДФ. Пируват возвращается в мезофилл, где из него регенерируется ФЕП с затратой АТФ.
Оторванный CO2 в хлоропластах клеток обкладки уходит на обычный C3-путь темновой фазы фотосинтеза, т. е. в цикл Кальвина.
Фотосинтез по пути Хэтча-Слэка требует больше энергозатрат.
Считается, что C4-путь возник в эволюции позже C3 и во многом является приспособлением против фотодыхания.
АТФ, НАД+, НАДФ+, ФАД
Аденозинтрифосфорная кислота (АТФ) — универсальный источник и основной аккумулятор энергии в живых клетках. АТФ содержится во всех клетках растений и животных. Количество АТФ в среднем составляет 0,04% (от сырой массы клетки), наибольшее количество АТФ (0,2-0,5%) содержится в скелетных мышцах. В клетке молекула АТФ расходуется в течение одной минуты после ее образования. У человека количество АТФ, равное массе тела, образуется и разрушается каждые 24 часа.
АТФ – мононуклеотид, состоящий из остатков азотистого основания (аденина), рибозы и трех остатков фосфорной кислоты. Поскольку АТФ содержит не один, а три остатка фосфорной кислоты, она относится к рибонуклеозидтрифосфатам.
Поскольку АТФ содержит не один, а три остатка фосфорной кислоты, она относится к рибонуклеозидтрифосфатам.
Для большинства видов работ, происходящих в клетках, используется энергия гидролиза АТФ. При этом при отщеплении концевого остатка фосфорной кислоты АТФ переходит в АДФ (аденозиндифосфорную кислоту), при отщеплении второго остатка фосфорной кислоты – в АМФ (аденозинмонофосфорную кислоту). Выход свободной энергии при отщеплении как концевого, так и второго остатков фосфорной кислоты составляет около 30,6 кДж/моль. Отщепление третьей фосфатной группы сопровождается выделением только 13,8 кДж/моль. Связи между концевым и вторым, вторым и первым остатками фосфорной кислоты называются макроэргическими (высокоэнергетическими).
Запасы АТФ постоянно пополняются. В клетках всех организмов синтез АТФ происходит в процессе фосфорилирования, т.е. присоединения фосфорной кислоты к АДФ. Фосфорилирование происходит с разной интенсивностью при дыхании (митохондрии), гликолизе (цитоплазма), фотосинтезе (хлоропласты).
Рис. Гидролиз АТФ
АТФ является основным связующим звеном между процессами, сопровождающимися выделением и накоплением энергии, и процессами, протекающими с затратами энергии. Кроме этого, АТФ наряду с другими рибонуклеозидтрифосфатами (ГТФ, ЦТФ, УТФ) является субстратом для синтеза РНК.
Кроме АТФ есть и другие молекулы с макроэргическими связями – УТФ (уридинтрифосфорная кислота), ГТФ (гуанозинтрифосфорная кислота), ЦТФ (цитидинтрифосфорная кислота), энергия которых используются для биосинтеза белка (ГТФ), полисахаридов (УТФ), фосфолипидов (ЦТФ). Но все они образуются за счет энергии АТФ.
Помимо мононуклеотидов, важную роль в реакциях обмена веществ играют динуклеотиды (НАД+, НАДФ+, ФАД), относящиеся к группе коферментов (органические молекулы, сохраняющие связь с ферментом только в ходе реакции). НАД+ (никотинамидадениндинуклеотид), НАДФ+ (никотинамидадениндинуклеотидфосфат) – динуклеотиды, имеющие в своем составе два азотистых основания – аденин и амид никотиновой кислоты – производное витамина РР), два остатка рибозы и два остатка фосфорной кислоты (рис. .). Если АТФ – универсальный источник энергии, то НАД+ и НАДФ+ – универсальные акцепторы, а их восстановленные формы – НАДН и НАДФН – универсальные доноры восстановительных эквивалентов (двух электронов и одного протона). Входящий в состав остатка амида никотиновой кислоты атом азота четырехвалентен и несет положительный заряд (НАД+). Это азотистое основание легко присоединяет два электрона и один протон (т.е. восстанавливается) в тех реакциях, в которых при участии ферментов дегидрогеназ от субстрата отрываются два атома водорода (второй протон уходит в раствор):
.). Если АТФ – универсальный источник энергии, то НАД+ и НАДФ+ – универсальные акцепторы, а их восстановленные формы – НАДН и НАДФН – универсальные доноры восстановительных эквивалентов (двух электронов и одного протона). Входящий в состав остатка амида никотиновой кислоты атом азота четырехвалентен и несет положительный заряд (НАД+). Это азотистое основание легко присоединяет два электрона и один протон (т.е. восстанавливается) в тех реакциях, в которых при участии ферментов дегидрогеназ от субстрата отрываются два атома водорода (второй протон уходит в раствор):
Субстрат-Н2 + НАД+ субстрат + НАДН + Н+
Рис. . Структура молекулы динуклеотидов НАД+ и НАДФ+.
А – присоединение фосфатной группы к остатку рибозы в молекуле НАД. Б – присоединение двух электронов и одного протона (аниона Н-) к НАД+.
В обратных реакциях ферменты, окисляя НАДН или НАДФН, восстанавливают субстраты, присоединяя к ним атомы водорода (второй протон приходит из раствора).
ФАД – флавинадениндинуклеотид – производное витамина В2 (рибофлавина) также является кофактором дегидрогеназ, но ФАД присоединяет два протона и два электрона, восстанавливаясь до ФАДН2.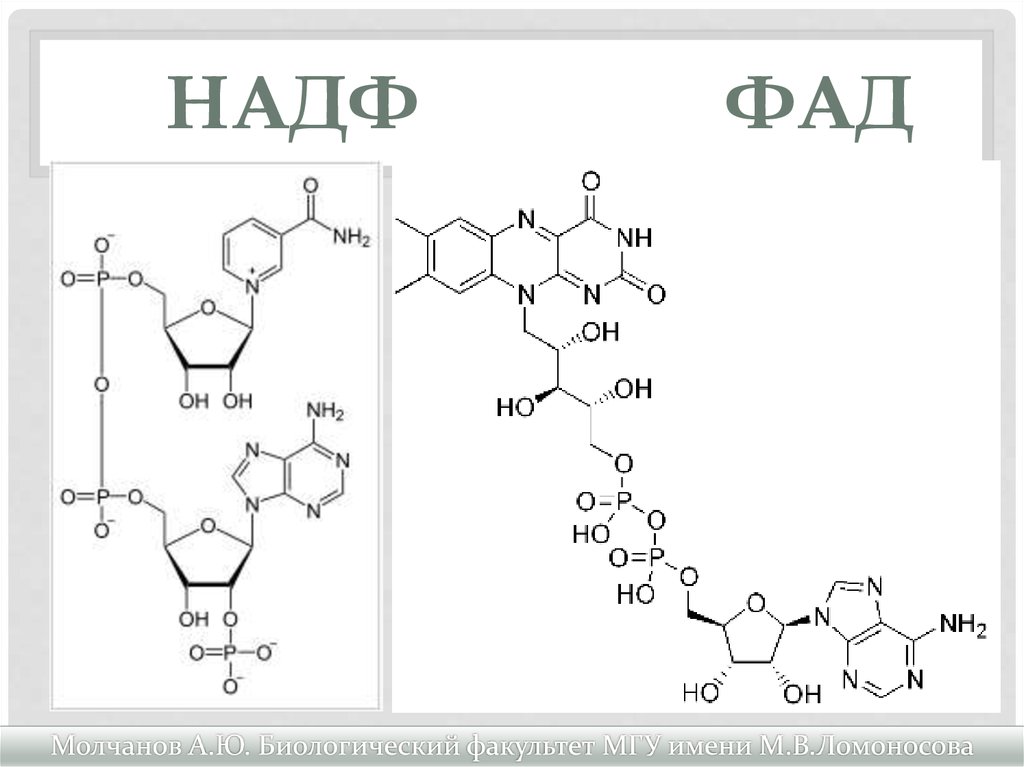
Подпишитесь на наш канал в Telegram
4.3: НАД и НАДФ — LibreTexts по биологии
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 4629
- Джон В. Кимбалл
- Университет Тафтса и Гарвард
Никотинамидадениндинуклеотид (НАД) и родственный ему никотинамидадениндинуклеотидфосфат (НАДФ) являются двумя наиболее важными коферментами в клетке. НАДФ — это просто НАД с присоединенной третьей фосфатной группой, как показано внизу рисунка.
Рисунок \(\PageIndex{1}\): НАД и НАДФ Из-за положительного заряда атома азота в никотинамидном кольце (вверху справа) окисленные формы этих важных окислительно-восстановительных реагентов часто обозначают как НАД + 9.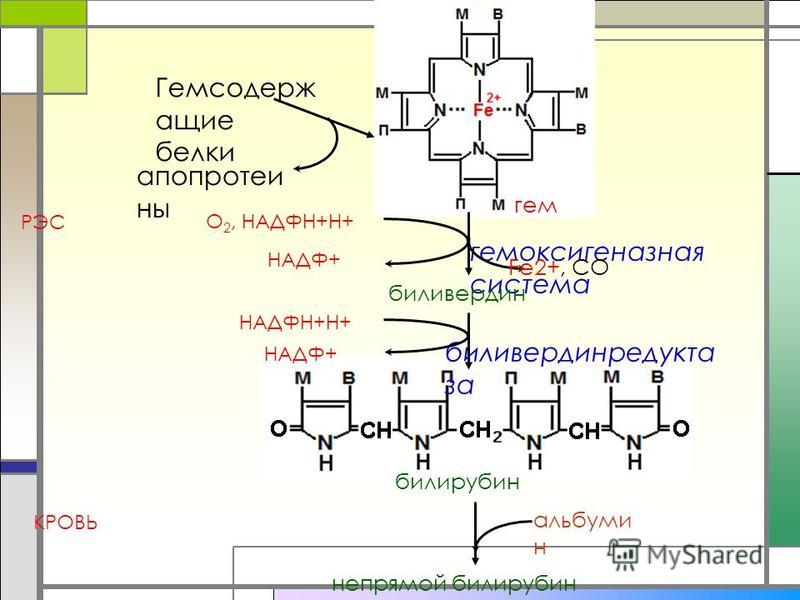 0035 и НАДФ + соответственно.
0035 и НАДФ + соответственно.
В клетках большинство процессов окисления осуществляется путем удаления атомов водорода. Оба эти кофермента играют решающую роль в этом. Каждая молекула НАД + (или НАДФ + ) может приобрести два электрона; то есть восстанавливаться на два электрона. Однако восстановление сопровождает только один протон. Другой протон, образующийся при удалении двух атомов водорода из окисляемой молекулы, высвобождается в окружающую среду. Для НАД реакция следующая: 9{+}}\]
НАД участвует во многих окислительно-восстановительных реакциях в клетках, в том числе в гликолизе и большинстве реакций в цикле лимонной кислоты клеточного дыхания.
НАДФ представляет собой восстановитель, образующийся в результате световых реакций фотосинтеза, потребляемый в цикле фотосинтеза Кальвина и используемый во многих других анаболических реакциях как у растений, так и у животных.
В условиях, существующих в нормальной клетке, атомы водорода, показанные красным цветом, диссоциируют от этих кислых веществ.
Эта страница под названием 4.3: NAD и NADP распространяется под лицензией CC BY 3.0 и была создана, изменена и/или курирована Джоном В. Кимбаллом с использованием исходного контента, который был отредактирован в соответствии со стилем и стандартами платформы LibreTexts; подробная история редактирования доступна по запросу.
- Наверх
- Была ли эта статья полезной?
- Тип изделия
- Раздел или Страница
- Автор
- Джон В. Кимбалл
- Лицензия
- СС BY
- Версия лицензии
- 3,0
- Показать оглавление
- нет
- Теги
- Никотинамидадениндинуклеотид (НАД)
- никотинамидадениндинуклеотидфосфат (НАДФ)
- источник@https://www.
 biology-pages.info/
biology-pages.info/
Содержание НАД⁺ и его роль в митохондриях
. 2015;1241:39-48.
дои: 10.1007/978-1-4939-1875-1_4.
Вэй Ли 1 , Энтони А. Сов
принадлежность
- 1 Медицинский колледж Weill Cornell, 1300 York Avenue LC216, New York, NY, 10065, USA.
- PMID: 25308486
- DOI: 10.1007/978-1-4939-1875-1_4
Вэй Ли и др.
Методы Мол Биол.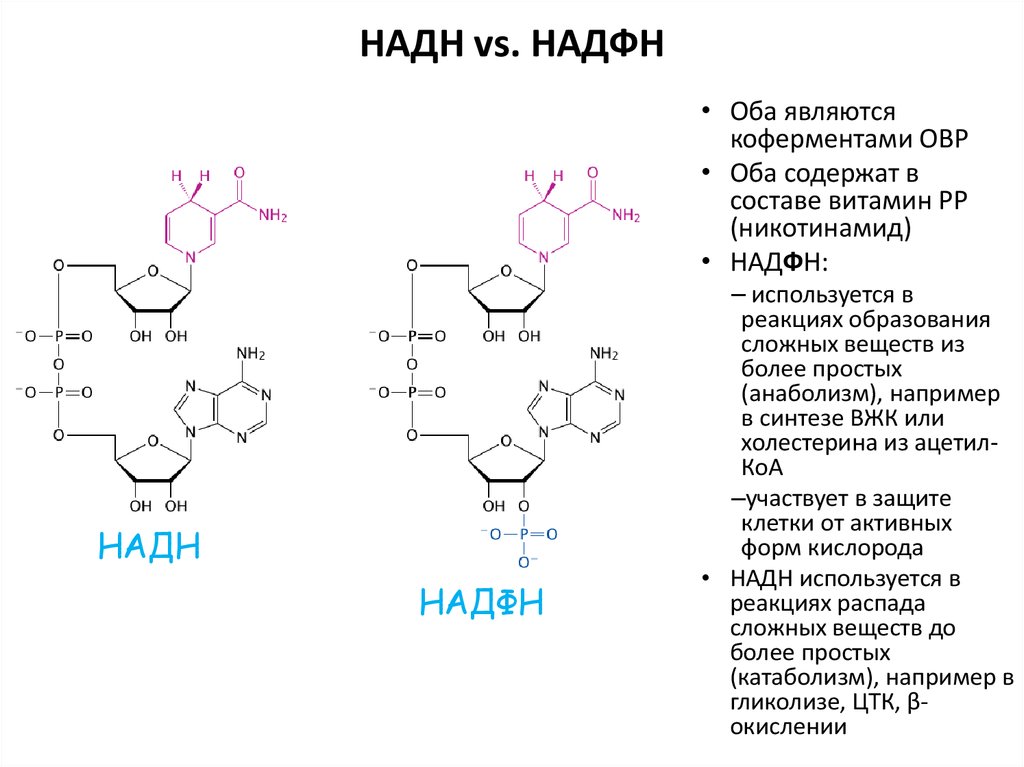 2015.
2015.
. 2015;1241:39-48.
дои: 10.1007/978-1-4939-1875-1_4.
Авторы
Вэй Ли 1 , Энтони А. Сов
принадлежность
- 1 Медицинский колледж Weill Cornell, 1300 York Avenue LC216, New York, NY, 10065, USA.
- PMID: 25308486
- DOI: 10.1007/978-1-4939-1875-1_4
Абстрактный
Никотинамидадениндинуклеотид (НАД(+)) является центральным метаболическим коферментом/косубстратом, участвующим в клеточном энергетическом обмене и выработке энергии.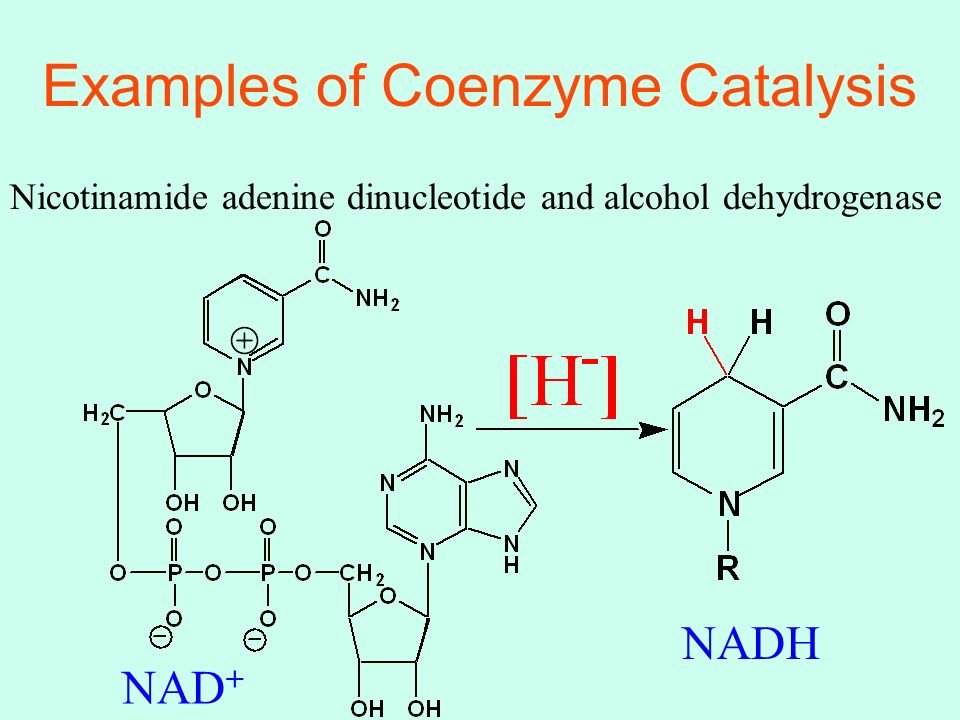 Он может быть легко восстановлен двумя электронными эквивалентами и образует форму НАДН, которая является меньшинством по отношению к НАД(+) в большинстве физиологических условий. НАД(+) играет важную роль не только в окислительно-восстановительных реакциях в клетках, но и как сигнальная молекула. Например, NAD(+) играет ключевую роль в функционировании митохондрий посредством участия в пируватдегидрогеназе, цикле трикарбоновых кислот и окислительном фосфорилировании. Он также служит субстратом для деацилаз SIRT3, SIRT4 и SIRT5, которые модифицируют посттрансляционные модификации белков лизина в митохондриальном компартменте. Недавняя работа подчеркнула биологическую значимость динамических изменений митохондриального NAD(+). Это увеличило потребность в стандартизированных и эффективных методах измерения содержания NAD(+) в этой органелле. Чтобы определить концентрации NAD(+) в клетках и, в частности, в митохондриях, мы описываем два анализа для определения NAD(+): анализ ферментативного циклирования и изотопное разведение.
Он может быть легко восстановлен двумя электронными эквивалентами и образует форму НАДН, которая является меньшинством по отношению к НАД(+) в большинстве физиологических условий. НАД(+) играет важную роль не только в окислительно-восстановительных реакциях в клетках, но и как сигнальная молекула. Например, NAD(+) играет ключевую роль в функционировании митохондрий посредством участия в пируватдегидрогеназе, цикле трикарбоновых кислот и окислительном фосфорилировании. Он также служит субстратом для деацилаз SIRT3, SIRT4 и SIRT5, которые модифицируют посттрансляционные модификации белков лизина в митохондриальном компартменте. Недавняя работа подчеркнула биологическую значимость динамических изменений митохондриального NAD(+). Это увеличило потребность в стандартизированных и эффективных методах измерения содержания NAD(+) в этой органелле. Чтобы определить концентрации NAD(+) в клетках и, в частности, в митохондриях, мы описываем два анализа для определения NAD(+): анализ ферментативного циклирования и изотопное разведение.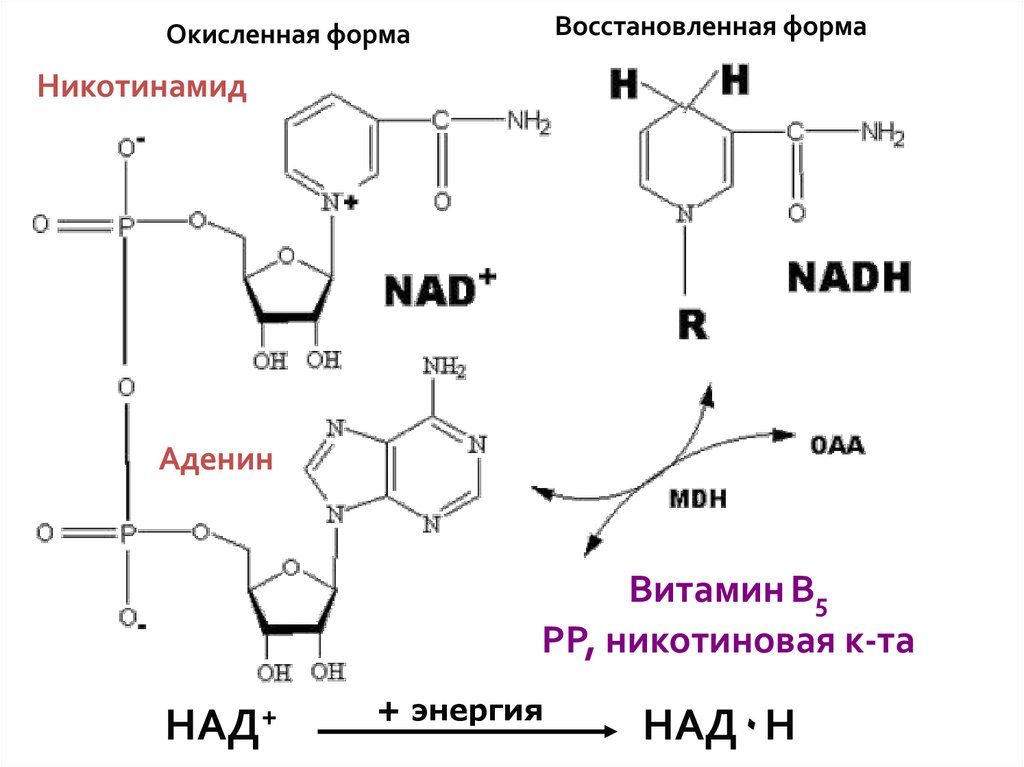 Циклический анализ содержит образец NAD(+), лактат, лактатдегидрогеназу, диафоразу и резазурин. В анализе изотопного разведения используется синтетический (18)O-NAD(+) в качестве внутреннего стандарта, а обработанные образцы фракционируют с помощью ВЭЖХ, а затем определяют концентрацию NAD(+) по (16)O- и (18)O-NAD( +) отношение пиков (664/666) в положительном режиме МС.
Циклический анализ содержит образец NAD(+), лактат, лактатдегидрогеназу, диафоразу и резазурин. В анализе изотопного разведения используется синтетический (18)O-NAD(+) в качестве внутреннего стандарта, а обработанные образцы фракционируют с помощью ВЭЖХ, а затем определяют концентрацию NAD(+) по (16)O- и (18)O-NAD( +) отношение пиков (664/666) в положительном режиме МС.
Похожие статьи
Анализы для определения клеточного и митохондриального содержания NAD + и NADH.
Ян Ю, Сов А.А. Ян Ю и др. Методы Мол Биол. 2021;2310:271-285. дои: 10.1007/978-1-0716-1433-4_15. Методы Мол Биол. 2021. PMID: 34096008
Субстраты и механизмы регуляции митохондриальных сиртуинов Sirt3 и Sirt5 человека.

Шликер К., Герц М., Папатеодору П., Каххольц Б., Беккер К.Ф., Стигборн К. Шликер С. и др. Дж Мол Биол. 2008 10 октября; 382 (3): 790-801. doi: 10.1016/j.jmb.2008.07.048. Epub 2008 25 июля. Дж Мол Биол. 2008. PMID: 18680753
Методы ферментативного анализа на основе высокоэффективной жидкостной хроматографии: активность цепи переноса электронов в митохондриях скелетных мышц человека.
Ритов В.Б., Меньшикова Е.В., Келли Д.Е. Ритов В.Б. и соавт. Анальная биохимия. 2004 1 октября; 333 (1): 27-38. doi: 10.1016/j.ab.2004.05.014. Анальная биохимия. 2004. PMID: 15351277
Ферменты, участвующие в метаболизме L-лактата у человека.
Адева М., Гонсалес-Лукан М.
 , Секо М., Донапетри К.
Адева М. и др.
Митохондрия. 2013 ноябрь;13(6):615-29. doi: 10.1016/j.mito.2013.08.011. Epub 2013 9 сентября.
Митохондрия. 2013.
PMID: 24029012
Обзор.
, Секо М., Донапетри К.
Адева М. и др.
Митохондрия. 2013 ноябрь;13(6):615-29. doi: 10.1016/j.mito.2013.08.011. Epub 2013 9 сентября.
Митохондрия. 2013.
PMID: 24029012
Обзор.Метаболизм НАД и АДФ-рибозы в митохондриях.
Долле К., Рэк Дж. Г., Циглер М. Долле С. и соавт. FEBS J. 2013 Aug; 280(15):3530-41. дои: 10.1111/февраль 12304. Epub 2013 3 июня. ФЕБС Дж. 2013. PMID: 23617329 Обзор.
Посмотреть все похожие статьи
Цитируется
Ингибирующее действие гинзенозида соединения K на липополисахарид-стимулированные воспалительные реакции в макрофагах путем регуляции сиртуина 1 и гистондеацетилазы 4.
Кан Х, Ким С, Ли Джей, Ким Б.
 Кан Х и др.
Питательные вещества. 2023 27 марта; 15 (7): 1626. дои: 10.3390/nu15071626.
Питательные вещества. 2023.
PMID: 37049466
Бесплатная статья ЧВК.
Кан Х и др.
Питательные вещества. 2023 27 марта; 15 (7): 1626. дои: 10.3390/nu15071626.
Питательные вещества. 2023.
PMID: 37049466
Бесплатная статья ЧВК.Биоактивные соединения как ингибиторы воспаления, окислительного стресса и метаболических дисфункций посредством регуляции окислительно-восстановительного баланса клеток и состояния ацетилирования гистонов.
Кан Х, Ким Б. Кан Х и др. Еда. 2023 февраль 22;12(5):925. doi: 10.3390/foods12050925. Еда. 2023. PMID: 36
6 Бесплатная статья ЧВК. Обзор.Потенциальное синергетическое добавление соединений, стимулирующих NAD+, как стратегия увеличения продолжительности жизни.
Шарма А., Чаблоз С., Лапидес Р.
 А., Ройдер Э., Эвальд С.Ю.
Шарма А. и др.
Питательные вещества. 2023 14 января; 15 (2): 445. дои: 10.3390/nu15020445.
Питательные вещества. 2023.
PMID: 36678315
Бесплатная статья ЧВК.
Обзор.
А., Ройдер Э., Эвальд С.Ю.
Шарма А. и др.
Питательные вещества. 2023 14 января; 15 (2): 445. дои: 10.3390/nu15020445.
Питательные вещества. 2023.
PMID: 36678315
Бесплатная статья ЧВК.
Обзор.Ускоренное старение нейронов in vitro ∼часы плавления ∼.
Инагаки Э., Йошимацу С., Окано Х. Инагаки Э. и др. Front Aging Neurosci. 2022 9 августа; 14:868770. doi: 10.3389/fnagi.2022.868770. Электронная коллекция 2022. Front Aging Neurosci. 2022. PMID: 36016855 Бесплатная статья ЧВК. Обзор.
Реакция на гипоксию, вызванную окислительным взрывом, связана с воспалительными профилями макрофагов, как показала ассоциация всего генома клетки.
Эмам М.


 biology-pages.info/
biology-pages.info/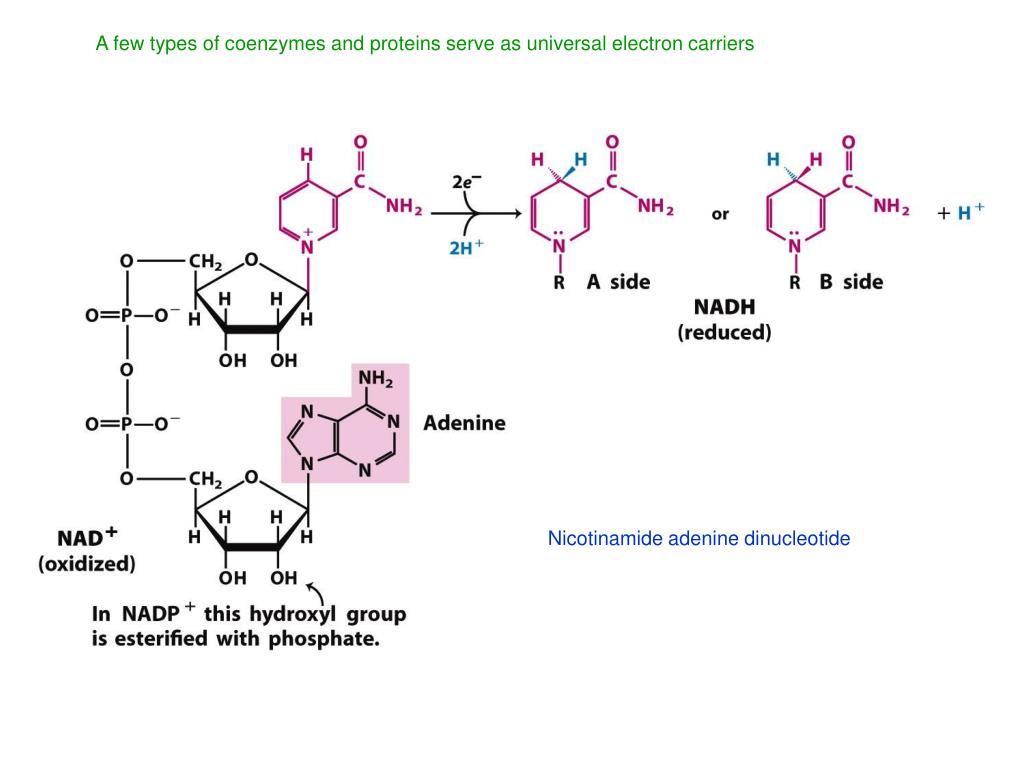
 , Секо М., Донапетри К.
Адева М. и др.
Митохондрия. 2013 ноябрь;13(6):615-29. doi: 10.1016/j.mito.2013.08.011. Epub 2013 9 сентября.
Митохондрия. 2013.
PMID: 24029012
Обзор.
, Секо М., Донапетри К.
Адева М. и др.
Митохондрия. 2013 ноябрь;13(6):615-29. doi: 10.1016/j.mito.2013.08.011. Epub 2013 9 сентября.
Митохондрия. 2013.
PMID: 24029012
Обзор.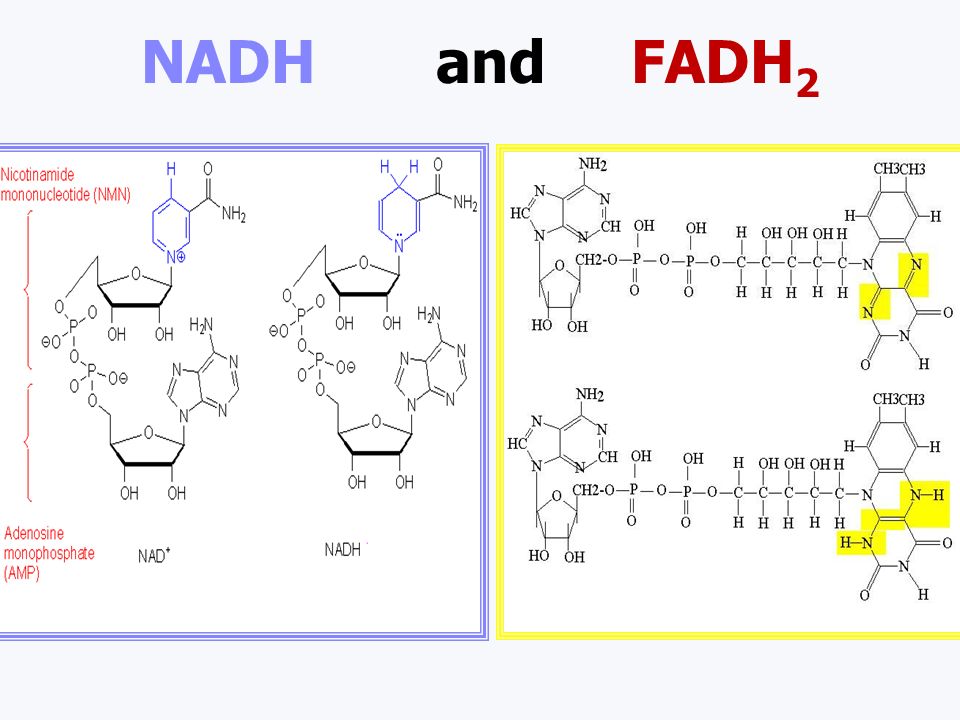 Кан Х и др.
Питательные вещества. 2023 27 марта; 15 (7): 1626. дои: 10.3390/nu15071626.
Питательные вещества. 2023.
PMID: 37049466
Бесплатная статья ЧВК.
Кан Х и др.
Питательные вещества. 2023 27 марта; 15 (7): 1626. дои: 10.3390/nu15071626.
Питательные вещества. 2023.
PMID: 37049466
Бесплатная статья ЧВК. А., Ройдер Э., Эвальд С.Ю.
Шарма А. и др.
Питательные вещества. 2023 14 января; 15 (2): 445. дои: 10.3390/nu15020445.
Питательные вещества. 2023.
PMID: 36678315
Бесплатная статья ЧВК.
Обзор.
А., Ройдер Э., Эвальд С.Ю.
Шарма А. и др.
Питательные вещества. 2023 14 января; 15 (2): 445. дои: 10.3390/nu15020445.
Питательные вещества. 2023.
PMID: 36678315
Бесплатная статья ЧВК.
Обзор.
Leave A Comment