Окисление органических веществ перманганатом калия
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Окислительно-восстановительные реакции
Окислительно-восстановительные
реакции (ОВР) — это реакции, сопровождающиеся
изменением степени окисления элементов
вследствие смещения или полного перехода
электронов от одних атомов или ионов к
другим. Окисление
– процесс отдачи электронов атомом,
молекулой или ионом; восстановление —
процесс присоединения электронов
атомом, молекулой или ионом. Окисление
и восстановление — это взаимосвязанные
процессы, протекающие одновременно.
Окислителями могут быть атомы и молекулы
некоторых неметаллов; сложные ионы и
молекулы, содержащие атомы элементов
в высшей или в одной из высших степеней
окисления MnO4—, NO3—, SO42-, Cr2O72-, ClO3—, PbO2 и др. ; положительно заряженные ионы
металлов (Fe3+, Au3+, Ag+, Sn4+, Hg2+ и др.). Типичными восстановителями
являются почти все металлы и некоторые
неметаллы (С, Н2 и др.) в свободном состоянии; отрицательно
заряженные ионы неметаллов (S2-, I— и др.), катионы, степень окисления которых
может возрасти (Sn2+, Fe2+, Cu+ и др.). Если вещество содержит элемент
в промежуточной степени окисления, то
в зависимости от условий проведения
реакции оно может быть и окислителем и
восстановителем. Например, нитрит калия
в присутствии сильного окислителя
проявляет восстановительные свойства,
окисляясь при этом до нитрата
; положительно заряженные ионы
металлов (Fe3+, Au3+, Ag+, Sn4+, Hg2+ и др.). Типичными восстановителями
являются почти все металлы и некоторые
неметаллы (С, Н2 и др.) в свободном состоянии; отрицательно
заряженные ионы неметаллов (S2-, I— и др.), катионы, степень окисления которых
может возрасти (Sn2+, Fe2+, Cu+ и др.). Если вещество содержит элемент
в промежуточной степени окисления, то
в зависимости от условий проведения
реакции оно может быть и окислителем и
восстановителем. Например, нитрит калия
в присутствии сильного окислителя
проявляет восстановительные свойства,
окисляясь при этом до нитрата
3KNO2 + K2Cr2O7 + 4H2SO4 = 3KNO3 + Cr2(SO4)3 + K2SO4 + 4H2O
При взаимодействии с восстановителем, наоборот проявляет окислительные свойства
2KNO2 + 2KI + 2H2SO4 = 2NO + I2 + 2K2SO4 + 2H2O
Такая
окислительно-восстановительная
двойственность характерна также для
Н2О2, H2SO3 (и ее солей) и т. д.
д.
Составление уравнений ОВР.
Метод электронного баланса основан на сравнении степеней окисления атомов в исходных и конечных веществах. В основе его лежит правило, что число электронов, отданных восстановителем, должно равняться числу электронов, присоединенных окислителем.
Рассмотрим данный метод на реакции взаимодействия сероводорода с перманганатом калия в кислой среде.
H2S + KMnO4 + H2SO4 = S + MnSO4 + K2SO4 + H2O
Затем определяем изменение степеней окисления атомов
H2S-2 + KMn+7O4 + H2SO4 = S0 + Mn+2SO4 + K2SO4 + H2O
Отсюда видно, что степень окисления изменяется у серы и марганца
Далее
составляем электронные уравнения, т. е.
изображаем процессы отдачи и присоединения
электронов:
е.
изображаем процессы отдачи и присоединения
электронов:
S-2 – 2e = S5
Mn+7 + 5e = Mn+2 2
Находим коэффициенты при окислителе и восстановителе, а затем при других реагирующих веществах. Из электронных уравнений видно, что надо взять 5 молекул H2S и 2 молекулы KMnO4, тогда получим 5 атомов S и 2 молекулы MnSO4. Кроме того, из сопоставления атомов в левой и правой частях уравнения найдем, что образуется также 1 молекула K2SO4 и 8 молекул воды.
Окончательное уравнение реакции будет иметь вид:
5H2S + 2KMnO4 + 3H2SO4 = 5S + 2MnSO4 + K2SO4 + 8H2O
Правильность
написания уравнения проверяется путем
подсчета атомов каждого элемента в
левой и правой частях уравнения.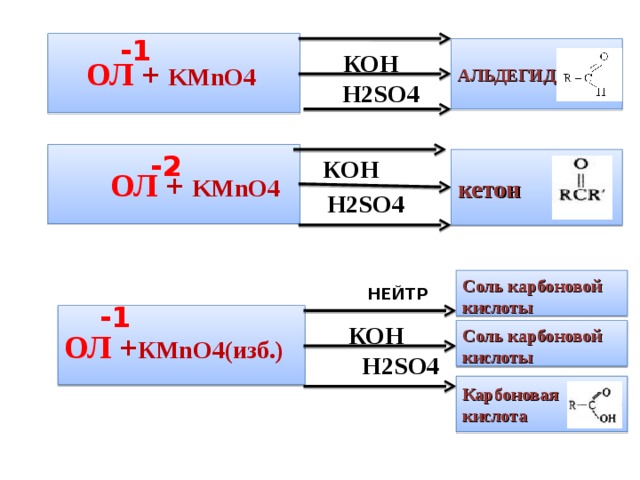
Лабораторная работа. Окислительно-восстановительные реакции Опыт 1. Окислительные свойства kMnO4 в различных средах.
В три конические колбы поместить по 3 капли раствора KMnO4. Затем в первую добавить 2 капли раствора 2 н. H2SO4, во вторую — 2 капли дистиллированной воды, в третью -2 капли раствора NaOH, после чего добавлять по каплям в каждую пробирку раствор Na2SO3 до изменения цвета раствора. Как ведет себя KMnO4 в кислой, нейтральной и щелочной среде ?
KMnO4 + Na2SO3 + H2SO4 MnSO4 + Na2SO4 + K2SO4 + H2O
KMnO4 + Na2SO3 + H2O MnO2 + Na2SO4 + KOH
KMnO4 + Na2SO3 + NaOH Na2MnO4 + К2SO4 + H2O
Определить
степень окисления для всех элементов,
расставить коэффициенты в уравнениях
реакций.
Опыт 2. Окислительные свойства дихромата калия.
Налейте в две пробирки по 3-4 капли раствора K2Cr2O7, добавьте в одну из пробирок 3-4 капли 2 н. раствора H2SO4, в другую — 3-4 капли 2 н. раствора щелочи. Обратите внимание на изменение цвета раствора во второй пробирке. Добавьте во все пробирки сульфита натрия. Дайте объяснения наблюдаемым явлениям.
К2Cr2O7+ H2SO4 + Na2SO3Cr2 (SO4) 3 + К2SO4+ Na2SO4+ H2O
Определите
степень окисления для всех элементов,
расставьте коэффициенты в уравнениях
реакций.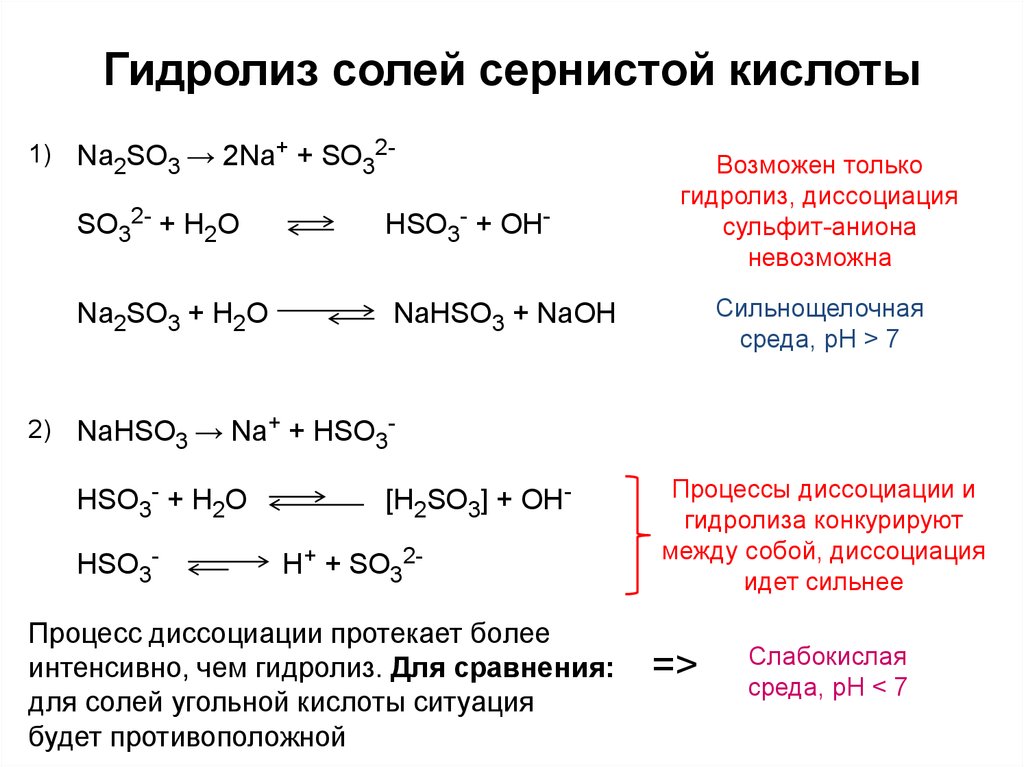
Опыт 3.Восстановление дихромата калия.
В пробирку налить 5-6 капель раствора дихромата калия, добавить 2-3капли серной кислоты и внести несколько кристалликов сульфида калия. Встряхнуть содержимое пробирки. Наблюдать изменение окраски.
Опыт 4. Окислительно–восстановительные свойства соединений железа (III)
В пробирку налить 4-5 капель раствора KMnO4 и 1-2 капли H2SO4 по каплям добавить раствор сульфата железа (II) до обесцвечивания раствора.
В
пробирку налить 4-5 капель раствора
хлорида железа и 1-2 капли раствора иодида
калия. Отметить изменение окраски
раствора. В пробирку с 7-8 каплями крахмала
внести 1-2 капли полученного раствора.
Определить степень окисления для всех
элементов, расставить коэффициенты в
уравнениях реакций.
KMnO4 + FeSO4 + H2SO4 MnSO4 + Fe2 (SO4 ) 3 + K2SO4 + H2O
FeCl3 +KI FeCl2+KCl+I2
Опыт 5. Самоокисление и самовосстановление (диспропорционирование) сульфита натрия.
В
две цилиндрические пробирки поместить
по 2-3 кристаллика Na2SO3.
Одну пробирку оставить в качестве
контрольной. Вторую закрепить в штативе
и нагревать в течение 5-6 мин. Дать пробирке
остыть. В обе пробирки внести по 2-3 мл
дистиллированной воды, размешать
стеклянными палочками до растворения
солей, находящихся в пробирках. Добавить
в каждую пробирку по 2-3 мл раствора CuSO4.
Отметить окраску осадков в пробирках.
Как объяснить различие окраски? Черный
осадок, полученный во второй пробирке,
представляет собой сульфид меди. Какой
продукт прокаливания сульфита натрия
дал с сульфатом меди этот осадок? Написать
уравнение реакции разложения сульфита
натрия, учитывая, что вторым продуктом
прокаливания является сульфит натрия.
Добавить
в каждую пробирку по 2-3 мл раствора CuSO4.
Отметить окраску осадков в пробирках.
Как объяснить различие окраски? Черный
осадок, полученный во второй пробирке,
представляет собой сульфид меди. Какой
продукт прокаливания сульфита натрия
дал с сульфатом меди этот осадок? Написать
уравнение реакции разложения сульфита
натрия, учитывая, что вторым продуктом
прокаливания является сульфит натрия.
Na2SO3 + H2O +CuSO4 H2SO4+ Cu2O + NaOH
Определить степень окисления для всех элементов, расставить коэффициенты в уравнениях реакций.
Опыт 6. Окислительные свойства пероксида водорода.
В
пробирку с 5-6 каплями раствора KI прибавить 3-4 капли 2 н H2SO4 и затем по каплям прибавлять раствор H2O2 до появления желтой окраски. Для
обнаружения в растворе йода внести в
пробирку несколько капель хлороформа
или бензола. Составьте уравнение реакции.
Для
обнаружения в растворе йода внести в
пробирку несколько капель хлороформа
или бензола. Составьте уравнение реакции.
KI + H2O2 + H2SO4I2 + H2O + K2SO4
Определить степень окисления для всех элементов, расставить коэффициенты в уравнениях реакций.
Опыт 7. Восстановительные свойства пероксида водорода.
В
пробирку с 5-6 каплями KMnO4 прибавить 3-4 капли 2 н H2SO4,
5-6 капель пероксида водорода и подогреть.
Что происходит? Составить уравнение
реакции, учитывая, что пероксид водорода
окисляется до кислорода.
KMnO4 + H2O2 + H2SO4 MnSO4 + O2 + K2SO4 + H2O
Определить степень окисления для всех элементов, расставить коэффициенты в уравнениях реакций.
Опыт 8. Окисление меди азотной кислотой.
В пробирку поместить кусочек медной проволоки и прибавить 5-6 капель 0,2 н HNO3. Отметить выделение газа, растворение меди и изменение цвета раствора. Составить электронные уравнения реакции, указав окислитель и восстановитель. Определить степень окисления для всех элементов, расставить коэффициенты в уравнениях реакций.
Cu + HNO3 Cu(NO3)2 + NO + H2O
Контрольные вопросы
1. Какие из
следующих реакций являются
окислительно-восстановительными:
Какие из
следующих реакций являются
окислительно-восстановительными:
a) Na2CO3 + SiO2 = Na2SiO3 + CO2 б) Fe2O3 + CO = 2FeO + CO2
в) K2Cr2O7 + 2KOH = 2K2CrO4 + H2O
2. Определить окислитель и восстановитель и подобрать коэффициенты в следующих реакциях окисления-восстановления:
a) Na2SO3 + I2 + H2O = Na2SO4 + HI б) S + HNO3 = H2SO4 + NO
3. Степень
окисления +2 в соединениях имеют металлы:
Cu,
Al, Zn,
Sn,
Pb,
Cr, Fe,
Mn
Степень
окисления +2 в соединениях имеют металлы:
Cu,
Al, Zn,
Sn,
Pb,
Cr, Fe,
Mn
4.Степень окисления +3 в соединениях имеют металлы: Cu, Al, Zn, Sn, Pb, Cr, Fe, Mn
5.Степень окисления +1 в соединениях имеют металлы: Cu, Al, Zn, Sn, Pb, Cr, Fe, Mn, Na, Ca, Ag
Какова степень окисления Mn в $KMn{{O}_{4}}$ и S в $N{{a}_{2}}{{S}_{2}}{{O}_ {3}}$?
Last updated date: 10th Mar 2023
•
Total views: 270k
•
Views today: 2.52k
Answer
Verified
270k+ views
Hint: Oxidation number or oxidation state is заряд, приобретаемый атомом элемента, когда он теряет или приобретает электроны при переходе из свободного состояния в связанное состояние с атомами других элементов. Он может быть положительным, отрицательным или нулевым.
Полный ответ:
> Степень окисления щелочных металлов (например, Na, K, Li и т. д.) всегда принимается равной +1.
д.) всегда принимается равной +1.
> Степень окисления кислорода равна -2 во всех его соединениях, за некоторыми исключениями. Степень окисления O в пероксидах (например, $N{{a}_{2}}{{O}_{2}}$, ${{H}_{2}}{{O}_{2}}$ ), супероксид (например, $K{{O}_{2}}$) и $O{{F}_{2}}$ равны -1, $-\dfrac{1}{2}$ и +2, соответственно.
Степень окисления Mn в перманганате калия $KMn{{O}_{4}}$ рассчитывается следующим образом:
Пусть степень окисления Mn равна ‘’. Окисление К равно +1, а О равно -2. $KMn{{O}_{4}}$ — нейтральное соединение, поэтому суммарный заряд на нем принимается равным нулю.
1(+1)+x+4(-2)=0
1+x-8=0
x=7
Следовательно, степень окисления Mn в +7.
Степень окисления S в тиосульфате натрия, $N{{a}_{2}}{{S}_{2}}{{O}_{3}}$ можно рассчитать как:
Для расчета степени окисления S in $N{{a}_{2}}{{S}_{2}}{{O}_{3}}$, мы должны сначала взглянуть на его структуру.
Имеет два атома серы в разных степенях окисления. Так как сера ${{S}_{2}}$ связана с серой ${{S}_{1}}$ координационной двойной связью. Известно, что ${{S}_{1}}$ отдает свою электронную пару ${{S}_{2}}$. Следовательно, степень окисления ${{S}_{2}}$ равна -2.
Так как сера ${{S}_{2}}$ связана с серой ${{S}_{1}}$ координационной двойной связью. Известно, что ${{S}_{1}}$ отдает свою электронную пару ${{S}_{2}}$. Следовательно, степень окисления ${{S}_{2}}$ равна -2.
Пусть теперь степень окисления серы ${{S}_{1}}$ равна ‘$x$’. Оба атома Na имеют степень окисления +1, а все три атома O находятся в степени окисления -2. Общий заряд соединения равен 0. Таким образом, степень окисления другого атома серы можно рассчитать как:
2(+1)+x+1(-2)+3(-2)=0
2+x-2-6=0
x-6=0
x=6
Следовательно, степень окисления S в $N{{a}_{2}}{{S}_{2}}{{O}_{3}}$ это +6.
Следовательно, степень окисления Mn в $KMn{{O}_{4}}$ равна +7, а S в $N{{a}_{2}}{{S}_{2} {{O}_{3}}$ равно +6.
Примечание: Обычно мы допускаем ошибку при расчете степени окисления S в $N{{a}_{2}}{{S}_{2}}{{O}_{3}} $. Мы можем просто вычислить его равным +2, как показано ниже, что неверно.
2+2x+3(-2)=0
2x-4=0
x=2
Два атома серы находятся в разных степенях окисления в $N{{a}_{2}}{{S}_ {2}}{{O}_{3}}$.
Недавно обновленные страницы
В Индии по случаю бракосочетания фейерверк 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть организованы 12 класса химии JEE_Main
Что из следующего имеет самый высокий электродный потенциал Химический класс 12 JEE_Main
Что из перечисленного ниже является истинным пероксидом A rmSrmOrm2 Химический класс 12 JEE_Main
Какой элемент обладает наибольшим атомным радиусом А 11 класс химии JEE_Main
Фосфин получают из следующей руды Кальций 12 класс химии JEE_Main
В Индии по случаю бракосочетания фейерверки 12 класса химии JEE_Main
Щелочноземельные металлы Ba Sr Ca и Mg могут быть расположены химический класс 12 JEE_Main
Что из следующего имеет самый высокий электродный потенциал химический класс 12 JEE_Main
Что из следующего является истинным пероксидом A rmSrmOrm2 химический класс 12 JEE_Main
Этот элемент обладает самой большой атомной радиусом A Cemising 11 Chemistry Jee_main
Фосфин получен из следующей руды A -Calcium Class 12 Chemistry Jee_main
Трендовые сомнения
Состояния окисления.

- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 131419
Необходимое обучение | Необходимые СИЗ |
|---|---|
Основы безопасности лаборатории UC | Лабораторный халат, защитные очки, нитриловые перчатки |
Оборудование | Химикаты |
Четыре стакана по 50 мл | 60 мл 0,01 М KMnO 4 |
Белый лист бумаги | 4 мл 3M H 2 SO 4 |
60 мл 0,02 М NaHSO 3 | |
6 мл 2М NaOH | |
Процедура:
- Поместите по 15 мл 0,01 М раствора KMnO 4 в каждый из четырех стаканов емкостью 50 мл, обозначенных буквами A, B, C и D.
 Поместите стаканы на белый лист бумаги для лучшей видимости.
Поместите стаканы на белый лист бумаги для лучшей видимости. - Отложите стакан D в качестве эталона; это степень окисления +7 Mn (фиолетовый)
- В стакан A добавьте 4 мл 3M H 2 SO 4 (кислотная среда). При перемешивании медленно добавьте ~32 мл 0,02 М NaHSO 3 . Обратите внимание на переход от фиолетового к бесцветному. Это +2 состояние Mn .
2MnO4 — (aq) + H + (aq) + 5HSO 3 — (aq) ↔ 2Mn 2+ (aq) + 5SO 4 2- (водн.) + 3H 2 O (л)
4) В химический стакан B добавьте 6 мл 2M NaOH (основное состояние). При перемешивании медленно добавьте ~8 мл 0,02 М NaHSO 3 . Обратите внимание на изменение цвета с фиолетового на зеленый. Это +6 состояние Mn.
2MnO 4 — (aq) + 3OH — (aq) + HSO 3 — (aq) ↔ 2MnO 4 2- (aq) + SO 4 2- (водн. ) + 2H 2 O (л)
) + 2H 2 O (л)
5) При перемешивании медленно добавьте ~20 мл 0,02 М NaHSO 3 в химический стакан C (нейтральное состояние). Обратите внимание на образование коричневого осадка, указывающего на состояние +4 Mn.
OH — + 2MNO 4 — (AQ) + 3HSO 3 — (AQ) ↔ 2MNO 2 (AQ) ↔ 2MNO 2 (AQ) ↔ 2MNO 2 (AQ) ↔ 2MNO 2 (AQ) 9 2 2 Опасности: Перманганат калия является сильным окислителем, поэтому держите его подальше от восстановителей. KMnO 4 также окрашивает кожу. Серная кислота и гидроксид натрия могут вызвать сильные ожоги. При попадании на кожу промыть большим количеством воды. СОП: Коррозионное вещество – гидроксид натрия, серная кислота, Окислитель – перманганат калия Утилизация (на складе) Цель состоит в том, чтобы преобразовать все соединения марганца в Mn(II) и выбросить его в раковину.. 29017. 0 (AQ). водный) + 2H 2 O (л) 

 Поместите стаканы на белый лист бумаги для лучшей видимости.
Поместите стаканы на белый лист бумаги для лучшей видимости.
Leave A Comment