Фазовые переходы • Джеймс Трефил, энциклопедия «Двести законов мироздания»
Чтобы вещество перешло из твердого состояния в жидкое (плавление или таяние), из жидкого в газообразное (кипение или испарение) или из твердого в газообразное (возгонка или сублимация), требуется поступление энергии извне. При обратных процессах (таких, как конденсация или кристаллизация) вещество, напротив, отдает энергию.
В обычных условиях любое вещество пребывает в одном из трех состояний — твердом, жидком или газообразном (см. Агрегатные состояния вещества). Каждому из этих условий соответствует своя структура связей между молекулами и/или атомами, характеризующаяся определенной энергией связи между ними. Для изменения этой структуры нужен либо приток тепловой энергии извне (например, при плавлении твердого вещества), либо отток энергии вовне (например, при кристаллизации).
Взяв, для начала, твердое вещество, мы понимаем умозрительно, что в нем молекулы/атомы связаны в некую жесткую кристаллическую или аморфную структуру, — при незначительном нагреве они лишь начинают «трястись» вокруг своей фиксированной позиции (чем выше температура, тем больше амплитуда колебаний). При дальнейшем нагревании вещества молекулы расшатываются всё сильнее, пока, наконец, не срываются с «насиженного» места и не отправляются в «свободное плавание». Это и есть плавление или таяние твердого вещества в жидкость. Поступление же энергии, необходимой для таяния вещества, называют теплотой плавления.
При дальнейшем нагревании вещества молекулы расшатываются всё сильнее, пока, наконец, не срываются с «насиженного» места и не отправляются в «свободное плавание». Это и есть плавление или таяние твердого вещества в жидкость. Поступление же энергии, необходимой для таяния вещества, называют теплотой плавления.
График изменения температуры твердого вещества при переходе им точки плавления сам по себе весьма интересен. До точки плавления по мере нагревания атомы/молекулы раскачиваются вокруг своего фиксированного положения всё сильнее, и поступление каждой дополнительной порции тепловой энергии приводит к повышению температуры твердого тела. Однако по достижении твердым веществом температуры плавления, оно на какое-то время так и остается при этой температуре, несмотря на продолжающийся приток тепла, пока в нем не накопится достаточное количество тепловой энергии для разрыва жестких межмолекулярных связей. То есть, в процессе фазового перехода вещества из твердого состояния в жидкое энергия поглощается им без повышения температуры, поскольку вся она уходит на разрыв межмолекулярных связей.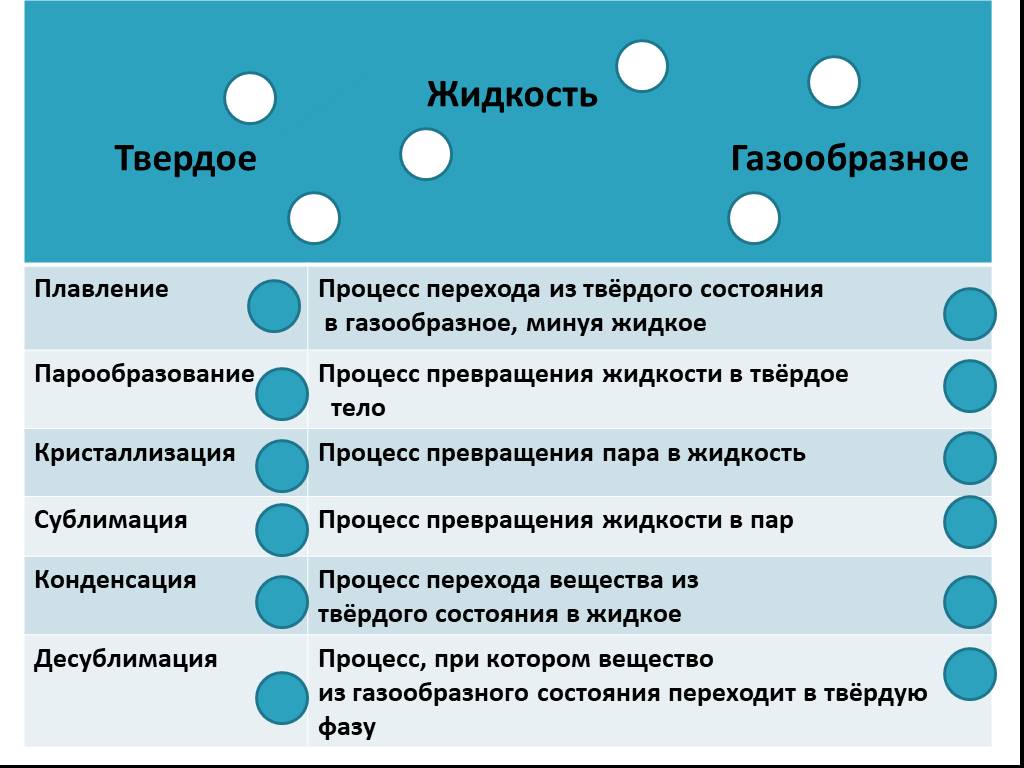 Вот почему кубик льда в коктейле даже в самую жару остается ледяным по температуре, пока не растает весь. При этом, тая, кубик льда отбирает тепло у окружающего его коктейля (и тем самым охлаждает его до приятной температуры), а сам набирается энергии, которая требуется ему для разрыва межмолекулярных связей и окончательного саморазрушения.
Вот почему кубик льда в коктейле даже в самую жару остается ледяным по температуре, пока не растает весь. При этом, тая, кубик льда отбирает тепло у окружающего его коктейля (и тем самым охлаждает его до приятной температуры), а сам набирается энергии, которая требуется ему для разрыва межмолекулярных связей и окончательного саморазрушения.
Количество теплоты, необходимое для плавления или испарения единицы объема твердого вещества или жидкости, называется, соответственно, скрытой теплотой плавления или скрытой теплотой испарения. И величины здесь фигурируют порой немалые. Например, для нагревания 1 кг воды от 0°С до 100°С требуется «всего» 420 000 джоулей (Дж) тепловой энергии, а для того, чтобы обратить этот килограмм воды в 1 кг пара с температурой, равной тем же 100°С, — целых 2 260 000 Дж энергии.
После того, как твердая масса полностью превратилась в жидкость, дальнейшее поступление тепла повлечет вновь за собой повышение температуры вещества. В жидком состоянии молекулы вещества по-прежнему находятся в близком контакте, но жесткие межмолекулярные связи между ними разорваны, и силы взаимодействия, удерживающие молекулы вместе, на несколько порядков слабее, чем в твердом теле, поэтому молекулы начинают достаточно свободно перемещаться друг относительно друга.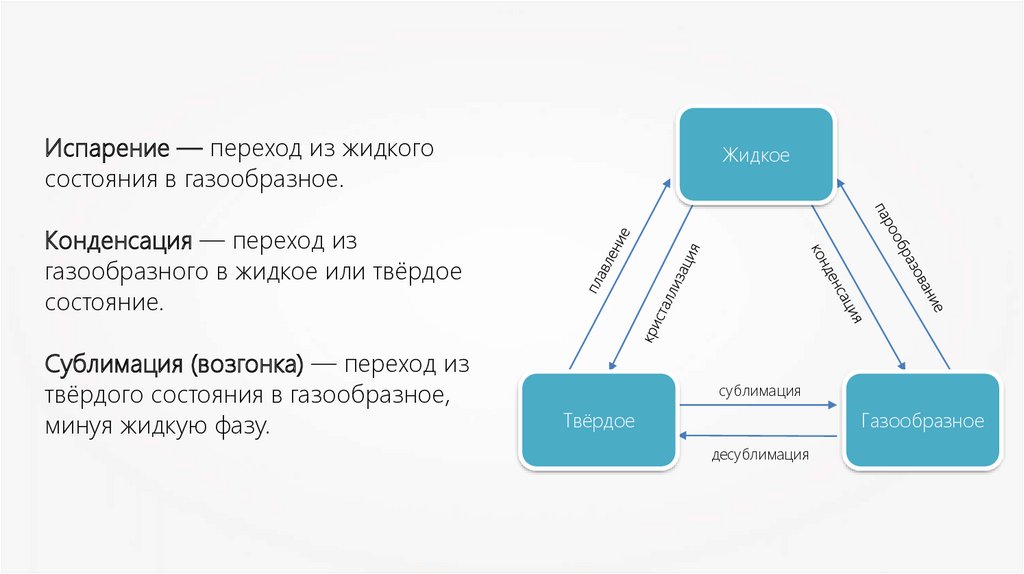 Дальнейшее поступление тепловой энергии доводит жидкость до фазы кипения, и начинается активное испарение или парообразование.
Дальнейшее поступление тепловой энергии доводит жидкость до фазы кипения, и начинается активное испарение или парообразование.
И, опять же, как было описано в случае таяния или плавления, на какое-то время вся дополнительно поступающая энергия уходит на разрыв жидкостных связей между молекулами и высвобождение их в газообразное состояние (при неизменной температуре кипения). Энергия, затрачиваемая на разрыв этих, казалось бы, некрепких связей, — т. н. скрытая теплота парообразования — также требуется немалая (см. пример выше).
Все те же процессы при оттоке энергии (остужении) вещества происходят в обратном порядке. Сначала газ остывает с понижением температуры, и так происходит, пока он не достигнет точки конденсации — температуры, при которой начинается сжижение, — и она в точности равна температуре испарения (кипения) соответствующей жидкости. При конденсации, по мере того, как силы взаимного притяжения между молекулами начинают брать верх над энергией теплового движения, газ начинает превращаться в жидкость — «конденсироваться». При этом выделяется так называемая удельная теплота конденсации — она в точности равна скрытой удельной теплоте испарения, о которой уже говорилось. То есть, сколько энергии вы потратили на испарение определенной массы жидкости, ровно столько энергии пар и отдаст в виде тепла при конденсации обратно в жидкость.
При этом выделяется так называемая удельная теплота конденсации — она в точности равна скрытой удельной теплоте испарения, о которой уже говорилось. То есть, сколько энергии вы потратили на испарение определенной массы жидкости, ровно столько энергии пар и отдаст в виде тепла при конденсации обратно в жидкость.
То, что количество теплоты, выделяемое при конденсации, весьма высоко, — факт легко проверяемый: достаточно поднести ладонь к носику кипящего чайника. Помимо жара от пара, как такового, ваша кожа пострадает еще и от теплоты, выделившейся в результате его конденсации в жидкую воду.
При дальнейшем остывании жидкости до точки замерзания (температура которой равна точке таяния), еще раз начнется процесс отдачи тепловой энергии вовне без понижения температуры самого вещества. Этот процесс называется кристаллизацией, и при нем выделяется ровно столько же тепловой энергии, сколько отбирается из окружающей среды при плавлении (переходе вещества из твердой фазы в жидкую).
Есть и еще один тип фазового перехода — из твердого состояния вещества непосредственно в газообразное (минуя жидкость). Такое фазовое превращение называется возгонкой, или сублимацией. Самый бытовой пример: вывешенное сушиться на мороз сырое белье. Вода в нем сначала кристаллизуется в лед, а затем — под воздействием прямых солнечных лучей — микроскопические кристаллики льда попросту испаряются, минуя жидкую фазу. Другой пример: на рок-концертах «сухой лед» (замороженная двуокись углерода CO2) используется для устройства дымовой завесы — она испаряется прямо в воздух, окутывая выступающих музыкантов и также минуя жидкую фазу. Соответственно, на преобразование твердого вещества непосредственно в газ затрачивается энергия сублимации.
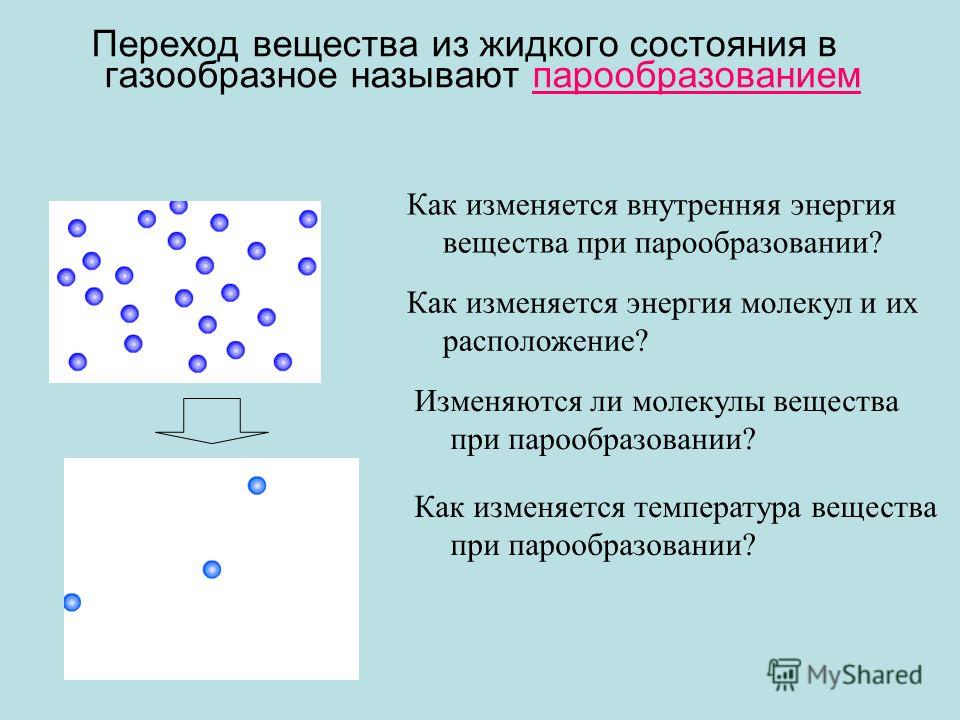
Как называется переход их жидкого состояния в газообразное?
Прочее › Чем отличается › Чем отличается газообразное состояние вещества от твердого и жидкого?
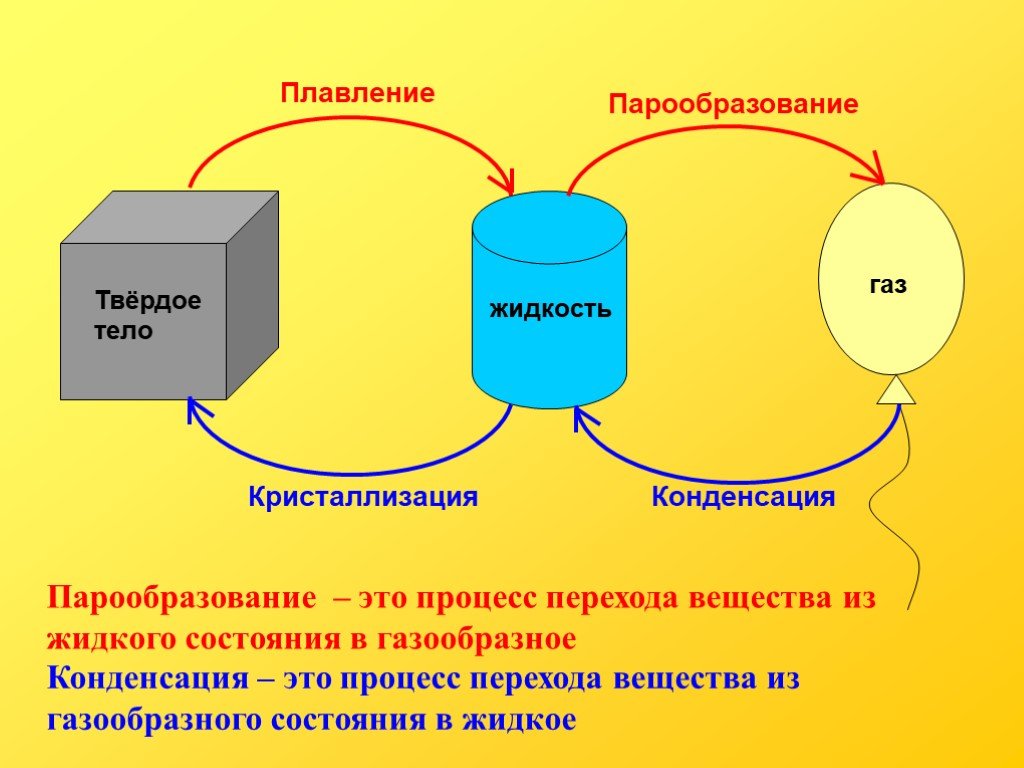
Переход из жидкого в газообразное состояние называют испарением, а противоположный ему переход из газообразного состояния в жидкое — конденсацией.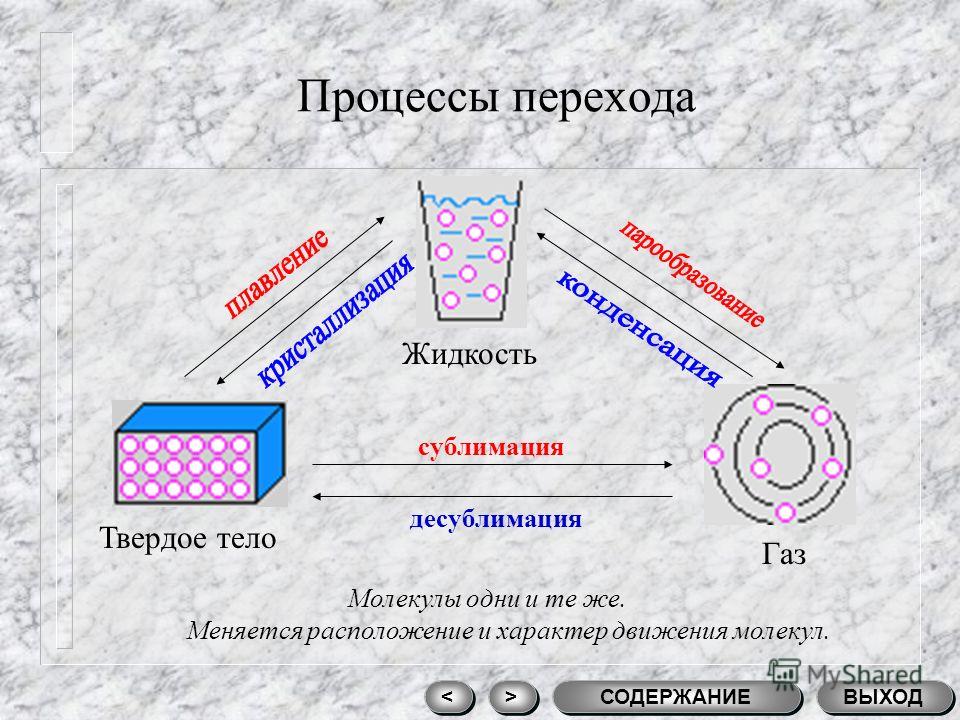 Переход из твёрдого состояния в газообразное, минуя жидкое, называют сублимацией или возгонкой.
Переход из твёрдого состояния в газообразное, минуя жидкое, называют сублимацией или возгонкой.
- Как называется процесс преобразования газа в жидкость?
- Какие способы относятся к переходу жидкости в газообразное состояние?
- Как называется процесс перехода воды из жидкого состояния в парообразное или газообразное?
- Что нужно чтобы вода из жидкого состояния перешла в газообразное?
- Как называется процесс при котором происходит преобразования СПГ из жидкого состояния в газообразное?
- Что называется сублимацией?
- Что называется процессом плавления?
- Как называется процесс из твёрдого состояния в газообразное?
- Как называется прямой переход вещества из твёрдого состояния в газообразное?
- Как называется процесс перехода вещества из жидкого?
- Как называется переход вещества из одного состояния в другое?
- Как называется процесс перехода воды?
- Что такое Декарбонизация газа?
- Как получить жидкость из газа?
- В каком случае газ можно превратить в жидкость?
- Чем отличается жидкости от газа?
Как называется процесс преобразования газа в жидкость?
Процесс преобразования вещества в другое агрегатное состояние происходит при нагревании воды по достижении точки изменения своего состояния — кипения. Обратный переход из газа в жидкое состояние называется конденсацией.
Обратный переход из газа в жидкое состояние называется конденсацией.
Какие способы относятся к переходу жидкости в газообразное состояние?
Процесс перехода из жидкого состояния в газообразное называется парообразованием. У этого процесса есть две разновидности: испарение и кипение.
Как называется процесс перехода воды из жидкого состояния в парообразное или газообразное?
Испаре́ние — процесс фазового перехода вещества из жидкого состояния в парообразное или газообразное, происходящий на поверхности вещества.
Что нужно чтобы вода из жидкого состояния перешла в газообразное?
Превращение жидкой воды в пар — это испарение. Испарение происходит при любой температуре, а полностью вода становится газообразной, если температура выше \(100\) градусов.
Как называется процесс при котором происходит преобразования СПГ из жидкого состояния в газообразное?
Регазифика́ция сжи́женного приро́дного га́за (СПГ) — процесс преобразования СПГ из жидкого состояния в газообразное, после чего он становится пригодным для обычного использования — подачи по трубопроводам потребителям и закачки в газовые баллоны.
Что называется сублимацией?
СУБЛИМА́ЦИЯ И ДЕСУБЛИМА́ЦИЯ, переход вещества из твёрдого состояния в газообразное и обратно без образования расплава при изменении темп-ры. Термин «сублимация» (от лат. sublimo — возносить) эквивалентен возгонке.
Что называется процессом плавления?
Плавле́ние — это процесс перехода тела из кристаллического твёрдого состояния в жидкое, то есть переход вещества из одного агрегатного состояния в другое.
Как называется процесс из твёрдого состояния в газообразное?
Сублима́ция (от лат. sublimo «возносить»), возго́нка — переход вещества из твёрдого состояния сразу в парообразное, минуя стадию плавления (перехода в жидкое состояние) и кипения.
Как называется прямой переход вещества из твёрдого состояния в газообразное?
Ответы1. Переход из твердого агрегатного состояния в газообразное, минуя жидкое называется «сублимация».
Как называется процесс перехода вещества из жидкого?
Переход вещества из жидкого состояния в твёрдое называют кристаллизацией.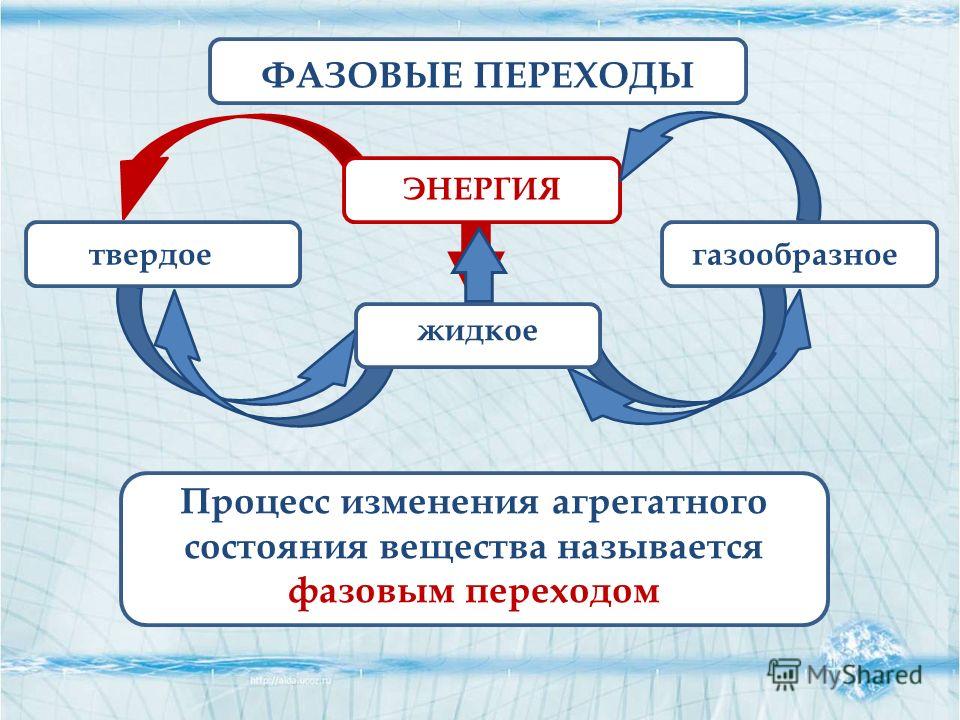 Выделение теплоты сопровождается уменьшением внутренней энергии вещества.
Выделение теплоты сопровождается уменьшением внутренней энергии вещества.
Как называется переход вещества из одного состояния в другое?
Переход из одного агрегатного состояния в другое называется фазовым переходом. Переход вещества из твердого состояния в жидкое называется плавлением, а температуру, при которой это происходит, — температурой плавления.
Как называется процесс перехода воды?
Круговоро́т воды́ в приро́де (гидрологи́ческий цикл), влагооборо́т — процесс циклического перемещения воды в земной биосфере. Состоит из испарения воды, переноса паров воздушными течениями, их конденсации, выпадения в виде осадков (дождь, снег и т.
Что такое Декарбонизация газа?
В контексте мировой экологии этот комплекс мер направлен на уменьшение выбросов углекислого газа в атмосферу. Сейчас декарбонизация означает отказ от углеводородов и переход к низкоуглеродной энергетике, использование экологичных видов энергии, таких как ветер, вода и солнце.
Как получить жидкость из газа?
Газ можно превратить в жидкость двумя способами:
- путем понижения температуры;
- путем сжимания под высоким давлением.

В каком случае газ можно превратить в жидкость?
При сжатии газ может перейти в жидкость, если его температура ниже так называемой критической температуры. Критическая температура является характеристикой конкретного газа и зависит от сил взаимодействия между его молекулами. Так, например, газ гелий можно сжижить только при температуре меньшей, чем 4,2 К.
Чем отличается жидкости от газа?
Жидкость — это вещество, которое свободно течет, имеет определенный объем, но не имеет постоянной формы. Газ относится к состоянию вещества, которое не имеет какой-либо формы, но полностью соответствует форме контейнера, в которую оно помещается. Твердые тела имеют фиксированную форму и объем.
Сублимация и осаждение — Энергетическое образование
Энергетическое образованиеМеню навигации
ИСТОЧНИКИ ЭНЕРГИИ
ИСПОЛЬЗОВАНИЕ ЭНЕРГИИ
ЭНЕРГЕТИЧЕСКОЕ ВОЗДЕЙСТВИЕ
ИНДЕКС
Поиск
Сублимация
Рисунок 1: Кусок твердого диоксида углерода (сухой лед), сублимирующийся из твердого вещества непосредственно в газ. [1]
[1]
Сублимация — это тип фазового перехода, при котором твердое вещество сразу превращается в газ, минуя жидкую фазу. Противоположность сублимации
Одним из распространенных примеров сублимации является твердый диоксид углерода, известный как сухой лед. При комнатной температуре (293 К) и давлении (1,01 бар) сухой лед сублимируется в пары углекислого газа. Сублимация — это эндотермический процесс, который происходит ниже тройной точки вещества на его фазовой диаграмме. [3] На рис. 2 показана фазовая диаграмма диоксида углерода, где сублимация может происходить ниже тройной точки (216,55 К и 5,17 бар).
 Температура и давление, при которых происходит сублимация, зависят от химических и физических свойств системы. Энергия, связанная с непосредственным переходом твердого тела в газообразное, называется скрытой теплотой сублимации.
Температура и давление, при которых происходит сублимация, зависят от химических и физических свойств системы. Энергия, связанная с непосредственным переходом твердого тела в газообразное, называется скрытой теплотой сублимации.Сублимация происходит и со снегом. Это означает, что когда воздух особенно сухой (низкая влажность), вода превращается прямо из снега или льда в водяной пар, не будучи вообще жидкой.
Рисунок 2: Фазовая диаграмма двуокиси углерода, показывающая, как происходит сублимация ниже тройной точки. [5] Более высокое давление сделало бы сухой лед «мокрым», так как образовалась бы жидкая двуокись углерода.
Посетите вики-сайт UC Davis Chem для получения дополнительной информации о сублимации.
Осаждение
Как указывалось ранее, осаждение из паровой фазы противоположно сублимации. Осаждение – это когда вещество в газообразной форме меняет свое состояние и становится твердым. Газообразное вещество получает осажденного (обычно в виде кристаллов) минуя промежуточное жидкое состояние. Примером отложения является превращение водяного пара в атмосфере непосредственно в лед, например, при образовании инея. [2]
Газообразное вещество получает осажденного (обычно в виде кристаллов) минуя промежуточное жидкое состояние. Примером отложения является превращение водяного пара в атмосфере непосредственно в лед, например, при образовании инея. [2]
Для дальнейшего чтения
- Твердое, жидкое, газообразное
- Скрытая теплота
- Удельная скрытая теплота
- Изменение фазы
- Или просмотрите случайную страницу
Ссылки
- ↑ Helmenstine, Anne Marie, Ph.D. «Определение сублимации (фазовый переход в химии)», ThoughtCo, 16 февраля 2021 г. [Онлайн]. Доступно: thinkco.com/definition-of-sublimation-phase-transition-604665. [Проверено: 12 мая 2021 г.]
- ↑ 2.0 2.1 2.2 «Сублимация и круговорот воды», USGS [онлайн]. Доступно: https://www.usgs.gov/special-topic/water-science-school/science/sublimation-and-water-cycle?qt-science_center_objects=0#qt-science_center_objects [Проверено: 13 мая 2021 г.
 ]
] - ↑ «Сублимация (физика)», Энциклопедия всемирного наследия. [В сети]. Доступно: http://self.gutenberg.org/articles/Sublimation_(physics). [Проверено: 14 мая 2021 г.]
- ↑ «Фазы материи», UCSB Physics. [В сети]. Доступно: http://web.physics.ucsb.edu/~lecturedemonstrations/Composer/Pages/48.36.html. [Проверено: 12 мая 2021 г.]
- ↑ «Сверхкритический диоксид углерода», Википедия, 2021 г. [Онлайн]. Доступно: https://en.wikipedia.org/wiki/Суперкритический_диоксид углерода. [Проверено: 12 мая 2021 г.]
Прямой переход из твердого состояния в газообразное называется: A. Диссоциацией B. Разложением C. Сублимацией D. Растворением
Дата последнего обновления: 12 марта 2023 г. : 5.28k
Ответить
Проверено
247.2k+ просмотров
Подсказка: Проверить фазовые переходы заданных состояний. Переход может быть из твердого состояния в жидкое, из жидкого в газообразное и из твердого в газообразное и многое другое.
Полный ответ:
Переход вещества непосредственно из твердого состояния в газообразное, минуя жидкое состояние, называется сублимацией.
Ответ: Вариант(С)
При фазовом переходе из твердого состояния в газообразное химическая идентичность вещества не изменяется. Обратная сублимация, то есть переход из газа в твердое состояние, известна как осаждение. Примером сублимации является СУХОЙ ЛЕД. Сухой лед претерпевает физические изменения, когда он сублимирует из твердого состояния в газообразное без предварительного плавления в жидкость. Тот же $C{{O}_{2}}$ все еще присутствует; он просто претерпевает фазовый переход и становится бесцветным газом.
Итак, правильный ответ — «Вариант С».
Примечание:
Изучение фазовых переходов различных состояний, обратимых и необратимых процессов переходов на примерах из повседневной жизни.

 ]
]
Leave A Comment