ЕГЭ. Строение вещества (типы химической связи, типы кристаллических решеток, степень окисления) 11 класс
Тема 3: Типы химической связи
Урок 4: ЕГЭ. Строение вещества (типы химической связи, типы кристаллических решеток, степень окисления)
- Видео
- Тренажер
- Теория
Заметили ошибку?
Задания с выбором ответов А1-А16
|
Вопрос |
Комментарий |
|
А1. Сложными веществами называют:
|
Простое вещество – это соединение, образованное атомами одного химического элемента, а сложное вещество образовано атомами различных химических элементов. Правильный ответ 2. |
|
А2. Наибольшую температуру плавления имеет вещество формула которого:
|
Нужно знать, какие кристаллические решетки имеют данные вещества: СН4 – молекулярную, SiO2 – атомную, Sn – металлическую, КF –ионную.Наиболее высокой температурой плавления характеризуются вещества с атомной кристаллической решеткой. Правильный ответ 2. |
|
А3. Веществами молекулярного строения являются все вещества ряда:
|
Сера, сахар, глицин, глицерин – вещества молекулярного строения. Поваренная соль и медный купорос имеют ионную кристаллическую решетку. Правильный ответ 4. |
|
А4. К веществам молекулярного строения относится:
|
Анализируем: к какому типу кристаллических решеток относятся данные вещества. СаО, КF, С2Н5ОNa имеют ионную кристаллическую решетку. С6Н12О6 – молекулярную. |
|
А5. Из перечисленных веществ немолекулярное строение имеет:
|
Если в веществе содержится несколько атомов (I2), то это вещество молекулярного строения.
Правильный ответ 3. |
|
А6.Химическая связь в бромиде калия:
|
Бромид калия (КBr) – это типичная соль, образованная атомами, резко отличающимися по электроотрицательности. Правильный ответ 4. |
|
А7. Какая связь возникает между атомами химических эелентов с порядковыми номерами 8 и 16?
|
Это S и О. Это неметаллы. Их электроотрицательности близки. Значит, связь ковалентная полярная.
Правильный ответ 2. |
|
А8. Связь в соединении, образованном между атомом водорода и элементом, имеющим электронную конфигурацию 2,8,6, является:
|
Находим элемент по распределению электронов в атоме. Их сумма равна количеству протонов, порядковому номеру. Правильный ответ 2. |
|
А9. В ковалентных водородных соединениях состава НЭ число общих электронных пар равно:
|
Атом водорода имеет только один электрон, поэтому при взаимодействии с другими атомами он может образовывать только одну общую электронную пару. Правильный ответ 1. |
|
А10. Одна из связей в ионе аммония образована:
|
В ионе аммония есть 4 ковалентные связи. Правильный ответ 1. |
|
А11. Степень окисления фосфора в соединении h4PO4 равна:
|
Сумма степеней окисления с учетом количества атомов, должна быть равна 0. Н+, О-2, поэтому Р+5.
Правильный ответ 4. |
|
А 12. Постоянную степень окисления имеет атом элемента: 1. Cl 2. C 3. Cu 4. Na |
Так как элементы I-A группы имеют один валентный электрон, то они могут проявлять лишь одну степень окисления +1. Правильный ответ 4. |
|
А13. Кристаллическая решетка графита:
|
Графит образован углеродом – неметаллом. Правильный ответ 1. |
|
А14. В узлах кристаллических решеток веществ молекулярного строения находятся:
|
В узлах кристаллических решеток веществ молекулярного строения находятся молекулы.
Правильный ответ 1. |
|
А15. Из приведенных ниже веществ атомную кристалличекую решетку имеет:
|
Магний – это металл. Он имеет металлическую кристаллическую решетку. Сера, нафталин – молекулярную кристаллическую решетку. Правильный ответ 4. |
|
А16. Для веществ с металлической кристаллической решеткой нехарактерным свойством является:
|
Для металлов характерны такие свойства: электро- и теплопроводность, пластичность, металлический блеск. Хрупкость – это свойство, обратное пластичности, значит, металлы им обладать не могут. Правильный ответ 3. |
Задания с кратким ответом и на соответствие В1-В7
Задания с развернутым ответом С1-С2
Подведение итога урока
На уроке рассматривалось решение задач из ЕГЭ по теме «Строение вещества (типы химической связи, типы кристаллических решеток, степени окисления)».
Список литературы
- Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- Попель П. П. Химия: 11 кл.: учебник для общеобразовательных учебных заведений / П. П. Попель, Л. С. Кривля. – К.: ИЦ «Академия», 2008. – 240 с.: ил.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Интернет-портал «interneturok.ru» (Источник)
- Интернет-портал «ege.
 edu.ru» (Источник)
edu.ru» (Источник) - Интернет-портал «chemport.ru» (Источник)
- Интернет-портал «Химик.ру» (Источник)
Домашнее задание
- №№ 11–33 (с. 23) Рудзитис Г. Е. Химия. Основы общей химии. 11 класс: учебник для общеобразовательных учреждений: базовый уровень/ Г. Е. Рудзитис, Ф. Г. Фельдман. – 14-е издание. – М.: Просвещение, 2012.
- При полном окислении 2 г простого вещества образуется 18 г оксида состава Э2О. Найти молярную массу простого вещества.
- Определите валентность и степень окисления углерода в соединениях: С2Н5ОН, СН3СООН.
Заметили ошибку?
Расскажите нам об ошибке, и мы ее исправим.Видеоурок: ЕГЭ. Строение вещества (типы химической связи, типы кристаллических решеток, степень окисления) по предмету Химия за 11 класс.
Химическая связь и Типы кристаллических решеток | Тест по химии (11 класс):
Тест по теме:
«Химическая связь и типы кристаллических решеток»
I вариант
Часть А
- Формула вещества, образованного ковалентной неполярной связью:
- SiO2 2) F2 3) CaO 4) h3S
- Формула вещества, образованного ковалентной полярной связью:
- Nh4 2) Na2S 3) h3 4) Fe2O3
- Ионная связь характерна для:
- Меди 2) хлорида железа(III) 3) сероводорода 4) хлора
- Молекулярное строение имеет каждое из двух веществ:
- Ch5 и Na2CO3 3) C2H5ONa и Nh5Cl
- Ch4OCh4 и HCL 4) C2H5OH и алмаз
- Пара химических элементов, способных к образованию ковалентной полярной связи:
- Fe и S 2) C и O 3) Ba и S 4) Na и Cl
- Между какими атомами возникает водородная связь:
- Водородом и любым другим элементом
- Водородом и атомом с большей атомной массой
- Водородом и элементами с высокой электроотрицательностью
- Водородом и неметаллами
- Какой вид связи в молекуле кислорода:
- Ионная 2) Металлическая
3) Ковалентная полярная 4) Ковалентная неполярная
- Ряд формул веществ, каждое из которых образовано ионной связью:
1) Al2O3 P2O5 NaCl 2) SO3 CaO KF
3) HCl Al(NO3 )3 Na3P 4) KBr Li3N CuS
- Атом химического элемента, образующего с галогеном соединение с ионной связью, имеет электронную конфигурацию:
- 1s22s22p63s23p4 3) 1s22s22p63s23p64s23d6
- 1s22s22p6 4) 1s22s22p63s23p64s23d104p5
- Соединения с ковалентной полярной и ковалентной неполярной связью являются соответственно:
1) KI и O2 2) h3S и Fe
3) N2O5 и Cu 4) CO и h3
- Какое вещество является примером внутримолекулярной водородной связи:
- сероводород 2) ДНК 3) углевода 4) борная кислота
- Выберите тип кристаллической решетки веществ, для которых характерны следующие свойства: низкие температуры плавления, летучесть, малая твердость:
- атомная 2) молекулярная 3) ионная 4) металлическая
- Верны ли следующие суждения?
А. Для вещества с ионной связью характерны тугоплавкость, пластичность и высокие температуры плавления.
Для вещества с ионной связью характерны тугоплавкость, пластичность и высокие температуры плавления.
В. Ковалентная полярная связь образуется по обменному механизму.
1) верно только А 2) верно только В
3) оба суждения верны 4) оба суждения неверны
- Верны ли следующие суждения:
А. В молекуле хлороводорода атомы связаны ковалентной полярной связью.
В. Между атомами, имеющими распределение электронов по слоям 2е 8е 8е 2е и 2е 8е 7е, возникает ионная связь.
- Верно только А 2) верно только В
3) верны оба суждения 4) оба суждения неверны
Часть В
- Установите соотношение между названием вещества и его химической связи
1) Ch4OH | А) Металлическая |
2) CCL4 | Б) Ковалентная полярная |
3) Al | В) Ионная |
4 )BaS | Г) Ковалентная неполярная |
5) F2 | Д) Водородная |
- Установите соотношение между названием вещества и его кристаллической решеткой:
1) SiO2 | А) Молекулярная |
2) h3O | Б) Ионная |
3) Cu | В) Атомная |
4) KOH | Г) Металлическая |
Тест по теме:
«Химическая связь и типы кристаллических решеток»
II вариант
Часть А
- Формула вещества, образованного ковалентной неполярной связью:
- Cu 2) h3O 3) HBr 4) Cl2
- Формула вещества, образованного ковалентной полярной связью:
- NaCl 2) Fe 3) KOH 4) P2O5
- Ионная связь характерна для:
- хлороводорода 2) оксида магния 3) водорода 4) железа
- Кристаллическую структуру, подобную структуре алмаза, имеет:
- кремнезем 3)оксид натрия
- оксид углерода (II) 4) белый фосфор
- Пара химических элементов, способных к образованию ковалентной полярной связи:
- K и Br 2) Mg и I 3) H и Cl 4) Cu и S
- Каковы особенности водородной связи:
- Невысокая прочность, распространенность
- Высокая прочность, распространенность
- Невысокая прочность, редкость
- Высокая прочность, редкость
- Какой вид связи в молекуле брома:
- Ковалентная полярная 3) Водородная
- Ионная 4) Ковалентная неполярная
- Ряд формул веществ, каждое из которых образовано ионной связью:
1) AlBr3 Na2S N2O5 3) Mg(NO3)2 KI (Nh5)2SO4
2) Nh4 Nh5Cl CaS 4) h3 BaBr2 SiO2
- Укажите НЕ правильное утверждение:
- Водородная связь присутствует в молекулах белков
- Водородная связь бывает межмолекулярной и внутримолекулярной
- Водородная связь прочная
- Водородная связь образуется между атомом водорода и сильно электроотрицательным атомом
- Соединения с ионной связью и металлической являются соответственно:
1) Nh5Cl и Fe 3) Al2O3 и C
2) KBr и O3 4) HNO3 и Cu
11. В каком веществе водородная связь наиболее прочная:
В каком веществе водородная связь наиболее прочная:
1) Вода 2) аммиак 3) соляная кислота 4) плавиковая кислота
12. Вещества с атомной кристаллической решеткой:
1) хрупкие и легкоплавкие 3) очень твердые и тугоплавкие
3) проводят электрический ток в растворах 4) твердые и легкоплавкие
13. Верны ли следующие суждения о неметаллах?
А. Все неметаллы являются химически активными веществами.
В. Неметаллы обладают только окислительными свойствами.
1) верно только А 3) верно только В
2) верны оба суждения 4) оба суждения неверны
14. Отметьте группу, в которой перечислены ТОЛЬКО вещества с ковалентным типом связи:
1) Ацетон, оксид магния, сульфат хрома (III) 3) Вода, йодоводород, ртуть
2) Озон, 2-метилпропановая кислота, оксид хлора (VII) 4) Хлорид цезия, бензол, водород
Часть В
15. Установите соотношение между названием вещества и его химической связи
Установите соотношение между названием вещества и его химической связи
1) O2 | А) Ионная |
2) C2H5OH | Б) Металлическая |
3) Fe | В) Ковалентная полярная |
4) HCl | Г) Водородная |
5) LiI | Д) Ковалентная неполярная |
16. Установите соотношение между названием вещества и его кристаллической решеткой:
1) O2 | А) Атомная |
2) Fe | б) Металлическая |
3) BaCl2 | В) Ионная |
4) P красный | Г) Молекулярная |
Ответы
I | II |
| 1)4 |
| 2)4 |
| 3)2 |
| 4)1 |
| 5)3 |
| 6)1 |
| 7)4 |
| 8)3 |
| 9)3 |
| 10)1 |
| 11)4 |
| 12)3 |
| 13)3 |
| 14)2 |
15) 1- Д 2- Б 3 – А 4 – В 5 — Г | 15)1 – Д 2 – Г 3 – Б 4 – В 5 — А |
16) 1 – В 2 – А 3 – Г 4 — Б | 16)1 – Г 2 – Б 3 – В 4 — А |
Кристаллическая структура сверхпроводящей фазы гидрида серы
Кристаллическая структура сверхпроводящей фазы гидрида серы
Скачать PDF
Ваша статья скачана
Слайдер с тремя статьями на слайде. Используйте кнопки «Назад» и «Далее» для перемещения по слайдам или кнопки контроллера слайдов в конце для перемещения по каждому слайду.
Используйте кнопки «Назад» и «Далее» для перемещения по слайдам или кнопки контроллера слайдов в конце для перемещения по каждому слайду.
Скачать PDF
- Опубликовано:
- Мари Эйнага 1 na1 ,
- Масафуми Саката 1 ,
- Такахиро Исикава 1 ,
- 6 Шиями Кацу ORCID: orcid.org/0000-0003-0560-8325 1 na1 ,
- Еремец Михаил Иванович 2 na1 ,
- Дроздов Александр П. 2 ,
- Иван А. Троян 2 ,
- Хирао Наохиса 3 и
- …
- Ясуо Охиши 7 6 1 3
Физика природы том 12 , страницы 835–838 (2016)Процитировать эту статью
14 тыс.
 обращений
обращений279 цитирований
83 Альтметрический
Сведения о показателях
Субъекты
- Строение твердых и жидких тел
- Сверхпроводящие свойства и материалы
Abstract
Недавно в H 2 S (или D 2 S) при высоком гидростатическом давлении 1,2 была обнаружена сверхпроводящая критическая температура выше 200 K. Эти измерения были интерпретированы с точки зрения разложения этих материалов на элементарную серу и богатый водородом гидрид, который отвечает за сверхпроводимость, хотя прямых экспериментальных доказательств этого механизма до сих пор не было.
 Здесь мы приводим кристаллическую структуру сверхпроводящей фазы сероводорода (и сульфида дейтерия) в нормальном и сверхпроводящем состояниях, полученную с помощью измерений синхротронной рентгеновской дифракции в сочетании с измерениями электрического сопротивления как при комнатной, так и при низких температурах. Мы находим, что сверхпроводящая фаза в основном хорошо согласуется с теоретически предсказанной объемно-центрированной кубической (ОЦК) структурой для H 3 S 3 . Присутствие элементарной серы также проявляется на рентгенограммах, что подтверждает механизм разложения H 2 S до H 3 S + S под давлением 4,5,6 .
Здесь мы приводим кристаллическую структуру сверхпроводящей фазы сероводорода (и сульфида дейтерия) в нормальном и сверхпроводящем состояниях, полученную с помощью измерений синхротронной рентгеновской дифракции в сочетании с измерениями электрического сопротивления как при комнатной, так и при низких температурах. Мы находим, что сверхпроводящая фаза в основном хорошо согласуется с теоретически предсказанной объемно-центрированной кубической (ОЦК) структурой для H 3 S 3 . Присутствие элементарной серы также проявляется на рентгенограммах, что подтверждает механизм разложения H 2 S до H 3 S + S под давлением 4,5,6 .Главная
Недавно в сероводородной системе 1,2 обнаружен очень высокий T c 200 K. Эта работа была инициирована предсказанием существенной сверхпроводимости в H 2 S (ссылка 7), что, в свою очередь, вытекает из идеи, что металлические сплавы с преобладанием водорода могут быть сверхпроводниками с высокой критической температурой, подобными чистому металлическому водороду 8 .

Сверхпроводящий переход доказан резким падением сопротивления до нуля, сильным изотопическим эффектом при исследовании D 2 S, сдвигом сверхпроводящего перехода с магнитным полем и, наконец, измерениями магнитной восприимчивости и намагниченности . В качестве вероятного объяснения авторы 1,2 предположил, что H 2 S разлагается под давлением (с помощью температуры) на чистую серу и некоторое количество гидрида серы с более высоким содержанием водорода (например, SH 4 или аналогичный). В это же время появилась теоретическая работа, в которой рассматривалось другое исходное вещество (H 2 S) 2 H 2 (стехиометрия H 3 S) и найдены R 3 m и
6 Im -3 м сооружений под давлением выше 111 ГПа и 180 ГПа соответственно 3 . Эти структуры и другие стехиометрические соединения в дальнейшем тщательно изучались теоретически различными группами в многочисленных работах 4,6,9,10,11,12,13,14,15,16,17,18,19,20,21,22, 23,24,25 и T c ∼ 200 K для структуры Im -3 m . Дроздов А.П., Еремец М.И., Троян И.А. Обычная сверхпроводимость при 190 К при высоких давлениях. Препринт на http://arxiv.org/abs/1412.0460 (2014 г.).
Дроздов А. П., Еремец М. И., Троян И. А., Ксенофонтов В., Шилин С. И. Обычная сверхпроводимость при 203 кельвина при высоких давлениях в сероводородной системе. Природа 525 , 73–77 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Duan, D. et al. Индуцированная давлением металлизация плотного (h3S)2h3 с высокотемпературной сверхпроводимостью c . науч. Респ. 4 , 6968 (2014).
Артикул Google Scholar
Бернштейн, Н.
 , Хеллберг, К.С., Йоханнес, М.Д., Мазин, И.И. и Мел, М.Дж. Какие сверхпроводники в гидридах серы под давлением и почему. Физ. Ред. B 91 , 060511(R) (2015).
, Хеллберг, К.С., Йоханнес, М.Д., Мазин, И.И. и Мел, М.Дж. Какие сверхпроводники в гидридах серы под давлением и почему. Физ. Ред. B 91 , 060511(R) (2015).Артикул ОБЪЯВЛЕНИЯ Google Scholar
Duan, D. et al. Разложение твердого сероводорода под давлением. Физ. Ред. B 91 , 180502(R) (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Errea, I. et al. Сероводород высокого давления из первых принципов: сильно ангармонический фонон-опосредованный сверхпроводник. Физ. Преподобный Летт. 114 , 157004 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Ли, Ю., Хао, Дж., Лю, Х., Ли, Ю. и Ма, Ю. Металлизация и сверхпроводимость плотного сероводорода. J. Chem. физ. 140 , 174712 (2014).

Артикул ОБЪЯВЛЕНИЯ Google Scholar
Ashcroft, N.W. Металлические сплавы с преобладанием водорода: высокотемпературные сверхпроводники? Физ. Преподобный Летт. 92 , 187002 (2004 г.).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Акаси, Р., Кавамура, М., Цунеюки, С., Номура, Ю. и Арита, Р. Исследование из первых принципов зависимости давления и кристаллической структуры температуры сверхпроводящего перехода в сжатых гидридах серы. Физ. Ред. B 91 , 224513 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Флорес-Ливас, Дж. А., Санна, А. и Гросс, Э. К. У. Высокотемпературная сверхпроводимость в гидридах серы и селена при высоком давлении. евро. физ. J. B 89 , 63 (2016).
ОБЪЯВЛЕНИЕ Google Scholar
Ге, Ю.
 , Чжан, Ф. и Яо, Ю. Возможная сверхпроводимость приближается к ледяной точке. Препринт на http://arxiv.org/abs/1507.08525 (2015 г.).
, Чжан, Ф. и Яо, Ю. Возможная сверхпроводимость приближается к ледяной точке. Препринт на http://arxiv.org/abs/1507.08525 (2015 г.).Папаконстантопулос, Д. А., Кляйн, Б. М., Мел, М. Дж. и Пикетт, У. Э. Cubic h4S около 200 ГПа: сверхпроводник атомарного водорода, стабилизированный серой. Физ. B 91 , 184511 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Li, Y. et al. Продукты диссоциации и структуры твердого h3S при сильном сжатии. Физ. Ред. B 93 , 020103 (R) (2016 г.).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Quan, Y. & Pickett, W. E. Особенности Ван Хова и размытие спектра в высокотемпературном сверхпроводнике h4S. Физ. Преподобный Летт. 93 , 104526 (2016).
Google Scholar
Бьянкони, А.
 и Ярлборг, Т. Переходы Лифшица и нулевые флуктуации решетки в гидриде серы, демонстрирующие сверхпроводимость при комнатной температуре. Ноябрь. Суперконд. Матер. 1 , 37–49 (2015).
и Ярлборг, Т. Переходы Лифшица и нулевые флуктуации решетки в гидриде серы, демонстрирующие сверхпроводимость при комнатной температуре. Ноябрь. Суперконд. Матер. 1 , 37–49 (2015).Google Scholar
Никол, Э. Дж. и Карботт, Дж. П. Сравнение гидрида серы под давлением с обычными сверхпроводниками. Физ. Ред. B 91 , 220507(R) (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Дегтяренко Н., Мазур Е. Причины высокотемпературной сверхпроводимости в сероводородной электрон-фононной системе. Препринт на http://arxiv.org/abs/1507.05749 (2015 г.).
Дурайски А.П., Щешняк Р. и Ли Ю. Термодинамические свойства сверхпроводника h3S без БКШ. Физика С 515 , 1–6 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Дурайски А.
 П., Щешняк Р. и Пьетронеро Л. Высокотемпературное исследование сверхпроводящего водорода и сульфида дейтерия. Энн. физ. http://dx.doi.org/10.1002/andp.201500316 (2015 г.).
П., Щешняк Р. и Пьетронеро Л. Высокотемпературное исследование сверхпроводящего водорода и сульфида дейтерия. Энн. физ. http://dx.doi.org/10.1002/andp.201500316 (2015 г.).Горьков Л., Кресин В. Давление и высокая T c сверхпроводимость: приложения к гидридам серы. Препринт на http://arxiv.org/abs/1511.06926 (2015).
Hirsch, J. E. & Marsiglio, F. Дырочная сверхпроводимость в h3S и других сульфидах под высоким давлением. Physica C 511 , 45–49 (2015).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Банацки, П. О механизме высокотемпературной сверхпроводимости в сероводороде при 200 ГПа: переход в сверхпроводящее антиадиабатическое состояние при взаимодействии с Н-колебаниями. Результаты Физ. 6 , 1–2 (2016).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Errea, I.
 et al. Квантовая симметризация водородных связей в сверхпроводящей сероводородной системе. Природа 532 , 81–84 (2016).
et al. Квантовая симметризация водородных связей в сверхпроводящей сероводородной системе. Природа 532 , 81–84 (2016).Артикул ОБЪЯВЛЕНИЯ Google Scholar
Акаши Р., Сано В., Арита Р. и Цунеюки С. Возможные фазы Магнели и самосплавление в сверхпроводящем гидриде серы. Препринт на http://arxiv.org/abs/1512.06680 (2015 г.).
Исикава Т. и др. Сверхпроводящая фаза H5S2 в системе сера-водород под высоким давлением. Науч. Респ. 6 , 23160 (2016).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Луо, Х., Грин, Р. Г. и Руофф, А. Л. β -фаза серы Po при 162 ГПа: рентгеноструктурное исследование до 212 ГПа. Физ. Преподобный Летт. 71 , 2943–2946 (1993).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Берч, Ф.
 Изотерма конечной деформации и скорости для монокристаллического и поликристаллического NaCl при высоких давлениях и 300 °K. Ж. Геофиз. Рез. 83 , 1257–1268 (1978).
Изотерма конечной деформации и скорости для монокристаллического и поликристаллического NaCl при высоких давлениях и 300 °K. Ж. Геофиз. Рез. 83 , 1257–1268 (1978).Артикул ОБЪЯВЛЕНИЯ Google Scholar
Мацуока Т. и др. Возвратная металлическая фаза под давлением в литии. Физ. Ред. B 89 , 144103 (2014).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Джанноцци, П. и др. QUANTUM ESPRESSO: модульный программный проект с открытым исходным кодом для квантового моделирования материалов. J. Phys. Конденс. Материя 21 , 395502 (2009).
Артикул Google Scholar
Пердью, Дж. П., Берк, К. и Эрнзерхоф, М. Упрощенное приближение обобщенного градиента. Физ. Преподобный Летт. 77 , 3865–3868 (1996).

Артикул ОБЪЯВЛЕНИЯ Google Scholar
Вандербильт Д. Мягкие самосогласованные псевдопотенциалы в обобщенном формализме собственных значений. Физ. Ред. B 41 , 7892–7895 (1990).
Артикул ОБЪЯВЛЕНИЯ Google Scholar
Мари Эйнага, Кацуя Симидзу и Михаил И. Еремец: Эти авторы внесли одинаковый вклад в эту работу.
Kyokugen, Высшая школа инженерных наук, Университет Осаки, Мачиканеямачо 1-3, Toyonaka, Osaka 560-8531, Япония
Mari Einaga, Masafuma Soakata, Shakaha, The Masafuma, The Masafuma, Shaka, Sura,
.

Институт химии им. Макса Планка, Хан-Майтнер-Вег 1, 55128 Майнц, Германия
Михаил И. Еремец, Александр П. Дроздов и Иван А. Троян
JASRI/SPring-8, 1-1-1, Sayo-cho, Sayo-gun, Hyogo 679-5198, Япония
Naohisa Hirao & Yasuo Ohishi
- Mari Einaga
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Масафуми Саката
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Takahiro Ishikawa
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Katsuya Shimizu
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Еремец Михаил Иванович
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Дроздов Александр Петрович
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Троян Иван А.

Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Naohisa Hirao
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Yasuo Ohishi
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
Синтез семи гидридов лантана под высоким давлением со значительной вариабельностью содержания водорода
- Доминик Ланиэль
- Флориан Трибель
- Наталья Дубровинская
Nature Communications (2022)
Синтез в кремнии тройных супергидридов с высоким Tc при самом низком давлении
- Роман Лукреци
- Симоне Ди Катальдо
- Кристоф Хайль
npj Расчетные материалы (2022)
Разбавленный углерод в h4S под давлением
- Сяоюй Ван
- Тянге Би
- Ева Зурек
npj Расчетные материалы (2022)
Первопринципный поиск горячей сверхпроводимости в тройных гидридах La-X-H
- Симоне Ди Катальдо
- Вольфганг фон дер Линден
- Лилия Боэри
npj Расчетные материалы (2022)
Высокотемпературная сверхпроводимость в гидридах: экспериментальные данные и детали
- Еремец М.
 И.
И. - Миньков В.С.
- Баликас Л.
Журнал сверхпроводимости и нового магнетизма (2022)
- Еремец М.
- Исследовательская статья
- Открытый доступ
- Опубликовано:
- Georgies Alene Asres 1 ,
- José J. Baldoví 2,3 ,
- Aron Dombovari 1 ,
- Topias Järvinen 1 ,
- Gabriela Simone Lorite 1 ,
- Melinda Mohl 1 ,
- Андрей Щукарев 4 ,
- Алехандро Перес Пас 3,5 ,
- Lede Xian 2,3 ,
- Jyri-Pekka Mikkola 4,6 ,
- Anita Lloyd Spetz 1,7 ,
- Heli Jantunen 1 ,
- Ángel Rubio 2,3 &
- …
- Кристиан Кордас 1
2948 доступов
63 Цитаты
Сведения о показателях
Нери, Г. Первые пятьдесят лет хеморезистивных газовых сенсоров. Хемосенсоры 2015 , 3 , 1–20.
Артикул Google Scholar
Деван, Р. С.; Патил, Р.А.; Лин, Дж. Х.; Ма, Ю. Р. Одномерные наноструктуры оксидов металлов: последние разработки в области синтеза, характеристик и приложений. Доп. Функц. Матер. 2012 , 22 , 3326–3370.
Артикул Google Scholar
Короценков Г. Управление газоотдачей путем структурно-химической модификации пленок оксидов металлов: современное состояние и подходы. Активация датчика. Б хим. 2015 , 107 , 209–232.

Артикул Google Scholar
Пальмизано, В.; Вайднер, Э.; Бун-Бретт, Л.; Бонато, К.; Харскамп, Ф .; Моретто, П.; Пост, МБ; Берджесс, Р .; Ривкин, К.; Баттнер, В. Дж. Селективность и устойчивость к ядам коммерческих датчиков водорода. Междунар. Дж. Водородная энергия 2015 , 40 , 11740–11747.
Артикул Google Scholar
Моди, А.; Кораткар, Н.; Ласс, Э .; Вэй, Б.К.; Аджаян, П. М. Миниатюрные датчики ионизации газа с использованием углеродных нанотрубок. Природа 2003 , 424 , 171–174.
Артикул Google Scholar
Уша, С. П.; Мишра, С.К.; Гупта, Б. Д. Волоконно-оптические датчики сероводорода с использованием тонкой пленки ZnO / наночастиц ZnO: сравнение поверхностного плазмонного резонанса и резонанса с потерями.
 Активация датчика. Б хим. 2015 , 218 , 196–204.
Активация датчика. Б хим. 2015 , 218 , 196–204.Артикул Google Scholar
Чен Г.Г.; Паронян, Т. М.; Пигос, Э. М.; Арутюнян, А. Р. Улучшенное определение газа в чистых углеродных нанотрубках при непрерывном освещении ультрафиолетовым светом. Науч. Респ. 2012 , 2 , 343.
Артикул Google Scholar
Щедин Ф.; Гейм, А.К.; Морозов, С. В.; Хилл, EW; Блейк, П.; Кацнельсон, М.И.; Новоселов К. С. Обнаружение индивидуальных молекул газа, адсорбированных на графене. Нац. Матер. 2007 , 6 , 652–655.
Артикул Google Scholar
Джаната Дж.; Йосович, М. Проводящие полимеры в электронных химических сенсорах.
 Нац. Матер. 2003 , 2 , 19–24.
Нац. Матер. 2003 , 2 , 19–24.Артикул Google Scholar
Каннан, П.К.; Поздно, ди-джей; Морган, Х .; Раут, К.С. Последние разработки в области двумерных слоистых неорганических наноматериалов для датчиков. Наномасштаб 2015 , 7 , 13293–13312.
Артикул Google Scholar
Ли Б.Л.; Ван, JP; Цзоу, HL; Гарадж, С .; Лим, CT; Се, JP; Ли, Н.Б.; Леонг Д.Т. Низкоразмерные датчики на основе наноструктур дихалькогенидов переходных металлов. Доп. Функц. Матер. 2016 , 26 , 7034–7056.
Артикул Google Scholar
Перкинс, Ф. К.; Фридман, А.Л.; Кобас, Э.; Кэмпбелл, PM; Джерниган, Г.Г.; Йонкер, Б.
 Т. Определение химических паров с помощью монослоя MoS 2 . Нано Летт. 2013 , 13 , 668–673.
Т. Определение химических паров с помощью монослоя MoS 2 . Нано Летт. 2013 , 13 , 668–673.Артикул Google Scholar
Чо Б.; Хам, М.Г.; Чой, М .; Юн, Дж.; Ким, А. Р.; Ли, Ю.-Дж.; Парк, С.-Г.; Квон, Дж.-Д.; Ким, CS; Сонг, М. и др. Обнаружение газа на основе переноса заряда с использованием атомарного слоя MoS 2 . науч. Респ. 2015 , 5 , 8052.
Артикул Google Scholar
Поздний, Д. Дж.; Хуанг, Ю.-К.; Лю, Б.; Ачарья, Дж.; Широдкар, С. Н.; Луо, JJ; Ян, А. М.; Чарльз, Д.; Вагмаре, У. В.; Дравид, В.П. и соавт. Чувствительность атомарно-тонкослойных транзисторов MoS 2 . СКД Нано 2013 , 7 , 4879–4891.
Артикул Google Scholar
Ван, К.
 Х.; Калантар-Заде, К.; Кис, А .; Коулман, Дж. Н.; Страно М.С. Электроника и оптоэлектроника двумерных дихалькогенидов переходных металлов. Нац. нанотехнологии. 2012 , 7 , 699–712.
Х.; Калантар-Заде, К.; Кис, А .; Коулман, Дж. Н.; Страно М.С. Электроника и оптоэлектроника двумерных дихалькогенидов переходных металлов. Нац. нанотехнологии. 2012 , 7 , 699–712.Артикул Google Scholar
Ко, К.Ю.; Песня, Ж.-Г.; Ким, Ю .; Чой, Т .; Шин, С .; Ли, CW; Лук-порей.; Ку, Дж .; Ли, Х .; Ким, Дж. и др. Улучшение газочувствительных характеристик нанолистов дисульфида вольфрама большой площади за счет функционализации поверхности. АКС Нано 2016 , 10 , 9287–9296.
Артикул Google Scholar
О’Брайен, М.; Лук-порей.; Морриш, Р.; Бернер, Северная Каролина; МакЭвой, Н .; Уолден, Калифорния; Дюсберг, Г.С. Плазменный синтез WS 2 для приложений обнаружения газов. Хим. физ. лат. 2014 , 615 , 6–10.

Артикул Google Scholar
Чжоу, Си Джей; Ян, WH; Чжу, Х.Л. Механизм переноса заряда и его влияние на закрепление уровня Ферми для молекул газа, адсорбированных на монослое WS 2 . J. Chem. физ. 2015 , 142 , 214704.
Артикул Google Scholar
Асрес, Джорджия; Домбовари, А .; Сипола, Т .; Пскас, Р .; Куковец, А .; Конья, З .; Попов, А .; Лин, Дж.-Ф.; Лорите, Г.С.; Мол, М. и др. Роман WS 2 гибридный материал нанопроволока-наночешуйки, синтезированный из нанопроволок WO 3 в парах серы. науч. Респ. 2016 , 6 , 25610.
Артикул Google Scholar
Ма, Дж. М.; Мэй, Л.; Чен, Ю. Дж.; Ли, QH; Ван, TH; Сюй, З .
 ; Дуань, XC; Zheng, W. J. α-Fe 2 O 3 наноцепи: ионотермический синтез на основе ацетата аммония и сверхчувствительные сенсоры для H 9 с низким содержанием ppm0099 2 С газ. Наномасштаб 2013 , 5 , 895–898.
; Дуань, XC; Zheng, W. J. α-Fe 2 O 3 наноцепи: ионотермический синтез на основе ацетата аммония и сверхчувствительные сенсоры для H 9 с низким содержанием ppm0099 2 С газ. Наномасштаб 2013 , 5 , 895–898.Артикул Google Scholar
Ли, З. Дж.; Хуанг, YW; Чжан, Южная Каролина; Чен, В. М.; Куанг, З .; Ао, Д.Ю.; Лю, В .; Fu, Y. Q. Датчик газа с быстрым откликом и восстановлением H 2 S на основе наночастиц α-Fe 2 O 3 с пределом обнаружения на уровне миллиардных долей. Дж. Азар. Матер. 2015 , 300 , 167–174.
Артикул Google Scholar
Манорама, С.; Деви, Г.С.; Рао, В. Дж. Сенсор сероводорода на основе оксида олова, нанесенного методом распылительного пиролиза и химического осаждения из паровой фазы в микроволновой плазме.
 Заяв. физ. лат. 1994 , 64 , 3163–3165.
Заяв. физ. лат. 1994 , 64 , 3163–3165.Артикул Google Scholar
Нир, Дж.; Кнобельспис, С.; Бирер, Б.; Волленштейн, Дж.; Пальцер, С. Новый метод выборочного определения концентрации сероводорода с использованием слоев CuO. Активация датчика. Б Хим 2016 , 222 , 625–631.
Артикул Google Scholar
Чжан Ф.; Чжу, А. В.; Луо, Ю. П.; Тиан, Ю .; Ян, JH; Цинь, Ю. Нанолисты CuO для чувствительного и селективного определения H 2 S с высокой восстановительной способностью. J. Phys. хим. С 2010 , 114 , 19214–19219.
Артикул Google Scholar
Ли, Ю. Х.; Луо, В .; Цинь, Н .
 ; Донг, JP; Вэй, Дж .; Ли, В .; Фэн, С.С.; Чен, JC; Сюй, JQ; Эльзатари, А.А. и соавт. Высокоупорядоченные мезопористые оксиды вольфрама с большим размером пор и кристаллическим каркасом для обнаружения H 2 S. Анжю. хим., межд. Эд. 2014 , 53 , 9035–9040.
; Донг, JP; Вэй, Дж .; Ли, В .; Фэн, С.С.; Чен, JC; Сюй, JQ; Эльзатари, А.А. и соавт. Высокоупорядоченные мезопористые оксиды вольфрама с большим размером пор и кристаллическим каркасом для обнаружения H 2 S. Анжю. хим., межд. Эд. 2014 , 53 , 9035–9040.Артикул Google Scholar
Ли, З. Дж.; Ниу, XY; Лин, ZJ; Ван, NN; Шен, HH; Лю, В .; Сан, К.; Фу, YQ; Ван, З. Г. Гидротермально синтезированные нанопроволоки CeO 2 для обнаружения H 2 S при комнатной температуре. Дж. Сплав. Комп. 2016 , 682 , 647–653.
Артикул Google Scholar
Ли М.; Чжоу, Д. Х.; Чжао, Дж.; Чжэн, ZP; Он, Дж. Г.; Ху, Л.; Ся, З .; Тан, Дж.; Лю, Х. Резистивные датчики газа на основе коллоидных квантовых точек (CQD) для обнаружения сероводорода.
 Активация датчика. Б хим. 2015 , 217 , 198–201.
Активация датчика. Б хим. 2015 , 217 , 198–201.Артикул Google Scholar
Пердью, Дж. П.; Берк, К.; Эрнцерхоф, М. Упрощенное приближение обобщенного градиента. Физ. Преподобный Летт. 1996 , 77 , 3865–3868.
Артикул Google Scholar
Джанноцци, П.; Барони, С.; Бонини, Н .; Каландра, М.; Машина.; Р.; Каваццони, К.; Черезоли, Д.; Кьяротти, Г.Л.; Кокачони, М.; Дабо, И. и др. QUANTUM ESPRESSO: модульный программный проект с открытым исходным кодом для квантового моделирования материалов. J. Phys. Конденс. Материя 2009 , 21 , 395502.
Артикул Google Scholar
Grimme, S. Полуэмпирический функционал плотности типа GGA, построенный с поправкой на дальнюю дисперсию.
 Дж. Вычисл. хим. 2006 , 27 , 1787–1799.
Дж. Вычисл. хим. 2006 , 27 , 1787–1799.Артикул Google Scholar
Хартвигсен, К.; Гедекер, С .; Хаттер, Дж. Релятивистские сепарабельные гауссовские псевдопотенциалы в двойном пространстве от H до Rn. Физ. Версия B 1998 , 58 , 3641–3662.
Артикул Google Scholar
Монкхорст, Х. Дж.; Пак, Дж. Д. Специальные точки для интеграции Бриллюэнзона. Физ. Версия B 1976 , 13 , 5188–5192.
Артикул Google Scholar
Тан, В.; Санвилл, Э.; Хенкельман, Г. Алгоритм анализа Бейдера на основе сетки без смещения решетки. J. Phys. Конденс. Материя 2009 , 21 , 084204.

Артикул Google Scholar
Куккола Дж.; Мол, М .; Лейно, А.-Р.; Маклин, Дж.; Халонен, Н .; Щукарев, А; Конья, З .; Янтунен, Х .; Кордас, К. Датчики водорода комнатной температуры на основе металла, декорированного WO 9.0099 3 нанопроволоки. Активация датчика. Б хим. 2013 , 186 , 90–95.
Артикул Google Scholar
Линартс, О.; Партонс, Б.; Питерс, Ф. М. Адсорбция H 2 O, NH 3 , CO, NO 2 и NO на графене: исследование первых принципов. Физ. Версия B 2008 , 77 , 125416.
Артикул Google Scholar
Перроцци, Ф.; Эмамджомех, С. М.; Паолуччи, В.; Тальери, Г.; Оттавиано, Л.; Канталини, К. Термическая стабильность хлопьев WS 2 и газочувствительные свойства композита WS 2 /WO 3 с H 2 , NH 3 и NO 2 .
 Активация датчика. Б хим. 2017 , 243 , 812–822.
Активация датчика. Б хим. 2017 , 243 , 812–822.Артикул Google Scholar
Куккола Дж.; Мол, М .; Лейно, А.-Р.; Тот, Г.; Ву, М.-К.; Щукарев, А.; Попов, А .; Миккола, Ж.-П.; Лаури, Дж.; Риихимяки, М. и соавт. Датчики газа, напечатанные струйной печатью: декорированные металлом наночастицы WO 3 и их газочувствительные свойства. Дж. Матер. хим. 2012 , 22 , 17878–17886.
Артикул Google Scholar
Куккола Дж.; Маклин, Дж.; Халонен, Н .; Киллонен, Т .; Тот, Г.; Сабо, М .; Щукарев, А.; Миккола, Ж.-П.; Янтунен, Х .; Кордас, К. Датчики газа на основе анодного оксида вольфрама. Активация датчика Б хим. 2011 , 153 , 293–300.
Артикул Google Scholar
Ча, Ж.
 -Х.; Чой, С.-Дж.; Ю, С .; Ким, И.-Д. 2D WS 2 — многоканальные углеродные нановолокна, функционализированные краями: влияние структуры с обильными краями WS 2 на комнатную температуру NO 2 определение. Дж. Матер. хим. А 2017 , 5 , 8725–8732.
-Х.; Чой, С.-Дж.; Ю, С .; Ким, И.-Д. 2D WS 2 — многоканальные углеродные нановолокна, функционализированные краями: влияние структуры с обильными краями WS 2 на комнатную температуру NO 2 определение. Дж. Матер. хим. А 2017 , 5 , 8725–8732.Артикул Google Scholar
Исследовательский отдел микроэлектроники, Факультет информационных технологий и электротехники, Университет Оулу, P.O. Box 4500, FI-
Георгис Ален Асрес, Арон Домбовари, Топиас Ярвинен, Габриэла Симоне Лорите, Мелинда Мохл, Анита Ллойд Спец, Хели Янтунен и Кристиан Кордас
ДинамикаИнститут проектирования и проектирования им. Материи, Лурупер Шоссе 149, 22761, Гамбург, Германия
José J. Baldoví, Lede Xian и Ángel Rubio
Группа нано-биоспектроскопии, Европейский центр теоретической спектроскопии (ETSF), Паисский университет, CFM SCIC-UPV/EHU-MPC DIPC , Avenida Tolosa 72, 20018, San Sebastian, Spain
José J.
 Baldoví, Alejandro Pérez Paz, Lede Xian и Ángel Rubio
Baldoví, Alejandro Pérez Paz, Lede Xian и Ángel RubioТехническая химия, Химический факультет, Химико-биологический центр, Umeå9 University, SE- Умео, Швеция
Андрей Щукарев и Юри-Пекка Миккола
Школа химических наук и инженерии, Школа физики и нанотехнологий, Технический университет Ячай, Уркуки, Эквадор
Алехандро Перес Пас
Сенсорные и исполнительные системы, Факультет физики, химии и биологии, Университет Линчёпинга, SE- 58183, Линчёпинг, Швеция
Anita Lloyd Spetz
- Georgies Alene Asres
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- José J. Baldoví
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Aron Dombovari
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Академия
- Topias Järvinen
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Gabriela Simone Lorite
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Melinda Mohl
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Андрей Щукарев
Посмотреть публикации автора
Вы также можете искать этого автора в PubMed Google Scholar
- Alejandro Pérez Paz
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Lede Xian
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Jyri-Pekka Mikkola
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Anita Lloyd Spetz
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Heli Jantunen
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Анхель Рубио
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
- Krisztian Kordás
Просмотр публикаций автора
Вы также можете искать этого автора в PubMed Google Scholar
 Расчетное T c , а также его зависимость от давления 9 близки к экспериментальным данным 1,2 . Это говорит о том, что высокие 9Наблюдаемый в экспериментах 0119 T c относится не к H 2 S, а к H 3 S в структуре Im -3 m . Более поздние расчеты подтвердили эту идею: H 2 S действительно неустойчива при высоких давлениях и должна разлагаться на серу и высшие гидриды, скорее всего, на H 3 S 4,6,12 . Цель настоящей работы — экспериментально проверить структуру сверхпроводящего сероводорода и сравнить ее с теоретически предсказанной структурой.
Расчетное T c , а также его зависимость от давления 9 близки к экспериментальным данным 1,2 . Это говорит о том, что высокие 9Наблюдаемый в экспериментах 0119 T c относится не к H 2 S, а к H 3 S в структуре Im -3 m . Более поздние расчеты подтвердили эту идею: H 2 S действительно неустойчива при высоких давлениях и должна разлагаться на серу и высшие гидриды, скорее всего, на H 3 S 4,6,12 . Цель настоящей работы — экспериментально проверить структуру сверхпроводящего сероводорода и сравнить ее с теоретически предсказанной структурой. Образцы готовили так же, как описано в работах 1,2—H 2 S нагружали при температуре ∼200 К, затем повышали давление до ∼150–170 ГПа и образец отжигали при комнатной температуре . Типичные рентгеновские дифрактограммы (XRD) гидрида серы и дейтерида серы, находящихся под давлением 150–173 ГПа, показаны на рис. 1. Рентгенограммы образцов гидрида серы и дейтерида серы не отличаются друг от друга. Дифракционные картины, по-видимому, создаются двумя основными фазами. Это ясно следует из разной зависимости пиков от давления (рис. 2 и дополнительный рисунок 3) и разного изменения интенсивности при сканировании образца по его диаметру (дополнительный рисунок 1): одна группа соответствует элементной сере β -Po структура 26 и другая группа описывается ОЦК структурой H 3 S из теоретической работы 3 . Можно сделать вывод, что H 2 S (D 2 S) твердый, скорее всего, разлагается под давлением по пути: 3H 2 S → 2H 3 S + S.
1. Рентгенограммы образцов гидрида серы и дейтерида серы не отличаются друг от друга. Дифракционные картины, по-видимому, создаются двумя основными фазами. Это ясно следует из разной зависимости пиков от давления (рис. 2 и дополнительный рисунок 3) и разного изменения интенсивности при сканировании образца по его диаметру (дополнительный рисунок 1): одна группа соответствует элементной сере β -Po структура 26 и другая группа описывается ОЦК структурой H 3 S из теоретической работы 3 . Можно сделать вывод, что H 2 S (D 2 S) твердый, скорее всего, разлагается под давлением по пути: 3H 2 S → 2H 3 S + S.
a , Раскатанное порошковое дифракционное изображение гидрида серы при 150 ГПа при комнатной температуре, записанное на фотопластинке. b , c , Интегральные рентгенограммы, полученные с вычитанием фона для гидрида серы ( b ) и дейтерида серы ( c ). Кривые ОЦК H 3 S и β -Po элементарной серы при 150 ГПа и 170 ГПа, рассчитанные согласно ссылкам 5, 26, показаны под экспериментально полученными диаграммами. Звездочками обозначены пики, не принадлежащие образцу, как следует из сканирования образца (дополнительный рис. 1): эти пики остаются неизменными, тогда как пики образца меняются с радиусом образца как по положению, так и по интенсивности. Незакрашенные кружки указывают на отражение от фазы IV высокого давления элементарной серы (несоразмерно модулированная объемно-центрированная моноклинная структура). d , Рентгенограммы дейтерида серы при 173 ГПа при 300 К и 13 К. Пики, отмеченные звездочками, не являются отражениями от образца. Результаты анализов показаны в дополнительной таблице 1.
Кривые ОЦК H 3 S и β -Po элементарной серы при 150 ГПа и 170 ГПа, рассчитанные согласно ссылкам 5, 26, показаны под экспериментально полученными диаграммами. Звездочками обозначены пики, не принадлежащие образцу, как следует из сканирования образца (дополнительный рис. 1): эти пики остаются неизменными, тогда как пики образца меняются с радиусом образца как по положению, так и по интенсивности. Незакрашенные кружки указывают на отражение от фазы IV высокого давления элементарной серы (несоразмерно модулированная объемно-центрированная моноклинная структура). d , Рентгенограммы дейтерида серы при 173 ГПа при 300 К и 13 К. Пики, отмеченные звездочками, не являются отражениями от образца. Результаты анализов показаны в дополнительной таблице 1.
Изображение в натуральную величину
Рисунок 2: Зависимость XRD от давления в образцах гидрида серы и дейтерида серы. a , b , рентгенограммы, полученные при комнатной температуре и различных давлениях для гидрида серы ( a ) и дейтерида серы ( b ). Верхние (красные) и нижние (зеленые) галочки указывают положения пиков предсказанной ОЦК-структуры H 3 S и β -Po элементарной серы соответственно. Пики, отмеченные звездочками, не принадлежат образцу, как следует из дополнительного рис. 1. При понижении давления в гидриде серы отчетливо наблюдается фазовый переход элементарной серы — пик от β -Po серы постепенно исчезает и что из фазы IV (незаштрихованный кружок) усиливается. с , Зависимость атомного объема гидрида серы и дейтерида серы от давления. Экспериментальные данные получены при увеличении давления и аппроксимируются уравнением состояния Берча первого порядка (черная сплошная линия). Объемы гексагональной ( R 3 м ) и ОЦК ( Im -3 м ) фаз, полученные из теоретической работы 3 , показаны в виде закрашенных квадратов и треугольников закрашенных соответственно, соединенных пунктирными линиями. Расчетные стандартные отклонения меньше размера символов.
Верхние (красные) и нижние (зеленые) галочки указывают положения пиков предсказанной ОЦК-структуры H 3 S и β -Po элементарной серы соответственно. Пики, отмеченные звездочками, не принадлежат образцу, как следует из дополнительного рис. 1. При понижении давления в гидриде серы отчетливо наблюдается фазовый переход элементарной серы — пик от β -Po серы постепенно исчезает и что из фазы IV (незаштрихованный кружок) усиливается. с , Зависимость атомного объема гидрида серы и дейтерида серы от давления. Экспериментальные данные получены при увеличении давления и аппроксимируются уравнением состояния Берча первого порядка (черная сплошная линия). Объемы гексагональной ( R 3 м ) и ОЦК ( Im -3 м ) фаз, полученные из теоретической работы 3 , показаны в виде закрашенных квадратов и треугольников закрашенных соответственно, соединенных пунктирными линиями. Расчетные стандартные отклонения меньше размера символов.
Изображение полного размера
Зависимость атомного объема V атм гидрида серы и дейтерида серы от давления показана на рис. 2c. Он соответствует уравнению состояния Берча первого порядка 27 с модулем объемного сжатия B 0 = 506 (30) ГПа и его производной по давлению B 0 ′ = 6 (фиксировано). Значение экспериментально наблюдаемого В атм немного больше, но сжимаемость хорошо согласуется с расчетом Дуана 3 . Зависимость от давления нормированного атомного объема V / V 0 элементарной серы в структуре β -Po показана на дополнительном рисунке 3. Она хорошо согласуется с экспериментальными данными исх. 26 при высоких давлениях P > 170 ГПа и с помощью наших расчетов теории функционала плотности (см. Методы).
Наши измерения рентгеновской дифракции порошка не позволяют нам различить предсказанные ОЦК структуры: Im -3 м и R 3 м . В этих структурах положения атомов серы одинаковы, а единственное отличие состоит в положении атомов водорода: атомы водорода расположены симметрично между соседними атомами серы в структуре Im -3 m и несколько асимметрично в Структура R 3 м (дополнительный рис. 2). Однако положение атомов водорода нельзя определить по измерениям порошка, поскольку атомы водорода являются чрезвычайно слабыми рассеивателями.
В этих структурах положения атомов серы одинаковы, а единственное отличие состоит в положении атомов водорода: атомы водорода расположены симметрично между соседними атомами серы в структуре Im -3 m и несколько асимметрично в Структура R 3 м (дополнительный рис. 2). Однако положение атомов водорода нельзя определить по измерениям порошка, поскольку атомы водорода являются чрезвычайно слабыми рассеивателями.
Низкотемпературные данные помогут в дальнейшем анализе. Мы одновременно измеряли XRD и электрическое сопротивление на той же установке 28 (рис. 3). Переход в сверхпроводящее состояние определялся по резкому падению сопротивления (рис. 3а, б). Мы обнаружили, что нормальное и сверхпроводящее состояние имеют одинаковую структуру, так как рентгенограммы одинаковы при комнатной и низких температурах (рис. 1г). При этом структура образца заметно не меняется в диапазоне давлений 92–173 ГПа. Это контрастирует с зависимостью критической температуры от давления, которая имеет ярко выраженный излом при 150 ГПа для H 3 S и 160 ГПа для D 3 S (рис. 3в). Этот излом находит естественное объяснение в теоретических предсказаниях 9,23 : зависимость критической температуры сверхпроводимости от давления различна в R 3 m фазе при более низких давлениях и в Im -3 m фазы при более высоких давлениях. Наши измерения XRD подтверждают эту интерпретацию, поскольку R 3 m и Im -3 m различаются только упорядочением атомов водорода, и одни и те же рентгенограммы должны быть одинаковыми в обеих областях давлений. Таким образом, можно сделать вывод, что самая высокая критическая температура 203 К (ссылка 2) соответствует фазе Im -3 m .
3в). Этот излом находит естественное объяснение в теоретических предсказаниях 9,23 : зависимость критической температуры сверхпроводимости от давления различна в R 3 m фазе при более низких давлениях и в Im -3 m фазы при более высоких давлениях. Наши измерения XRD подтверждают эту интерпретацию, поскольку R 3 m и Im -3 m различаются только упорядочением атомов водорода, и одни и те же рентгенограммы должны быть одинаковыми в обеих областях давлений. Таким образом, можно сделать вывод, что самая высокая критическая температура 203 К (ссылка 2) соответствует фазе Im -3 m .
a , b , Температурная зависимость сопротивления в гидриде серы (при уменьшении давления) ( a ) и дейтерид серы (при повышении давления) ( b ). c , Зависимость от давления критической температуры сверхпроводимости T c гидрида серы (черные точки) и дейтерида серы (красные точки). Открытые кружки и квадраты взяты из исх. 2. Точки, отмеченные заштрихованными символами, взяты из настоящей работы: кружки – данные о снижении давления, квадраты и треугольники – о повышении давления. Пунктирные линии (черная для гидрида серы и красная для дейтерида серы) указывают на фазовую границу между R 3 м и Im -3 м структурные фазы. Столбики погрешностей показывают разницу между начальной температурой T c и температурой нулевого сопротивления при каждом давлении в a и b .
c , Зависимость от давления критической температуры сверхпроводимости T c гидрида серы (черные точки) и дейтерида серы (красные точки). Открытые кружки и квадраты взяты из исх. 2. Точки, отмеченные заштрихованными символами, взяты из настоящей работы: кружки – данные о снижении давления, квадраты и треугольники – о повышении давления. Пунктирные линии (черная для гидрида серы и красная для дейтерида серы) указывают на фазовую границу между R 3 м и Im -3 м структурные фазы. Столбики погрешностей показывают разницу между начальной температурой T c и температурой нулевого сопротивления при каждом давлении в a и b .
Полноразмерное изображение
Методы
Образец и электрические зонды были подготовлены методом, аналогичным исх. 2. Измерения порошковой дифракции с угловой дисперсией проводились на SPring-8 (линия BL10XU) с монохроматическим пучком с энергией ∼30,0 кэВ ( λ ∼ 0,412–0,414 Å). XRD и электрическое сопротивление измеряли одновременно с помощью криостата 28 . Дифрактограммы записывали с помощью фотопластинки со временем экспозиции от 120 до 300 с. Четырехзондовые электрические измерения проводились с мостом сопротивления переменному току (Linear Research, LR-700). Мы определили зависимость давления от объема серы β -Po с помощью расчетов из первых принципов, основанных на теории функционала плотности. Квантовый ЭСПРЕССО код 29 использовалась для расчетов, в которых использовались приближение обобщенного градиента Пердью–Берка–Эрнзергофа 30 и ультрамягкий псевдопотенциал Вандербильта 31 . Интегрирование в пространстве k по зоне Бриллюэна проводилось на сетке 24 × 24 × 24, а пороговое значение энергии базиса плоской волны было установлено на уровне 80 Ry.
XRD и электрическое сопротивление измеряли одновременно с помощью криостата 28 . Дифрактограммы записывали с помощью фотопластинки со временем экспозиции от 120 до 300 с. Четырехзондовые электрические измерения проводились с мостом сопротивления переменному току (Linear Research, LR-700). Мы определили зависимость давления от объема серы β -Po с помощью расчетов из первых принципов, основанных на теории функционала плотности. Квантовый ЭСПРЕССО код 29 использовалась для расчетов, в которых использовались приближение обобщенного градиента Пердью–Берка–Эрнзергофа 30 и ультрамягкий псевдопотенциал Вандербильта 31 . Интегрирование в пространстве k по зоне Бриллюэна проводилось на сетке 24 × 24 × 24, а пороговое значение энергии базиса плоской волны было установлено на уровне 80 Ry.
Доступность данных.
Необработанные данные были получены на установке синхротронного излучения SPring-8 (линия луча BL10XU). Производные данные, подтверждающие результаты этого исследования, можно получить у соответствующего автора по запросу.
Производные данные, подтверждающие результаты этого исследования, можно получить у соответствующего автора по запросу.
Литература
Скачать ссылки
Благодарности
Работа выполнена по предложению № 2015A0112 SPring-8. Это исследование было поддержано Японским обществом содействия науке, грантом в помощь для специально продвигаемых исследований, № 26000006, JSPS KAKENHI, грантом для молодых ученых (B), № 15K17707 и Европейским исследовательским советом, 2010 г. -Расширенный грант 267777.
Информация об авторе
Примечания автора
Авторы и принадлежность
Авторы
Вклады
ME принимал участие во всех измерениях XRD, интерпретации данных и написании рукописи. РС. выполнены криогенные операции и сбор данных РФА. К.С. выполнил 90 119 на месте измерений электрического сопротивления в измерениях XRD и написал рукопись. Т.И. выполнены вспомогательные расчеты для интерпретации данных. M.I.E. разработал исследование и участвовал в экспериментах XRD и написании рукописи. А.П.Д. готовили образец в ячейке с алмазными наковальнями для всех экспериментов. И.А.Т. участвовал в создании рамановской установки. Н.Х. и Ю.О. выполнил оптимизацию синхротронных РФА и криогенных операций. М.Е., К.С. и M.I.E. в равной степени внесли свой вклад в эту статью.
Н.Х. и Ю.О. выполнил оптимизацию синхротронных РФА и криогенных операций. М.Е., К.С. и M.I.E. в равной степени внесли свой вклад в эту статью.
Автор, ответственный за переписку
Переписка с Мари Эйнага.
Декларации этики
Конкурирующие интересы
Авторы не заявляют о конкурирующих финансовых интересах.
Дополнительная информация
Дополнительная информация
Дополнительная информация (PDF 1031 kb)
Права и разрешения
Перепечатки и разрешения
Эта статья цитируется
0097
Скачать PDF
Сверхчувствительные датчики газа h3S на основе гибридных материалов p-типа WS2
Сверхчувствительный H 2 Датчики газа S на основе p-типа WS 2 Гибридные материалы
Скачать PDF
Скачать PDF
Нано исследования том 11 , страницы 4215–4224 (2018)Процитировать эту статью
Abstract
Ожидается, что наноструктурированные сульфиды металлов благодаря своей более высокой собственной электропроводности и химической стабильности по сравнению с их оксидными аналогами оживят материалы для резистивных химических сенсоров. В данном документе мы исследуем газочувствительные свойства гибридных материалов WS 2 нанопроволока-наночешуйки и демонстрируем их превосходную чувствительность (0,043 ppm -1 ), а также высокую селективность в отношении H 2 S по сравнению с CO, NH 3 , H 2 и NO (с соответствующими чувствительностью 0,002, 0,0074, 0,0002 и 0,0046 частей на миллион -1 соответственно). Измерения газового отклика, дополненные результатами анализа рентгеновской фотоэлектронной спектроскопии и расчетами из первых принципов, основанными на теории функционала плотности, позволяют предположить, что собственных электронных свойств исходного WS 2 недостаточно для объяснения наблюдаемой высокой чувствительности к H. 2 S. Большую роль в этом поведении также играет допирование O в S-позициях WS 2 решетка. Результаты настоящего исследования открывают новые возможности для использования наноматериалов на основе дисульфидов переходных металлов в качестве эффективных альтернатив оксидам металлов в будущих приложениях для управления промышленными процессами, безопасности, охраны здоровья и окружающей среды.
В данном документе мы исследуем газочувствительные свойства гибридных материалов WS 2 нанопроволока-наночешуйки и демонстрируем их превосходную чувствительность (0,043 ppm -1 ), а также высокую селективность в отношении H 2 S по сравнению с CO, NH 3 , H 2 и NO (с соответствующими чувствительностью 0,002, 0,0074, 0,0002 и 0,0046 частей на миллион -1 соответственно). Измерения газового отклика, дополненные результатами анализа рентгеновской фотоэлектронной спектроскопии и расчетами из первых принципов, основанными на теории функционала плотности, позволяют предположить, что собственных электронных свойств исходного WS 2 недостаточно для объяснения наблюдаемой высокой чувствительности к H. 2 S. Большую роль в этом поведении также играет допирование O в S-позициях WS 2 решетка. Результаты настоящего исследования открывают новые возможности для использования наноматериалов на основе дисульфидов переходных металлов в качестве эффективных альтернатив оксидам металлов в будущих приложениях для управления промышленными процессами, безопасности, охраны здоровья и окружающей среды.
Скачайте, чтобы прочитать полный текст статьи
Ссылки
Скачать ссылки
Благодарности
Финансирование получено от программы Bio4Energy, Академии Финляндии (проекты Suplacat и ClintoxNP (№ 268944)), Университета Оулу (исследовательское сообщество More than Moore) и Высшей школы Университета Оулу (Infotech Оулу) признается. Мы признаем поддержку со стороны ЕС (№ ERC-2016-AdG-694097 QSpec-NewMat) и правительство Басков «Grupos Consolidados UPV/EHU» (№ IT578-13). J. J. B. и L. D. X. благодарят ЕС за стипендию Марии Кюри (№ h3020-MSCA-IF-2016-751047 и h3020-MSCA-IF-2015-709382). A. P. P. благодарит постдокторскую стипендию испанской программы «Juan de la Cierva-incorporación» (№ IJCI-2014-20147). Мы также хотели бы поблагодарить Сами Саукко (Центр микроскопии и нанотехнологий Университета Оулу) за помощь в проведении ПЭМ-анализа. ALS признает область стратегических исследований правительства Швеции в области материаловедения функциональных материалов в Университете Линчёпинга (факультетский грант SFO-Mat-LiU № 2009).-00971).
Мы также хотели бы поблагодарить Сами Саукко (Центр микроскопии и нанотехнологий Университета Оулу) за помощь в проведении ПЭМ-анализа. ALS признает область стратегических исследований правительства Швеции в области материаловедения функциональных материалов в Университете Линчёпинга (факультетский грант SFO-Mat-LiU № 2009).-00971).
Информация об авторе
Авторы и организации
3 Химический факультет Химическая инженерия, Центр технологической химии им. Йохана Гадолина, Университет Або Академи, FI-20500, Або-Турку, Финляндия
Юри-Пекка Миккола
Авторы
Авторы, переписывающиеся
Переписка с
Анхель Рубио или Кристиан Кордас.

 Связь ионная.
Связь ионная. Это № 1 – S. Они между собой образуют h3S. Оба неметаллы, с небольшой разницей в электроотрицательности.
Это № 1 – S. Они между собой образуют h3S. Оба неметаллы, с небольшой разницей в электроотрицательности.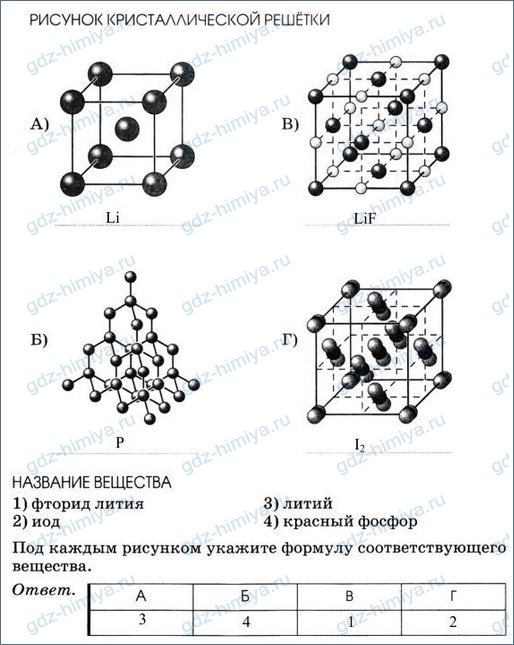 Три из них образованы по обменному механизму, одна – по донорно-акцепторному.
Три из них образованы по обменному механизму, одна – по донорно-акцепторному. Значит, кристаллическая решетка не может быть ионной, металлической или молекулярной.
Значит, кристаллическая решетка не может быть ионной, металлической или молекулярной.
 edu.ru» (Источник)
edu.ru» (Источник)
Leave A Comment