Гликолиз — это… Что такое Гликолиз?
 Схема гликолиза
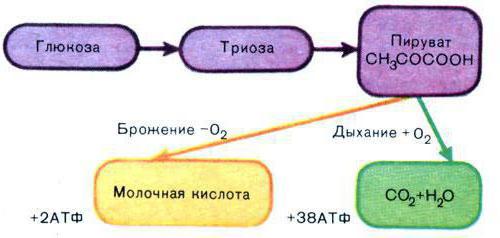
Схема гликолизаГлико́лиз (фосфотриозный путь, или шунт Эмбдена — Мейерхофа, или путь Эмбдена-Мейергофа-Парнаса ) — ферментативный процесс последовательного расщепления глюкозы в клетках, сопровождающийся синтезом АТФ. Гликолиз при аэробных условиях ведёт к образованию пировиноградной кислоты (пирувата), гликолиз в анаэробных условиях ведёт к образованию молочной кислоты (лактата). Гликолиз является основным путём катаболизма глюкозы в организме животных.
Название «гликолиз» происходит от греч. γλυκός, glykos — сладкий и греч. λύσης, lysis — растворение.
Общий обзор
Гликолитический путь представляет собой 10 последовательных реакций, каждая из которых катализируется отдельным ферментом.
Процесс гликолиза условно можно разделить на два этапа. Первый этап, протекающий с расходом энергии 2-х молекул АТФ, заключается в расщеплении молекулы глюкозы на 2 молекулы глицеральдегид-3-фосфата. На втором этапе происходит НАД-зависимое окисление глицеральдегид-3-фосфата, сопровождающееся синтезом АТФ. Сам по себе гликолиз является полностью анаэробным процессом, то есть не требует для протекания реакций присутствия кислорода.
Гликолиз — один из древнейших метаболических процессов, известный почти у всех живых организмов. Предположительно гликолиз появился более 3,5 млрд лет назад у первичных прокариотов.
Локализация
В клетках эукариотических организмов десять ферментов, катализирующих распад глюкозы до ПВК, находятся в цитозоле, все остальные ферменты, имеющие отношение к энергетическому обмену, — в митохондриях и хлоропластах. Поступление глюкозы в клетку осуществляется двумя путями: натрий-зависимый симпорт (преимущественно для энтероцитов и эпителия почечных канальцев) и облегчённая диффузия глюкозы с помощью белков-переносчиков. Работа этих белков-транспортёров контролируется гормонами и, в первую очередь, инсулином. Сильнее всего инсулин стимулирует транспорт глюкозы в мышцах и жировой ткани.
Результат
Результатом гликолиза является превращение одной молекулы глюкозы в две молекулы пировиноградной кислоты (ПВК) и образование двух восстановительных эквивалентов в виде кофермента НАД∙H.
Полное уравнение гликолиза имеет вид:
- Глюкоза + 2НАД+ + 2АДФ + 2Фн = 2НАД∙Н + 2ПВК + 2АТФ + 2H2O + 2Н
При отсутствии или недостатке в клетке кислорода пировиноградная кислота подвергается восстановлению до молочной кислоты, тогда общее уравнение гликолиза будет таким:
- Глюкоза + 2АДФ + 2Фн = 2лактат + 2АТФ + 2H2O.
Таким образом, при анаэробном расщеплении одной молекулы глюкозы суммарный чистый выход АТФ составляет две молекулы, полученные в реакциях субстратного фосфорилирования АДФ.
У аэробных организмов конечные продукты гликолиза подвергаются дальнейшим превращениям в биохимических циклах, относящихся к клеточному дыханию. В итоге после полного окисления всех метаболитов одной молекулы глюкозы на последнем этапе клеточного дыхания — окислительном фосфорилировании, происходящем на митохондриальной дыхательной цепи в присутствии кислорода, — дополнительно синтезируются ещё 34 или 36 молекулы АТФ на каждую молекулу глюкозы.
Путь
Первой реакцией гликолиза является фосфорилирование молекулы глюкозы, происходящее при участии тканеспецифичного фермента гексокиназы с затратой энергии 1 молекулы АТФ; образуется активная форма глюкозы — глюкозо-6-фосфат (Г-6-Ф):
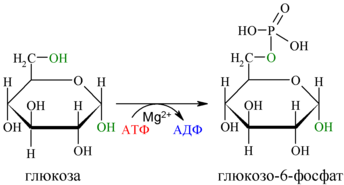
Для протекания реакции необходимо наличие в среде ионов Mg
Фосфорилирование глюкозы преследует две цели: во-первых, из-за того что плазматическая мембрана, проницаемая для нейтральной молекулы глюкозы, не пропускает отрицательно заряженные молекулы Г-6-Ф, фосфорилированная глюкоза оказывается запертой внутри клетки. Во-вторых, при фосфорилировании глюкоза переводится в активную форму, способную участвовать в биохимических реакциях и включаться в метаболические циклы.
Печёночный изофермент гексокиназы — глюкокиназа — имеет важное значение в регуляции уровня глюкозы в крови.
В следующей реакции (2) ферментом фосфоглюкоизомеразой Г-6-Ф превращается во
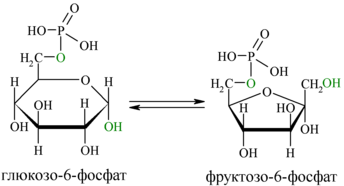
Энергия для этой реакции не требуется, и реакция является полностью обратимой. На данном этапе в процесс гликолиза может также включаться путём фосфорилирования и фруктоза.
Далее почти сразу друг за другом следуют две реакции: необратимое фосфорилирование фруктозо-6-фосфата (3) и обратимое альдольное расщепление образовавшегося фруктозо-1,6-бифосфата (Ф-1,6-бФ) на две триозы (4).
Фосфорилирование Ф-6-Ф осуществляется фосфофруктокиназой с затратой энергии ещё одной молекулы АТФ; это вторая
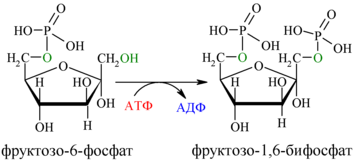
Альдольное расщепление Ф-1,6-бФ происходит под действием альдолазы фруктозо-1,6-бифосфата:
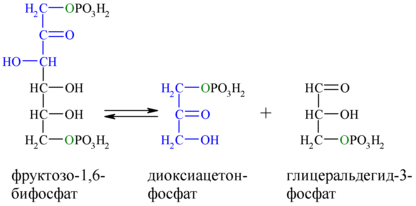
В результате четвёртой реакции образуются дигидроксиацетонфосфат и глицеральдегид-3-фосфат, причём первый почти сразу под действием фосфотриозоизомеразы переходит во второй (
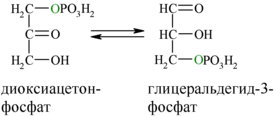
Каждая молекула глицеральдегидфосфата окисляется НАД+ в присутствии дегидрогеназы глицеральдегидфосфата до 1,3-дифосфоглицерата (6):
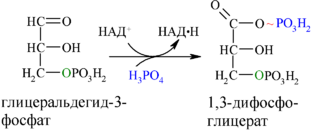
Далее с 1,3-дифосфоглицерата, содержащего макроэргическую связь в 1 положении, ферментом фосфоглицераткиназой на молекулу АДФ переносится остаток фосфорной кислоты (реакция 7) — образуется молекула АТФ:
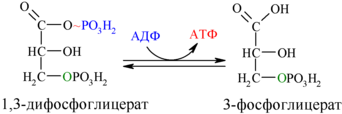
Это первая реакция субстратного фосфорилирования. С этого момента процесс расщепления глюкозы перестаёт быть убыточным в энергетическом плане, так как энергетические затраты первого этапа оказываются компенсированными: синтезируются 2 молекулы АТФ (по одной на каждый 1,3-дифосфоглицерат) вместо двух потраченных в реакциях 1 и 3. Для протекания данной реакции требуется присутствие в цитозоле АДФ, то есть при избытке в клетке АТФ (и недостатке АДФ) её скорость снижается. Поскольку АТФ, не подвергающийся метаболизму, в клетке не депонируется а просто разрушается, то эта реакция является важным регулятором гликолиза.
Затем последовательно: фосфоглицеролмутаза образует 2-фосфоглицерат (8):
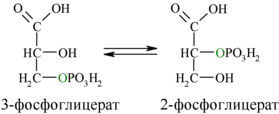
Енолаза образует фосфоенолпируват (9):
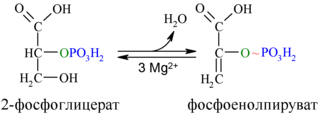
И наконец происходит вторая реакция субстратного фосфорилирования АДФ с образованием енольной формы пирувата и АТФ (10):
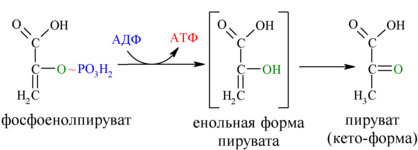
Реакция протекает под действием пируваткиназы. Это последняя ключевая реакция гликолиза. Изомеризация енольной формы пирувата в пируват происходит неферментативно.
С момента образования Ф-1,6-бФ с выделением энергии протекают только реакции 7 и 10, в которых и происходит к субстратное фосфорилирование АДФ.
Дальнейшее развитие
Окончательная судьба пирувата и НАД∙H, образованных в процессе гликолиза зависит от организма и условий внутри клетки, в особенности от наличия или отсутствия кислорода или других акцепторов электронов.
У анаэробных организмов пируват и НАД∙H далее подвергаются брожению. При молочнокислом брожении, например, у бактерий пируват под действием фермента лактатдегидрогеназы восстанавливается в молочную кислоту. У дрожжей сходным процессом является спиртовое брожение, где конечными продуктами будут этанол и углекислый газ. Известно также маслянокислое и лимоннокислое брожение.
Маслянокислое брожение:
- глюкоза → масляная кислота + 2 CO2 + 2 H2O.
Спиртовое брожение:
- глюкоза → 2 этанол + 2 CO2.
Лимоннокислое брожение:
- глюкоза → лимонная кислота + 2 H2O.
Брожение имеет важное значение в пищевой промышленности.
У аэробов пируват как правило попадает в цикл трикарбоновых кислот (цикл Кребса), а НАД∙H в итоге окисляется кислородом на дыхательной цепи в митохондриях в процессе окислительного фосфорилирования.
Несмотря на то, что метаболизм человека преимущественно аэробный, в интенсивно работающих скелетных мышцах наблюдается анаэробное окисление. В условиях ограниченного доступа кислорода пируват превращается в молочную кислоту, как происходит при молочнокислом брожении у многих микроорганизмов:
- ПВК + НАД∙Н + H+ → лактат + НАД+.
Боли в мышцах, возникающие через некоторое время после непривычной интенсивной физической нагрузки, связаны с накоплением в них молочной кислоты.
Образование молочной кислоты является тупиковой ветвью метаболизма, но не является конечным продуктом обмена веществ. Под действием лактатдегидрогеназы молочная кислота окисляется снова, образуя пируват, который и участвует в дальнейших превращениях.
Регуляция гликолиза
Различают местную и общую регуляцию.
Местная регуляция осуществляется путём изменения активности ферментов под действием различных метаболитов внутри клетки.
Регуляция гликолиза в целом, сразу для всего организма, происходит под действием гормонов, которые, влияя через молекулы вторичных посредников, изменяют внутриклеточный метаболизм.
Важное значение в стимуляции гликолиза принадлежит инсулину. Глюкагон и адреналин являются наиболее значимыми гормональными ингибиторами гликолиза.
Инсулин стимулирует гликолиз через:
- активацию гексокиназной реакции;
- стимуляцию фосфофруктокиназы;
- стимуляцию пируваткиназы.
Также на гликолиз влияют и другие гормоны. Например, соматотропин ингибирует ферменты гликолиза, а тиреоидные гормоны являются стимуляторами.
Регуляция гликолиза осуществляется через несколько ключевых этапов. Реакции, катализируемые гексокиназой (1), фосфофруктокиназой (3) и пируваткиназой (10) отличаются существенным уменьшением свободной энергии и являются практически необратимыми, что позволяет им быть эффективными точками регуляции гликолиза.
Регуляция гексокиназы
Гексокиназа ингибируется продуктом реакции — глюкозо-6-фосфатом, который аллостерически связывается с ферментом, изменяя его активность.
По причине того, что основная масса Г-6-Ф в клетке производится путём расщепления гликогена, гексокиназная реакция, по сути, для протекания гликолиза не является необходимой, и фосфорилирования глюкозы в регуляции гликолиза исключительной важности не имеет. Гексокиназная реакция является важным этапом регуляции концентрации глюкозы в крови и в клетке.
При фосфорилировании глюкоза теряет способность транспортироваться через мембрану молекулами-переносчиками, что создаёт условия для накопления её в клетке. Ингибирование гексокиназы Г-6-Ф ограничивает поступление глюкозы в клетку, предотвращая её чрезмерное накопление.
Глюкокиназа (IV изотип гексокиназы) печени не ингибируется глюкозо-6-фосфатом, и клетки печени продолжают накапливать глюкозу даже при высоком содержании Г-6-Ф, из которого в дальнейшем синтезируется гликоген. По сравнению с другими изотипами глюкокиназа отличается высоким значением константы Михаэлиса, то есть на полную мощность фермент работает только в условиях высокой концентрации глюкозы, которая бывает почти всегда после приёма пищи.
Глюкозо-6-фосфат может превращаться обратно в глюкозу при действии глюкозо-6-фосфатазы. Ферменты глюкокиназа и глюкозо-6-фосфатаза участвуют в поддержании нормальной концентрации глюкозы в крови.
Регуляция фосфофруктокиназы
Интенсивность протекания фосфофруктокиназной реакции решающим образом сказывается на всей пропускной способности гликолиза, а стимуляция фосфофруктокиназы считается наиболее важным этапом регуляции.
Фосфофруктокиназа (ФФК) — это тетрамерный фермент, существующий поочерёдно в двух конформационных состояниях (R и T), которые находятся в равновесии и попеременно переходят из одного в другое. АТФ является одновременно и субстратом, и аллостерическим ингибитором ФФК.
В каждой из субъединиц ФФК имеется по два центра связывания АТФ: субстратный сайт и сайт ингибирования. Субстратный сайт одинаково способен присоединять АТФ при любой конформации тетрамера. В то время как сайт ингибирования связывает АТФ исключительно, когда фермент находится в конформационном состоянии T. Другим субстратом ФФК является фруктозо-6-фосфат, который присоединяется к ферменту предпочтительно в R-состоянии. При высокой концентрации АТФ сайт ингибирования занимается, переходы между конформациями фермента становятся невозможными, и большинство молекул фермента оказываются стабилизированными в T-состоянии, неспособном присоединить Ф-6-Ф. Однако ингибирование фосфофруктокиназы АТФ подавляется АМФ, который присоединяется к R-конформациям фермента, стабилизируя таким образом состояние фермента для связывания Ф-6-Ф.
Наиболее важным же аллостерическим регулятором гликолиза и глюконеогенеза является фруктозо-2,6-бифосфат, который не является промежуточным звеном этих циклов. Фруктозо-2,6-бифосфат аллостерически активирует фосфофруктокиназу.
Синтез фруктозо-2,6-бифосфата катализируется особым бифункциональным ферментом — фосфофруктокиназой-2/фруктозо-2,6-бифосфатазой (ФФК-2/Ф-2,6-БФаза). В нефосфорилированной форме белок известен как фосфофруктокиназа-2 и имеет каталитическую активность по отношению к фруктозо-6-фосфату, синтезируя фруктозо-2-6-бифосфат. В результате чего значительно стимулируется активность ФФК и сильно ингибируется активность фруктозо-1,6-бифосфатазы. То есть при условии активности ФФК-2 равновесие этой реакции между гликолизом и глюконеогенезом смещается в сторону первого — синтезируется фруктозо-1,6-бифосфат.
В фосфорилированном виде бифункциональный фермент не обладает киназной активностью, а наоборот в его молекуле активируется сайт, который гидролизует Ф2,6БФ на Ф6Ф и неорганический фосфат. Метаболический эффект фосфорилирования бифункционального фермента состоит в том, что аллостерическая стимуляция ФФК прекращается, аллостерическое ингибирование Ф-1,6-БФазы ликвидируется и равновесие смещается в сторону глюконеогенеза. Продуцируется Ф6Ф и затем — глюкоза.
Взаимопревращения бифункционального фермента осуществляются цАМФ-зависимой протеинкиназой (ПК), которая в свою очередь регулируется циркулирующими в крови пептидными гормонами.
Когда в крови снижается концентрация глюкозы, тормозится также и образование инсулина, а выделение глюкагона напротив стимулируется, и его концентрация в крови резко повышается. Глюкагон (и другие контринсулярные гормоны) связываются с рецепторами плазматической мембраны клеток печени, вызывая активацию мембранной аденилатциклазы. Аденилатциклаза катализирует превращение АТФ в циклический АМФ. цАМФ связывается с регуляторной субъединицей протеинкиназы, вызывая высвобождение и активизацию её каталитических субъединиц, которые фосфорилирует ряд ферментов, включая и бифункциональную ФФК-2/Ф-2,6-БФазу. При этом в печени прекращается потребление глюкозы и активизируются глюконеогенез и гликогенолиз, восстанавливая нормогликемию.
Пируваткиназа
Следующим шагом, где осуществляется регуляция гликолиза, является последняя реакция — этап действия пируваткиназы. Для пируваткиназы также описан ряд изоферментов, имеющих особенности регуляции.
Печёночная пируваткиназа (L-тип) регулируется при фосфорилировании, аллстерическими эффекторами и путём регуляции экспрессии генов. Фермент ингибируется АТФ и ацетил-КоА и активируется фруктозо-1,6-бифосфатом. Ингибирование пируваткиназы АТФ происходит подобно действию АТФ на ФФК. Связывание АТФ с сайтом ингибирования фермента уменьшает его сродство к фосфоенолпирувату. Печёночная пируваткиназа фосфорилируется и ингибируется протеинкиназой, и таким образом также находится под гормональным контролем. Кроме того, активность печёночной пируваткиназы регулируется и количественно, то есть изменением уровня его синтеза. Это медленная, долговременная регуляция. Увеличение в рационе углеводов стимулирует экспрессию генов, кодирующих пируваткиназу, в результате уровень фермента в клетке повышается.
М-тип пируваткиназы, найденный в головном мозге, мышцах и других глюкозо-потребных тканях не регулируется протеинкиназой. Это принципиально в том, что метаболизм этих тканей определяется только внутренними потребностями и не зависит от уровня глюкозы в крови.
Мышечная пируваткиназа не подвержена внешним влияниям, таким как понижение уровня глюкозы в крови или выброс гормонов. Внеклеточные условия, которые приводят к фосфорилированию и ингибированию печёночного изофермента, не изменяют активность пируваткиназы М-типа. То есть интенсивность гликолиза в поперечнополосатой мускулатуре определяется только условиями внутри клетки и не зависит от общей регуляции.
Значение
Гликолиз — катаболический путь исключительной важности. Он обеспечивает энергией клеточные реакции, в том числе и синтез белка. Промежуточные продукты гликолиза используются при синтезе жиров. Пируват также может быть использован для синтеза аланина, аспартата и других соединений. Благодаря гликолизу производительность митохондрий и доступность кислорода не ограничивают мощность мышц при кратковременных предельных нагрузках.
См. также
Ссылки
ГЛИКОЛИЗ. «БИОЛОГИЧЕСКАЯ ХИМИЯ», Березов Т.Т., Коровкин Б.Ф.
Гликолиз (от греч. glycys – сладкий и lysis – растворение, распад) – это последовательность ферментативных реакций, приводящих к превращению глюкозы в пируват с одновременным образованием АТФ.
При аэробных условиях пируват проникает в митохондрии, где полностью окисляется до СО2 и Н2О. Если содержание кислорода недостаточно, как это может иметь место в активно сокращающейся мышце, пируват превращается в лактат.
Итак, гликолиз – не только главный путь утилизации глюкозы в клетках, но и уникальный путь, поскольку он может использовать кислород, если
последний доступен (аэробные условия), но может протекать и в отсутствие кислорода (анаэробные условия).
Анаэробный гликолиз – сложный ферментативный процесс распада глюкозы, протекающий в тканях человека и животных без потребления кислорода. Конечным продуктом гликолиза является молочная кислота. В процессе гликолиза образуется АТФ. Суммарное уравнение гликолиза можно представить следующим образом:
В анаэробных условиях гликолиз – единственный процесс в животном организме, поставляющий энергию. Именно благодаря гликолизу организм человека и животных определенный период может осуществлять ряд физиологических функций в условиях недостаточности кислорода. В тех случаях, когда гликолиз протекает в присутствии кислорода, говорят об аэробном гликолизе .
Последовательность реакций анаэробного гликолиза, так же как и их промежуточные продукты, хорошо изучена. Процесс гликолиза катализируется одиннадцатью ферментами, большинство из которых выделено в гомогенном, клисталлическом или высокоочищенном виде и свойства которых достаточно известны. Заметим, что гликолиз протекает в гиало-плазме (цитозоле) клетки.
Первой ферментативной реакцией гликолиза является фосфорилирование, т.е. перенос остатка ортофосфата на глюкозу за счет АТФ. Реакция катализируется ферментом гексокиназой:
Образование глюкозо-6-фосфата в гексокиназной реакции сопровождается освобождением значительного количества свободной энергии системы и может считаться практически необратимым процессом.
Наиболее важным свойством гексокиназы является ее ингибирование глюкозо-6-фосфатом, т.е. последний служит одновременно и продуктом реакции, и аллостерическим ингибитором.
Фермент гексокиназа способен катализировать фосфорилирование не только D-глюкозы, но и других гексоз, в частности D-фруктозы, D-маннозы и т.д. В печени, кроме гексокиназы, существует фермент глюкокиназа, который катализирует фосфорилирование только D-глюкозы. В мышечной ткани этот фермент отсутствует (подробнее см. главу 16).
Второй реакцией гликолиза является превращение глюкозо-6-фос-фата под действием фермента глюкозо-6-фосфатизомеразы во фруктозо-6-фосфат:
Эта реакция протекает легко в обоих направлениях, и для нее не требуется каких-либо кофакторов.
Третья реакция катализируется ферментом фосфофруктокиназой; образовавшийся фруктозо-6-фосфат вновь фосфорилируется за счет второй молекулы АТФ:
Данная реакция аналогично гексокиназной практически необратима, протекает в присутствии ионов магния и является наиболее медленно текущей реакцией гликолиза. Фактически эта реакция определяет скорость гликолиза в целом.
Фосфофруктокиназа относится к числу аллостерических ферментов. Она ингибируется АТФ и стимулируется АМФ . При значительных величинах отношения АТФ/АМФ активность фосфофруктокиназы угнетается и гликолиз замедляется. Напротив, при снижении этого коэффициента интенсивность гликолиза повышается. Так, в неработающей мышце активность фосфофруктокиназы низкая, а концентрация АТФ относительно высокая. Во время работы мышцы происходит интенсивное потребление АТФ и активность фосфофруктокиназы повышается, что приводит к усилению процесса гликолиза.
Четвертую реакцию гликолиза катализирует фермент альдолаза. Под влиянием этого фермента фруктозо-1,6-бисфосфат расщепляется на две фосфотриозы:
Эта реакция обратима. В зависимости от температуры равновесие устанавливается на различном уровне. При повышении температуры реакция сдвигается в сторону большего образования триозофосфатов (дигидро-ксиацетонфосфата и глицеральдегид-3-фосфата).
Пятая реакция – это реакция изомеризации триозофосфатов. Катализируется ферментом триозофосфатизомеразой:
Равновесие данной изомеразной реакции сдвинуто в сторону дигид-роксиацетонфосфата: 95% дигидроксиацетонфосфата и около 5% глице-ральдегид-3-фосфата. В последующие реакции гликолиза может непосредственно включаться только один из двух образующихся триозофосфатов, а именно глицеральдегид-3-фосфат. Вследствие этого по мере потребления в ходе дальнейших превращений альдегидной формы фосфотриозы ди-гидроксиацетонфосфат превращается в глицеральдегид-3-фосфат.
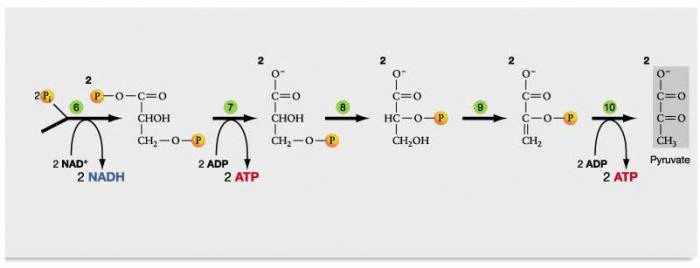
Образованием глицеральдегид-3-фосфата как бы завершается первая стадия гликолиза. Вторая стадия – наиболее сложная и важная. Она включает окислительно-восстановительную реакцию (реакция гликолитической оксидоредукции), сопряженную с субстратным фосфорилированием, в процессе которого образуется АТФ.
В результате шестой реакции глицеральдегид-3-фосфат в присутствии фермента глицеральдегидфосфатдегидрогеназы, кофермента НАД и неорганического фосфата подвергается своеобразному окислению с образованием 1,3-бисфосфоглицериновой кислоты и восстановленной формы НАД (НАДН). Эта реакция блокируется йод- или бромацетатом, протекает в несколько этапов:
1,3-Бисфосфоглицерат представляет собой высокоэнергетическое соединение (макроэргическая связь условно обозначена знаком «тильда» ~). Механизм действия глицеральдегидфосфатдегидрогеназы сводится к следующему: в присутствии неорганического фосфата НАД+ выступает как акцептор водорода, отщепляющегося от глицеральдегид-3-фосфата. В процессе образования НАДН глицеральдегид-3-фосфат связывается с молекулой фермента за счет SH-групп последнего. Образовавшаяся связь богата энергией, но она непрочная и расщепляется под влиянием неорганического фосфата, при этом образуется 1,3-бисфосфоглицериновая кислота.
Седьмая реакция катализируется фосфоглицераткиназой, при этом происходит передача богатого энергией фосфатного остатка (фосфатной группы в положении 1) на АДФ с образованием АТФ и 3-фосфогли-цериновой кислоты (3-фосфоглицерат):
Таким образом, благодаря действию двух ферментов (глицеральде-гидфосфатдегидрогеназы и фосфоглицераткиназы) энергия, высвобождающаяся при окислении альдегидной группы глицеральдегид-3-фосфата до карбоксильной группы, запасается в форме энергии АТФ. В отличие от окислительного фосфорилирования образование АТФ из высокоэнергетических соединений называется субстратным фосфорилированием.
Восьмая реакция сопровождается внутримолекулярным переносом оставшейся фосфатной группы, и 3-фосфоглицериновая кислота превращается в 2-фосфоглицериновую кислоту (2-фосфоглицерат).
Реакция легкообратима, протекает в присутствии ионов Mg2+. Кофактором фермента является также 2,3-бисфосфоглицериновая кислота аналогично тому, как в фосфоглюкомутазной реакции роль кофактора выполняет глюкозо-1,6-бисфосфат:
Девятая реакция катализируется ферментом енолазой, при этом 2-фосфоглицериновая кислота в результате отщепления молекулы воды переходит в фосфоенолпировиноградную кислоту (фосфоенолпируват), а фосфатная связь в положении 2 становится высокоэргической:
Енолаза активируется двухвалентными катионами Mg2+или Мn2+ и ингибируется фторидом.
Десятая реакция характеризуется разрывом высокоэргической связи и переносом фосфатного остатка от фосфоенолпирувата на АДФ (субстратное фосфорилирование). Катализируется ферментом пируваткиназой:
Для действия пируваткиназы необходимы ионы Mg2+, а также одновалентные катионы щелочных металлов (К+ или др.). Внутри клетки реакция является практически необратимой.
В результате одиннадцатой реакции происходит восстановление пировиноградной кислоты и образуется молочная кислота. Реакция протекает при участии фермента лактатдегидрогеназы и кофермента НАДН, образовавшегося в шестой реакции:
Последовательность протекающих при гликолизе реакций представлена на рис. 10.3.
Рис. 10.3. Последовательность реакций гликолиза.
1 - гексокиназа; 2 — фосфоглюкоизоме-раза; 3 — фосфофруктокиназа; 4 — альдо-лаза; 5 — триозофосфатизомераза; 6 — гли-церальдегидфосфатдегидрогеназа; 7 -фосфоглицераткиназа; 8 — фосфоглицеромутаза; 9 — енолаза; 10 - пируватки-наза; 11 - лактатдегидрогеназа.
Реакция восстановления пирувата завершает внутренний окислительно-восстановительный цикл гликолиза. НАД+ при этом играет роль промежуточного переносчика водорода от глицеральдегид-3-фосфата (6-я реакция) на пировиноградную кислоту (11-я реакция), при этом сам он регенерируется и вновь может участвовать в циклическом процессе, получившем название гликолитический оксидоредукции.
Биологическое значение процесса гликолиза заключается прежде всего в образовании богатых энергией фосфорных соединений. На первых стадиях гликолиза затрачиваются 2 молекулы АТФ (гексокиназная и фосфофрук-токиназная реакции). На последующих образуются 4 молекулы АТФ (фосфоглицераткиназная и пируваткиназная реакции). Таким образом, энергетическая эффективность гликолиза в анаэробных условиях составляет 2 молекулы АТФ на одну молекулу глюкозы.
Как отмечалось, основной реакцией, лимитирующей скорость гликолиза, является фосфофруктокиназная. Вторая реакция, лимитирующая скорость и регулирующая гликолиз – гексокиназная реакция. Кроме того, контроль гликолиза осуществляется также ЛДГ и ее изоферментами.
В тканях с аэробным метаболизмом (ткани сердца, почек и др.) преобладают изоферменты ЛДГ1 и ЛДГ2 (см. главу 4). Эти изоферменты инги-бируются даже небольшими концентрациями пирувата, что препятствует образованию молочной кислоты и способствует более полному окислению пирувата (точнее, ацетил-КоА) в цикле трикарбоновых кислот.
В тканях человека, в значительной степени использующих энергию гликолиза (например, скелетные мышцы), главными изоферментами являются ЛДГ5 и ЛДГ4. Активность ЛДГ5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ1. Преобладание изоферментов ЛДГ4 и ЛДГ5 обусловливает интенсивный анаэробный гликолиз с быстрым превращением пирувата в молочную кислоту.
Как отмечалось, процесс анаэробного распада гликогена получил название гликогенолиза. Вовлечение D-глюкозных единиц гликогена в процесс гликолиза происходит при участии 2 ферментов – фосфорилазы а и фосфо-глюкомутазы. Образовавшийся в результате фосфоглюкомутазной реакции глюкозо-6-фосфат может включаться в процесс гликолиза. После образования глюкозо-6-фосфата дальнейшие пути гликолиза и гликогенолиза полностью совпадают:
В процессе гликогенолиза в виде макроэргических соединений накапливаются не две, а три молекулы АТФ (АТФ не тратится на образование глюкозо-6-фосфата). Кажется, что энергетическая эффективность глико-генолиза выглядит несколько более высокой по сравнению с процессом гликолиза, но эта эффективность реализуется только при наличии активной фосфорилазы а. Следует иметь в виду, что в процессе активации фосфо-рилазы b расходуется АТФ (см. рис. 10.2).
Предыдущая страница | Следующая страница
СОДЕРЖАНИЕ
Еще по теме:Гликолиз — SportWiki энциклопедия
Гликолиз – процесс распада одной молекулы глюкозы с выделением энергии, достаточной для «зарядки» двух молекул АТФ, протекает в саркоплазме под воздействием 10 специальных ферментов.
C6H12O6 + 2H3PO4 + 2АДФ = 2C3H6O3 + 2АТФ + 2H2O.
Гликолиз может протекать без потребления кислорода (такие процессы называются анаэробными) и с потреблением кислорода (аэробный гликолиз) способен быстро восстанавливать запасы АТФ в мышце.
При занятиях бодибилдингом и высокоинтенсивных упражнениях происходит анаэробный гликолиз, с образованием молочной кислоты.
Во время динамических нагрузок, таких как бег, плавание и т.п., происходит аэробный гликолиз.
Аэробный гликолиз происходит в митохондриях под воздействием специальных ферментов и требует затрат кислорода, а соответственно и времени на его доставку. Окисление происходит в несколько этапов, сначала идет гликолиз, но образовавшиеся в ходе промежуточного этапа этой реакции две молекулы пирувата не преобразуются в молекулы молочной кислоты, а проникают в митохондрии, где окисляются в цикле Кребса до углекислого газа СО2 и воды Н2О и дают энергию для производства еще 38 молекул АТФ. Суммарное уравнение реакции окисления глюкозы выглядит так:
C6H12O6 + 6O2 + 38АДФ + 38H3PO4 = 6CO2 + 44H2O + 38АТФ
Распад глюкозы по аэробному пути (аэробный гликолиз) дает энергию для восстановления 38 молекул АТФ. Аэробное окисление в 19 раз эффективнее анаэробного гликолиза.
Подробное описание в статье: Энергообеспечение мышечной деятельности
Анаэробный гликолиз глюкозы в эритроцитах, 2,3-БФГ и эффект Бора[править | править код]
Рис. 18.1. Анаэробный гликолиз в эритроцитах Рис. 18.2. Образование 2,3-бисфосфоглицерата в эритроцитахЭритроциты транспортируют большое количество кислорода, которым снабжают все органы человека. По иронии судьбы сами они не могут использовать этот кислород. Источником энергии для эритроцитов служит глюкоза, при окислении которой в ходе анаэробного гликолиза в эритроцитах образуется АТФ (рис. 18.1). Аэробное окисление глюкозы в эритроцитах невозможно, так как в них отсутствуют митохондрии и вместе с ними все ферменты цикла Кребса. Кроме того, в них отсутствуют также ферменты, необходимые для окисления жирных кислот и использования кетоновых тел.
Функция эритроцитов — транспорт кислорода ко всем органам и тканям организма. Гемоглобин эритроцитов прочно связывается с кислородом, образуя оксигемоглобин. Однако в периферических тканях эритроциты должны отдать этот кислород другим клеткам. Это осуществляется благодаря явлению, известному под названием эффекта Бора. Эффект Бора создается благодаря двум факторам: протонам и 2,3-бисфосфоглицерату (рис. 18.2).
- Протоны вытесняют кислород из оксигемоглобина
Работающим мышцам необходим АТФ, и поэтому в них интенсивно функционирует цикл Кребса. В цикле Кребса образуется диоксид углерода, который проникает в эритроциты и реагирует с водой, образуя угольную кислоту (эту реакцию катализирует карбоангидраза). Угольная кислота самопроизвольно диссоциирует, образуя бикарбонат и протон, что приводит к местному возрастанию концентрации протонов (Н+), т.е. понижению pH. Протоны высвобождают кислород из гемоглобина, и кислород диффундирует из эритроцитов в периферические ткани. Здесь он связывается с миоглобином и переносит кислород в дыхательную цепь, где он используется для синтеза АТФ путем окислительного фосфорилирования.
- Высвобождение кислорода в периферических тканях: 2,3-бисфосфоглицерат (2,3-БФГ) стабилизирует структуру дезоксигемоглобина. Помимо протонов, в создании эффекта Бора принимает участие 2,3-бисфосфоглицерат (2.3-БФГ) (рис. 18.2). В медицинской литературе распространено и другое название этого вещества — 2,3-дифосфоглицерат (2,3-ДФГ). 2.3-БФГ образуется в анаэробных условиях в эритроцитах. Процесс образования 2,3-БФГ происходит в дополнительной реакции гликолиза, получившей название
2,3-БФГ-шунта (шунт Рапопорта-Люберинга) (рис. 18.2). В периферических тканях молекула 2,3-БФГ связывается с дезоксигемоглобином и стабилизирует его структуру, не позволяя ему захватывать кислород от соседней молекулы оксигемоглобина.
- Связывание гемоглобина с кислородом в легких. Эритроциты переносят дезоксигемоглобин и связанный с ним СО2 в легкие. Поскольку в легких имеет место высокое парциальное давление кислорода, он вытесняет С02 из гемоглобина, и С02 выходит из легких при выдохе. Кислород связывается с гемоглобином, образуя оксигемоглобин, 2,3-БФГ вытесняется, и эритроциты переносят к периферическим тканям следующую порцию кислорода.
Эмбриональный гемоглобин имеет низкое сродство к 2,3-БФГ[править | править код]
Гемоглобин — тетрамер. состоящий из двух альфа-цепей и двух бета-цепей. Фетальный гемоглобин имеет иное строение: он состоит из двух а-цепей и двух у-цепей. По сравнению с нормальным гемоглобином взрослого человека, фетальный гемоглобин имеет более низкое сродство к 2,3-БФГ. Это значит, что сродство к кислороду у фетального гемоглобина выше, чем у гемоглобина материнского организма. Благодаря этому происходит транспорт кислорода от материнского организма к азолу.
2.3- БФГ и высотная адаптация[править | править код]
Предположим, что некий житель низин решил провести отпуск в горах. В первые дни отпуска даже незначительные физические нагрузки вызовут у него усталость и одышку. Но за несколько дней произойдет адаптация к высокогорью — в эритроцитах повысится концентрация 2,3-БФГ. Благодаря этому ткани станут получать кислород в достаточном количестве. несмотря на то что его концентрация в разреженном горном воздухе невысока. Повышение концентрации 2,3-БФГ — ответная реакция организма на недостаток кислорода
У курящих лиц концентрация 2,3-БФГ в эритроцитах выше, чем у некурящих. Так организм компенсирует сниженное вследствие постоянного воздействия угарного газа обеспечение тканей кислородом. Компенсаторное повышение уровня 2.3- БФГ также часто наблюдается у больных хроническими анемиями, обструктивной болезнью легких, при врожденных пороках сердца и муковисцидозе.
Энзимопатии гликолитического пути в эритроцитах[править | править код]
В редких случаях из-за врожденной недостаточности гликолитических ферментов в эритроцитах развивается наследственная несфероцитарная гемолитическая анемия. Это заболевание может быть весьма тяжелым, поскольку в эритроцитах гликолиз — единственный путь синтеза и АТФ и 2.3-БФГ.
Нарушения гликолитического ферментативного аппарата могут по-разному сказываться на метаболизме 2.3-БФГ (рис. 18.2). Если нарушение расположено проксимально по отношению к 2.3-БФГ-шунту (например, при недостаточности гексокиназы, фосфоглюкоизомеразы или альдолазы А), уровень 2,3-БФГ будет снижен, так как будет снижена интенсивность синтеза его предшественников. Если же нарушение расположено после 2.3-БФГ-шунта (например, недостаточность пируваткиназы). концентрация 2.3-БФГ в эритроцитах будет повышена.
Кроме того, у ряда больных была обнаружена недостаточность бифункционального фермента шунта — БФГ-мутазы/2,3-БФГ-фосфагазы. У таких больных концентрация 2.3- БФГ была низкой.
Номенклатура альдолаз[править | править код]
Чтобы учащийся не путал разные термины, необходимо разобраться в номенклатуре альдолаз. Альдолаза (полное название — фруктозо-1,6-бисфосфат-атьдолаза) по официальной номенклатуре называется D-глицеральдегид-З-фосфатлиазой (КФ 4.1.2.13). Она выполняет три функции:
- катализирует реакцию конденсации дигидрокснацетон-фосфата и глицеральдегид-З-фосфата. Продукт этой реакции — фруктозо-1,6-бисфосфат;
- катализирует расщепление фруктозо-1,6-бисфосфата на лигилроксиацетонфосфат и минеральдегид-3-фосфат;
- катализирует расщепление других, структурно близких фосфатов сахаров. Так. альдолаза катализирует расщепление фруктозо-1-фосфата на дигидроксиацетонфосфат и глицеральдегид (примечание: раньше фермент, выполняющий эту функцию, называли кетозо-1-фосфат-альдолазой. КФ 4.1.2.7).
У животных обнаружены три формы альдолазы.
Альдолаза А. Содержится в эритроцитах и мышцах. При наследственной гемолитической анемии в крови содержится дефектная форма альдолазы А.
Альдолаза В. Недостаточность альдолазы В приводит к наследственной непереносимости фруктозы. Альдолаза В присутствует в печени, почках и тонком кишечнике.
Альдолаза С. Содержится в головном мозге.
Взаимосвязь гликолиза и аэробных реакций[править | править код]
Два способа оценки аэробных возможностей организма (прямая оценка показателя максимального устойчивого состояния по лактату и косвенная оценка аэробно-анаэробного перехода) основаны на классической теории активации гликолиза, предложенной А. Хиллом. В основу этой теории легла гипотеза о том, что активация гликолиза в мышечном волокне запускается при снижении аэробного ресинтеза АТФ. Основной причиной снижения аэробного ресинтеза АТФ должно быть неадекватное снабжение клетки кислородом, т.е. фактически снижение внутриклеточного парциального давления кислорода до критического уровня (0,1—0,5 мм рт. ст.), ниже которого нормальное функционирование митохондрий невозможно. Прямо проверить данное предположение оказалось методически достаточно сложно.
Относительно недавно появились исследования, в которых in situ было измерено внутримышечное парциальное давление кислорода, связанного с миоглобином, во время максимального теста с возрастающей нагрузкой в т. gracilis у собаки методом криомикроспектроскопии. Среднее парциальное давление кислорода, связанного с миоглобином, при работе на уровне МПК значительно выше критического и составляет 5,5 мм рт. ст., при этом не удается обнаружить связь между ПК мышцей или средним парциальным давлением кислорода в волокне и концентрацией лактата в мышце или суммарным выходом лактата из мышцы.
Сходные результаты получены при измерении внутримышечного парциального давления кислорода во время максимального теста с повышающейся нагрузкой (50-100% от пикового ПК) у тренированных велосипедистов в условиях in vivo при разгибании ноги в коленном суставе. Исследователи получили достаточно неожиданный результат. Оказалось, что парциальное давление кислорода в миоглобине не изменяется на протяжении всего теста с возрастающей нагрузкой (50—100% от пикового ПК) вплоть до отказа от работы. Среднее парциальное давление кислорода, связанного с миоглобином, составляет 3,1 мм рт. ст. Любопытно, при работе в гипоксических условиях (F,02—0,12) парциальное давление кислорода, связанного с миоглобином, оказывается достоверно ниже, чем в нормоксии и составляет 2,1 мм рт. ст. Оно также не изменяется во всем диапазоне нагрузок (50~100% от пикового ПК). При этом потребление кислорода тканями рабочей ноги, измеренное с помощью прямого метода (по Фику), линейно растет вплоть до отказа от работы, как в гипоксических, так и в нормоксических условиях.
Таким образом, даже при гипоксии во время максимальной нагрузки парциальное давление кислорода в миоглобине не падает ниже критического уровня. Однако при этом наблюдается увеличение скорости суммарного выхода лактата из рабочей мышцы, измеренное с помощью прямого метода. Причем работа в условиях гипоксии приводила к значительно более интенсивному выходу лактата (относительно нормированной мощности работы), чем работа в нормоксических условиях. На основании этих данных можно сделать вывод о том, что парциальное напряжение кислорода в активной мышечной клетке не является ключевым фактором, активирующим гликолиз. В то же время опыты с гипоксией дают основание полагать, что парциальное давление кислорода в цитоплазме может модулировать активность гликолиза. Увеличение суммарного выхода лактата из мышцы, как в условиях нормоксии, так и в условиях гипоксии, регулируется, главным образом, активацией симпато-адреналовой системы. Это подтверждается сходной динамикой концентрации адреналина в артериальной крови и суммарного выхода лактата из рабочей мышцы. Влияние симпато-адреналовой системы на гликолиз подтверждается и рядом других работ, в которых исследовали изменения концентрации катехоламинов во время нагрузки, а также опытами с применением бета-блокаторов.
Среди других возможных кандидатов на роль активаторов гликолиза выделяют: АДФ, АМФ, неорганический фосфат, отношение креатин/фосфокреатин и цитоплазматический окислительно-востановительный потенциал (НАДН+/НАД+).
Суммируя результаты описанных исследований, можно сказать, что парциальное давление кислорода в цитоплазме мышечной клетки не опускается до критичного уровня даже при работе максимальной аэробной мощности. Это означает, что активность гликолиза в мышечном волокне во время работы не зависит от скорости аэробного ресинтеза АТФ или, по крайней мере, зависит не только от нее.
ГЛИКОЛИЗ — Большая Медицинская Энциклопедия
ГЛИКОЛИЗ (греч, glykys сладкий + lysis разрушение, распад) — сложный ферментативный процесс превращения глюкозы, протекающий в тканях животных и человека без потребления кислорода и приводящий к образованию молочной кислоты и АТФ.
C6H12O6 + 2АДФ + 2Фнеорг. —> 2CH3CHOHCOOH + 2АТФ + 2H2O.
Именно благодаря Гликолизу организм человека и животных может осуществлять ряд физиологических функций в условиях недостаточности кислорода.
В тех случаях, когда Гликолиз протекает на воздухе или в атмосфере кислорода, говорят об аэробном Гликолизе. В анаэробных условиях Гликолиз — единственный процесс в животном организме, поставляющий энергию. В аэробных условиях Гликолиз является первой стадией окислительного превращения глюкозы и других углеводов до конечных продуктов этого процесса — углекислоты и воды. Процессами, аналогичными Гликолизу, у растений и микроорганизмов являются различные виды брожения (см.). Впервые термин «гликолиз» был предложен Лепином (Lepine) в 1890 г.
Последовательность реакций в процессе Г., также как и их промежуточные продукты, хорошо изучены. Реакции Г. катализируются одиннадцатью ферментами, большинство из которых выделены в гомогенном, кристаллическом или высоко очищенном виде и свойства которых тщательно изучены.
Наиболее интенсивен Г. в скелетных мышцах, в печени, сердце, мозге и других органах. В клетке Г. протекает в гиалоплазме.

Первой ферментативной реакцией (см. схему), открывающей цепь реакций Г., является реакция взаимодействия D-глюкозы с АТФ (2), приводящая к образованию глюкозо-6-фосфата и обеспечивающая возможность дальнейшего превращения глюкозы в процессе Г. Реакция катализируется гексокиназой (см.). Эта реакция сопровождается выделением значительного количества энергии и поэтому практически необратима. В скелетных мышцах и печени глюкозо-6-фосфат в больших количествах образуется также при катаболизме гликогена, т. е. при гликогенолизе.
Второй реакцией Г. (схема, реакция 2) является изомеризация глюкозо-6-фосфата во фруктозо-6-фосфат, катализируемая глюкозофосфатизомеразой, не нуждающейся в присутствии каких-либо кофакторов. Образующая смесь двух гексозомонофосфатов, состоящая приблизительно на 80% из глюкозо-6-фос-фата и на 20% из фруктозо-6-фосфата с примесью нек-рого количества других фосфомоноэфиров, носит название эфира Эмбдена. Такая же смесь, но состоящая из глюкозо-6-фосфата почти наполовину, называется эфиром Робисона.
Фруктозо-6-фосфат, далее в фосфофруктокиназной реакции (схема, реакция 3) за счет АТФ фосфорилируется во фруктозо-1,6-дифосфат. Фруктозодифосфат является специфическим субстратом именно для Г., тогда как предыдущие реакции характерны не только для Г., но и для окислительного распада углеводов. Фосфофруктокиназа — регуляторный фермент, имеющий на молекуле 7, а по данным некоторых авторов, 12 центров связывания субстратов, кофакторов и ингибиторов. Фермент активируется ионами двухвалентных металлов, неорганическим фосфатом, АДФ, АМФ, циклическим 3′,5′-АМФ. Активность фермента также повышается в присутствии фруктозо-6-фосфата и фруктозо-1,6-дифосфата. Ингибируют фермент АТФ и цитрат.
Реакция, катализируемая фосфофруктокиназой, является наиболее медленно текущей реакцией Г., определяющей скорость всего процесса. Главными факторами в клетке, контролирующими фосфофруктокиназу, являются относительные концентрации АТФ и АДФ. Когда величина отношения АТФ/АДФ + Фнеорг. значительна, что достигается в процессе окислительного фосфорилирования (см.), происходит угнетение фосфофруктокиназы, и Г. замедляется. При снижении величины отношения АТФ/АДФ + Фнеорг. интенсивность Г. повышается. В неработающей мышце активность фосфофруктокиназы низка, что объясняется высокой концентрацией АТФ (см. Аденозинтрифосфорная кислота). В процессе работы, когда происходит интенсивное потребление АТФ, активность фосфофруктокиназы увеличивается, что приводит к интенсификации Г., а следовательно, и к усиленному образованию АТФ. При диабете, голодании и других условиях, вызывающих переключение энергетического обмена на использование жиров, содержание цитрата в клетке может возрасти в несколько раз. Величина торможения фосфофруктокиназы цитратом достигает при этом 70—80%.
Следующий этап Г. катализирует фруктозодифосфатальдолаза (схема, реакция 4). Фруктозо-1,6-дифосфат расщепляется на две фосфотриозы: диоксиацетонфосфат и глицеральдегид-3-фосфат. Под влиянием триозофосфатизомеразы (схема, реакция 5) происходит взаимопревращение, фосфотриоз. Равновесие этой реакции сдвинуто в сторону образования диоксиацетонфосфата: на 96% диоксиацетонфосфата приходится всего 4% глицеральдегид-3-фосфата, но именно он и участвует в дальнейших превращениях в процессе Г. Благодаря высокой активности триозофосфатизомеразы преимущественное образование диоксиацетонфосфата не лимитирует скорости Г. в целом. Образованием глицеральдегид-3-фосфата (3-фосфоглицеринового альдегида) заканчивается первая стадия Г.
Вторая стадия Г. является общим путем превращения всех углеводов и рассматривается как наиболее сложная и важная часть процесса, приводящая к образованию АТФ. Центральной реакцией Г. является реакция гликолитической оксидоредукции, сопряженной с фосфорилированием,— реакция окисления 3-фосфоглицеринового альдегида (схема, реакция 6), катализируемая глицеральдегидфосфатдегидрогеназой. Этот фермент состоит из четырех идентичных субъединиц, каждая из которых представляет собой полипептидную цепь с 330 аминокислотными остатками. Каждая субъединица несет одну молекулу НАД+ и 4 свободные SH-группы. В ходе реакции, идущей в присутствии неорганического фосфата, НАД+ выступает как акцептор водорода, отщепляющегося от глицеральдегид-3-фосфата. При восстановлении НАД+ происходит связывание глицеральдегид-3-фос-фата с молекулой фермента за счет SH-групп последнего. Образовавшаяся связь, богатая энергией, непрочна и расщепляется под влиянием неорганического фосфата, при этом образуется 1,3-дисфосфоглицериновая к-та (1,3-дифосфоглицерат). Последующая реакция (схема, реакция 7) приводит к передаче богатого энергией фосфатного остатка на молекулу АДФ с образованием АТФ и 3-фосфоглицериновой к-ты (3-фосфоглицерата). Для реакции, катализируемой фосфоглицераткиназой, необходимы ионы двухвалентных металлов: Mg2+, Mn2+ или Ca2+. Далее (схема, реакция 8) 3-фосфоглицериновая к-та превращается в 2-фосфоглицериновую к-ту (2-фосфоглицерат). Реакцию катализирует фосфоглицерат-фосфомутаза в присутствии двух кофакторов: иона Mg2+ и 2,3-дифосфоглицериновой к-ты. Следующий этап Г.— образование фосфоенолпирувата, богатого энергией предшественника АТФ (схема, реакция 9). Превращение 2-фосфоглицериновой к-ты (2-фосфоглицерата) в фосфоенолпируват осуществляется в результате реакции дегидратации, катализируемой фосфопируват-гидратазой. Фермент, катализирующий эту реакцию, нуждается в Mg2+, Mn2+, Zn2+ или Cd2+, антагонистами которых являются ионы Ca2+ или Sr2+. Реакцию между фосфоенолпируватом и АДФ (схема, реакция 10) с образованием пировиноградной к-ты (пирувата) и АТФ катализирует пируваткиназа, требующая для проявления своей активности ионов Mg2+ или Mn2+ и K+; Ca2+ выступает как конкурентный антагонист этих ионов. Для максимальной активности пируваткиназа нуждается также в присутствии одновалентных катионов K+, Rb+ или Cs+, антагонистами которых являются катионы Na+ и Li+. Обратимое восстановление пирувата в молочную к-ту (лактат) за счет восстановленного НАД+ (НАДН) является конечным этапом Г. (схема, реакция 11). Реакцию катализирует лактатдегидрогеназа (см.).
Благодаря трем необратимым реакциям — гексокиназной, фосфофруктокиназной и пируваткиназной Г. сам по себе является необратимым процессом (его равновесие сдвинуто в сторону образования молочной к-ты). На I стадии Г. затрачиваются две молекулы АТФ, на II стадии образуются четыре молекулы АТФ. Т. о., энергетическая эффективность Г. (всего две молекулы АТФ на одну молекулу глюкозы) сравнительно низка. Тем не менее роль Г. велика, т. к. только благодаря ему организм может осуществлять ряд физиол, функций в условиях недостаточного снабжения тканей и органов кислородом. Такие условия создаются, напр., в энергично работающей скелетной мышце. Присутствие кислорода тормозит Г. (явление, называемое эффектом Пастера — см. Пастера эффект). В сердечной мышце в процессах образования энергии гликолитический путь распада углеводов занимает небольшое место. Активность ферментов Г. в сердце значительно ниже, чем в скелетных мышцах. Реальная скорость Г. меняется в зависимости от снабжения сердечной мышцы кислородом и интенсивности в ней окислительных процессов. Но даже при наиболее оптимальных условиях снабжения кислородом в мышце сердца всегда идет Г. Субстраты гликолитических реакций (фосфорилированные сахара, пируват, молочная к-та) используются сердечной мышцей в процессах пластического обмена веществ и в цикле Трикарбоновых к-т (см. Трикарбоновых кислот цикл) в качестве субстратов окисления. Большую роль Г. приобретает в сердце в условиях дефицита кислорода. Бурный аэробный Г. происходит в опухолях, где он является основным источником энергии. Опухолевые ткани характеризуются отсутствием эффекта Пастера. В них регулирующая роль фосфофруктокиназы утрачивается.
Нормальное течение Г. возможно только в том случае, если в ткани присутствуют АДФ, субстраты для фосфоглицераткиназной и пируваткиназной реакций, а также НАД и неорганический фосфат, необходимые для реакции гликолитической оксидоредукции (угнетение гликолитической оксидоредукции в сердечной мышце, обусловленное уменьшением содержания НАД, наблюдалось в условиях экспериментального миокардита). Основной, лимитирующей скорость Г. реакцией является реакция, катализируемая фосфофруктокиназой (см. схему, реакция 3). Вторым этапом, лимитирующим скорость и регулирующим Г., после фосфофруктокиназной реакции является гексокиназная реакция (см. схему, реакция 1). Широкий изоферментный спектр этого фермента обусловливает возможность тонкой регуляции Г. на его начальном, пусковом этапе. Динамичный характер связи гексокиназы с митохондриями и микросомами, а также изменения свойств этого фермента при взаимодействии с субклеточными структурами делают механизм регуляции Г. очень чувствительным.
Отсутствие регулирующей роли фосфофруктокиназы и крайне высокая активность гексокиназы превращают злокачественную опухоль в мощный насос, непрерывно извлекающий глюкозу из организма. При этом интенсивность Г. такова, что перепад между концентрацией глюкозы в артериальной крови и ткани опухоли достигает 60—80 мг% (артериальная кровь) против нуля (опухолевая ткань).
В норме контроль Г. осуществляется также лактатдегидрогеназой (ЛДГ) и ее изоферментами (см. Лактатдегидрогеназа), которые характеризуются специфической локализацией в органах и тканях. В тканях с аэробным метаболизмом (ткани сердца, почек, эритроциты) преобладают ЛДГ-1 и ЛДГ-2. Эти изоферменты ингибируются даже небольшими концентрациями пирувата, что препятствует образованию молочной к-ты и способствует более полному окислению пирувата в цикле Трикарбоновых к-т. В тканях человека, в значительной степени зависимых от энергии, образующейся в процессе Г. (скелетные мышцы), главными изоферментами ЛДГ являются ЛДГ-4 и ЛДГ-5. Активность ЛДГ-5 максимальна при тех концентрациях пирувата, которые ингибируют ЛДГ-1. Преобладание изоферментов ЛДГ-4 и ЛДГ-5 обусловливает интенсивный анаэробный Г. с быстрым превращением пирувата в молочную к-ту. Заметное увеличение относительного содержания ЛДГ-5 было отмечено при адаптации организмов и клеток в культурах к гипоксии. Во многих тканях человека (ткани селезенки, поджелудочной и щитовидной желез, надпочечников, лимф, узлов) преобладает изофермент ЛДГ-3. В тканях эмбриона и плода человека присутствуют все 5 изо-ферментов лактатдегидрогеназы, среди которых преобладает ЛДГ-3. Вскоре после рождения у ребенка картина распределения изоферментов в органах и тканях становится такой же, как и у взрослого человека. Изменение изоферментного спектра в эмбриогенезе особенно выражено в скелетных мышцах. При различных миопатиях (см.) наблюдается аномальное распределение изоферментов ЛДГ: увеличение одних и уменьшение или даже полное исчезновение других. При прогрессирующей мышечной дистрофии (болезнь Дюшенна) преобладают изоферменты ЛДГ-1, ЛДГ-2 и ЛДГ-3. При других формах мышечной дистрофии (миотоническая дистрофия, дерматомиозит, болезнь Верднига — Гоффманна) характерно уменьшение или даже отсутствие ЛДГ-5 в скелетных мышцах, что коррелирует со сниженным образованием молочной к-ты у больных этими формами миопатий после физ. работы. При ряде патол, состояний благодаря увеличению проницаемости клеточных мембран изо-ферменты лактатдегидрогеназы в избыточном количестве поступают в кровь. Активность лактатдегидрогеназы и характер распределения ее изоферментов в сыворотке крови специфически изменяются при инфаркте миокарда (см.), заболеваниях печени и желчевыводящих путей, ревматизме (см.). В клинике для дифференциальной диагностики этих заболеваний применяют простые методы определения относительного распределения изоферментов лактатдегидрогеназы в сыворотке крови, основанные на их различной электрофоретической подвижности.
В организме человека и животных существуют ферментативные механизмы, обеспечивающие протекание Г. в обратном направлении, т. е. синтез глюкозы, а также гликогена из молочной к-ты. Этот процесс носит название глюконеогенеза; он интенсивно протекает в печени, куда в больших количествах током крови доставляется молочная к-та. Энергия для осуществления этого процесса образуется также в печени в результате полного окисления нек-рой части (ок. 15%) молочной к-ты. Предшественниками глюкозы в глюконеогенезе могут быть пируват или любое соединение, превращающееся в процессе катаболизма в пируват или один из промежуточных продуктов цикла Трикарбоновых к-т, а также так наз. гликогенные аминокислоты.
Большинство стадий глюконеогенеза представляет собой обращение реакций Г. Три реакции Г.— гексокиназная, фосфофруктокиназная и пируваткиназная — необратимы, поэтому глюконеогенез идет в обход этих реакций.
Первую реакцию глюконеогенеза — превращение молочной к-ты в пировиноградную — катализирует лактатдегидрогеназа. Синтез фосфоенолпирувата из пирувата осуществляется в несколько этапов. Первый этап локализуется в митохондриях.
Пируват под влиянием пируваткарбоксилазы (КФ 6.4.1.1), активной только в присутствии ацетилкофермента А, карбоксилируется при участии CO2 с образованием оксалоацетата. В реакции участвует АТФ, поэтому продуктами реакции наряду с оксалоацетатом являются АДФ и ортофосфат:

Оксалоацетат в результате декарбоксилировании и фосфорилирования под влиянием фосфопируваткарбоксилазы (КФ 4.1.1.32) превращается в фосфоенол пируват. Донором фосфатного остатка в реакции служит гуанозинтрифосфат или инозинтрифосфат:

Фосфопируваткарбоксилаза присутствует как в гиалоплазме, так и в митохондриях, но распределение фермента у человека и животных различно. У морских свинок, кроликов, овец, коров и у человека фосфопируваткарооксилаза присутствует в обеих фракциях. В эмбриональной печени крыс и морских свинок, не способной к глюконеогенезу, присутствует только митохондриальный фермент. В гиалоплазме активность фосфопируваткарбоксилазы появляется только в постнатальный период; одновременно печень становится способной к глюконеогенезу.
Поскольку в глюконеогенезе участвует фосфопируваткарбоксилаза превращение оксалоацетата в фосфоенолпируват происходит именно в гиалоплазме. Оксалоацетат, образовавшийся в митохондриях, не может перейти в гиалоплазму, т. к. мембрана митохондрий для него непроницаема. В митохондриях оксалоацетат восстанавливается в яблочную к-ту (малат), к-рая способна диффундировать из митохондрий в гиалоплазму, где и окисляется с образованием оксалоацетата, который, в свою очередь, превращается в фосфоенол пируват.
Последующие реакции глюконеогенеза, катализируемые ферментами Г., приводят к образованию фруктозо-1 ,6-дифосфата. Превращение фруктозо-1 ,6-дифосфата во фруктозо-6-фосфат, а затем и глюкозо-6-фосфата в глюкозу катализируют специфические фосфатазы, гидролитически отщепляющие неорганический фосфат.
При глюконеогенезе фруктозо-1,6-дифосфатаза (гексозодифосфатаза; КФ 3.1.3.11) катализирует ключевую реакцию D-фруктозо-1,6-дифосфат + H2O —> D-фруктозо-б-фосфат + ортофосфат) и соответственно действие, к-рое оказывает на нее АТФ и АМФ, противоположно их действию на фосфофруктокиназу (см. выше): гексозодифосфатаза активируется под влиянием АТФ и ингибируется АМФ. Когда величина отношения АТФ/АДФ низка, в клетке происходит расщепление глюкозы, когда эта величина высока — расщепление глюкозы прекращается. В аэробных условиях значительно эффективнее, чем в анаэробных, из клетки удаляется неорганический фосфат й АДФ и накапливается АТФ, что приводит к подавлению Г. и стимуляции глюконеогенеза. Пируваткарбоксилаза также чувствительна к величине отношения АТФ/АДФ, т. к. ингибируется АДФ. Ацетил-КоА активирует пируваткарбоксилазу.
В регуляции Г. и глюконеогенеза большую роль играет инсулин (см.). При недостаточности его происходит повышение концентрации глюкозы в крови (гипергликемия), избыточное выведение глюкозы с мочой (глюкозурия) и уменьшение содержания гликогена в печени. При этом мышцы утрачивают способность использовать в процессе Г. глюкозу крови. В печени при общем снижении интенсивности биосинтетических процессов (биосинтеза белков, биосинтеза жирных к-т из глюкозы) наблюдается усиленный синтез ферментов глюконеогенеза. При введении инсулина больным диабетом все перечисленные метаболические нарушения исчезают: нормализуется проницаемость для глюкозы мембран мышечных клеток, восстанавливается соотношение между Г. и глюконеогенезом. Инсулин контролирует эти процессы на генетическом уровне как регулятор синтеза ферментов. Он является индуктором образования ключевых ферментов Г.: гексокиназы, фосфофруктокиназы и пируваткиназы. Одновременно инсулин действует как репрессор синтеза ферментов глюконеогенеза.
Клин, признаки преобладания Г. над аэробной фазой распада углеводов наблюдаются чаще всего при гипоксических состояниях, обусловленных различными нарушениями кровообращения или дыхания, высотной болезнью, анемией, понижением активности системы тканевых окислительных ферментов при некоторых инфекциях и интоксикациях, гипо- и авитаминозами, в результате относительной гипоксии при чрезмерной мышечной работе. При усилении Г. происходит накопление пирувата и лактата с соответствующим закислением тканей, изменением кислотно-щелочного равновесия, уменьшением щелочных резервов. У больных сахарным диабетом активация процессов Г. и недостаточный ресинтез лактата в гликоген печени также нередко приводят к увеличению содержания в крови лактата и пирувата; в этих случаях ацидоз может достигать высокой степени с развитием диабетической молочнокислой комы. Торможение ресинтеза гликогена из лактата и пирувата, образовавшихся в результате Г., наблюдается при поражениях паренхимы печени (поздние стадии гепатита, цирроз печени и т. п.), поэтому увеличение содержания в сыворотке крови лактата и пирувата может служить показателем нарушения функции печени.
Высокая интенсивность Г. в опухолевых тканях используется для определения чувствительности опухолей к нек-рым противоопухолевым препаратам: подавление Г. в срезах опухоли под влиянием исследуемого химиопрепарата свидетельствует о чувствительности к нему данной опухоли.
Библиография:
Дэгли С. и Никольсон Д. Е. Метаболические пути, пер. с англ., М., 1973, библиогр.;
Ленинджер А. Биохимия, пер. с англ., М., 1976; Проблемы медицинской химии, под ред. В. С. Шапота и Э. Г. Ларского, М., 1973, библиогр.; Уилкинсон Дж. Изоферменты, пер. с англ., М., 1968.
Г. А. Соловьева, Г. К. Алексеев.
Гликолиз
☰
Гликолиз (греч. glycos — сладкий, lysis — расщепление) — первый этап клеточного дыхания, представляющий собой последовательность реакций, в ходе которых одна молекула глюкозы (C6H12O6) расщепляется на две молекулы пировиноградной кислоты (C3H4O3). Реакции протекают в цитоплазме без участия кислорода, но при участии ферментов. В пирувате атомы углерода оказываются в более окисленной форме, так как четыре атома водорода отщепляются и восстанавливают другое соединение (НАД до НАД · H2).
Суммарное уравнение реакции гликолиза
C6H12O6 → 2C3H4O3 + 4H + 2АТФ
Чистый выход энергии, запасенной в АТФ, всего две молекулы, что говорит о малой эффективности этого этапа клеточного дыхания. Основная часть энергии глюкозы остается в пировиноградной кислоте, а также запасается в НАД · H2. При аэробном дыхании эта энергия потом используется для получения основного количества молекул АТФ.
Поскольку глюкоза при гликолизе теряет четыре атома водорода, то происходит ее окисление. Акцепторами водорода выступают молекулы никотинамидадениндинуклеотида (НАД+).
Глюкоза не сразу распадается до пирувата, а через ряд последовательных реакций. Суммарно их можно представить в виде трех этапов:
Глюкоза фосфорилируется за счет фосфатных групп АТФ и превращается в фруктозо-1,6-бифосфат. При этом используются две молекулы АТФ, которые становятся АДФ.
Фруктозо-1,6-бифосфат расщепляется на два фосфорилированных трехуглеродных сахара.
Эти сахара превращаются в пировиноградную кислоту. При этом синтезируется четыре молекулы АТФ, а к двум молекулам НАД присоединяется водород.
В гликолизе участвуют около девяти ферментов, составляющих конвейер. Как видно из схемы, гликолиз протекает в десять стадий.
При дальнейшем окислении пировиноградной кислоты в митохондриях используется энергия, запасенная в НАД · H2.
В процессе эволюции гликолиз – первым способом получения АТФ. В наше время он характерен как для прокариот, так и эукариот как один из этапов клеточного дыхания.
Следует иметь в виду, что в клетках гликолиз — не единственный способ окисления глюкозы.
это важный биохимический процесс :: SYL.ru
Гликолиз — это главный процесс катаболизма различных углеводов для многих живых организмов. Именно он позволяет генерировать энергию в виде молекул АТФ в тех клетках, где не происходит фотосинтез. Анаэробный гликолиз протекает при наличии или отсутствии кислорода.
Специфика процесса
Многочисленные исследования химической сути данного процесса продемонстрировали, что у начальных этапов брожения и дыхания есть сходство. Благодаря этому открытию ученые объяснили единство в живом мире. Анаэробный гликолиз происходит после того, как прошел цикл трикарбоновых кислот, завершился перенос свободных электронов. В митохондрии попадает пируват, происходит его окисление до углекислого газа. Это приводит к выделению свободной энергии из гексозы. Ферменты, являющиеся ускорителями гликолитических реакций, во многих клетках находятся в растворимой форме в цитозоле. Ускорители процесса окисления гексоз, происходящего в присутствии кислорода, сконцентрированы в митохондриальных мембранах.
Для расщепления молекулы углевода, включающего шесть атомов углерода на две молекулы, необходимо присутствие десяти активных ферментов. Исследователям удалось выделить их в чистом виде, изучить их физические и химические характеристики.
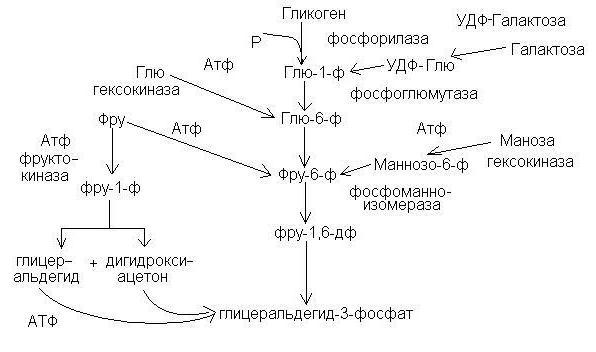
Стадии процесса
Процесс гликолиза происходит в клетках живых организмов. Он сопровождается образованием пировиноградной кислоты, состоит из нескольких этапов. Для дыхательного распада нужно активировать глюкозу. Происходит подобный процесс при фосфорилировании атома углерода при взаимодействии с АТФ.
глюкоза + АТФ = глюкозо-6-фосфат + АДФ
Для проведения данного химического взаимодействия используют катионы магния и гексокиназу (фермент). Далее происходит изомеризация продукта реакции в фруктозу-6-фосфат. В качестве катализатора применяют фермент фосфоглюкоизомеразу.
Гликолиз глюкозы характеризуется еще одной стадией, в которой участвует АТФ. Присоединение фосфорной кислоты происходит к первому атому углерода во фруктозе. Последующие этапы гликолиза связаны с расцеплением полученного фруктозо-1,6-дифосфата до триоз, образованием ФГА (3-фосфоглицеринового альдегида).
Гликолиз — многостадийный процесс, связанный с выделением энергии. При расщеплении одной молекулы глюкозы получают две молекулы ФГА, поэтому происходит их повтор.
Гликолиз — это процесс, который в суммарном виде представлен уравнением:
C6h22O6 + 2АТФ + 2НАД + 2Фн + 4АДФ → 2ПВК 2НАДН + 2Н+ + 4АТФ + 2АДФ
Регуляция гликолиза
Гликолиз — это важный для живого организма процесс. Он направлен на выполнение двух функций:
- генерация АТФ при расщеплении молекул гексозы;
- транспортировка строительных блоков для последующего процесса синтеза.
Регуляция данного процесса направлена на полное удовлетворение этих потребностей живой клетки. Реакции, в которых катализаторами выступают ферменты, являются необратимыми.
Особое значение в осуществлении регуляторной функции принадлежит фосфофруктокиназе. Данный фермент выполняет регуляторную функцию, характеризует скорость протекания процесса.
Физиологическое значение
Гликолиз можно считать универсальным способом катаболизма глюкозы. Его активно используют про- и эукариотические организмы. Ферменты, являющиеся катализаторами гликолиза, растворяются в воде, накапливаются в цитозоле. Часть клеток и тканей животных могут катаболизировать гексозу только путем гликолиза. Например, подобные способности есть у клеток почечных каналов, нейронов мозга.
В жировой ткани и печени есть некоторые отличия в физиологической роли гликолиза. При пищеварении в жировой ткани и в печени данный процесс является источником субстратов, используемых в синтезе жиров.
Часть тканей растений запасают крахмал в клубнях. Водные растения энергию получают через гликолиз.
В анаэробных условиях происходит превращение пирувата в этанол и лактат. Процесс сопровождается выделением большого количества энергии.
Гликолиз имеет существенное физиологическое значение в адипоцитах. С его помощью вместо окислительного процесса происходит липогенез, позволяющий снижать окислительный стресс.
Медицинская значимость
По мере накопления лактата, который образуется при анаэробных условиях, развивается в крови лактацидоз. Он приводит к понижению реакции среды крови, что сопровождается резкими нарушениями в метаболизме клеток. Подобный процесс происходит при патологических процессах, связанных с нарушениями снабжения кислородом тканей. Например, при инфаркте миокарда, кровотечениях, легочной эмболии. Обусловлен этот процесс сахарным диабетом, при котором вместо аэробного гликолиза происходит анаэробный процесс.
Учитывая, что инсулин является ускорителем гликолиза, при первом типе диабета наблюдается замедление гликолиза. Именно поэтому те препараты, которые стимулируют ферменты, используемые для данного процесса, выполняют функцию лечения заболевания.
Заключение
Гликолиз — это процесс, который необходим для полноценной жизнедеятельности организмов. При раковых заболеваниях потребление глюкозы увеличивается в десять раз, поэтому именно от гликолиза зависит жизнеспособность опухолевых клеток.
После детального изучения особенностей протекания данного процесса ученым удалось использовать гликолиз не только для питания клеток, но и для лечения некоторых заболеваний.
ГЛИКОЛИЗ — это… Что такое ГЛИКОЛИЗ?
(от греч. glykys-сладкий и lysis — разложение, растворение, распад), анаэробное (без участия О 2) негидро-литич. расщепление углеводов (гл. обр. глюкозы) в цитоплазме под действием ферментов, сопровождающееся синтезом АТФ и заканчивающееся образованием молочной к-ты (см. рис.). Г. одной молекулы глюкозы м. б. выражен след. ур-нием:
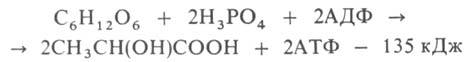
где АДФ-аденозиндифосфат. Субстратами Г. кроме глюкозы м. б. другие моносахариды, а также полисахариды. В мышечной ткани, где основной субстрат Г.-гликоген, процесс начинается с р-ции I и наз. гликогенолизом. У растений субстратом для Г. может служить крахмал. Первые этапы Г., спиртового и нек-рых. др. видов брожения сходны.
Стадии, в к-рых осуществляются необратимые р-ции (II-IV), играют существ. роль в регуляции скорости Г. Наиб. важный регуляторный фермент-фосфофруктокиназа, катализирующая р-цию III; ее активность ингибируется АТФ, НАДН, лимонной и жирными к-тами, стимулируется АДФ и АМФ. Р-ции II и IV катализируются соотв. гексокиназой и пируваткиназой, активность к-рых регулируется адениловыми нуклеотидами, промежуточными продуктами Г. и цикла трикарбоновых к-т. У животных и человека в регуляции Г. принимают участие также гормоны. 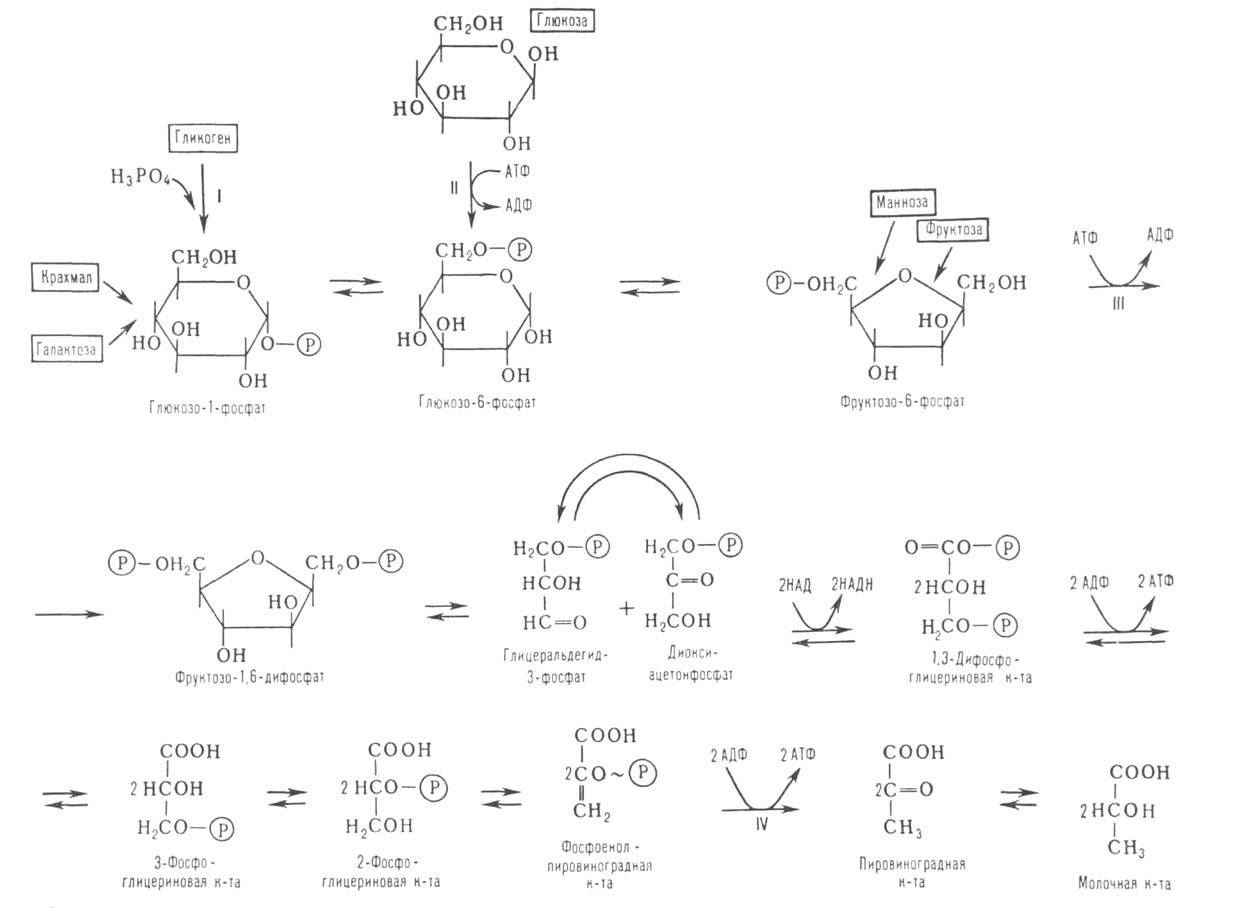
Схема гликолиза. В одинарных рамках-субстраты гликолиза, АТФ -аденозинтрифосфат, АДФ-аденозиндифосфат, НАДН и НАД-соотв. восстановленная и окисленная формы никотинамидадениндинуклеотида, Р-остаток фосфорной к-ты, ~ -высокоэргич. связь.
В условиях недостаточности кислорода Г.-единств. процесс, поставляющий энергию для осуществления физиол. ф-ций организма. В аэробных условиях Г.-первая стадия окислит. превращения углеводов: в присут. О 2 пировиноградная к-та может подвергаться дальше окислит. декарбоксилированию, а образующаяся уксусная к-та в виде СН 3 С(О)КоА (КоА-остаток кофермента А) полностью окисляться до СО 2 и воды в цикле трикарбоновых к-т.
Интенсивный Г. происходит в скелетных мышцах, где он поставляет энергию для мышечных сокращений, а также в печени, сердце, мозге животных и человека. В клетках осуществляется тонкая регуляция окислит. и анаэробного обмена. Подавление Г. дыханием в присут. О 2 (эффект П а с т е р а) обеспечивает клетке Наиб. экономный механизм образования богатых энергией соединений. В тканях, где такой эффект отсутствует (напр., в эмбриональных и опухолевых), Г. протекает очень активно. В нек-рых тканях с интенсивным Г. наблюдается подавление тканевого дыхания (эффект Крабтри).
Г.-простейшая форма биол. механизма аккумулирования энергии углеводов в АТФ. Считают, что он возник в период, когда в атмосфере Земли не было О 2. При энергетически более выгодном аэробном окислении из одной молекулы глюкозы образуется 38 молекул АТФ.
Лит.: Мецлер Д., Биохимия, пер. с англ., т. 2, М., 1980, с. 335-38; Основы биохимии, пер. с англ., т. 2, М., 1981, с. 557-82; Страйер Л., Биохимия, пер. с англ., т. 2, М., 1985, с. 23-48, 115-38. Н. В. Гуляева.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
Гликолиз— схема, этапы, путь (цикл), продукты, ферменты — (Обновлено
Наше тело постоянно нуждается в энергии для функционирования. Даже в состоянии покоя для основного функционирования клеток требуется значительное количество энергии. Три четверти этой энергии получают из углеводов, которые мы потребляем с пищей.
Глюкоза — это простейшая форма сахара, на которую расщепляются пищевые углеводы, и с этой молекулы начинаются этапы производства энергии.Таким образом, глюкоза является основным топливом для нашего тела.
Что такое гликолиз: определение
Гликолиз — это первый шаг в процессе производства энергии из молекулы глюкозы. По определению, гликолиз — это ферментативная деградация глюкозы с образованием молекулы, обеспечивающей энергию, АТФ (аденозинтрифосфат).
Процесс и где происходит гликолиз?
Поскольку каждая клетка в организме нуждается в энергии, гликолиз происходит во всех клетках, и местом гликолиза является цитоплазма .Из-за своей неизбежности гликолиз может происходить как в присутствии, так и в отсутствие кислорода.
Соответственно, эти два типа известны как аэробный гликолиз и анаэробный гликолиз соответственно.
Анаэробный гликолиз важен для таких клеток, как красные кровяные тельца, в которых отсутствуют митохондрии, необходимые для анаэробных реакций, и для скелетных мышц, где частые приступы нехватки кислорода не редкость

Рисунок 1: Уравнение аэробного гликолиза
Источник изображения: www3.med.unipmn.it
Исходным веществом или реагентом при гликолизе является глюкоза. Он проходит ряд этапов для образования конечного продукта — пирувата.

Изображение 2: Процесс гликолиза
Источник изображения: upload.wikimedia.org
Процесс гликолиза включает серию стадий, начиная с глюкозы в качестве реагента. Первый шаг важен и является одним из трех необратимых шагов в этом процессе. В присутствии фермента гексокиназы глюкоза захватывает фосфатную группу АТФ и образует глюкозо-6-фосфат.
Помимо гликолиза, это соединение является воротами для многих других важных процессов, таких как синтез гликогена и липидов.
На следующем этапе не происходит синтеза нового соединения, а просто происходит перегруппировка атомов (изомеризация) с образованием фруктозо-6-фосфата из глюкозо-6-фосфата, и этот этап катализируется ферментом изомеризацией фосфогексозы.
Следующий шаг — это второй необратимый шаг в процессе, более важный в регулировании гликолиза.Фруктозо-6-фосфат фосфорилируется АТФ до фруктозо-1,6-бисфосфата в присутствии фосфофруктокиназы 1.
Фруктозо-1,6-бисфосфат — это 6-углеродное соединение, такое же, как у глюкозы. На этом этапе он расщепляется ферментом альдолазой на два разных соединения — глицерадегид-3-фосфат и дигидроксиацетонфосфат. Оба представляют собой 3 углеродных соединения, которые взаимозаменяемы.
На следующем этапе предположим, что 2 молекулы глицеральдегид-3-фосфата проходят процесс одновременно.
Глицеральдегид-3-фосфат (G3P) фосфорилируется до 1,3-бисфосфоглицерата (1,3 BPG) неорганическим фосфатом под действием фермента глицеральдегид-3-фосфатдегидрогеназы. Эта реакция опосредована НАД.
1,3 BPG превращается в 3-фосфоглицерат ферментом фосфоглицераткиназой, а удаленный из него фосфат используется для синтеза АТФ из АДФ. Таким образом, на этом этапе генерируются 2 молекулы АТФ, учитывая, что 2 молекулы G3P подвергаются гликолизу одновременно
3-фосфоглицерат превращается в фосфоенолпируват (PEP) энолазой.Фосфатная группа удаляется из PEP, с помощью которого АДФ фосфорилируется до АТФ в присутствии пируваткиназы. Конечный продукт — пируват. Это последний этап аэробного гликолиза, который необратим и дает 2 молекулы АТФ
Этапы гликолиза (ферменты и пути)

Анимация гликолиза, часть 1 — ссылка
Анимация гликолиза, часть 2: — ссылка
Аэробный и анаэробный гликолиз: различия
Когда имеется достаточное количество кислорода, пируват превращается в ацетил-Со А в митохондриях, а затем входит в цикл лимонной кислоты.В анаэробных условиях пируват превращается в лактат в присутствии лактатдегидрогеназы.
Преимущество этой стадии состоит в том, что НАДФН окисляется до НАД, который повторно вступает в гликолиз на стадии дегидрогеназы G3P и продолжает генерировать АТФ посредством обычных стадий. Таким образом энергия производится даже в отсутствие кислорода.

Рисунок 3: Аэробный и анаэробный гликолиз
Источник диаграммы: www.sivabio.50webs.com
Анаэробный гликолиз происходит в скелетных мышцах, головном мозге, почках и печени при недостатке кислорода, тогда как в эритроцитах он происходит даже в присутствии кислорода.Из-за отсутствия митохондрий, что неизбежно на стадиях, следующих за производством пирувата, гликолиз в эритроцитах всегда является анаэробным.
Регулирование гликолиза
Как упоминалось выше, три необратимых этапа, которые катализируются ферментами гексокиназой, фосфофруктокиназой и пируваткиназой, являются регуляторными этапами гликолиза.

Изображение 4: Этапы регулирования гликолиза
Источник диаграммы: quizlet.com
- Как и в случае любой химической реакции, когда реагент (глюкоза) присутствует в избытке, скорость реакции увеличивается.Активируются ферменты гликолиза.
- Кроме того, повышенное количество глюкозы приводит к секреции инсулина, что, в свою очередь, увеличивает активность гликолитических ферментов.
- Глюкагон и эпинерфрин ощущают падение уровня глюкозы в крови и ингибируют гликолитические ферменты. Они повышают уровень цАМФ, который ингибирует фермент пируваткиназу, фосфорилируя и делая его неактивным. Этот режим регулирования очень быстрый.
- 5’-AMP — косвенный индикатор количества АТФ в системе.Когда АТФ истощается, что приводит к увеличению образования АМФ, это воспринимается как недостаток энергии в системе. Таким образом, АМФ активирует фермент фосфофруктокиназу и вызывает мгновенное изменение скорости гликолиза.
- АТФ и цитрат ингибируют фермент фосфофруктокиназу, в то время как ингибирование АТФ блокируется фруктозой 2,6-бисфосфатом, который образуется из фосфофруктокиназы II
АТФ, произведенный Glycolysis
| Катализирующие ферменты | Способ производства АТФ | Количество АТФ |
|---|---|---|
| Глицеральдегид-3-фосфатдегидрогеназа | Окисление 2 НАДН в дыхательной цепи | 6 * |
| Фосфоглицераткиназа | Фосфорилирование на уровне субстрата | 2 |
| Пируваткиназа | Фосфорилирование на уровне субстрата | 2 |
| Итого | 10 |
После того как 2 молекулы АТФ потребляются в реакциях, катализируемых гексокиназой и ферментом фосфофруктокиназой, чистое производство АТФ составляет 8
Фосфорилирование на уровне субстрата
Когда фосфатная группа переносится с субстрата на АДФ с образованием АТФ, это называется фосфорилированием на уровне субстрата.При гликолизе фосфорилирование на уровне субстрата происходит в 2 разных этапа

Изображение 5: Фосфорилирование на уровне субстрата
Источник изображения: bio100.class.uic.edu

Блок-схема 6: При гликолизе — АТФ, полученные на этапах 7 и 10 на рисунке, являются фосфорилированием на уровне субстрата.
Источник схемы: twisteddnas.files.wordpress.com
Разница между гликолизом и циклом Креба
Гликолиз — это первый шаг в процессе производства энергии из молекулы глюкозы, который заканчивается производством 2 молекул пирувата, который затем превращается в лимонную кислоту и входит в цикл лимонной кислоты, также известный как цикл Креба, для дальнейшего производства энергии.
| ГЛИКОЛИЗ | ЦИКЛ КРЕБА |
|---|---|
| Реагентом является одна молекула глюкозы | Реагентом является пируват, который превращается в лимонную кислоту, которая затем входит в цикл |
| Продукт представляет собой 2 молекулы пировиноградной кислоты | Пируват окисляется до диоксида углерода и воды |
| Встречается в цитоплазме клетки | Встречается в митохондриях клетки |
| Это может происходить как аэробно, так и анаэробно | Это может происходить только в присутствии кислорода |
| Произведено 8 молекул АТФ | Произведено 24 молекулы АТФ |
| Произведено 2 молекулы НАДН | Произведено 6 молекул НАДН и 2 молекулы FADh3 |
Гликолиз против цикла Креба
Часто задаваемые вопросы
Сколько НАДН производится при гликолизе?

Какие продукты гликолиза?

Где происходит клеточное дыхание?
Наука
- Анатомия и физиология
- Астрономия
- Астрофизика
- Биология
- Химия
- наука о планете Земля

Leave A Comment