Гидролитическое расщепление белков
Главный, но возможно не единственный путь распада белков в организме – гидролиз. Гидролитический распад белков протекает в любой клетке организма в основном в специальных субклеточных элементах – лизосомах, где сосредоточены гидролитические ферменты и где осуществляется деструкция высокомолекулярных веществ до низкомолекулярных метаболитов.
Вместе с тем, определенная часть ферментов, ускоряющих распад белков, есть в цитоплазме клетки, а некоторые из них секретируются в желудочно-кишечном тракте, обеспечивая внеклеточное переваривание белков.
Гидролиз белков может быть частичным (до пептидов) и полным (до аминокислот). При частичном (неполном) гидролизе в белковой молекуле распадаются лишь некоторые пептидные связи, как правило, по соседству со строго определенными аминокислотными радикалами. Этот процесс ускоряется специфическими протеолитическими ферментами (протеиназы).
В свою очередь пептиды гидролизуются до аминокислот при участии ряда пептидаз.
Следовательно, ферментный аппарат пищеварительного тракта осуществляет поэтапное, строго избирательное расщепление пептидных связей белковой молекулы вплоть до конечных продуктов гидролиза белков – свободных аминокислот.
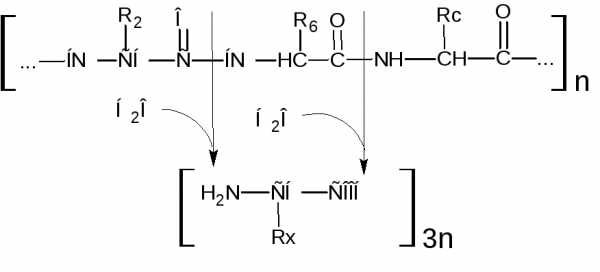
Свободные аминокислоты могут подвергаться дальнейшему распаду, включаясь в гликолиз или сразу же в цикл Кребса (рис. 2).
Катаболизм аминокислот
Первая реакция, которой подвергается аминокислота при катаболизме, это реакция освобождения от аминогруппы, которая может осуществляться либо путем переаминирования, либо дезаминирования. В реакции переаминирования участвуют все аминокислоты за исключением лизина. В результате этой реакции образуются -кетокислоты.
Для животных тканей, растений и большинства микрорганизмов преобладающим типом реакций является окислительное дезаминирование аминокислот, за исключением гистидина, подвергающегося внутримолекулярному дезаминированию.
Окислительное дезаминирование аминокислот приводит к образованию аммиака и углеродного скелета в форме -кетокислоты. Эта реакция идет в две ступени: в первой – аминокислота окисляется до иминокислоты:
во второй – иминокислота превращается в кетокислоту:
В результате окислительного дезаминирования образуются -аминокислоты, которые могут включаться в цикл Кребса через пируват, ацетил-КоА, оксалоацетат,-кетоглутарат и т.д.
Например, при окислительном дезаминировании аланина образуется пируват:
Пируват, как было сказано ранее, является главным конечным продуктом процесса гликолиза при катаболизме углеводов. Далее ПВК в результате окислительного декарбоксилирования (этап III) превращается в ацетил-КоА, который окисляется в цикле Кребса (рис. 2, Приложение А).
Включение остальных аминокислот можно представить в виде общей сводной схемы:
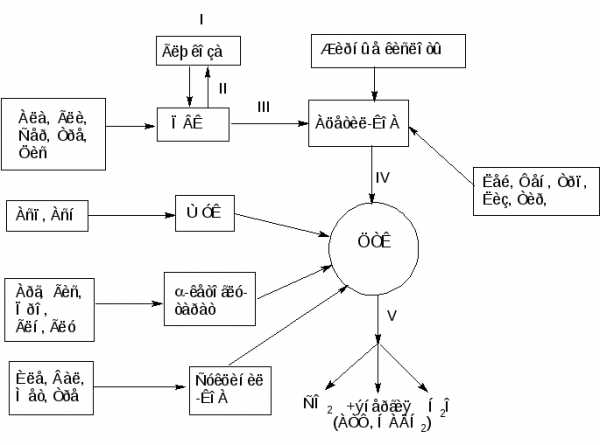
Рисунок 6 – Катаболизм аминокислот
Пять аминокислот (Фен, Лиз, Лей, Трп, Тир) считаются «кетогенными», поскольку они являются предшественниками кетоновых тел, в частности ацетоуксусной кислоты, в то время как большинство других аминокислот, обозначаемых как «гликогенные», служат в организме источником энергии, или углеводов, в частности глюкозы. Разделение аминокислот на «кетогенные» и «гликогенные» носит, однако, условный характер, поскольку отдельные участки углеродных атомов Лиз, Трп, Фен, Тир могут включаться и в молекулы предшественников глюкозы, например Фен и Тир – в фумарат. Истинно «кетогенной» аминокислотой является только Лейцин.
studfiles.net
1.3 Гидролитическое расщепление белков
|
| СООН | малатдегидрогеназа | СООН | ||||
|
|
|
| С O+ НАДН + Н+ | ||||
HO |
| С Н + НАД+ | ||||||
| ||||||||
| ||||||||
|
|
| СН2 | (цитоплазма) |
|
| Ch3 | |
|
|
|
|
|
| |||
|
|
| СООН |
|
|
| СООН | |
| малат |
| оксалоацетат | |||||
|
|
|
|
|
|
| (ЩУК) | |
2) Превращение оксалоацетата в фосфоенолпируват происходит в цитоплазме клетки:
СООН |
|
| Ch4 |
| ||||
С O + ГТФ | фосфоенолпируват- |
| Р +ГДФ + СО | |||||
| CH |
| O | |||||
|
|
| ||||||
карбоксикиназа |
| СООН | 2 | |||||
| ||||||||
| СООН |
|
|
| ||||
| фосфоенолпируват | |||||||
оксалоацетат | ||||||||
|
| (ФЕП) |
| |||||
| (ЩУК) |
|
|
| ||||
|
|
|
|
|
|
| ||
3) Образовавшийся фосфоенолпируват (ФЕП) по пути гликолиза превращается в ПВК (рис. 3), а пируват в результате окислительного декарбоксилирования в ацетил-КоА,который поступая в цикл Кребса, полностью окисляется до СО2 и Н2О, с выделением энергии.
С учетом выше сказанного, видно, что образовавшийся пропионил, в конечном счете, должен превратиться в ацетил-КоАи окислиться в цикле Кребса. Таким образом, все жирные кислоты в результатеβ-окисленияпревращаются в аце-тил-КоА,который сгорает в цикле Кребса (этап IV), (рис 2, Приложение А).
Главный, но возможно не единственный путь распада белков в организме – гидролиз. Гидролитический распад белков протекает в любой клетке организма в основном в специальных субклеточных элементах – лизосомах, где сосредоточены гидролитические ферменты и где осуществляется деструкция высокомолекулярных веществ до низкомолекулярных метаболитов.
Вместе с тем, определенная часть ферментов, ускоряющих распад белков, есть в цитоплазме клетки, а некоторые из них секретируются в желудочно-кишеч-ном тракте, обеспечивая внеклеточное переваривание белков.
Гидролиз белков может быть частичным (до пептидов) и полным (до аминокислот). При частичном (неполном) гидролизе в белковой молекуле распадаются лишь некоторые пептидные связи, как правило, по соседству со строго определенными амнокислотными радикалами. Этот процесс ускоряется специфическими протеолитическими ферментами (протеиназы).
В свою очередь пептиды гидролизуются до аминокислот при участии ряда пептидаз.
Следовательно, ферментный аппарат пищеварительного тракта осуществляет поэтапное, строго избирательное расщепление пептидных связей белко-
studfiles.net
Гидролитическое расщепление — белок — Большая Энциклопедия Нефти и Газа, статья, страница 1
Гидролитическое расщепление — белок
Cтраница 1
Гидролитическое расщепление белков под влиянием пепсина приводит к образованию смеси протеоз и пептонов. [1]
При полном гидролитическом расщеплении белков образуются аминокислоты. [3]
О степени гидролитического расщепления белка можно поэтому судить, определяя число освободившихся карбоксильных или аминных групп или тех и других одновременно. [4]
Протеазы — катализируют гидролитическое расщепление белков
В основе работы Сэнджера лежало гидролитическое расщепление белка на небольшие фрагменты и определение аминокислотной последовательности в них. Для гидролиза был использован набор специфических ферментов, каждый из которых был способен расщеплять полипептидную цепь в определенном месте. Сэнджер установил, что молекулу инсулина образуют две полипептидные цепи ( 21 и 30 аминокислотных остатков), связанные друг с другом дисульфидными связями ( — S-S -), которые образуются между остатками содержащей серу аминокислоты — цистеина. [6]
При повышении активности папаина увеличивается гидролитическое расщепление белков муки, клейковины, дрожжей и других растительных продуктов. Расщепление белков часто сопровождается снижением качества продуктов. [7]
Аналогичным образом устанавливается содержание всех других аминокислот, образующихся в результате гидролитического расщепления изучаемого белка. [8]
На стадии образования ацетил — КоА в процесс метаболизма, наряду с углеводами ( гексозами), вступают продукты гидролитического расщепления белков и жиров — аминокислоты, жирные кислоты, глицерин. [9]
К первому относятся денатурационные изменения белков под действием нагревания в присутствии воды, трения и давления, а также под действием растворителей. Второе связано с гидролитическим расщеплением белков, которое может протекать при обработке мятки и шрота водяным паром. К третьему направлению относятся взаимодействия свободных аминогрупп белков с разнообразными соединениями семян альдегидной и кетонной природы с образованием новых соединений. К этому направлению относятся также взаимодействия свободных аминогрупп с липидами, имеющими кислотные свойства, — фосфолипидами и свободными жирными кислотами. [10]
По положению амидной группы различают а -, Р — и другие аминокислоты. Все аминокислоты являются продуктами гидролитического расщепления белков и встречаются во всех тканях и жидкостях растений и животных. В клетке, где идет синтез белка, имеется более 20 различных аминокислот. Их чередование в полимерных молекулах обеспечивает все многообразие белковых форм. [11]
То обстоятельство, что полученные синтетически полипептиды в ряде случаев оказались тождественными природным пептидам, полученным при неполном гидролитическом расщеплении белков, не могло не привести к выводу, что полипептиды могут рассматриваться в качестве фрагментов сложных белковых молекул. Фишера также следовало, что белки представляют собой особый класс органических соединений. [12]
К последним принадлежит, например, кератин волпг и тпррсхи. Не изменяются под влиянием пепсина и наиболее просто построенные белки — пдотамдаы. Что касается коллагена, эластина и некоторых других белковых веществ опорных тканей, то они изменяются только при длительнрм воздействии пепсина. Легко расщепляются пепсином мышечные белки ( миозин и миоген), а также альбумины и глобулины как животного, так и растительного происхождения. Под влиянием пепсина происходит распад молекулы белка, который характеризуется расщеплением пептидных связей между определенными аминокислотами и соответственно увеличением количества свободных карбоксильных и аминных групп. Следовательно, пепсин осуществляет гидролитическое расщепление белка. [14]
Дальнейшее расщепление полипептидов происходит под действием пептидаз — карбоксипептидазы, амино-пептидазы и дипсптидаз. Карбоксипептидаза катализирует процесс гидролиза полипептида со стороны свободной карбоксильной группы. Лминопептидаза и дипепти-дазы содержатся в соке тонких кишок. Аминопсптидаза катализирует гидролитическое расщепление полипептида со стороны свободной аминогруппы. Дипептиды, образовавшиеся в результате действия перечисленных ферментов, расщепляются ( при участии дипептидаз) на свободные аминокислоты. Таким образом, конечными продуктами гидролитического расщепления белков и желудочно-кишечном тракте являются аминокислоты, которые и усваиваются организмом. [15]
Страницы: 1 2
www.ngpedia.ru
Крахмал расщепление гидролитическое — Справочник химика 21
Если к раствору крахмала прибавить незначительное ко—личество слюны, содержащей фермент амилазу, и через определенные промежутки времени к отдельным пробам добавлять раствор йода, то жидкость окрашивается сначала в синий, а затем в фиолетовый, красный, оранжевый и желтый (Цвет . Изменение окрасни в последовательно взятых порциях смеси обусловлено гидролитическим расщеплением крахмала амилазой слюны с образованием промежуточных продуктов распада—декстринов. Некоторые декстрины окрашиваются йодом в красный цвет. [c.103]Фермент амилаза катализирует гидролитическое расщепление крахмала с образованием мальтозы. Промежуточными продуктами могут быть различные декстрины. Степень гидролиза крахмала можно контролировать по цветной реакции с иодом. Крахмал дает с иодом синее окрашивание, декстрины в зависимости от размеров молекул окрашиваются иодом в разные цвета (фиолетовый, красно-бурый), а конечные продукты (мальтоза или глюкоза) с иодом окраски не дают. [c.75]
Так, нанример, дисахариды — сахароза и лактоза, несмотря на хорошую их растворимость в воде, непосредственно не всасываются в кишечнике. Они могут быть усвоены организмом лишь после расщепления на соответствующие моносахариды. Будучи же введены, минуя кишечник, непосредственно в кровь (парентерально), дисахариды тканями не используются и в основном выделяются с мочой в неизмененном виде. Что касается полисахаридов, представляющих собой еще более сложные углеводы, нерастворимые в воде, то они тем более пе могут быть непосредственно усвоены организмом. Будучи введены с пищей через рот, крахмал и гликоген подвергаются в пищеварительном тракте под действием соответствующих ферментов перевариванию, т. е. гидролитическому расщеплению. При 240 [c.240]
При ферментативном расщеплении крахмала было показано, что гликозидные связи атакуются четырьмя основными типами гидролитических ферментов 1) а-амилазой, катализирующей случайный равновероятностный гидролиз а-14-связей 2) Р-ами-лазой, катализирующей ступенчатый гидролиз чередующихся а-1- 4-связей 3) амилазами, которые катализируют ступенчатый [c.299]
После установления основного химического свойства крахмала— его гидролитического расщепления, стало ясно, что макромолекулы крахмала состоят из остатков циклической а-глюкозы. [c.298]
Гидролитическое расщепление углеводов — крахмала и гликогена — начинается во рту под влиянием ферментов амилазы и а-глюкозидазы (мальтазы), вырабатываемых слюнными железами. В желудке действие ферментов слюны [c.156]
При нагревании с кислотами или при действии амилаз крахмал подвергается гидролитическому расщеплению. В первом случае гидролиз доходит до конца с образованием в итоге d-глюкозы при действии же амилаз гидролиз доходит до образования мальтозы. В том и в другом случае гидролиз не идет сразу до конечных продуктов, но проходит через ряд промежуточных продуктов, называющихся декстринами, которые представляют углеводы с более короткой цепью, чем в крахмале. [c.174]
Другой метод, основанный на гидролитическом расщеплении углеводов (крахмал, древесная мука и сахар, особенно тростниковый), приводит к образованию смеси глицерина с другими гликоля-ми. При этом из ди- или полисахарида сначала получают гексозы, которые затем подвергают гидрогенизации в 40-50 % водном растворе в присутствии никеля (Р = 300 атм., 1= 80-180 °С). [c.9]
ГИДРОЛИТИЧЕСКОЕ РАСЩЕПЛЕНИЕ КРАХМАЛА [c.375]
Крахмал является важнейшим углеводом пищевых продуктов (хлеба, круп, картофеля). Большие его количества перерабатываются в патоку и глюкозу. Получение глюкозы и патоки из крахмала основано на гидролитическом его расщеплении под действием минеральных кислот. Удобнее всего использовать здесь серную кислоту, так как ее легко удалить в виде гипса после обработки мелом. [c.118]
Сахарозу и восстанавливающие раствор Фелинга моносахариды определяют этим раствором после проведения инверсии (вариант А). Нерастворенный крахмал определяют также раствором Фелинга после отделения его фильтрованием и гидролитического расщепления (вариант Б). Приведенными способами (А и Б) можно определить сахар или крахмал в концентрациях от 10 мг на 1 л воды. [c.374]
Растворимый крахмал — первичный продукт гидролитического расщепления картофельного крахмала, полученный путем обработки последнего разбавленной соляной кислотой. [c.133]
Глюкоза. -Глюкоза (стр. 285), или виноградный сахар — один из наиболее распространенных в природе моносахаридов. Она является составным элементом тростникового сахара (стр. 310), клетчатки (стр. 318) растительного и животного крахмала и других ди- и полисахаридов (стр. 310, 318). В технике глюкозу обычно получают гидролитическим расщеплением крахмала или клетчатки, а чистую -глюкозу — из тростникового сахара. Кристаллизуется -глюкоза в зависимости от условий кристаллизации (стр. 292) либо в а-пиранозной форме (т. плавл. 146°), либо в р-пиранозной форме (т. плавл. 148—150°). Оптические свойства глюкозы были рассмотрены на стр. 292 и 293. [c.295]
Гидролитическое расщепление- крахмала (исчезновение синей окраски с йодом) произойдет, только в присутствии амилазы (пробирка № У), а расщепление мочевины (появление розового окрашивания фенолфталеина) только в присутствии уреазы (пробирка 3). [c.41]
Продукты сельского и лесного хозяйства. Некоторые химические производства используют в качестве сырья продукты сельского лесного хозяйства. Так, например, у нас в СССР этиловый спирт производят сбраживанием глюкозы, образующейся при гидролитическом расщеплении клетчатки (из древесины) или крахмала (из хлебных злаков и картофеля). Из того же сырья получают витамин С и лимонную кислоту. Скипидар и канифоль производят сухой перегонкой древесины хвойных пород, витамин А, цит-раль и другие душистые вещества — из эфирных масел. [c.19]
При действии минеральных кислот полисахариды, не обладающие свойствами сахаров, распадаются на монозы. Чаще всего конечным продуктом полного гидролиза является О-глюкоза крахмал, гликоген, целлюлоза и лихенин при полном кислотном расщеплении образуют лишь виноградный сахар. Из других сложных углеводов в аналогичных условиях образуются манноза, галактоза, фруктоза или пентозы — арабиноза, ксилоза, фукоза. Многие относящиеся к этой группе несахароподобные полисахариды получили свои названия по конечным продуктам гидролитического расщепления, — например маннаны, галактаны, арабаны. [c.453]
Своеобразный весьма интересный класс каталитических реакций представляют собой реакции с участием энзимов. Некоторые авторы выделяют эту группу реакций в особый раздел — энзиматический метод анализа Эти реакции представляют особый интерес для биохимии, так как по их скорости можно определить концентрации энзимов, коэнзимов, субстрата и ингибиторов. В качестве ингибиторов могут иногда выступать ионы некоторых металлов (например, ионы меди при реакции гидролит
www.chem21.info
Гидролитическое расщепление жиро — Справочник химика 21
Работа 26. Гидролитическое расщепление жира при действий панкреатической липазы (гидролаза эфиров глицерина) [c.50]ЛИПАЗЫ (греч. lipos — жир) — ферменты, катализирующие гидролитическое расщепление жиров на глицерин и жирные кислоты. Л. содержатся в желудочном и кишечном соках, соке поджелудочной железы и в грудном молоке, в тканях животных и растений, а также [c.148]
Глицерин представляет собой трехатомный спирт. Он образуется при гидролитическом расщеплении жиров по следующей реакции [c.151]
Продукты, гидролитического расщепления жиров всасываются Б тонком кишечнике. Глицерин растворим в иоде и всасывается легко. Жирные кислоты образуют растворимые комплексные соединения с желчными кислотами (так называемые холеиновые кислоты), которые также всасываются в кишечнике. Холеиновые кислоты затем [c.185]
Работа 27. Кинетика гидролитического расщепления жира под действием липазы [c.51]
Техническая переработка жиров. В промышленности реакция гидролитического расщепления жиров широко используется для получения глицерина и жирных кислот или их солей, т. е. мыла. Расщепление проводят как в кислой, так и в щелочной [c.269]
В желудке жиры и липоиды не подвергаются значительному изменению, так как под влиянием имеющегося в желудке фермента липазы расщепляются только эмульгированные жиры (например, жир молока). Гидролитическое расщепление жиров и жироподобных веществ происходит в кишечнике под влиянием липазы и других ферментов, вырабатываемых поджелудочной железой. Небольшое количество липазы выделяется слизистой оболочкой кишечника и присутствует в кишечном соке. Липаза поджелудочной железы выделяется в малоактивной форме и активируется желчью. [c.137]
Какие ферменты производят гидролитическое расщепление жиров в органах и тканях [c.156]
Необходимо отметить, что термин омыление распространяют н на гидролитическое расщепление жиров, несмотря на то, что при гидролизе жира мыла (соли жирной кислоты) не образуются. Более того, омылением называют расщепление (гидролиз) любого сложного эфира, например уксусноэтилового, несмотря на то, чю продуктом расщепления явится в данном случае соль низкомолекулярной кислоты натриевая соль уксусной кислоты), которая мылом не является. [c.140]
Техническая переработка жиров. В промышленности реакция гидролитического расщепления жиров широко используется для получения глицерина и жирных кислот или их солей, т. е. мыла. Расщепление проводят как в кислой, так и в щелочной средах. В первом случае образуются глицерин и смесь свободных кислот — стеарин [c.275]
В Советском Союзе глицерин получают главным образом при гидролитическом расщеплении жиров. Этот процесс протекает при действии воды по следующему уравнению [c.54]
Скорость гидролитического расщепления жиров находится в прямой зависимости от концентрации водородных ионов, которые, как и ионы гидроксила, являются катализаторами этой реакции. В производстве при гидролизе жиров источником ионов водорода обычно служит серная кислота. Однако на этот про- [c.100]
Гидролиз жиров можно провести также с помощью концентрированной серной кислоты. Продукты взаимодействия серной кислоты с жирными кислотами глицеридов способствуют образованию тонкой эмульсии, вследствие чего поверхность соприкосновения воды с жиром увеличивается. Здесь свободная серная кислота действует как катализатор. При всех способах гидролитического расщепления жиров обязательным компонентом является вода. Без воды этот процесс невозможен, и он протекает значительно интенсивнее, когда ж р находится в виде высокодисперсной эмульсии. [c.101]
При щелочном расщеплении лсоли жирных кислот, называемые мылами. Поэтому процесс гидролитического расщепления жиров и был назван омылением. Так не совсем правильно называют и гидролиз других сложных эфиров. [c.347]
В промышленности глицерин получают главным образом при гидролитическом расщеплении жиров. В настоящее время технически разработан и находит также практическое применение способ получения глицерина из пропилена. [c.51]
Гидролитическое расщепление жиров осуществляется для разделения глицеридов на их составные части — на жирные кислоты и глицерин [c.105]
Липазы — катализируют гидролитическое расщепление жиров с образованием глицерина и соответствующих жирных кислот. [c.112]
Биологическое значение процесса эмульгирования жиров состоит в значительном увеличении площади поверхности контакта субстрата и фермента липазы при гидролитическом расщеплении жира, что проявляется в увеличении скорости процесса расщепления. [c.235]
Жиры обладают довольно большим поверхностным натяжением, которое спбсобствует сливанию их в общую массу. Фермент липаза не может проникнуть в глубь такой массы, а поэтому необходимым условием гидролитического расщепления жиров является их эмульгирование. В состоянии эмульсии поверхность жиров сильно увеличивается, что значительно облегчает и ускоряет действие липаз. Эмульгирование жиров происходит в тонких кишках. [c.61]
В технике гидролитическое расщепление жиров имеет очень большое значение и осуществляется при действии на жир водяного пара при повышенном давлении или воды при атмосферном давлении в присутствии катализаторов, оснований, кислот или ферментов. При нагревании жиров с водой при давлении 2,5 МПа (25 кгс/см ) и температуре 220°С происходит его расщепление с образованием жирных кислот и глицерина. На этом основан широко распространенный в СССР безреактивный метод расщепления жиров. [c.101]
При гидрогенизации кроме основных процессов отверждения жира протекают и побочные реакции, обусловливающие некоторые производственные потери. Так, при термическом распаде жира могут образовываться свободные жирные кислоты, акролеин и кетоны. Акролеин легко реагирует с водой, образуя гидрак-риловый альдегид СН2ОНСН2СНО. При высокой температуре гидрирования последний, взаимодействуя с водой, дает ацетальдегид, формальдегид, муравьиную кислоту и метанол. Попадание влаги делает возможным гидролитическое расщепление жира с образованием свободных жирных кислот и глицерина. Примеси водорода, поступающего на гидрогенизацию, СО2 и СО в присутствии катализатора восстанавливают
www.chem21.info
Гидролитическое расщепление связи — Справочник химика 21
Первому выражению [293] часто отдают предпочтение на том основании, что, подбирая соответствующие параметры, в том числе иногда очень большие значения п, с его помощью можно описать все три участка экспериментальных кривых у(К), хотя формальный характер этого уравнения очевиден. Второе уравнение—(5.10) [292], —по сути совпадающее с известным уравнением Журкова, имеет гораздо более определенный физический смысл и описывает кинетику гидролитического расщепления связей на фронте трещины. [c.96]Тетрагидрофуран получают из фурана гидрированием в присутствии никеля Ренея. Это лучший способ восстановления фурана, хотя реакция иногда сопровождается гидролитическим расщеплением связи С—О с раскрытием цикла. Большинство фуранов не удается восстановить при использовании металла в аммиаке, однако фуранкарбоновые кислоты [71] и третичные амиды [72] в этих условиях дают дигидропроизводные. [c.388]
Не очень высокая вяжущая активность щелочных боратных связок связана с относительной легкостью гидролитического расщепления связей В—О. [c.102]
При взаимодействии с концентрированной щелочью ( 5 М) происходит гидролитическое расщепление связей С—О и С—С и [c.637]
По предположению Шемякина, гидролитическое расщепление связи С=С протекает через стадию сравнительно легко осуществляющейся первичной гидратации [c.320]
Поскольку речь идет о химической стабильности связи 51—С, то дать ей общую характеристику невозможно. Рассмотрим ранее приведенный пример необыкновенной устойчивости тетраметилсилана к действию концентрированной серной кислоты и противоположный ему пример легкого гидролитического расщепления связи —С=С—81. Здесь решающим оказывается поведение органического радикала, связанного с кремнием, поведение других реагентов, условия реакции и влияние остальных заместителей. [c.201]
Эта реакция протекает обычно быстрее, чем гидролитическое расщепление связи 51—Н [ИбП. В настоящее время известны некоторые типы заместителей, которые повышают устойчивость [c.261]
Если метасистокс(и) обрабатывают этилмеркаптидом натрия, то реакция идет совершенно по другому пути. При этом происходит не гидролитическое расщепление связи Р—8, а отщепление метильной группы [101 с образованием метилэтилсульфида [c.461]
В настоящее время можно считать установленным, что гидролитическое расщепление связей по схеме [c.5]
Амфотерный характер гидроксида алюминия проявляется в том, что при добавлении к нему раствора щелочи снова происходит растворение осадка с образованием гидроксокомплек-сов. Можно предположить, что сначала происходит гидролитическое расщепление связей А1—О—А1 и образуются аквагидрок-сокомплексы А1(П1). При дальнейшем протолизе ОН -ионы становятся акцепторами протонов [c.385]
При замещении натрия в твердой лигносульфоновой кислоте, полученной из солянокислотного лигнина, водородом и при нагреве кислоты с водой происходило ее растворение. В результате кипячения с этанолом свободной лигносульфоновой кислоты была получена частично этоксилированная лигносульфоновая кислота. Поскольку солянокислотный лигнин был свободен от углеводов, растворение твердой лигносульфоновой кислоты могло явиться результатом только гидролитического расщепления связей между лигнинными структурными звеньями. [c.378]
Вообще говоря, пиперидеины и пирролины существуют преимущественно в иминной форме, а не в таутомерной енаминной N-aлкилпpoизвoдныe не имеют альтернативы и существуют только в форме енаминов. Эти циклические имины устойчивы к гидролитическому расщеплению связи Н=С в отличии от ациклических иминов, но тем не менее они легко вступают в реакции нуклеофильного присоединения по азометиновому атому углерода. Примером этому может служить тот факт, что и пиперидеин и пирролин существуют в виде тримеров, образующихся в результате нуклеофильного присоединения атома азота одной молекулы к азометиновому атому углерода другой молекулы, и т. д. [c.653]
Эрдман, один из первых исследователей изомеризации а-нафтил-аминсульфокислот и их солей, полагал, что термическая парегруппиров-ка нафтионатов обусловлена гидролитическим расщеплением связи С—5 с образованием а-нафтиламина и пиросульфата, которые при дальнейшем взаимодействии дают соль изомерной сульфокислоты [125] (см. также [132]). [c.146]
Направление, соответствующее константе представляет собой реакцию внутреннего аминолиза, а ксоответствуют процессу гидролитического расщепления амидиых и пептидных связей соответственно. При pH 5,0 Си (II) катализирует гидролитическое расщепление связей и несколько подавляет реакцию ами-нолиза. Уменьшение к под действием иона металла может быть связано с участием нуклеофильной аминогруппы 5 образовании комплекса, приводящем к снижению ее основности. [c.130]
Гидролитическое расщепление связи между атомами углерода-протекает тем легче, чем сильнее отяжелены кислородом соответствующие места молекулы. Применение этой реакции с препаративной целью ограничивается лишь немногими, однако имеющими большое значение областями, наиболее важной из которых является расщепление 1,3-дикетОнов и эфиров 1,3-кетокислот [см. примечание 112, стр. 656]. [c.521]
При разложении пентаборана дейтерированным спиртом СгНбОВ образуются ВН(ОС2Н5)2 и ВВ(ОС2Н5)2 в отношении 1 1 [42]. Это свидетельствует об образовании связи В—Н при гидролитическом расщеплении связи В—В. При алкоголизе пентаборана, так же как и при гидролизе, происходит последовательное отщепление борановых групп. [c.297]
Механизм термической деструкции пирронов аналогичен механизму деструкции полиимидов и Полибензимидазолов [50, 52]. Вода, выделяющаяся в результате дополнительной циклизации при температурах до 390 °С, вызывает гидролитическое расщепление связи СО [c.1025]
Гидролитическое расщепление связи кремний —цикл в 1-алкил-1 -триэтилсилил-ферроценах [557] [c.479]
Гидролитический путь разложения пестицидов в почве характерен для соединений, в состав которых входят амиды и эфиры. Основные из них — фенилкарбаматы (хлорИФК) и ацетамиды (пропанид). Их гидролиз в «почве состоит в разрыве амидной или эфирной связей и образовании анилина, углекислого газа и спирта (у фенилкарбама-тов) или анилина алифатической кислоты (у пропанида). Гидролитическое расщепление связано с быстрой детоксикацией исходного вещества. [c.55]
Гидролитическое расщепление связи С—В в присутствии солей металлов. Водные растворы солей некоторых переходных метал.лов реагируют с арилборньши кислотами следующим образом (Л1п1еу е1 а ., 1930). [c.101]
Будучи са
www.chem21.info
Гидролитическое расщепление белков
Главный, но возможно не единственный путь распада белков в организме – гидролиз. Гидролитический распад белков протекает в любой клетке организма в основном в специальных субклеточных элементах – лизосомах, где сосредоточены гидролитические ферменты и где осуществляется деструкция высокомолекулярных веществ до низкомолекулярных метаболитов.
Вместе с тем, определенная часть ферментов, ускоряющих распад белков, есть в цитоплазме клетки, а некоторые из них секретируются в желудочно-кишечном тракте, обеспечивая внеклеточное переваривание белков.
Гидролиз белков может быть частичным (до пептидов) и полным (до аминокислот). При частичном (неполном) гидролизе в белковой молекуле распадаются лишь некоторые пептидные связи, как правило, по соседству со строго определенными амнокислотными радикалами. Этот процесс ускоряется специфическими протеолитическими ферментами (протеиназы).
В свою очередь пептиды гидролизуются до аминокислот при участии ряда пептидаз.
Следовательно, ферментный аппарат пищеварительного тракта осуществляет поэтапное, строго избирательное расщепление пептидных связей белковой молекулы вплоть до конечных продуктов гидролиза белков – свободных амнокислот.
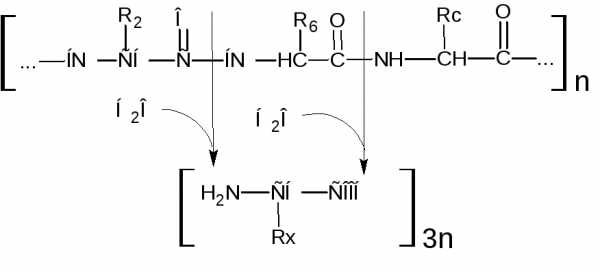
Свободные аминокислоты могут подвергаться дальнейшему распаду, включаясь в гликолиз или сразу же в цикл Кребса (рис. 2, Приложение А).
Катаболизм аминокислот
Первая реакция, которой подвергается аминокислота при катаболизме, это реакция освобождения от аминогруппы, которая может осуществляться либо путем переаминирования, либо дезаминирования. В реакции переаминирования участвуют все аминокислоты за исключением лизина. В результате этой реакции образуются -кетокислоты.
Для животных тканей, растений и большинства микрорганизмов преобладающим типом реакций является окислительное дезаминирование аминокислот, за исключением гистидина, подвергающегося внутримолекулярному дезаминированию.
Окислительное дезаминирование аминокислот приводит к образованию аммиака и углеродного скелета в форме -кетокислоты. Эта реакция идет в две ступени: в первой – аминокислота окисляется до иминокислоты:
во второй – иминокислота превращается в кетокислоту:
В результате окислительного дезаминирования образуются -аминокислоты, которые могут включаться в цикл Кребса через пируват, ацетил-КоА, оксалоацетат,-кетоглутарат и т.д.
Например, при окислительном дезаминировании аланина образуется пируват:
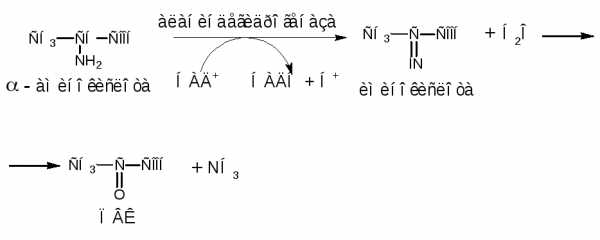
Пируват, как было сказано ранее, является главным конечным продуктом процесса гликолиза при катаболизме углеводов. Далее ПВК в результате окислительного декарбоксилирования (этап III) превращается в ацетил-КоА, который окисляется в цикле Кребса (рис. 2, Приложение А).
Включение остальных аминокислот можно представить в виде общей сводной схемы:
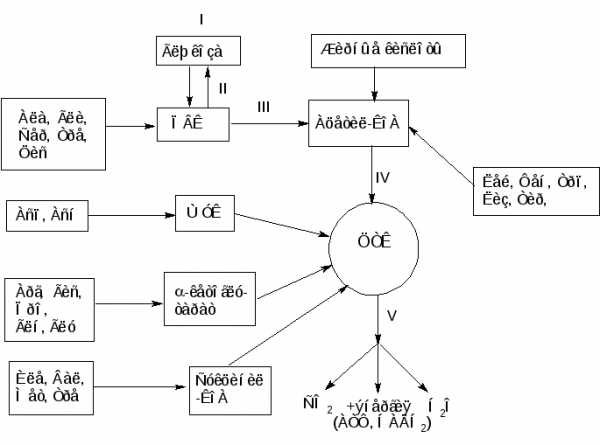
Рисунок 6 – Катаболизм аминокислот
Пять аминокислот (Фен, Лиз, Лей, Трп, Тир) считаются «кетогенными», поскольку они являются предшественниками кетоновых тел, в частности ацетоуксусной кислоты, в то время как большинство других аминокислот, обозначаемых как «гликогенные», служат в организме источником энергии, или углеводов, в частности глюкозы. Разделение аминокислот на «кетогенные» и «гликогенные» носит, однако, условный характер, поскольку отдельные участки углеродных атомов Лиз, Трп, Фен, Тир могут включаться и в молекулы предшественников глюкозы, например Фен и Тир – в фумарат. Истинно «кетогенной» аминокислотой является только Лейцин.
studfiles.net

Leave A Comment