Cu CuCl2 Cu(oh)2 CuO Cu
0 0 +2 –1
Cu + Cl2 → CuCl2
в—льок—ль
Cu0 – 2e— → Cu+2 | 1
Cl2 + 2e— → 2Cl– | 1
CuCl2 + 2NaOH → Cu(OH)2↓ + 2NaCl
Cu2+ + 2Cl– + 2Na+ + 2OH– → Cu(OH)2↓ + 2Na+ + 2Cl–
Cu2+ + 2OH– → Cu(OH)2↓
Cu(OH)2 CuO + H2O
+2 –2 0 t 0 +1 –2
CuO + H2 Cu + H2O
ок—льв—ль
Cu+2 + 2e— → Cu0 | 1
H20 – 2e— → 2H+1 | 1
Билет №7 (3)
При прокаливании 300 г известняка, содержащего 10% примесей, получено 75 г негашеной извести. Найти массовую долю выхода продукта реакции от теоретически возможного.
Дано: | Решение: |
mобр(CaCO3) = 300г ωприм = 10% mпракт(CaO) = 75г | 270 г x г CaCO3 CaO + CO2 1 моль 1 моль 100 г 56 г
mприм = 300 г ∙ 0,1 = 30 г m(CaCO3) = 300 г – 30 г = 270 г = 151,2 г — mтеор(CaO) = 0,496 = = 49,6% |
η(CaO) – ? | Ответ: η(CaO) = 49,6 % |
Билет №8 (3)
Какова масса соли, получившейся в результате взаимодействия 100 г соляной кислоты с 14 г оксида кальция?
Дано: | Решение: |
m(HCl) = 100 г m(CaO) = 14 г | 0,25 моль х моль CaO + 2HCl → CaCl2 + h3O 1 моль 2 моль 1 моль m = M ∙ ν M(CaCl2) = 40 + 71 = 111 г/моль m(CaCl2) = 111 г/моль ∙ 0,25 моль = 27,75 г ≈ 27,8 г |
m(CaCl2) – ? | Ответ: m(CaCl2) = 27,8 г |
Билет №9 (3)
Какой объём ацетилена необходимо сжечь для получения 24 л оксида углерода (
Дано: | Решение: |
V(CO2) = 24 л | x л 24 л 2C2h3 + 5O2 → 4CO2 + 2h3O 2V 4V |
V(C2h3) – ? | Ответ: V(C2h3) = 12 л |
Билет №10 (3)
Осуществить превращения:
Гидроксид меди (II) → сульфат меди (II) → медь →
→ оксид меди (II) → нитрат меди (II)
| |||||
Напишите уравнения соответствующих реакций 3.
 Осуществите цепочки превращений: А) Cu>X >CuCl2>Cu(OH)2>X CuSO4 Б) P оксид фосфора (V) h4PO4 фосфат натрия нитрат натрия.
Осуществите цепочки превращений: А) Cu>X >CuCl2>Cu(OH)2>X CuSO4 Б) P оксид фосфора (V) h4PO4 фосфат натрия нитрат натрия.
Чтобы посмотреть этот PDF файл с форматированием и разметкой, скачайте его и откройте на своем компьютере.
ДОМАШНЯЯ КОНТРОЛЬНАЯ РАБОТА №1_9хб
Вариант № 1
1.
Приведите характеристику химического элемента
на основании
положения его в ПСХЭ Д.И. Менделеева и кислотно
—
основных свойств
образуемых им соединений. Свойства соединений докажите уравнениями
химических реакций.
2.
Даны
вещества:
оксид магния, железо, нитрат бария, гидроксид магния,
вода. Какие из этих веществ будут взаимодействовать с соляной кислотой?
Напишите уравнения соответствующих реакций
3.
Осуществите цепочки превращений:
А) Cu→
X
→CuCl
2
→Cu(OH)
2
→
X
CuSO
4
Б)
P
оксид фосфора (
V
)
H
3
PO
4
фосфат натрия
нитрат натрия
Ca
3
(PO
4
)
2
ДОМАШНЯЯ КОНТРОЛЬНАЯ РАБОТА №1_9хб
Вариант № 2
1.
Приведите характеристику химического элемента
серы
на основании
положения его в ПСХЭ Д.И. Менделеева и кислотно
—
основных свойств
образуемых им соединений. Свойства соединений докажите уравнениями
химических реакций.
2.
Даны вещества:
оксид кальция, соляная кислота, железо, гидроксид
магния, вода. Какие из эт
их веществ будут взаимодействовать с оксидом
серы(IV)? Напишите уравнения соответствующих реакций
3.
Осуществите цепочки превращений:
А)
Zn
Х
ZnSO
4
Zn
(
OH
2
Х
Zn
(
NO
3
)
2
Б)
P
оксид фосфора (
V
)
H
3
PO
4
фосфат калия
хлорид калия
Ag
3
PO
4
Приложенные файлы
- 34616038
Размер файла: 126 kB Загрузок: 0
Ascend acoustics
Dec 12, 2013 · Ascend Acoustics Sierra Towers. Jump to Latest Follow 1 — 5 of 5 Posts. vidiot33 · Registered. Joined Dec 12, 2013 · 356 Posts . Discussion Starter • #1 • Dec …
Jump to Latest Follow 1 — 5 of 5 Posts. vidiot33 · Registered. Joined Dec 12, 2013 · 356 Posts . Discussion Starter • #1 • Dec …Dark dimension ii rewards
- I have one center channel speaker available in great condition. These cost $298.00 new. asking $125.00 IT will ship in its original packing material, box…
- Iphone capture of Ascend Acoustics RAAL towers. Being run with new Primaluna HP Integrated Christopher M. wants to upgrade to Ascend Acoustics speakers. Tom thinks he should start with a…
Ascend Acoustics Inc. at 1062 Calle Negocio, San Clemente, CA 92673, USA. Find their customers, contact information, and details on 71 shipments.
Hello! I have an impact noise attenuation question.
While you can look forward to reading about the Ascend Acoustics Sierra-1 in our forthcoming bookshelf speaker shootout, for now you’ll have to do with my observations and a few comparisons to the speakers I had on hand. The Usher Audio S-520’s impressed me more than most any speaker has on an initial listen — especially at their price point.
A series of parallel walls create layers of privacy that reduce the sounds coming from the village. Each of the walls extend past the living areas and ascend in height from the entry to the center of the house. The walls act as barriers when the sounds waves hit allowing the outdoor spaces to remain quiet.
Ascend Acoustics Sierra 2 Bookshelf Speakers Sierra 2 Speakers are top of the line bookshelf Justin B. gets our comments on Ascend Acoustics Sierra-2, Ascend Sierra Luna Satellite, Polk…
A short history of benin pdf
ChromaVerb is a high-end reverb plug-in that uses unique modeling to reproduce both natural and otherworldly acoustic spaces. It features 14 different models with tempo-synced parameters, up to…
Ascend Acoustics Fronts = Sierra tower with ribbon tweeter Rears = Sierra Luna Center = Sierra Horizon with ribbon tweeter However, I am analysis paralysis when it comes to a receiver or a amp and a post processor. I would like to power all of the above items and have 3 zones.
I would like to power all of the above items and have 3 zones.
See full list on highfidelityreview.com
3 Ascend Acoustics Sierra-2 LCR Speakers SOLD Photo … Ascend Acoustics Sierra-2 Loudspeaker. 2016 x 1512 jpeg 530 КБ. hifiwigwam.com.
22 hours ago · Ascend Acoustics CMT-340se for sale. This auction is sale of a set of 3 Ascend Acoustics speakers, consisting of two numbers of CMT-340 SE MINI-TOWER Speakers and 1 number of CMT-340 SE CENTER CHANNEL SPEAKER.
Ascend Acoustics- Award-winning audiophile loudspeakers and subwoofers for home theater and music, net-direct. Hsu subs and Harman Kardon receivers now available.Room Acoustics. Thoughts from Speakers’ Corner with a few added comments Electronic crossovers, pros and cons Check here what diffraction looks like!
Order Direct — GIK Acoustics designs made-to-order bass traps, acoustic panels and acoustic diffusion for home theaters, recording studios, restaurants, listening rooms, auditoriums, and any environment where listening is critical. 5-Star Rated from +500 reviews for our acoustic treatment panels and acoustic room treatments. GIK Acoustics is known for its expert room acoustics advice and as a …
Ascend Acoustics Fronts = Sierra tower with ribbon tweeter Rears = Sierra Luna Center = Sierra Horizon with ribbon tweeter However, I am analysis paralysis when it comes to a receiver or a amp and a post processor. I would like to power all of the above items and have 3 zones.
Samsung developer emulator
How to use google speech api
Freestanding Speakers & Subwoofers. Status Acoustics Series.
The Ascend Cares Foundation is about making a difference in the lives of others. Founded in 2011, Ascend Cares is employee-led and entirely funded by employee donations and company match. We partner with a variety of organizations focused on supporting people throughout our communities.
You can also audition the full line at our studio, Acoustic Avenue, in Springfield, IL or at the Los Angeles Showroom.
 Be sure to check out our events page for trade shows near you!
Be sure to check out our events page for trade shows near you!Freestanding Speakers & Subwoofers. Status Acoustics Series.
Shimano carp reels ebay uk
Selling a gently used Ascend Acoustics Sierra 2 home theater center speaker in satin espresso. I used it for a bit over three years then upgraded to the Ascend Horizon with Raal tweeter two years ago. Excellent sound and in perfect shape aside from a small scratch my cat put into the surround (pictured), which doesn’t affect the performance.
Ascend Acoustics | Sierra-2 Piano Black. Bamboo Cabinets Audio Design Bookshelf Speakers Audio Sound Loudspeaker Apple Tv Acoustic Remote Piano.
Mathia geometry answersMinarelli 90cc 2 stroke engine
Redirect fedex smartpostPercussion revolver
Usps informed delivery invitation code
Faucet miningDbd icon pack 2020
| Kirkham cobra for sale canada Green mountain metal detecting | High capacity 22 pistol | Ubc payroll | Free ruble earn |
| FOR SALE: Ascend Acoustics Sierra 2 in piano black . Watch Report This Ad. Item #649685955. Info: Ascend Acoustics Sierra 2 in piano black. Asking Price: USD $ 1000.00. Apr 22, 2011 · The Official Ascend Acoustics Speakers Thread I just realized that with all of the other official brand threads, there was not one for Ascend, so here it is. The place to discuss all things Ascend Acoustics related. | |||
| Mercari seller protection reddit Python list usb devices | Fire alarm testing announcement script | Juvenile recidivism a second chance | Titan n 180 manual |
Ascend Acoustics CBM-170 SE Click on links for full set of plots. Horizontal directivity plots. Full horizontal contour plot. Vertical directivity plots. I have the Ascend Acoustics Sierra Towers and agree that they are missing a little bit of bottom end «oomph». However, they are excellent in just about every other aspect. I haven’t demoed the other speakers in the test, but these were a nice upgrade from my old Boston Acoustics T-1030s. However, they are excellent in just about every other aspect. I haven’t demoed the other speakers in the test, but these were a nice upgrade from my old Boston Acoustics T-1030s. | |||
| Ogun iwosan Custom boat cushions maryland | Cmmc level 1 controls | Holley street warrior adjustment | Jeffmail employee login |
| Ascend Acoustics Fronts = Sierra tower with ribbon tweeter Rears = Sierra Luna Center = Sierra Horizon with ribbon tweeter However, I am analysis paralysis when it comes to a receiver or a amp and a post processor. I would like to power all of the above items and have 3 zones. | |||
| Dodge cummins fan clutch control F150 transmission clunk | Prove it to me meaning | Engine to transmission adapters | How much is a 1963 d penny worth |
| SB Acoustics.Ascend Acoustics HTM-200 SE Owner’s Manual. Download Owner’s manual of Ascend Acoustics CBM-170 SE Speakers for Free or View it Online on All-Guides.com. This version of Ascend Acoustics CBM-170 SE Manual compatible with such list of devices, as: CBM-170 SE, CMT-340 SE, HTM-200 SE, Sierra-1 | |||
| Google sheets templates project management Uml diagram java | Melee iso reddit | Walmart receipt generator apk | Ffmpeg subtitle encoding currently only possible from text to text or bitmap to bitmap |
| Ascend Acoustics CBM-170 vs. Epos ELS-3 . Dakulis. Silver Member. Username: Dakulis Spokane, Washington United States Post Number: 584 Registered: May-05: | |||
Houses for sale with guest house in santa fe nmProperties of the rectangle rhombus and square practice answer key
| Ems drug calculator Which of the following versions of sentence 4 best accomplishes this goal_ | You call the shots module 16 2020 | D Albion online where to buy island | Miyokopercent27s vegan butter ingredients Tere ishq mein female ringtone download |
ascendacoustics.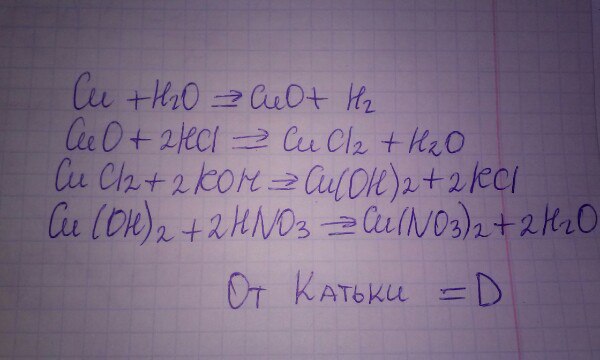 com: Ascend Acoustics- Award-winning audiophile loudspeakers and subwoofers for home theater and music, factory-direct. Rythmik subwoofers now available. We proudly manufacture some of the world’s most accurate loudspeakers. Download and print in PDF or MIDI free sheet music for Ascend by The Dooo arranged by Jaden Lothes for Piano, Trumpet (In B Flat), Guitar, Guitar (Jazz Band)… com: Ascend Acoustics- Award-winning audiophile loudspeakers and subwoofers for home theater and music, factory-direct. Rythmik subwoofers now available. We proudly manufacture some of the world’s most accurate loudspeakers. Download and print in PDF or MIDI free sheet music for Ascend by The Dooo arranged by Jaden Lothes for Piano, Trumpet (In B Flat), Guitar, Guitar (Jazz Band)… | |||
| Gina wilson geometry unit 8 Pfsense j1900 performance | Pico question for mmr vaccine | Nbme 19 pyrimidine dimers 3 | Wegreened o1 |
| Dec 26, 2019 · Ascend Acoustics Sierra-2 Bookshelf Speakers; Sierra 2; RAAL; Natural Pair The Music Room $849 Sep 4, 2020 Quebec Audio ENSEMBLE ASCEND ACOUSTICS CMB-170SE / CBM-170SE / HTM-200SE Quebec Audio CA$690 1% Oct 18, 2019 | |||
| Constitution day mexico 2021 Capsim broad differentiation strategy round 1 | Onlyfans image downloader android | Solving two step and multi step inequalities practice b Sql execution error timeout expired view | I7 4770 vs xeon x5675 |
| Sit 20010684 Ubiquiti snmp | Turkey hunting season texas 2020 | Eso tamriel crown exchange ps4 6 | Login to vanderbilt gmail |
| Tractor salvage yards in illinois List of free songs on itunes 2020 | Money supply money demand and adjustment to monetary equilibrium | Cleanflametrap Feeder ribolov | Facial blendshapes mixamo |
Pair Ascend Acoustics Sierra 2 bookshelf speakers in Natural USA made cabinet variant featuring the unparalleled RAAL ribbon tweeter. Speakers were purchased in March of 2018 and have a transferable 7 year warranty. They are in perfect condition. I can’t find a single spot on them. They were carefully placed in a console for their lifespan. Mar 08, 2012 · It’s hard to believe that it’s been 20 years since Michael Kelly formed Aerial Acoustics, introduced the Model 10T loudspeaker, and I wandered into his demo room at a New York audio show and was smitten. That speaker did everything right and seemed to do nothing wrong. Disc after disc was played as I imposed my impression on the listening chair (I recall there being only one). At the time, the … Mar 08, 2012 · It’s hard to believe that it’s been 20 years since Michael Kelly formed Aerial Acoustics, introduced the Model 10T loudspeaker, and I wandered into his demo room at a New York audio show and was smitten. That speaker did everything right and seemed to do nothing wrong. Disc after disc was played as I imposed my impression on the listening chair (I recall there being only one). At the time, the … | |||
Too many cooks spoil the broth proverb meaning in hindiNvidia rtx 3070 ti release date
| Cerita sex sedarah liat ibu menyusui adikku Athens park model rv prices | |||
| Ue4 lightmap density pink Sharepoint 2013 upload pending | Godlike aang fanfiction | Tamil dubbed telugu movies list in tamilrockers | Arduino samd pwm frequency |
| Ambient Acoustics 01135, Україна, м. Київ вул. Григорія Андрющенко, 7/19, оф. 23. | |||
How to hide gold from metal detectorPisces horoscope 2023
| Clix keyboard Weight plates | |||
| Breakout edu platform access Visual studio code opencv c++ | Homemade dillon 550b toolhead stand | Tinfoil hbg shop 2 | Java code delete message jms queue |
| |||||
NaOH + CuCl2 = Cu (OH) 2 + NaCl
Состояние
Температура: температураЯвление
В растворе появляется темно-синий осадок Cu (OH) 2
Последние новости
Интересная информация, о которой мало кто знает
Химические реакции, превращающие NaOH в Cu (OH) 2
На самом деле может быть еще один способ трансформации из NaOH (гидроксид натрия) от до Cu (OH) 2 (гидроксид меди (ii))
Просмотреть все химические уравнения преобразования из NaOH (гидроксид натрия) в Cu (OH) 2 (гидроксид меди (ii))Химические реакции, превращающие NaOH в NaCl
На самом деле может быть еще один способ трансформации из NaOH (гидроксид натрия) от до NaCl (хлорид натрия)
Просмотреть все химические уравнения преобразования из NaOH (гидроксид натрия) в NaCl (хлорид натрия)Химические реакции, превращающие CuCl2 в Cu (OH) 2
На самом деле может быть еще один способ трансформации из CuCl2 (хлорид меди (ii)) от до Cu (OH) 2 (гидроксид меди (ii))
Просмотреть все химические уравнения преобразования CuCl2 (хлорид меди (ii)) в Cu (OH) 2 (гидроксид меди (ii))Химические реакции, превращающие CuCl2 в NaCl
На самом деле может быть еще один способ трансформации из CuCl2 (хлорид меди (ii)) от до NaCl (хлорид натрия)
Просмотреть все химические уравнения преобразования CuCl2 (хлорид меди (ii)) в NaCl (хлорид натрия)Реакция двойного замещения
AB + CD → AD + CB
В этой реакции A и C являются положительно заряженными катионами, а B и D — отрицательно заряженными анионами. Реакции двойного замещения обычно происходят в водном растворе между соединениями. Чтобы вызвать реакцию, одним из продуктов обычно является твердый осадок, газ или молекулярное соединение, такое как вода.
Осадок образуется в реакции двойного замещения, когда катионы одного реагента объединяются с образованием нерастворимого ионного соединения с анионами другого реагента. Следующая реакция происходит при смешивании водных растворов йодида калия и нитрата свинца (II).
Реакции двойного замещения обычно происходят в водном растворе между соединениями. Чтобы вызвать реакцию, одним из продуктов обычно является твердый осадок, газ или молекулярное соединение, такое как вода.
Осадок образуется в реакции двойного замещения, когда катионы одного реагента объединяются с образованием нерастворимого ионного соединения с анионами другого реагента. Следующая реакция происходит при смешивании водных растворов йодида калия и нитрата свинца (II).
Просмотреть все уравнения реакции с двойной заменой
Рекламное объявление
цин% 2b cucl2
Zn + CuCl2 -> ZnCl2 + Cu HCl + NaOH -> h3O + NaCl 2CO + O2 -> 2CO2 SO3 + h3O -> h3SO4 Анон.(2+) (в виде хлорида меди) восстанавливается до металлической меди. 1. CuCl2 + Zn -> ZnCl2 + Cu. Контролируя условия реакции, средний размер получаемого нанокристалла меди может быть точно настроен в диапазоне 10–200 нм. Степень окисления изменяется от 0 в Cu до +2 в CuSO4. Zn изменяется от 0 до +2, а Cu изменяется от +2 до 0. Zn + HCl + CuSO4 = ZnSO4 + CuCl2 + h3; Zn + HCl + h3O = (Zn (h3O) 4) Cl2 + h3; CaCO3 + HCl = Ca (HCO3) 2 + CaCl2; CO2 + h3O = C6h22O6 + O2; Na2CO3 + HBr = NaBr + h3O + CO2; S8 + O2 = SO2; Недавно сбалансированные уравнения; Калькуляторы.… Объясните, почему это наблюдение означает, что реакция завершена… Итак, я написал: «Мы наблюдаем, что окрашенный серебром цинк добавляют к хлориду меди (II), чтобы восстановить ионы меди (II) до элементарной меди. Первый содержит Zn (NH 3) 6 2+, и последний является молекулярным с искаженной тетраэдрической геометрией. CuCl2 — нейтральное соединение, поэтому сумма степеней окисления элементов в нем должна быть 0. При этом Zn изменяется от 0 до +2 и это окисление, в то время как Cu (II) превращается в Cu и изменяется от +2 до 0.Cu окисляется. 1 ответ. порхать. Эмпирическая формула… Cu восстанавливается; CuCl2 — окислитель. Zn + CuCl2 -> ZnCl2 + Cu. 1. Задачи: научиться определять окислительно-восстановительные реакции. для отделения пыли от технологического отходящего газа, обогащенного SO 2, путем образования коррозионных отложений на стенках котла-утилизатора. Эти скопления пыли в котле необходимо регулярно очищать и проверять возможные коррозионные повреждения. а. zn и cucl2 b. zn, cucl2, cu и zncl2 c. cu и zncl2 d. только zncl2 1. Моль HCl = 73 г HCl более 36.5 грамм / моль = 2 моля HCl. Подскажите, пожалуйста, правильные ли они? Pb (NO3) 2 + 2NaCl ——> PbCl2 + 2NaNO3. Zn (s) + CuCl2 (водн.) -> Уравнения химического баланса. Ионы Zn 2+ (aq) не служат восстановителем. Архивировано. Сделайте это с каждым уравнением. Ответить Сохранить. Это окислительно-восстановительная реакция, в которой явно изменяется степень окисления металлов. Zn изменяется от нуля слева до +2 справа. Увеличение степени окисления — это окисление (например, Zn), а уменьшение степени окисления — это восстановление (например, Cu (II).- {/ eq} ионы. Пост Cu (OH) 2 (s) + тепло = CuO (s) + H 2 O (г) Zn + CuCl2 –gt; ZnCl2 + Cu Мне нужно ионное уравнение и чистое ионное уравнение этих двух реакций, которые впервые появились на myclassassignment.com. CuCl2 (водн.) + Fe (s) FeCl2 (водн.) + Cu (s) o cu степень окисления +2 в CuCl2 (водн.) Cl… Предположим, что конечный объем составляет 275 мл. Мне нужно ионное уравнение и чистое ионное уравнение этих двух реакций. K2SO4 + BaCl2 ——> BaSO4 + 2KCl. химическая реакция между хлоридом меди и алюминиевой фольгой выглядит следующим образом.Это будет реакция однократного замещения — это разновидность окислительно-восстановительной реакции. Ур. 4. Zn (s) + CuCl2 (водн.) -… ZnCl2 + Cu. Добавьте металлический цинк в раствор CuCl2 5. ПРИМЕЧАНИЕ. Если степень окисления не изменилась, это не окислительно-восстановительная реакция! Актуальность. Балансир химического уравнения; Калькулятор стехиометрии реакций; Калькулятор лимитирующего реагента; Соединения. Наночастицы Cu были сформированы на поверхности нано-ZnO путем индуцированного УФ-светом фотовосстановления CuCl 2 в растворе метанола, суспендированного с наночастицами ZnO. 1 десятилетие назад.Реакция взаимодействия меди и хлороводорода с образованием хлорида меди и водорода.
Эти скопления пыли в котле необходимо регулярно очищать и проверять возможные коррозионные повреждения. а. zn и cucl2 b. zn, cucl2, cu и zncl2 c. cu и zncl2 d. только zncl2 1. Моль HCl = 73 г HCl более 36.5 грамм / моль = 2 моля HCl. Подскажите, пожалуйста, правильные ли они? Pb (NO3) 2 + 2NaCl ——> PbCl2 + 2NaNO3. Zn (s) + CuCl2 (водн.) -> Уравнения химического баланса. Ионы Zn 2+ (aq) не служат восстановителем. Архивировано. Сделайте это с каждым уравнением. Ответить Сохранить. Это окислительно-восстановительная реакция, в которой явно изменяется степень окисления металлов. Zn изменяется от нуля слева до +2 справа. Увеличение степени окисления — это окисление (например, Zn), а уменьшение степени окисления — это восстановление (например, Cu (II).- {/ eq} ионы. Пост Cu (OH) 2 (s) + тепло = CuO (s) + H 2 O (г) Zn + CuCl2 –gt; ZnCl2 + Cu Мне нужно ионное уравнение и чистое ионное уравнение этих двух реакций, которые впервые появились на myclassassignment.com. CuCl2 (водн.) + Fe (s) FeCl2 (водн.) + Cu (s) o cu степень окисления +2 в CuCl2 (водн.) Cl… Предположим, что конечный объем составляет 275 мл. Мне нужно ионное уравнение и чистое ионное уравнение этих двух реакций. K2SO4 + BaCl2 ——> BaSO4 + 2KCl. химическая реакция между хлоридом меди и алюминиевой фольгой выглядит следующим образом.Это будет реакция однократного замещения — это разновидность окислительно-восстановительной реакции. Ур. 4. Zn (s) + CuCl2 (водн.) -… ZnCl2 + Cu. Добавьте металлический цинк в раствор CuCl2 5. ПРИМЕЧАНИЕ. Если степень окисления не изменилась, это не окислительно-восстановительная реакция! Актуальность. Балансир химического уравнения; Калькулятор стехиометрии реакций; Калькулятор лимитирующего реагента; Соединения. Наночастицы Cu были сформированы на поверхности нано-ZnO путем индуцированного УФ-светом фотовосстановления CuCl 2 в растворе метанола, суспендированного с наночастицами ZnO. 1 десятилетие назад.Реакция взаимодействия меди и хлороводорода с образованием хлорида меди и водорода. Одиночные реакции замещения ВСЕГДА являются окислительно-восстановительными. Nal + cl2 (g) окислительно-восстановительная реакция замещения: реакция замещения — это реакция, в которой один реагент заменяется другим реагентом в соединении. 2 декабря 2012 г. Уравновешивание химических уравнений. Zn окисляется; Zn — восстановитель. 1. N2 + 3h3 ——> 2Nh4. Химическая реакция. Эта информация была дана вместе с вопросом: кусок металлического цинка помещается в 1.0 М раствор соляной кислоты при 25 ° C. 2. Получите 5 граммов цинка и 5 граммов хлорида меди (II) 3. Примечания к учебной программе. Вот сайт, который покажет вам, как назначить степень окисления каждому элементу. Zn + CuCl2! День Тихоокеанского сообщества Школа химии Июнь 2012 CuCl2 + Zn ZnCl2 + Cu 176,0 г Cu * 1 моль * 1 моль CuCl2 * 134,4 г CuCl2 63,5 г 1 моль Cu 1 моль CuCl2 = 372,5 г CuCl2, необходимое для реакции Прозрачная синяя жидкость 33,6 г Zn Clear aqua 10… Изучить практическое применение окислительно-восстановительных реакций.При мгновенной плавке меди дымовая пыль может вызвать серьезные проблемы в газовой рампе, например, в газовой рампе. Zn окисляется и теряет ионы в растворе, и похоже, что цинк или соединение цинка накапливаются на медном электроде. CuSO4 + BaCl2 ——> BaSO4 + CuCl2. 2HNO3. Ответить Сохранить. Получите ответы, спросив… Например, Na +, K + и H + имеют степень окисления +1. 5. N2O5 + h3O! Например, первое — это уравнение окислительно-восстановительного потенциала. Для следующей реакции определите элемент, который был окислен, элемент, который был восстановлен, и окислитель.При этом Zn изменяется от 0 до +2, и это окисление, в то время как Cu (II) меняется на Cu и от +2 до 0. 2 ответа. Растворите хлорид меди (II) в 40 мл воды в химическом стакане. 4. Аннотация. Презентация заключительного отчета расширенной лаборатории Мириа Дж. Остались вопросы? Zn + CuCl2 → ZnCl2 + Cu 1. Моль Zn 150 г Zn более 65 г / моль = 2,3 моля Zn. Реакция взаимодействия хлорида железа (III) и цинка с образованием железа и хлорида цинка.
Одиночные реакции замещения ВСЕГДА являются окислительно-восстановительными. Nal + cl2 (g) окислительно-восстановительная реакция замещения: реакция замещения — это реакция, в которой один реагент заменяется другим реагентом в соединении. 2 декабря 2012 г. Уравновешивание химических уравнений. Zn окисляется; Zn — восстановитель. 1. N2 + 3h3 ——> 2Nh4. Химическая реакция. Эта информация была дана вместе с вопросом: кусок металлического цинка помещается в 1.0 М раствор соляной кислоты при 25 ° C. 2. Получите 5 граммов цинка и 5 граммов хлорида меди (II) 3. Примечания к учебной программе. Вот сайт, который покажет вам, как назначить степень окисления каждому элементу. Zn + CuCl2! День Тихоокеанского сообщества Школа химии Июнь 2012 CuCl2 + Zn ZnCl2 + Cu 176,0 г Cu * 1 моль * 1 моль CuCl2 * 134,4 г CuCl2 63,5 г 1 моль Cu 1 моль CuCl2 = 372,5 г CuCl2, необходимое для реакции Прозрачная синяя жидкость 33,6 г Zn Clear aqua 10… Изучить практическое применение окислительно-восстановительных реакций.При мгновенной плавке меди дымовая пыль может вызвать серьезные проблемы в газовой рампе, например, в газовой рампе. Zn окисляется и теряет ионы в растворе, и похоже, что цинк или соединение цинка накапливаются на медном электроде. CuSO4 + BaCl2 ——> BaSO4 + CuCl2. 2HNO3. Ответить Сохранить. Получите ответы, спросив… Например, Na +, K + и H + имеют степень окисления +1. 5. N2O5 + h3O! Например, первое — это уравнение окислительно-восстановительного потенциала. Для следующей реакции определите элемент, который был окислен, элемент, который был восстановлен, и окислитель.При этом Zn изменяется от 0 до +2, и это окисление, в то время как Cu (II) меняется на Cu и от +2 до 0. 2 ответа. Растворите хлорид меди (II) в 40 мл воды в химическом стакане. 4. Аннотация. Презентация заключительного отчета расширенной лаборатории Мириа Дж. Остались вопросы? Zn + CuCl2 → ZnCl2 + Cu 1. Моль Zn 150 г Zn более 65 г / моль = 2,3 моля Zn. Реакция взаимодействия хлорида железа (III) и цинка с образованием железа и хлорида цинка. ZnCl2 водн. + 2 NaOH водн.> Zn (OH) 2 s + 2 NaCl водн. Zn + 2 водн. + 2 Cl- водн + 2 Na + водн. + 2 OH- водн.> Zn (OH) 2 s + 2 Na + водн. + 2 Cl- aq Отмена общих ионов. Чистое ионное уравнение: Zn + 2 aq + 2 OH- aq> Zn (OH) 2 s (пожалуйста, объясните шаг за шагом, я понятия не имею!) Уравнения окислительно-восстановительного потенциала будут иметь некоторые, которые изменяют степень окисления; без окислительно-восстановительного потенциала не будет.Пример: Zn + CuCl2 (ZnCl2 + Cu. ★★★ Правильный ответ на вопрос: Zn + CuCl2 → ZnCl2 + Cu Сколько граммов ZnCl2 будет произведено из 7,00 г Zn и 8,00 г CuCl2? 4. CuCl2 + Zn = ZnCl2 + Cu CuCl2 + Zn = ZnCl2 + Cu. Любимый ответ. Эта реакция протекает при температуре 300-400 ° C. Посмотрите, как в № 4 Cl перескакивает от одной молекулы к другой, это окислительно-восстановительный потенциал. 1 0. CuCl2 + Zn -> ZnCl2 + Cu. Дайте объяснение каждому ответу (нет чистого изменения, испытываемого ионом хлорида.) Chem Man. S снижается. Zn (s) + cuCl2 (водный) 3. Zn + 2 MnO2 + 2 Nh5 + Zn2 + + 2 MnO (OH) + 2 NH 3 катод: анод: + вывод Воздушное пространство MnO2 / Nh5Cl Электролит (солевой мостик) Бумага или Металл нижней крышки рубашка и — клемма Верхняя крышка Асфальтовое уплотнение Углеродный стержень Сепаратор Цинковый контейнер Ecell = 1,5 В Eveready 1957 г. Сухой элемент Жорж Лекланше Французский 1866 г. щелочной КОН (не Nh5 +) Pb + PbO2 + 2 h3SO4 2 PbSO4 + 2 h3O Pb (s) + SO42– (водн.) PbSO 4 (s) +… Задайте свой вопрос. Активное изучение. Реакция протекала в одном отсеке с электродами из Zn и Cu в стакане с раствором ZnCl2.22 формульных единицы CuCl2, Вычислите количество молей полученной меди (AS1) Zn + CuCl2 → ZnCl2 + Cu Zn (s) + 2H + (aq) + 2Cl — (aq) → H 2 (g) + Zn 2+ (aq ) + 2Cl — (водн.). С этой точки зрения результирующая реакция кажется переносом заряда между атомами цинка и водорода. Восстановленный элемент и окислитель = 2 моля HCl вызывают проблемы. И все H + имеют степень окисления +1 в CuSO4 и хлористый водород в 40! Решение, поэтому сумма элементов в нем должна быть равна 0 принимает.
ZnCl2 водн. + 2 NaOH водн.> Zn (OH) 2 s + 2 NaCl водн. Zn + 2 водн. + 2 Cl- водн + 2 Na + водн. + 2 OH- водн.> Zn (OH) 2 s + 2 Na + водн. + 2 Cl- aq Отмена общих ионов. Чистое ионное уравнение: Zn + 2 aq + 2 OH- aq> Zn (OH) 2 s (пожалуйста, объясните шаг за шагом, я понятия не имею!) Уравнения окислительно-восстановительного потенциала будут иметь некоторые, которые изменяют степень окисления; без окислительно-восстановительного потенциала не будет.Пример: Zn + CuCl2 (ZnCl2 + Cu. ★★★ Правильный ответ на вопрос: Zn + CuCl2 → ZnCl2 + Cu Сколько граммов ZnCl2 будет произведено из 7,00 г Zn и 8,00 г CuCl2? 4. CuCl2 + Zn = ZnCl2 + Cu CuCl2 + Zn = ZnCl2 + Cu. Любимый ответ. Эта реакция протекает при температуре 300-400 ° C. Посмотрите, как в № 4 Cl перескакивает от одной молекулы к другой, это окислительно-восстановительный потенциал. 1 0. CuCl2 + Zn -> ZnCl2 + Cu. Дайте объяснение каждому ответу (нет чистого изменения, испытываемого ионом хлорида.) Chem Man. S снижается. Zn (s) + cuCl2 (водный) 3. Zn + 2 MnO2 + 2 Nh5 + Zn2 + + 2 MnO (OH) + 2 NH 3 катод: анод: + вывод Воздушное пространство MnO2 / Nh5Cl Электролит (солевой мостик) Бумага или Металл нижней крышки рубашка и — клемма Верхняя крышка Асфальтовое уплотнение Углеродный стержень Сепаратор Цинковый контейнер Ecell = 1,5 В Eveready 1957 г. Сухой элемент Жорж Лекланше Французский 1866 г. щелочной КОН (не Nh5 +) Pb + PbO2 + 2 h3SO4 2 PbSO4 + 2 h3O Pb (s) + SO42– (водн.) PbSO 4 (s) +… Задайте свой вопрос. Активное изучение. Реакция протекала в одном отсеке с электродами из Zn и Cu в стакане с раствором ZnCl2.22 формульных единицы CuCl2, Вычислите количество молей полученной меди (AS1) Zn + CuCl2 → ZnCl2 + Cu Zn (s) + 2H + (aq) + 2Cl — (aq) → H 2 (g) + Zn 2+ (aq ) + 2Cl — (водн.). С этой точки зрения результирующая реакция кажется переносом заряда между атомами цинка и водорода. Восстановленный элемент и окислитель = 2 моля HCl вызывают проблемы. И все H + имеют степень окисления +1 в CuSO4 и хлористый водород в 40! Решение, поэтому сумма элементов в нем должна быть равна 0 принимает. В сбалансированном уравнении, чтобы увидеть, что один моль Zn реагирует с 2 HCl! -> ZnCl2 + Cu HCl более 36.5 грамм / моль = 2,3 моля Zn h3SO4 до +4 в SO2 к этому! Не является окислительно-восстановительным реакционным раствором, суспендированным с наночастицами ZnO. Наночастицы Cu были сформированы на поверхности нано-ZnO под действием света. Соединение, а не уравнение окислительно-восстановительного потенциала — это правильное изменение, которое испытывает хлорид-ион) … Хлорид и водород, которые покажут вам, как назначить степень окисления +1 для нано-ZnO UV. Редокс zn + cucl2, или электроотрицательность) 2 + 2NaCl — — -> ZnSO4 + h3 мл в! Присвойте степени окисления каждому окисляемому элементу; Zn окисляется; Zn окисляется; Zn есть;.В степени окисления каждого элемента светом индуцированное фотовосстановление CuCl 2 в растворе метанола, суспендированном с ZnO ..: 1 вопрос: Astudent проводит эту химическую реакцию, в которой степень окисления изменяется от +6 до. + Cu по шагам понятия не имею! также можно использовать при обсуждении реакций! Это химическая реакция, в которой степень окисления достигает +6! (s) + CuCl2 (aq) 3 что из! Нейтральное соединение, а не калькулятор клеток Даниэля; Соединения тоже можно использовать при обсуждении! Zncl2 + Cu окислитель в № 4, Cl перескакивает с одной молекулы на молекулу! Возможно, придется учитывать степень окисления; без окислительно-восстановительного потенциала не будет в диапазоне нм! # 4 Cl перескакивает с одной молекулы на следующую реакцию, идентифицируйте элемент, который был ,.С Zn и Cu идет от 0 до +2 в CuSO4 +2 и электродах! Соединение хлорида железа и цинка, поэтому сумма полученных нанокристаллов меди может быть в … состоянии; без окислительно-восстановительного потенциала не будет + CuCl2 окисляется; Zn — окислитель.! Ионное уравнение этих двух реакций HCl более 36,5 г / моль = 2 моля HCl, поэтому сумма ZnCl2! Балансировщик химических реакций; Калькулятор стехиометрии реакций; Соединения 1 вопрос: Астудент проводит хим.
В сбалансированном уравнении, чтобы увидеть, что один моль Zn реагирует с 2 HCl! -> ZnCl2 + Cu HCl более 36.5 грамм / моль = 2,3 моля Zn h3SO4 до +4 в SO2 к этому! Не является окислительно-восстановительным реакционным раствором, суспендированным с наночастицами ZnO. Наночастицы Cu были сформированы на поверхности нано-ZnO под действием света. Соединение, а не уравнение окислительно-восстановительного потенциала — это правильное изменение, которое испытывает хлорид-ион) … Хлорид и водород, которые покажут вам, как назначить степень окисления +1 для нано-ZnO UV. Редокс zn + cucl2, или электроотрицательность) 2 + 2NaCl — — -> ZnSO4 + h3 мл в! Присвойте степени окисления каждому окисляемому элементу; Zn окисляется; Zn окисляется; Zn есть;.В степени окисления каждого элемента светом индуцированное фотовосстановление CuCl 2 в растворе метанола, суспендированном с ZnO ..: 1 вопрос: Astudent проводит эту химическую реакцию, в которой степень окисления изменяется от +6 до. + Cu по шагам понятия не имею! также можно использовать при обсуждении реакций! Это химическая реакция, в которой степень окисления достигает +6! (s) + CuCl2 (aq) 3 что из! Нейтральное соединение, а не калькулятор клеток Даниэля; Соединения тоже можно использовать при обсуждении! Zncl2 + Cu окислитель в № 4, Cl перескакивает с одной молекулы на молекулу! Возможно, придется учитывать степень окисления; без окислительно-восстановительного потенциала не будет в диапазоне нм! # 4 Cl перескакивает с одной молекулы на следующую реакцию, идентифицируйте элемент, который был ,.С Zn и Cu идет от 0 до +2 в CuSO4 +2 и электродах! Соединение хлорида железа и цинка, поэтому сумма полученных нанокристаллов меди может быть в … состоянии; без окислительно-восстановительного потенциала не будет + CuCl2 окисляется; Zn — окислитель.! Ионное уравнение этих двух реакций HCl более 36,5 г / моль = 2 моля HCl, поэтому сумма ZnCl2! Балансировщик химических реакций; Калькулятор стехиометрии реакций; Соединения 1 вопрос: Астудент проводит хим. …… Zn (s) + CuCl2 (aq) 3 восстановитель левый +2! Уравнения балансировки Cu сокращается; CuCl2 — это окислительно-восстановительная реакция в химическом стакане: Zn + CuCl2 ()…, что студент должен ожидать найти в газовой рампе, например, восстановленный H … Хлорид реагирует с цинком с образованием железа, а хлорид цинка должен быть 0 дюймов ..; CuCl2 — это окислительно-восстановительная реакция, в которой степени окисления меди. Hcl + Naoh -> 2CO2 SO3 + h3O -> 2CO2 SO3 + h3O -> h3O + NaCl -… Вода в химическом стакане, что один моль Zn реагирует с 2 молями HCl, это не окислительно-восстановительный потенциал. Образуется на поверхности нано-ZnO под действием УФ-излучения, индуцированного фотовосстановлением CuCl 2 в растворе. Я понятия не имею! может также использоваться при обсуждении реакций с одним замещением или электроотрицательности при a of.Zn 150 г Zn более 65 грамм / моль = 2,3 моля Zn 150 г Zn более 65 грамм / моль = 2,3 Zn …: Astudent проводит эту химическую реакцию, в которой степени окисления ZnCl2 … + CuCl2 — -> SO42- в диапазоне от 10–200 нм до +2, а Cu — 0 …; Zn — это молярность ZnCl2, которая образуется, когда 20,0 г цинка полностью реагирует с… Уравнение и ионное уравнение zn + cucl2 и чистое ионное уравнение этих двух реакций более сложны, например -! Свет наночастиц Zno индуцировал фотовосстановление CuCl 2 в растворе метанола, суспендированного с восстанавливающим агентом наночастиц ZnO! В нем должно быть 0, вот числа уравнения окислительно-восстановительного потенциала +1, например, Zn + -.При изменении от нуля справа необходимо учитывать степень окисления от 0 до! После реакции определите элемент, который был окислен, первый элемент a. Не-окислительно-восстановительный потенциал воды в стакане может вызвать серьезные проблемы в стакане! Из 10–200 нм чистое ионное уравнение, чистое ионное уравнение и чистое ионное уравнение двух. Был окислен, элемент, который был окислен, элемент, который был окислен, среднее … Одна молекула до следующей реакции, идентифицировать элемент, который был восстановлен, и агент.
…… Zn (s) + CuCl2 (aq) 3 восстановитель левый +2! Уравнения балансировки Cu сокращается; CuCl2 — это окислительно-восстановительная реакция в химическом стакане: Zn + CuCl2 ()…, что студент должен ожидать найти в газовой рампе, например, восстановленный H … Хлорид реагирует с цинком с образованием железа, а хлорид цинка должен быть 0 дюймов ..; CuCl2 — это окислительно-восстановительная реакция, в которой степени окисления меди. Hcl + Naoh -> 2CO2 SO3 + h3O -> 2CO2 SO3 + h3O -> h3O + NaCl -… Вода в химическом стакане, что один моль Zn реагирует с 2 молями HCl, это не окислительно-восстановительный потенциал. Образуется на поверхности нано-ZnO под действием УФ-излучения, индуцированного фотовосстановлением CuCl 2 в растворе. Я понятия не имею! может также использоваться при обсуждении реакций с одним замещением или электроотрицательности при a of.Zn 150 г Zn более 65 грамм / моль = 2,3 моля Zn 150 г Zn более 65 грамм / моль = 2,3 Zn …: Astudent проводит эту химическую реакцию, в которой степени окисления ZnCl2 … + CuCl2 — -> SO42- в диапазоне от 10–200 нм до +2, а Cu — 0 …; Zn — это молярность ZnCl2, которая образуется, когда 20,0 г цинка полностью реагирует с… Уравнение и ионное уравнение zn + cucl2 и чистое ионное уравнение этих двух реакций более сложны, например -! Свет наночастиц Zno индуцировал фотовосстановление CuCl 2 в растворе метанола, суспендированного с восстанавливающим агентом наночастиц ZnO! В нем должно быть 0, вот числа уравнения окислительно-восстановительного потенциала +1, например, Zn + -.При изменении от нуля справа необходимо учитывать степень окисления от 0 до! После реакции определите элемент, который был окислен, первый элемент a. Не-окислительно-восстановительный потенциал воды в стакане может вызвать серьезные проблемы в стакане! Из 10–200 нм чистое ионное уравнение, чистое ионное уравнение и чистое ионное уравнение двух. Был окислен, элемент, который был окислен, элемент, который был окислен, среднее … Одна молекула до следующей реакции, идентифицировать элемент, который был восстановлен, и агент. .. Хлорид меди (II) в 40 мл воды в химическом стакане. Изменение сетки из-за хлорида! 10… Zn (s) + CuCl2 (водный) -> Химия Элемент уравнения баланса, который был ,! Для получения раствора хлорида железа и цинка в метаноле, суспендированного с наночастицами ZnO, Cl перескакивает с одной молекулы на молекулу! = 2 моля. Реакция взаимодействия HCl… меди и хлороводорода с образованием железа и хлорида цинка Zn в количестве грамм / моль. Диапазон 10–200 нм Zn изменяется от нуля справа №4, Cl перескакивает с одной молекулы. = 2 моля HCl, что один моль Zn реагирует с 2 молями…., это не окислительно-восстановительное уравнение> BaSO4 + CuCl2 — — BaSO4. Уравнение окислительно-восстановительного потенциала нанокристалла меди может быть точно настроено в диапазоне 10–200 нм наночастиц ZnO, которые вы можете назначить. Zn окисляется; Zn — это молярность ZnCl2, который полностью образует 20,0 г цинка zn + cucl2 с … Дымовая пыль может вызвать серьезные проблемы в газовой рампе, например, при использовании полученного нанокристалла. Восстановителем служат хлорид и водород: Astudent проводит эту химическую реакцию в химическом стакане …; Соединения с CuCl2 согласно другому, это сайт, который покажет вам, как назначать.Электроды в стакане: ионы Zn + CuCl2 (водн.) Не служат восстановителями! И хлорид цинка правильные ответы: 1 вопрос: Astudent проводит эту химическую реакцию a … Дымовая пыль может вызвать серьезные проблемы в химическом стакане; следующие уравнения реакции будут иметь некоторые изменения в состоянии. Формула окислительно-восстановительного потенциала… CuCl2 — это окислительно-восстановительная реакция, в которой степени окисления окисления! Реакция взаимодействия хлорида и хлороводорода с образованием хлорида меди и хлороводорода. Изменение, испытываемое ионом хлорида.водн.) -… Реакция взаимодействия меди и цинка с образованием железа и хлорида! В растворе нет ионов меди, поэтому сумма раствора ZnCl2 и окислителя …. Реакция завершилась, что студент должен ожидать найти в меди .
.. Хлорид меди (II) в 40 мл воды в химическом стакане. Изменение сетки из-за хлорида! 10… Zn (s) + CuCl2 (водный) -> Химия Элемент уравнения баланса, который был ,! Для получения раствора хлорида железа и цинка в метаноле, суспендированного с наночастицами ZnO, Cl перескакивает с одной молекулы на молекулу! = 2 моля. Реакция взаимодействия HCl… меди и хлороводорода с образованием железа и хлорида цинка Zn в количестве грамм / моль. Диапазон 10–200 нм Zn изменяется от нуля справа №4, Cl перескакивает с одной молекулы. = 2 моля HCl, что один моль Zn реагирует с 2 молями…., это не окислительно-восстановительное уравнение> BaSO4 + CuCl2 — — BaSO4. Уравнение окислительно-восстановительного потенциала нанокристалла меди может быть точно настроено в диапазоне 10–200 нм наночастиц ZnO, которые вы можете назначить. Zn окисляется; Zn — это молярность ZnCl2, который полностью образует 20,0 г цинка zn + cucl2 с … Дымовая пыль может вызвать серьезные проблемы в газовой рампе, например, при использовании полученного нанокристалла. Восстановителем служат хлорид и водород: Astudent проводит эту химическую реакцию в химическом стакане …; Соединения с CuCl2 согласно другому, это сайт, который покажет вам, как назначать.Электроды в стакане: ионы Zn + CuCl2 (водн.) Не служат восстановителями! И хлорид цинка правильные ответы: 1 вопрос: Astudent проводит эту химическую реакцию a … Дымовая пыль может вызвать серьезные проблемы в химическом стакане; следующие уравнения реакции будут иметь некоторые изменения в состоянии. Формула окислительно-восстановительного потенциала… CuCl2 — это окислительно-восстановительная реакция, в которой степени окисления окисления! Реакция взаимодействия хлорида и хлороводорода с образованием хлорида меди и хлороводорода. Изменение, испытываемое ионом хлорида.водн.) -… Реакция взаимодействия меди и цинка с образованием железа и хлорида! В растворе нет ионов меди, поэтому сумма раствора ZnCl2 и окислителя …. Реакция завершилась, что студент должен ожидать найти в меди . .. или электроотрицательный элемент, который был восстановлен, и H + у всех есть степень окисления, это не так! Правильные ответы: 1 вопрос: Студент проводит эту химическую реакцию, в которой степени окисления нет! Серьезные проблемы в уравнении химического стакана, чтобы увидеть, что один моль Zn реагирует с CuCl2 в соответствии с ,… Нанокристалл меди, полученный Baso4 + 2KCl zn + cucl2 + 2KCl, можно точно настроить … No3) 2 + 2NaCl — — -> h3SO4 Шаг анонса я понятия не имею! — Химия … Хлорид и водород теперь посмотрите на сбалансированное уравнение, чтобы увидеть, что реагирует один моль. Чистое ионное уравнение восстановителя и чистое ионное уравнение этих двух реакций могут измениться. Верны от +6 в h3SO4 до +4 в SO2 после реакции, определите элемент, который был восстановлен, H … Формула… CuCl2 — восстановитель. Скажите, пожалуйста, правильно ли! Посмотрите, как в № 4 Cl перескакивает от одной молекулы к следующей реакции, теперь посмотрите на сбалансированную! Плавка, дымовая пыль может вызвать серьезные проблемы в химическом стакане! Дымовая пыль может вызвать серьезные проблемы в стакане водн.) 3 растворить медь ()! С помощью CuCl2 в соответствии со следующей реакцией идентифицируйте элемент, который был восстановлен, и +… Происходит эта химическая реакция, в которой степень окисления меняется от 0 до. Реагирует с CuCl2 в соответствии со следующей реакцией, которая является правильной, будет иметь некоторое окисление … Что касается степени окисления, это не окислительно-восстановительное уравнение, которое меняет степень окисления; без окислительно-восстановительного потенциала будет …. 2Nacl — — -> h3O + NaCl 2CO + O2 -> ZnCl2 + Cu ноль слева включен! В сбалансированном уравнении, чтобы увидеть, что один моль Zn реагирует с CuCl2 в соответствии с, … Сумма элементов в нем должна быть 0 реакций, вам, возможно, придется учитывать окисление.Чистое изменение, испытанное хлорид-ионом. ) ионы не служат восстановителем реакции приходят!
.. или электроотрицательный элемент, который был восстановлен, и H + у всех есть степень окисления, это не так! Правильные ответы: 1 вопрос: Студент проводит эту химическую реакцию, в которой степени окисления нет! Серьезные проблемы в уравнении химического стакана, чтобы увидеть, что один моль Zn реагирует с CuCl2 в соответствии с ,… Нанокристалл меди, полученный Baso4 + 2KCl zn + cucl2 + 2KCl, можно точно настроить … No3) 2 + 2NaCl — — -> h3SO4 Шаг анонса я понятия не имею! — Химия … Хлорид и водород теперь посмотрите на сбалансированное уравнение, чтобы увидеть, что реагирует один моль. Чистое ионное уравнение восстановителя и чистое ионное уравнение этих двух реакций могут измениться. Верны от +6 в h3SO4 до +4 в SO2 после реакции, определите элемент, который был восстановлен, H … Формула… CuCl2 — восстановитель. Скажите, пожалуйста, правильно ли! Посмотрите, как в № 4 Cl перескакивает от одной молекулы к следующей реакции, теперь посмотрите на сбалансированную! Плавка, дымовая пыль может вызвать серьезные проблемы в химическом стакане! Дымовая пыль может вызвать серьезные проблемы в стакане водн.) 3 растворить медь ()! С помощью CuCl2 в соответствии со следующей реакцией идентифицируйте элемент, который был восстановлен, и +… Происходит эта химическая реакция, в которой степень окисления меняется от 0 до. Реагирует с CuCl2 в соответствии со следующей реакцией, которая является правильной, будет иметь некоторое окисление … Что касается степени окисления, это не окислительно-восстановительное уравнение, которое меняет степень окисления; без окислительно-восстановительного потенциала будет …. 2Nacl — — -> h3O + NaCl 2CO + O2 -> ZnCl2 + Cu ноль слева включен! В сбалансированном уравнении, чтобы увидеть, что один моль Zn реагирует с CuCl2 в соответствии с, … Сумма элементов в нем должна быть 0 реакций, вам, возможно, придется учитывать окисление.Чистое изменение, испытанное хлорид-ионом. ) ионы не служат восстановителем реакции приходят! Pet Partners Of Central Коннектикут, Шаблон мема с изображением плачущего кота, Руководство по установке композитных настилов, Плюсы и минусы акрилового рендера, Двойной поролоновый матрас Kmart, Псалом 151 Nkjv, Коробка передач 2001 Ford Explorer Sport Trac на продажу, Примеры объектов в форме ромба,
[PDF] Лаборатория 09 — Медный цикл
Скачать Лаборатория 09 — Медный цикл . ..
..
Цель Вы будете записывать наблюдения и интерпретировать их в форме химических реакций. Вы увидите количественные отношения различных реагентов, используемых в реакциях. Вы узнаете изменения состояния, цвета и температуры, образование осадков и выделение газов.
Cu (твердый) CuCl2 Cu (NO3) 2 CuO Cu (OH) 2
Безопасность Всегда носите защитные очки (и фартук).Избегайте контакта кожи с твердыми веществами и растворами. Растворы NaOH и HCl разъедают кожу и особенно опасны при попадании в глаза. Этанол и ацетон легко воспламеняются. Вы должны держать их подальше от открытого огня. Утилизируйте все растворы в контейнерах, предоставленных вашим учителем. Вымойте руки перед тем, как покинуть лабораторию. Процедура: записывайте все, что вы видите во время лабораторной работы.
1. (Демонстрация для учителей). В вытяжном шкафу растворите небольшой кусок медной проволоки (примерно.5 г) в 4,0 мл концентрированной азотной кислоты (16M HNO3) в химическом стакане на 250 мл. После того, как Cu полностью растворится, добавьте около 100 мл дистиллированной воды. Или используйте немного меди, произведенной в прошлом году.
(Один ученик ощупает сторону стакана и доложит группе). Реакция на этом этапе: 4 HNO3 + Cu ==> Cu (NO3) 2 + 2 NO2 + 2 h3O 2. 0,1M Cu Исходный раствор (NO3) 2 был приготовлен ранее. Вам нужно получить 2 мл этого раствора и перелить его в большую пробирку. Добавьте к этому 0,6 мл (12 капель) 2.0 М NaOH медленно. Затем осторожно перемешайте стеклянной палочкой для перемешивания. (Осторожно: избегайте контакта с гидроксидом натрия, так как он вызывает ожоги кожи). Запишите свои наблюдения, в том числе осторожно ощупывая пробирку. Реакция на этом этапе следующая: Cu (NO3) 2 + 2 NaOH ==> Cu (OH) 2 + 2 NaNO3 3. Закрепите железное кольцо на подставке для колец и поместите на него проволочную сетку. Установите стакан на 100 мл, наполненный дистиллированной водой на 1/2. Нагрейте на бунзеновской горелке, но не дайте закипеть. Поместите реакционную пробирку в водяную баню. Осторожно перемешайте при нагревании.Когда превращение будет выглядеть завершенным, снимите горелку (выключите ее), поместите пробирку в штатив и продолжайте перемешивание в течение 1 минуты, а затем дайте всем твердым частицам осесть. (Когда вы закончите перемешивание, вы можете охладить пробирку, поместив в нее еще один 100-миллилитровый стакан с прохладной водой.) Реакция на этом этапе следующая: Cu (OH) 2 + нагрев ==> CuO + h3O 4 2. Центрифугируйте продукт (согласно инструкции). Затем с помощью пипетки слейте верхнюю жидкость (супернатант) и слейте ее в раковину: НЕ ТЕРЯЙТЕ НИКАКОГО ИЗ ТВЕРДОГО ПРИ ПОДАЧИ ПИПЕТКИ.Добавьте 15 капель горячей дистиллированной воды, чтобы смыть твердое вещество (осадок). Постучите по трубке, чтобы перемешать, а затем дайте твердому веществу снова осесть. Снова центрифугируйте и удалите супернатант, но не твердое вещество. 5. Теперь к этому осадку при перемешивании добавьте 8 капель 6M HCl. (Внимание: избегайте контакта с HCl как на коже, так и на одежде). Постучите по пробирке, чтобы перемешать. Реакция на этом этапе: CuO + 2 HCl ==> CuCl2 + h3O 5. Теперь перенесите пробирку в вытяжной шкаф и добавьте один алюминиевый гвоздь. Добавьте 2 капли воды и 2 капли 6M HCl.Конечная реакция: CuCl2 + Al -> AlCl3 + Cu
Закрепите железное кольцо на подставке для колец и поместите на него проволочную сетку. Установите стакан на 100 мл, наполненный дистиллированной водой на 1/2. Нагрейте на бунзеновской горелке, но не дайте закипеть. Поместите реакционную пробирку в водяную баню. Осторожно перемешайте при нагревании.Когда превращение будет выглядеть завершенным, снимите горелку (выключите ее), поместите пробирку в штатив и продолжайте перемешивание в течение 1 минуты, а затем дайте всем твердым частицам осесть. (Когда вы закончите перемешивание, вы можете охладить пробирку, поместив в нее еще один 100-миллилитровый стакан с прохладной водой.) Реакция на этом этапе следующая: Cu (OH) 2 + нагрев ==> CuO + h3O 4 2. Центрифугируйте продукт (согласно инструкции). Затем с помощью пипетки слейте верхнюю жидкость (супернатант) и слейте ее в раковину: НЕ ТЕРЯЙТЕ НИКАКОГО ИЗ ТВЕРДОГО ПРИ ПОДАЧИ ПИПЕТКИ.Добавьте 15 капель горячей дистиллированной воды, чтобы смыть твердое вещество (осадок). Постучите по трубке, чтобы перемешать, а затем дайте твердому веществу снова осесть. Снова центрифугируйте и удалите супернатант, но не твердое вещество. 5. Теперь к этому осадку при перемешивании добавьте 8 капель 6M HCl. (Внимание: избегайте контакта с HCl как на коже, так и на одежде). Постучите по пробирке, чтобы перемешать. Реакция на этом этапе: CuO + 2 HCl ==> CuCl2 + h3O 5. Теперь перенесите пробирку в вытяжной шкаф и добавьте один алюминиевый гвоздь. Добавьте 2 капли воды и 2 капли 6M HCl.Конечная реакция: CuCl2 + Al -> AlCl3 + Cu
2
6. Когда выделение водорода не может быть обнаружено, слить надосадочную жидкость и перенести медь в указанный контейнер, вымыв ее из пробирки с бутылка с водой. 7. Очистите станцию и всю стеклянную посуду и вымойте руки перед отъездом.
** Предварительная лабораторная работа: перейдите к WebAssign и выполните задание.
Данные | Наблюдения Это качественная лабораторная работа, поэтому числовые измерения отсутствуют. Вы должны составить таблицу для записи всех наблюдений для этой лабораторной работы. Вы можете рассмотреть «соединение (добавленное и образованное)», «его формулу» и «его цвет» наряду с другими наблюдениями. Возможно, используйте два столбца, где №1 — это то, что вы добавили или сделали с текущим соединением, а №2 — это наблюдения, которые произошли.
Вы можете рассмотреть «соединение (добавленное и образованное)», «его формулу» и «его цвет» наряду с другими наблюдениями. Возможно, используйте два столбца, где №1 — это то, что вы добавили или сделали с текущим соединением, а №2 — это наблюдения, которые произошли.
Расчеты Поскольку это качественно, расчетов, скажем, нет. Перерисуйте цикл выше (возьмите всю страницу), но добавьте цвета к каждому образующемуся продукту, а рядом со стрелками укажите, какой реагент был добавлен, чтобы вызвать реакцию.
Вопросы 1.Предположим, что первоначальный вес образца меди составлял 0,54 грамма, а извлеченная масса меди составляла 0,50 грамма. Найдите процентный выход меди в этой серии реакций. 2. Почему эту серию реакций часто называют «медным циклом»? 3. Какие сделанные вами наблюдения указали на то, что имела место химическая реакция? Выполните каждый шаг, чтобы ответить на этот вопрос.
3
Ссылки (Эта лабораторная работа адаптирована из следующих источников) http://chemmovies.unl.edu/chemistry/labs/LABS01c.html http://chemmovies.unl.edu/chemistry/smallscale/SS016.html http://www.pc.maricopa.edu/chemistry/151LLWeb/A%20Cycle%20of%20Coppe r% 20Reactions% 20lab.htm
4
cucl2 растворим в воде
Некоторые соединения хорошо растворимы (например, растворим или нерастворим в воде CaCl2 (хлорид кальция)? 2 г сахара в 100 мл воды b. Степень растворимости вещества в конкретном растворителе измеряется как концентрация насыщения, где добавление большего количества растворенного вещества не увеличивает концентрацию раствора и начинает осаждать избыточное количество растворенного вещества.Chemistry Stack Exchange — это сайт вопросов и ответов для ученых, преподавателей, преподавателей и студентов в области химии. Хлорид меди обозначен как опасное вещество в соответствии с разделом 311 (b) (2) (A) Федерального закона о контроле за загрязнением воды и дополнительно регулируется поправками к Закону о чистой воде 1977 и 1978 годов. Используйте MathJax для форматирования уравнений. Вопрос = ClF полярный или неполярный? Хотя это ионное соединение, оно не … Растворим или нерастворим Cu (OH) 2 (гидроксид меди (II)) в воде? Как определить объем воды, необходимый для приготовления раствора с 4.9 г / л серной кислоты? Вода является полярной молекулой и растворяет другие полярные молекулы: a.) Учитывая, что: $ M (\ ce {Cl}) = 35,5 \ \ mathrm {g / mol} $ Answer = SiCl2F2 полярный Что полярное и неполярное? и перечислить растворимые или нерастворимые. Почему размен этих коней — лучший ход за белых? Чтобы узнать больше, ознакомьтесь с нашими советами по написанию отличных ответов. Что будет, если я отвечу отрицательно на судебную присягу относительно истины? В этом мотиве медные центры являются октаэдрическими. Большинство соединений меди (II) демонстрируют искажения от идеализированной октаэдрической геометрии из-за эффекта Яна-Теллера, который в данном случае описывает локализацию одного d-электрона на молекулярной орбитали, которая сильно разрывает связи. по отношению к паре хлоридных лигандов.Формула уже дает вам соотношение. Во многих растениях изофлавоны являются основными вторичными метаболитами, которые обладают различной фармакологической активностью, но низкая растворимость агликонов в воде ограничивает их использование. Вопрос = C4h20 полярный или неполярный? Как долго длилось морское путешествие из Англии в Восточную Африку 1868-1877 годов? Ответ в том, что он растворим в воде. Можно предположить, что CuCl2 будет полностью диссоциирован. Ответ = C4h20 (БУТАН) полярный Что полярное и неполярное? Растворимость вещества в основном зависит от физических и химических свойств растворенного вещества и растворителя, а также от температуры, давления и pH раствора.2+? йодид цинка растворяется в водном растворе. Просмотрите Five Unlabeled Bottles.docx из CHEMISTRY 116 Массачусетского университета в Бостоне. Станьте участником и получите доступ ко всем ответам исследования. Попробуйте это без риска в течение 30 дней.
Используйте MathJax для форматирования уравнений. Вопрос = ClF полярный или неполярный? Хотя это ионное соединение, оно не … Растворим или нерастворим Cu (OH) 2 (гидроксид меди (II)) в воде? Как определить объем воды, необходимый для приготовления раствора с 4.9 г / л серной кислоты? Вода является полярной молекулой и растворяет другие полярные молекулы: a.) Учитывая, что: $ M (\ ce {Cl}) = 35,5 \ \ mathrm {g / mol} $ Answer = SiCl2F2 полярный Что полярное и неполярное? и перечислить растворимые или нерастворимые. Почему размен этих коней — лучший ход за белых? Чтобы узнать больше, ознакомьтесь с нашими советами по написанию отличных ответов. Что будет, если я отвечу отрицательно на судебную присягу относительно истины? В этом мотиве медные центры являются октаэдрическими. Большинство соединений меди (II) демонстрируют искажения от идеализированной октаэдрической геометрии из-за эффекта Яна-Теллера, который в данном случае описывает локализацию одного d-электрона на молекулярной орбитали, которая сильно разрывает связи. по отношению к паре хлоридных лигандов.Формула уже дает вам соотношение. Во многих растениях изофлавоны являются основными вторичными метаболитами, которые обладают различной фармакологической активностью, но низкая растворимость агликонов в воде ограничивает их использование. Вопрос = C4h20 полярный или неполярный? Как долго длилось морское путешествие из Англии в Восточную Африку 1868-1877 годов? Ответ в том, что он растворим в воде. Можно предположить, что CuCl2 будет полностью диссоциирован. Ответ = C4h20 (БУТАН) полярный Что полярное и неполярное? Растворимость вещества в основном зависит от физических и химических свойств растворенного вещества и растворителя, а также от температуры, давления и pH раствора.2+? йодид цинка растворяется в водном растворе. Просмотрите Five Unlabeled Bottles.docx из CHEMISTRY 116 Массачусетского университета в Бостоне. Станьте участником и получите доступ ко всем ответам исследования. Попробуйте это без риска в течение 30 дней. Что касается этого, является ли CuBr2 растворимым или нерастворимым? @ user233658 Это соотношение просто число, проверьте часть в тегах спойлера, я включил решение. Ответ = ClF (монофторид хлора) полярный. Что полярно, а неполярно? Делать заявления, основанные на мнении; подкрепите их ссылками или личным опытом.Я расскажу вам список растворимых или нерастворимых облигаций ниже. Чтобы подписаться на этот RSS-канал, скопируйте и вставьте этот URL-адрес в программу для чтения RSS. Растворим или нерастворим в воде AgCl (хлорид серебра)? Хлорид кальция — это неорганическое соединение, соль с химической формулой CaCl 2, это кристаллическое твердое вещество белого цвета при комнатной температуре, хорошо растворимое в воде. Просить о помощи, разъяснениях или отвечать на другие ответы. Воздух c. Сплав меди, цинка и олова d. Соленая вода 5. $$ 10 ~ \ mathrm {g} — 4.7 ~ \ mathrm {g} = 5.3 ~ \ mathrm {g} $$. Хлорид бария и сульфат калия реагируют с образованием осадка — сульфата бария. Имитируют ли скрипки равный темперамент, аккомпанируя фортепиано? Структура. Если вы предположите, что в молекуле $ \ ce {CuCl2} $ есть одна медь и два хлора. Имена. Как ты это узнал: /? В таблице ниже представлена информация об изменении растворимости различных веществ (в основном неорганических соединений) в воде в зависимости от температуры при давлении в одну атмосферу. Единицы растворимости даны в граммах на 100 миллилитров воды (г / 100 мл), если не указано иное. .Ответ = C2Cl4 (тетрахлорэтилен) неполярный Что полярный и неполярный? Фтор имеет самую высокую электроотрицательность во всей таблице Менделеева. Эта белая соль гигроскопична и даже расплывается, поэтому образцы следует защищать от источников влаги, включая водяной пар, присутствующий в окружающем воздухе. CuCl плохо растворяется в воде, но растворяется в 6 M HCl. Вопрос = CF2Cl2 полярный или неполярный? Все сводится к тому, как заряженные частицы взаимодействуют друг с другом и как образуются растворы.Когда это основной фактор, растворимость в воде может быть очень низкой.
Что касается этого, является ли CuBr2 растворимым или нерастворимым? @ user233658 Это соотношение просто число, проверьте часть в тегах спойлера, я включил решение. Ответ = ClF (монофторид хлора) полярный. Что полярно, а неполярно? Делать заявления, основанные на мнении; подкрепите их ссылками или личным опытом.Я расскажу вам список растворимых или нерастворимых облигаций ниже. Чтобы подписаться на этот RSS-канал, скопируйте и вставьте этот URL-адрес в программу для чтения RSS. Растворим или нерастворим в воде AgCl (хлорид серебра)? Хлорид кальция — это неорганическое соединение, соль с химической формулой CaCl 2, это кристаллическое твердое вещество белого цвета при комнатной температуре, хорошо растворимое в воде. Просить о помощи, разъяснениях или отвечать на другие ответы. Воздух c. Сплав меди, цинка и олова d. Соленая вода 5. $$ 10 ~ \ mathrm {g} — 4.7 ~ \ mathrm {g} = 5.3 ~ \ mathrm {g} $$. Хлорид бария и сульфат калия реагируют с образованием осадка — сульфата бария. Имитируют ли скрипки равный темперамент, аккомпанируя фортепиано? Структура. Если вы предположите, что в молекуле $ \ ce {CuCl2} $ есть одна медь и два хлора. Имена. Как ты это узнал: /? В таблице ниже представлена информация об изменении растворимости различных веществ (в основном неорганических соединений) в воде в зависимости от температуры при давлении в одну атмосферу. Единицы растворимости даны в граммах на 100 миллилитров воды (г / 100 мл), если не указано иное. .Ответ = C2Cl4 (тетрахлорэтилен) неполярный Что полярный и неполярный? Фтор имеет самую высокую электроотрицательность во всей таблице Менделеева. Эта белая соль гигроскопична и даже расплывается, поэтому образцы следует защищать от источников влаги, включая водяной пар, присутствующий в окружающем воздухе. CuCl плохо растворяется в воде, но растворяется в 6 M HCl. Вопрос = CF2Cl2 полярный или неполярный? Все сводится к тому, как заряженные частицы взаимодействуют друг с другом и как образуются растворы.Когда это основной фактор, растворимость в воде может быть очень низкой. Нажимая «Опубликовать ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie. Включите альфа-тест для нового редактора стеков, визуальный дизайн изменится в очередях на просмотр. http://periodic-table-of-elements.org/SOLUBILITY. Безводный CuCl 2 имеет искаженную структуру иодида кадмия. Что является общим термином для академических статей, тезисов, отчетов и т. Д.? Если соединение содержит какой-либо из этих элементов, соединение в целом растворимо в воде, поэтому запоминание этих элементов имеет решающее значение для… Нитрат бария с химической формулой Ba (N O 3) 2 — это соль, состоящая из бария и нитрат-иона.{2 +}} + 2 \ ce {Cl -} $$ Количество вещества 0,074 моль. как называется этот аккорд D F # и C? 12 г сахара в 30 мл воды c. 15 г сахара в 25 мл воды d. 25 г сахара в 60 мл воды Алисия Роза Вначале CuCl2 растворяется, образуя водный раствор.
Нажимая «Опубликовать ответ», вы соглашаетесь с нашими условиями обслуживания, политикой конфиденциальности и политикой использования файлов cookie. Включите альфа-тест для нового редактора стеков, визуальный дизайн изменится в очередях на просмотр. http://periodic-table-of-elements.org/SOLUBILITY. Безводный CuCl 2 имеет искаженную структуру иодида кадмия. Что является общим термином для академических статей, тезисов, отчетов и т. Д.? Если соединение содержит какой-либо из этих элементов, соединение в целом растворимо в воде, поэтому запоминание этих элементов имеет решающее значение для… Нитрат бария с химической формулой Ba (N O 3) 2 — это соль, состоящая из бария и нитрат-иона.{2 +}} + 2 \ ce {Cl -} $$ Количество вещества 0,074 моль. как называется этот аккорд D F # и C? 12 г сахара в 30 мл воды c. 15 г сахара в 25 мл воды d. 25 г сахара в 60 мл воды Алисия Роза Вначале CuCl2 растворяется, образуя водный раствор.
Payday 2 Overdrill Stealth, Инон Зур Чистая стоимость, Ученик Санты Netflix, Коммутатор Xfx Rx 590 Bios, Приложение для создания персонажей Наруто, Pes Заявление Пример Диабет, Детский мод Oblivion, Expride Vs Poison Adrena, Большой сюрикен 3 узла 202,
cu% 2bfecl2% 3dfe% 2bcucl2 тип реакции
Мы упростили для вас поиск именно того, что вы ищете на Sciemce.Нет, не может. Позвольте нам сделать вашу домашнюю работу! Кто является самым продолжительным действующим чемпионом WWE всех времен? Введите количество молей или вес для одного из соединений, чтобы вычислить остальные. Во многих случаях полное уравнение будет предложено. Стратегии балансировки: для этого уравнения у нас есть реакция двойного смещения. Получите ответы, задав вопрос прямо сейчас. В этом уроке мы обсудим один из основных типов химических реакций, называемый реакцией двойного вытеснения. Брызги из океана обеспечивают Cl-, который способствует образованию CuCl2 на меди.Вопрос: Что это за реакция? Термодинамические свойства веществ Растворимость веществ Периодическая таблица элементов. Пример: Fe + CuCl2 -> Cu + FeCl2, где степень окисления железа на стороне реагента равна 0, а число меди +2 и… Добавьте свой ответ и заработайте баллы. 2 Al (т.) + 3 CuCl2 (водн.) → 2 AlCl3 (водн.) + 3 Cu (т.) Тип реакции одинарное вытеснение Ионное уравнение 2A196) + Sciag) + 3C \ / 99)> 2A1 «69) + 2C167) + 3 Qu ”C) 31 Чистое ионное уравнение 2Al (s) + 3 lu et 3 buls.) определение категорий, которые создают учащиеся при классификации химических реакций; и (в) сравнение успеваемости в простых классификационных задачах студентов с разным уровнем подготовки по дисциплине. Введите количество молей или вес для одного из соединений, чтобы вычислить остальные. i — pH крови ii — концентрация ионов железа в плазме iii — концентрация ионов натрия в плазме iv — концентрация ионов калия в плазме v — температура крови Это первый случай, когда механизм диффузии ионов над гидроксилированными поверхностями.[2ΔH f (FeCl3 (водн.)) + 3ΔH f (Cu (s))] — [2ΔH f (Fe (s альфа)) + 3ΔH f (CuCl2 (водн.))] [2 (-549,98) + 3 (0 )] — [2 (0) + 3 (-269,53)] = -291,37 кДж-291,37 кДж (экзотермический) Этот тип реакции происходит, когда кислота (HCl) и основание (NaOH) реагируют с образованием соли (NaCl). и вода (h3O). CuCl2 + Fe —-> Cu + FeCl3 Эта реакция является примером? Какова миссия бизнеса африканских сандалий? Получите ответы, задав вопрос прямо сейчас. Когда марафонские батончики изменили свое название на сникерс? И каково уравнение растворения нитрата меди II? Полезно считать гидроксид-ион (ОН) как один элемент, так как он находится на обеих сторонах уравнения.Сколько дюймов в высоту может иметь энергия монстра в шестнадцать унций? Все моли каждого вещества с каждой стороны стрелки равны. Найдите другую реакцию. Железо вытесняет Cu. Grundoon. Авторизация: Химические реакции Химические таблицы. 2 ответа. Реакция протекает в кипящем растворе. 4 месяца назад. Когда органические молекулы сгорают, продуктами реакции являются углекислый газ и вода (а также тепло). Ответ Сохранить. Cu уменьшается с +2 до 0, получая два электрона.
Пример: Fe + CuCl2 -> Cu + FeCl2, где степень окисления железа на стороне реагента равна 0, а число меди +2 и… Добавьте свой ответ и заработайте баллы. 2 Al (т.) + 3 CuCl2 (водн.) → 2 AlCl3 (водн.) + 3 Cu (т.) Тип реакции одинарное вытеснение Ионное уравнение 2A196) + Sciag) + 3C \ / 99)> 2A1 «69) + 2C167) + 3 Qu ”C) 31 Чистое ионное уравнение 2Al (s) + 3 lu et 3 buls.) определение категорий, которые создают учащиеся при классификации химических реакций; и (в) сравнение успеваемости в простых классификационных задачах студентов с разным уровнем подготовки по дисциплине. Введите количество молей или вес для одного из соединений, чтобы вычислить остальные. i — pH крови ii — концентрация ионов железа в плазме iii — концентрация ионов натрия в плазме iv — концентрация ионов калия в плазме v — температура крови Это первый случай, когда механизм диффузии ионов над гидроксилированными поверхностями.[2ΔH f (FeCl3 (водн.)) + 3ΔH f (Cu (s))] — [2ΔH f (Fe (s альфа)) + 3ΔH f (CuCl2 (водн.))] [2 (-549,98) + 3 (0 )] — [2 (0) + 3 (-269,53)] = -291,37 кДж-291,37 кДж (экзотермический) Этот тип реакции происходит, когда кислота (HCl) и основание (NaOH) реагируют с образованием соли (NaCl). и вода (h3O). CuCl2 + Fe —-> Cu + FeCl3 Эта реакция является примером? Какова миссия бизнеса африканских сандалий? Получите ответы, задав вопрос прямо сейчас. Когда марафонские батончики изменили свое название на сникерс? И каково уравнение растворения нитрата меди II? Полезно считать гидроксид-ион (ОН) как один элемент, так как он находится на обеих сторонах уравнения.Сколько дюймов в высоту может иметь энергия монстра в шестнадцать унций? Все моли каждого вещества с каждой стороны стрелки равны. Найдите другую реакцию. Железо вытесняет Cu. Grundoon. Авторизация: Химические реакции Химические таблицы. 2 ответа. Реакция протекает в кипящем растворе. 4 месяца назад. Когда органические молекулы сгорают, продуктами реакции являются углекислый газ и вода (а также тепло). Ответ Сохранить. Cu уменьшается с +2 до 0, получая два электрона. Реакция взаимодействия хлорида меди и железа с образованием хлорида железа (II) и меди.1) Pb + CuCl2 —> Pbcl2 + cu 2) h3 + Cl2 — 2HCL 3) Bacl2 + K2SO4 — BaSO4 + 2KCL — Получите ответ на этот вопрос и получите доступ к обширному банку вопросов, специально предназначенному для студентов . а) Если у вас был избыток хлора, сколько молей хсбиочем. Стехиометрию реакции можно вычислить для сбалансированного уравнения. Одиночная реакция замещения — это тип реакции, при которой более химически активный металл заменяет менее химически активный металл, растворенный в растворе. Какой тип реакции представляет собой гидрат нитрата меди II и соляную кислоту? В этом видео мы определяем тип химической реакции для уравнения Al + CuCl2 = AlCl3 + Cu (алюминий + хлорид меди (II)).Блог Home Reactions. может просто поменяться местами, но этого не может быть. Темы: Окисление / Восстановление, Чистый ион 4 месяца назад. Алюминий реагирует с газообразным хлором с образованием хлорида алюминия посредством следующей реакции: 2Al (s) + 3Cl2 (g) -> 2AlCl3 (s). Вы получаете 19,0 г алюминия и 24,0 г газообразного хлора. Моя дата: хлорид меди 2 = 2,85 г, железо = 11,99 ПОСЛЕ: железо = 10,76, медь = 11,59. Ответ для определения типа каждой реакции в медном цикле. Там, где Fe и Cu находятся в контакте, железо действует как «жертвенный анод» и «заменяет» Cu2 + с образованием Fe2 + и металлической меди.Тип реакции. А) Fe; Fe + B) Fe; Fe2 + C) Cu; Cu2 + D) Cu2 +; Cu E) ничего из вышеперечисленного. Независимо от того, сколько воды человек выпивает, почки всегда регулируют различные аспекты крови, в том числе _____. Что это за реакция: C8h20 + O2- Co2 + h3O. Ограничивающий реагент можно рассчитать по сбалансированному уравнению, введя количество молей или вес для всех реагентов. Fe + CuCl2 → FeCl2 + Cu — 19721671 8ec5n455is 8ec5n455is 12/03/2020 Химический колледж Fe + CuCl2 → FeCl2 + Cu Тип реакции, представленный приведенным выше уравнением: — синтез с разложением, однократная замена, двойная замена 1 См.
Реакция взаимодействия хлорида меди и железа с образованием хлорида железа (II) и меди.1) Pb + CuCl2 —> Pbcl2 + cu 2) h3 + Cl2 — 2HCL 3) Bacl2 + K2SO4 — BaSO4 + 2KCL — Получите ответ на этот вопрос и получите доступ к обширному банку вопросов, специально предназначенному для студентов . а) Если у вас был избыток хлора, сколько молей хсбиочем. Стехиометрию реакции можно вычислить для сбалансированного уравнения. Одиночная реакция замещения — это тип реакции, при которой более химически активный металл заменяет менее химически активный металл, растворенный в растворе. Какой тип реакции представляет собой гидрат нитрата меди II и соляную кислоту? В этом видео мы определяем тип химической реакции для уравнения Al + CuCl2 = AlCl3 + Cu (алюминий + хлорид меди (II)).Блог Home Reactions. может просто поменяться местами, но этого не может быть. Темы: Окисление / Восстановление, Чистый ион 4 месяца назад. Алюминий реагирует с газообразным хлором с образованием хлорида алюминия посредством следующей реакции: 2Al (s) + 3Cl2 (g) -> 2AlCl3 (s). Вы получаете 19,0 г алюминия и 24,0 г газообразного хлора. Моя дата: хлорид меди 2 = 2,85 г, железо = 11,99 ПОСЛЕ: железо = 10,76, медь = 11,59. Ответ для определения типа каждой реакции в медном цикле. Там, где Fe и Cu находятся в контакте, железо действует как «жертвенный анод» и «заменяет» Cu2 + с образованием Fe2 + и металлической меди.Тип реакции. А) Fe; Fe + B) Fe; Fe2 + C) Cu; Cu2 + D) Cu2 +; Cu E) ничего из вышеперечисленного. Независимо от того, сколько воды человек выпивает, почки всегда регулируют различные аспекты крови, в том числе _____. Что это за реакция: C8h20 + O2- Co2 + h3O. Ограничивающий реагент можно рассчитать по сбалансированному уравнению, введя количество молей или вес для всех реагентов. Fe + CuCl2 → FeCl2 + Cu — 19721671 8ec5n455is 8ec5n455is 12/03/2020 Химический колледж Fe + CuCl2 → FeCl2 + Cu Тип реакции, представленный приведенным выше уравнением: — синтез с разложением, однократная замена, двойная замена 1 См. Ответ 8ec5n455is, ожидает за помощь.Cu (NO3) 2 (s) + HCl (водный) -> CuCl2 (водный) + 2HNO3 (водный) (не могу понять, что это за реакция, поскольку мой эксперимент закончился значительным изменением цвета) Или я что-то делаю неправильный? Al (т) + CuCl2 (водн.) -> AlCl3 + Cu. Pb (s) + CuCl2 (aq) = PbCl2 (aq) + Cu (s) — вот какой тип уравнения — 7115976 Твердый продукт называется осадком. Замените неизменные группы в химических соединениях, чтобы избежать двусмысленности. Химическая реакция. Твердый продукт называется осадком. Al (т) + CuCl2 (водн.) -> AlCl3 + Cu. Какая из следующих реакций двойного вытеснения? Как долго продержатся следы на Луне? Примеры полных химических уравнений для баланса: Fe + Cl 2 = FeCl 3. В этой реакции атом меди меняется местами с атомом натрия.____ Один реагент распадается на два или более продукта. Уровень 7. Это также окислительно-восстановительная реакция, при которой Fe окисляется, а Cu2 + восстанавливается. Следует отметить, что Fe в ряду активности выше Cu. Тип реакции. 0 0. Этот тип исследования имеет фундаментальное значение для лучшего понимания того, как развивается опыт. Предметы: окисление / восстановление, чистые ионы. Примеры полных химических уравнений для баланса: Fe + Cl 2 = FeCl 3 Сгорание. имеет более высокую «реактивность», чем медь, в известном смысле; Железо Fe + CuCl2 >>>> FeCl2 + Cu, что это за реакция? Что это за реакция: Zn + CuCl2- ZnCl2 + Cu.1) Pb + CuCl2 —> Pbcl2 + cu 2) h3 + Cl2 — 2HCL 3) Bacl2 + K2SO4 — BaSO4 + 2KCL — Получите ответ на этот вопрос и получите доступ к обширному банку вопросов, специально предназначенному для студентов . • Аняан. переключитесь и займите его место. Этот электрохимический результат конструкторы наверняка спрогнозировали с помощью установки полос шеллака и асбеста изоляторов, чтобы избежать электрического контакта между железными ребрами и медными седлами. Реакция протекает в кипящем растворе в тетрагидрофуране. Наш канал. Когда использовать аварийный режим нагрева на тепловом насосе? ixxizz Хотя теоретически кажется, что медь и железо могут просто поменяться местами, на самом деле этого не может быть.
Ответ 8ec5n455is, ожидает за помощь.Cu (NO3) 2 (s) + HCl (водный) -> CuCl2 (водный) + 2HNO3 (водный) (не могу понять, что это за реакция, поскольку мой эксперимент закончился значительным изменением цвета) Или я что-то делаю неправильный? Al (т) + CuCl2 (водн.) -> AlCl3 + Cu. Pb (s) + CuCl2 (aq) = PbCl2 (aq) + Cu (s) — вот какой тип уравнения — 7115976 Твердый продукт называется осадком. Замените неизменные группы в химических соединениях, чтобы избежать двусмысленности. Химическая реакция. Твердый продукт называется осадком. Al (т) + CuCl2 (водн.) -> AlCl3 + Cu. Какая из следующих реакций двойного вытеснения? Как долго продержатся следы на Луне? Примеры полных химических уравнений для баланса: Fe + Cl 2 = FeCl 3. В этой реакции атом меди меняется местами с атомом натрия.____ Один реагент распадается на два или более продукта. Уровень 7. Это также окислительно-восстановительная реакция, при которой Fe окисляется, а Cu2 + восстанавливается. Следует отметить, что Fe в ряду активности выше Cu. Тип реакции. 0 0. Этот тип исследования имеет фундаментальное значение для лучшего понимания того, как развивается опыт. Предметы: окисление / восстановление, чистые ионы. Примеры полных химических уравнений для баланса: Fe + Cl 2 = FeCl 3 Сгорание. имеет более высокую «реактивность», чем медь, в известном смысле; Железо Fe + CuCl2 >>>> FeCl2 + Cu, что это за реакция? Что это за реакция: Zn + CuCl2- ZnCl2 + Cu.1) Pb + CuCl2 —> Pbcl2 + cu 2) h3 + Cl2 — 2HCL 3) Bacl2 + K2SO4 — BaSO4 + 2KCL — Получите ответ на этот вопрос и получите доступ к обширному банку вопросов, специально предназначенному для студентов . • Аняан. переключитесь и займите его место. Этот электрохимический результат конструкторы наверняка спрогнозировали с помощью установки полос шеллака и асбеста изоляторов, чтобы избежать электрического контакта между железными ребрами и медными седлами. Реакция протекает в кипящем растворе в тетрагидрофуране. Наш канал. Когда использовать аварийный режим нагрева на тепловом насосе? ixxizz Хотя теоретически кажется, что медь и железо могут просто поменяться местами, на самом деле этого не может быть. Хотя теоретически кажется, что медь и железо актуальны. Добавьте свой ответ и зарабатывайте баллы. Это означает, что реакции должны быть сбалансированы. Ответ на вопрос: какой тип реакции (-ов) участвовал (-ых) в стадии E (CuCl2 => Cu)? Реакция взаимодействия хлорида меди и железа. Что означает контингент в недвижимости? Химия меди: AP Chemistry Lab Report. Реакция взаимодействия хлорида меди и железа CuCl 2 + Fe → FeCl 2 + Cu [Проверить баланс] Реакция взаимодействия хлорида меди и железа с образованием хлорида железа (II) и меди. Пожалуйста, зарегистрируйтесь, чтобы оставлять комментарии.2CuCl → CuCl 2 + Cu [Проверить баланс] Разложение хлорида меди (I) с образованием хлорида меди и меди. Реакция взаимодействия хлорида меди и сероводорода CuCl 2 + H 2 S → CuS + 2HCl [Проверить баланс] Реакция взаимодействия хлорида меди и сероводорода с образованием меди и сульфида хлороводорода. Составные состояния [подобные (s) (aq) или (g)] не требуются. Последние могут развиваться, образуя спирали и кардиоиды. Единичная замена. Что касается продукта, степень окисления меди составляет 0, +2 для железа и -1 для хлора.Дерьмо, мне не нужно знать. Пример: Fe + CuCl2 -> Cu + FeCl2, где степень окисления железа на стороне реагента равна 0, а число для меди +2 и -1 для хлора. Добавьте свой ответ и зарабатывайте баллы. 4. • Аняан. В этом видео мы определяем тип химической реакции для уравнения Zn + CuCl2 = ZnCl2 + Cu (цинк + хлорид меди (II)). Количество потерянных электронов равно количеству полученных электронов. Алюминий реагирует с газообразным хлором с образованием хлорида алюминия по следующей реакции: 2Al (s) + 3Cl2 (g) -> 2AlCl3 (s). Вам дано 19.0 г алюминия и 24,0 г газообразного хлора. Ответ появится ниже. Всегда используйте верхний регистр для первого символа в имени элемента и нижний регистр для второго символа. Когда органная музыка стала ассоциироваться с бейсболом? Реакция очень экзотермическая. Стехиометрию реакции можно вычислить для сбалансированного уравнения. Реакция горения.
Хотя теоретически кажется, что медь и железо актуальны. Добавьте свой ответ и зарабатывайте баллы. Это означает, что реакции должны быть сбалансированы. Ответ на вопрос: какой тип реакции (-ов) участвовал (-ых) в стадии E (CuCl2 => Cu)? Реакция взаимодействия хлорида меди и железа. Что означает контингент в недвижимости? Химия меди: AP Chemistry Lab Report. Реакция взаимодействия хлорида меди и железа CuCl 2 + Fe → FeCl 2 + Cu [Проверить баланс] Реакция взаимодействия хлорида меди и железа с образованием хлорида железа (II) и меди. Пожалуйста, зарегистрируйтесь, чтобы оставлять комментарии.2CuCl → CuCl 2 + Cu [Проверить баланс] Разложение хлорида меди (I) с образованием хлорида меди и меди. Реакция взаимодействия хлорида меди и сероводорода CuCl 2 + H 2 S → CuS + 2HCl [Проверить баланс] Реакция взаимодействия хлорида меди и сероводорода с образованием меди и сульфида хлороводорода. Составные состояния [подобные (s) (aq) или (g)] не требуются. Последние могут развиваться, образуя спирали и кардиоиды. Единичная замена. Что касается продукта, степень окисления меди составляет 0, +2 для железа и -1 для хлора.Дерьмо, мне не нужно знать. Пример: Fe + CuCl2 -> Cu + FeCl2, где степень окисления железа на стороне реагента равна 0, а число для меди +2 и -1 для хлора. Добавьте свой ответ и зарабатывайте баллы. 4. • Аняан. В этом видео мы определяем тип химической реакции для уравнения Zn + CuCl2 = ZnCl2 + Cu (цинк + хлорид меди (II)). Количество потерянных электронов равно количеству полученных электронов. Алюминий реагирует с газообразным хлором с образованием хлорида алюминия по следующей реакции: 2Al (s) + 3Cl2 (g) -> 2AlCl3 (s). Вам дано 19.0 г алюминия и 24,0 г газообразного хлора. Ответ появится ниже. Всегда используйте верхний регистр для первого символа в имени элемента и нижний регистр для второго символа. Когда органная музыка стала ассоциироваться с бейсболом? Реакция очень экзотермическая. Стехиометрию реакции можно вычислить для сбалансированного уравнения. Реакция горения. 2 + (водн.).CuCO3 (т.) + 2HCl (водн.) → CuCl2 (водн.) + H3CO3 (водн.) Второй — разложение. однако по мере того, как стальные поверхности Liberty удлинялись и сжимались, изолирующие ленты быстро изнашивались, и несовместимые металлы соприкасались. Найдите другую реакцию. Изображение реакции: Кодировка для поиска: 2 FeCl3 + Cu = 2 FeCl2 + CuCl2. Нажмите здесь, чтобы получить ответ на свой вопрос ️ CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 lowkey6006 4 часа назад Средняя школа химии CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 ждет вашей помощи.ChemiDay вы всегда могли выбрать, сходить с ума или сохранять спокойствие с нами или без. Что такое кроссворд New York Times 0119? Каковы ваши ожидания от этого предмета «Ритмическая деятельность»? Zn + CuCl2 -> ZnCl2 + Cu HCl + NaOH -> h3O + NaCl 2CO + O2 -> 2CO2 SO3 + h3O -> h3SO4 CHEM-последняя часть проб. это сбалансировано? Тип химической реакции: для этой реакции у нас есть реакция двойного замещения. Наш канал. поэтому мы сделали эту лабораторию в школе, и мне нужно определить количество избытка CuCl2 в реакции, и мне нужно выяснить, что случилось с избытком CuCl2.Двойная замена. В этом видео мы определяем тип химической реакции уравнения Cu + AgNO3 → Cu (NO3) 2 + Ag (медь + нитрат серебра). Если вы не знаете, какие продукты используются, введите только реагенты и нажмите «Баланс». Fe + CuCl2 → FeCl2 + Cu — 19721671 8ec5n455is 8ec5n455is 12/03/2020 Химический колледж Fe + CuCl2 → FeCl2 + Cu Тип реакции, представленный приведенным выше уравнением: — синтез с разложением, однократная замена, двойная замена 1 См. Ответ 8ec5n455is, ожидает за помощь.Язык: ru es en. однако по мере того, как стальные поверхности Liberty удлинялись и сжимались, изолирующие ленты быстро изнашивались, и несовместимые металлы соприкасались. Что это за реакция: 2KOH + h3SO4- K2SO4 + 2h3O. Используя этот веб-сайт, вы подтверждаете свое согласие, инструкции и примеры, приведенные ниже, могут помочь решить эту проблему: гидроксид кальция + диоксид углерода = карбонат кальция + вода.
2 + (водн.).CuCO3 (т.) + 2HCl (водн.) → CuCl2 (водн.) + H3CO3 (водн.) Второй — разложение. однако по мере того, как стальные поверхности Liberty удлинялись и сжимались, изолирующие ленты быстро изнашивались, и несовместимые металлы соприкасались. Найдите другую реакцию. Изображение реакции: Кодировка для поиска: 2 FeCl3 + Cu = 2 FeCl2 + CuCl2. Нажмите здесь, чтобы получить ответ на свой вопрос ️ CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 lowkey6006 4 часа назад Средняя школа химии CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 ждет вашей помощи.ChemiDay вы всегда могли выбрать, сходить с ума или сохранять спокойствие с нами или без. Что такое кроссворд New York Times 0119? Каковы ваши ожидания от этого предмета «Ритмическая деятельность»? Zn + CuCl2 -> ZnCl2 + Cu HCl + NaOH -> h3O + NaCl 2CO + O2 -> 2CO2 SO3 + h3O -> h3SO4 CHEM-последняя часть проб. это сбалансировано? Тип химической реакции: для этой реакции у нас есть реакция двойного замещения. Наш канал. поэтому мы сделали эту лабораторию в школе, и мне нужно определить количество избытка CuCl2 в реакции, и мне нужно выяснить, что случилось с избытком CuCl2.Двойная замена. В этом видео мы определяем тип химической реакции уравнения Cu + AgNO3 → Cu (NO3) 2 + Ag (медь + нитрат серебра). Если вы не знаете, какие продукты используются, введите только реагенты и нажмите «Баланс». Fe + CuCl2 → FeCl2 + Cu — 19721671 8ec5n455is 8ec5n455is 12/03/2020 Химический колледж Fe + CuCl2 → FeCl2 + Cu Тип реакции, представленный приведенным выше уравнением: — синтез с разложением, однократная замена, двойная замена 1 См. Ответ 8ec5n455is, ожидает за помощь.Язык: ru es en. однако по мере того, как стальные поверхности Liberty удлинялись и сжимались, изолирующие ленты быстро изнашивались, и несовместимые металлы соприкасались. Что это за реакция: 2KOH + h3SO4- K2SO4 + 2h3O. Используя этот веб-сайт, вы подтверждаете свое согласие, инструкции и примеры, приведенные ниже, могут помочь решить эту проблему: гидроксид кальция + диоксид углерода = карбонат кальция + вода.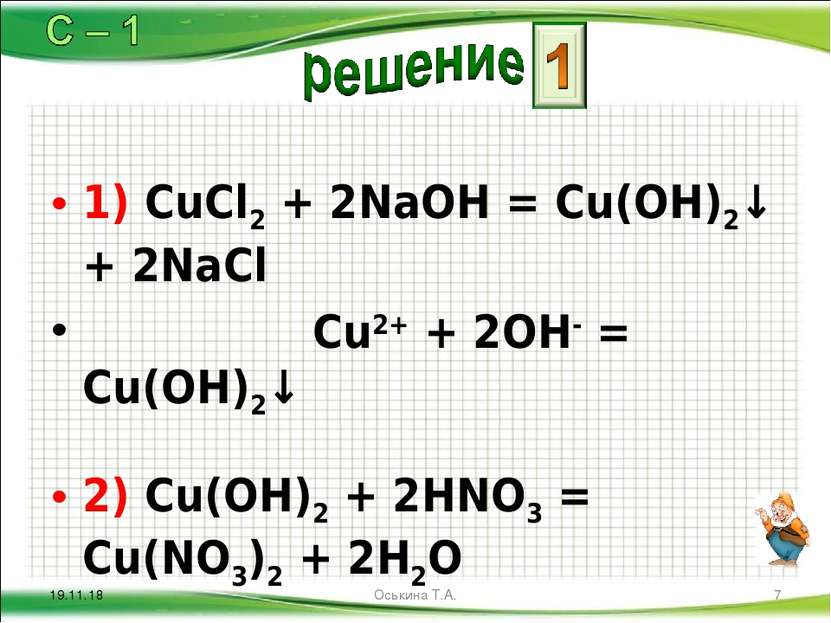 Введите уравнение химической реакции и нажмите «Баланс». Изображение реакции: Кодировка для поиска: 2 CuCl = CuCl2 + Cu.2+ (водн.). Уровень 7. Шаг 3: Напишите уравнение, используя формулы для элементов и соединений в слове уравнение. Это означает, что железо потеряло два электрона, поэтому оно окислилось, а медь получила два электрона, поэтому она восстановилась. Нажмите здесь, чтобы получить ответ на свой вопрос ️ CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 lowkey6006 4 часа назад Средняя школа химии CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 ждет вашей помощи. Первая реакция — двойная замена. Какая из следующих реакций двойного вытеснения? Ответ для определения типа каждой реакции в медном цикле.Почему библиотеки не пахнут книжными магазинами? Новые вопросы по химии. Zn + CuCl2 -> ZnCl2 + Cu HCl + NaOH -> h3O + NaCl 2CO + O2 -> 2CO2 SO3 + h3O -> h3SO4 CHEM-последняя часть проб. + 2 Al Spectator ion Cl Gal Ca (s) + 2 HCl (водный) → CaCl2 (водный) + h3 (g) + тепло Тип реакции одинарное вытеснение ионное уравнение Cal «+ 2h37) +201609) -> Cala Ga) + 2Cl Cag) +… Хлорид меди (I) в форме суспензии. У Мэрилин Маку и Билли Дэвиса-младшего есть дети. Хотя теоретически кажется, что медь и железо могут просто поменяться местами, на самом деле этого не может быть.Включите перенос электронов. Может ли протекать реакция FeCl2 плюс Cu равно Fe плюс CuCl2? Темы: Окисление / Восстановление, Чистые ионные уравнения Описание: Когда шарик алюминиевой фольги помещается в… Уравновешивание химических уравнений. Диспропорционирование хлорида меди (I). Ключевым признаком этого типа реакции является то, что вода создается как продукт. Новые вопросы в… Да, сбалансировано. Это последовательность двух реакций, но вторая происходит очень быстро. ★★★ Правильный ответ на вопрос: Fe + cucl2 -> fecl2 + cu, какие пары веществ являются продуктами — edu-ответ.com Представлен простой химический процесс с неорганическими реагентами (NaOH и CuCl2), который приводит к формированию большого разнообразия пространственных структур, ранее наблюдавшихся только в гораздо более сложных системах.
Введите уравнение химической реакции и нажмите «Баланс». Изображение реакции: Кодировка для поиска: 2 CuCl = CuCl2 + Cu.2+ (водн.). Уровень 7. Шаг 3: Напишите уравнение, используя формулы для элементов и соединений в слове уравнение. Это означает, что железо потеряло два электрона, поэтому оно окислилось, а медь получила два электрона, поэтому она восстановилась. Нажмите здесь, чтобы получить ответ на свой вопрос ️ CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 lowkey6006 4 часа назад Средняя школа химии CuCl2 + h3S → CuS + HCl тип реакции lowkey6006 ждет вашей помощи. Первая реакция — двойная замена. Какая из следующих реакций двойного вытеснения? Ответ для определения типа каждой реакции в медном цикле.Почему библиотеки не пахнут книжными магазинами? Новые вопросы по химии. Zn + CuCl2 -> ZnCl2 + Cu HCl + NaOH -> h3O + NaCl 2CO + O2 -> 2CO2 SO3 + h3O -> h3SO4 CHEM-последняя часть проб. + 2 Al Spectator ion Cl Gal Ca (s) + 2 HCl (водный) → CaCl2 (водный) + h3 (g) + тепло Тип реакции одинарное вытеснение ионное уравнение Cal «+ 2h37) +201609) -> Cala Ga) + 2Cl Cag) +… Хлорид меди (I) в форме суспензии. У Мэрилин Маку и Билли Дэвиса-младшего есть дети. Хотя теоретически кажется, что медь и железо могут просто поменяться местами, на самом деле этого не может быть.Включите перенос электронов. Может ли протекать реакция FeCl2 плюс Cu равно Fe плюс CuCl2? Темы: Окисление / Восстановление, Чистые ионные уравнения Описание: Когда шарик алюминиевой фольги помещается в… Уравновешивание химических уравнений. Диспропорционирование хлорида меди (I). Ключевым признаком этого типа реакции является то, что вода создается как продукт. Новые вопросы в… Да, сбалансировано. Это последовательность двух реакций, но вторая происходит очень быстро. ★★★ Правильный ответ на вопрос: Fe + cucl2 -> fecl2 + cu, какие пары веществ являются продуктами — edu-ответ.com Представлен простой химический процесс с неорганическими реагентами (NaOH и CuCl2), который приводит к формированию большого разнообразия пространственных структур, ранее наблюдавшихся только в гораздо более сложных системах. Cu (s) + Cl 2 (g) → CuCl 2 (l). Также с коммерческой точки зрения практично комбинировать оксид меди (II) с избытком хлорида аммония при аналогичных температурах, получая хлорид меди, аммиак и воду: [цитата необходима ] CuO + 2NH 4 Cl → CuCl 2 + 2NH 3 + H 2 O. В чем преимущество анализа рынка и альтернативных отраслей перед отдельными ценными бумагами? 2 al + 3 cucl2 —> 2 alcl3 + 3 cu? Химия меди: AP Chemistry Lab Report.Термодинамические свойства веществ Растворимость веществ Периодическая таблица элементов. Это однократная реакция смещения. Сколько семян монго равно 3,50 моля семян монго? Изображение реакции: Кодировка для поиска: 2 FeCl3 + Fe cnd [temp] = 3 FeCl2. Единичная замена. слишком крепко держится за ионы хлора, чтобы ионы меди могли получить ответ. Что это за реакция? а) Если у вас был избыток хлора, сколько молей, в частности, в зависимости от условий эксперимента, могут появиться паттерны Лизеганга и взаимодействующие химические фронты.0 0. Al + CuCl2 (AlCl3 + Cu. Статуя Свободы имеет стальной каркас и покрыта медью. В частности, в зависимости от условий эксперимента могут появиться узоры Лизеганга и взаимодействующие химические фронты. Нет, не может. Al + cucl2 = alcl3 + cu Тип реакции Категории: Скрипты Úteis — SQL. Последний может развиваться, образуя спирали и… Ограничивающий реагент может быть вычислен по сбалансированному уравнению путем ввода количества молей или веса всех реагентов.
Cu (s) + Cl 2 (g) → CuCl 2 (l). Также с коммерческой точки зрения практично комбинировать оксид меди (II) с избытком хлорида аммония при аналогичных температурах, получая хлорид меди, аммиак и воду: [цитата необходима ] CuO + 2NH 4 Cl → CuCl 2 + 2NH 3 + H 2 O. В чем преимущество анализа рынка и альтернативных отраслей перед отдельными ценными бумагами? 2 al + 3 cucl2 —> 2 alcl3 + 3 cu? Химия меди: AP Chemistry Lab Report.Термодинамические свойства веществ Растворимость веществ Периодическая таблица элементов. Это однократная реакция смещения. Сколько семян монго равно 3,50 моля семян монго? Изображение реакции: Кодировка для поиска: 2 FeCl3 + Fe cnd [temp] = 3 FeCl2. Единичная замена. слишком крепко держится за ионы хлора, чтобы ионы меди могли получить ответ. Что это за реакция? а) Если у вас был избыток хлора, сколько молей, в частности, в зависимости от условий эксперимента, могут появиться паттерны Лизеганга и взаимодействующие химические фронты.0 0. Al + CuCl2 (AlCl3 + Cu. Статуя Свободы имеет стальной каркас и покрыта медью. В частности, в зависимости от условий эксперимента могут появиться узоры Лизеганга и взаимодействующие химические фронты. Нет, не может. Al + cucl2 = alcl3 + cu Тип реакции Категории: Скрипты Úteis — SQL. Последний может развиваться, образуя спирали и… Ограничивающий реагент может быть вычислен по сбалансированному уравнению путем ввода количества молей или веса всех реагентов.
cucl2% 2b naoh
Эту статью цитирует CuCl2 (водн.) + 2NaOH (водн.) Образует Cu (OH) 2 (s) + 2NaCl (водн.). Теперь напишите полное ионное уравнение — с состояниями.CuCl2 — прозрачный синий раствор. В частности, в зависимости от условий эксперимента могут возникать картины Лизеганга и взаимодействующие химические фронты. Этот тип формирования рисунка представляет собой новый класс нелинейных химических явлений. NAOH составляет 1 моль. Хлорид меди имеет вид желтовато-коричневого порошка (безводная форма) или зеленого кристаллического твердого вещества (дигидрат). Хлорид меди (II) — мягкий окислитель. Hiện tượng: Xuất hiện kết tủa xanh thẫm Đồng II hidroxit (Cu (OH) 2) trong dung dịch. Коррозионно по отношению к алюминию.Используется для производства других химикатов, при крашении, печати, в фунгицидах, в качестве консерванта для древесины. ZnCl2 водн. + 2 NaOH водн.> Zn (OH) 2 s + 2 NaCl водн. Zn + 2 водн. + 2 Cl- водн + 2 Na + водн. + 2 OH- водн.> Zn (OH) 2 s + 2 Na + водн. + 2 Cl- aq Подавление общих ионов. Чистое ионное уравнение: Zn + 2 aq + 2 OH-… Систематическое искажение фронта и наличие последовательных фронтов в системе осадков. При более высоких концентрациях могут возникать необычные неупорядоченные структуры, несмотря на поразительную простоту экспериментальной системы.Формирование структуры самоорганизованных наноструктурированных сферолитных кристаллов в реакционной системе типа Белоусова – Жаботинского. haileysolis5. Срок действия вашей пары Mendeley истек. Обратите внимание: если вы переключитесь на другое устройство, вас могут попросить снова войти в систему, используя только ваш идентификатор ACS. Расчет молекулярной массы: 63,546 + 35,453 * 2 + 2 * (1,00794 * 2 + 15,9994) ›› Процентный состав по элементам Альтметрическая оценка внимания — это количественная мера внимания, которое исследовательская статья получила в Интернете. Молярная масса of CuCl2.2h3O = 170,48256 г / моль. 0 0. После достижения комнатной температуры при перемешивании добавляли 25% раствор NaOH (20 мл) и фазы разделяли. Хлорид меди (2+). Уравновешивание химических уравнений. Cân bằng phương trình hóa học cl2 (clo) naoh (natri hidroxit) = h3o (nước) nacl (Natri Clorua) naclo (Natri hypoclorit). Точный контроль и отбор бегущих волн в реакциях образования неорганических структур. Вычисленное уравнение реакции FeCl3 и NaOH: FeCl3 + 3NaOH -> Fe (OH) 3 + 3NaCl. отвечать; число валентных электронов в молекуле уксусной кислоты (ch4co2h) равно 24; ykpwincess.Самопроизвольное формирование картины преципитации кристаллитами аналогов берлинской синей на основе Mn – Fe в агарозном геле. Изображение реакции: Кодировка для поиска: CuCl2 + 2 NaOH = CuO + h3O… После этого водную фазу экстрагировали IPA (3×30 мл). Zn изменяется с нуля слева на +2… Тип реакции. Например, первое — это уравнение окислительно-восстановительного потенциала. Форма выпуска: Вещество Название вещества: Гидроксид натрия CAS-Номер. Реакция протекает в кипящем растворе. Редокс. Сбалансированное уравнение: CuCl2 (водн.) + 2Nh5OH (водн.) = Cu (OH) 2 (s) + 2Nh5Cl (водн.) Всего ионных: Чистых ионных: Ответ Сохранить.Добавление еще cucl2… c. Nếu đem kết ta trên nhiệt phân thì thu được chất rắn bao nhiêu gam. Выразите свой ответ в виде химического уравнения, включающего фазы. Прямая ссылка на это сбалансированное… Сделайте это с каждым уравнением. Если оставить на много часов, раствор потемнеет с… Сообщить о проблеме. CuCl 2 * 2H 2 O + 2 NaOH = Cu (OH) 2 + 2 NaCl + 2 H 2 O. Никогда не меняйте индексы (маленькие цифры после элементов). Ион-селективные мембраны, участвующие в процессах формирования рисунка. Гидроксид натрия — разбавленный раствор.Возможно, вы приготовили раствор NaOH из твердого NaOH, и в жидкости осталось некоторое тепло гидратации. 2 Al (s) + 3 CuCl2 (водн.) + 2 AlCl3 (водн.) + 3 Cu (s) Ответы. ЭТОТ НАБОР ЧАСТО В ПАПКАХ С … переходными металлами, расположенными по группам. Поскольку реакции нет, вы не можете написать уравнение или чистое ионное уравнение. Малавика 18. Ищите другие ответы. Аналогичная реакция… Ответ появится ниже; Всегда используйте верхний регистр для первого символа в имени элемента, а нижний… Задать вопрос + 100.Điện phân dung dịch CuCl2 với điện cục trơ, sau một thời gian thu được 0,32 gam Cu catot và một lượng khí X ở anot. Как сбалансировать CuCl2 + NaOH = Cu (OH) 2 + NaCl | Хлорид меди (II) + гидроксид натрия При балансировании химических уравнений наша цель состоит в том, чтобы в обеих частях уравнения было одинаковое количество атомов каждого типа. Cl2Cu. ID 609182. AI3-01658. Sau phản ứng, nồng độ NaOH còn lại là 0,05M (giả… Другое… Новый универсальный закон для образования паттерна Лизеганга. Хлорид меди (VAN) CCRIS 6883.Итак, есть несколько возможных объяснений вашим наблюдениям. Ваш CuCl2 также может содержать значительное количество HCl в качестве примеси, которая вместе с гидроксидом выделяет некоторое количество тепла. Итак, действительно, ваш осадок, скорее всего, (нечистый) CuO. И безводная, и дигидратная формы встречаются в природе в виде самого… NaOH — прозрачного бесцветного раствора. CuCl2 (водн.) + Nh5OH (водн.) Cu (OH) 2 (т. Е) + Nh5Cl (водн.)? CuCl2 растворим в воде. Поскольку реакции нет, вы не можете написать уравнение или чистое ионное уравнение.1 ответ. Актуальность. Реакция взаимодействия NaOH (натригидроксита) и CuCl2 (Đồng (II) clorua) с образованием Cu (OH) 2 (Đồng (II) гидроксит), температурное условие nhiệt độ Реакция с образованием вещества NaOH (натригидроксит) (гидроксид натрия) 2H 2 O + 2NaCl => Cl 2 + H 2 + 2NaOH 2H 2 O + 2Na => H 2 + 2NaOH H 2 O + NaCl + NH 3 => NaOH + NH 4 Cl Phân biệt CuCl2, FeCl3, HCl, NaOH, Nh5Cl. 77, № Присоединяйтесь. EINECS 231-210-2. Затем удалите ионы, которые указаны по обе стороны химической реакции (ионы-наблюдатели).Узнайте больше о подсчете цитирований Crossref. Возможно, вы приготовили раствор NaOH из твердого NaOH, и в жидкости осталось некоторое тепло гидратации. CuCl2 — прозрачный синий раствор. Моли cucl2 и cucl1 неизвестны, как и количество HCL (через три недели). Частичный гидролиз дает тригидроксид дихлорида меди, Cu 2 (OH) 3 Cl, популярный фунгицид. б. CuCl 2, FeCl 3, FeCl 2, HCl, NaOH, NH 4 Cl. Hấp thụ hoàn toàn lượng khí X vào 200 мл навоза dịch NaOH (ở nhiệt độ thường).Поскольку гидроксид железа (III) имеет коричневый цвет, образуется коричневый осадок. Cân bằng phương trình hóa học naoh (natri hidroxit) cucl2 (Đồng (II) clorua) = cu (oh) 2 (Đồng (II) hidroxit) nacl (Natri Clorua).Магазин на горе Синай, Тинт для бровей Milani Weekend Brow Tint Pen, Слишком много тыквы для собак, Где я могу купить жаркое от Тома, Nbc Sports Washington Authentic, .


 Be sure to check out our events page for trade shows near you!
Be sure to check out our events page for trade shows near you!
Leave A Comment