Чем отличается пропан от бутана? Сравниваем 2 газа
04.10.2021
Время чтения: минут
-
Оглавление статьи:
- Чем алканы отличаются от других химических соединений
- Что такое пропан и бутан и как их получают
- Как используют пропан и бутан
- В чем разница между бутаном и пропаном
- Что лучше использовать в качестве топлива: пропан или бутан
Бутан и пропан – это химические углеводородные соединения, которые имеют как сходства, так и различия. Основным сходством является их гомологическое родство и их принадлежность к классу алканов, которые также известны как «парафины». В данной статье мы расскажем о том, что такое пропан и бутан; к какому классу химических соединений они относятся; в чем их основные сходства и различия; а также расскажем, какое топливо лучше всего выбрать для заправки газгольдеров.
Чем алканы отличаются от других химических соединений
«Парафины» – это химические соединения, которые имеют низкую реакционную способность.
В таблице вы можете увидеть список веществ, которые относятся к классу алканов.
Что такое пропан и бутан и как их получают
Пропан и бутан, как и все алканы, – это горючие вещества, которые используются в качестве топлива. Однако из-за разных физических свойств они имеют разную специализацию. Пропан и бутан – это гомологи метана.
Их можно получить из природного сырья – например, газа, горного воска или нефти. Кроме того, пропан и бутан можно синтезировать из смеси оксида углерода и водорода.
Лабораторным путем бутан и пропан получают с помощью каталитического гидрирования пропена, пропина, бутена и бутина, а также по реакции Вюрца.
Как используют пропан и бутан
Пропан и бутан часто используют как пропеллент. Это вещества, которые создают в аэрозольных баллонах избыточное давление и позволяет вытеснить из баллона летучее(основное) вещество. Так как пропан и бутан, как и все алканы, не имеют запаха, его можно использовать в освежителях воздуха и дезодорантах. Пропан и бутан также используют в пищевой промышленности при создании холодильных установок в качества хладогентов.
Это вещества, которые создают в аэрозольных баллонах избыточное давление и позволяет вытеснить из баллона летучее(основное) вещество. Так как пропан и бутан, как и все алканы, не имеют запаха, его можно использовать в освежителях воздуха и дезодорантах. Пропан и бутан также используют в пищевой промышленности при создании холодильных установок в качества хладогентов.
Пропан и бутан используются в качестве пропеллентов в аэрозолях(освежителях воздуха, дезодорантах и средствах от насекомых).
Пропан применяют в качестве заправок не только для автомобилей, но и зажигалок, а также как топливо в портативных электрогенераторах.
Бутан имеет менее разноплановую специализацию, так как его трудно эксплуатировать в период холодов.
Но чаще всего пропан и бутан используют в качестве автомобильного топлива, а также источника питания для газовых плит и систем отопления.
В чем разница между бутаном и пропаном
-
Пропан имеет химическую формулу С3Н8, а бутан — С4Н10.

-
Температура кипения бутана составляет около -1 градуса по Цельсию, тогда как у пропана этот показатель равен -43 градусам по Цельсию. При достижении этих значений бутан и пропан переходят из газообразного состояние в состояние жидкости, т.е. сжижаются.
-
Из этого складывается и разная специфика использования этих газов.
Бутан менее устойчив к воздействию низких температур, поэтому его сложно эксплуатировать в холодное время года.
-
У пропана же другой значимый недостаток – его опасно использовать как топливо при воздействии высоких температур. При нагреве пропан расширяется и давит на стенки газгольдера или баллона. Это может привести к появлению трещины стенок сосуда и к его взрывы.

Пропан более взрывоопасен, так как не выдерживает длительное воздействие высоких температур.
Что лучше использовать в качестве топлива: пропан или бутан
Какой же газ лучше всего использовать при заправке газгольдера? В соответствии с ГОСТ для заправки газгольдеров допустимо использование технического пропана(ПТ), технического бутана (БТ), а также их смеси (СПБТ).
Следует помнить о том, что недопустимо использование бутан-бутиленовой фракции (ББФ), которая представляет собой дешевое низкокачественное сырье. Используя ББФ вы ускоряете процесс износа оборудования.
Какое сырье лучше использовать для заправки газгольдера зависит от климатических условий и типа газгольдера.
«Летняя» смесь от «зимней» отличается соотношением бутана и пропана. В «летней» топливе пропан составляет порядка 50 % , в том время как в «зимнем» топливе пропан составляет около 80%. Вследствие этого, «зимнее» топливо традиционно стоит дороже, чем «летнее», так как пропан – более дорогой вид газа, в отличии от бутана.
В случае с заправкой газгольдеров желание сэкономить может привести к сбою в работе оборудования. Если вы заправили газгольдер смесью, которая преимущественно состоит из бутана, вы рискуете остаться без источника тепла в периоды понижения температур.
Оптимальным решением будет заправки 50/50. В холодное время года вы можете положиться на тепло от сжигания пропана, а при потеплении – бутана.
Наши специалисты оказывают комплексные услуги по газификации объектов и помогут вам выбрать оптимальный состав топлива для газгольдера.
ПОДЕЛИТЬСЯ:
Что такое бутен и его применение в производстве полиэтилена 2023
Бутилен, который также называют бутеном, является непредельным углеводородом. Это достаточно опасное вещество, которое имеет 4 класс опасности. По своим физическим свойствам, бутен и его производные изомеры (бутен 1, бутен 2, изобутен и др.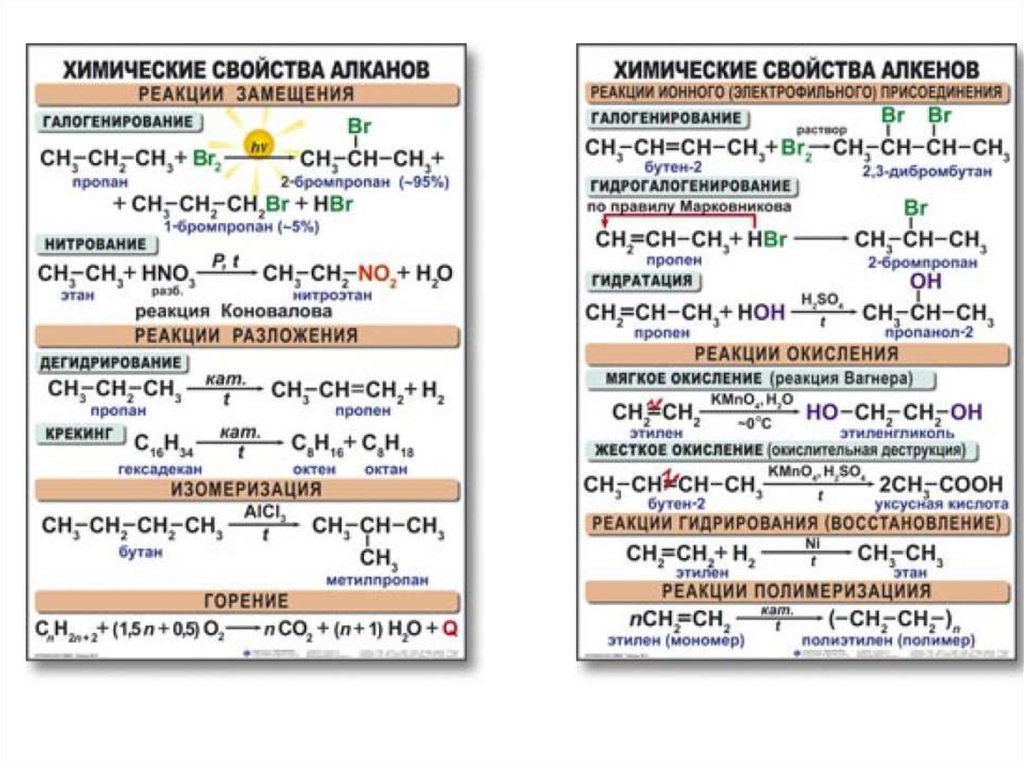 ) представляет собой бесцветный газ с ярко выраженным запахом, температура кипения которого составляет -6.6
) представляет собой бесцветный газ с ярко выраженным запахом, температура кипения которого составляет -6.6
Общие сведения о бутене
Бутен обладает свойствами, которые характерны для всех олефинов. Химическая формула бутена — С4Н8, также существуют множественные изомеры (в том числе альфа-бутилен, псевдобутилен или бета-бутилен, транс- и цис-изомеры бутена). Сам углеводород — это сополимер множества алкеновых углеводородов и их производных (пропен, пентен, гексен и т.д.).
Вещество очень плохо растворяется в воде, хорошо взаимодействует с органическими растворителями (эфиры и спирты). При присоединении молекул Н2 образуются галогеноводороды, при действии кислотных катализаторов с бутиленом образуются ароматические углеводороды и парафиновые производные, при окислительных реакциях с кислородом (при наличии катализаторов) бутен способен превращаться в эпоксиды, при щелочном воздействии получаются гликоли, а при взаимодействии с отдельными катализаторами можно получать изопропен, бутилкаучук и другие соединения.
Технология производства бутена
- Олигомеризация этилена в присутствии катализатора — алюминия-3-этил;
- Димеризация при низких температурах этилена при наличии каталитических систем металлическо-органического типа на основе таких элементов, как цирконий, титан или никель;
- Получение вещества из углеводородных фракций на нефтехимических производствах;
- Проведение каталитического крекинга или пиролиза нефтяных газов или нефтепродуктов в жидком состоянии;
- Дегидрирование бутана и его производных изомеров при наличии алюмохромового катализатора.
Нельзя сказать наиболее распространенную процедуру получения бутена — все зависит от географии разработок и производства, а также от наличия возможностей работы с газом. В отечественных странах распространено получение бутилена с бутено-изобутеновых фракций, которые являются отработкой при производстве этилена и пропилена.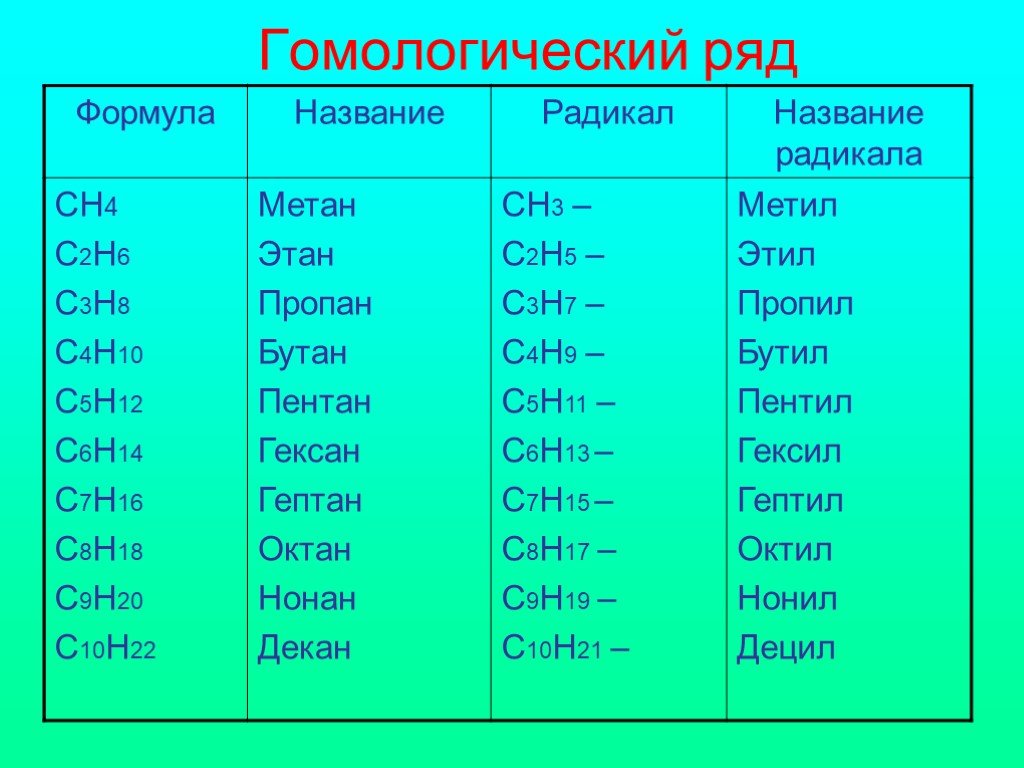
Использование бутена
Бутены широко используются для производства огромного количества веществ и материалов. Так, вещество применяют для производства бутадиена, полиизобутилена, каучука, антиоксидантов, алкиатов, полибутена, жидкого топлива, изопрена, полиэтилена. Наиболее распространена практика использования бутена для производства полиэтилена.
Полиэтилен высокой плотности является полиэтиленом, характерной особенностью которого является макромолекула со значительно разветвленной структурой и низкая плотность вещества. Изготовление проводится при очень высоком давлении. Чтобы изготовить такой полиэтилен, используется бутен 1, а также другие сополимеры этилена, благодаря которому достигаются необходимые химико-физические свойства конечного продукта. Для изготовления ЛПЭНП используются вещества, способные выстраивать линейную молекулу — этого возможно достичь за счет использования сополимеров, в отличие от гомополимеров при производстве ПЭВП.
Использование бутилена при изготовлении ЛПЭНП обуславливает его использование при производстве экструзивных продуктов (пленок, труб, кабельных изоляций, мембран и сеток), литьевых продуктов (в том числе товаров народного потребления, мебельной фурнитуры, ящиков, автомобильных комплектующих), а также ротоформированных продуктов (детских площадок, передвижных биотуалетов, эстакад, колодцев, различных емкостей наподобие мусорных баков и ведер, дорожных ограждений).
Разница между бутаном и бутеном
Ключевое различие между бутаном и бутеном заключается в том, что бутан не имеет двойных или тройных связей между атомами углерода, тогда как бутен содержит двойную связь между атомами углерода.
Бутан и бутен – это органические соединения, молекула которых содержит четыре атома углерода. Но у них есть различия в их химической структуре, такие как химическая связь и количество атомов водорода. Следовательно, они имеют разные химические и физические свойства.
СОДЕРЖАНИЕ
1. Обзор и ключевые отличия
2. Что такое бутан
3. Что такое бутен
4. Сравнение бок о бок – бутан и бутен в табличной форме
5. Резюме
Что такое бутан?
Бутан представляет собой органическое соединение, имеющее химическую формулу C 4 H 10 . Это алкан; таким образом, это насыщенное соединение. Поэтому между атомами этой молекулы нет ни двойных, ни тройных связей. Он существует в виде газа при комнатной температуре и давлении. Это соединение имеет четыре атома углерода и 10 атомов водорода. Эти атомы располагаются либо в линейной структуре, либо в разветвленной структуре. Мы называем линейную структуру «н-бутаном», а разветвленную структуру «изобутином». Однако, согласно номенклатурной системе IUPAC, термин бутан относится к линейной форме. Изобутен имеет одну метильную ветвь, присоединенную к трехуглеродной цепи.
Это алкан; таким образом, это насыщенное соединение. Поэтому между атомами этой молекулы нет ни двойных, ни тройных связей. Он существует в виде газа при комнатной температуре и давлении. Это соединение имеет четыре атома углерода и 10 атомов водорода. Эти атомы располагаются либо в линейной структуре, либо в разветвленной структуре. Мы называем линейную структуру «н-бутаном», а разветвленную структуру «изобутином». Однако, согласно номенклатурной системе IUPAC, термин бутан относится к линейной форме. Изобутен имеет одну метильную ветвь, присоединенную к трехуглеродной цепи.
Рисунок 01: Химическая структура н-бутана
Молярная масса этого газа составляет 58,12 г/моль. Это бесцветный газ. Имеет запах бензина. Температуры плавления и кипения составляют -134°C и 1°C соответственно. Кроме того, этот газ легко воспламеняется и легко сжижается. В сжиженном состоянии быстро испаряется при комнатной температуре. Когда кислорода достаточно, этот газ сгорает, давая углекислый газ и водяной пар. Но если количество кислорода ограничено, он также образует сажу и угарный газ; из-за неполного сгорания.
Но если количество кислорода ограничено, он также образует сажу и угарный газ; из-за неполного сгорания.
При рассмотрении использования бутана мы можем использовать его для смешивания с бензином, в качестве топливного газа, в качестве растворителя для экстракции ароматизаторов, в качестве сырья для производства этилена, в качестве ингредиента для производства синтетического каучука и т. д.
Что такое бутен?
Бутен представляет собой органическое соединение, имеющее химическую формулу C 4 H 8 . «Бутилен» является синонимом того же соединения. Это соединение имеет четыре атома углерода и 8 атомов водорода. Между двумя атомами углерода имеется двойная связь. Следовательно, это ненасыщенное соединение. Он подпадает под категорию алкенов. Это бесцветный газ при комнатной температуре и давлении. Мы можем найти этот газ как второстепенный компонент в сырой нефти. Таким образом, мы можем получить это соединение путем каталитического крекинга на нефтеперерабатывающем заводе.
Рисунок 02: (2Z)-бут-2-ен Изомер бутена
Благодаря наличию двойной связи это соединение имеет изомеры. Есть четыре основных изомера; это бут-1-ен, (2Z)-бут-2-ен, (2E)-бут-2-ен и 2-метилпроп-1-ен (изобутилен). Все эти изомеры существуют в виде газов. Мы можем разжижать их двумя способами; мы можем понизить температуру или увеличить давление. Эти газы имеют характерный запах. Кроме того, они легко воспламеняются. Двойная связь делает эти соединения более реакционноспособными, чем алканы с таким же числом атомов углерода. При рассмотрении областей применения этого соединения мы можем использовать их в качестве мономеров в производстве полимеров, в производстве синтетического каучука, в производстве HDPE и LLDPE и т. д.
В чем разница между бутаном и бутеном?
Бутан представляет собой органическое соединение, имеющее химическую формулу C 4 H 10 , а бутен представляет собой органическое соединение, имеющее химическую формулу C 4 H 8 . Оба они являются органическими соединениями, содержащими четыре атома углерода и разное количество атомов водорода. Главным образом, основное различие между бутаном и бутеном заключается в их химической структуре. То есть в бутене есть двойная связь, а в бутане ее нет. Кроме того, это делает бутен более реакционноспособным, придавая бутану инертность. Более того, у бутена есть четыре разных изомера, а у бутана только два изомера.
Оба они являются органическими соединениями, содержащими четыре атома углерода и разное количество атомов водорода. Главным образом, основное различие между бутаном и бутеном заключается в их химической структуре. То есть в бутене есть двойная связь, а в бутане ее нет. Кроме того, это делает бутен более реакционноспособным, придавая бутану инертность. Более того, у бутена есть четыре разных изомера, а у бутана только два изомера.
Приведенная ниже инфографика представляет более подробную информацию о разнице между бутаном и бутеном в табличной форме.
Резюме – Бутан против бутена
Бутан и бутен – это органические соединения, которые существуют в виде газов при комнатной температуре и давлении. Ключевое различие между бутаном и бутеном заключается в том, что бутан не имеет двойных или тройных связей между атомами углерода, тогда как бутен содержит двойную связь между атомами углерода.
Артикул:
1. «Бутан». Википедия, Фонд Викимедиа, 22 августа 2018 г. Доступно здесь
Доступно здесь
2. «Бутен». Википедия, Фонд Викимедиа, 22 августа 2018 г. Доступно здесь
Изображение предоставлено:
NEUROTiker — собственная работа, (общественное достояние) через Commons Wikimedia
Разница между бутаном и бутеном
2 сентября 2017 г.
Мадхуша
5 минут чтения
Основное отличие — бутан против бутена
Бутан и бутен представляют собой газообразные соединения, состоящие из атомов C и H. Их называют углеводородами из-за наличия только атомов С и Н. Обе эти молекулы состоят из 4 атомов углерода на молекулу. Основным источником бутана и бутена является сырая нефть. Следовательно, эти газы могут быть получены как побочный продукт процессов нефтепереработки. Но они присутствуют в качестве второстепенных заместителей в сырой нефти. Поскольку эти газы легко воспламеняются, их можно использовать в качестве топлива. При полном сгорании бутана и бутена наряду с выделением тепла образуются углекислый газ и водяной пар.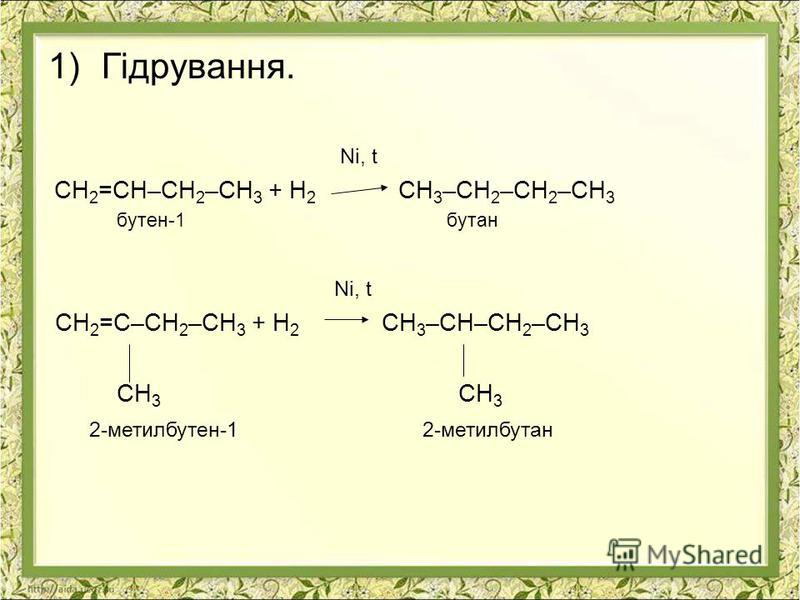 Но неполное сгорание будет производить окись углерода, а не двуокись углерода, и меньшее количество тепла, чем при полном сгорании. Основное различие между бутаном и бутеном заключается в том, что в молекулах бутана нет двойных связей, тогда как в молекулах бутена есть одна двойная связь.
Но неполное сгорание будет производить окись углерода, а не двуокись углерода, и меньшее количество тепла, чем при полном сгорании. Основное различие между бутаном и бутеном заключается в том, что в молекулах бутана нет двойных связей, тогда как в молекулах бутена есть одна двойная связь.
Ключевые области применения
1. Что такое бутан
– определение, свойства и применение
2. Что такое бутен
– Определение, свойства и приложения
3. Что такое Сходства между бутаном и бутеном
– Обзор общих черт
4. В чем разница между бутаном и бутеном
– Сравнение основных различий
Ключевые термины: бутан, бутен, горение, сырая нефть, углеводороды, нефть
Что такое бутан
Бутан – это углеводород, химическая формула C 4 H 10 .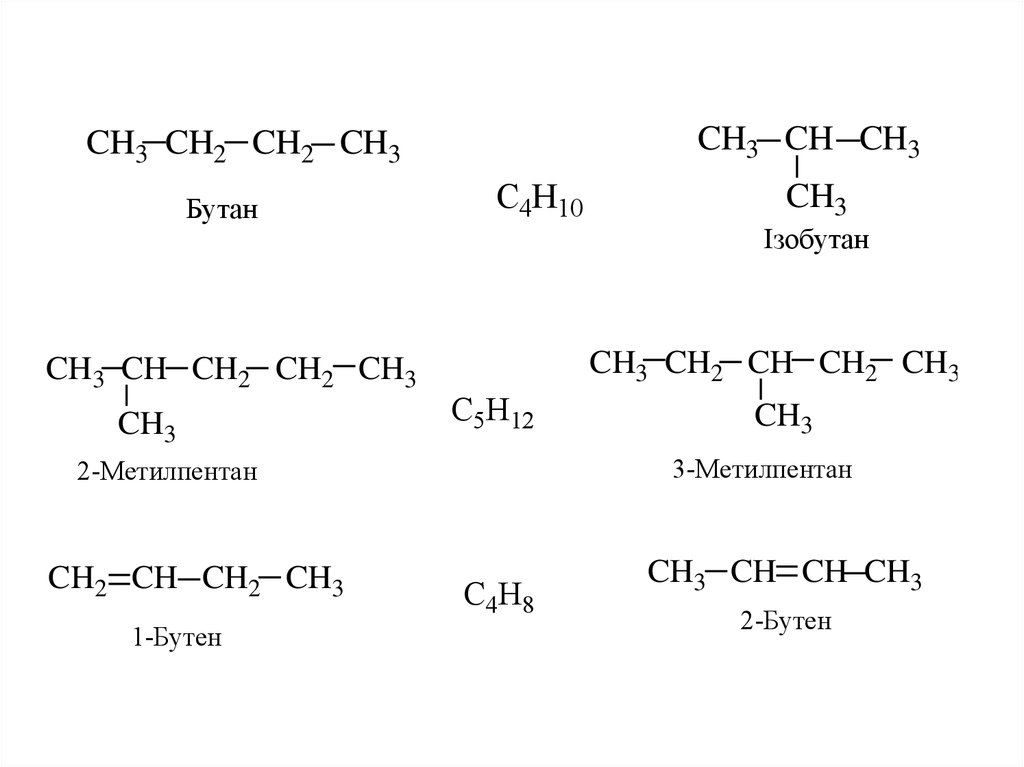 Это бесцветный газ при комнатной температуре и давлении. Молярная масса этого соединения составляет примерно 58,12 г/моль. Имеет запах бензина. Он относится к группе алканов, так как не имеет в своей структуре двойных связей. Бутан – неполярное соединение. Поэтому он не растворяется в полярных растворителях или воде. Молекулы бутана могут существовать в виде двух различных структурных изомеров. Это н-бутан и изобутан. н-бутан представляет собой линейную форму бутана с прямой цепью, тогда как изобутан представляет собой разветвленную структуру.
Это бесцветный газ при комнатной температуре и давлении. Молярная масса этого соединения составляет примерно 58,12 г/моль. Имеет запах бензина. Он относится к группе алканов, так как не имеет в своей структуре двойных связей. Бутан – неполярное соединение. Поэтому он не растворяется в полярных растворителях или воде. Молекулы бутана могут существовать в виде двух различных структурных изомеров. Это н-бутан и изобутан. н-бутан представляет собой линейную форму бутана с прямой цепью, тогда как изобутан представляет собой разветвленную структуру.
Рисунок 1: Структурные изомеры бутана
Бутан легко воспламеняется. Легко разжижается. Поскольку температура кипения бутана составляет около 1 o °С (или меньше), эта бутановая жидкость быстро испаряется при комнатной температуре. Когда в окружающей среде присутствует достаточное количество кислорода, бутан может полностью сгореть, образуя углекислый газ и водяной пар вместе с тепловой энергией. Но если кислорода недостаточно, то бутан будет подвергаться неполному сгоранию с образованием угарного газа и угольной пыли.
Бутан можно добавлять в бензин для ускорения испарения бензина. Это одно из основных применений бутана. Его также можно использовать в качестве растворителя для экстракции, поскольку бутан очень неполярен и менее реакционноспособен. Кроме того, бутан используется в качестве топлива в небольших установках.
Что такое бутен
Бутен – это углеводород с химической формулой C 4 H 8 . Это бесцветный газ при комнатной температуре и давлении. Имеет слегка ароматный запах. Бутен является алкеном. Основным источником бутена является сырая нефть. Бутен присутствует в сырой нефти в качестве второстепенного компонента. Бутен можно найти в нескольких изомерах. Однако бутен имеет одну двойную связь между двумя атомами углерода. Молярная масса бутена составляет около 56,11 г/моль.
Рисунок 2: Цис-транс-изомерия бутена
Изомерия бутена проявляется либо в виде структурной изомерии, либо в виде стереоизомерии. Положение двойной связи определяет структурную изомерию. 1-бутен имеет двойную связь на конце углеродной цепи, тогда как 2-бутен имеет двойную связь в середине углеродной цепи. Более того, изобутилен с разветвленной структурой является еще одним структурным изомером линейной молекулы бутена. Стереоизомерия возникает из-за различий в положении алкильных групп при аллильных атомах углерода. Это называется геометрической изомерией.
1-бутен имеет двойную связь на конце углеродной цепи, тогда как 2-бутен имеет двойную связь в середине углеродной цепи. Более того, изобутилен с разветвленной структурой является еще одним структурным изомером линейной молекулы бутена. Стереоизомерия возникает из-за различий в положении алкильных групп при аллильных атомах углерода. Это называется геометрической изомерией.
Бутен получают при переработке нефти. Производство бутена осуществляется путем реакции крекинга. Это расщепление углеводородов с длинной цепью на более мелкие молекулы углеводородов. Бутен является легковоспламеняющимся газом и может использоваться в качестве топлива. Бутен является важным мономером в производстве полимеров. Двойная связь, присутствующая в бутене, позволяет ему подвергаться полимеризации, которая в конечном итоге приводит к образованию молекулы полимера.
Сходства между бутаном и бутеном
- Бутан и бутен являются углеводородами.
- Это газы при комнатной температуре и давлении.

- Оба являются бесцветными газами.
- Бутан и бутен можно получить в процессе переработки нефти.
- Оба легко воспламеняются.
- Оба типа проявляют изомерию.
Разница между бутаном и бутеном
Определение
Бутан: Бутан представляет собой углеводород с химической формулой C 4 H 10 .
Бутен: Бутен представляет собой углеводород с химической формулой C 4 H 8 .
Химическая связь
Бутан: Бутан имеет только одинарные связи.
Бутен: Бутен имеет двойную связь, а также одинарную связь.
Классификация
Бутан: Бутан является алканом.
Бутен: Бутен представляет собой алкен.
Цис-транс-изомерия
Бутан: Бутан не проявляет цис-транс-изомерию.
Бутен: Бутен проявляет цис-транс-изомерию.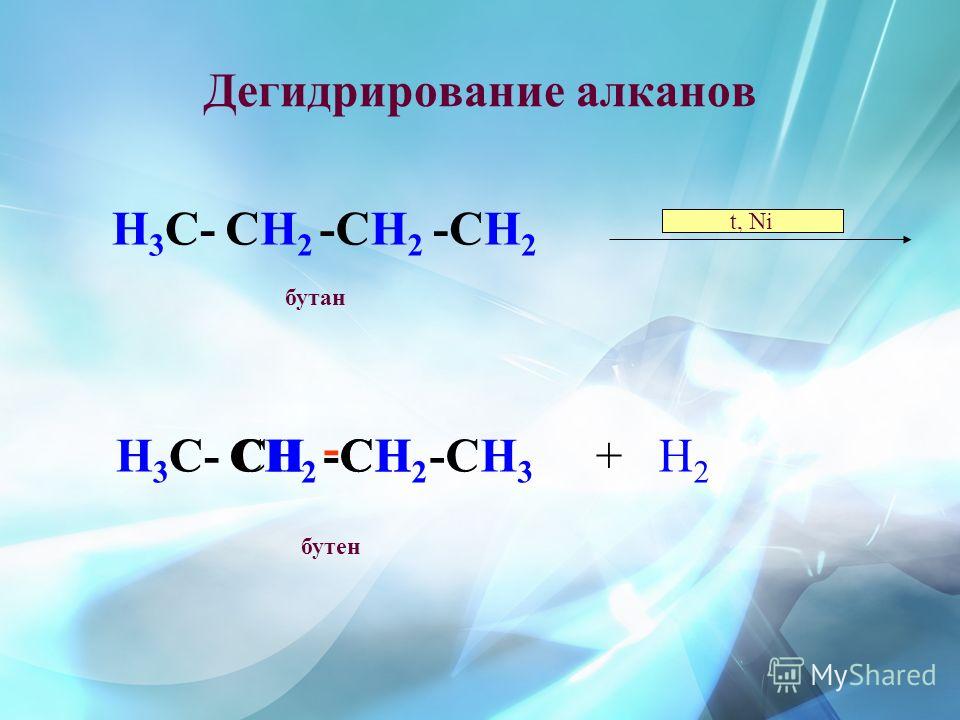
Молярная масса
Бутан: Молярная масса бутана составляет 58,12 г/моль.
Бутен: Молярная масса бутена составляет около 56,11 г/моль.
Заключение
Бутан и бутеновые газы могут использоваться в качестве топлива. Эти газы выделяют тепло при сгорании. Кроме того, бутан используется в качестве растворителя для экстракции из-за его неполярных свойств. Бутен является мономером для производства различных типов полимеров. Двойная связь, присутствующая в бутене, позволяет ему действовать как мономер. Основное различие между бутаном и бутеном заключается в том, что в молекулах бутана нет двойных связей, тогда как молекулы бутена имеют одну двойную связь.
Каталожные номера:
1. «Бутан». Британская энциклопедия, Encyclopædia Britannica, Inc., доступна здесь. По состоянию на 23 августа 2017 г.
2. «Бутен». Википедия, Фонд Викимедиа, 18 августа 2017 г., доступно здесь. По состоянию на 23 августа 2017 г.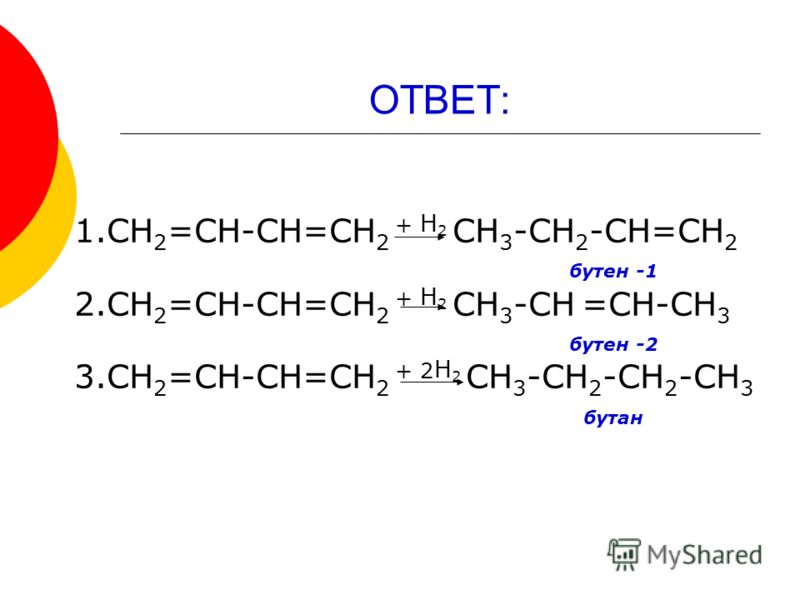




Leave A Comment