| Тест № 2 Тема «Ткани и органы» Вариант 1. 1. Ткань, состоящую из способных сокращаться многоядерных клеток, называют: 1) эпителиальная; 2) мышечная поперечнополосатая; 3) соединительная; 4) мышечная гладкая 2. Какая группа тканей обладает свойствами возбудимости и сократимости: 1) мышечная; 2) эпителиальная; 3) нервная; 4) соединительная. 3. В грудной полости у человека располагается: 1) желудок; 2) печень; 3) сердце; 4) поджелудочная железа. 4. Группа клеток организма, сходных по строению, выполняемым функциям, происхождению, называется: 1) органом; 2) тканью; 3) системой органов; 4) функциональной системой. 5. Сходство нервной и мышечной тканей – это: 1) сократимость; 2) проводимость; 3) возбудимость; 4) воспроизведение. 6. Структурной единицей нервной ткани является: 1) нейрон; 2) мышечное волокно; 3) лимфоцит; 4) лейкоцит. 7. Установите соответствие между характеристикой мышечной ткани и ее видом. ВИД ТКАНИ ХАРАКТЕРИСТИКА А) гладкая 1) образует средний слой кровеносных сосудов Б) поперечнополосатая 2) состоит из многоядерных клеток- волокон 3) образует скелетные мышцы 4) имеет поперечную исчерченность 5) сокращается медленно 8. Какая ткань изображена на рисунке? Опишите её. Тест № 2 Тема «Ткани и органы» Вариант 2. 1. Опорную функцию в организме человека выполняет ткань: 1) соединительная; 2) нервная; 3) эпителиальная; 4) мышечная. 2. Изменение диаметра кровеносных сосудов происходит за счет ткани: 1) эпителиальной; 2) соединительной; 3) гладкой мышечной; 4) поперечнополосатой мышечной. 3. Воздухоносные пути человека выстланы изнутри тканью: 1) соединительной; 2) мышечной поперечнополосатой; 3) эпителиальной; 4) мышечной гладкой. 4. Какая ткань составляет у человека основу мышц конечностей? 1) гладкая мышечная; 2) поперечнополосатая мышечная; 3) эпителиальная; 4) соединительная. 5. К выделительной системе органов относят: 1) кожу; 2) почки; 3) легкие; 4) слюнные железы. 6. Кровь, лимфа, хрящевая, костная, жировая ткани человека представляют разновидности ткани: 1) соединительной; 2) нервной; 3) мышечной; 4) эпителиальной. 7. Установите соответствие между функцией тканей и их типом: ТИП ФУНКЦИИ А. эпителиальная 1) ответная реакция организма на раздражение Б. соединительная 2) отложение питательных веществ В. нервная 3) передвижение веществ в организме 4) защита от механических повреждений 5) обеспечение обмена веществ между организмом и окружающей средой 8. Какая ткань изображена на рисунке? Опишите её. Ответы. Тема «Ткани и органы» Вариант 1
Вариант 2
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
Фамилия, имя: Вариант:
|
Возрастные изменения нервного аппарата сосудов головного и спинного мозга
Идентификация личности — одна из наиболее актуальных проблем судебной медицины. В последние годы в связи с участившимися случаями локальных вооруженных конфликтов, массовых катастроф и ростом неорганизованной миграции населения эта проблема становится особенно острой. При чрезвычайных происшествиях с массовыми человеческими жертвами обнаруживаются погибшие со значительными повреждениями тканей и органов, что затрудняет идентификацию личности. Поэтому при проведении экспертизы увеличивается диагностическое значение общих признаков (возраст, пол, рост, телосложение и др.). Например, определение возраста позволяет исключить тождество и решить вопрос о принадлежности останков одному или нескольким людям, а также ограничивает круг объектов, подлежащих дальнейшему сравнительному исследованию.
В последние годы в связи с участившимися случаями локальных вооруженных конфликтов, массовых катастроф и ростом неорганизованной миграции населения эта проблема становится особенно острой. При чрезвычайных происшествиях с массовыми человеческими жертвами обнаруживаются погибшие со значительными повреждениями тканей и органов, что затрудняет идентификацию личности. Поэтому при проведении экспертизы увеличивается диагностическое значение общих признаков (возраст, пол, рост, телосложение и др.). Например, определение возраста позволяет исключить тождество и решить вопрос о принадлежности останков одному или нескольким людям, а также ограничивает круг объектов, подлежащих дальнейшему сравнительному исследованию.
Основой для судебно-медицинского установления возраста является возрастная морфология — раздел антропологии, изучающий общие закономерности морфологических изменений тканей и органов в процессе онтогенеза. Для установления биологического возраста человека нами совместно с Ю.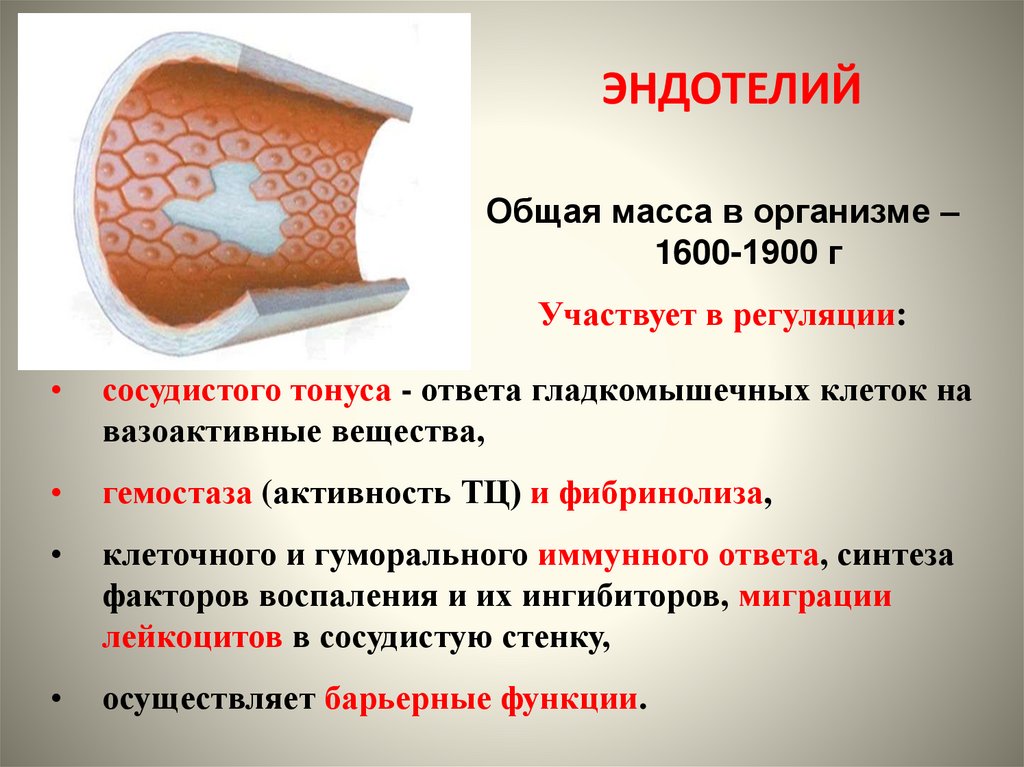
Пиальные и внутримозговые сосудистые системы головного и спинного мозга человека изучали в разные периоды постнатального онтогенеза (от 1 года до 90 лет). Гистологические исследования проводили методами Кампоса, Вейгерта—Паля, препараты окрашивали гематоксилином и эозином, по Ван-Гизону, Массону, 0,5% спиртовым раствором метиленового синего, а также с помощью инъекции сосудов раствором туши. Флюоресцентно-гистохимический метод с глиоксиловой кислотой использовали для идентификации адренергической иннервации, гистохимические методы Берта на холинацетилтрансферазу и Келле на ацетилхолинэстеразу — для выявления холинергической иннервации, на аспартатаминотранферазу — чувствительной иннервации. Методом Хоупа и Винсента в нервных сетях сосудов выявляли NADPH-диафоразу — элективный маркер NO-синтазы.
Артерии спинного мозга человека и животных сопровождаются чувствительными и двигательными волокнами, центры которых находятся в разных отделах нервной системы [1, 4—6]. Нервный аппарат кровеносных сосудов головного и спинного мозга представлен разнокалиберными нервными проводниками и полиморфными нервными окончаниями. Чувствительные нервные приборы имеют единый принцип организации и состоят из отводящего миелинового волокна, безмиелиновых арборизаций и полиморфных терминалей. Нервные сплетения представлены гетерогенными нервными волокнами трех размерных категорий: тонкими (до 3,9 мкм), средними (4,0—6,9 мкм) и толстыми (более 7 мкм).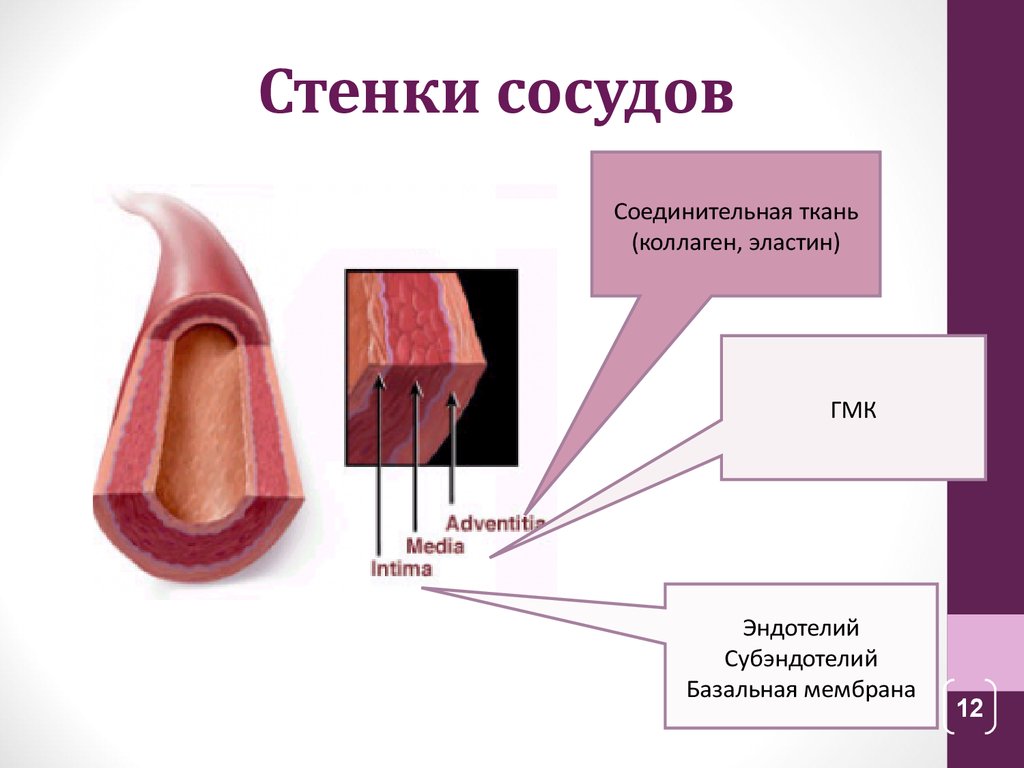
Результаты наших исследований подтверждают существующее представление о нейрохимической гетерогенности сосудистых нервных проводников. Значение холинергической иннервации оценивается в настоящее время однозначно: аксоны являются источниками ацетилхолина, который вызывает релаксацию артерий и вен. При большой плотности адренергических нервов роль их в регуляции мозговой гемодинамики все еще гипотетична. Предполагается, что обилие адренергических нервов поддерживает в стенках мозговых сосудов высокий тонус миоцитов, необходимый для защиты мозга от резких повышений системного кровяного давления.
В чувствительных волокнах кровеносных сосудов спинного мозга с большим постоянством гистохимическими методами выявляется аспартатаминотрансфераза, присутствие которой впервые обнаружено [1, 7] в сосудах головного мозга. Полученные данные не только представляют фактический материал для физиологических обобщений, но и открывают новые возможности идентификации чувствительных нервных элементов.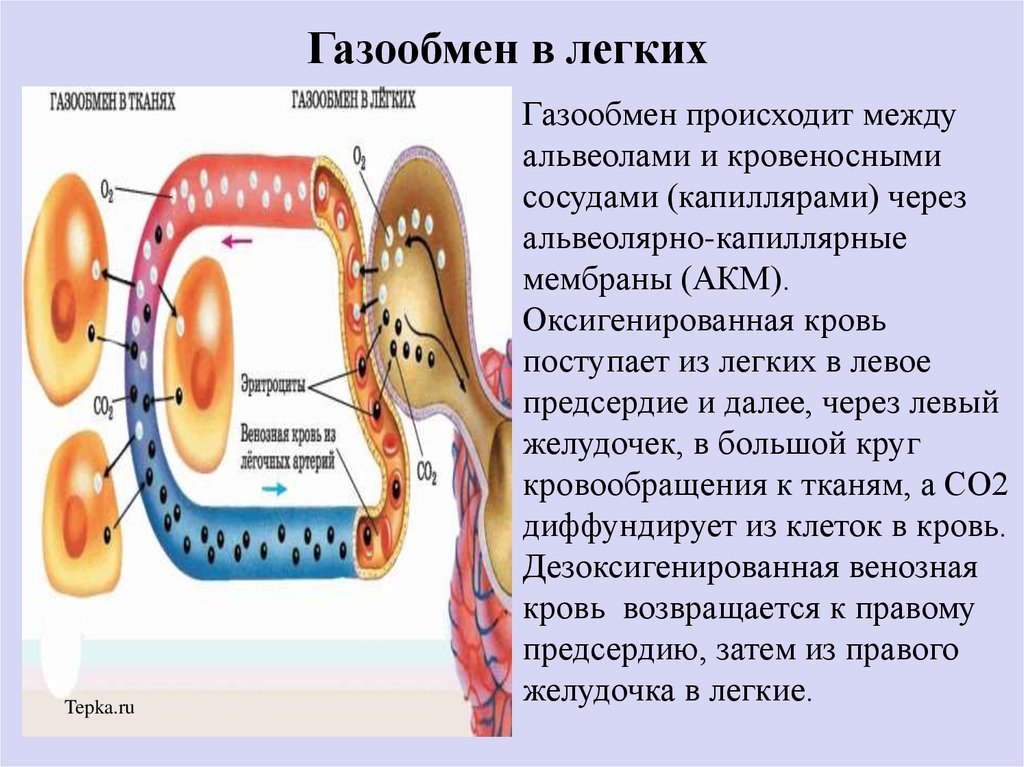
Концевые отделы чувствительных проводников, теряя миелиновую оболочку, образуют разные по форме и концентрации рецепторные разветвления. При характеристике чувствительных окончаний мы учитывали преимущественно структурные признаки терминальных разветвлений, их пространственную ориентацию и концентрацию [8—10].
Спинномозговые артерии, как и артерии мягкой оболочки мозга, сопровождаются эффекторными нервными волокнами, включающими холин- и адренергические аксоны. Долгое время считалось, что увеличение диаметра мозговых артерий осуществляется холинергическими нервами, влияние которых опосредуется ацетилхолином через мускариновые рецепторы мышечных клеток сосудов. Однако в последние годы дилататорную функцию холинергических нервов все чаще связывают с оксидом азота, который входит в состав недавно идентифицированной группы нейротрансмиттеров и дает выраженный сосудорасширяющий эффект [8, 11, 12]. Секреция оксида азота происходит при непременном участии ацетилхолина, который в кровеносных сосудах запускает всю нитроксидергическую систему.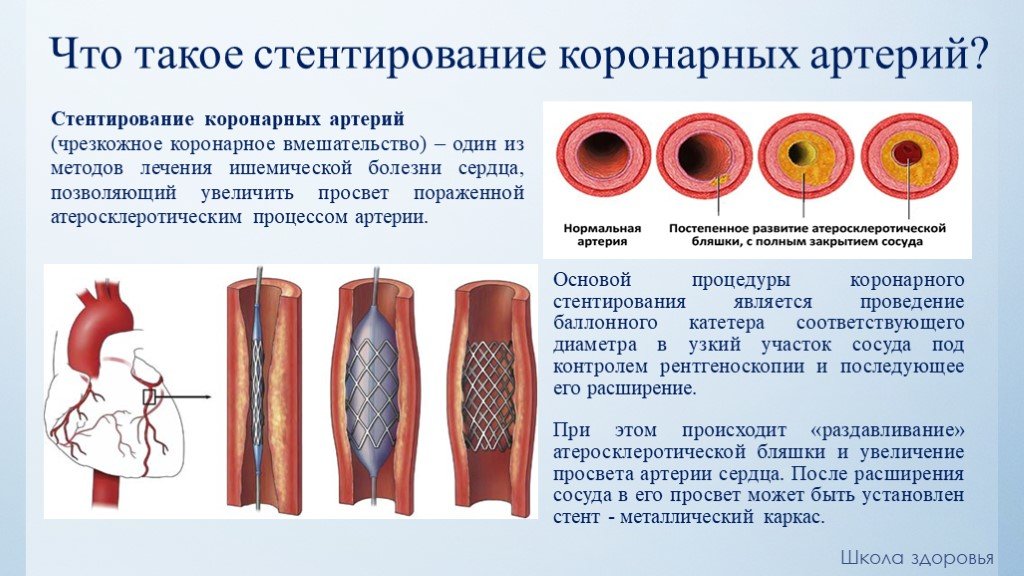
В сосудах спинного мозга, как и головного, уровень иннервированности существенно зависит от функциональной активности нейронов кровоснабжаемой области [3—5, 8, 12, 13]. Наиболее густые нервные сплетения свойственны артериям, расположенным в области утолщений спинного мозга.
Проведенные нами исследования показывают, что число варикозностей с уменьшением калибра артерий возрастает и имеет наиболее высокие значения на мелких пиальных и центральных артериях. Эти данные свидетельствуют о возрастании нервного контроля при уменьшении калибра артерий и объясняют высокую чувствительность мелких пиальных артерий к нервным стимулам. Установлено, что мелкие пиальные артерии имеют преимущественно холинергическую иннервацию, а внутримозговые сосуды — адренергическую [1, 3, 6, 14].
Установлено, что мелкие пиальные артерии имеют преимущественно холинергическую иннервацию, а внутримозговые сосуды — адренергическую [1, 3, 6, 14].
Ультраструктурная характеристика эфферентных нервных терминалей спинномозговых сосудов существенно не отличается от аналогичных структур мозговых артерий. В профилях аксонов соответственно местам локализации варикозных утолщений выявляются мелкие электронно-плотные, катехоламиносодержащие везикулы, мелкие агранулярные пузырьки, заполненные ацетилхолином, крупные гранулярные везикулы, содержащие, вероятно, нейропептиды. Нервные окончания располагаются от гладкомышечных клеток артерий на расстоянии не менее 60 нм, что свидетельствует о бессинаптическом характере нейромышечных соединений [5, 6, 11, 12, 15].
К клеткам, структурно и функционально связанным с кровеносными сосудами головного и спинного мозга, относят хромаффиноциты, меланоциты и мастоциты. В связи с наличием в цитоплазме материала, оформленного в виде гранул, их называют гранулоцитами, а за участие в обмене биогенных моноаминов — моноаминоцитами.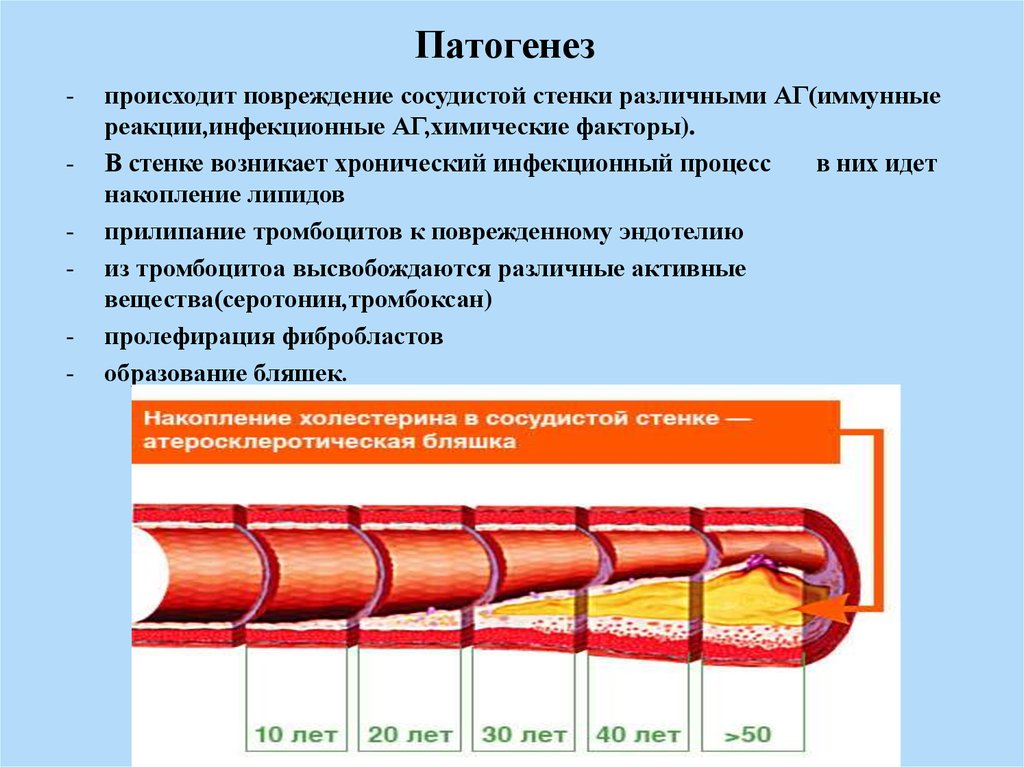
Изучение нервного аппарата артерий спинного мозга человека позволило установить, что афферентная и эфферентная иннервация существенно меняется в процессе онтогенеза [1, 4, 12, 13]. Морфологический субстрат иннервационных связей дифференцируется в значительной степени после рождения.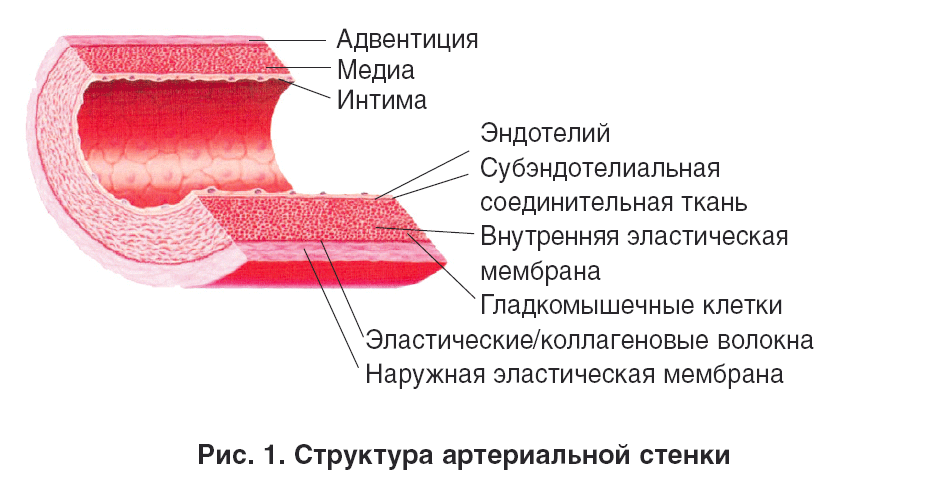
 Снижение плотности сплетений происходит за счет редукции числа толстых и средних проводников. У людей пожилого и старческого возраста отмечается ослабление чувствительности сердечно-сосудистой системы к нервным влияниям, что сопровождается прогрессированием инволютивных изменений после 65 лет. Мякотные волокна сосудов местами выглядят резко утолщенными, извитыми, гиперхромными. Увеличение диаметра нервов, вероятно, объясняется нарастанием массы соединительнотканной стромы. Сопутствующие сосудистые заболевания, в первую очередь атеросклероз и гипертоническая болезнь, оказывают существенное влияние на возрастные изменения нервных сплетений, выраженность которых зависит от тяжести и особенно продолжительности болезни [8, 9, 14, 15, 19].
Снижение плотности сплетений происходит за счет редукции числа толстых и средних проводников. У людей пожилого и старческого возраста отмечается ослабление чувствительности сердечно-сосудистой системы к нервным влияниям, что сопровождается прогрессированием инволютивных изменений после 65 лет. Мякотные волокна сосудов местами выглядят резко утолщенными, извитыми, гиперхромными. Увеличение диаметра нервов, вероятно, объясняется нарастанием массы соединительнотканной стромы. Сопутствующие сосудистые заболевания, в первую очередь атеросклероз и гипертоническая болезнь, оказывают существенное влияние на возрастные изменения нервных сплетений, выраженность которых зависит от тяжести и особенно продолжительности болезни [8, 9, 14, 15, 19].Период становления чувствительной иннервации как в пре-, так и в постнатальном онтогенезе сопровождается повышением доли компактных рецепторных форм, что является общей закономерностью развития афферентной иннервации сосудов ЦНС. Общими чертами, характерными для процесса старения, следует считать гетерогенность и гетерохронность. Инволютивные процессы больше касаются компактных разновидностей рецепторов, чем диффузных. Причиной тому служит возрастная инволюция преимущественно толстых миелиновых проводников, которые образуют эти чувствительные окончания. Таким образом, сосудистая рецепция в старости имеет преимущественно спинальную природу, о чем свидетельствует относительная интактность диффузных чувствительных форм [1, 4].
Инволютивные процессы больше касаются компактных разновидностей рецепторов, чем диффузных. Причиной тому служит возрастная инволюция преимущественно толстых миелиновых проводников, которые образуют эти чувствительные окончания. Таким образом, сосудистая рецепция в старости имеет преимущественно спинальную природу, о чем свидетельствует относительная интактность диффузных чувствительных форм [1, 4].
Развитие нервного аппарата артерий спинного мозга отражает процесс непрерывной дифференцировки симпатического ствола, становление которого сопровождается увеличением количества дефинитивных узлов. Становление нервных сплетений происходит благодаря формирующему действию двух механизмов: концентрации и дисперсии. Первый проявляется возрастанием толщины поверхностных нервных пучков, второй — многократным делением интраадвентициальных стволиков.
В первые дни после рождения увеличение плотности холинергических терминалей несколько снижается, что сопряжено, по-видимому, с усиленным ростом тел нервных клеток и дифференцировкой всей ткани нервных узлов.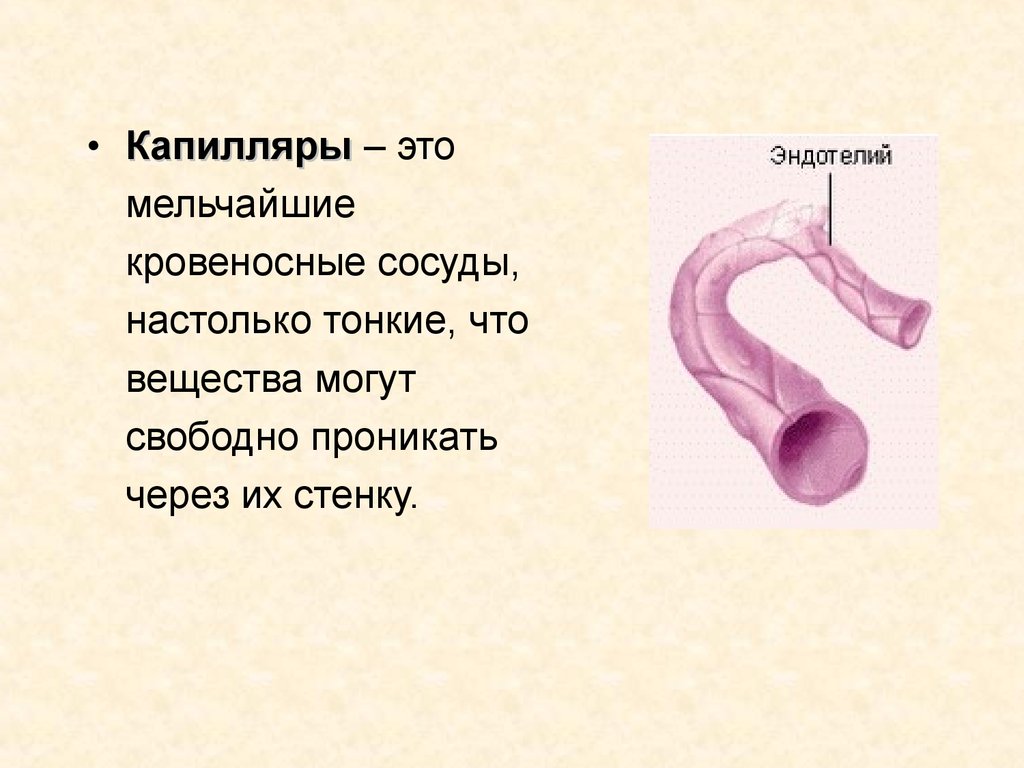 Снижение активности холинэстеразы в период постнатального развития свойственно всем нервным структурам. В дальнейшем увеличение объема холинергических нейронов, возрастание их способности синтезировать и накапливать ацетилхолин ведет к повышению уровня иннервированности спинномозговых сосудов в первые годы жизни. В период полового созревания (13—18 лет) концентрация адрен- и холинергических нервных волокон, активность медиаторов и ферментов достигают дефинитивного состояния и практически не меняются до 45 лет.
Снижение активности холинэстеразы в период постнатального развития свойственно всем нервным структурам. В дальнейшем увеличение объема холинергических нейронов, возрастание их способности синтезировать и накапливать ацетилхолин ведет к повышению уровня иннервированности спинномозговых сосудов в первые годы жизни. В период полового созревания (13—18 лет) концентрация адрен- и холинергических нервных волокон, активность медиаторов и ферментов достигают дефинитивного состояния и практически не меняются до 45 лет.
С возрастом отмечается ослабление нервных влияний на ткань, происходит редукция нервно-волокнистых структур, которой предшествует постепенное уменьшение в них запасов трансмиттеров и ферментов. Первые инволютивные изменения в нервных сплетениях артерий отмечаются в возрасте 45—54 лет, причиной чего могут служить дистрофические изменения в клетках симпатического ствола и в ганглиях блуждающего нерва. В процессе старения последовательно снижается интенсивность люминесценции нервных проводников, активность ферментов, концентрация варикозностей, что характерно для начала постмедиаторного периода онтогенеза вегетативной нервной системы [20, 21]. Изменения ярче выражены в адренергических сплетениях, чем в холинергических. Процесс денервации протекает интенсивнее в сосудах задней поверхности спинного мозга, чем в передних соименных артериях. Однако изменения в нервной системе при старении нельзя сводить только к инволютивным процессам, поскольку часть нервных волокон сохраняет типичную для зрелого возраста структуру. Число нервных волокон снижается параллельно содержанию катехоламинов и ферментов в нервных структурах сосудов [2, 17, 18].
Изменения ярче выражены в адренергических сплетениях, чем в холинергических. Процесс денервации протекает интенсивнее в сосудах задней поверхности спинного мозга, чем в передних соименных артериях. Однако изменения в нервной системе при старении нельзя сводить только к инволютивным процессам, поскольку часть нервных волокон сохраняет типичную для зрелого возраста структуру. Число нервных волокон снижается параллельно содержанию катехоламинов и ферментов в нервных структурах сосудов [2, 17, 18].
Гранулосодержащие клетки появляются в первые 2 мес эмбриогенеза, опережая в своем развитии адренергический нервный аппарат. На этом основании П.А. Мотавкин и соавт. [2, 6] приходят к выводу, что в раннем онтогенезе симпатический контроль мозгового кровообращения осуществляется эндокринными клетками адвентициальной оболочки, а в более позднем периоде эту роль принимает на себя адренергическая иннервация сосудов.
В первые дни после рождения ребенка хромаффиноциты в спинномозговых сосудах встречаются довольно редко и их содержание практически не меняется до старческого возраста.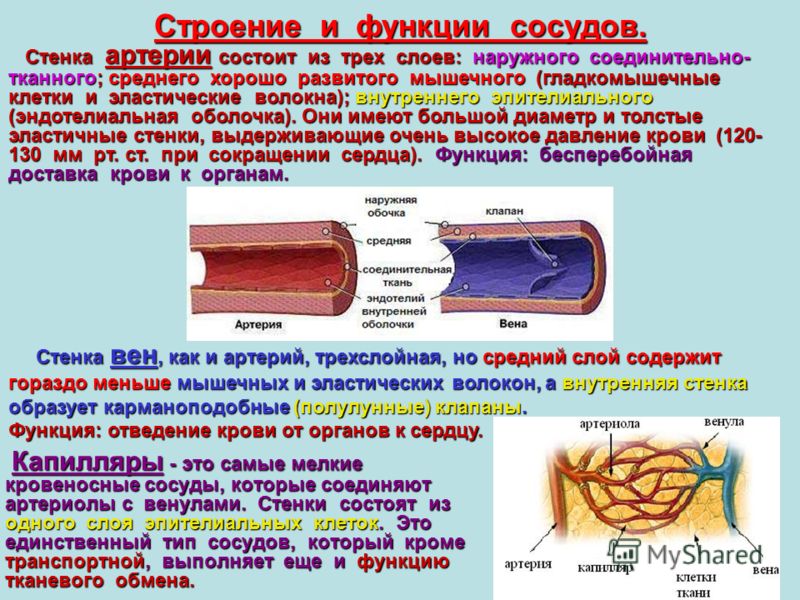 Концентрация тканевых базофилов прогрессивно возрастает от 8-й недели пренатального онтогенеза до 2—3 лет жизни. После некоторого спада следующий пик роста приходится на 13—17 лет, что можно объяснить адаптивными процессами, обусловленными половым созреванием. С 17-летнего возраста до старости концентрация тканевых базофилов практически не меняется. Концентрация меланоцитов после рождения несколько снижается и стабилизируется в период с 8 до 55 лет.
Концентрация тканевых базофилов прогрессивно возрастает от 8-й недели пренатального онтогенеза до 2—3 лет жизни. После некоторого спада следующий пик роста приходится на 13—17 лет, что можно объяснить адаптивными процессами, обусловленными половым созреванием. С 17-летнего возраста до старости концентрация тканевых базофилов практически не меняется. Концентрация меланоцитов после рождения несколько снижается и стабилизируется в период с 8 до 55 лет.
Инволютивные процессы в гранулосодержащих клетках начинаются значительно позже, чем в нервном аппарате кровеносных сосудов, что имеет свой биологический смысл. Функция сосудов, постепенно теряющих к старости свои прямые нервные связи, начинает регулироваться биологически активными веществами гранулосодержащих клеток. Так, тканевые базофилы могут играть роль элементов гуморальной системы, а гистамин может выступать в роли медиатора. В этой связи обращает на себя внимание увеличение числа тканевых базофилов в тканях некоторых органов у лиц пожилого возраста.
Флюорометрические исследования мягкой оболочки и артерий спинного мозга человека показывают, что на протяжении жизни у человека общее содержание биогенных моноаминов, соотношение различных типов и их качественные характеристики варьируют [1, 17]. Во 2-й половине пренатального онтогенеза в исследуемых образцах определяются адреналин, норадреналин, дофамин, серотонин и триптамин — все амины, свойственные зрелому человеку. Среди катехоламинов особенно велика доля дофамина. У детей качественные и количественные параметры биогенных моноаминов, установленные флюориметрически, не отличаются от аналогичных значений у взрослого человека. На протяжении длительного периода жизни (до 45 лет) содержание биогенных моноаминов в сосудах мягкой мозговой оболочки спинного мозга остается практически неизменным. Выборочные исследования, проведенные в старческом возрасте, позволили установить, что после 75 лет происходит снижение общего содержания аминов, среди которых обращает на себя внимание троекратное сокращение уровня норадреналина. Регрессивные изменения содержания норадреналина можно объяснить выраженной деструкцией адренергического нервного аппарата кровеносных сосудов в старости. Уровень других катехоламинов снижается более плавно из-за продолжающейся деятельности гранулосодержащих клеток.
Регрессивные изменения содержания норадреналина можно объяснить выраженной деструкцией адренергического нервного аппарата кровеносных сосудов в старости. Уровень других катехоламинов снижается более плавно из-за продолжающейся деятельности гранулосодержащих клеток.
Как показали наши исследования, в процессе онтогенеза различные механизмы регуляции дополняют и заменяют друг друга, обеспечивая адекватный кровоток, соответствующий метаболическим запросам вещества спинного мозга [1, 4, 6]. Период становления системы управления сопровождается сокращением популяции гранулосодержащих клеток и повышением значения вегетативной нервной системы. Неодновременное рекапитулятивное подключение разнородных подсистем в онтогенезе определяет гетерогенность и гетерохромность развития механизмов управления спинальной гемодинамикой, зависит от функциональной зрелости иннервируемого субстрата и способствует адаптивным перестройкам кровообращения, поддерживающим адекватный энергический баланс развивающихся тканей. Благодаря сдвигам, происходящим в процессе регулирования функций организма при старении, не только развиваются признаки угасания, но и появляются новые приспособительные механизмы, поддерживающие определенный гомеостатический уровень. В старости, когда происходит деструкция адренергического нервного аппарата сосудов, его функцию, точно так же, как и в раннем эмбриогенезе, принимают на себя хромаффиноциты, тканевые базофилы и меланоциты, которые, как уже отмечалось, обладают способностью накапливать и выделять биогенные моноамины. Если у взрослого человека они дополняют и пролонгируют эффект нервного импульса, то в эмбриональном периоде и в старости являются главным источником биогенных моноаминов. Анализ полученных результатов позволяет заключить, что возрастная перестройка нервного и местного нейроэндокринного аппарата артерий осуществляется на основе принципа кооперирования.
Благодаря сдвигам, происходящим в процессе регулирования функций организма при старении, не только развиваются признаки угасания, но и появляются новые приспособительные механизмы, поддерживающие определенный гомеостатический уровень. В старости, когда происходит деструкция адренергического нервного аппарата сосудов, его функцию, точно так же, как и в раннем эмбриогенезе, принимают на себя хромаффиноциты, тканевые базофилы и меланоциты, которые, как уже отмечалось, обладают способностью накапливать и выделять биогенные моноамины. Если у взрослого человека они дополняют и пролонгируют эффект нервного импульса, то в эмбриональном периоде и в старости являются главным источником биогенных моноаминов. Анализ полученных результатов позволяет заключить, что возрастная перестройка нервного и местного нейроэндокринного аппарата артерий осуществляется на основе принципа кооперирования.
Полученные данные о возрастных перестройках нервного аппарата спинномозговых артерий имеют не только теоретическое значение, но и могут быть использованы для решения вопросов судебно-медицинской практики. Как мы уже отмечали, прогрессивное повышение концентрации холинергических нервных волокон на спинномозговых артериях в период дифференцировки нервных сплетений дает основание использовать их морфометрические параметры для установления возраста ребенка. Был составлен эмпирический ряд зависимости между возрастом ребенка и количеством холинергических нервных волокон на передней спинальной артерии в верхнем бассейне спинного мозга. Математическая обработка полученных данных позволила вывести следующую формулу: у = 0,41х — 12,04, где у — возраст ребенка, х — концентрация холинергических нервных волокон на передней спинальной артерии. Этот способ позволяет определить возраст до 16 лет. Ошибка при определении возраста составляет ± 1 год при уровне надежности 95%.
Как мы уже отмечали, прогрессивное повышение концентрации холинергических нервных волокон на спинномозговых артериях в период дифференцировки нервных сплетений дает основание использовать их морфометрические параметры для установления возраста ребенка. Был составлен эмпирический ряд зависимости между возрастом ребенка и количеством холинергических нервных волокон на передней спинальной артерии в верхнем бассейне спинного мозга. Математическая обработка полученных данных позволила вывести следующую формулу: у = 0,41х — 12,04, где у — возраст ребенка, х — концентрация холинергических нервных волокон на передней спинальной артерии. Этот способ позволяет определить возраст до 16 лет. Ошибка при определении возраста составляет ± 1 год при уровне надежности 95%.
Таким образом, внедрение в экспертную практику современных достижений фундаментальных исследований способствует объективизации судебно-медицинских критериев определения возраста человека.
Анатомия, кровеносные сосуды — StatPearls
Уильям Д. Такер; Йингёт Арора; Кунал Махаджан.
Такер; Йингёт Арора; Кунал Махаджан.
Информация об авторе и организациях
Последнее обновление: 8 августа 2022 г.
Введение
Периферическая сосудистая система (PVS) включает все кровеносные сосуды, существующие вне сердца. Периферическая сосудистая система классифицируется следующим образом: Аорта и ее ветви:
Функция и структура каждого сегмента периферической сосудистой системы различаются в зависимости от органа, который он снабжает кровью. Помимо капилляров, все кровеносные сосуды состоят из трех слоев:
Адвентиция или внешний слой, обеспечивающий структурную поддержку и форму сосуда
Средняя оболочка или средний слой, состоящий из эластичной и мышечной ткани, который регулирует внутренний диаметр сосуда
Интима оболочки или внутренний слой, состоящий из эндотелиальной выстилки, которая обеспечивает путь движения крови без трения
Внутри каждого слоя количество мышечных и коллагеновых фибрилл варьируется в зависимости от размера и расположения сосуда.
Артерии
Артерии играют важную роль в снабжении органов кровью и питательными веществами. Артерии всегда находятся под высоким давлением. Чтобы справиться с этим стрессом, у них много эластичной ткани и меньше гладкой мускулатуры. Наличие эластина в крупных кровеносных сосудах позволяет этим сосудам увеличиваться в размерах и изменять свой диаметр. Когда артерия достигает определенного органа, она подвергается дальнейшему разделению на более мелкие сосуды, в которых больше гладкой мускулатуры и меньше эластичной ткани. По мере уменьшения диаметра кровеносных сосудов скорость кровотока также уменьшается. По оценкам, в артериальной системе содержится от 10% до 15% от общего объема крови. Эта особенность высокого системного давления и низкого объема типична для артериальной системы.
В организме есть два основных типа артерий: (1) эластичные артерии и (2) мышечные артерии. Мышечные артерии включают артерии с анатомическими названиями, такие как, например, плечевая артерия, лучевая артерия и бедренная артерия.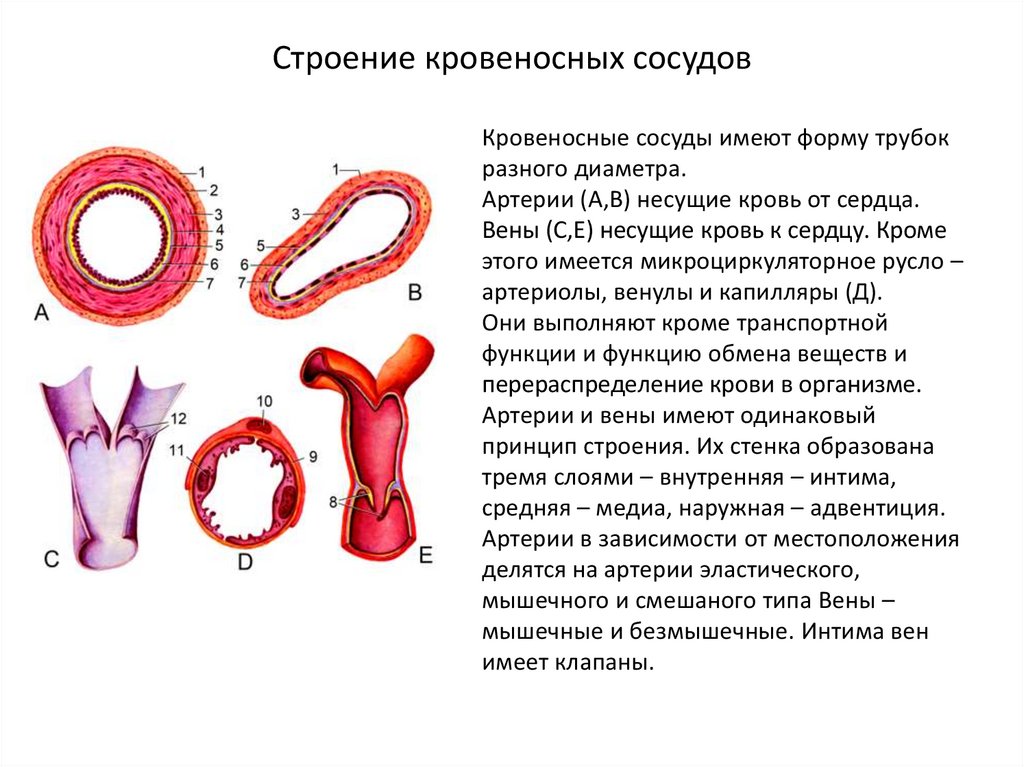 Мышечные артерии содержат больше гладкомышечных клеток в среднем слое, чем эластические артерии. Эластические артерии – это ближайшие к сердцу артерии (аорта и легочные артерии), которые содержат гораздо больше эластической ткани в средней оболочке, чем мышечные артерии. Эта особенность эластичных артерий позволяет им поддерживать относительно постоянный градиент давления, несмотря на постоянную насосную деятельность сердца.
Мышечные артерии содержат больше гладкомышечных клеток в среднем слое, чем эластические артерии. Эластические артерии – это ближайшие к сердцу артерии (аорта и легочные артерии), которые содержат гораздо больше эластической ткани в средней оболочке, чем мышечные артерии. Эта особенность эластичных артерий позволяет им поддерживать относительно постоянный градиент давления, несмотря на постоянную насосную деятельность сердца.
Артериолы
Артериолы снабжают кровью органы и состоят в основном из гладких мышц. Вегетативная нервная система влияет на диаметр и форму артериол. Они реагируют на потребность тканей в большем количестве питательных веществ/кислорода. Артериолы играют значительную роль в системном сосудистом сопротивлении из-за отсутствия в стенках значительного количества эластической ткани.
Размер артериол варьируется от 8 до 60 микрометров. Артериолы далее подразделяются на метаартериолы.
Капилляры
Капилляры представляют собой тонкостенные сосуды, состоящие из одного эндотелиального слоя.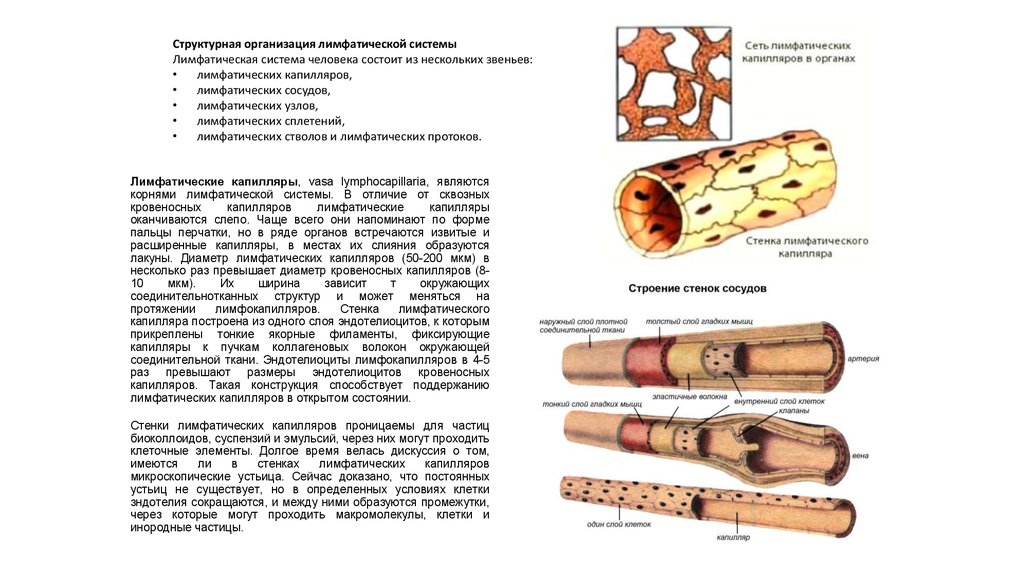 Из-за тонких стенок капилляра обмен питательными веществами и метаболитами происходит преимущественно путем диффузии. Просвет артериол регулирует ток крови по капиллярам.
Из-за тонких стенок капилляра обмен питательными веществами и метаболитами происходит преимущественно путем диффузии. Просвет артериол регулирует ток крови по капиллярам.
Венулы
Венулы – самые маленькие вены, в которые поступает кровь из капилляров. Они также играют роль в обмене кислорода и питательных веществ на водные продукты. Между капиллярами и венулами расположены посткапиллярные сфинктеры. Венула очень тонкостенная и легко подвержена разрыву при чрезмерном объеме.
Вены
Кровь течет из венул в более крупные вены. Как и в артериальной системе, стенки вен состоят из трех слоев. Но в отличие от артерий, венозное давление низкое. Вены тонкостенные и менее эластичные. Эта функция позволяет венам удерживать очень высокий процент циркулирующей крови. Венозная система может вмещать большой объем крови при относительно низком давлении, что называется высокой емкостью. В любой момент времени почти три четверти объема циркулирующей крови содержится в венозной системе.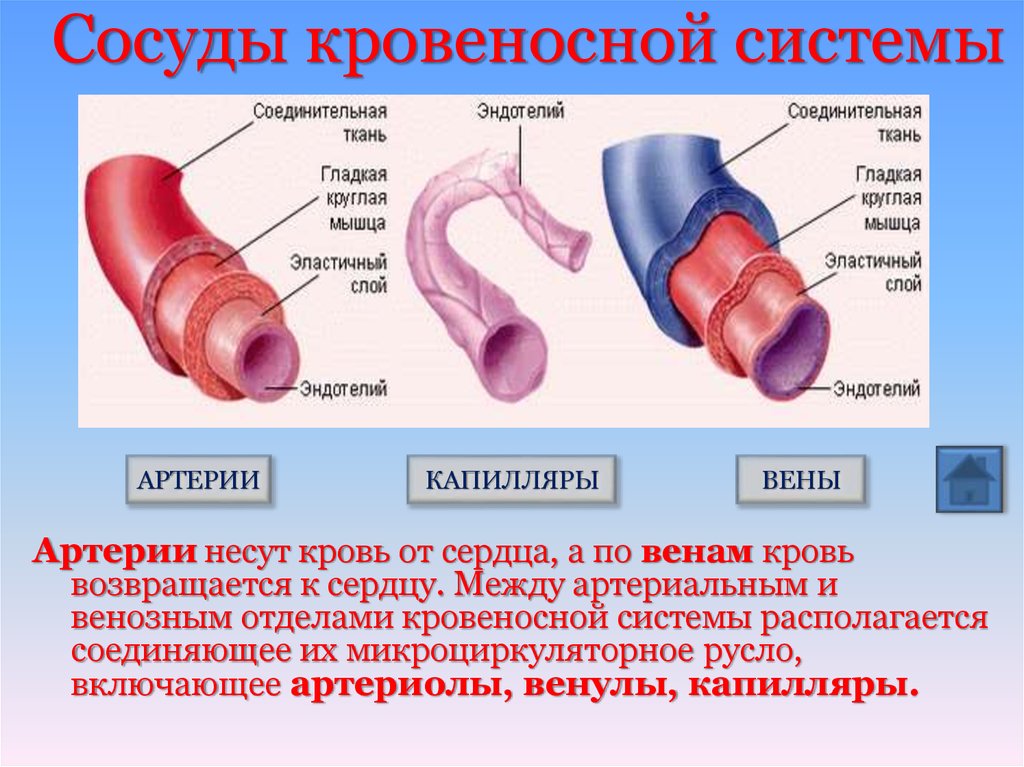 Внутри вен также можно найти односторонние клапаны, которые позволяют крови течь к сердцу в прямом направлении. Сокращения мышц помогают кровотоку в венах ног. На прямой кровоток от нижних конечностей к сердцу также влияют дыхательные изменения, влияющие на градиенты давления в брюшной полости и грудной полости. Этот перепад давления является самым высоким во время глубокого вдоха, но небольшой перепад давления наблюдается в течение всего дыхательного цикла.
Внутри вен также можно найти односторонние клапаны, которые позволяют крови течь к сердцу в прямом направлении. Сокращения мышц помогают кровотоку в венах ног. На прямой кровоток от нижних конечностей к сердцу также влияют дыхательные изменения, влияющие на градиенты давления в брюшной полости и грудной полости. Этот перепад давления является самым высоким во время глубокого вдоха, но небольшой перепад давления наблюдается в течение всего дыхательного цикла.
Структура и функция
Сосуды транспортируют питательные вещества к органам/тканям и транспортируют отходы от органов/тканей в кровь. Основной целью и важной ролью сосудистой системы является ее участие в насыщении организма кислородом.[1] Дезоксигенированная кровь из периферических вен транспортируется обратно к сердцу из капилляров в венулы, в вены, в правые отделы сердца, а затем в легкие. Насыщенная кислородом кровь из легких транспортируется в левую часть сердца в аорту, затем в артерии, артериолы и, наконец, в капилляры, где происходит обмен питательными веществами.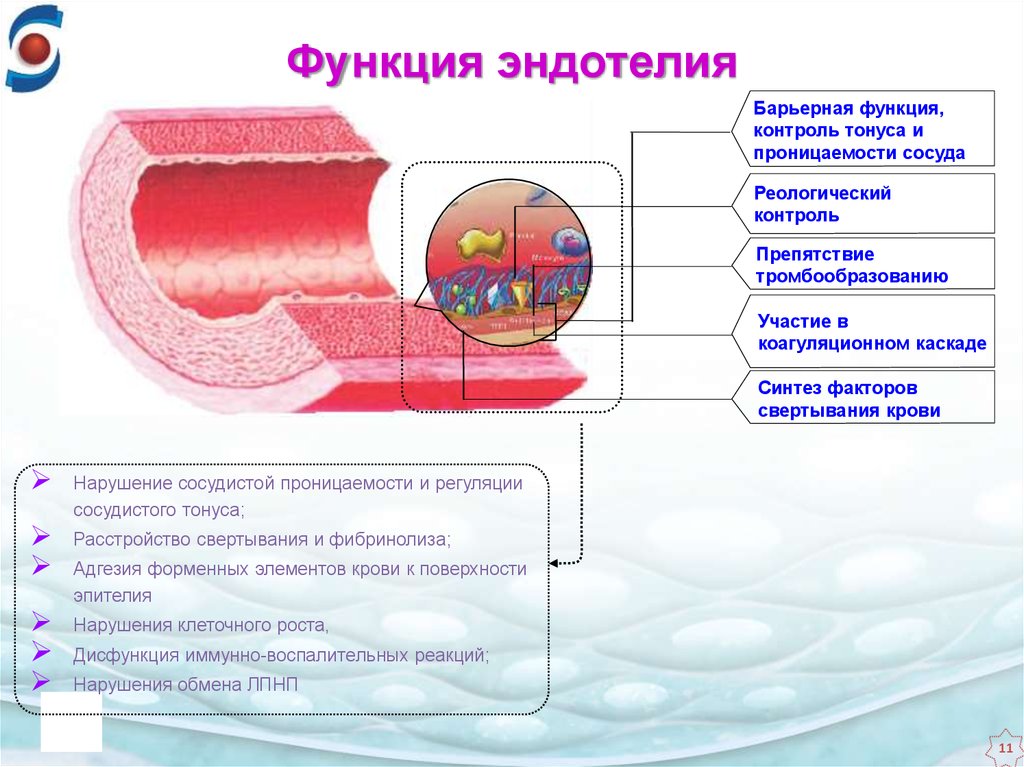 Загрузка и выгрузка кислорода и питательных веществ происходят в основном в капиллярах.
Загрузка и выгрузка кислорода и питательных веществ происходят в основном в капиллярах.
Эмбриология
Кровеносные сосуды возникают из мезодермального зародышевого слоя. Эмбриональное развитие сосудов и сердца начинается в середине третьей недели жизни. Кровообращение плода через эту сосудистую систему начинается примерно на восьмой неделе развития.
Образование кровеносных сосудов происходит посредством двух основных механизмов: (1) васкулогенеза и (2) ангиогенеза.
Васкулогенез — это процесс образования кровеносных сосудов у эмбриона. Взаимодействия между клетками-предшественниками и различными факторами роста управляют клеточной дифференцировкой, наблюдаемой при васкулогенезе[2]. Мезодермальные клетки-предшественники и их рецепторы реагируют на FGF2, превращаясь в гемангиобласты. Затем рецепторы гемангиобластов реагируют на VEGF, вызывая дальнейшую дифференцировку в эндотелиальные клетки.[3] Затем эти эндотелиальные клетки сливаются, образуя первые полые кровеносные сосуды. К первым кровеносным сосудам, образованным в результате васкулогенеза, относятся дорсальная аорта и кардинальные вены.
К первым кровеносным сосудам, образованным в результате васкулогенеза, относятся дорсальная аорта и кардинальные вены.
Все другие сосуды в организме человека образуются в результате ангиогенеза. Ангиогенез — это процесс, при котором новые кровеносные сосуды образуются из эндотелиального слоя ранее существовавшего сосуда. Взаимодействия с участием VEGF управляют ангиогенезом. Этот процесс является преобладающей формой неоваскуляризации у взрослых.
Кровоснабжение и лимфатическая система
Стенки крупных кровеносных сосудов, таких как аорта и полая вена, снабжаются кровью vasa vasorum. Этот термин переводится как «сосуд сосуда».
Существуют три типа vasa vasorum (1) vasa vasorum internae, (2) vasa vasorum externae и (3) венозные vasa vasorae. Vasa vasorum internae берут начало из просвета сосуда и проникают через стенку сосуда, снабжая кислородом и питательными веществами. Vasa vasorum externae отходят от близлежащего разветвляющегося сосуда и возвращаются в более крупную стенку сосуда[4].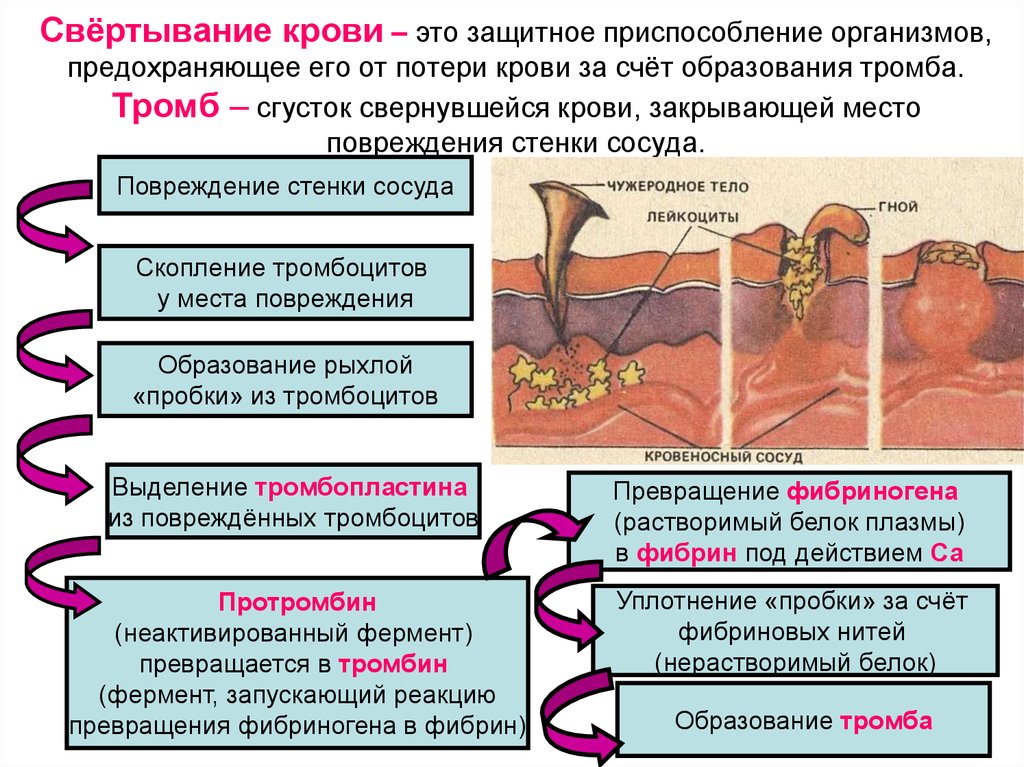 Некоторые инфекции, такие как поздние проявления третичного сифилиса, могут привести к эндартерииту vasa vasorum восходящей аорты.[5] Венозные vasa vasorae берут начало в стенке сосуда и впадают в близлежащую вену, обеспечивая венозный отток стенок сосуда.
Некоторые инфекции, такие как поздние проявления третичного сифилиса, могут привести к эндартерииту vasa vasorum восходящей аорты.[5] Венозные vasa vasorae берут начало в стенке сосуда и впадают в близлежащую вену, обеспечивая венозный отток стенок сосуда.
Нервы
Симпатическая нервная система в первую очередь иннервирует кровеносные сосуды. Гладкие мышцы сосудов содержат рецепторы альфа-1, альфа-2 и бета-2.[6] Тонкий баланс между влиянием симпатической и парасимпатической нервной системы отвечает за лежащий в основе физиологический тонус сосудов. Специализированные рецепторы, расположенные в дуге аорты и сонных артериях, получают информацию о кровяном давлении (барорецепторы) и содержании кислорода (хеморецепторы) из проходящей крови. Затем эта информация передается ядру одиночного пути через блуждающий нерв.[7] Затем наступает сужение или расслабление кровеносных сосудов, что определяется симпатической реакцией организма.
Мышцы
Кровеносные сосуды содержат только гладкомышечные клетки. Эти мышечные клетки находятся в средней оболочке вместе с эластическими волокнами и соединительной тканью. Хотя сосуды содержат только гладкие мышцы, сокращение скелетных мышц играет важную роль в движении крови от периферии к сердцу по венозной системе.
Эти мышечные клетки находятся в средней оболочке вместе с эластическими волокнами и соединительной тканью. Хотя сосуды содержат только гладкие мышцы, сокращение скелетных мышц играет важную роль в движении крови от периферии к сердцу по венозной системе.
Хирургические аспекты
Повреждение многих кровеносных сосудов может иметь потенциально серьезные последствия. Правило успешной операции заключается в том, что операционное поле должно иметь как адекватное артериальное кровоснабжение, так и адекватный венозный отток. Отсутствие любого из них приведет к субоптимальным результатам и осложнениям для пациента. Особое внимание следует уделить тому, чтобы избежать повреждения более крупных сосудов (НПВ, аорты и т. д.) и любых сосудов, особенно уязвимых во время определенных хирургических процедур [8].
Клиническое значение
Повреждение или заболевание кровеносных сосудов вызывает различные заболевания, включая гипертонию, образование аневризмы, разрыв аневризмы, заболевание периферических сосудов, тромбоз глубоких вен, легочную эмболию, транзиторную ишемическую атаку, инсульт и многие другие. Некоторые заболевания напрямую связаны с врожденным заболеванием сосудов, в то время как другие являются побочными эффектами заболевания сосудов.[9][10] Клинически заболевание сосудов представляет собой серьезную проблему. CDC приписывает 1 миллиард долларов в день затратам на сердечно-сосудистые заболевания и инсульт в Соединенных Штатах.
Некоторые заболевания напрямую связаны с врожденным заболеванием сосудов, в то время как другие являются побочными эффектами заболевания сосудов.[9][10] Клинически заболевание сосудов представляет собой серьезную проблему. CDC приписывает 1 миллиард долларов в день затратам на сердечно-сосудистые заболевания и инсульт в Соединенных Штатах.
Контрольные вопросы
Доступ к бесплатным вопросам с несколькими вариантами ответов по этой теме.
Комментарий к этой статье.
Рисунок
Оболочки глаза. Схема кровеносных сосудов глаза в горизонтальном разрезе. Внесите вклад Grey’s Anatomy Plates
Рисунок
Общий кожный покров. Распределение кровеносных сосудов в коже подошвы стопы. Предоставлено Grey’s Anatomy Plates
Ссылки
- 1.
Алкадхим М., Зоккали С., Аббасифард С., Авила М.Дж., Патель А.С., Саттаров К., Уолтер С.М., Баай А.А. Хирургическая сосудистая анатомия минимально инвазивного латерального поясничного межтелового доступа: трупный и рентгенографический анализ.
 Eur Spine J. 2015 Nov; 24 Suppl 7: 906-11. [PubMed: 26487472]
Eur Spine J. 2015 Nov; 24 Suppl 7: 906-11. [PubMed: 26487472]- 2.
Рейес М., Дудек А., Джахагирдар Б., Куди Л., Маркер П.Х., Верфейли К.М. Исправление: Происхождение эндотелиальных предшественников в постнатальном костном мозге человека. Джей Клин Инвест. 2008 ноябрь; 118 (11): 3813. [Бесплатная статья PMC: PMC2575714] [PubMed: 27809420]
- 3.
Takahashi T, Takase Y, Yoshino T, Saito D, Tadokoro R, Takahashi Y. Ангиогенез в развивающемся спинном мозге: исключение кровеносных сосудов из области нервных предшественников опосредовано VEGF и его антагонистами. ПЛОС Один. 2015;10(1):e0116119. [Бесплатная статья PMC: PMC4293145] [PubMed: 25585380]
- 4.
Гессл М., Росол М., Маляр Н.М., Фитцпатрик Л.А., Бейли П.Е., Замир М., Ритман Э.Л. Функциональная анатомия и гемодинамические характеристики vasa vasorum в стенках коронарных артерий свиней. Anat Rec A Discov Mol Cell Evol Biol. 2003 г., июнь; 272 (2): 526-37.
 [В паблике: 12740947]
[В паблике: 12740947]- 5.
Paulo N, Cascarejo J, Vouga L. Сифилитическая аневризма восходящей аорты. Interact Cardiovasc Thorac Surg. 2012 Февраль; 14 (2): 223-5. [Бесплатная статья PMC: PMC3279976] [PubMed: 22159251]
- 6.
Sheng Y, Zhu L. Взаимодействие между вегетативной нервной системой и кровеносными сосудами. Int J Physiol Pathophysiol Pharmacol. 2018;10(1):17-28. [Бесплатная статья PMC: PMC5871626] [PubMed: 29593847]
- 7.
Мацусима Т., Кацута Т., Йошиока Ф. [Анатомия яремного отверстия и подъязычного канала]. Нихон Джибиинкока Гаккай Кайхо. 2015 Январь; 118(1):14-24. [В паблике: 26506628]
- 8.
Andall RG, Matusz P, du Plessis M, Ward R, Tubbs RS, Loukas M. Клиническая анатомия вариантов пузырной артерии: обзор более 9800 случаев. Сур Радиол Анат. 2016 июль; 38 (5): 529-39. [PubMed: 26698600]
- 9.
Аггарвал С., Камар А., Шарма В., Шарма А. Аневризма брюшной аорты: всесторонний обзор.
 Опыт Клин Кардиол. 2011 Весна;16(1):11-5. [Бесплатная статья PMC: PMC3076160] [PubMed: 21523201]
Опыт Клин Кардиол. 2011 Весна;16(1):11-5. [Бесплатная статья PMC: PMC3076160] [PubMed: 21523201]- 10.
Кандория А., Неги П., Махаджан К., Пури С. Миксома левого предсердия, осложненная острой эмболией в левую подключичную артерию. BMJ Case Rep. 2016 11 июля 2016 г. [бесплатная статья PMC: PMC4956981] [PubMed: 27402653]
Кровеносные сосуды | Encyclopedia.com
Определение
Кровь Сосуды составляют непрерывную систему каналов, по которым кровь переносит кислород и питательные вещества ко всем тканям тела и отходы из них.
Описание
Структура
Все кровеносные сосуды (кроме капилляров) имеют сходную трехслойную структуру. Самый внутренний слой, называемый интимной оболочкой, состоит из монослоя эндотелиальных клеток, называемого эндотелием. Интимная оболочка помогает ограничить поступление веществ в стенку сосуда, контролировать диаметр кровеносных сосудов, регулировать коагуляцию. Полый центр кровеносного сосуда называется просветом и представляет собой пространство, через которое течет кровь.
Средний слой называется средней оболочкой и отделен от интимной оболочки оболочкой из высокоэластичного материала, называемой внутренней эластичной пластинкой. Средняя оболочка состоит из кругового расположения гладкомышечных клеток, коллагена и эластических волокон; он составляет основную часть стенки большинства артерий, но в венах он тоньше и содержит меньше гладкомышечных клеток. Гладкие мышцы содержат сократительные элементы, отвечающие за сокращение (вазоконстрикцию) и расслабление (вазодилатацию). Таким образом, tunica media придает прочность, эластичность и сократительную способность стенке сосуда.
Среднюю оболочку окружает адвентициальная оболочка (два слоя разделены внешней эластичной пластинкой). Этот внешний слой содержит матрицу из коллагеновых и эластических волокон, которые поддерживают фибробласты (клетки, секретирующие волокнистые белки , коллаген и эластин ), нервы и vasa vasorum (мелкие кровеносные сосуды, которые снабжают стенки крупных артерий и вен кислородом и питательными веществами). ).
).
Артерии и артериолы
Артерии – это кровеносные сосуды, несущие кровь от сердце. Артериальная кровь богата кислородом, за исключением крови, переносимой легочной артерией от сердца к легким для насыщения кислородом. Аорта является самой крупной артерией в организме человека и берет начало в левом желудочке сердца. Этот сосуд и его основные ветви (общая сонная, общая подвздошная, подключичная и плечеголовная артерии) называются артериями эластического типа, поскольку они расширяются и сужаются в ответ на пульсирующий поток крови и изменение объема крови.
Эластичные артерии разветвляются, чтобы стать мышечными артериями, сосудами с толстыми стенками, которые транспортируют кровь к определенным органам. Мышечные артерии дают сосуды сопротивления; к ним относятся мелкие артерии и артериолы. По мере того, как артерии становятся меньше, их стенки становятся тоньше и состоят из меньшего количества коллагена и эластина. Стенки мелких артерий состоят из нескольких слоев гладкомышечных клеток, а артериол — из одного или двух.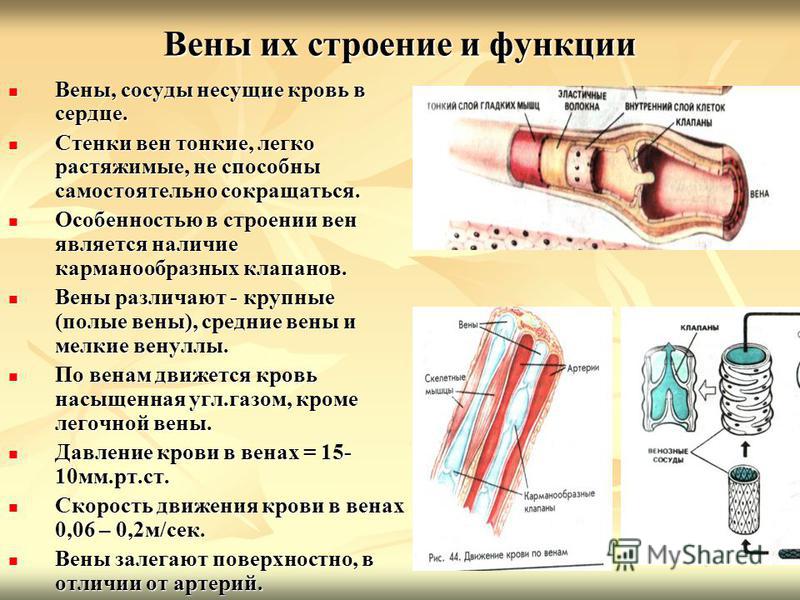 Таким образом, сосуды сопротивления менее эластичны, но более активно регулируют приток крови в капиллярное русло.
Таким образом, сосуды сопротивления менее эластичны, но более активно регулируют приток крови в капиллярное русло.
Анастомозы образуются в месте слияния артерий и артериол, образуя альтернативные каналы доставки крови. Они обеспечивают коллатеральное кровообращение в случае окклюзии (закупорки) артерии.
Обменные сосуды
Обменные сосуды включают капилляры и посткапиллярные венулы. Стенки капилляров состоят только из интимы (тонкого слоя эндотелиальных клеток). Средний диаметр просвета как раз достаточно велик, чтобы позволить эритроцитам (красным кровяным тельцам) проходить в один ряд. Обменные сосуды — это место, где газы, питательные вещества и отходы обмениваются между кровью и окружающими тканями.
Существует три основных типа капилляров: непрерывные, фенестрированные и прерывистые. Непрерывные капилляры являются наиболее распространенным типом в организме человека и находятся в коже, мышцах, легких и центральной нервной системе. Они обладают низкой проницаемостью и поэтому допускают лишь ограниченное прохождение веществ через стенку капилляра.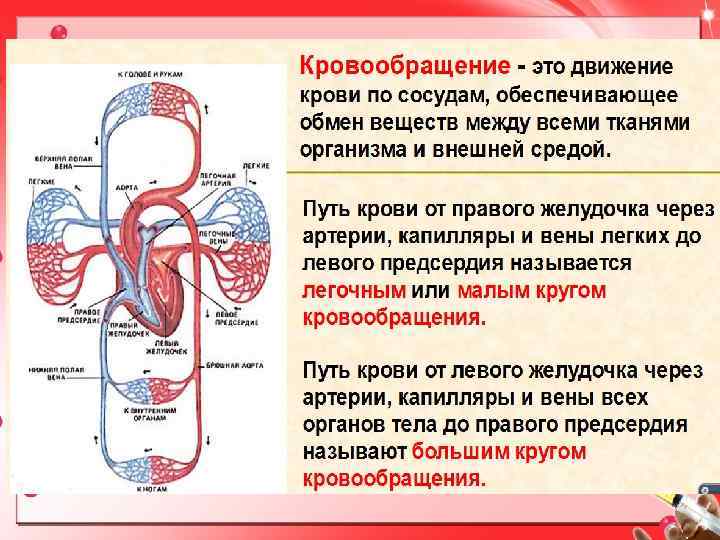 Фенестрированные капилляры гораздо более проницаемы, чем непрерывные капилляры; в их стенках имеются круглые поры или фенестры, закрытые тонкой диафрагмой. Прерывистые капилляры, также называемые синусоидами, имеют промежутки между эндотелиальными клетками, которые достаточно велики, чтобы даже эритроциты могли проходить через стенку капилляра. Они находятся в печень, селезенка и костный мозг, а также некоторые железы внутренней секреции.
Фенестрированные капилляры гораздо более проницаемы, чем непрерывные капилляры; в их стенках имеются круглые поры или фенестры, закрытые тонкой диафрагмой. Прерывистые капилляры, также называемые синусоидами, имеют промежутки между эндотелиальными клетками, которые достаточно велики, чтобы даже эритроциты могли проходить через стенку капилляра. Они находятся в печень, селезенка и костный мозг, а также некоторые железы внутренней секреции.
Капиллярное русло представляет собой сеть капилляров, соединяющих артериолы с венулами; обычно имеется от 10 до 100 капилляров на ложе. Артериолы дают начало либо капиллярам, либо метартериолам, сосудам, которые шире настоящих капилляров и непосредственно соединяют артериолы с венулами. Истинные капилляры ответвляются от артериол или метартериол и окружены у своего начала прекапиллярным сфинктером, что позволяет регулировать кровоток в капилляре. Артериовенозные (AV) шунты представляют собой анастомозы, которые полностью обходят капиллярное русло; они часто наблюдаются в тканях, требующих повышенного кровотока.
Вены и венулы
Вены — это кровеносные сосуды, несущие кровь от капиллярного русла к сердцу. Капилляры образуют венулы (маленькие вены, стенки которых состоят из тонкого слоя эндотелиальных клеток), которые, в свою очередь, сливаются, образуя вены. Кровь от головы, шеи и рук поступает в верхнюю полую вену, а в нижнюю полую вену поступает кровь от туловища и ног; эти крупные вены впадают в правое предсердие сердца. Вены несут кровь, бедную кислородом, за исключением легочной вены, которая несет обогащенную кислородом кровь от легких к сердцу.
Стенки вен тоньше, а просвет больше, чем у артерий. Они могут вмещать большой объем крови и могут действовать как резервуары крови, содержащие до 70% общего объема крови в организме. Поэтому вены и венулы называют емкостными сосудами. Большинство вен имеют систему клапанов, парных складок интимы, препятствующих обратному току крови.
Функция
Кровяное давление
Кровяное давление определяется как сила на единицу площади, с которой текущая кровь действует на стенку сосуда; это может быть представлено уравнением Артериальное давление = поток × сопротивление .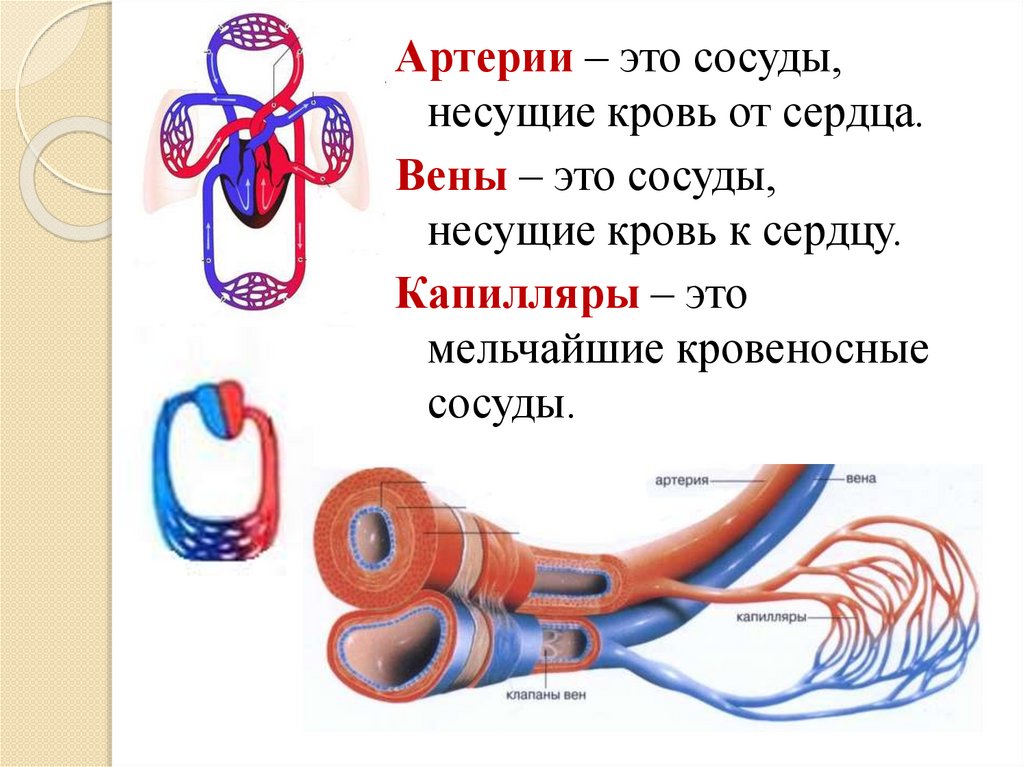 Артериальное давление обычно выражается в мм рт. ст. (читается как «миллиметры ртутного столба»). Обычно его записывают двумя числами: систолическое давление превышает диастолическое давление. Систола — это период сердечного цикла , в котором аортальный клапан открывается и кровь поступает в аорту; систолическое давление – это максимальное давление во время систолы. Точно так же диастола — это период, когда левый желудочек расслабляется, чтобы он мог снова наполниться кровью; Поэтому диастолическое давление измеряют во время диастолы. Обычно считается, что у здорового молодого человека артериальное давление должно быть 120/80 мм рт. ст. (т. е. систолическое давление 120 мм рт. ст. и диастолическое давление 80 мм рт. ст.).
Артериальное давление обычно выражается в мм рт. ст. (читается как «миллиметры ртутного столба»). Обычно его записывают двумя числами: систолическое давление превышает диастолическое давление. Систола — это период сердечного цикла , в котором аортальный клапан открывается и кровь поступает в аорту; систолическое давление – это максимальное давление во время систолы. Точно так же диастола — это период, когда левый желудочек расслабляется, чтобы он мог снова наполниться кровью; Поэтому диастолическое давление измеряют во время диастолы. Обычно считается, что у здорового молодого человека артериальное давление должно быть 120/80 мм рт. ст. (т. е. систолическое давление 120 мм рт. ст. и диастолическое давление 80 мм рт. ст.).
Артериальное давление пропорционально кровотоку (количество крови, протекающей через сосуд в единицу времени) и сосудистому сопротивлению. Давление варьируется по всей сердечно-сосудистой системе в зависимости от типа и размера кровеносного сосуда.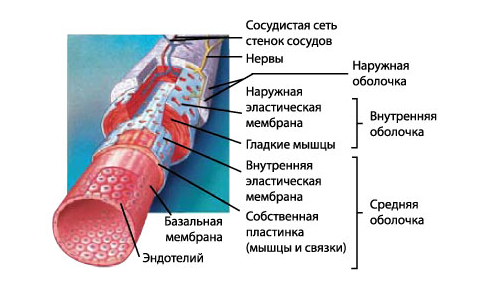 Самое высокое системное кровяное давление обнаруживается в аорте и постепенно снижается по ходу артериальной системы; он достигает своей нижней точки в венах.
Самое высокое системное кровяное давление обнаруживается в аорте и постепенно снижается по ходу артериальной системы; он достигает своей нижней точки в венах.
Существует ряд факторов, влияющих на кровяное давление. Физические характеристики человека (например, пол, возраст, вес, раса или социально-экономический статус) могут положительно или отрицательно влиять на артериальное давление. Такие действия, как еда, питье, сон или курение, вызывают изменения давления, как и умственная деятельность или эмоции, такие как 9.0031 тревога или опасение. Различные расстройства, такие как атеросклероз, анемия и сахарный диабет , оказывают неблагоприятное воздействие на кровяное давление.
Капиллярная динамика
Капиллярное русло — это место, где происходит обмен газами, питательными веществами и отходами между кровью и окружающими тканями. Он окружен интерстициальной жидкостью или лимфой, которая вырабатывается лимфатической системой . Вещества перемещаются между кровью и интерстициальной жидкостью через стенку капилляра путем диффузии (движение от высокой концентрации к низкой). Кислород и питательные вещества перемещаются из крови в интерстициальную жидкость, тогда как углекислый газ и отходы перемещаются в противоположном направлении. Газы, такие как кислород или углекислый газ, и жирорастворимые питательные вещества диффундируют через клеточные мембраны эндотелиальных клеток. Небольшие отверстия в стенке капилляра, называемые щелевидными порами или щелями, существуют там, где эндотелиальные клетки граничат друг с другом; небольшие водорастворимые питательные вещества или отходы могут диффундировать через эти щели.
Кислород и питательные вещества перемещаются из крови в интерстициальную жидкость, тогда как углекислый газ и отходы перемещаются в противоположном направлении. Газы, такие как кислород или углекислый газ, и жирорастворимые питательные вещества диффундируют через клеточные мембраны эндотелиальных клеток. Небольшие отверстия в стенке капилляра, называемые щелевидными порами или щелями, существуют там, где эндотелиальные клетки граничат друг с другом; небольшие водорастворимые питательные вещества или отходы могут диффундировать через эти щели.
В капиллярной динамике участвуют два типа давления. Гидростатическое давление — это сила, приходящаяся на единицу площади, с которой жидкость (кровь) действует на стенку сосуда. Коллоидно-осмотическое давление – это давление, необходимое для предотвращения осмоса жидкости через полупроницаемую мембрану. Транскапиллярная фильтрация определяется не только этими давлениями внутри сосудов, но и такими же давлениями вне сосудов. Осмотическое давление — это косвенное измерение относительных концентраций воды и растворенного вещества в растворе; чем выше осмотическое давление раствора, тем ниже концентрация воды и, следовательно, выше концентрация растворенного вещества в растворе.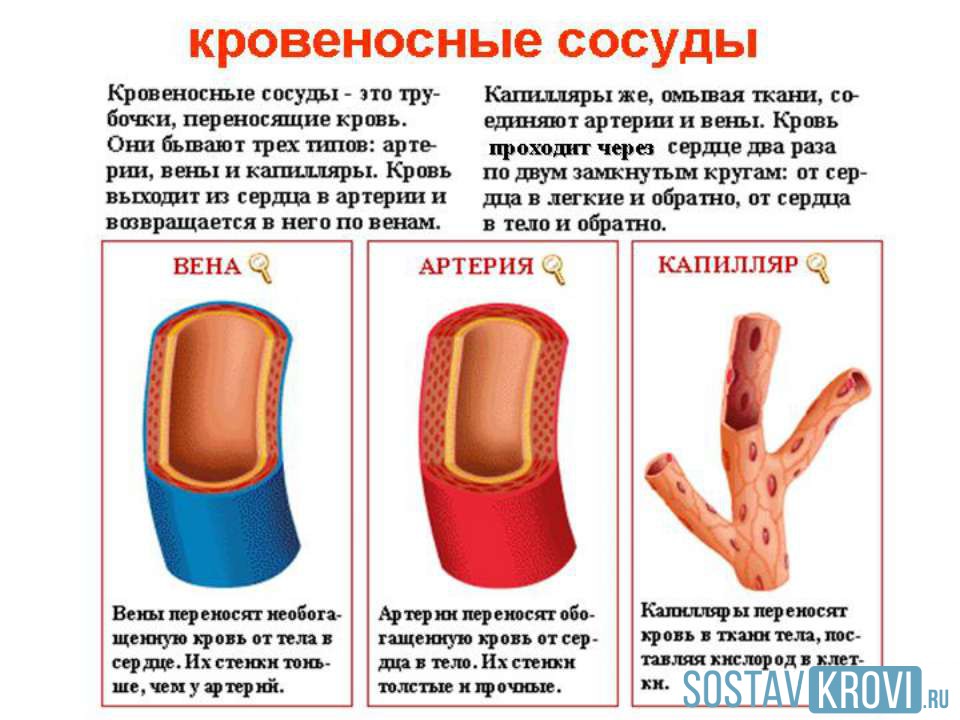 В капилляре осмотические силы проявляются главным образом белками, относительно непроницаемыми для стенки капилляра.
В капилляре осмотические силы проявляются главным образом белками, относительно непроницаемыми для стенки капилляра.
Роль в здоровье человека
В «Обновленной статистике по сердечным заболеваниям и инсультам» за 2006 г., опубликованной Американской кардиологической ассоциацией, говорится, что сердечно-сосудистые заболевания (ССЗ) ежегодно с 1900 г. исключение 1918 г. В 2003 г. на сердечно-сосудистые заболевания приходилось 37,3% всех смертей в США; по оценкам, более 71 миллиона американцев страдают от одного или нескольких сердечно-сосудистых заболеваний.
Существует множество факторов, повышающих риск сердечно-сосудистых заболеваний. К ним относятся:
- Основные факторы риска: табачный дым, раса, наследственность, сахарный диабет, высокий уровень холестерина, гипертония, отсутствие физической активности и ожирение.
- Сопутствующие факторы риска: стресс, высокий уровень триглицеридов, алкоголь, оральные контрацептивы, беременность, менопауза, и синдром X (набор факторов риска, включающий ожирение, непереносимость глюкозы, гипертонию и высокий уровень холестерина).

Кровеносные сосуды и кровоток могут реагировать на множество факторов местного контроля, включая нервные (такие как шок ) или гормональные импульсы (например, гнев или страх). Сами кровеносные сосуды также могут расти (процесс, называемый ангиогенезом) или перестраиваться в ответ на такие заболевания, как ишемия и гипертония.
Общие заболевания и расстройства
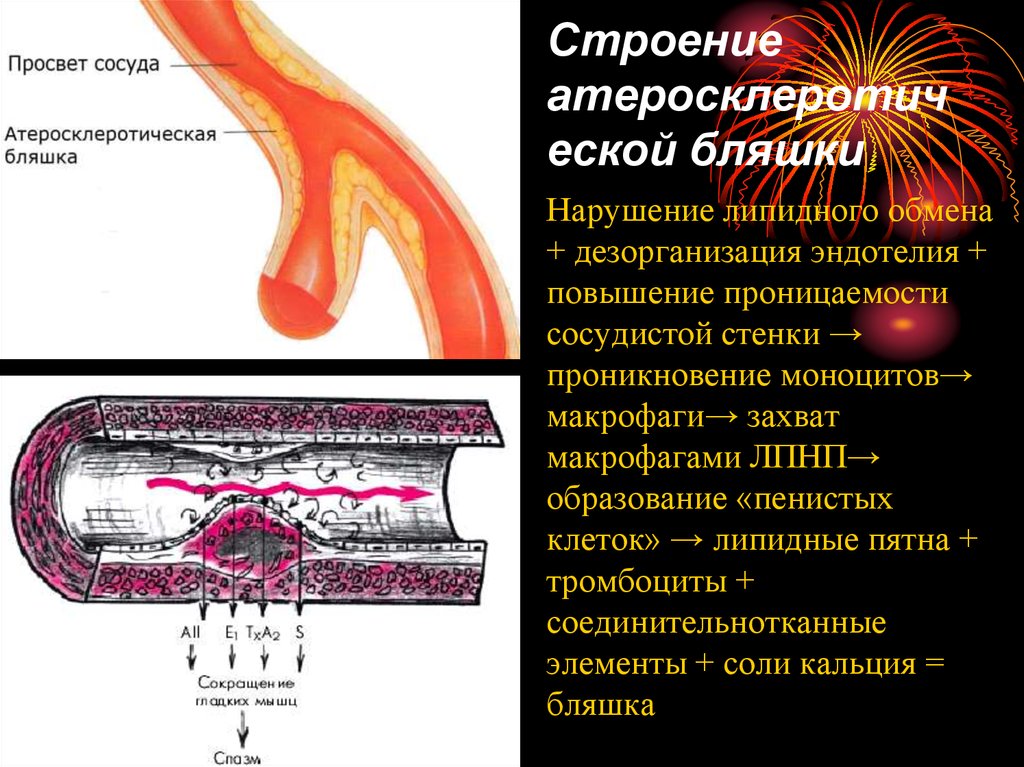
- Атеросклероз: По данным Американской кардиологической ассоциации, на атеросклероз приходится почти 75% всех смертей, связанных с сердечно-сосудистыми заболеваниями. Он включает накопление липидов и других веществ на внутренней оболочке артерии; область нарастания называется бляшкой. В результате артериальная стенка утолщается и твердеет, теряя эластичность. Тромбы (сгустки крови) образуются при разрыве бляшек; если они закупоривают артерию, это может привести к сердечному приступу или инсульту.
- Инсульт: Инсульт возникает, когда мозг лишается кислорода из-за нарушения кровотока, часто вызванного тромбом или разрывом кровеносного сосуда.
 В зависимости от области мозга, которая повреждена, неврологическое повреждение может быть обратимым или необратимым и может включать кому, паралич, проблемы со зрением или речью, судороги или нарушение памяти.
В зависимости от области мозга, которая повреждена, неврологическое повреждение может быть обратимым или необратимым и может включать кому, паралич, проблемы со зрением или речью, судороги или нарушение памяти. - Варикозное расширение вен: необратимые изменения диаметра и/или длины вен могут быть результатом повреждения или выхода из строя венозных клапанов. Сила тяжести, ожирение, беременность и возраст также могут играть роль в развитии варикозного расширения вен.
- Гемангиомы: Обычно это доброкачественные сосудистые аномалии, которые могут проявляться небольшими безвредными родимыми пятнами или мешочками сосудистых тканей разного размера, которые могут выступать из кожи. Гемангиомы часто представляют собой только косметические пятна, но могут, в зависимости от их расположения, вызывать обструкцию дыхательных путей, блокировать зрение, или блокировать жизненно важные органы.
- Аневризма: Аневризма возникает в результате расширения стенки кровеносного сосуда из-за ослабления стенки в результате болезни, высокого кровяного давления или врожденных дефектов.
 Аневризма брюшной аорты является наиболее распространенным типом. Разрыв аневризмы является серьезным неотложным состоянием и требует хирургического вмешательства.
Аневризма брюшной аорты является наиболее распространенным типом. Разрыв аневризмы является серьезным неотложным состоянием и требует хирургического вмешательства.
КЛЮЧЕВЫЕ ТЕРМИНЫ
Анастомозы — Соединения, образующиеся в месте слияния артерий и артериол, обеспечивающие альтернативные каналы доставки крови.
Артерии — Кровеносные сосуды, несущие кровь от сердца.
Диастолическое давление — Диастола — это период, в течение которого левый желудочек расслабляется, чтобы он мог снова наполниться кровью; Поэтому диастолическое давление измеряют во время диастолы.
Гидростатическое давление — Сила на единицу площади, с которой жидкость (кровь) действует на стенку сосуда.
Люмен— Полая середина кровеносного сосуда.
Осмотическое давление — Давление, необходимое для предотвращения осмоса жидкости через полупроницаемую мембрану. Это косвенное измерение концентрации воды и растворенных веществ в растворе.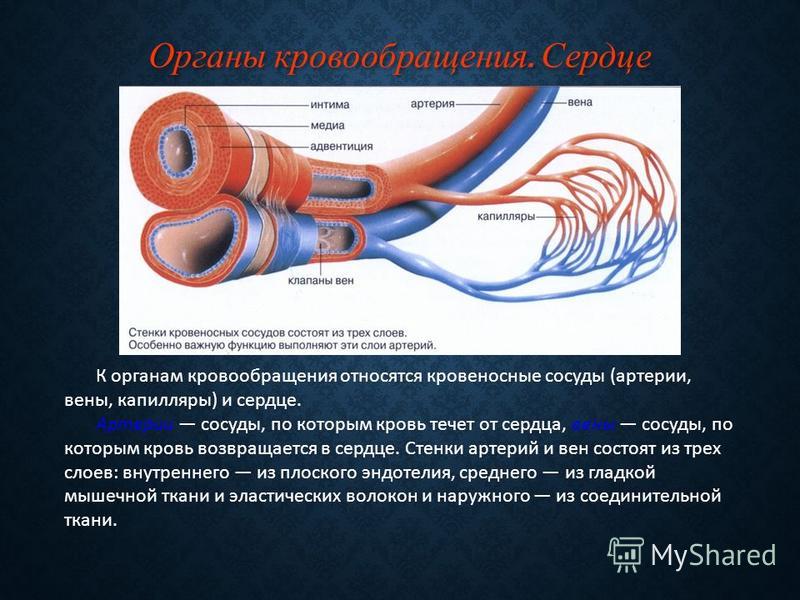
Систолическое давление — Систола — это период сердечного цикла, при котором аортальный клапан открывается и кровь поступает в аорту; систолическое давление – это максимальное давление во время систолы.
Tunica intima, media, adventitia— Три слоя, из которых состоят стенки крупных артерий и вен.
Vasa vasorum — Мелкие кровеносные сосуды, снабжающие стенки крупных артерий и вен кислородом и питательными веществами.
Вены — Кровеносные сосуды, несущие кровь от капиллярного русла к сердцу.
Ресурсы
КНИГИ
Aaronson, Philip, et al. Краткий обзор сердечно-сосудистой системы . Оксфорд, Великобритания: Blackwell Sciences, Ltd., 19.99.
Чанг, Джон Б. и др. Учебник ангиологии . Нью-Йорк: Springer-Verlag, 2000.
Diehm, C., et al. Цветной атлас сосудистых заболеваний . Берлин: Springer-Verlag, 2000.
Мариеб, Элейн Н. Основы анатомии и физиологии человека .


 Eur Spine J. 2015 Nov; 24 Suppl 7: 906-11. [PubMed: 26487472]
Eur Spine J. 2015 Nov; 24 Suppl 7: 906-11. [PubMed: 26487472]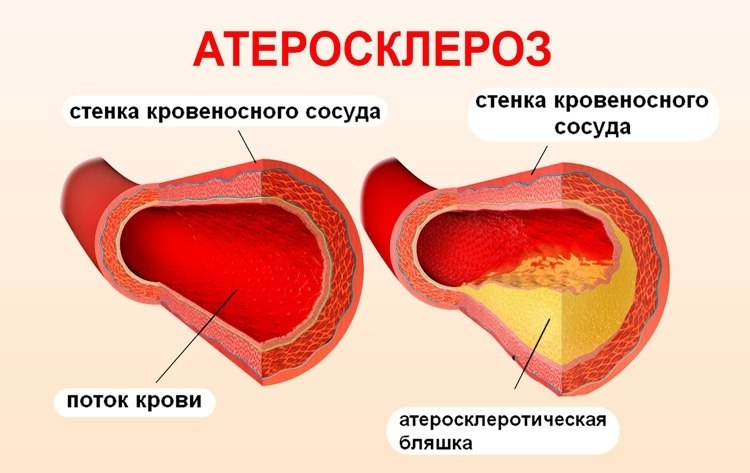 [В паблике: 12740947]
[В паблике: 12740947]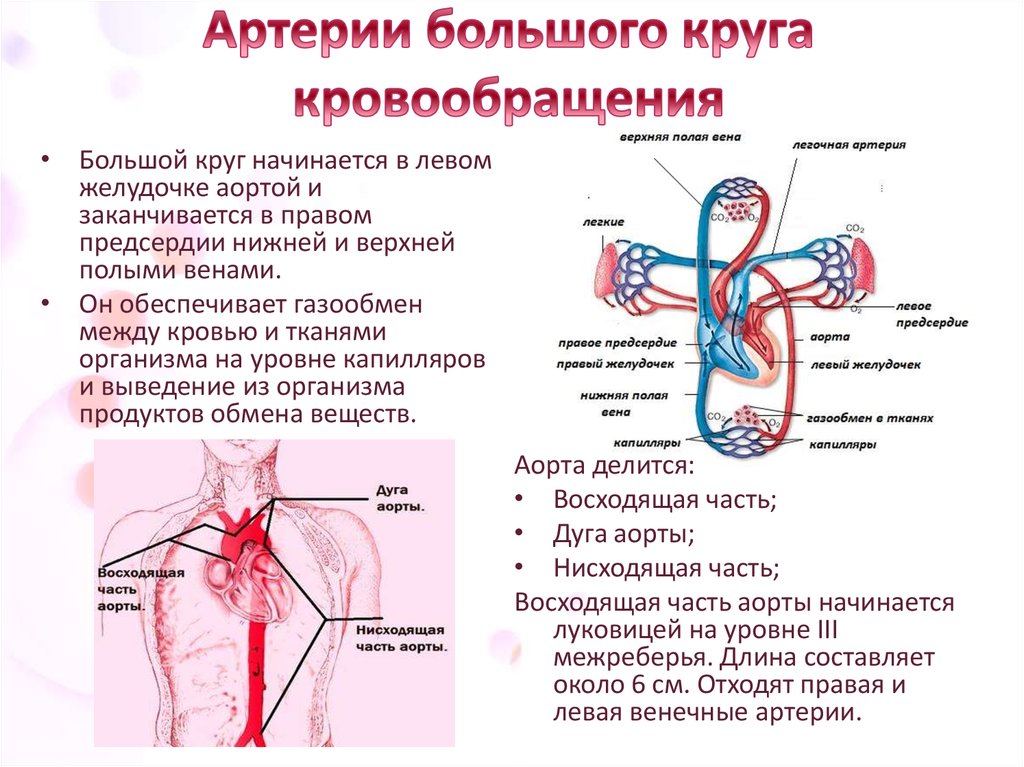 Опыт Клин Кардиол. 2011 Весна;16(1):11-5. [Бесплатная статья PMC: PMC3076160] [PubMed: 21523201]
Опыт Клин Кардиол. 2011 Весна;16(1):11-5. [Бесплатная статья PMC: PMC3076160] [PubMed: 21523201]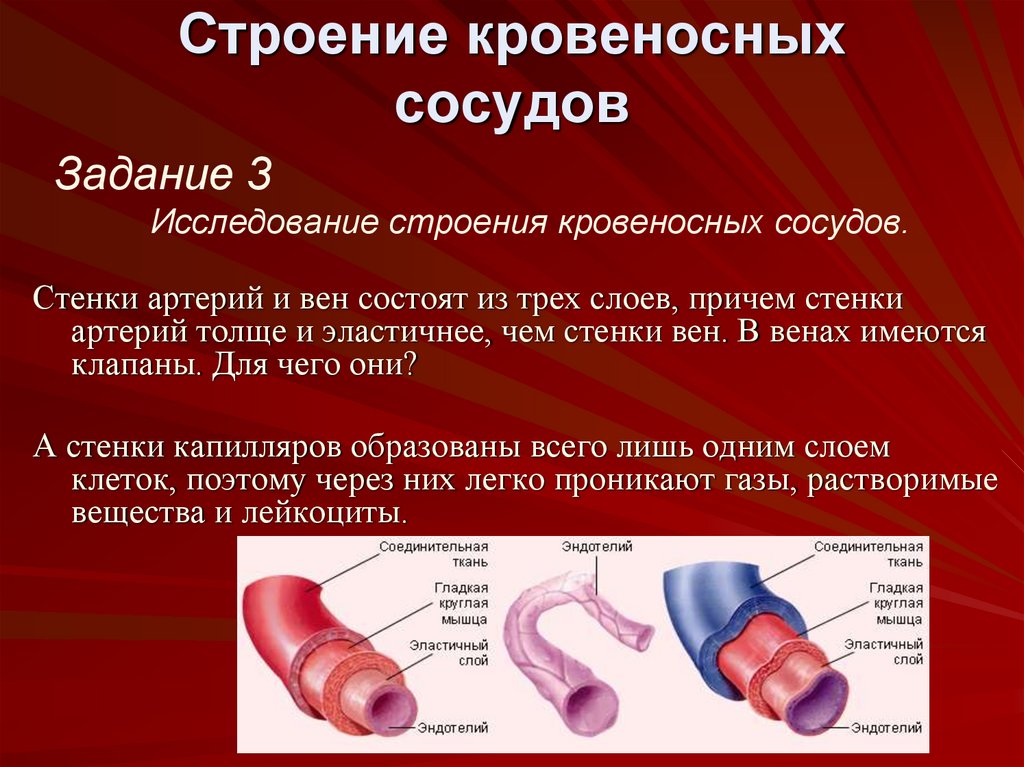
 В зависимости от области мозга, которая повреждена, неврологическое повреждение может быть обратимым или необратимым и может включать кому, паралич, проблемы со зрением или речью, судороги или нарушение памяти.
В зависимости от области мозга, которая повреждена, неврологическое повреждение может быть обратимым или необратимым и может включать кому, паралич, проблемы со зрением или речью, судороги или нарушение памяти. Аневризма брюшной аорты является наиболее распространенным типом. Разрыв аневризмы является серьезным неотложным состоянием и требует хирургического вмешательства.
Аневризма брюшной аорты является наиболее распространенным типом. Разрыв аневризмы является серьезным неотложным состоянием и требует хирургического вмешательства.
Leave A Comment