Типы кристаллических решёток — урок. Химия, 8–9 класс.
Большинство твёрдых веществ имеет кристаллическое строение, которое характеризуется строго определённым расположением частиц. Если соединить частицы условными линиями, то получится пространственный каркас, называемый кристаллической решёткой. Точки, в которых размещены частицы кристалла, называют узлами решётки. В узлах воображаемой решётки могут находиться атомы, ионы или молекулы.
В зависимости от природы частиц, расположенных в узлах, и характера связи между ними различают четыре типа кристаллических решёток: ионную, металлическую, атомную и молекулярную.
Ионными называют решётки, в узлах которых находятся ионы.
Их образуют вещества с ионной связью. В узлах такой решётки располагаются положительные и отрицательные ионы, связанные между собой электростатическим взаимодействием.
Ионные кристаллические решётки имеют соли, щёлочи, оксиды активных металлов. Ионы могут быть простые или сложные. Например, в узлах кристаллической решётки хлорида натрия находятся простые ионы натрия Na+ и хлора Cl−, а в узлах решётки сульфата калия чередуются простые ионы калия K+ и сложные сульфат-ионы SO42−.
Связи между ионами в таких кристаллах прочные. Поэтому ионные вещества твёрдые, тугоплавкие, нелетучие. Такие вещества хорошо растворяются в воде.
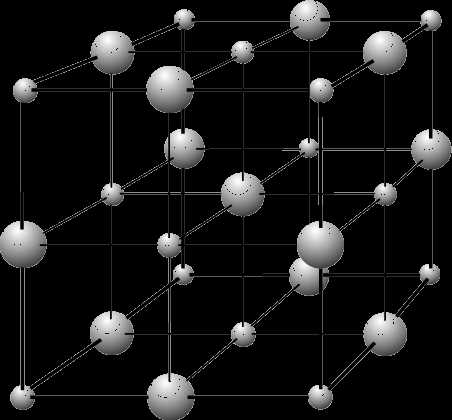
Кристаллическая решётка хлорида натрия
Кристалл хлорида натрия
Металлическими называют решётки, которые состоят из положительных ионов и атомов металла и свободных электронов.
Их образуют вещества с металлической связью. В узлах металлической решётки находятся атомы и ионы (то атомы, то ионы, в которые легко превращаются атомы, отдавая свои внешние электроны в общее пользование).
Такие кристаллические решётки характерны для простых веществ металлов и сплавов.
Температуры плавления металлов могут быть разными (от \(–37\) °С у ртути до двух-трёх тысяч градусов). Но все металлы имеют характерный металлический блеск, ковкость, пластичность, хорошо проводят электрический ток и тепло.
Металлическая кристаллическая решётка

Металлические изделия
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, соединённые ковалентными связями.
Такой тип решётки имеет алмаз — одно из аллотропных видоизменений углерода. К веществам с атомной кристаллической решёткой относятся графит, кремний, бор и германий, а также сложные вещества, например, карборунд SiC и кремнезём, кварц, горный хрусталь, песок, в состав которых входит оксид кремния(\(IV\)) SiO2.
Таким веществам характерны высокая прочность и твёрдость. Так, алмаз является самым твёрдым природным веществом. У веществ с атомной кристаллической решёткой очень высокие температуры плавления и кипения. Например, температура плавления кремнезёма — \(1728\) °С, а у графита она выше — \(4000\) °С. Атомные кристаллы практически нерастворимы.
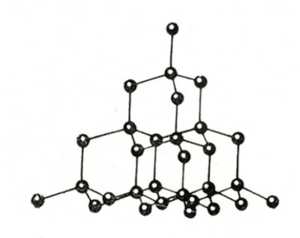
Кристаллическая решётка алмаза
Алмаз
Молекулярными называют решётки, в узлах которых находятся молекулы, связанные слабым межмолекулярным взаимодействием.
Несмотря на то, что внутри молекул атомы соединены очень прочными ковалентными связями, между самими молекулами действуют слабые силы межмолекулярного притяжения. Поэтому молекулярные кристаллы имеют небольшую прочность и твёрдость, низкие температуры плавления и кипения. Многие молекулярные вещества при комнатной температуре представляют собой жидкости и газы. Такие вещества летучи. Например, кристаллические иод и твёрдый оксид углерода(\(IV\)) («сухой лёд») испаряются, не переходя в жидкое состояние. Некоторые молекулярные вещества имеют запах.
Такой тип решётки имеют простые вещества в твёрдом агрегатном состоянии: благородные газы с одноатомными молекулами (He,Ne,Ar,Kr,Xe,Rn), а также неметаллы с двух- и многоатомными молекулами (h3,O2,N2,Cl2,I2,O3,P4,S8).
Молекулярную кристаллическую решётку имеют также вещества с ковалентными полярными связями: вода — лёд, твёрдые аммиак, кислоты, оксиды неметаллов. Большинство органических соединений тоже представляют собой молекулярные кристаллы (нафталин, сахар, глюкоза).
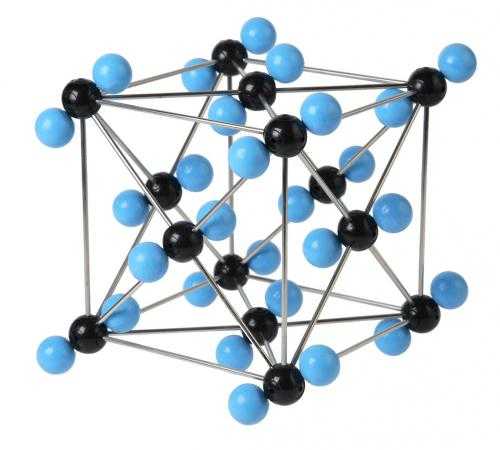
Кристаллическая решётка углекислого газа

«Сухой лёд»
Кристаллики иода
Если известно строение вещества, то можно предсказать его свойства.
Попробуем определить, каковы примерно температуры плавления у фторида натрия, фтороводорода и фтора.
У фторида натрия — ионная кристаллическая решётка. Значит, его температура плавления будет высокой. Фтороводород и фтор имеют молекулярные кристаллические решётки. Поэтому их температуры плавления будут невысокими. Молекулы фтороводорода полярные, а фтора — неполярные. Значит, межмолекулярное взаимодействие у фтороводорода будет сильнее, и его температура плавления будет выше по сравнению со фтором.
Экспериментальные данные подтверждают эти предположения: температуры плавления NaF, HF и F2 составляют соответственно \(995\) °С, \(–83\) °С, \(–220\) °С.
Источники:
Габриелян О. С. Химия. 8 класс. Учебник для общеобразовательных учреждений. М.: Дрофа, 2013. — 133 с.
www.yaklass.ru
Кристаллические решетки: виды, свойства
Содержание:
Определение кристаллической решетки
Как мы знаем, все материальные вещества могут пребывать в трех базовых состояниях: жидком, твердом, и газообразном. Правда есть еще состояние плазмы, которое ученые считают ни много ни мало четвертым состоянием вещества, но наша статья не о плазме. Твердое состояние вещества потому твердое, так как имеет особую кристаллическую структуру, частицы которой находятся в определенном и четко заданном порядке, создавая, таким образом, кристаллическую решетку. Строение кристаллической решетки состоит из повторяющихся одинаковых элементарных ячеек: атомов, молекул, ионов, других элементарных частиц, связанных между собой различными узлами.
Виды кристаллических решеток
В зависимости от частиц кристаллической решетки существует четырнадцать типов оной, приведем наиболее популярные из них:
- Ионная кристаллическая решетка.
- Атомная кристаллическая решетка.
- Молекулярная кристаллическая решетка.
- Металлическая кристаллическая решетка.
Далее более подробно опишем все типы кристаллической решетки.
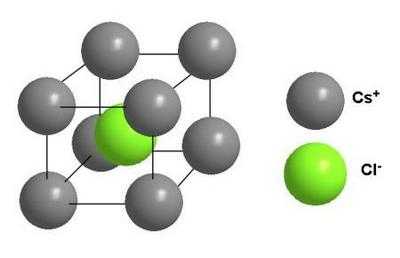
Ионная кристаллическая решетка
Главной особенностью строения кристаллической решетки ионов являются противоположные электрические заряды, собственно, ионов, вследствие чего образуется электромагнитное поле, определяющее свойства веществ, имеющих ионную кристаллическую решетку. А это тугоплавкость, твердость, плотность и возможность проводить электрический ток. Характерным примером ионной кристаллической решетки может быть поваренная соль.
Атомная кристаллическая решетка
Вещества с атомной кристаллической решеткой, как правило, имеют в своих узлах, состоящих собственно из атомов сильные ковалентные связи. Ковалентная связь происходит, когда два одинаковых атома делятся друг с другом по-братски электронами, образуя, таким образом, общую пару электронов для соседних атомов. Из-за этого ковалентные связи сильно и равномерно связывают атомы в строгом порядке – пожалуй, это самая характерная черта строения атомной кристаллической решетки. Химические элементы с подобными связями могут похвастаться своей твердостью, высокой температурой плавления. Атомную кристаллическую решетку имеют такие химические элементы как алмаз, кремний, германий, бор.
Молекулярная кристаллическая решетка
Молекулярный тип кристаллической решетки характеризуется наличием устойчивых и плотноупакованных молекул. Они располагаются в узлах кристаллической решетки. В этих узлах они удерживаются такими себе вандервальсовыми силами, которые в десять раз слабее сил ионного взаимодействия. Ярким примером молекулярной кристаллической решетки является лед – твердое вещество, имеющее однако свойство переходить в жидкое – связи между молекулами кристаллической решетки совсем слабенькие.
Металлическая кристаллическая решетка
Тип связи металлической кристаллической решетки гибче и пластичнее ионной, хотя внешне они весьма похожи. Отличительной особенностью ее является наличие положительно заряженных катионов (ионов метала) в узлах решетки. Между узлами живут электроны, участвующие в создании электрического поля, эти электроны еще называются электрическим газом. Наличие такой структуры металлической кристаллической решетки объясняет ее свойства: механическую прочность, тепло и электропроводность, плавкость.
Кристаллические решетки, видео
И в завершение подробное видео пояснения о свойствах кристаллических решеток.
Эта статья доступна на английском — Crystal Lattice in Chemistry.
www.poznavayka.org
тип, строение, сходство с графитом

Узнав физические свойства алмаза и графита, ученые отметили, что это разные формы углерода. Первый – это драгоценный минерал, один из самых твердых в мире. По принятой у геммологов шкале Мооса алмаз имеет наибольший балл твердости – 10. Графит по этой системе не дотягивает даже до 2. Блестящая драгоценность и грифель простого карандаша состоят из углерода. Различие этих минералов определяет тип кристаллической решетки. Но свойства их сильно отличаются друг от друга. Об этом читайте ниже.
Что такое алмаз и графит
Алмаз – самый твердый минерал. Внешне это прозрачный камень, у которого четко видна кристаллическая форма. Диаманты бесцветные, но встречаются разные оттенки, среди которых даже черный. Цвет зависит от природных условий, в которых формировался камень, а также от различных примесей в его структуре.

Графит – хрупкое, жирное на ощупь вещество, имеющее металлический блеск, состоящее из молекул углерода, расположенных слоями и образующих мелкие тонкие пластинки. При его нажатии на листке остается след.
Состав минералов
Первое, с чего начнем рассмотрение характеристики алмаза и графита, это состав минералов. Оба – из углерода, шестого элемента периодической системы.
Поскольку алмаз и графит состоят из частиц углерода, тип вещества у них – индивидуальный, а качественный состав образован соединениями атомов углерода. Формула алмаза и графита в химии проста – С, углерод. Этот химический элемент не имеет запаха, поэтому ни алмаз, ни графит ничем не пахнут.

Хотя химическая формула алмаза имеет схожесть с формулой графита, у структур, в которые соединяются атомы углерода, образуя кристаллическую решетку, есть разница.
Когда у минералов кристаллические решетки имеют отличие, но для них характерен идентичный химический состав, их называют полиморфами. Рассматриваемые минералы – разные виды полиморфных модификаций углерода.
Как и где находят углеродные минералы
Сходство элементарного химического состава не обуславливает схожие свойства веществ. Различия объясняются сложностями происхождения двух разных углеродных пород. Алмазы образуются под действием сильного давления после сверхбыстрого охлаждения. А если атмосферное давление занижено, то при довольно высокой температуре образуется графит.

Подтверждением того, что алмаз и графит образовались не одинаково, служит их нахождение в природе. Около 80% всех бриллиантов добывают в кимберлитовых трубках – глубоких воронках, образованных магмой, вышедшей после взрыва и выхода наружу подземного газа.
Графитовых же месторождений много в осадочных породах и пластах, образованных магмой.
Химическая связь в углеродных минералах
Частицы, из которых состоят твердые вещества, соединены в кристаллические решетки. Науке известны 4 вида таких решеток – ионная, молекулярная, атомная и металлическая.
Внешне драгоценный кристалл схож с кристаллами соли, но у солей ионная кристаллическая решетка.
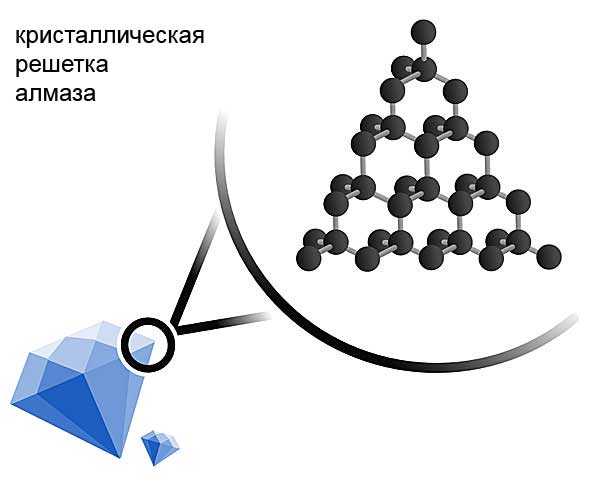
Тип кристаллической решетки алмаза, как и его полиморфа графита, атомная. В ее узлах лежат атомы углерода. Агрегатное состояние – твердое тело. Но все же по твердости углеродные полиморфы различны.
Свойство алмаза быть таким прочным обусловлено силой химической связи атомов. Структура диаманта трехмерная, атомы углерода в нем расположены в форме трехгранной пирамиды, тетраэдра. Каждая атомарная частица одинаково крепко соединяется со всеми четырьмя соседними, это осуществлено посредством ковалентной связи.
Атомарно графит – это множество слоев шестиугольных фигур, в каждой вершине которых расположен атом углерода. Его слоистая структура двухмерна. Связь в слоях ковалентная сильная, а между слоями гораздо слабее, как у веществ с молекулярной кристаллической решеткой. Пласты связаны непрочно. Поэтому твердость графита меньше по сравнению с бриллиантом.
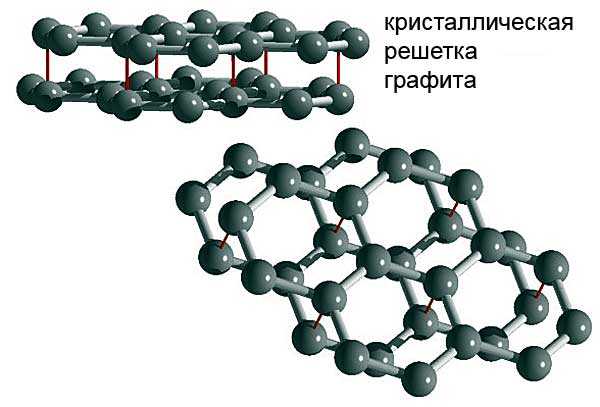
Взаимосвязь атомного строения и физики минерала
Рассмотрим, как внешне проявляется геометрия атомов. Различие свойств алмаза и графита напрямую связано с типом строения кристаллической решетки. Кристаллическая решетка алмаза имеет звенья из 4 хорошо соединенных атомов углерода. Они образовали сверхпрочные ковалентные сигма-связи. Оптические свойства межатомных соединений поглощают свет, делая кристалл прозрачным. А крепкая фиксация отрицательно заряженных элементарных частиц в однородных по силе связях придает ему твердость и свойства диэлектрика.
Образованные ковалентные пи-соединения гексагональной кристаллической решетки графита скрепляют атомы углерода в слои. При такой связи несколько электронов остаются свободными, поэтому пласты скреплены между собой незначительно. Движение нелокализованных элементарных частиц со знаком минус придает графиту электропроводность. У них отсутствует световая проводимость, что лишает вещество прозрачности, поэтому у графита цвет черный.
Аллотропные модификации углерода
Аллотропия – это способность химических элементов существовать в двух и более физических формах (аллотропах). Самой широкой из всех открытых является аллотропия углерода.
Если вы перечислите основные углеродные аллотропные видоизменения, то это будут:
- алмаз;
- графит;
- карбин;
- фуллерен.
Из указанных выше два аллотропа углерода синтезированы. Карбин и фуллерен – полученные искусственно аллотропные видоизменения углерода. Карбин – порошок из мелких кристалликов черного цвета. После открытия в лаборатории было найдено и природное вещество. Фуллерен – синтезированный в конце прошлого века в США желтый кристалл около 5 мм в диаметре.

Аллотропические формы углерода могут трансформироваться. Сам по себе переход алмаза в другое состояние не произойдет. Но при нагревании кристалла в безвоздушном пространстве до 1800 градусов он превратится в графит.
Известны методы, позволяющие осуществить и обратные превращения.
Как получить драгоценный камень из графита
Получить алмаз можно из графита. При давлении выше 1000 Па и температуре 3000 градусов с добавлением металлов углерод в графите меняет ковалентные связи. Полученные в результате камни мутные и пористые.
Другой метод – это применение ударной волны, после которой можно любоваться чистыми, прозрачными кристаллами правильной геометрической формы, но очень маленького размера.

Несовершенство этих методов привело к выводу, что алмазы лучше всего выращивать. При нагреве бриллианта до 1,5 тысячи градусов он растет. Но это дорого, поэтому сегодня искусственные драгоценности получают из метана.
Физические и химические свойства
Алмаз не обладает электропроводностью, но тепло проводит. Хорошо преломляет и отражает свет. Прозрачен, имеет блеск. Плавится при 3700-4000 градусов. Лавуазье впервые сжег диамант в 18 веке.
Позже ученые выяснили, что в соединении с кислородом алмаз горит при 721-800 градусах, испаряясь углекислым газом. Без воздуха может перейти в графит при нагреве до 2001-3000 градусов. Химические свойства говорят об устойчивости к воздействию кислот.

Графит электро-и-теплопроводный, нерастворим кислотами и водой, теплостойкий. Температура плавления 2500 – 3000 градусов. Не горит до 250-300 градусов, но при сжигании с температурой выше 300 и до 1000 превращается в углекислый газ.
Сравнительная характеристика
Сравним строение алмаза и графита и их физические свойства: твердость, теплопроводность, электропроводность, особенности химической связи.
О характеристиках минералов расскажет подробная сравнительная таблица:
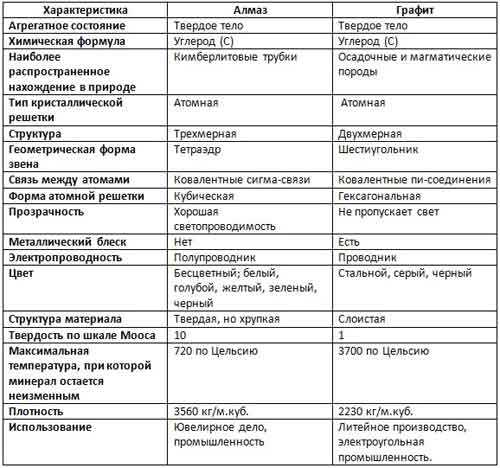
Применение в промышленности
Ювелиры ограняют состоящий из углерода алмаз, и он получает блеск бриллианта. Об этом читайте в статье «Что такое бриллиант и для чего он нужен».
В промышленности используют камни, которые имеют трещины, сколы, иные дефекты. Из них делают подшипники, сверла. Необработанные острые кристаллы применяют в электронике в качестве игл, в микросхемах, счетчиках прослойки из алмазов. Из алмазного порошка производят детали различных механизмов, обрамляют шлифовочные круги. Подробнее об этом – в статье «Области применения технических алмазов».

Алмаз имеет меньше ценности в промышленности, чем графит. Черный мягкий минерал встречается и в канцелярском карандаше, и в числе компонентов литейного производства, и в электроугольной промышленности. Электропроводные свойства графита используют для изготовления электродов.
Напишите, пожалуйста, в комментариях, о каких свойствах алмаза и графита вы узнали впервые.
Если статья вам понравилась, ставьте лайки и делитесь ссылкой на нее с друзьями в соцсетях.
Загрузка…pulskamnya.ru
Кристаллические решетки | himiyaklas.ru
Поговорим о твердых телах. Твердые тела можно разделить на две большие группы: аморфные и кристаллические. Разделять мы их будем по принципу есть порядок или нет.
В аморфных веществах молекулы располагаются хаотично. В их пространственном расположении нет никаких закономерностей. По сути, аморфные вещества – это очень вязкие жидкости, настолько вязкие, что твердые.
Отсюда и название: «а-» – отрицательная частица, «morphe» – форма. К аморфным веществам относятся: стекла, смолы, воск, парафин, мыло.
Отсутствие порядка в расположении частиц обусловливает физические свойства аморфных тел: они не имеют фиксированных температур плавления. По мере нагревания их вязкость постепенно снижается, и они также постепенно переходят в жидкое состояние.
В противоположность аморфным веществам существуют кристаллические. Частицы кристаллического вещества пространственно упорядочены. Это правильная структура пространственного расположения частиц в кристаллическом веществе называется кристаллической решеткой.
В отличии от аморфных тел, кристаллические вещества имеют фиксированные температуры плавления.
В зависимости от того какие частицы находятся в узлах решетки, и от того какие связи удерживают их различают: молекулярную, атомную, ионную и металлическую решетки.
Для чего принципиально важно знать, какая у вещества кристаллическая решетка? Что она определяет? Все. Структура определяет, как химические и физические свойства вещества.
Самый простой пример: ДНК. У всех организмов на земле она построена из одинакового набора структурных компонентов: нуклеотидов четырех видов. А какое многообразие жизни. Это все определяется структурой: порядком, в котором эти нуклеотиды расположены.
Молекулярная кристаллическая решетка.
Типичный пример вода – в твердом состоянии (лед). В узлах решетки находятся целые молекулы. И удерживают их вместе межмолекулярные взаимодействия: водородные связи, силы Ван-дер-Ваальса.
Связи эти слабые, поэтому молекулярная решетка – самая непрочная, температура плавления таких веществ низкая.
Хороший диагностический признак: если вещество имеет при нормальных условиях жидкое или газообразное состояние и/или имеет запах – то скорее всего у этого вещества молекулярная кристаллическая решетка. Ведь жидкое и газообразное состояния – это следствие того, что молекулы на поверхности кристалла плохо держатся (связи то слабые). И их «сдувает». Это свойство называется летучестью. А сдутые молекулы, диффундируя в воздухе доходят до наших органов обоняния, что субъективно ощущается как запах.
Молекулярную кристаллическую решетку имеют:
- Некоторые простые вещества неметаллов: I2, P, S (то есть все неметаллы, у которых не атомная решетка).
- Почти все органические вещества (кроме солей).
- И как уже говорилось ранее, вещества при нормальных условиях жидкие, либо газообразные (будучи замороженными) и/или имеющие запах (NH3, O2, H2O, кислоты, CO2).
Атомная кристаллическая решетка.
В узлах атомной кристаллической решетки, в отличие от молекулярной, располагаются отдельные атомы. Получается, что удерживают решетку ковалентные связи (ведь именно они связывают нейтральные атомы).
Классический пример – эталон прочности твердости – алмаз (по химической природе – это простое вещество углерод). Связи: ковалентные неполярные, так как решетку образуют только атомы углерода.
А вот, например, в кристалле кварца (химическая формула которого SiO2) есть атомы Si и O. Поэтому связи ковалентные полярные.
Физические свойства веществ с атомной кристаллической решеткой:
- прочность, твердость
- высокие температуры плавления (тугоплавкость)
- нелетучие вещества
- нерастворимы (ни в воде, ни в других растворителях)
Все эти свойства обусловлены прочностью ковалентных связей.
Веществ в атомной кристаллической решеткой немного. Особой закономерности нет, поэтому их нужно просто запомнить:
- Аллотропные модификации углерода (C): алмаз, графит.
- Бор (B), кремний (Si), германий (Ge).
- Только две аллотропные модификации фосфора имеют атомную кристаллическую решетку: красный фосфор и черный фосфор. (у белого фосфора – молекулярная кристаллическая решетка).
- SiC – карборунд (карбид кремния).
- BN – нитрид бора.
- Кремнезем, горный хрусталь, кварц, речной песок – все эти вещества имеют состав SiO2.
- Корунд, рубин, сапфир – у этих веществ состав Al2O3.
Наверняка возникает вопрос: С – это и алмаз, и графит. Но они же совершенно разные: графит непрозрачный, пачкает, проводит электрический ток, а алмаз прозрачный, не пачкает и ток не проводит. Отличаются они структурой.
И то, и то – атомная решетка, но разная. Поэтому и свойства разные.
Ионная кристаллическая решетка.
Классический пример: поваренная соль: NaCl. В узлах решетки располагаются отдельные ионы: Na+ и Cl–. Удерживает решетку электростатические силы притяжения между ионами («плюс» притягивается к «минусу»), то есть ионная связь.
Ионные кристаллические решетки довольно прочные, но хрупкие, температуры плавления таких веществ довольно высокие (выше, чем у представителей металлической, но ниже чем у веществ с атомной решеткой). Многие растворимы в воде.
С определением ионной кристаллической решетки, как правило, проблем не возникает: там, где ионная связь – там ионная кристаллическая решетка. Это: все соли, оксиды металлов, щелочи (и другие основные гидроксиды).
Металлическая кристаллическая решетка.
Металлическая решетка реализуется в простых веществах металлах. Ранее мы говорили, что все великолепие металлической связи можно понять лишь вместе с металлической кристаллической решеткой. Час настал.
Главное свойство металлов: электроны на внешнем энергетическом уровне плохо удерживаются, поэтому легко отдаются. Потеряв электрон металл превращается в положительно заряженный ион – катион:
Na0 – 1e → Na+
В металлической кристаллической решетке постоянно протекают процессы отдачи, и присоединения электронов: от атома металла в одном узле решетки отрывается электрон. Образуется катион. Оторвавшийся электрон притягивается другим катионом (или этим же): вновь образуется нейтральный атом.
В узлах металлической кристаллической решетки находятся как нейтральные атомы, так и катионы металла. А между узлами путешествуют свободные электроны:
Эти свободные электроны называются электронным газом. Именно они обусловливают физические свойства простых веществ металлов:
- тепло- и электропроводность
- металлический блеск
- ковкость, пластичность
Это и есть металлическая связь: катионы металлов притягиваются к нейтральным атомам и все это «склеивают» склеивают свободные электроны.
Как определить тип кристаллической решетки.

P.S. Есть кое-что в школьной программе и программе ЕГЭ по этой теме то, с чем мы не совсем согласны. А именно: обобщение, о том, что любая связь металл-неметалл – это ионная связь. Это допущение, намеренно сделано, видимо, для упрощения программы. Но это ведет к искажению. Граница между ионной и ковалентной связью условная. У каждой связи есть свой процент «ионности» и «ковалентности». Связь с малоактивным металлом имеет малый процент «ионности», она больше похожа на ковалентную. Но по программе ЕГЭ, она «округляется» в сторону ионной. Это порождает, порой абсурдные вещи. Например, Al2O3 – вещество с атомной кристаллической решеткой. О какой ионности здесь может идти речь. Только ковалентная связь может удерживать таким образом атомы. Но по стандарту «металл-неметалл» мы квалифицируем эту связь как ионную. И получается противоречие: решетка атомная, а связь ионная. Вот к чему приводит, излишнее упрощение.
himiyaklas.ru
Строение различных веществ. Тип кристаллической решётки.
Для большинства веществ характерна способность в зависимости от условий находиться в одном из трех агрегатных состояний: твердом, жидком или газообразном.
Например, вода при нормальном давлении в интервале температур 0-100oC является жидкостью, при температуре выше 100оС способна существовать только в газообразном состоянии, а при температуре менее 0оС представляет собой твердое вещество.
Вещества в твердом состоянии различают аморфные и кристаллические.
Характерными признаками аморфных веществ является отсутствие четкой температуры плавления: их текучесть плавно увеличивается с ростом температуры. К аморфным веществам относятся такие соединения, как воск, парафин, большинство пластмасс, стекло и т.д.
Все же кристаллические вещества обладают конкретной температурой плавления, т.е. вещество с кристаллическим строением переходит из твердого состоянии в жидкое не постепенно, а резко, при достижении конкретной температуры. В качестве примера кристаллических веществ можно привести поваренную соль, сахар, лед.
Разница в физических свойствах аморфных и кристаллических твердых веществ обусловлена прежде всего особенностями строения таких веществ. В чем заключается разница между веществом в аморфном и кристаллическом состоянии, проще всего понять из следующей иллюстрации:
Как можно заметить, в аморфном веществе, в отличие от кристаллического, отсутствует какой-либо порядок в расположении частиц. Если же в кристаллическом веществе мысленно соединить прямой два близкорасположенных друг к другу атома, то можно обнаружить, что на этой линии на строго определенных промежутках будут лежать одни и те же частицы:
Таким образом, в случае кристаллических веществах можно говорить о таком понятии, как кристаллическая решетка.
Кристаллической решеткой называют пространственный каркас, соединяющий точки пространства, в которых находятся частицы, образующие кристалл.
Точки пространства, в которых находятся образующие кристалл частицы, называют узлами кристаллической решетки.
В зависимости от того, какие частицы находятся в узлах кристаллической решетки, различают: молекулярную, атомную, ионную и металлическую кристаллические решетки.
В узлах молекулярной кристаллической решетки
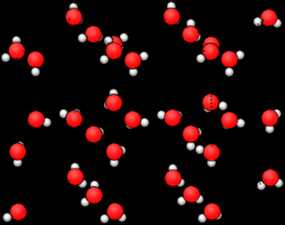 Кристаллическая решетка льда как пример молекулярной решетки
Кристаллическая решетка льда как пример молекулярной решеткинаходятся молекулы, внутри которых атомы связаны прочными ковалентными связями, однако сами молекулы удерживаются друг возле друга слабыми межмолекулярными силами. Вследствие таких слабых межмолекулярных взаимодействий кристаллы с молекулярной решеткой являются непрочными. Такие вещества от веществ с иными типами строения отличаются существенно более низкими температурами плавления и кипения, не проводят электрический ток, могут как растворяться, так и не растворяться в различных растворителях. Растворы таких соединений могут как проводить, так и не проводить электрический ток в зависимости от класса соединения. К соединениям с молекулярной кристаллической решеткой относятся многие простые вещества — неметаллы (отвержденные H2, O2, Cl2, ромбическая сера S8, белый фосфор P4), а также многие сложные вещества – водородные соединения неметаллов, кислоты, оксиды неметаллов, большинство органических веществ. Следует отметить, что, если вещество находится в газообразном или жидком состоянии, говорить о молекулярной кристаллической решетке неуместно: корректнее использовать термин — молекулярный тип строения.
Кристаллическая решетка алмаза как пример атомной решеткиВ узлах атомной кристаллической решетки
находятся атомы. При этом все узлы такой кристаллической решетки «сшиты» между собой посредством прочных ковалентных связей в единый кристалл. Фактически, такой кристалл является одной гигантской молекулой. Вследствие особенностей строения все вещества с атомной кристаллической решеткой являются твердыми, обладают высокими температурами плавления, химически мало активны, не растворимы ни в воде, ни в органических растворителях, а их расплавы не проводят электрический ток. Следует запомнить, что к веществам с атомным типом строения из простых веществ относятся бор B, углерод C (алмаз и графит), кремний Si, из сложных веществ — диоксид кремния SiO2 (кварц), карбид кремния SiC, нитрид бора BN.
У веществ с ионной кристаллической решеткой
в узлах решетки находятся ионы, связанные друг с другом посредством ионных связей.
Поскольку ионные связи достаточно прочны, вещества с ионной решеткой обладают сравнительно высокой твердостью и тугоплавкостью. Чаще всего они растворимы в воде, а их растворы, как и расплавы проводят электрический ток.
К веществам с ионным типом кристаллической решетки относятся соли металлов и аммония (NH4+), основания, оксиды металлов. Верным признаком ионного строения вещества является наличие в его составе одновременно атомов типичного металла и неметалла.
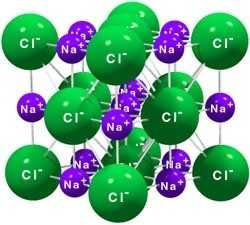 Кристаллическая решетка хлорида натрия как пример ионной решетки
Кристаллическая решетка хлорида натрия как пример ионной решетки| Однако следует отметить, что в веществах с ионным типом строения нередко можно обнаружить, помимо ионных, также ковалентные полярные связи. Это наблюдается в случае сложных ионов, т.е. состоящих из двух или более химических элементов (SO42-, NH4+, PO43- и т.д.). Внутри таких сложных ионов атомы связаны друг с другом ковалентными связями. |
Металлическая кристаллическая решетка
наблюдается в кристаллах свободных металлов, например, натрия Na, железа Fe, магния Mg и т.д. В случае металлической кристаллической решетки, в ее узлах находятся катионы и атомы металлов, между которыми движутся электроны. При этом движущиеся электроны периодически присоединяются к катионам, таким образом нейтрализуя их заряд, а отдельные нейтральные атомы металлов взамен «отпускают» часть своих электронов, превращаясь, в свою очередь, в катионы. Фактически, «свободные» электроны принадлежат не отдельным атомам, а всему кристаллу.
Металлическая кристаллическая решеткаТакие особенности строения приводят к тому, что металлы хорошо проводят тепло и электрический ток, часто обладают высокой пластичностью (ковкостью).
Разброс значений температур плавления металлов очень велик. Так, например, температура плавления ртути составляет примерно минус 39 оС (жидкая в обычных условиях), а вольфрама — 3422 °C. Следует отметить, что в обычных условиях все металлы, кроме ртути, являются твердыми веществами.
scienceforyou.ru
Кристаллическая решетка алмаза и другие характеристики
Алмаз — минерал, который является не чем иным, как модификацией углерода. Чистый алмаз имеет формулу, состоящую всего из одного элемента. Камень обладает уникальными свойствами в природе, поэтому кристаллическая решетка алмаза заинтересовала ученых, и структура вещества продолжает изучаться.
Идеальный алмаз можно представить как гигантскую молекулу углерода. Состав минерала ученые изучили только в конце XVIII века. С того момента начались попытки искусственного синтеза алмаза в лабораториях, но они были бессмысленными, поскольку отстроить кристаллическую решетку с нуля не получалось.
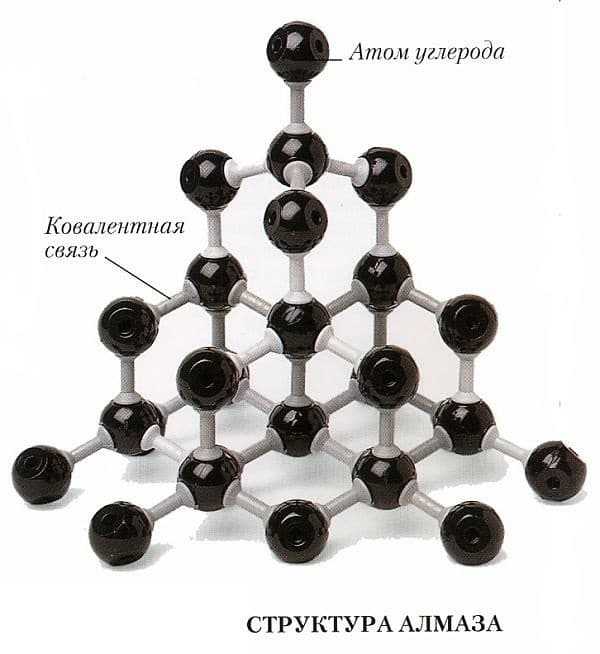
Структура алмаза
А еще техника не была на таком уровне, чтоб создать условия для образования алмаза. Только в пятидесятых годах ХХ века ученые смогли синтезировать алмаз самостоятельно. Этим занимались такие страны, как СССР, США и ЮАР.
Строение вещества
Вся загвоздка и сложность производства заключалась в уникальной структуре алмаза. Между атомами в химии может сформироваться четыре типа связи:
- ковалентная;
- ионная;
- металлическая;
- водородная.
Самая прочная из них — ковалентная связь. Она также имеет свои подвиды: сигма-связи и пи-связи. Второй подвид менее прочный. В алмазе есть несколько миллионов атомов углерода, которые соединены между собой с помощью ковалентных связей.
Пространственное расположение атомов и их соединения называются кристаллической решеткой. Именно ее строение и обусловливает такую характеристику, как твердость вещества. Элементарная ячейка структуры алмаза выглядит как куб. То есть алмаз кристаллизуется в кубической сингонии, если пользоваться научной терминологией.
На вершинах этого куба находится по атому углерода. По одному атому располагается в каждой грани, а еще четыре — внутри куба. Центральные атомы в гранях являются общими для двух ячеек, а те, что находятся в вершинах куба, — общие для восьми ячеек. Между собой атомы соединены ковалентными сигма-связями.
Такая структура и упаковка считается наиболее плотной. Каждый атом углерода располагается в центре тетраэдра и связан по всем сторонам. Поскольку валентность углерода равняется четырем, то все связи оказываются перекрытыми, и взаимодействие с веществом со стороны невозможно.
Расстояние между атомами одинаковое, свободных электронов нет, поэтому минерал является хорошим диэлектриком. Твердость алмаза достигается именно благодаря такому строению. Эти характеристики, в свою очередь, и стали причиной широкого использования камней. Они применяются не только в ювелирном деле, но и в качестве абразива, а также покрытия для инструментов.
Но не все в природе идеально. Даже в алмазах часто встречаются примеси. Такая структура позволяет минералу выглядеть абсолютно прозрачным, без включений. Но добываемые камни не всегда обладают ювелирными свойствами из-за большого количества дефектов и примесей.
Кристалл алмаза может содержать такие вещества:
- алюминий;
- кальций;
- магний;
- гранит.
Иногда в составе встречается вода, углекислота или другие газы. Примеси в кристалле располагаются неравномерно и несколько нарушают кристаллическую структуру. Если дефекты располагаются на периферии, что происходит чаще, тогда с ними можно бороться с помощью огранки.
Аллотропные модификации
Не только алмаз имеет подобный тип строения кристаллической решетки. Другие элементы из четвертой группы также имеют похожую структуру. Но все дело в атомной массе. Атомы углерода располагаются на близком расстоянии друг от друга, что делает связи прочнее. А вот с увеличением атомной массы элементы располагаются дальше и прочность соединений между ними падает.
А также у углерода есть в природе аллотропные модификации, куда, кроме алмаза, входят и другие вещества:
- графит;
- лонсдейлит;
- сажа, уголь;
- фуллерены;
- углеродные нанотрубки.
Ученых интересовала возможность превращения графита в алмаз. Сделать это можно только под действиями очень высокого давления и температуры.
Все дело в том, что графит отличается по пространственному расположению атомов и связям между ними. Если у алмаза все связи ковалентные-сигма, то пространственные связи графита — пи-соединения. А также в решетке графита остается несколько свободных электронов у атомов, которые перемещаясь, создают эффект электропроводности. Такая форма решетки называется гексагональной. Поэтому графит по шкале твердости имеет показатель единицу.
Лонсдейлиты еще не изучены окончательно, поскольку их добывают либо искусственно, либо из метеоритов, упавших на землю.
А вот фуллерены имеют кристаллическую решетку, напоминающую мяч, сложенный из восьмиугольников. По углам фигур расположены не атомы, а молекулы углерода. Эти вещества также продолжают исследовать.
Химический состав алмаза записывается формулой или элементом С.
Кроме показателя твердости — 10 из 10 по шкале Мооса — алмаз обладает такими характеристиками:
- Плотность — 3,5 г/см3.
- Камень довольно хрупкий. Несмотря на твердость, алмаз можно разрушить резким ударом.
- Спайность. Плотность у вещества неравномерная. Камень раскалывается по параллельным граням кристалла. Спайность должна учитываться при огранке камня, поскольку расчет ювелира и последующий удар определяет плоскость скола и отсекает ненужные примеси.
- Камень должен быть прозрачным. Тогда после огранки он будет играть на свету. Самые дорогие экземпляры называют алмазами чистой воды. Но все равно встречается до 5 % примесей в структуре, что искажает кристаллическую решетку, а иногда и портит вид камня.
- Если воздействовать на камень рентгеновскими лучами, то прочность ковалентных связей нарушится. В результате решетка станет рыхлой и твердость вещества также снизится. Но после этой процедуры появится интересное свойство: камень будет излучать свет в синей и зеленой части спектра.
В природе добытый минерал имеет форму кристалла с разным количеством граней. Иногда добывают не полные камни, а только сколы от больших алмазов. Определить скол это или полноценный минерал можно, изучив строение кристаллической решётки. Грани минералов часто покрыты наростами и углублениями.
Цвет алмаза также отличается разнообразием. Встречаются желтые, красноватые или даже черные оттенки алмазов. Конечно, кристаллическая решетка у камней изменена. Но свойства от этого страдают не сильно. Такие минералы называют фантазийными. Их окраска может быть неравномерной и зависеть от примесей в структуре.
Идеальное строение существует только у искусственных алмазов. Производство этих камней требует затравки в виде натурального кристалла, а также большого количества денежных вложений и аппаратуры. Но именно изучение кристаллической решетки и повлияло на развитие этой отрасли.
dedpodaril.com
Кристаллические решетки
Вещество может существовать в трех агрегатных состояниях: газообразном, жидком, твёрдом. Например, кислород, является газом, но при температуре -194 0С он превращается в голубую жидкость, а при температуре -218,8 0С – затвердевает в снегообразную массу, состоящую из кристаллов синего цвета.
Твёрдые вещества делят на кристаллические и аморфные. Аморфные вещества не имеют четкой температуры плавления, при нагревании размягчаются и переходят в текучее состояние. К аморфным веществам относятся пластмассы, воск, шоколад, пластилин, жевательные резинки.
Кристаллические вещества состоят из частиц, которые имеют четкое расположение в определенных точках пространства. Если соединить эти частицы, то получится своеобразный каркас, который называется кристаллической решеткой. А точки, где находятся частицы – узлами кристаллической решетки. В узлах кристаллической решетки могут находиться ионы, атомы, молекулы. Эти частицы совершают колебательные движения. При повышении температуры размах этих колебаний увеличивается, что приводит к тепловому расширению тел.
Кристаллическая решётка
В зависимости от типа частиц в кристаллической решетки и характера связи между ними, различают ионные, атомные, молекулярные и металлические кристаллические решётки.
Ионные кристаллические решётки
Ионными, называются кристаллические решётки, в узлах которых находятся ионы. Их образуют вещества с ионным типом связи. Это соли, основания, некоторые оксиды. Например, кристалл хлорида натрия, построен из чередующихся ионов Na+ и Cl—. Они образуют решётку в виде куба. Связи в этом кристалле очень прочные, поэтому вещества с ионным типом связи имеют высокую твердость и прочность, они нелетучи и тугоплавки.
Атомные кристаллические решётки
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы. Эти атомы между собой соединены очень прочными ковалентными связями. Атомную кристаллическую решётку имеет алмаз. Ограненный и отшлифованный алмаз называют бриллиантом. Он широко используется в ювелирном деле.
Кроме алмаза атомную кристаллическую решётку имеют и такие простые вещества, как бор, кремний, германий, и сложные: кремнезём, кварц, песок, горный хрусталь, в состав которых входит SiO2. Вещества с атомной кристаллической решеткой имеют высокие температуры плавления, они прочные и твёрдые, практически нерастворимые.
Молекулярные кристаллические решётки
Молекулярная кристаллическая решётка – это кристаллическая решетка, в узлах которой находятся молекулы. Связи у веществ с молекулярной кристаллической решёткой могут быть ковалентными полярными, как в молекулах HCl, H2O, и ковалентными неполярными, как в молекулах O2, O3, N2, H2 и др. Атомы внутри молекулы связаны прочно, а вот связи между самими молекулами непрочные. Поэтому вещества с молекулярной кристаллической решеткой имеют малую твердость, низкие температуры плавления и кипения, летучи. К веществам с молекулярной кристаллической решеткой относятся: лед (вода в твердом агрегатном состоянии), который уже при температуре выше 0 0С переходит в жидкое состояние, его кристаллическая структура разрушается; твердый оксид углерода (IV) – «сухой лед», который возгоняется при увеличении температуры, т.е. превращается в газ, твёрдые хлороводород и сероводород, твёрдые простые вещества. Такие как, одноатомные благородные газы, двухатомные молекулы (O2, N2, H2, Cl2, I2), трёхатомные (O3), четырёхатомные, как Р4, восьмиатомные молекулы, как S8. Молекулярную кристаллическую решетку имеют большинство органических веществ: глюкоза, сахар, нафталин, спирт, лимонная кислота.
Металлические кристаллические решётки
Металлическую кристаллическую решётку имеют вещества с металлическим типом связи. В узлах этой кристаллической решетки находятся ионы металла и свободные электроны. Поэтому вещества с этим типом связи обладают ковкостью, пластичностью, имеют металлический блеск, электро- и теплопроводны.
Для веществ молекулярного строения справедлив закон французского химика Ж. Л. Пруста – закон постоянства состава: молекулярные химические соединения независимо от способа их получения имеют постоянный состав и свойства. Закон Пруста – основной из законов химии, однако он несправедлив для веществ немолекулярного строения.
videouroki.net

Leave A Comment