о чем может рассказать человеческий геном и стоит ли доверять генетическим тестам
Более 15 лет назад завершился признанный одним из главных проектов XX столетия проект «Геном человека». Благодаря его участникам в том числе методы геномики стали доступнее широкому потребителю. Сегодня любой может сделать генетические тесты и, например, определить свое происхождение. Но что конкретно стоит за такими тестами, зачем с научной точки зрения изучать различные популяции, как работают популярные генетические методы и почему к некоторым из них стоит относиться более критично — об этом мы поговорили со специалистами по биоинформатике, сотрудниками лаборатории «Компьютерные технологии» Университета ИТМО.
«Геном человека»: что показало одно из главных исследований XX века
Информация о биохимических реакциях в клетках передается из поколения в поколение и реализуется для обеспечения жизнедеятельности клетки.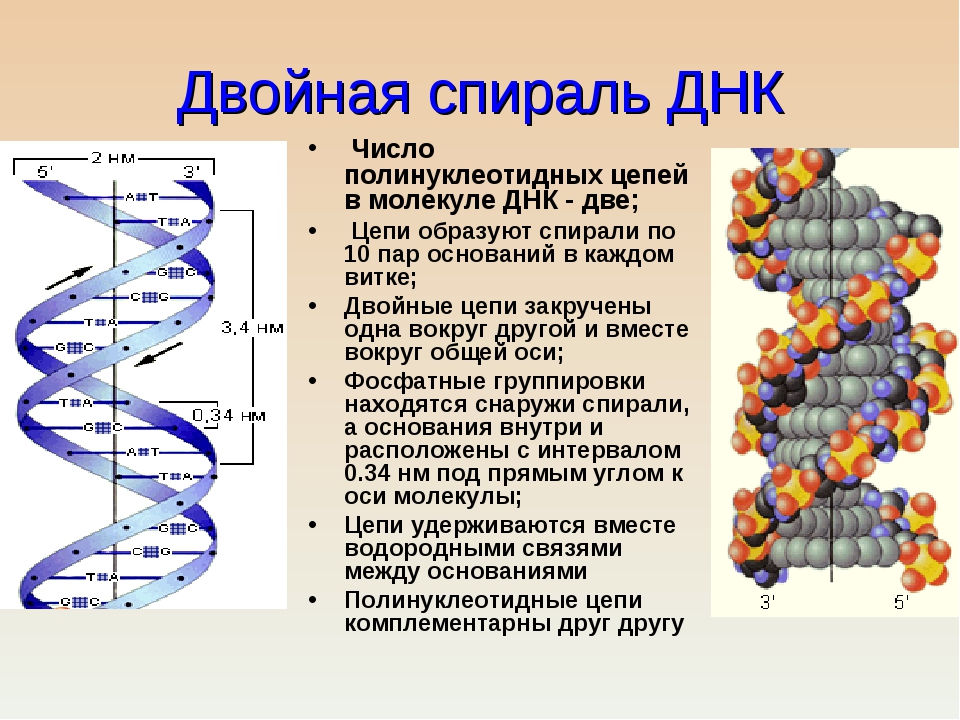
Таким образом, если узнать последовательность пар оснований молекулы ДНК, то можно понять, как происходят химические реакции, наследственность у данного вида организмов, и, в частности, понять, как возникают и развиваются те или иные заболевания. Такую задачу перед собой поставил знаменитый проект «Геном человека», цель которого заключалась в том, чтобы представить в виде карты полную последовательность (геном) ДНК человека.
Почему все оказалось не так однозначно?
«По итогам проекта
“Геном человека” ожидалось, что ученые расшифруют геном и мы поймем, как именно происходят химические реакции в клетке. Но на самом деле все не так просто. Проект предоставил инструмент, который позволяет понимать, что происходит внутри, он стал некой стартовой точкой. Например, после его реализации стало проще и дешевле анализировать другие геномы, чтобы анализировать геном отдельного человека, не нужно все начинать заново, можно использовать референсный геном, полученный в ходе проекта», — рассказывает Алексей Сергушичев, научный сотрудник международной лаборатории «Компьютерные технологии» Университета ИТМО.
Стоит отметить, что различные методы исследования ДНК были известны еще в 80-е годы прошлого века.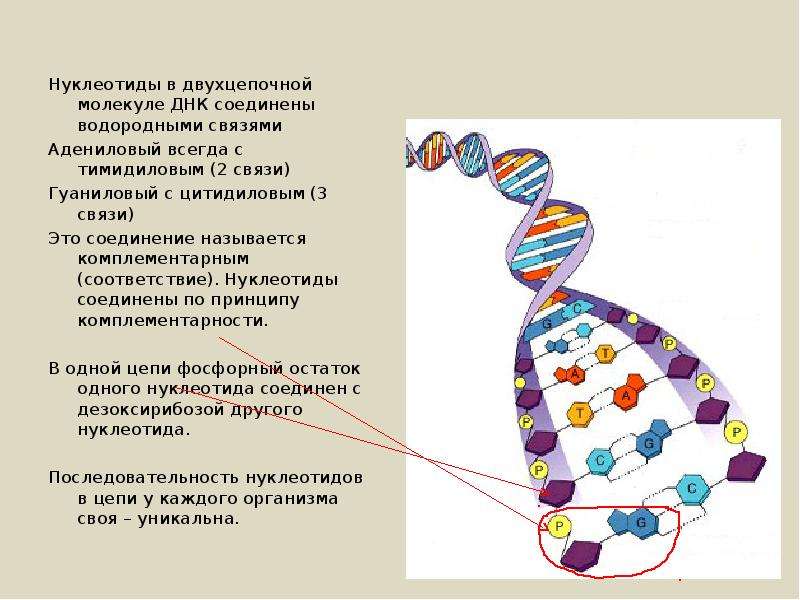 Среди них, например, секвенирование по методу Сэнгера (впервые этот метод секвенирования был предложен Фредериком Сэнгером в 1977 году, за что он был удостоен Нобелевской премии по химии в 1980 году), при котором можно прочитать небольшой фрагмент ДНК. Предложенные ранее методы уже позволяли находить отдельные гены для так называемых менделевских заболеваний — заболеваний, являющихся результатом нарушения работы единичного гена, или таких, которые имеют простую наследственность. Но большинство заболеваний гораздо сложнее и требуют других подходов.
Среди них, например, секвенирование по методу Сэнгера (впервые этот метод секвенирования был предложен Фредериком Сэнгером в 1977 году, за что он был удостоен Нобелевской премии по химии в 1980 году), при котором можно прочитать небольшой фрагмент ДНК. Предложенные ранее методы уже позволяли находить отдельные гены для так называемых менделевских заболеваний — заболеваний, являющихся результатом нарушения работы единичного гена, или таких, которые имеют простую наследственность. Но большинство заболеваний гораздо сложнее и требуют других подходов.
Современные способы генетических исследований: GWAS и поиск редких мутаций
Параллельно с работой «Геном человека» начали разрабатываться так называемые ДНК-микрочипы. Это устройства, созданные по аналогии с микросхемами и предназначенные для одновременного выявления множества определенных последовательностей ДНК. ДНК-микрочип обычно выглядит как отполированная кремниевая пластина, на поверхности которой закреплены специальные ДНК-зонды.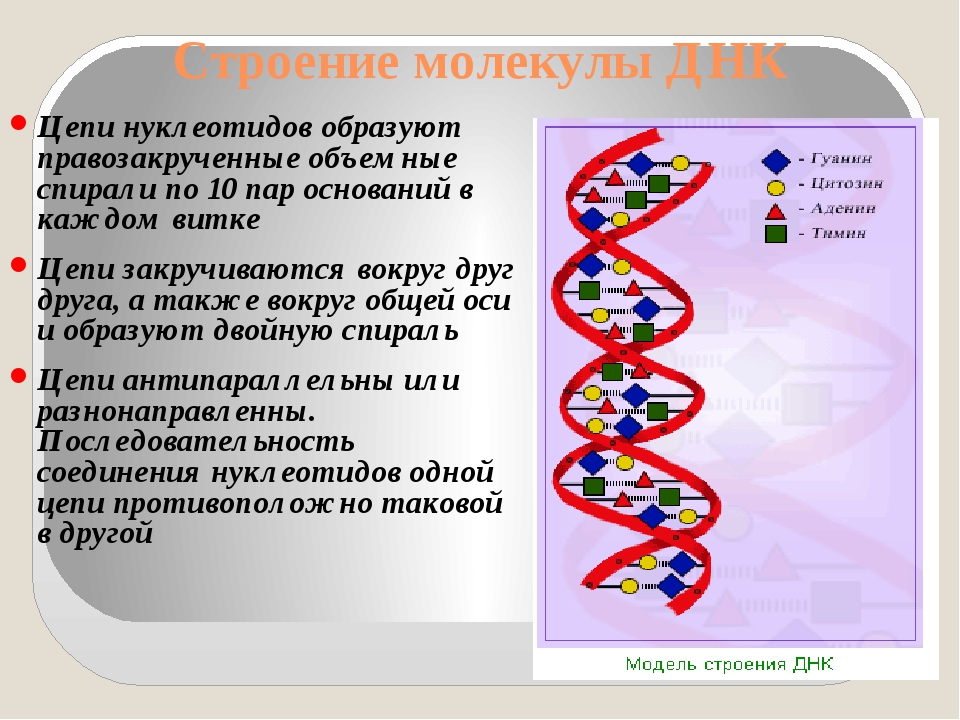 Зонд — это небольшой искусственно синтезированный участок ДНК, который нацелен на выявление одной мутации. На чипах разных производителей может находиться до нескольких миллионов зондов. С помощью такого метода можно посмотреть, есть ли определенные мутации в ДНК конкретного человека или нет.
Зонд — это небольшой искусственно синтезированный участок ДНК, который нацелен на выявление одной мутации. На чипах разных производителей может находиться до нескольких миллионов зондов. С помощью такого метода можно посмотреть, есть ли определенные мутации в ДНК конкретного человека или нет.
Как отмечает Алексей Сергушичев, одним из наиболее прямолинейных методов генетических исследований на сегодняшний момент является полногеномный поиск ассоциаций (GWAS — Genome-wide association studies). GWAS направлен на поиск однонуклеотидных полиморфизмов (различий в последовательности ДНК в один нуклеотид) и связанных с ними фенотипических различий. Сегодня такой метод часто применяется для поиска генетических факторов риска различных заболеваний, но для достоверных выводов требует очень большого количества участников.
«Этот метод построен на следующем принципе: как правило, берется большое количество людей, у которых есть определенное заболевание, а также большое количество здоровых, они сравниваются и, например, обнаруживается, что определенная мутация чуть чаще встречается у больных, чем у здоровых, — говорит Алексей.
— Но проблема в том, что это тест на ассоциации, он ничего не говорит про каузативность, что является настоящей причиной заболевания, он просто показывает, что в определенном участке есть что-то, что как-то действует на болезнь. При GWAS испытуемых можно разделять по больным и здоровым, а кто-то даже пытается таким образом смотреть, от чего зависит IQ. На самом деле можно разделить по любому признаку и попытаться поискать какие-то ассоциации
».
Также он добавляет, что метод работает только на частых мутациях. Если определенная мутация представлена в популяции с большой частотой, значит ее с большой долей вероятности можно найти как среди больных, так и среди здоровых людей, а после за счет разницы между группами испытуемых постараться найти определенные закономерности. С другой стороны, так как таких мутаций в популяции много, эффект от каждой из них в отдельности не очень большой, объясняет Алексей Сергушичев.
Нередко в отчетах компаний, которые делают популярные генетические тесты, можно встретить вывод, что у человека есть определенная мутация, повышающая предрасположенность к какому-то заболеванию, например, в полтора раза.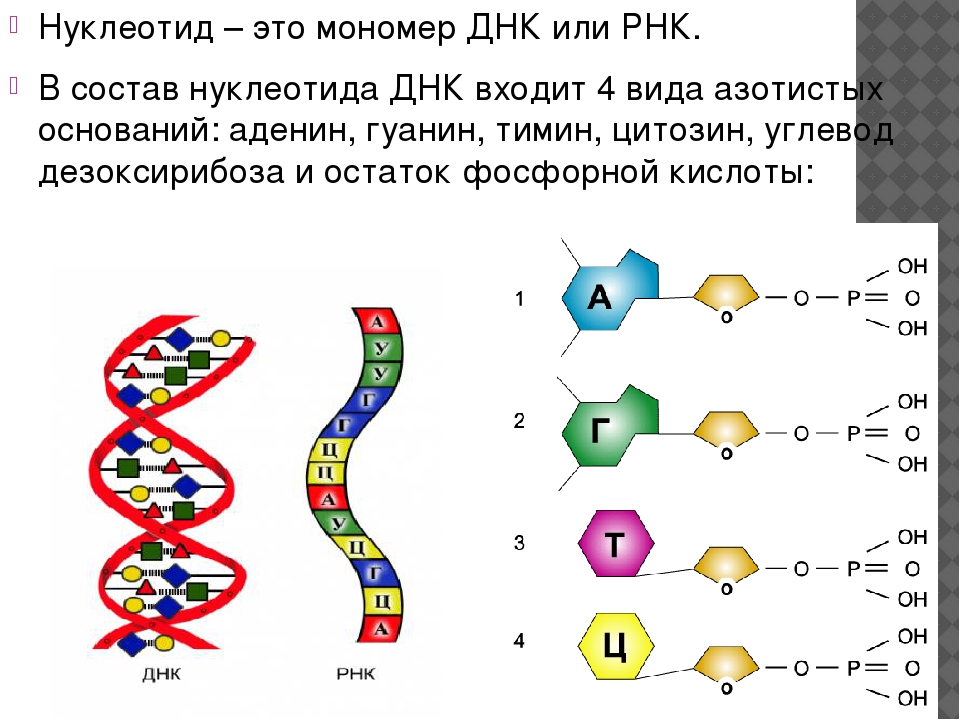 Может показаться, что это много, но на практике обозначать увеличение риска с одного до полутора процентов. В этом случае необходимо учитывать другие факторы, в том числе образ жизни человека, влияние среды и так далее, эффект которых может быть во много раз больше генетической составляющей. Поэтому полагаться только на результаты гентеста некорректно.
Может показаться, что это много, но на практике обозначать увеличение риска с одного до полутора процентов. В этом случае необходимо учитывать другие факторы, в том числе образ жизни человека, влияние среды и так далее, эффект которых может быть во много раз больше генетической составляющей. Поэтому полагаться только на результаты гентеста некорректно.
Другой случай — конкретные гены или мутации, для которых четко доказан эффект. Известный пример — ген BRCA1, который в прессе назвали «геном Джоли». Это произошло после того, как стало известно, что знаменитая голливудская актриса Анджелина Джоли сделала превентивную мастэктомию после обнаружения при секвенировании мутантного гена BRCA1, который передался ей по наследству. Особенности этих мутаций в высокой пенетрантности и аутосомно-доминантном типе наследования. Высокая пенетрантность означает, что они имеют высокую степень проявляемости, то есть наличие мутации с большой вероятностью приводит к заболеванию. Аутосомно-домининантный тип наследования говорит о том, что достаточно мутации лишь в одной из двух копий гена.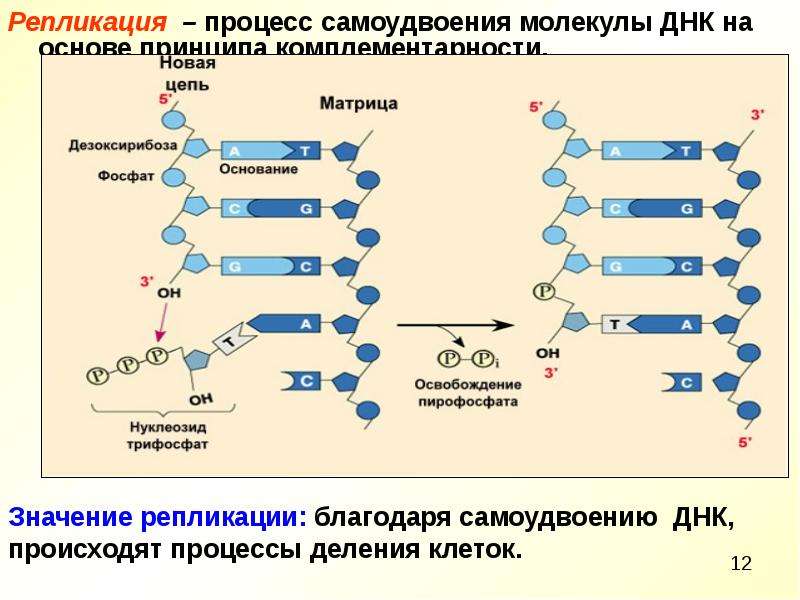
В случае семейной предрасположенности к какому-либо онкологическому заболеванию врачи неслучайно советуют пройти генетическое тестирование, которое поможет определить вероятность развития заболевания. Для ряда онкологических заболеваний уже хорошо известно, какие мутации в гене приводят к их возникновению с большой вероятностью.
Генный банк Китая. Источник: shutterstock.comПоиск редких мутаций
Другой способ генетических исследований — Rare variant association studies, или поиск редких мутаций. Они, напротив, очень редко встречаются в популяции, но зато эффект каждой из них в отдельности достаточно большой.
«Если GWAS делается с помощью ДНК-микрочипов, исследователи измеряют частые мутации и по ним пытаются что-либо проанализировать, при методе Rare variant association studies делается либо полное экзомное секвенирование, либо полное геномное. Экзом — это только та часть, которая кодирует белки. Делать экзомное секвенирование дороже, чем метод микрочипов, образец стоит порядка 1000 долларов, а микрочип — порядка сотни долларов, — говорит Алексей Сергушичев.
— Но при методе поиска редких мутаций, если находится действительно редкая мутация, которой нет у здоровых людей в популяции, а среди больных она встречается значительно чаще, то можно сказать, что она действительно имеет значительный эффект, после чего этот эффект можно изучить уже более детально».
Актуальные исследования
Поиском редких мутаций сегодня занимаются научные группы. Например, такого рода исследования делают и специалисты лаборатории «Компьютерные технологии» совместно с сотрудниками НМИЦ имени В. А. Алмазова, которые секвенируют экзомы для пациентов с врожденными кардиологическими заболеваниями.
Ряд других проектов посвящены изучению механизмов возникновения рака, а также выработке различных способов для эффективной терапии. Например, в одной из работ Алексей Сергушичев в составе исследовательской группы изучал метаболические аспекты онкологических заболеваний и, в частности, на примере рака легких смотрел, как опухоль может жить без глюкозы. В результате исследования ученые показали, что из-за мутации одного из генов при развитии опухоли раковые клетки во время своего развития действительно получают возможность не только использовать в питании глюкозу, но и другие вещества, например, глутамин. Также было доказано, что если этот ген попытаться заблокировать, то удастся стабилизировать развитие опухоли на одном уровне.
В результате исследования ученые показали, что из-за мутации одного из генов при развитии опухоли раковые клетки во время своего развития действительно получают возможность не только использовать в питании глюкозу, но и другие вещества, например, глутамин. Также было доказано, что если этот ген попытаться заблокировать, то удастся стабилизировать развитие опухоли на одном уровне.
Еще одно актуальное направление в области борьбы с онкологическими заболеваниями — иммунотерапия. В прошлом году Нобелевскую премию в области физиологии и медицины получили Джеймс Эллисон из США и Тасуку Хондзё из Японии. Ученые обнаружили два разных чекпоинта — механизма, с помощью которых организм подавляет активность Т-лимфоцитов, иммунных клеток-убийц. Если заблокировать эти механизмы, то Т-лимфоциты «выходят на свободу» и отправляются на битву с раковыми клетками. Это называют иммунотерапией рака, и она уже несколько лет применяется в клиниках.
Исследования ученых Университета ИТМО, которые проводятся совместно с исследователями Университета в Сент-Луисе также посвящены разработке механизмов, которые позволят направить иммунную систему на конкретную опухоль пациента с помощью персонализированной противораковой вакцины.
Потребительская геномика
За последнее десятилетие методы генетического анализа, подходы медицинской генетики и геномики стали доступнее массовому потребителю. Объем совокупного глобального рынка исследований, посвященных геномике, оценивается в десятки миллиардов долларов. Медицинские клиники и стартапы предлагают основанные на генетическом анализе услуги, в России этот рынок также продолжает расти.
ДНК-микрочип. Источник: blog.genotek.ruОдной из популярных услуг в последние годы стали генетические тесты на определение этнической принадлежности. Анализ этнического происхождения производится путем поиска в геноме заказчика генетических маркеров, специфичных для одной из четырех историко-популяционных групп людей. По маркерам определяется процент предков заказчика из конкретного региона. Иными словами, результат анализа показывает соотношение историко-популяционных групп в геноме заказчика.
Однако стоит понимать, что популяционная генетика не имеет никакого отношения к национальностям и современным политическим границам. Здесь идет речь об очень ранних временных отрезках: 150-50 тысяч лет назад. Именно поэтому если ваш результат теста выдаст, например, что ваши предки были на 70% из скандинавских стран, не стоит интерпретировать их с точки зрения современных государственных границ. Результат такого теста выглядит как карта мира без современных политических границ, где очерчен ареал таких же людей с определенной вероятностью. В вашем случае это, скорее всего, будет зона, в которую включены скандинавские страны, Вологодская, Архангельская область России и другие близлежащие территории.
Здесь идет речь об очень ранних временных отрезках: 150-50 тысяч лет назад. Именно поэтому если ваш результат теста выдаст, например, что ваши предки были на 70% из скандинавских стран, не стоит интерпретировать их с точки зрения современных государственных границ. Результат такого теста выглядит как карта мира без современных политических границ, где очерчен ареал таких же людей с определенной вероятностью. В вашем случае это, скорее всего, будет зона, в которую включены скандинавские страны, Вологодская, Архангельская область России и другие близлежащие территории.
Сегодня компании также предлагают потребителям сделать тесты на различные заболевания. Как отмечает Алексей Сергушичев, ряд компаний делают тесты на конкретные заболевания, для тех мутаций, для которых есть очень четкий эффект (например, это уже обозначенные мутации BRCA 1, BRCA 2), также есть много компаний, которые используют метод ДНК-микрочипов, по которым ищут взаимосвязи между мутациями и теми или иными признаками. Он добавляет, что к результатам генетических тестов следует относиться с осторожностью, в большинстве случаев необходимо смотреть на семейную историю, а также на другие факторы.
Он добавляет, что к результатам генетических тестов следует относиться с осторожностью, в большинстве случаев необходимо смотреть на семейную историю, а также на другие факторы.
Результат теста на определение этнической принадлежности: движение предков по отцовской линии. Источник: demo.genotek.ru«Все по-разному научились продавать генетические тесты покупателям. Например, есть даже такие компании, которые готовы сказать про вашего ребенка, есть ли у него способности к спорту или нет. Разумеется, такие вещи плохо воспринимаются научной средой, потому что в таких случаях генетический эффект очень маленький, куда большую роль играет эффект среды — в этом случае количество тренировок и так далее. Кроме того, нужно особо осторожно подходить к подбору научных статей, на которые опираются генетические тесты. Далеко не все из них действительно качественные», — говорит он, добавляя, что с генетическим тестами хорошо работают компании, которые имеют дело с мутациями, высокий эффект которых четко доказан, а также с теми, кто также принимают во внимание семейную историю и другие факторы.
Зачем изучать популяции с точки зрения науки?
Однако изучать популяции интересно не только, чтобы понять, откуда мы «ведем свой род», но и для конкретных научных целей. В последние годы проводится множество исследований, направленных на изучение влияния генетического полиморфизма на эффективность действия лекарств. Есть данные, что некоторые лекарства потенциально имеют генетические особенности выведения из организма, различаются и особенности усвоения препаратов.
В 2008 году Интернациональный исследовательский консорциум объявил о начале проекта «1000 геномов», который заключался в попытке полного секвенирования (расшифровки) геномов по крайней мере тысячи человек по всему земному шару для создания наиболее детальной и применимой в медицинских целях картины генетической вариабельности человеческого генома. Основываясь на результатах генетических экспертиз, проведенных независимыми исследовательскими группами, сформированными из специалистов в разных областях, авторы проекта планировали создать карту генома человека, которая позволит выявить значимые с медицинской точки зрения вариации ДНК.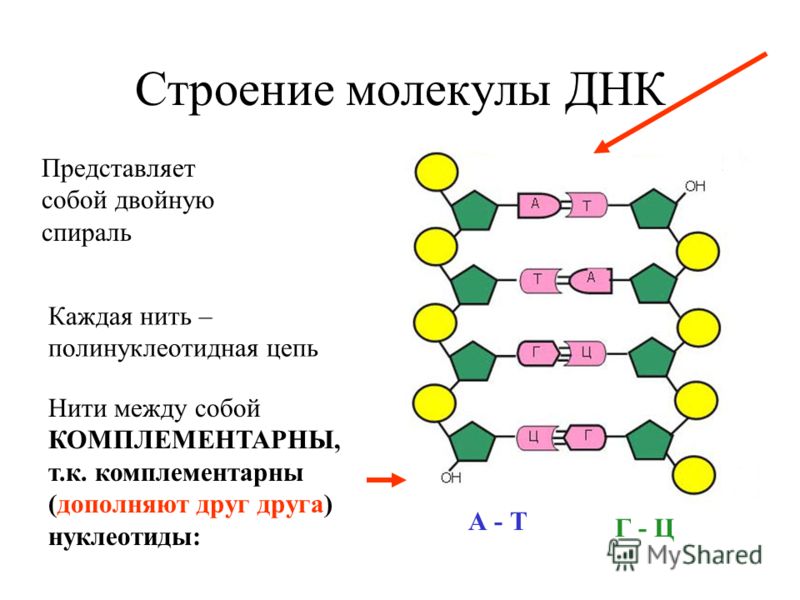
Четыре года спустя старта проекта его авторы опубликовали результаты первого этапа. В них описывались профили редких и распространенных генетических вариаций 1092 человек, относящихся к 14 популяциям в Европе, Африке, Восточной Азии, Северной и Южной Америках. Исследование также показало, что в распределении редких генных вариантов большую роль играет география, то есть этническая принадлежность носителя генома. Профили вариантов варьируют от популяции к популяции.
Генеалогическое древо, связывающее 70 тысяч человек (красным показаны браки). Источник: nplus1.ruВ России реализуется собственный проект «Российские геномы». Его целью является создание открытой базы данных, содержащей анонимную информацию о полногеномных последовательностях по меньшей мере от 3000 мужчин и женщин из разных регионов России (их предки являются коренными жителями данного региона в нескольких поколениях), а также описание вариаций в геноме у этих групп, определение особенностей, влияющих на распространение заболеваний и создание информационной базы медицински-значимых геномных вариантов, характерных для населения России.
С данными проекта «Российские геномы» работала и сотрудница лаборатории «Компьютерные технологии» Екатерина Носкова, которая определяла демографическую историю для жителей Пскова, Новгорода и Якутии.
«Демографическая история — это история развития нескольких популяций, которая включает в себя информацию о том, сколько лет назад эти популяции были одной, сколько лет назад они разделились, какова была численность каждой популяции и как она менялась с течением времени. Если мы говорим о людях, есть популярная модель, которая называется “Выход людей из Африки”. В этой модели участвуют африканцы и евроазиатская популяция, и ставится задача узнать, когда разделились африканская и евроазиатская популяция. С помощью реализации различных методов удается выводить такие истории», — рассказывает она.
По словам Алексея Сергушичева, во многих странах популяционные исследования частично финансируют крупные фармкомпании, в России, где такие проекты находятся полностью на обеспечении государства, такая модель пока не распространена. Во многой причина этому — требования к защите персональных данных. К слову, накануне Роспотребнадзор подготовил законопроект, согласно которому информация, полученная из биологического и генетического материала россиян, должна подлежать защите. Соответствующий документ опубликован на портале нормативно-правовых актов.
Во многой причина этому — требования к защите персональных данных. К слову, накануне Роспотребнадзор подготовил законопроект, согласно которому информация, полученная из биологического и генетического материала россиян, должна подлежать защите. Соответствующий документ опубликован на портале нормативно-правовых актов.
Коронавирус: ученые выявили гены, от которых зависит тяжесть болезни
Автор фото, Science Photo Library
Подпись к фото,До сих пор оставалось загадкой, почему у одних людей коронавирус проходит в легкой форме, а другим требуется госпитализация
Одна из главных загадок пандемии коронавируса заключается в том, что одни люди переносят заболевание практически без симптомов, а другие оказываются в реанимации.
Опубликованные в журнале Nature результаты обследования более чем 2 тыс. пациентов реанимационных отделений показали, что у всех них присутствуют гены, которые могут усугублять симптомы Covid-19.
Это, в свою очередь, может пролить свет на то, где именно происходит сбой в иммунной системе, и помочь подобрать новые методы лечения.
А в таком лечении, как полагает консультант Королевской больницы Эдинбурга профессор Кеннет Бейли, возглавлявший Геномный проект (Genomicc project), необходимость не отпадет даже по мере того, как будут создаваться новые вакцины.
«Вакцины должны резко снизить заболеваемость, однако, скорее всего, врачи во всем мире еще много лет будут лечить больных в отделениях реанимации, так что нужно срочно изыскивать новые методы лечения», — убежден профессор Бейли.
Агрессивные клетки
В ходе исследования ученые изучили ДНК пациентов почти 200 отделений реанимации британских больниц, попавших туда с диагнозом «коронавирус».
Затем геномы эти людей сравнили с геномами здоровых людей с целью выявить возможные различия и нашли несколько. Первым из них оказался ген TYK2.
«Этот ген является частью системы, которая делает ваши иммунные клетки более агрессивными», — объясняет профессор Бейли.
Но если у этого гена имеется дефект, иммунная система может перегреться, и тогда у пациента может начаться сильное воспаление, опасное для легких.
Для сдерживания таких процессов (к примеру, ревматоидного артрита) применяются антивоспалительные лекарства, однако смогут ли они помочь в случае с коронавирусом, можно будет выяснить в ходе масштабных клинических испытаний.
Слишком мало интерферона?
Генетические отличия были также обнаружены в гене DPP9, который играет важную роль при воспалениях, и в гене OAS, препятствующем репликации вируса.
У пациентов отделений реанимации были выявлены и вариации гена IFNAR2, который связан с выработкой интерферона — мощной антивирусной молекулы, которая запускает иммунную систему при первом признаке инфекции.
Считается, что если организм вырабатывает слишком мало интерферона, это дает вирусу преимущество, он успевает быстро размножиться, и это усиливает болезнь.
Интерферон можно прописывать в качестве лечения, однако ВОЗ по результатам клинических испытаний пришла к выводу, что он не помогает больным коронавирусом в особо тяжелой форме.
Тем не менее, как утверждает профессор Университета Рокфеллера в Нью-Йорке Жан-Лоран Казанова, изучавший влияние интерферона, важную роль играет время начала его приема.
«Думаю, если начать принимать его в первые один-два-три-четыре дня с момента заболевания, интерферон будет работать, потому что он даст организму молекулы, которые пациент не в состоянии сам производить», — говорит профессор Казанова.
Когда все становится плохо
По словам генетика из Имперского колледжа Лондона доктора Ванессы Санчо-Шимицу, новые открытия в области генетики позволили детально изучить биологические механизмы заболевания.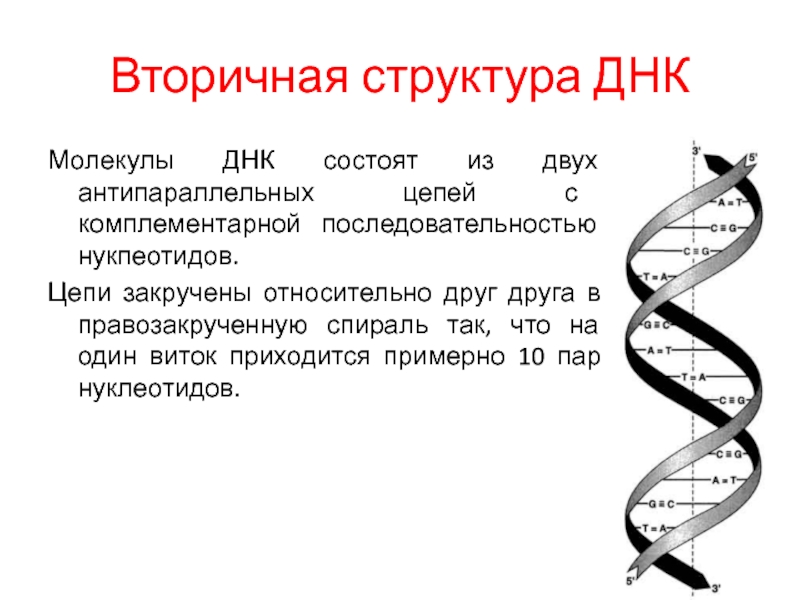
«Это хороший пример сверхточной медицины, когда мы можем определить сам момент, в который что-то в организме пошло не так, — рассказала она в интервью Би-би-си. — Результаты этих генетических исследований помогут нам выявить пути дальнейшего терапевтического вмешательства».
При этом геном не спешит открывать все свои тайны.
Геномный проект и ряд других исследований уже выявили генные кластеры на хромосоме-3, тесно связанные с тяжелыми симптомами заболевания, однако биологическая подоплека этих процессов пока не выяснена.
Поэтому генетики намерены расширить круг пациентов, вовлеченных в исследования.
«Нам интересны все пациенты, но особенно хотелось бы видеть представителей этнических меньшинств, которых непропорционально много среди тяжелобольных, — говорит профессор Бейли. — К тому же срочно требуется найти новые методы лечения этого заболевания, и нам необходимо сделать правильный выбор, что испытывать в первую очередь, потому что у нас нет времени на ошибки».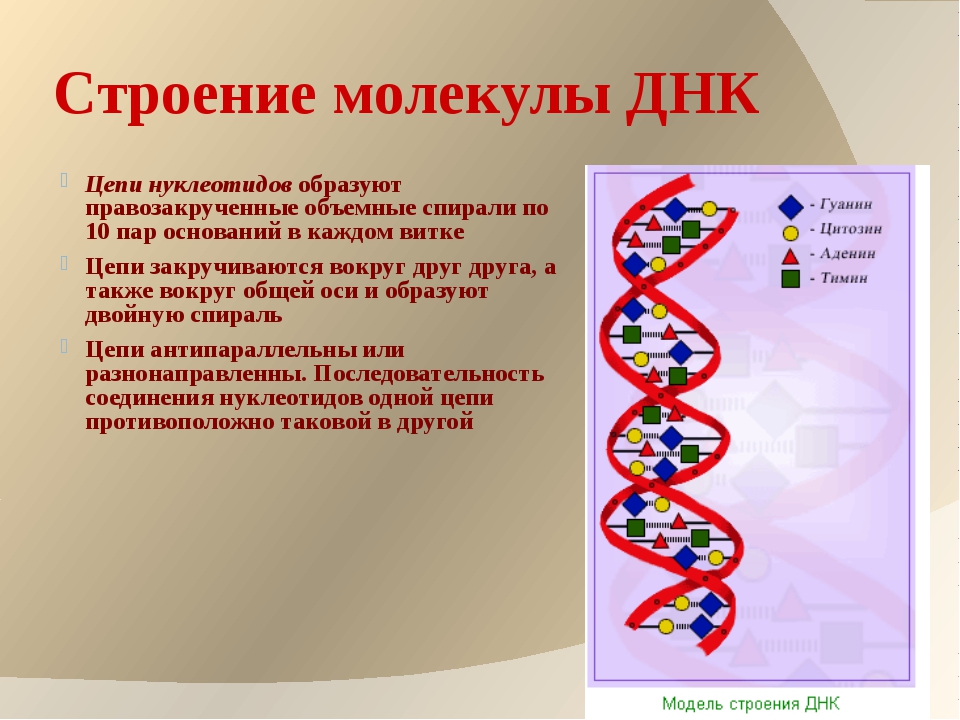
как работают «лекарства для генов»
Мало кто знает, что на основе ДНК и РНК можно сделать лекарства, способные противостоять инфекции и даже исправлять мутации у людей с генетическими заболеваниями. О том, как работают разнообразные методы этой отрасли и какие проблемы в ней только предстоит разрешить, школьникам «Сириуса» рассказал Валентин Власов – доктор биологических наук, академик РАН и научный руководитель Института химической биологии и фундаментальной медицины СО РАН.
Как заставить гены молчать
Нуклеотиды – «буквы» ДНК (дезоксирибонуклеиновой кислоты) и РНК (рибонуклеиновой кислоты), молекул, в которых хранится и передается генетическая информация. Хотя «букв» в этом своеобразном алфавите всего четыре (А, У, Г и Ц в ДНК и А, Т, Г и Ц в РНК), с их помощью можно записать осмысленный «текст» – гены (инструкцию по сборке белков, о которой ученикам недавно рассказывал другой гость, Денис Ребриков). Эта инструкция переписывается с двуцепочечной молекулы ДНК, которая находится в ядрах наших клеток, на одноцепочечную молекулу РНК, и уже с нее синтезируется белок.
Но нуклеотиды не просто служат для записи инструкций по сборке – из их цепочек можно делать лекарства, которые будут разрушать систему синтеза белка у вирусов или бактерий, привязываться к определенным молекулам или даже «чинить» мутации в генах. Лекарства на основе нуклеотидов действуют по относительно легко объяснимому принципу и обычно очень специфичны: на каждую конкретную последовательность можно «натравить» свою цепочку нуклеотидов. Это работает потому, что каждый из четырех типов «букв» может образовать пару с другим. В ДНК две цепи держатся вместе, так как в каждой из них напротив стоят определенные буквы, тянущие друг к другу «руки» химических связей.
Если сделать цепочку нуклеотидов, соответствующую последовательности РНК, которая будет создана с нужного (а точнее – ненужного) гена, то наше лекарство, используя все те же связи между парными буквами, сыграет роль «второй цепи», сделает молекулу похожей на ДНК и заблокирует эту последовательность. С нее не произведется белок, и вред «неправильного» гена будет нейтрализован.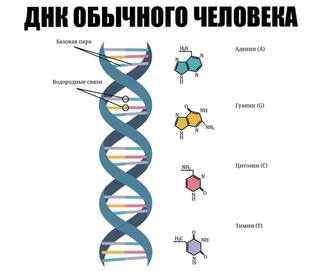 Такие цепочки называют антисенс-РНК (или антисмысловыми РНК), так как они лишают записанный в определенном гене «текст» его «смысла» . При этом по теории вероятности произвольно выбранная последовательность из всего 20 нуклеотидов у человека встретится лишь один раз на весь геном, так что риск ошибки очень невелик.
Такие цепочки называют антисенс-РНК (или антисмысловыми РНК), так как они лишают записанный в определенном гене «текст» его «смысла» . При этом по теории вероятности произвольно выбранная последовательность из всего 20 нуклеотидов у человека встретится лишь один раз на весь геном, так что риск ошибки очень невелик.
Множество разных лекарств на основе нуклеиновых кислот легко одновременно делать на заводе: из одних и тех же типов нуклеотидов строится огромное количество последовательностей. Работать такие лекарства могут по-разному: менять структуру гена, действовать на одну из стадий синтеза белка, на активирование РНК перед этим синтезом и так далее.
Ирония судьбы и нуклеиновый Уроборос
Первая научная публикация на эту тему появилась в 1967 году, а Валентин Власов стал одним из ее соавторов. Вскоре биологи получили письмо из США: некий студент по имени Джон Саммертон поздравлял коллег и сетовал, что самому ему также приходила эта идея, но вот финансирование получить не удалось.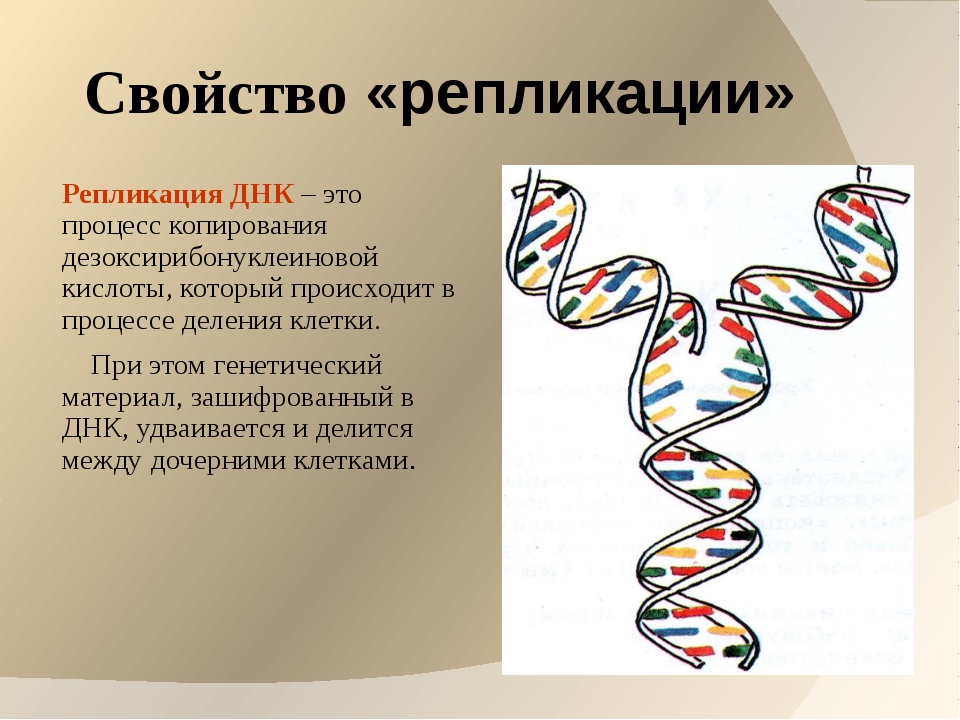 Три десятка лет спустя он откроет морфолино – одну из молекул, при помощи которой можно блокировать синтез определенных белков, – и станет главой крупнейшей компании по производству противовирусных лекарств на основе цепочек нуклеотидов (один из примеров – препарат от вируса Эбола).
Три десятка лет спустя он откроет морфолино – одну из молекул, при помощи которой можно блокировать синтез определенных белков, – и станет главой крупнейшей компании по производству противовирусных лекарств на основе цепочек нуклеотидов (один из примеров – препарат от вируса Эбола).
Некоторые рибонуклеиновые кислоты не просто блокируют РНК, чтобы с нее не мог производиться белок, а разрезают ее – то есть выполняют работу, которую обычно делают ферменты (белки, которые катализируют реакции). Теоретически такие молекулы могли стать основой будущей жизни, катализируя воспроизводство самих себя во времена, когда еще не было ни белков, ни ДНК. Такие многофункциональные рибонуклеиновые кислоты назвали рибозимами – от «рибонуклеиновая кислота» (РНК), и «энзим» (фермент). За открытие рибозимов Сидни Олтмен и Томас Чек получили Нобелевскую премию по химии.
В 1998 году биологи открыли еще один интересный эффект, который назвали РНК-интерференцией. Наша клетка «привыкла» видеть РНК в виде одной цепи.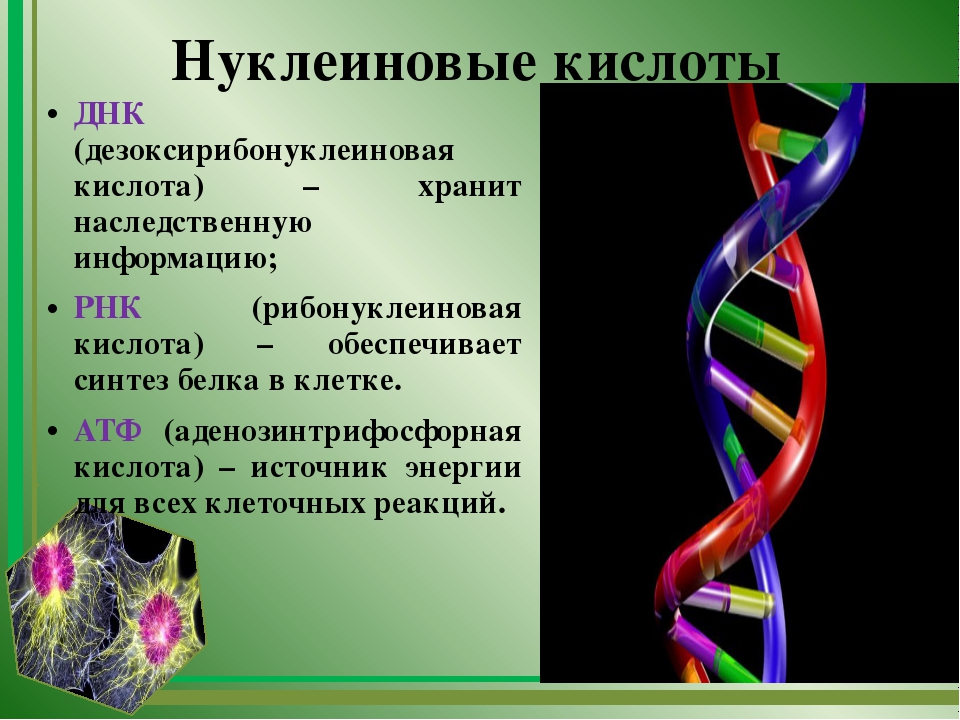 Появление двуцепочечной часто означает вторжение геномных паразитов – вирусов, у которых можно встретить такую причудливую конструкцию. Поэтому такая РНК вызывает немало подозрений, и клетки научились заставлять «молчать» гены, которым она соответствует. Введя в клетку специально подобранную двуцепочечную РНК, можно добиться блокировки определенного гена.
Появление двуцепочечной часто означает вторжение геномных паразитов – вирусов, у которых можно встретить такую причудливую конструкцию. Поэтому такая РНК вызывает немало подозрений, и клетки научились заставлять «молчать» гены, которым она соответствует. Введя в клетку специально подобранную двуцепочечную РНК, можно добиться блокировки определенного гена.
«Генетические ножницы» и путеводные аптамеры
В начале 90-х годов ученые развили технологию, при помощи которой можно получать аптамеры – цепочки нуклеотидов, удивительно точно распознающие определенную «мишень». Такой мишенью может стать белок, который нужно блокировать или просто обнаружить. Чтобы создать аптамеры, достаточно насинтезировать много случайных последовательностей нуклеотидов, а потом предоставить этим цепочкам возможность связаться с мишенью – клюнуть на молекулярную «удочку». Затем молекулы, которые избежали этой участи, отмываются специальным раствором. Этот процесс можно повторить несколько раз. После такого искусственного отбора остаются только те молекулы, которые хорошо привязываются к нужной мишени. Это и есть аптамеры. Их можно размножить при помощи специальной реакции, которая называется ПЦР, и использовать в медицине. К примеру, уже сейчас существуют аптамеры, которые связываются с белками на поверхности клеток рака простаты. Ученые присоединили их к лекарственной молекуле, и теперь она сама может находить свою цель.
После такого искусственного отбора остаются только те молекулы, которые хорошо привязываются к нужной мишени. Это и есть аптамеры. Их можно размножить при помощи специальной реакции, которая называется ПЦР, и использовать в медицине. К примеру, уже сейчас существуют аптамеры, которые связываются с белками на поверхности клеток рака простаты. Ученые присоединили их к лекарственной молекуле, и теперь она сама может находить свою цель.
Еще один знаменитый многообещающий метод, CRISPR/Cas9, ученые подсмотрели у бактерий. У нас в организме есть множество разновидностей иммунных клеток, а бактериальные организмы одноклеточны. Несмотря на это, у них есть собственный иммунитет, позволяющий защищаться от вирусов. Бактерии вносят кусочки ДНК своих врагов в специальную «картотеку», которую хранят в своем геноме. Если тот же вирус появляется в клетке снова и хочет синтезировать белок за ее счет, специальные белки Cas будут узнать его РНК и разрезать ее. Если же в такую «картотеку» вставить нужную нам последовательность, систему CRISPR/Cas9 можно использовать для редактирования генов. Эту систему часто сравнивают с волшебными генетическими ножницами – место разреза можно выбрать довольно точно, так что ее перспективы в редактировании человеческого генома более чем заманчивы. Более того, метод уже применили для излечения генетических заболеваний у первых пациентов.
Эту систему часто сравнивают с волшебными генетическими ножницами – место разреза можно выбрать довольно точно, так что ее перспективы в редактировании человеческого генома более чем заманчивы. Более того, метод уже применили для излечения генетических заболеваний у первых пациентов.
Бдительный иммунитет и светлое будущее
Однажды в экспериментах с мышами, больными энцефалитом, Валентин Власов и его коллеги обнаружили, что иммунный ответ возник не только у мышей, которым ввели специфические для вируса энцефалита последовательности, но и у группы контроля, которой просто вводили случайные цепочки нуклеотидов. Ученые решили, что эксперимент не удался, но позднее другие биологи оказались упорнее и сообразительнее и выяснили, чем вызван этот странный эффект.
«Природа тоже умная и широко использует этот принцип – олигонуклеотиды действуют слишком хорошо, а не просто прилипают. Мы ожидали, что наш олигонуклеотид свяжется и будет мешать синтезу белка. Оказалось, что в клетке есть фермент рибонуклеаза H, который атакует такие комплексы и разрезает их.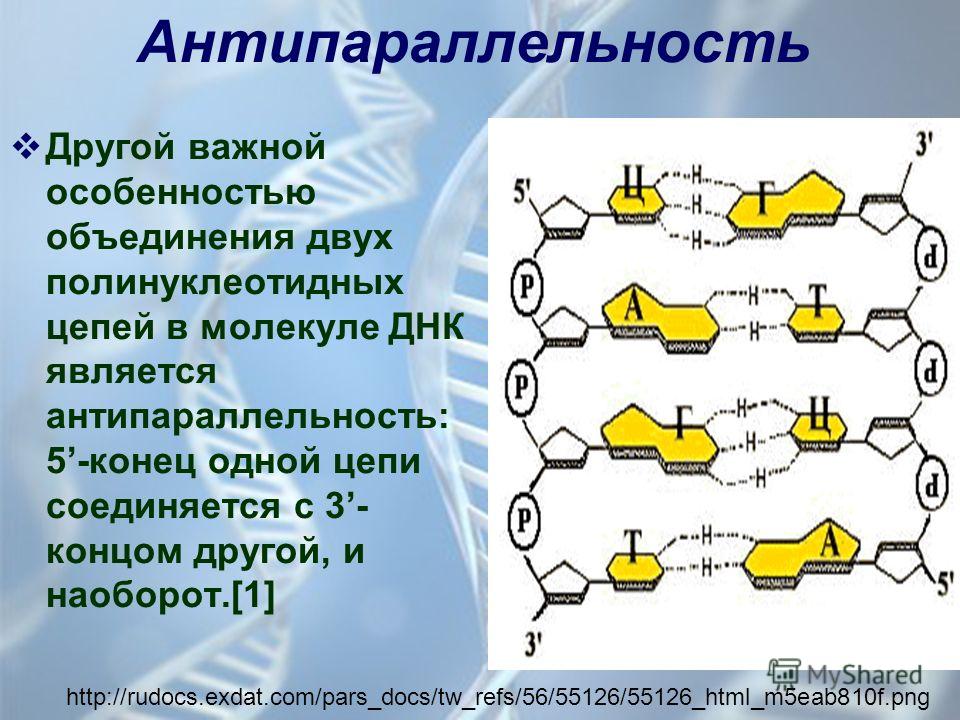 То есть, можно не просто блокировать мишень, а уничтожить ее», – рассказал академик.
То есть, можно не просто блокировать мишень, а уничтожить ее», – рассказал академик.
Так была открыта «нелюбовь» организма к чужим нуклеиновым кислотам. Ученые установили, что наш иммунитет умеет отличать их от «родных» по некоторым признакам. Например, в наших генах на последовательностях Г-Ц висит специальная метка – метильная группа. У бактерий ее нет, поэтому последовательность без метки наша клетка принимает за бактериальную и начинает «воевать» против нее.
Несмотря на такое разнообразие потенциальных лекарств на основе нуклеиновых кислот, до реального применения дошли лишь несколько. Активно внедрять эту группу лекарств в клиническую практику мешают ее недостатки: такие молекулы могут быть беззащитны перед ферментами организма, которые будут стремиться их разрезать, да и клеточная оболочка тоже очень привередливо относится ко всевозможным непрошеным гостям, тем более если они большого размера и тоже заряжены отрицательно, как и она сама (а значит, будут от нее отталкиваться). К тому же, организм большой, и во все клетки сразу лекарство не доставить. Напротив – чаще всего оно требуется только в клетках определенного типа. Поэтому ученые подбирают нуклеиновым кислотам носители (например, золотые наночастицы), химически модифицируют их, привязывают к ним молекулы, которые сыграют роль «системы самонаведения». Решить эти задачи предстоит сегодняшним школьникам – и, возможно, вскоре они увидят широкое применение этой отрасли в медицине.
К тому же, организм большой, и во все клетки сразу лекарство не доставить. Напротив – чаще всего оно требуется только в клетках определенного типа. Поэтому ученые подбирают нуклеиновым кислотам носители (например, золотые наночастицы), химически модифицируют их, привязывают к ним молекулы, которые сыграют роль «системы самонаведения». Решить эти задачи предстоит сегодняшним школьникам – и, возможно, вскоре они увидят широкое применение этой отрасли в медицине.
Панлейкопения кошек (кошачья чумка): симптомы и лечение, вакцина. | Фелиферон
Лечение, как правило, заключается в подавлении вторичной бактериальной инфекции, борьбе с обезвоживанием и восстановлении электролитного баланса. Применение сыворотки в качестве средства этиотропной терапии в большинстве случаев носит решающее значение, однако для поддержания стойкой положительной динамики течения болезни также необходимы средства этиотропной терапии, действие которых заключается в стимуляции клеточного и гуморального иммунного ответа. Наиболее эффективным считается применение интерферонов, которые помимо иммуностимулирующего эффекта обладают также прямым противовирусным и антипролиферативным действием, сочетание которых важно в лечении именно панлейкопении, учитывая тропность вируса к местам быстрого деления клеток. Использование в ветеринарии интерферонов человека имеет значительные ограничения ввиду наработки антител в организме животных на чужеродный интерферон.
Наиболее эффективным считается применение интерферонов, которые помимо иммуностимулирующего эффекта обладают также прямым противовирусным и антипролиферативным действием, сочетание которых важно в лечении именно панлейкопении, учитывая тропность вируса к местам быстрого деления клеток. Использование в ветеринарии интерферонов человека имеет значительные ограничения ввиду наработки антител в организме животных на чужеродный интерферон.
В 2015 году на базе Научно-технологического центра «БиоИнвест» разработан препарат Фелиферон.
Фелиферон — это уникальный видоспецифический интерферон кошки, обладающий противовирусным и иммуностимулирующим действием. Выпускается в форме раствора для инъекций. Применяется в дозе 200-400 тысяч МЕ на одно животное. Дозировка зависит от тяжести состояния.
Механизм действия состоит в подавлении репродукции ДНК- и РНК-содержащих вирусов в инфицированных клетках, повышении резистентности здоровых клеток организма к заражению вирусами, усилении фагоцитарной активности макрофагов и увеличении специфической цитотоксичности лимфоцитов.
Установлено, что при добавлении Фелиферона в схему комплексной терапии панлейкопении у кошек отмечается:
- раннее улучшение клинического состояния в сравнении с животными, не получавшими Фелиферон;
- благоприятное течение заболевания в сравнении с животными, не получавшими Фелиферон;
- раннее клиническое выздоровление (на 2 дня раньше в сравнении с животными, не получавшими Фелиферон).
На основании проведенных клинических исследований рекомендовано использовать препарат Фелиферон в схеме комплексного лечения панлейкопении кошек в дозе 200 000 МЕ внутримышечно, 1 раз в день, курс лечения 5-7 дней, в зависимости от динамики течения заболевания. В тяжелых клинических случаях, на усмотрение ветеринарного врача, препарат Фелиферон может быть назначен в разовой дозе 400 000 МЕ по той же схеме.
Применение препарата Фелиферон не вызывает у животных побочных действий и осложнений.
Подробнее о препарате Фелиферон
Код ДНК: какие тайны скрывает главная молекула
МОСКВА, 25 апр — РИА Новости Крым. Ровно 65 лет назад британские ученые Джеймс Уотсон и Фрэнсис Крик опубликовали статью о расшифровке структуры ДНК, заложив основы новой науки — молекулярной биологии. Это открытие изменило очень многое в жизни человечества. РИА Новости рассказывает о свойствах молекулы ДНК и о том, почему она так важна.
Ровно 65 лет назад британские ученые Джеймс Уотсон и Фрэнсис Крик опубликовали статью о расшифровке структуры ДНК, заложив основы новой науки — молекулярной биологии. Это открытие изменило очень многое в жизни человечества. РИА Новости рассказывает о свойствах молекулы ДНК и о том, почему она так важна.
Весной 1868 года молодой швейцарский врач Фридрих Мишер приехал в Университет города Тюбингена (Германия), чтобы заняться научной работой. Он намеревался узнать, из каких веществ состоит клетка. Для экспериментов выбрал лейкоциты, которые легко получить из гноя.
Отделяя ядро от протоплазмы, белков и жиров, Мишер обнаружил соединение с большим содержанием фосфора. Он назвал эту молекулу нуклеином («нуклеус» на латыни — ядро).
Это соединение проявляло кислотные свойства, поэтому возник термин «нуклеиновая кислота». Его приставка «дезоксирибо» означает, что молекула содержит H-группы и сахара. Потом выяснилось, что на самом деле это соль, но название менять не стали.
В начале XX века ученые уже знали, что нуклеин представляет собой полимер (то есть очень длинную гибкую молекулу из повторяющихся звеньев), звенья сложены четырьмя азотистыми основаниями (аденином, тимином, гуанином и цитозином), а нуклеин содержится в хромосомах — компактных структурах, которые возникают в делящихся клетках. Их способность передавать наследственные признаки продемонстрировал американский генетик Томас Морган в опытах на дрозофилах.
Модель, объяснившая гены
Структура ДНК
А вот что делает в ядре клетки дезоксирибонуклеиновая кислота, сокращенно ДНК, долго не понимали. Считалось, что она играет какую-то структурную роль в хромосомах. Единицам наследственности — генам — приписывали белковую природу. Прорыв совершил американский исследователь Освальд Эвери, опытным путем доказавший, что генетический материал передается от бактерии к бактерии посредством ДНК.
Считалось, что она играет какую-то структурную роль в хромосомах. Единицам наследственности — генам — приписывали белковую природу. Прорыв совершил американский исследователь Освальд Эвери, опытным путем доказавший, что генетический материал передается от бактерии к бактерии посредством ДНК.
Стало ясно, что ДНК нужно изучать. Но как? В то время ученым был доступен только рентген. Чтобы просвечивать им биологические молекулы, их приходилось кристаллизовать, а это сложно. Расшифровкой структуры белковых молекул по рентгенограммам занимались в Кавендишской лаборатории (Кембридж, Великобритания). Работавшие там молодые исследователи Джеймс Уотсон и Френсис Крик не располагали собственными экспериментальными данными по ДНК, поэтому они воспользовались рентгенограммами коллег из Королевского колледжа Мориса Уилкинса и Розалинды Франклин.
Уотсон и Крик предложили модель структуры ДНК, точно соответствующую рентгенограммам: две параллельные цепочки закручены в правую спираль. Каждая цепочка складывается произвольным набором азотистых оснований, нанизанных на остов их сахаров и фосфатов, и удерживается водородными связями, протянутыми между основаниями. Причем аденин соединяется только с тимином, а гуанин — с цитозином. Это правило называют принципом комплементарности.
Причем аденин соединяется только с тимином, а гуанин — с цитозином. Это правило называют принципом комплементарности.
Модель Уотсона и Крика объясняла четыре главных функции ДНК: репликацию генетического материала, его специфику, хранение информации в молекуле и ее способность мутировать.
Ученые опубликовали свое открытие в журнале Nature 25 апреля 1953 года. Через десять лет им вместе с Морисом Уилкинсом присудили Нобелевскую премию по биологии (Розалинда Франклин скончалась в 1958 году от рака в возрасте 37 лет).
«Теперь, более полувека спустя, можно констатировать, что открытие структуры ДНК сыграло в развитии биологии такую же роль, как в физике — открытие атомного ядра. Выяснение строения атома привело к рождению новой, квантовой физики, а открытие строения ДНК привело к рождению новой, молекулярной биологии», — пишет Максим Франк-Каменецкий, выдающийся генетик, исследователь ДНК, автор книги «Самая главная молекула».
Генетический код
Курение вейпов вредит ДНК — ученыеТеперь оставалось узнать, как эта молекула действует. Было известно, что ДНК содержит инструкции для синтеза клеточных белков, которые выполняют всю работу в клетке. Белки — это полимеры, состоящие из повторяющихся наборов (последовательностей) аминокислот. Причем аминокислот — всего двадцать. Виды животных отличаются друг от друга набором белков в клетках, то есть разными последовательностями аминокислот. Генетика утверждала, что эти последовательности задаются генами, которые, как тогда считали, служат первокирпичиками жизни. Но что такое гены, никто в точности не представлял.
Было известно, что ДНК содержит инструкции для синтеза клеточных белков, которые выполняют всю работу в клетке. Белки — это полимеры, состоящие из повторяющихся наборов (последовательностей) аминокислот. Причем аминокислот — всего двадцать. Виды животных отличаются друг от друга набором белков в клетках, то есть разными последовательностями аминокислот. Генетика утверждала, что эти последовательности задаются генами, которые, как тогда считали, служат первокирпичиками жизни. Но что такое гены, никто в точности не представлял.Ясность внес автор теории Большого взрыва физик Георгий Гамов, сотрудник Университета Джорджа Вашингтона (США). Основываясь на модели двухцепочечной спирали ДНК Уотсона и Крика, он предположил, что ген — это участок ДНК, то есть некая последовательность звеньев — нуклеотидов. Поскольку каждый нуклеотид — это одно из четырех азотистых оснований, то нужно просто выяснить, как четыре элемента кодируют двадцать. В этом состояла идея генетического кода.
К началу 1960-х установили, что белки синтезируются из аминокислот в рибосомах — своего рода «фабриках» внутри клетки. Чтобы приступить к синтезу белка, к ДНК приближается фермент, распознает определенный участок в начале гена, синтезирует копию гена в виде маленькой РНК (ее называют матричной), затем уже в рибосоме из аминокислот выращивается белок.
Чтобы приступить к синтезу белка, к ДНК приближается фермент, распознает определенный участок в начале гена, синтезирует копию гена в виде маленькой РНК (ее называют матричной), затем уже в рибосоме из аминокислот выращивается белок.
На этот вопрос ответили Маршалл Ниренберг и Генрих Маттеи из США. В 1961 году они впервые доложили свои результаты на биохимическом конгрессе в Москве. К 1967-му генетический код полностью расшифровали. Он оказался универсальным для всех клеток всех организмов, что имело далеко идущие последствия для науки.
Открытие структуры ДНК и генетического кода полностью переориентировало биологические исследования. То, что у каждого индивида уникальная последовательность ДНК, кардинально изменило криминалистику. Расшифровка генома человека дала антропологам совершенно новый метод изучения эволюции нашего вида. Недавно изобретенный редактор ДНК CRISPR-Cas позволил сильно продвинуть вперед генную инженерию. По всей видимости, в этой молекуле хранится решение и самых злободневных проблем человечества: рака, генетических заболеваний, старения.
То, что у каждого индивида уникальная последовательность ДНК, кардинально изменило криминалистику. Расшифровка генома человека дала антропологам совершенно новый метод изучения эволюции нашего вида. Недавно изобретенный редактор ДНК CRISPR-Cas позволил сильно продвинуть вперед генную инженерию. По всей видимости, в этой молекуле хранится решение и самых злободневных проблем человечества: рака, генетических заболеваний, старения.
Задания уровня В (ДМ 2004)
B1Папоротники относят к царству растений, так как
А) в процессе дыхания они поглощают кислород и выделяют углекислый газ
Б) в процессе фотосинтеза они образуют органические вещества и выделяют в атмосферу кислород
В) их клетки содержат хлоропласты
Г) их клетки содержат цитоплазму
Д) выполняют роль консументов в экосистеме
Е) выполняют роль продуцентов в экосистеме
Ответ: ____________. (Запишите соответствующие буквы в алфавитном порядке.)
B2
Неправильная осанка может привести к
А) смещению и сдавливанию внутренних органов
Б) нарушению кровоснабжения внутренних органов
В) изменению длины плечевого отдела верхних конечностей
Г) нарушению мышечного и связочного аппарата стопы
Д) деформации грудной клетки
Е) увеличению содержания минеральных веществ в костях
Ответ: ____________. (Запишите соответствующие буквы в алфавитном порядке.)
(Запишите соответствующие буквы в алфавитном порядке.)
B3
По каким признакам можно узнать молекулу ДНК?
А) состоит из одной полинуклеотидной нити
Б) состоит из двух полинуклеотидных нитей, закрученных в спираль
В) имеет нуклеотиды А, У, Ц, Г
Г) имеет нуклеотиды А, Т, Ц, Г
Д) является хранителем наследственной информации
Е) передает наследственную информацию из ядра к рибосоме
Ответ: ____________. (Запишите соответствующие буквы в алфавитном порядке.)
B4
Искусственный отбор в отличие от естественного
А) осуществляется человеком
Б) осуществляется природными экологическими факторами
В) происходит среди особей одного сорта, породы
Г) происходит среди особей природных популяций
Д) завершается получением новых культурных форм
Е) завершается возникновением новых видов
Ответ: ____________. (Запишите соответствующие буквы в алфавитном порядке.)
B5
Установите соответствие между особенностями строения животных и группами, к которым их относят в зависимости от вида потребляемой пищи.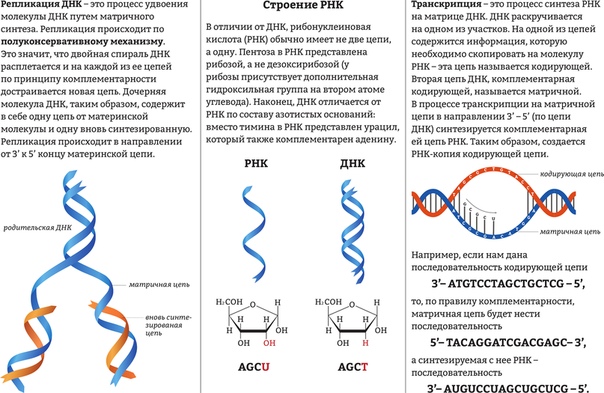
ОСОБЕННОСТИ СТРОЕНИЯ ГРУППЫ ЖИВОТНЫХ
1) хорошо развиты клыки А) растительноядные
2) клыки отсутствуют Б) хищники
3) слепая кишка короткая или редуцирована
4) желудок имеет несколько отделов
5) кишечник во много раз длиннее тела
6) кишечник короткий
1 2 3 4 5 6
B6
Установите соответствие между признаками изменчивости и её видами.
ПРИЗНАКИ ИЗМЕНЧИВОСТИ ИЗМЕНЧИВОСТЬ
1) обусловлена появлением новых сочетаний генов А) мутационная
2) 3) обусловлена изменением генов и хромосом
у потомков появляются новые признаки Б) комбинативная
4) у потомков сочетаются родительские признаки
5) у особей изменяется количество или структура ДНК
6) у особей не изменяется количество или структура ДНК
1 2 3 4 5 6
B7
Установите, в какой последовательности располагаются органы слухового анализатора, через которые звуковые колебания достигают рецепторов органа слуха.
А) наружное ухо
Б) перепонка овального окна
В) слуховые косточки
Г) барабанная перепонка
Д) жидкость в улитке
Е) рецепторы органа слуха
Ответы:
В1 БВЕ
В2 АБД
В3 БГД
В4 АВД
В5 БАБААБ
В6 БААБАБ
В7 АГВБДЕ
Как управлять ДНК – Наука – Коммерсантъ
Наследственная информация любого организма, как известно, хранится в молекуле ДНК. У человека последовательность из четырех букв (оснований ДНК) общей длиной около 3 млрд — геном — несет полную информацию об организме. На основе этой информации он развивается и умеет приспосабливаться к изменяющимся условиям окружающей среды.
Казалось бы, если мы получим доступ к информации, хранящейся в геноме, то сможем узнать все о нашей биологической природе. Неудивительно, что генетики сфокусировали значительные усилия на задаче прочтения ДНК. Благодаря революции в технологиях работы с ДНК конца XX века и созданию новых технологий чтения ДНК в начале XXI века исследователи наконец получили доступ к наследственной информации: в настоящее время любой человек за относительно небольшую сумму может прочитать свою ДНК. Что же он узнает о себе? К сожалению, очень немногое. Проблема в том, что из всего массива генетического текста мы точно понимаем смысл только той части, которая кодирует белки (кодирующей части генов). А она составляет в геноме только несколько процентов.
Что же он узнает о себе? К сожалению, очень немногое. Проблема в том, что из всего массива генетического текста мы точно понимаем смысл только той части, которая кодирует белки (кодирующей части генов). А она составляет в геноме только несколько процентов.
Исследования последних 10–15 лет указывают на то, что значительная доля генома с пока неизвестной функцией, скорее всего, нужна для регуляции работы той самой небольшой доли генов. Таким образом, на десятки тысяч генов человека приходятся сотни тысяч (или, по другим оценкам, миллионы) «управленцев», которые указывают, где и когда нужно работать каждому отдельному гену. Это очень важное явление, которое называется дифференциальной экспрессией (активностью) генов. Дело в том, что все клетки организма содержат одинаковый — совершенно полный — набор генетической информации. Однако клетки очень сильно отличаются, и причина этого в том, что в разных клетках работают разные наборы генов с разной интенсивностью, что в результате и определяет, как устроена клетка и какие функции она выполняет.
Для того чтобы читать информацию, регулирующую работу генов, в клетке имеется большой молекулярный аппарат транскрипции. Транскрипция — первый этап реализации наследственной информации: она переписывается с ДНК на небольшие копии — мРНК. Именно этот этап является ключевым с точки зрения регуляции активности (экспрессии) генов. Специфичные факторы транскрипции способны узнавать регуляторные элементы генома, связываться с ними и затем передавать посредством взаимодействия с другими белками сигнал на нужный ген.
Аппарат транскрипции — это одна из наиболее сложных молекулярных систем клетки: у человека имеется несколько тысяч таких факторов. Их слаженная работа обеспечивает работу всего генома. Факторы стоят на разных уровнях иерархии и выполняют очень разные молекулярные функции. Имеются факторы, которые специфически узнают определенную последовательность букв в ДНК. Другие факторы упаковывают или размечают молекулу ДНК и могут, например, переводить ее в нерабочее, «архивное», состояние. Существуют промежуточные факторы-посредники и т. д. Факторы транскрипции не работают поодиночке, а согласуют работу друг с другом: обычно для запуска одного гена требуется совместное присутствие нескольких десятков (до сотни) факторов.
Существуют промежуточные факторы-посредники и т. д. Факторы транскрипции не работают поодиночке, а согласуют работу друг с другом: обычно для запуска одного гена требуется совместное присутствие нескольких десятков (до сотни) факторов.
Итак, над генами стоит большой, сложно устроенный руководящий орган. С одной стороны, он умеет читать ДНК клетки, с другой — аппарат транскрипции реагирует на сигналы, поступающие в клетку извне. В ответ на поступающие сигналы (например, гормональные) клетка должна реагировать изменением экспрессии определенных генов, а реализуется эта реакция клетки через аппарат транскрипции. Интересно, например, что самый большой аппарат транскрипции — у клеток на ранних стадиях развития организма, когда они еще только выбирают, в какой тип клеток они разовьются. А у клеток, уже достигших зрелости, таких как нейрон или клетка мышцы, обычно происходит «сокращение штатов»: остаются только те, которые обслуживают специфические для этих клеток гены.
Таким образом, значительная часть наследственной информации распознается факторами транскрипции. В последнее время активно изучаются схожие с ними архитектурные факторы, распознающие определенные последовательности в ДНК и формирующие ее пространственную структуру. Вероятно, существуют и другие классы белков, умеющих прочитывать регуляторную информацию генома, которая пока непонятна нам. Важная фундаментальная научная задача — понять, как работает весь этот аппарат.
В последнее время активно изучаются схожие с ними архитектурные факторы, распознающие определенные последовательности в ДНК и формирующие ее пространственную структуру. Вероятно, существуют и другие классы белков, умеющих прочитывать регуляторную информацию генома, которая пока непонятна нам. Важная фундаментальная научная задача — понять, как работает весь этот аппарат.
Это важно также и с практической точки зрения. Прежде всего, нужно вспомнить, что множество болезней вызвано именно тем, что нарушается контроль за работой генов. Это может быть связано с тем, что факторы транскрипции не справляются с работой: они могут быть поломаны, их может быть недостаточно или, наоборот, слишком много. Яркий пример — раковая опухоль: в некоторых клетках происходит бесконтрольная активация генов, нужных для роста и размножения клеток, в результате начинается «бунт» этих клеток против своего организма. Виновные в таком сценарии чаще всего оказываются именно факторы транскрипции, причем имена многих участников уже известны ученым. Другой пример — из современной области стволовых клеток. Если мы будем знать, какие именно факторы транскрипции работают в той или иной ткани, то сможем вырастить в пробирке ткань заданного типа.
Другой пример — из современной области стволовых клеток. Если мы будем знать, какие именно факторы транскрипции работают в той или иной ткани, то сможем вырастить в пробирке ткань заданного типа.
В настоящее время изучение регуляции активности одного-единственного гена и факторов, которые его контролируют,— это большая научная задача. Наверное, нет еще такого гена, про регуляцию которого мы бы знали все. У исследователей, занимающихся механизмами регуляции экспрессии генов, еще много нерешенных задач. В Институте биологии гена РАН в Москве также ведутся исследования в этой области. Мы изучаем факторы транскрипции, которые выполняют разнообразные функции. Например, был найден фактор, который способен объединять две активности: он готовит матрицу ДНК к транскрипции, высвобождая ее из «архивированного» состояния, и одновременно собирает другие белки, которые запускают саму транскрипцию. Так осуществляется эффективный запуск работы генов, которые находятся под контролем этого фактора. Мы показали, что такой сценарий реализуется при действии внешних сигналов (например, некоторых гормонов): изученный фактор привлекается на нужные гены-мишени и запускает их работу.
Мы показали, что такой сценарий реализуется при действии внешних сигналов (например, некоторых гормонов): изученный фактор привлекается на нужные гены-мишени и запускает их работу.
Эти результаты были получены на мушке дрозофиле. Оказалось, что у других организмов, в том числе у позвоночных, есть схожие с ним белки. У мыши такой фактор присутствует в стволовых клетках мозга и важен для того, чтобы они не потеряли этот статус. Таким образом, изучение даже одного фактора транскрипции проводилось в целой серии работ и открыло новые механизмы регуляции активности клеток на уровне молекул и целых клеток. Работы активно продолжаются и, несомненно, мы узнаем еще много нового о том, как функционирует геном.
Работа отдельного гена контролируется несколькими десятками регуляторных элементов, которые могут быть расположены далеко от самого гена по последовательности генетического текста. С каждым элементом и с самим геном связывается целый набор различных факторов транскрипции, которые взаимодействуют друг с другом и с геном и таким образом регулируют его работу.
Юлий Шидловский, Институт биологии гена РАН
| Уотсон и Крик описывают структуру ДНК 1953 Фото: Модель молекулы ДНК В конце девятнадцатого века немецкий биохимик обнаружил, что нуклеиновые кислоты, длинноцепочечные полимеры нуклеотидов, состоят из сахара, фосфорной кислоты и нескольких азотсодержащих оснований. Позже было обнаружено, что сахар в нуклеиновой кислоте может быть рибозой или дезоксирибозой, давая две формы: РНК и ДНК.В 1943 году американец Освальд Эйвери доказал, что ДНК несет генетическую информацию. Он даже предположил, что ДНК может на самом деле быть геном. Большинство людей в то время думали, что ген будет белком, а не нуклеиновой кислотой, но к концу 1940-х годов ДНК была в значительной степени признана генетической молекулой. Ученым все еще нужно было выяснить структуру этой молекулы, чтобы быть уверенным, и понять, как она работает. В 1948 году Линус Полинг обнаружил, что многие белки имеют форму альфа-спирали, закрученной в спираль, как спираль.В 1950 году биохимик Эрвин Чаргафф обнаружил, что расположение азотистых оснований в ДНК широко варьируется, но количество определенных оснований всегда находится в соотношении один к одному. Эти открытия стали важной основой для более позднего описания ДНК. В начале 1950-х годов началась гонка за открытием ДНК. В Кембриджском университете аспирант Фрэнсис Крик и научный сотрудник Джеймс Уотсон (р. 1928) заинтересовались, особенно впечатленные работой Полинга. Тем временем в Королевском колледже в Лондоне Морис Уилкинс (р.1916) и Розалинда Франклин также изучали ДНК. Подход команды Кембриджа заключался в создании физических моделей, чтобы сузить круг возможностей и в конечном итоге создать точную картину молекулы. Команда Кинга применила экспериментальный подход, уделяя особое внимание дифракционным рентгеновским изображениям ДНК. В 1951 году Уотсон посетила лекцию Франклина о своей работе. Франклин, работая в основном в одиночку, обнаружила, что ее дифракция рентгеновских лучей показала, что «влажная» форма ДНК (в более высокой влажности) имела все характеристики спирали.Она подозревала, что вся ДНК была спиральной, но не хотела объявлять об этом открытии, пока у нее не будет достаточных доказательств и по другой форме. Уилкинс был разочарован. В январе 1953 года он показал Уотсон результаты Франклина, очевидно, без ее ведома или согласия. Уотсон и Крик предприняли решающий концептуальный шаг, предположив, что молекула состоит из двух цепочек нуклеотидов, каждая из которых имеет спираль, как обнаружил Франклин, но одна идет вверх, а другая — вниз.Крик только что узнал об открытиях Чаргаффа о парах оснований летом 1952 года. Он добавил это в модель, так что совпадающие пары оснований блокировались в середине двойной спирали, чтобы расстояние между цепями оставалось постоянным. Уотсон и Крик показали, что каждая цепь молекулы ДНК является шаблоном для другой. Во время деления клетки две нити разделяются, и на каждой нити строится новая «вторая половина», как и предыдущая. Таким образом ДНК может воспроизводить себя без изменения своей структуры — за исключением случайных ошибок или мутаций. Конструкция настолько точно соответствовала экспериментальным данным, что была почти сразу принята. Открытие ДНК было названо самой важной биологической работой за последние 100 лет, и область, которую она открыла, может стать научной границей для следующих 100. Связанные функции |
Может ли генетика вызвать депрессию?
Причины депрессии так же сбивают с толку исследователей, как и врачей и специалистов в области психического здоровья, которые ее лечат, и, возможно, больше всего, 300 миллионов человек в мире, у которых она есть.
Генетика может указывать на риск депрессии, но не всегда определяет, разовьется ли у человека это слишком распространенное психическое расстройство. Не существует «причины номер один» депрессии, и еще более сложной является взаимосвязь между генетикой, депрессией и другими известными способствующими факторами.
Если вам сказали, что у вас «ген депрессии», вы можете беспокоиться, что впадете в депрессию. Однако наличие генетической предрасположенности к заболеванию не всегда означает, что вы его заболеете. Это просто означает, что вы можете быть более восприимчивы к нему, чем человек, у которого нет такой же генетической структуры.
Это просто означает, что вы можете быть более восприимчивы к нему, чем человек, у которого нет такой же генетической структуры.
Роль генетики в депрессии
Насколько известно исследователям, именно взаимодействие генов и других факторов (таких как окружающая среда и травма) определяет, развивается ли у кого-то депрессия.
Некоторые исследования показали, что у кого-то, у кого-то из родственников первой степени родства с диагнозом депрессия (родитель, брат, сестра или ребенок) может быть в три раза больше шансов получить диагноз депрессии в течение жизни по сравнению с населением в целом.Взаимодействие с другими людьми
Однако важно отметить, что, хотя исследования показали четкую связь внутри семьи, эти результаты не учитывают тех, у кого депрессия развивается без семейного анамнеза.
Исследования показали, что гены играют роль в потенциальном риске многих состояний здоровья, включая депрессию.
Исследования показали, что депрессия имеет наследственный компонент. Некоторые исследования также показали, что женщины могут быть более восприимчивы к генетическим влияниям, связанным с депрессией, чем мужчины.Взаимодействие с другими людьми
Некоторые исследования также показали, что женщины могут быть более восприимчивы к генетическим влияниям, связанным с депрессией, чем мужчины.Взаимодействие с другими людьми
Понимание генетических вариаций
Наследственность — это сложное взаимодействие многих факторов, а не только отдельных генов. Изучая депрессию или другие состояния здоровья, исследователи часто ищут изменения в генах, которые называются вариантами. Эти изменения классифицируются в соответствии с эффектом (если таковой имеется), который они оказывают на ген.
Цвет глаз — это пример того, как варианты влияют на гены. Изменения в определенных генах, влияющих на выработку меланина, а также в некоторых других генах определяют цвет ваших глаз.Вы наследуете от своих родителей комбинацию генов, каждый со своими уникальными вариантами.
Семьи часто могут предсказать, какого цвета будут глаза у ребенка, посмотрев на родителей и других близких родственников, но варианты могут вести себя неожиданно. Например, у родителей с голубыми глазами может быть ребенок с карими глазами.
Например, у родителей с голубыми глазами может быть ребенок с карими глазами.
Наследственность — сложный процесс даже для такой, казалось бы, простой черты, как цвет глаз. Для таких состояний, как депрессия, исследования еще не определили в полной мере последствия генетических изменений.
Демистификация «гена депрессии»
Наличие генетического варианта может повысить вероятность — но не окончательно — того, что у вас разовьется состояние, связанное с этим вариантом.
Если ген, связанный с определенным заболеванием, изменен, он может с большей (или меньшей) вероятностью способствовать развитию этого состояния. Доброкачественный генетический вариант с меньшей вероятностью влияет на состояние, чем патогенный вариант.
В некоторых случаях исследователи идентифицируют генетический вариант, но не знают, какой эффект он оказывает (если таковой имеется).Эти варианты упоминаются как имеющие «неизвестное значение».
Несколько крупных полногеномных исследований предложили потенциальную генетическую связь с большим депрессивным расстройством. В 2017 году исследователи выявили два новых генетических варианта, связанных с депрессией.
В 2017 году исследователи выявили два новых генетических варианта, связанных с депрессией.
Исследование 2018 года, опубликованное в журнале Nature Genetics , выявило несколько генетических вариантов, которые оказались связаны с симптомами депрессии и, в некоторых случаях, с физическими различиями в мозге.Взаимодействие с другими людьми
Хотя исследование дало ценную информацию о потенциальной наследственности психических заболеваний, ни одно исследование не позволило однозначно идентифицировать единственный ген как причину депрессии.
Ученые полагают, что более вероятно, что все различные гены и генетические варианты вносят небольшой вклад в общий риск человека. Исследования показали, что гены могут передаваться по-разному (способы наследования), что является еще одним фактором, который может повлиять на чью-то генетическую предрасположенность к депрессии.Взаимодействие с другими людьми
Может ли генетика повлиять на лечение психических заболеваний?
Депрессию можно лечить с помощью лекарств, психотерапии и других вмешательств, таких как когнитивно-поведенческая терапия (КПТ). Некоторым людям может быть назначена комбинация лечения.
Некоторым людям может быть назначена комбинация лечения.
Ваши гены могут влиять на эффективность конкретного лечения. Например, исследования показали, что определенные гены могут влиять на то, насколько хорошо ваше тело поглощает, использует и выводит алкоголь и наркотики, включая антидепрессанты.Взаимодействие с другими людьми
Известно, что несколько генов влияют на метаболизм лекарств, но результаты этих исследований представляют интерес в первую очередь для врачей и исследователей.
Хотя некоторые потребительские наборы для геномных тестов предоставляют информацию о таких темах, как метаболизм лекарств, геномное тестирование — это не то же самое, что генетическое тестирование.
Кроме того, врачи и ученые не до конца понимают, насколько полезной может быть эта информация для потребителей. Поговорите со своим врачом, прежде чем использовать информацию о вашем геномном здоровье для принятия решений о вашем медицинском обслуживании, включая лечение депрессии.
Необходимы дополнительные исследования, чтобы понять, что результаты генетических исследований могут означать для антидепрессантов, а также других лекарств, используемых для лечения депрессии.
Помимо генетических факторов, если вам поставили диагноз депрессии и вы пытаетесь выбрать лечение, имейте в виду, что этот процесс может занять время. Возможно, вам придется попробовать несколько видов терапии, прежде чем вы найдете то, что вам подходит. Возможно, со временем вам даже придется скорректировать или изменить свой план лечения.
Перед тем, как начать прием лекарств от депрессии, расскажите своему врачу обо всех лекарствах, витаминах или лечебных травах, которые вы уже принимаете. Эти продукты могут взаимодействовать с антидепрессантами и влиять на их эффективность или даже вызывать серьезные побочные эффекты.
Пробуя разные подходы, оставайтесь на связи со своим врачом и командой психиатров. Обязательно сообщите им, если у вас возникнут побочные эффекты.
Влияет ли наследственность депрессии на детей?
Люди с депрессией могут быть обеспокоены тем, что передадут это заболевание своим детям.Хотя у депрессии может быть наследственный компонент, генетика — не единственный определяющий фактор. Другие факторы способствуют риску, а некоторые могут быть защитными.
Ребенок, один из родителей которого страдает депрессией, может иметь генетическую предрасположенность, но не обязательно впадать в депрессию. Также задействованы другие факторы, включая факторы окружающей среды или «триггеры».
С другой стороны, ребенок, у которого нет члена семьи с депрессией и который не имеет генетической предрасположенности к этому состоянию, может впасть в депрессию, если он подвергнется запускающему событию, например, травме.
Негенетические причины депрессии
Генетика — одна из нескольких потенциальных причин депрессии. Знание возможных причин может помочь вам лучше понять депрессию, но помните, что депрессия может развиться и при отсутствии четкой причины, и ее трудно определить. Другие известные факторы, способствующие возникновению всех форм депрессии и других психических заболеваний, включают:
Другие известные факторы, способствующие возникновению всех форм депрессии и других психических заболеваний, включают:
- Химия мозга: Люди с депрессией иногда имеют более низкий уровень нейротрансмиттеров (химические вещества мозга, которые влияют на настроение и самочувствие).Имеющиеся у них нейротрансмиттеры могут быть неэффективными или плохо работать.
- Изменения в структуре мозга: Мозг людей с депрессией может физически и структурно отличаться от мозга людей, которые не находятся в депрессии.
- Гормоны: Такие состояния, как беременность, заболевания щитовидной железы и менопауза, могут влиять на уровни гормонов. Низкий или высокий уровень гормонов может вызвать симптомы депрессии, особенно у людей с генетической предрасположенностью.
- Экстремальный стресс: Ситуативная депрессия или расстройство адаптации с подавленным настроением может развиться у человека, находящегося в очень стрессовой ситуации или переживающего травму.

Слово Verywell
Наличие генетической предрасположенности к депрессии может усугубить эти факторы и может повлиять на то, когда кто-то впадает в депрессию, а также на то, как долго могут длиться симптомы. Однако важно помнить, что депрессия может развиться у кого угодно, даже у кого-то, кто не предрасположен генетически и не подвержен известным факторам риска.
Выявление признаков депрессии и способность распознавать их в себе и других имеет решающее значение для обеспечения того, чтобы это состояние не оставалось без лечения.
РЕЗЮМЕ | ДНК-технологии в судебной медицине
отпечатков пальцев значительно расширились. Судмедэксперты могут ввести неопознанный шаблон скрытого отпечатка пальца в автоматизированную систему и в течение нескольких минут сравнить его с миллионами шаблонов человека, содержащимися в компьютерном файле.За свою короткую историю автоматизированному анализу отпечатков пальцев удалось раскрыть десятки тысяч преступлений.
Компьютерная технология, необходимая для автоматизированной системы идентификации по отпечатку пальца, сложна и сложна. Отпечатки пальцев представляют собой сложные геометрические узоры, и компьютер должен сохранять, распознавать и искать сложные и изменчивые узоры гребней и мелких деталей в миллионах отпечатков в файле. Несколько коммерчески доступных, но дорогих компьютерных систем используются по всему миру.Напротив, компьютерные технологии, необходимые для банков данных ДНК, относительно просты. Поскольку профили ДНК могут быть сокращены до списка генетических типов (следовательно, списка чисел), в репозиториях профилей ДНК можно использовать относительно простое и недорогое программное и аппаратное обеспечение. Следовательно, требования к компьютеру не должны представлять серьезной проблемы при разработке банков данных профилей ДНК.
Конфиденциальность и безопасность информации, относящейся к ДНК, являются особенно важными и сложными вопросами, потому что мы находимся в разгаре двух выдающихся технологических революций, которые не имеют никаких признаков ослабления: в молекулярной биологии, которая дает взрывной объем информации о генетике человека, и в компьютерных технологиях, которые движутся в сторону национальных и международных сетей, соединяющих растущие информационные ресурсы.
Даже простая информация о личности требует конфиденциальности. Так же, как файлы отпечатков пальцев могут быть использованы не по назначению, информация профиля ДНК может быть использована для поиска и сопоставления банков данных криминального прошлого или банков данных медицинских записей. Хранение информации на компьютере увеличивает вероятность злоупотребления. Например, адреса, номера телефонов, номера социального страхования, кредитные рейтинги, диапазон доходов, демографические категории и информация о хобби в настоящее время доступны для многих наших граждан в различных распределенных компьютеризированных источниках данных.Такие данные могут быть получены напрямую через доступ к конкретным источникам, таким как сервисы кредитного рейтинга, или через раскрытие статистической информации, которая относится к способности пользователя получить оценку желаемой статистики или характеристики из банка данных или коллекции банков данных. . Раскрытие информации может быть достигнуто посредством одного запроса или серии запросов к одному или нескольким банкам данных. С помощью информации ДНК запросы могут быть направлены на получение числовых оценок значений или на определение состояния атрибута человека посредством серии логических (да-нет) запросов к нескольким распределенным банкам данных.
С помощью информации ДНК запросы могут быть направлены на получение числовых оценок значений или на определение состояния атрибута человека посредством серии логических (да-нет) запросов к нескольким распределенным банкам данных.
Несколько частных лабораторий уже предлагают услуги банка ДНК (хранение образцов в морозильных камерах) врачам, генетическим консультантам и, в некоторых случаях, всем, кто платит за эту услугу. Обычно такая информация, как имя, адрес, дата рождения, диагноз, семейный анамнез, имя и адрес врача, а также имя и адрес генетического консультанта хранятся вместе с образцами.
Изменения в генах | Американское онкологическое общество
Генные мутации
Мутации — это аномальные изменения в ДНК гена.Строительные блоки ДНК называются основаниями. Последовательность оснований определяет ген и его функцию. Мутации включают изменения в расположении оснований, составляющих ген. Даже изменение только одной базы среди тысяч оснований, составляющих ген, может иметь серьезный эффект.
Мутация гена может повлиять на клетку разными способами. Некоторые мутации вообще останавливают образование белка. Другие могут изменить произведенный белок так, чтобы он больше не работал так, как должен, или он может даже не работать вообще.Некоторые мутации могут привести к включению гена и выработке большего количества белка, чем обычно. Некоторые мутации не оказывают заметного эффекта, но другие могут привести к заболеванию. Например, определенная мутация в гене гемоглобина вызывает серповидно-клеточную анемию.
Клетки становятся раковыми в основном из-за мутаций в их генах. Часто требуется много мутаций, прежде чем клетка станет раковой. Мутации могут затронуть разные гены, контролирующие рост и деление клеток.Некоторые из этих генов называются генами-супрессорами опухолей. Мутации также могут привести к тому, что некоторые нормальные гены станут вызывающими рак генами, известными как онкогены (онкогены и гены-супрессоры опухолей более подробно обсуждаются позже).
У нас есть 2 копии большинства генов, по одной от каждой хромосомы в паре. Чтобы ген полностью перестал работать и потенциально мог привести к раку, обе копии должны быть «выбиты» мутациями. Это означает, что для большинства генов требуется 2 мутации, чтобы этот ген полностью перестал работать.
Типы мутаций
Существует 2 основных типа генных мутаций, наследуемые и приобретенные:
Унаследованная генная мутация присутствует в яйцеклетке или сперме, из которых сформировался ребенок. После того, как яйцеклетка оплодотворена спермой, она создала одну клетку, называемую зиготой, которая затем разделилась, чтобы создать плод (который стал младенцем). Поскольку все клетки в организме произошли от этой первой клетки, этот вид мутации присутствует в каждой клетке тела (включая некоторые яйцеклетки или сперматозоиды) и поэтому может передаваться следующему поколению.Этот тип мутации также называется зародышевой линии (потому что клетки, которые развиваются в яйцеклетки и сперматозоиды, называются зародышевыми клетками) или наследственной .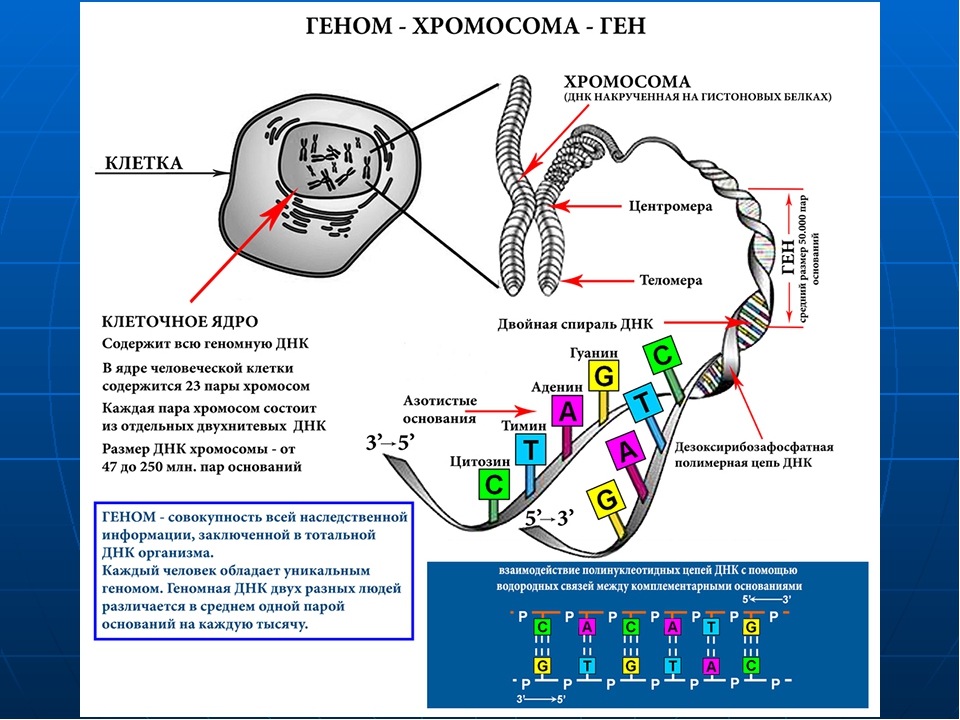 Считается, что унаследованные мутации являются прямой причиной лишь небольшой части случаев рака.
Считается, что унаследованные мутации являются прямой причиной лишь небольшой части случаев рака.
Приобретенная мутация отсутствует в зиготе, но приобретается спустя некоторое время в жизни. Это происходит в одной ячейке, а затем передается любым новым ячейкам, которые являются потомками этой ячейки. Такой мутации нет в яйцеклетке или сперме, из которых сформировался плод, поэтому она не может быть передана следующему поколению.Приобретенные мутации встречаются гораздо чаще, чем наследственные. Большинство видов рака вызвано приобретенными мутациями. Этот тип мутации также называют спорадической, или соматической.
Мутации и рак
Эксперты согласны с тем, что для возникновения рака требуется более одной мутации в клетке. Однако, когда кто-то унаследовал аномальную копию гена, его клетки уже начинают с одной мутации. Это упрощает (и ускоряет) накопление достаточного количества мутаций, чтобы клетка стала раковой.Вот почему унаследованный рак, как правило, возникает раньше в жизни, чем рак того же типа, который не передается по наследству.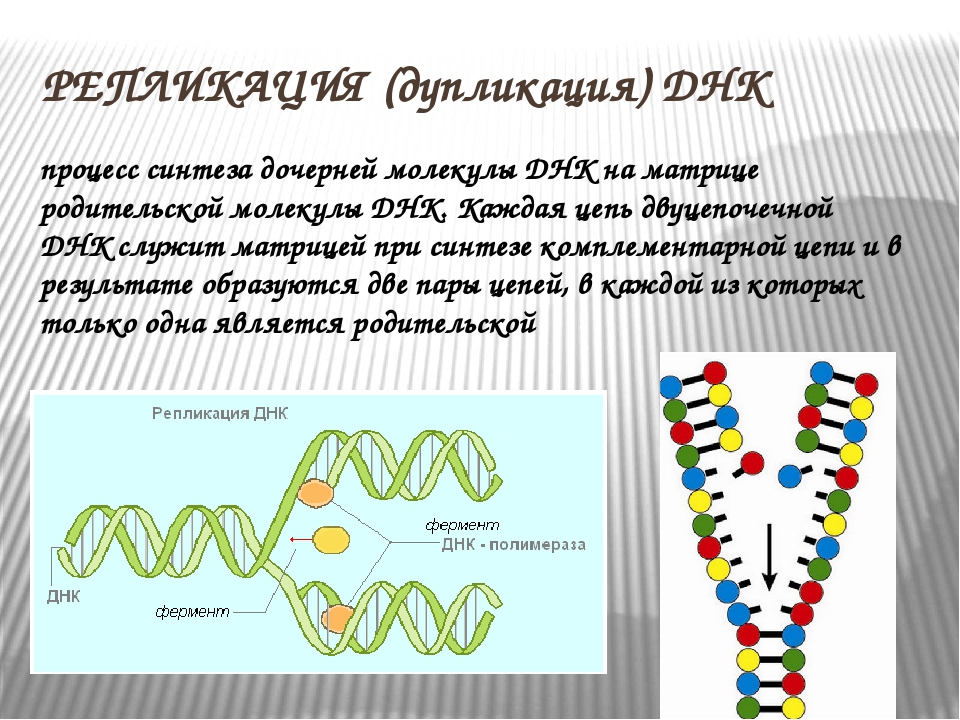
Даже если вы родились со здоровыми генами, некоторые из них могут измениться (мутировать) в течение вашей жизни. Эти приобретенные мутации вызывают большинство случаев рака. Некоторые приобретенные мутации могут быть вызваны факторами, которым мы подвергаемся в окружающей среде, включая сигаретный дым, радиацию, гормоны и диету. Другие мутации не имеют четкой причины и, кажется, происходят случайно по мере деления клеток.Чтобы клетка могла разделиться и образовать 2 новые клетки, она должна скопировать всю свою ДНК. При таком большом количестве ДНК в новой копии иногда допускаются ошибки (например, опечатки). Это приводит к изменениям ДНК (мутациям). Каждый раз, когда клетка делится, это еще одна возможность для мутации. Количество генных мутаций увеличивается со временем, поэтому с возрастом у нас повышается риск рака.
Важно понимать, что генные мутации происходят в наших клетках постоянно. Обычно клетка обнаруживает изменение и ремонтирует его.Если его невозможно восстановить, клетка получит сигнал, сообщающий ей о смерти в процессе, называемом апоптоз . Но если клетка не умирает и мутация не восстанавливается, это может привести к развитию рака у человека. Это более вероятно, если мутация затрагивает ген, участвующий в делении клетки, или ген, который обычно вызывает гибель дефектной клетки.
Но если клетка не умирает и мутация не восстанавливается, это может привести к развитию рака у человека. Это более вероятно, если мутация затрагивает ген, участвующий в делении клетки, или ген, который обычно вызывает гибель дефектной клетки.
У некоторых людей высокий риск развития рака, потому что они унаследовали мутации в определенных генах. Чтобы узнать больше об этом, см. Семейные синдромы рака .
Пенетранс
Для доминантных генов и мутаций термин пенетрантность используется для обозначения доли носителей мутации, у которых будет признак, синдром или заболевание. Если все люди, унаследовавшие мутацию, имеют заболевание, это называется полной пенетрантностью . Если не все люди, у которых есть мутация, заболевают, это называется неполной пенетрантностью . В общем, наследственные мутации, ведущие к раку, имеют неполную пенетрантность, а это означает, что не все с мутацией заболеют раком.Отчасти это связано с тем, что, хотя у человека есть мутация в одной копии гена, ему или ей необходимо приобрести как минимум еще одну мутацию, чтобы ген полностью перестал работать и возник рак.![]() Поскольку не все получают вторую мутацию, не все заболевают раком. Неполная пенетрантность также может быть вызвана тем, что даже если из-за мутации ген не функционирует, для возникновения рака могут потребоваться другие факторы.
Поскольку не все получают вторую мутацию, не все заболевают раком. Неполная пенетрантность также может быть вызвана тем, что даже если из-за мутации ген не функционирует, для возникновения рака могут потребоваться другие факторы.
Высокая проницаемость по сравнению с низкой
Генные мутации могут вызывать большие изменения в функции гена.Они могут даже привести к тому, что эта копия гена вообще перестанет работать. Когда унаследованная мутация оказывает достаточно сильное влияние на функцию гена, чтобы вызвать заболевание или заметную проблему у большинства людей, у которых он есть, эта мутация называется «высокой пенетрантностью».
Мутации с высокой пенетрантностью в генах предрасположенности к раку могут привести к тому, что многие люди в семье заболеют определенными видами рака — семейным раковым синдромом. Считается, что они вызывают лишь небольшую часть случаев рака в семье.Например, считается, что только около 1/5 случаев рака груди, передаваемых в семьях, вызывается мутациями с высокой пенетрантностью в таких генах, как BRCA1 и BRCA2 .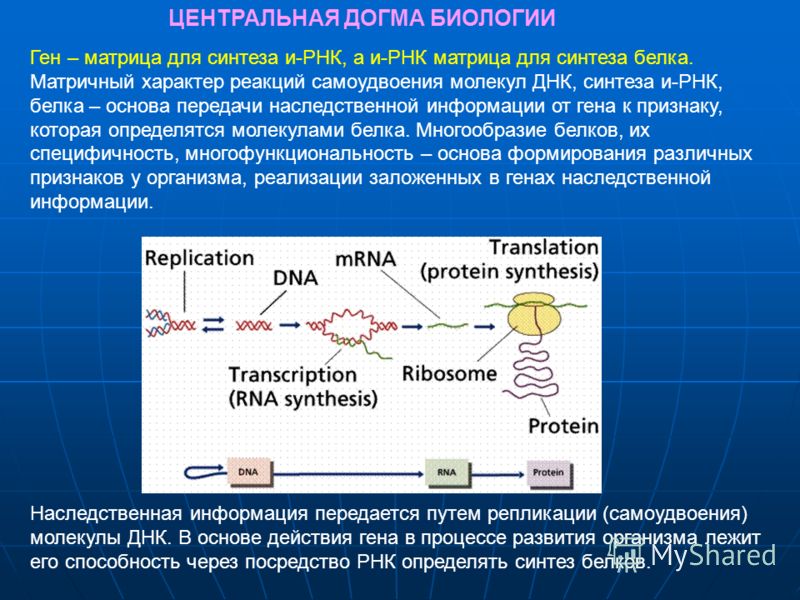
Однако некоторые унаследованные мутации, похоже, не сильно влияют на функцию генов и не часто вызывают очевидные проблемы. Эти мутации называют «низкой пенетрантностью». Мутации с низкой пенетрантностью могут влиять на риск рака за счет тонкого воздействия на такие вещи, как уровень гормонов, метаболизм или другие вещи, которые взаимодействуют с факторами риска рака.Считается, что мутации с низкой пенетрантностью вместе с вариантами генов (обсуждаемыми ниже) ответственны за большую часть риска рака, передаваемого в семьях.
Варианты гена
У людей также могут быть разные версии генов, которые не являются мутациями. Общие различия в генах называются вариантами . Эти версии передаются по наследству и присутствуют в каждой клетке тела. Наиболее распространенный тип варианта гена включает изменение только одного основания (нуклеотида) гена. Они называются однонуклеотидными полиморфизмами (SNP, произносится как «обрезки»).По оценкам, в ДНК каждого человека есть миллионы SNP.
Другие типы вариантов встречаются реже. Многие гены содержат последовательности оснований, которые повторяются снова и снова. Распространенный вариант предполагает изменение количества этих повторов.
Некоторые варианты не оказывают видимого влияния на функцию гена. Другие, как правило, тонко влияют на функцию генов, например, делая их немного более или менее активными. Эти изменения не вызывают напрямую рак, но могут повысить вероятность заболевания раком, влияя на такие факторы, как уровень гормонов и метаболизм.Например, некоторые варианты генов влияют на уровни эстрогена и прогестерона, что может повлиять на риск рака груди и эндометрия. Другие могут влиять на расщепление токсинов в сигаретном дыме, повышая вероятность заболевания раком легких и других видов рака.
Варианты генатакже могут играть роль в заболеваниях, которые влияют на риск рака, таких как диабет и ожирение.
Варианты и мутации с низкой пенетрантностью могут быть похожими. Основное различие между ними заключается в том, насколько они распространены.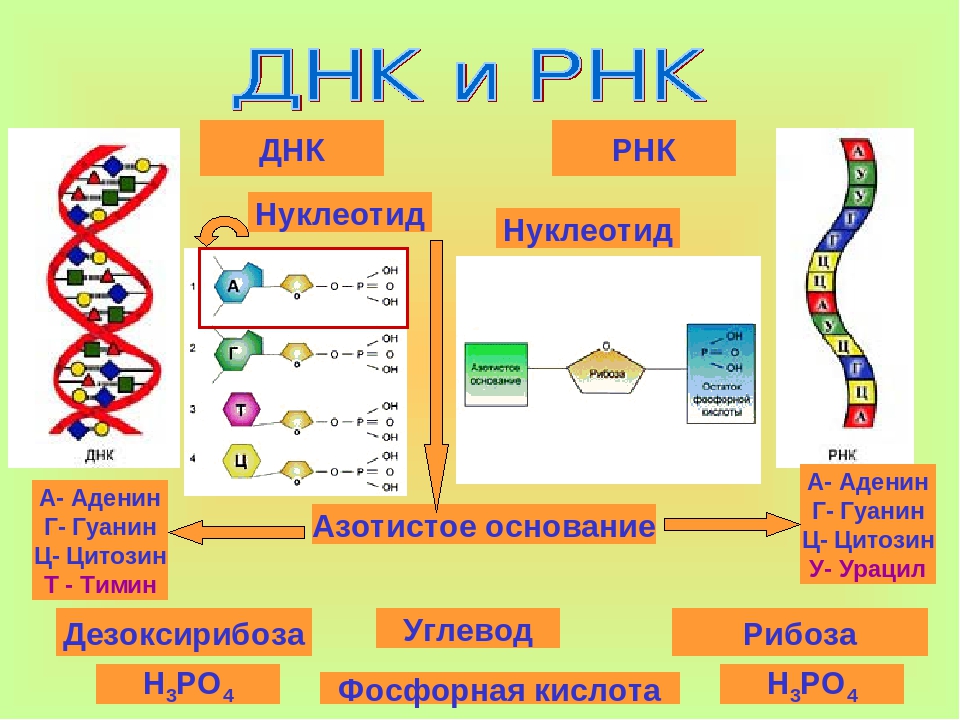 Мутации встречаются редко, а варианты генов встречаются чаще.
Мутации встречаются редко, а варианты генов встречаются чаще.
Тем не менее, поскольку эти варианты распространены и у кого-то их может быть много, их эффект может складываться. Исследования показали, что эти варианты могут влиять на риск рака и, вместе с мутациями с низкой пенетрантностью, они могут составлять большую часть риска рака, присущего семьям.
Другие способы, которыми клетки изменяют гены и активность генов
Хотя все клетки вашего тела содержат одни и те же гены (и ДНК), в одних клетках активны разные гены, чем в других.Даже в пределах определенной клетки некоторые гены в одни моменты активны, а в другие — неактивны. Включение и выключение генов в этом случае основано не на изменениях в последовательности ДНК (например, мутациях), а на других способах, называемых эпигенетическими изменениями .
Метилирование ДНК : В этом типе эпигенетических изменений молекула, называемая метильной группой, присоединяется к определенным нуклеотидам. Это изменяет структуру ДНК, так что ген не может запустить процесс создания белка, который он кодирует (этот процесс называется транскрипцией).Это в основном отключает ген. У некоторых людей с мутацией в одной копии гена предрасположенности к раку другая копия гена становится неактивной не из-за мутации, а из-за метилирования.
Это изменяет структуру ДНК, так что ген не может запустить процесс создания белка, который он кодирует (этот процесс называется транскрипцией).Это в основном отключает ген. У некоторых людей с мутацией в одной копии гена предрасположенности к раку другая копия гена становится неактивной не из-за мутации, а из-за метилирования.
Модификация гистона : Хромосомы состоят из ДНК, обернутой вокруг белков, называемых гистонами. Гистоновые белки можно изменить путем добавления (или вычитания) так называемой ацетильной группы. Добавление ацетильных групп (ацетилирование) может активировать (включить) эту часть хромосомы, в то время как их удаление (деацетилирование) может деактивировать ее (выключить).Метилирование также используется для активации и деактивации частей хромосом. Гистоновые белки также можно изменять путем добавления или вычитания метильных групп (метилирование и деметилирование). Хотя неизвестно, что аномальные модификации гистонов вызывают рак, лекарства, которые изменяют модификации гистонов, могут помочь в лечении рака, включая гены, которые помогают контролировать рост и деление клеток.
РНК-интерференция : РНК (рибонуклеиновая кислота) важна внутри клеток как средний этап, который позволяет генам кодировать белки.Но некоторые малые формы РНК могут мешать экспрессии генов, прикрепляясь к другим частям РНК или даже влияя на гистоны или саму ДНК. Разрабатываются лекарства, которые воздействуют на аномальные гены в раковых клетках посредством РНК-интерференции.
НАСА только что Франкенштейн разработал молекулу ДНК, которая может помочь нам найти инопланетян НАСА только что Франкенштейн разработал молекулу ДНК, которая может помочь нам найти инопланетян
Научная фантастика представляет инопланетян в виде всех, от злобных ксеноморфов до гунганов с утиными лицами (Джар-Джар, это ты?), Но когда дело доходит до фактического обнаружения внеземной жизни в каком-то далеком мире, нам нужно перейти к молекулярным уровень.Нам также может потребоваться перевернуть ДНК с ее пресловутой головы.
Исследования, финансируемые НАСА, теперь показывают, что могут быть альтернативные формы генетического материала.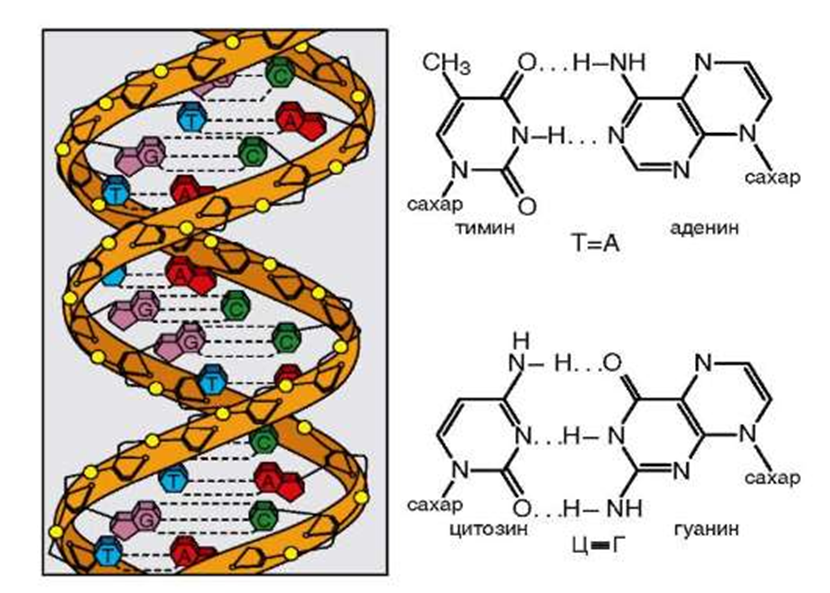 В исследовании, недавно опубликованном в журнале Science Magazine, ученых смогли синтезировать молекулярную систему, способную хранить и передавать информацию. Это может означать, что жизнь, которую мы ищем глубоко в космосе, не обязательно такая, как мы знаем ее на Земле.
В исследовании, недавно опубликованном в журнале Science Magazine, ученых смогли синтезировать молекулярную систему, способную хранить и передавать информацию. Это может означать, что жизнь, которую мы ищем глубоко в космосе, не обязательно такая, как мы знаем ее на Земле.
Хотя это не искусственно созданная форма жизни, она дает нам совершенно иное представление о том, как могут выглядеть ингредиенты для жизни на планетах, на которых земная жизнь никогда не сможет выжить.Модель Gaian того, что якобы необходимо для процветания, узка по сравнению с буквальной вселенной возможностей. Что, если есть жизнь, которая дышит чем-то, что было бы токсично для нас или не нуждалось в воде, чтобы выжить?
«Обнаружение жизни становится все более важной целью миссий НАСА по исследованию планет, и эта новая работа поможет нам разработать эффективные инструменты и эксперименты, которые расширят сферу наших исследований», — сказала Лори Глейз, исполняющая обязанности директора отдела планетологии НАСА.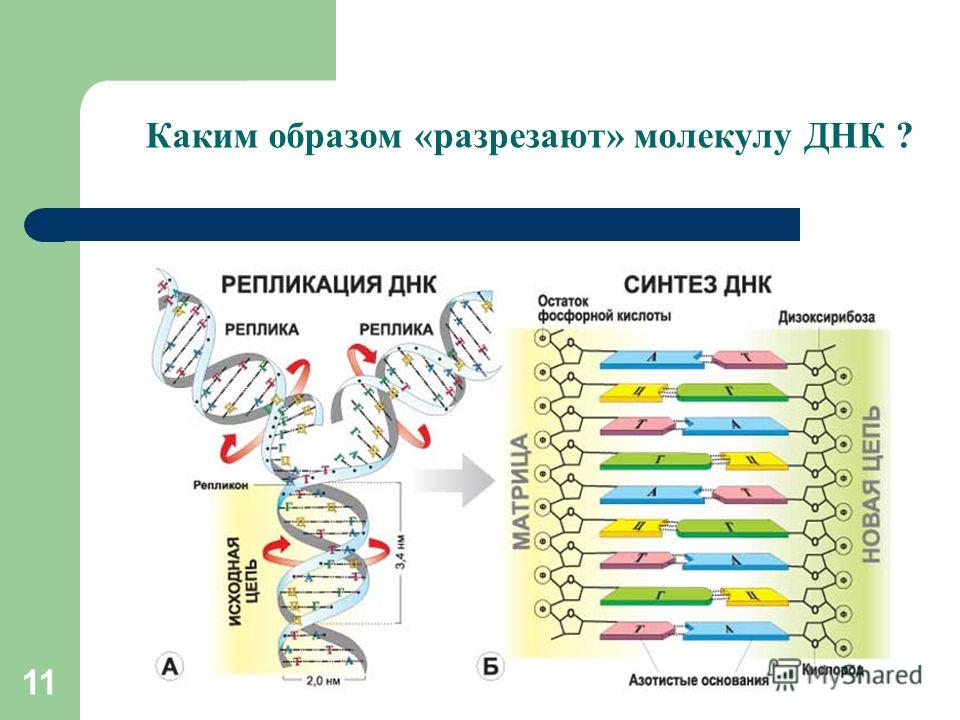 Дивизия.
Дивизия.
Исследовательская группа, стоявшая за этим умопомрачительным исследованием, смогла сфабриковать структуру чужеродной ДНК, которая может дать нам представление о том, как может выглядеть чужеродная ДНК. Он включил четыре нуклеотида, обнаруженных в ДНК Земли — аденин, цитозин, гуанин и тимин — и добавил еще четыре, которые отражают эти структуры, что вдвое увеличило информационные составляющие нашего генетического кода. Это ДНК хатимодзи.
От японских «хачи» (восемь) и «модзи» (буква) ДНК хатимодзи может делать все, что может ДНК Земли.Его структура позволяет передавать, хранить и развивать информацию в живом организме. Возможно, это не идеальное отражение потенциальных альтернативных версий ДНК, существующих на других планетах, но оно может помочь нам распознать их.
«Благодаря тщательному анализу роли формы, размера и структуры в ДНК хатимодзи, эта работа расширяет наше понимание типов молекул, которые могут хранить информацию во внеземной жизни в инопланетных мирах», — сказал руководитель исследования Стивен Беннер, команда которого в Фонде по прикладной молекулярной эволюции в Алачуа, Флорида, сотрудничал с лабораториями Техасского университета и медицинской школы Университета Индианы, а также с программным обеспечением ДНК в Анн-Арборе, штат Мичиган.
НАСА все еще изучает Марс в поисках признаков жизни и рассматривает Европу и Энцелад как потенциальные очаги для инопланетных организмов. ДНК Хатимодзи может помочь нам распознать генетический код, используемый незнакомыми формами жизни, используемыми в экстремальных условиях, таких как подземные океаны этих ледяных лун или ледяная пустыня Красной планеты.
Они действительно там? Может быть, мы наконец узнаем под микроскопом.
(через НАСА)
Палеонтологи спорят, обнаружили ли новые исследования признаки ДНК в окаменелостях динозавров | Умные новости
Около 75 миллионов лет назад на территории современной Монтаны погибло гнездо динозавров, питающихся растениями, под названием Hypacrosaurus stebingeri .Их окаменелости были найдены в 1980-х годах, и теперь международная группа ученых представила доказательства того, что старые кости содержат следы генетического материала.
В статье, опубликованной в National Science Review , подробно рассматриваются осколки черепа, которые у молодых динозавров были сделаны из мягкого хряща, а не из кости. Открытие небольшого размера, но вызывает огромные споры среди палеонтологов: что-то вроде микроскопических клеток, строительных блоков сложной жизни, с темными сгустками посередине.Если посмотреть на одну из возможных темных точек клетки в увеличенном масштабе, можно увидеть то, что, по мнению исследователей, является генетическим материалом.
Открытие небольшого размера, но вызывает огромные споры среди палеонтологов: что-то вроде микроскопических клеток, строительных блоков сложной жизни, с темными сгустками посередине.Если посмотреть на одну из возможных темных точек клетки в увеличенном масштабе, можно увидеть то, что, по мнению исследователей, является генетическим материалом.
Автор исследования Алида Баиллеул, палеонтолог из Китайской академии наук в Пекине, впервые обнаружила микроскопические шары в 2010 году, будучи студенткой Музея Скалистых гор, и быстро обнаружила их сходство с клетками. «Я немного испугалась — отходила от микроскопа, думала, возвращалась к микроскопу», — рассказывает она Майклу Грешко по телефону National Geographic .«Я подумал:« Боже мой, этого не может быть, они больше ничем не могут быть! »
Фотографии предполагаемых клеток во фрагменте черепа птенца. Слева видно, что две клетки делятся, а темная область напоминает ядро клетки, где хранится ДНК.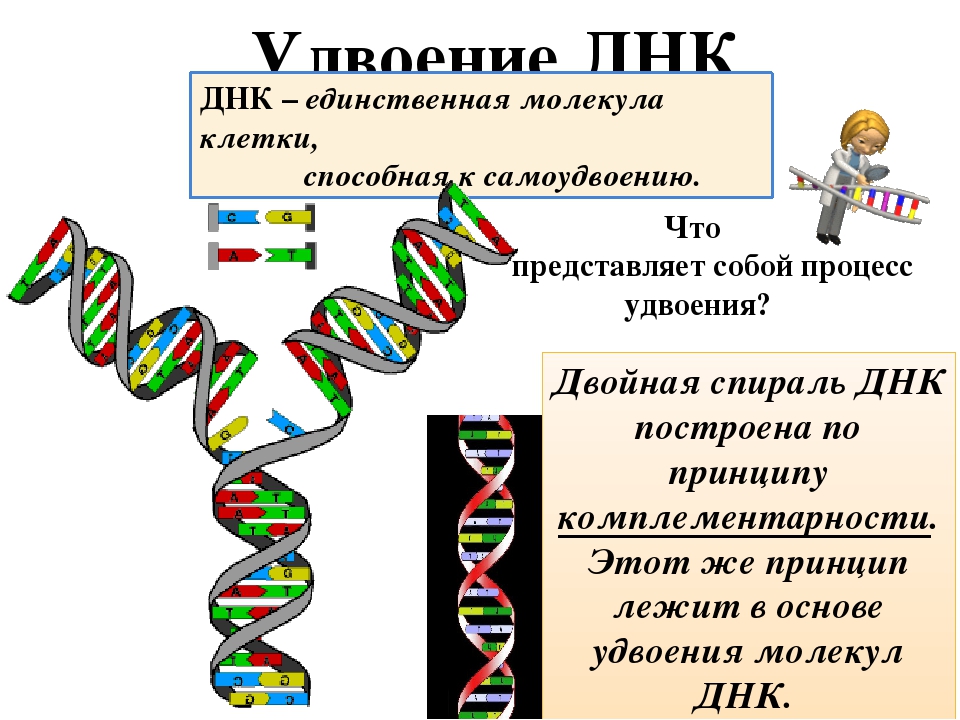 В центре то, что выглядит как нити ДНК. Справа краситель флуоресцирует красным, указывая на химические вещества, такие как ДНК.
(© Science China Press, фото Алиды Байлеул и Вэнься Чжэн)
В центре то, что выглядит как нити ДНК. Справа краситель флуоресцирует красным, указывая на химические вещества, такие как ДНК.
(© Science China Press, фото Алиды Байлеул и Вэнься Чжэн)После получения второго мнения от Мэри Швейцер, палеонтолога из Университета штата Северная Каролина и первого автора статьи, команда приступила к анализу своей находки.Это было удивительно, потому что крошечные структуры, такие как клетки и ДНК — молекулярная витая лестница, несущая в себе план клетки — заведомо хрупкие. Высокая температура или кислотность могут уничтожить их, и поэтому они требуют тщательного ухода, пока животное живо, а когда оно умирает, его нежные кусочки оказываются в прихоти окружающей среды.
Если бы исследователи нашли окаменелые клетки и ДНК, они были бы в несколько десятков раз старше, чем все найденные ранее, и теоретические пределы сохранности материалов, палеонтолог Эван Сайтта, который работает в Центре интегративных исследований в Полевом музее Естествознание в Чикаго, объясняет Джордж Дворски в Gizmodo .
Хрящ лишен пор, поэтому Байль и ее коллеги предполагают, что он мог защищать микроскопические структуры от внешней среды, говорят исследователи.
«Ископаемый, кальцинированный хрящ может быть идеальным местом для поиска исключительно сохранившихся биомолекул в других окаменелостях, поскольку эта ткань может быть менее подвержена загрязнению и внутреннему разложению, чем кость», — сказал палеонтолог Королевского музея Онтарио Дэвид Эванс, который не участвовал в исследовании. Новое исследование, сообщает National Geographic .«В кальцинированном хряще клетки захватываются и изолируются в своей матрице и с большей вероятностью сохраняются в герметичной микросреде».
Чтобы проверить свою находку, исследователи нанесли на окаменелости краситель, который прилипает к ДНК и флуоресцирует красным. Затем они покрасили живые клетки эму и сравнили их. Хотя окаменелость была намного тусклее, чем краска в клетках эму, она к чему-то прилипла.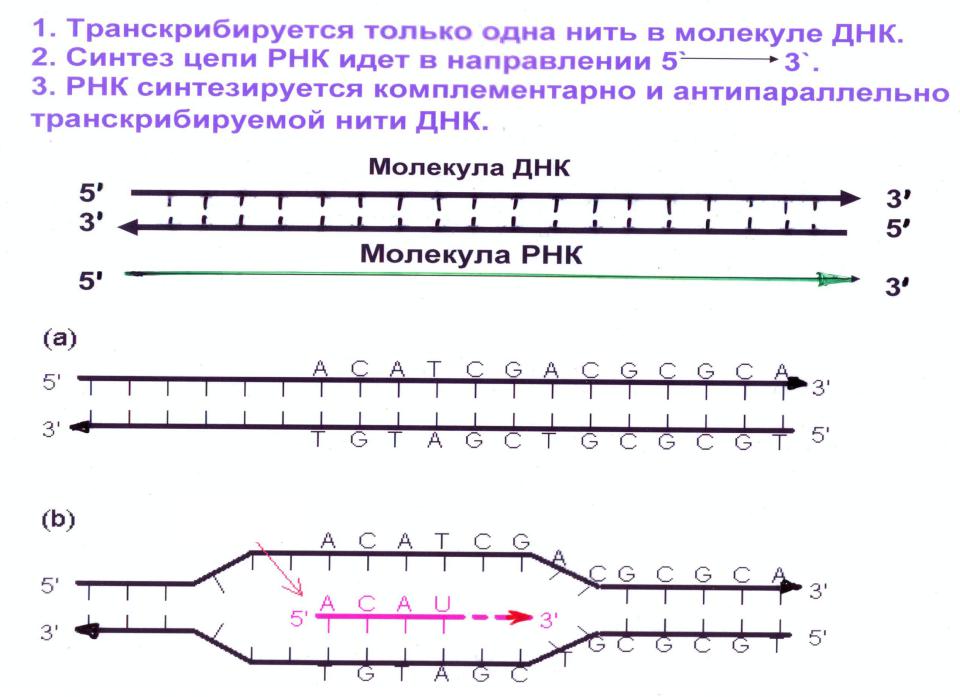
«Я даже не хочу называть это ДНК, потому что осторожен и не хочу преувеличивать результаты», — говорит Швейцер National Geographic .«В этих клетках есть что-то, что химически согласуется с ДНК и реагирует как на нее».
Исследователям пришлось бы извлечь ДНК-подобный материал из окаменелости и попытаться прочитать его химический код, чтобы окончательно подтвердить, действительно ли это ДНК, но, основываясь на их результатах, фрагменты слишком короткие для чтения. Он также мог стать сверхстабильным за счет связывания с самим собой и другими соседними молекулами. Эта реакция называется перекрестным связыванием, сообщает National Geographic.
Скептики, такие как палеонтолог из Бристольского университета Майкл Бентон, не уверены, что то, что обнаружили исследователи, вообще связано с фрагментом черепа. Обращаясь к Conversation , Бентон предполагает, что потенциальная ДНК могла появиться в результате современного заражения. Именно это произошло со многими заявлениями о древней ДНК в 1990-х годах, хотя в этих исследованиях использовалась другая методика тестирования, чем в команде Швейцера.
Именно это произошло со многими заявлениями о древней ДНК в 1990-х годах, хотя в этих исследованиях использовалась другая методика тестирования, чем в команде Швейцера.
Он также указывает, что Швейцер является соавтором нескольких исследований окаменелостей мягких тканей, которые были противоречивыми в их области.Сомнение Саитты также проистекает из того факта, что красители, подобные тем, которые используют исследователи, иногда дают ложные срабатывания, указывая на то, что их цель присутствует, когда на самом деле ее нет, — сказал он Gizmodo.
Швейцер не согласен и сообщает Gizmodo , что скептики «могут говорить все, что хотят», добавив, что «насколько мне известно, [красители] DAPI и PI не связываются ни с какой другой молекулой, кроме ДНК». Если скептики не придумают лучшего объяснения данных, она уверена в выводах своей команды.
«Это исследование все еще находится в зачаточном состоянии», — говорит Эванс National Geographic. «Но возможности абсолютно захватывающие, если мы приостановим наше недоверие, углубимся в данные и продолжим проверять и уточнять наши идеи о сохранении молекул в окаменелостях».
«Но возможности абсолютно захватывающие, если мы приостановим наше недоверие, углубимся в данные и продолжим проверять и уточнять наши идеи о сохранении молекул в окаменелостях».
Высшее образование в области биохимии
Темы:
Структура биологических молекул
Молекулярные взаимодействия
Организация и регулирование молекулярных комплексов
Гены и их экспрессия
Домашняя страница по биохимии для выпускников
Глава 1 — Истоки жизни
Первые признаки жизни ~ 3.5 миллиардов лет назад
Преджизненная атмосфера содержала H 2 O, N 2 , CO 2 , CH 4 , NH 3 и SO 2 .
Молния или ультрафиолетовое излучение могли обеспечить энергия для реакций с образованием простых органических соединений.
Экспериментальная проверка этой гипотезы показала, что
реакции примитивных атмосферных соединений могут привести к образованию аминокислот и
другие общие метаболиты, обнаруженные в современных клетках.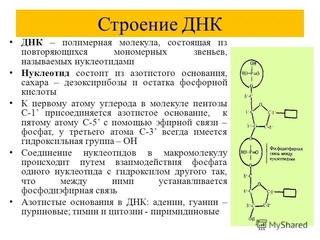
Эти соединения содержат многие функциональные группы необходим для современных биохимических реакций.
Простые органические соединения — сырье на срок химическая эволюция, в которой простые молекулы конденсировались вместе, чтобы сформировать более крупные функциональные блоки.
В какой-то момент могла возникнуть РНК-подобная молекула, которая может управлять собственной репликацией.
Следующий важный шаг: формирование пузырька вокруг самовоспроизводящиеся молекулы.
Заключение самовоспроизводящихся систем в пузырьки формируют первые клетки.
Позволяет ячейке поддерживать высокий местные концентрации необходимых компонентов,
, которые в противном случае могли бы рассеять далеко.
Ранние клетки приобрели способность катализировать реакции синтез необходимых соединений из простых прекурсоров.
Приобрел способность собирать энергию для этих реакций. из своего окружения.
из своего окружения.
Способность ранних клеток синтезировать биологические молекулы, использовать источник энергии и управлять собственной репликацией, что позволило им размножать.
Все организмы произошли от одного общего предка на основе консервативных последовательностей ключевых клеточных компонентов, таких как рибосома.
Современные организмы можно разделить на три царства жизнь:
Бактерии, археи и эукарии
Бактерии и археи:
Обычно группируются в классификация прокариот.
Одноклеточный и относительно простой внутренняя архитектура.
Заключен во внешнюю клеточную мембрану, но отсутствует внутренние мембранные отсеки.
Внутренняя цитоплазма выглядит однако организованы в разные регионы.
Отображение содержимого E.
coli клетка . Обратите внимание
организация ДНК и плотная упаковка содержимого клеток, в частности рибосом,
сайт синтеза белка.
Типовая ячейка: 70% H 2 O
Сухой вес в основном углерод 98% сухого веса состоит из C, N, O, H, Ca, P, K и S.
Eukaryotes состоят из Eukarya
Отличается от прокариот наличием ядра для инкапсулируют ДНК.
Может быть как одноклеточным, так и многоклеточным.
Эукариотические клетки охарактеризованы по органеллярной организации:
Ядро ДНК
Эндоплазматический ретикулум перевод, транслокация, модификация
Гольджи пост-трансляционный модификация
Митохондрии аэробные метаболизм (вероятно, произошел от бактерии)
Завод хлоропластов фотосинтез (вероятно, произошел от бактерии)
Лизосомы и пероксисомы деградационный метаболизм
Cytosol — остальная часть цитоплазма
Глава 3: Нуклеозиды, нуклеотиды и нуклеиновые кислоты
Азотистое основание плоские ароматические гетероциклические производные пурин или пиримидин
Нуклеозиды состоят из азотистого основания, связанного с сахар
(обычно рибоза или дезоксирибоза)
Нуклеотиды представляют собой нуклеозиды, присоединенные по крайней мере к одному фосфату группа
База (X = H) | Нуклеозид (X = рибоза) | Нуклеотид (X = рибозофосфат) | |
пуринов | |||
Аденин Ade A | Аденозин Адо A | Адениловая кислота Аденозинмонофосфат AMP | |
Гуанин Gua G | Гуанозин Guo G | Гуаниловая кислота Монофосфат гуанозина GMP | |
пиримидины | |||
Цитозин Cyt С | Цитидин Cyd С | Цитидиловая кислота Цитидина монофосфат CMP | |
Урацил Ура U | Уридин Urd U | Кислота уридиловая Монофосфат уридина УМП | |
Тимин Thy т | дезокситимидин dThd dT | Дезокситимидиловая кислота дезокситимидин монофосфат dTMP | |
Нуклеотидные сахара обычно представляют собой рибозу или дезоксирибозу
5 Рибонуклеотидный сахар = рибоза | 5 дезокси рибонуклеотид сахар = 2-дезоксирибоза |
Некоторые важные нуклеотиды
H 3 PO 4 + | + H 2 O | |||
Аденозиндифосфат ( ADP ) | Аденозинтрифосфат ( ATP ) |
Аденозинтрифосфат (АТФ):
Большая часть энергии из сотовых метаболизм проходит через АТФ в качестве промежуточного звена
Концентрация АТФ в клетках ~ 5 мМ
Но дневной оборот АТФ составляет общая масса
Энергия гидролиза используется для
вызвать другие реакции.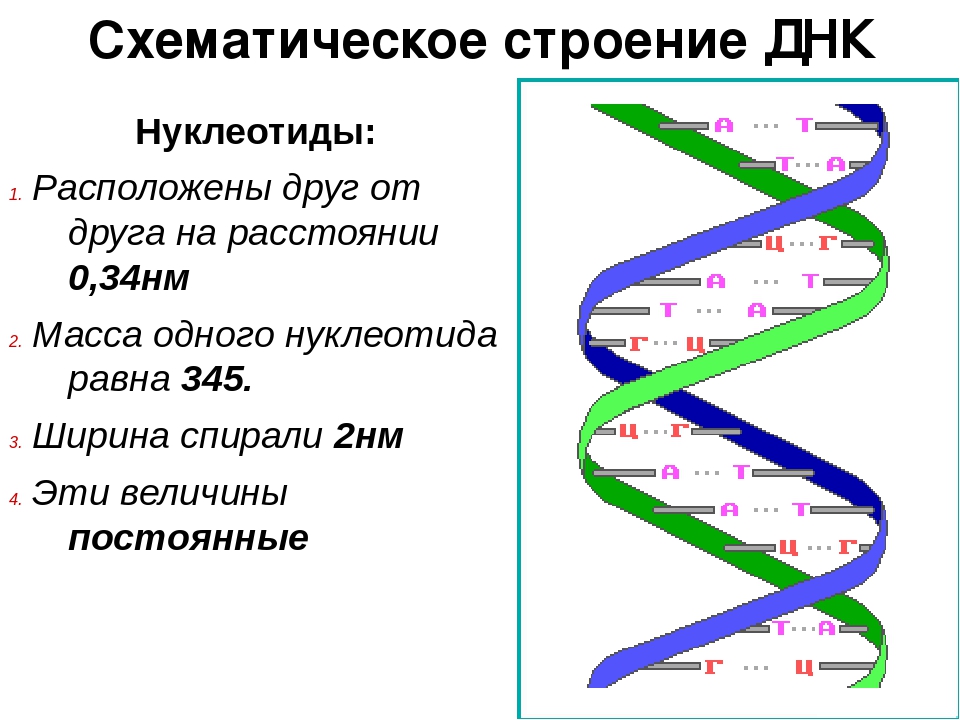
Иногда используется для формирования промежуточное соединение, необходимое для дальнейшего синтеза
Другие важные нуклеотиды и их использование:
Никотинамидадениндинуклеотид — NAD | Флавинадениндинуклеотид — FAD |
NAD + и NADP + может быть обратимо восстановлен с образованием НАДН или НАДФН при окислении-восстановлении реакции (никотинамид из витамина ниацин).
FAD также используется для окислительно-восстановительный (рибофлавиновая часть — витамин B 2 )
Все три действуют как переносчики электронов
Коэнзим A (CoA) — используется в качестве носителя ацильной группы. |
Нуклеиновые кислоты
Фосфодиэфирная связь связывает каждую нуклеотидную единицу с образованием полинуклеотидная цепь
Связь между нуклеотидами обычно составляет от 5 до 3O
Термий 5 и 3 концы
Образует полианион из-за отрицательно заряженного PO 4
Это РНК или ДНК?
Двойная спиральная структура ДНК
Состав основания ДНК:
Правило Чаргаффса: Для любого организма. % A =% T и% G =% C.
Но% G + C может широко варьироваться (25 75%)
Watson and Crick подержанная модель здание для описания структуры ДНК
Разъясненные правила Чаргаффа
Подгонка дифракции волокна измерения ДНК
Характеристики двойной спирали:
Две полинуклеотидные цепи, обернутые вокруг общей оси -> двойная спираль
Нити антипараллельны , но обе правосторонние
баз захоронены в ядре спирали сахарно-фосфатный каркас подвергается воздействию растворителя
Внутренние базы частично доступны через большие и второстепенные пазы двойной спирали
Основания образуют характерные наборы из водородных связей (разделение протона диполями) между дополнительные базы:
Пары A с T, G пары с C
называется дополнительной базой пар
Счета для Chargaffs правила
Размеры генома: |
| |
| Эукария |
| |
Homo sapiens. | 3 127 936 000 | |
Arabidopsis thaliana | 117 950 579 | |
Caenorhabditis elegans | 100 237 364 | |
Schizosaccharomyces pombe | 12 515 111 | |
Saccharomyces cerevisiae | 12 162 624 | |
Бактерии | ||
Escherichia coli К12 | 4 639 221 | |
Haemophilus influenzae Rd | 1,830,138 | |
Mycoplasma genitalium | 580 074 | |
| ||
Methanococcus jannaschii | 1,664,970 | |
Вирусы |
| |
9181 | ||
Вирус обезьяны 40 | 5243 | |
Бактериофаг л | 48502 | |
168 903 | ||
39937 | ||
Предлагаемый механизм репликации ДНК на основе взаимодополняемость баз:
Одна нить может служить шаблоном для синтеза новой копии его дополнения
Полимеры ДНК могут быть огромными.
Общая ДНК клетки — это ее геном
Геномы можно разделить на несколько молекул ( хромосом )
У большинства прокариот есть только одна двухцепочечная копия их геномов на клетку они гаплоид
Большинство эукариот имеют не только гаплоидные клетки,
, но также диплоид клетки, которые имеют по 2 копии каждой двухцепочечной хромосомы
Структура двухцепочечной ДНК относительно не изменяется. последовательностью ДНК
Одноцепочечные ДНК и РНК имеют тенденцию пытаться образовывать пары оснований с другими областями молекулы, которые комплементарны, поэтому структура может различаются для разных последовательностей.
Функция нуклеиновой кислоты
Эйвери, Маклауд и Маккарти
Изолированная ДНК патогенных штамм D. pneumoniae ,
смешал его с непатогенными штамм
Штамм-реципиентбыл преобразован (безвозвратно) в патогенный
ð ДНК является источником генетической информации
Как генетическая информация в ДНК выражается ячейка повлиять на ее поведение?
ДНК управляет транскрипцией информационных РНК ( мРНК )
мРНК транслируется в белок на рибосоме путем связывания оснований с аминоацил-тРНК
Центральная догма: ДНК-> РНК-> белок | Трансляция мРНК в белок |
изменение может повлиять на последовательность мРНК
, который, в свою очередь, может изменять последовательность белка.
Белки выполняют многие химические и структурные функции клетки, прямо или косвенно.
Большинство ферментов (биологических катализаторов) в клетке белки, но некоторые из них состоят из РНК.
Краткое введение в рекомбинантную ДНК (клонирование ДНК)
Ключ к клонированию — система рестрикции-модификации бактерий
Большинство бактерий могут связывать и поглощают ДНК из окружающей среды — трансформация
Вероятно, адаптация, позволяющая люди приобретают вариантные гены от других представителей своего вида.
Но если ДНК от другого видов, может нанести ущерб регуляции экспрессии генов.
Бактерии обладают биохимическим система, которая позволяет им получать ДНК своего вида, но не из прочие — Система ограничения-модификации .
Каждый вид (или штамм) бактерии имеют особую пару ферментов:
Сайт-специфическая ДНК-метилаза (добавляет группу CH 3 — к определенному типу нуклеотида)
и эндонуклеаза, разрезающая
ДНК, не метилированная при этом сайт.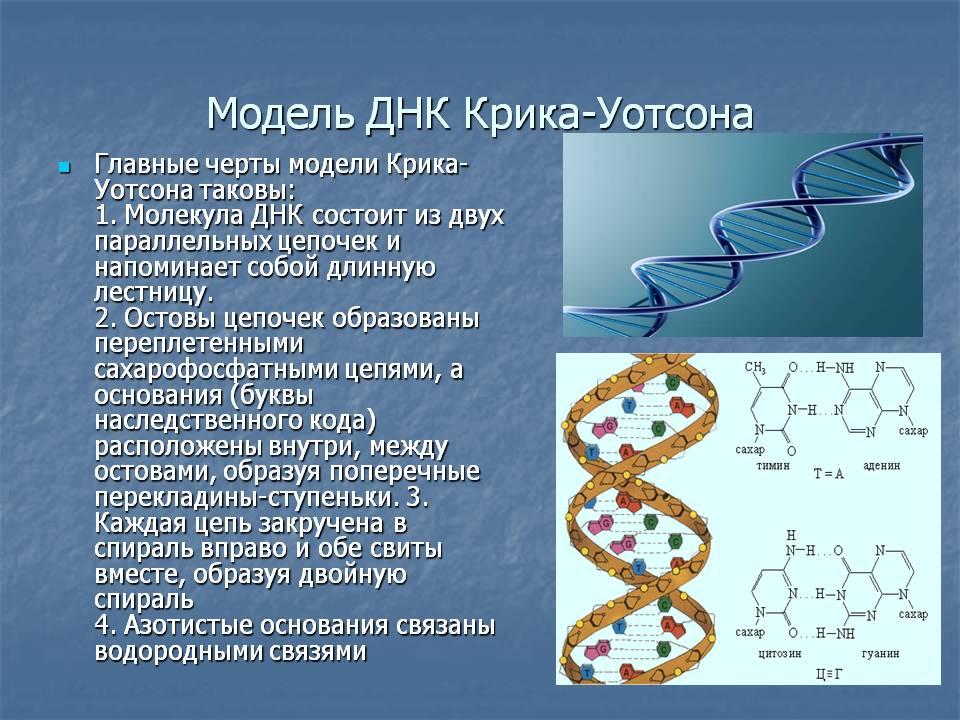
( Endo разрезает нуклеазой внутри цепи ДНК [или РНК]
Нуклеаза Exo удаляет нуклеотиды с концов)
Эндонуклеазы рестрикции имеют очищено от сотен разных видов
Самые известные палиндромные последовательности (последовательности, которые выглядят одинаково на любой цепи с любого направления)
Например.
Бактериальный штамм | Эндо. | Участок |
|
E. coli R | EcoR I | 5 ‘GAATTC 3’ 3 ‘CTTAAG 5’ | разрезает 3 фута из G оставляет 5 ‘свес |
H. | HindIII | 5 ‘AAGCTT 3’ 3 ‘TTCGAA 5’ | отрезки 3 фута 1-го A оставляет 5 ‘свес |
H.Эгипт | HaeII | 5 ‘RGCGCY 3’ 3 ‘YCGCGR 5’ | отрезает 3 фута последнего C листья 3 ‘свес |
Используется разными способами в ДНК клонирование, особенно для разрезания векторной ДНК и гена, представляющего интерес для гена сплайсинга в вектор:
«липкие концы» от EcoRI-разрез одного фрагмента может образовывать пары оснований из другого
фрагмент изолята со вставкой из геля отжигают липкие концы с плазмидной ДНК и лигируют с ДНК-лигазой.
ДНК-лигаза — Фермент репарации ДНК
восстанавливает разрывы в позвоночнике ДНК
Требуется высокоэнергетический кофактор.
Обычно используют фермент из фага Т4, который может лигировать тупые или липкие концы (использует АТФ).
Фермент E. coli требует НАД + вместо АТФ и только восстанавливает липкие концы.
Плазмиды
автономно копирующий круговой минихромосомы
наиболее производные от лекарственно-устойчивых бактерии
имеют начало репликации для амплификация ДНК и маркерного гена для отбора клеток, несущих его
Автоматическое секвенирование ДНК:
После клонирования ДНК можно секвенирование химическими или ферментативными методами.Химический метод все еще используется для экспериментов со следами, но практически все выполняется с использованием ДНК-полимеразы и обрывающих цепь нуклеотидов.
Реакция ферментативного секвенирования
Отжиг (гибридизация) одиночный
цепь оцДНК к специфическому олигонуклеотиду , праймеру (комплементарна последовательности фланкирующего вектора или известной последовательности
внутри вставки ДНК). Олигонуклеотид служит праймером для синтеза
ДНК с помощью ДНК-полимеразы с использованием плазмиды в качестве матрицы.
Олигонуклеотид служит праймером для синтеза
ДНК с помощью ДНК-полимеразы с использованием плазмиды в качестве матрицы.
Обычно немаркированный олигонуклеотид плюс все 4 дезоксинуклеотидтрифосфата (dNTPS)
Plus смесь разных 2′-3′- дидезоксинуклеотид трифосфат (ddNTP), к каждому из которых прикреплена характерная флуоресцентная метка.
ddNTP могут быть включены полимераза, но вызывает остановку синтеза цепи,
, так как у них нет свободных 3′-OH служить акцептором 5 ‘PO 4 в реакции полимеризации.
Таким образом, когда ddNTP включены в продукт ДНК, цепь ДНК не может быть удлинена и в то же время добавляется специальная цветная этикетка.
продуктов ДНК денатурированы (отделены от шаблона), а товары разделяются по размеру электрофорезом на полиакриламидном геле или капиллярной трубке.
Поскольку образцы выходят из
на дне геля для секвенирования они обнаруживаются с помощью лазерной флуориметрии и
автоматически записывается.
: обычно термостабильные полимеразы и цикл секвенирование аналогично ПЦР.
Автоматическое секвенирование геномов человека и других модельных организмов революционизирует способ молекулярной биология сделана. Другой игрок в этой революции — полимеразная цепочка. Реакция
Полимеразная цепная реакция (ПЦР)
ПЦР — это амплификация специфический фрагмент ДНК in vitro , направленный с помощью пары олигонуклеотидов для первичного синтеза ДНК в области между праймерами с помощью ДНК-полимеразы.
Последовательные раунды ДНК Синтез осуществляется путем предварительного нагрева матричной ДНК и праймеров до 94 до денатурировать шаблон (отдельный пряди),
охлаждение примерно до 50 до позволяют праймерам отжигаться (пара оснований) с шаблоном,
с последующей полимеризацией реакция с использованием ДНК-полимеразы
Цикл денатурации ДНК,
отжиг, синтез и полимеризация повторяются многократно.
Каждый раз реакция повторяется, в качестве шаблона используются продукты предыдущего цикла, а также исходный шаблон, вызывающий экспоненциальный синтез фрагмента ДНК между грунтовками.
Этот процесс был очень благодаря использованию термостабильных ДНК-полимераз и автоматических температурные цилеры.
Используя эту процедуру, один Молекула ДНК может быть специально усилена и обнаружена.
Используется множеством способов в молекулярная биология.
Не нужно знать последовательность ДНК между грунтовками,
так может амплифицировать ДНК родственных организм на основе праймеров известных консервативных областей.
Или используйте последовательность, идентифицированную из проекты секвенирования генома
Чувствительный метод обнаружения небольшое количество заражающих бактерий, мутантных клеток и т. д.
Может использоваться в сочетании с
обратная транскриптаза для амплификации конкретных последовательностей мРНК.
Выбор полимеразы снова важный. Thermus aquaticus ( Taq ) наиболее часто используется, но он подвержен ошибкам, отсутствует корректирует экзонуклеазу 3 ‘-> 5’ и теряет активность примерно после 35 циклов при высокая температура.
Другие организмы, например Pyrococcus furiousus , производят полимеразы, которые более термостабильны, менее подвержены ошибкам и имеют функцию корректуры.Разрешение более точная репликация более длинных генов (до 40 т.п.н.)
Много разных стратегий, все требуют: синтетический олигонуклеотид (ы) с желаемой мутацией удлинение олигонуклеотида с помощью ДНК-полимераза для реконструкции всей последовательности Анимированные вариант рисунка |
стратегия устранения стартовый шаблон дикого типа
e.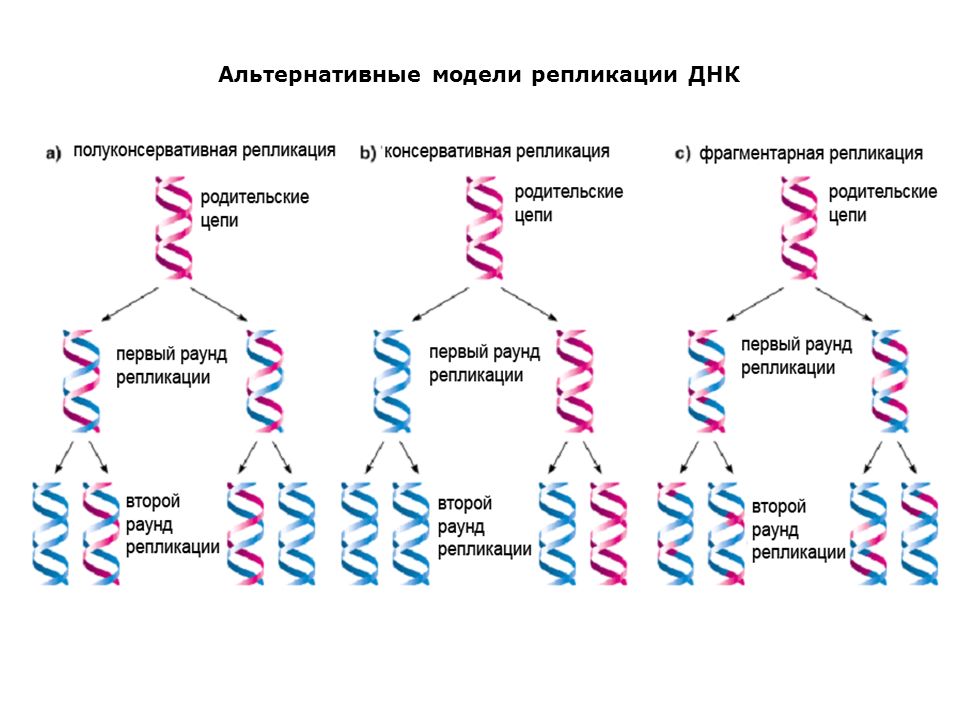

 — Но проблема в том, что это тест на ассоциации, он ничего не говорит про каузативность, что является настоящей причиной заболевания, он просто показывает, что в определенном участке есть что-то, что как-то действует на болезнь. При GWAS испытуемых можно разделять по больным и здоровым, а кто-то даже пытается таким образом смотреть, от чего зависит IQ. На самом деле можно разделить по любому признаку и попытаться поискать какие-то ассоциации
— Но проблема в том, что это тест на ассоциации, он ничего не говорит про каузативность, что является настоящей причиной заболевания, он просто показывает, что в определенном участке есть что-то, что как-то действует на болезнь. При GWAS испытуемых можно разделять по больным и здоровым, а кто-то даже пытается таким образом смотреть, от чего зависит IQ. На самом деле можно разделить по любому признаку и попытаться поискать какие-то ассоциации


 Она обнаружила, что ДНК может существовать в двух формах, в зависимости от относительной влажности окружающего воздуха. Это помогло ей сделать вывод, что фосфатная часть молекулы находится снаружи.Уотсон вернулась в Кембридж с довольно туманными воспоминаниями о фактах, которые представила Франклин, хотя и явно критически относилась к ее стилю лекций и внешнему виду. Основываясь на этой информации, Уотсон и Крик построили неудавшуюся модель. Это заставило главу их подразделения приказать им прекратить исследования ДНК. Но эта тема продолжала подниматься.
Она обнаружила, что ДНК может существовать в двух формах, в зависимости от относительной влажности окружающего воздуха. Это помогло ей сделать вывод, что фосфатная часть молекулы находится снаружи.Уотсон вернулась в Кембридж с довольно туманными воспоминаниями о фактах, которые представила Франклин, хотя и явно критически относилась к ее стилю лекций и внешнему виду. Основываясь на этой информации, Уотсон и Крик построили неудавшуюся модель. Это заставило главу их подразделения приказать им прекратить исследования ДНК. Но эта тема продолжала подниматься.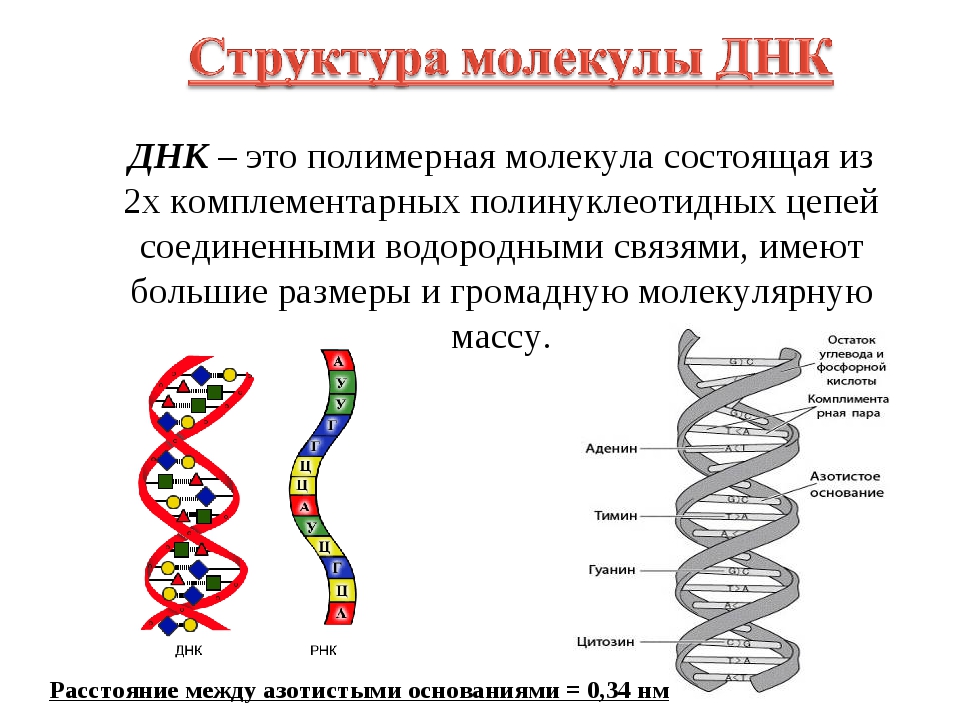 Позже Крик признался: «Боюсь, мы всегда относились к ней, скажем так, снисходительно».
Позже Крик признался: «Боюсь, мы всегда относились к ней, скажем так, снисходительно».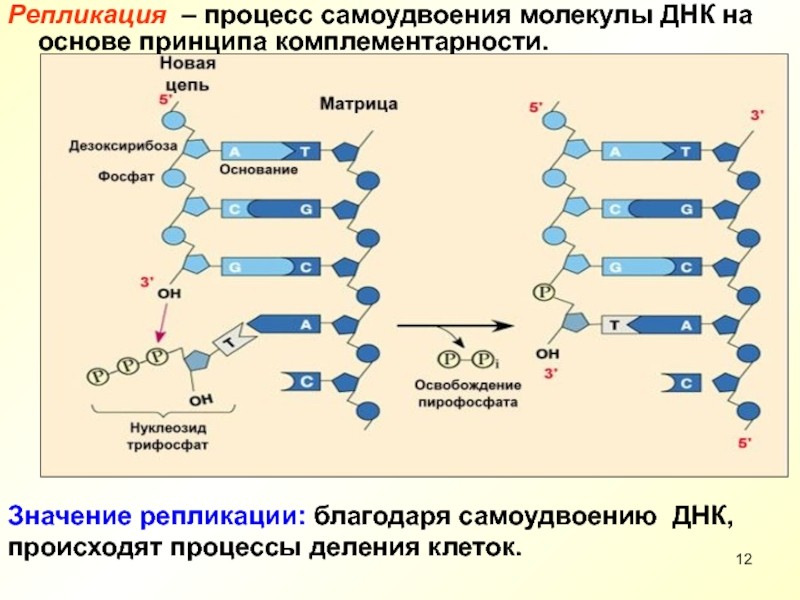 К 1962 году, когда Уотсон, Крик и Уилкинс получили Нобелевскую премию по физиологии / медицине, Франклин умер. Нобелевская премия присуждается только живым получателям и может быть разделена между тремя лауреатами. Будь она жива, попала бы в приз?
К 1962 году, когда Уотсон, Крик и Уилкинс получили Нобелевскую премию по физиологии / медицине, Франклин умер. Нобелевская премия присуждается только живым получателям и может быть разделена между тремя лауреатами. Будь она жива, попала бы в приз?
 Пантотенический
кислота — это витамин B 3 .
Пантотенический
кислота — это витамин B 3 .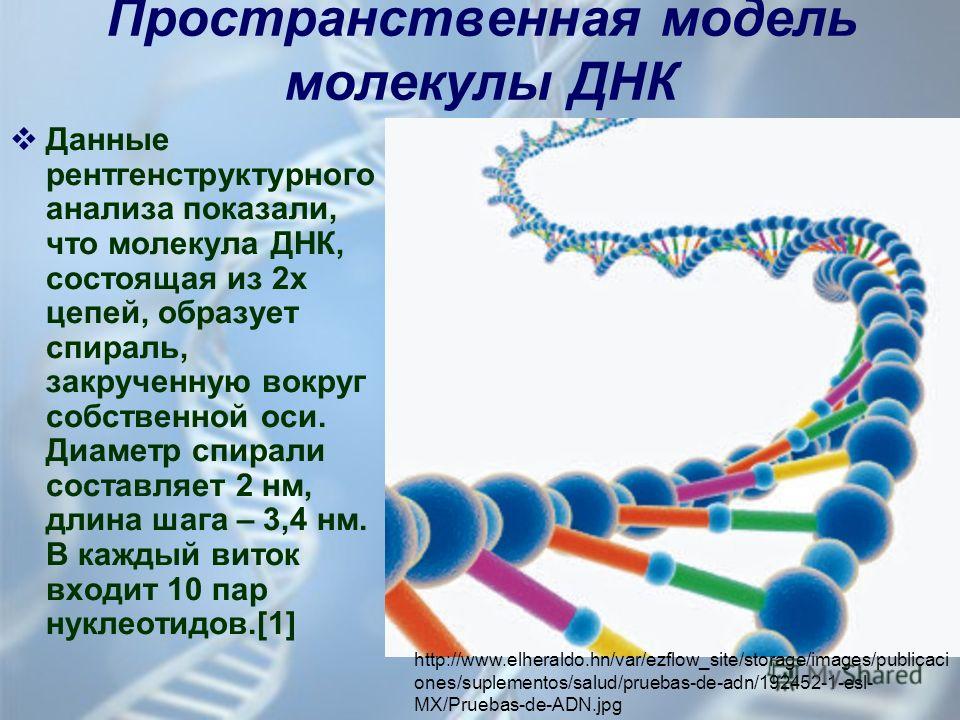 influenzae
influenzae
Leave A Comment