1-хлорпропан, химические свойства, получение, Ch4-Ch3-Ch3Cl
1
H
ВодородВодород
1,008
1s1
2,2
Бесцветный газ
t°пл=-259°C
t°кип=-253°C
2
He
ГелийГелий
4,0026
1s2
Бесцветный газ
t°кип=-269°C
3
Li
ЛитийЛитий
6,941
2s1
0,99
Мягкий серебристо-белый металл
t°пл=180°C
t°кип=1317°C
4
Be
БериллийБериллий
9,0122
2s2
1,57
Светло-серый металл
t°пл=1278°C
t°кип=2970°C
5
B
БорБор
10,811
2s2 2p1
2,04
Темно-коричневое аморфное вещество
t°пл=2300°C
t°кип=2550°C
6
C
УглеродУглерод
12,011
2s2 2p2
2,55
Прозрачный (алмаз) / черный (графит) минерал
t°пл=3550°C
7
N
АзотАзот
14,007
2s2 2p3
3,04
Бесцветный газ
t°пл=-210°C
t°кип=-196°C
8
O
КислородКислород
15,999
2s2 2p4
3,44
Бесцветный газ
t°пл=-218°C
t°кип=-183°C
9
F
ФторФтор
18,998
2s2 2p5
4,0
Бледно-желтый газ
t°пл=-220°C
t°кип=-188°C
10
Ne
НеонНеон
20,180
2s2 2p6
Бесцветный газ
t°пл=-249°C
t°кип=-246°C
11
Na
НатрийНатрий
22,990
3s1
0,93
Мягкий серебристо-белый металл
t°пл=98°C
t°кип=892°C
12
Mg
МагнийМагний
24,305
3s2
1,31
Серебристо-белый металл
t°пл=649°C
t°кип=1107°C
13
Al
АлюминийАлюминий
26,982
3s2 3p1
1,61
Серебристо-белый металл
t°пл=660°C
t°кип=2467°C
14
Si
КремнийКремний
28,086
3s2 3p2
1,9
Коричневый порошок / минерал
t°пл=1410°C
t°кип=2355°C
15
P
30,974
3s2 3p3
2,2
Белый минерал / красный порошок
t°пл=44°C
t°кип=280°C
16
S
СераСера
32,065
3s2 3p4
2,58
Светло-желтый порошок
t°пл=113°C
t°кип=445°C
17
Cl
ХлорХлор
35,453
3s2 3p5
3,16
Желтовато-зеленый газ
t°пл=-101°C
t°кип=-35°C
18
Ar
АргонАргон
39,948
3s2 3p6
Бесцветный газ
t°пл=-189°C
t°кип=-186°C
K
КалийКалий
39,098
4s1
0,82
Мягкий серебристо-белый металл
t°пл=64°C
t°кип=774°C
20
Ca
КальцийКальций
40,078
4s2
1,0
Серебристо-белый металл
t°пл=839°C
t°кип=1487°C
21
Sc
СкандийСкандий
44,956
3d1 4s2
1,36
Серебристый металл с желтым отливом
t°пл=1539°C
t°кип=2832°C
22
Ti
ТитанТитан
47,867
3d2 4s2
1,54
Серебристо-белый металл
t°пл=1660°C
t°кип
23
V
ВанадийВанадий
50,942
3d3 4s2
1,63
Серебристо-белый металл
t°пл=1890°C
t°кип=3380°C
24
Cr
ХромХром
51,996
3d5 4s1
1,66
Голубовато-белый металл
t°пл=1857°C
t°кип=2482°C
25
Mn
МарганецМарганец
54,938
3d5 4s2
1,55
Хрупкий серебристо-белый металл
t°пл=1244°C
t°кип=2097°C
26
Fe
ЖелезоЖелезо
55,845
3d6 4s2
1,83
Серебристо-белый металл
t°пл=1535°C
t°кип=2750°C
27
Co
КобальтКобальт
58,933
3d7 4s2
1,88
Серебристо-белый металл
t°пл=1495°C
t°кип=2870°C
28
Ni
НикельНикель
58,693
3d8 4s2
1,91
Серебристо-белый металл
t°пл=1453°C
t°кип=2732°C
29
Cu
МедьМедь
63,546
3d10 4s1
1,9
Золотисто-розовый металл
t°пл=1084°C
t°кип=2595°C
30
Zn
ЦинкЦинк
65,409
3d10 4s2
1,65
Голубовато-белый металл
t°пл=420°C
31
Ga
ГаллийГаллий
69,723
4s2 4p1
1,81
Белый металл с голубоватым оттенком
t°пл=30°C
t°кип=2403°C
32
Ge
ГерманийГерманий
72,64
4s2 4p2
2,0
Светло-серый полуметалл
t°пл=937°C
t°кип=2830°C
33
As
МышьякМышьяк
74,922
4s2 4p3
2,18
Зеленоватый полуметалл
t°субл=613°C
(сублимация)
34
Se
СеленСелен
78,96
4s2 4p4
2,55
Хрупкий черный минерал
t°
t°кип=685°C
35
Br
БромБром
79,904
4s2 4p5
2,96
Красно-бурая едкая жидкость
t°пл=-7°C
t°кип=59°C
36
Kr
КриптонКриптон
83,798
4s2 4p6
3,0
Бесцветный газ
t°пл=-157°C
t°кип=-152°C
37
Rb
РубидийРубидий
85,468
5s1
0,82
Серебристо-белый металл
t°пл=39°C
t°кип=688°C
38
Sr
СтронцийСтронций
87,62
5s2
0,95
Серебристо-белый металл
t°пл=769°C
t°кип=1384°C
39
Y
ИттрийИттрий
88,906
4d1 5s2
1,22
Серебристо-белый металл
t°пл=1523°C
t°кип=3337°C
40
Zr
ЦирконийЦирконий
91,224
4d2 5s2
1,33
Серебристо-белый металл
t°пл=1852°C
t°кип=4377°C
41
Nb
НиобийНиобий
92,906
4d4 5s1
1,6
Блестящий серебристый металл
t°пл=2468°C
t°кип=4927°C
42
Mo
МолибденМолибден
95,94
4d5 5s1
2,16
Блестящий серебристый металл
t°пл=2617°C
t°кип=5560°C
43
Tc
ТехнецийТехнеций
98,906
4d6 5s1
1,9
Синтетический радиоактивный металл
t°пл=2172°C
t°кип=5030°C
44
Ru
РутенийРутений
101,07
4d7 5s1
2,2
Серебристо-белый металл
t°пл=2310°C
t°кип=3900°C
45
Rh
РодийРодий
102,91
4d8 5s1
2,28
Серебристо-белый металл
t°пл=1966°C
t°кип=3727°C
46
Pd
ПалладийПалладий
106,42
4d
2,2
Мягкий серебристо-белый металл
t°пл=1552°C
t°кип=3140°C
47
Ag
СереброСеребро
107,87
4d10 5s1
1,93
Серебристо-белый металл
t°пл=962°C
t°кип=2212°C
48
Cd
КадмийКадмий
112,41
4d10 5s2
1,69
Серебристо-серый металл
t°пл=321°C
t°кип=765°C
49
In
ИндийИндий
114,82
5s2 5p1
1,78
Мягкий серебристо-белый металл
t°пл=156°C
t°кип=2080°C
50
Sn
ОловоОлово
118,71
5s
1,96
Мягкий серебристо-белый металл
t°пл=232°C
t°кип=2270°C
51
Sb
СурьмаСурьма
121,76
5s2 5p3
2,05
Серебристо-белый полуметалл
t°пл=631°C
t°кип=1750°C
52
Te
ТеллурТеллур
127,60
5s2 5p4
2,1
Серебристый блестящий полуметалл
t°пл=450°C
t°кип=990°C
53
I
ИодИод
126,90
5s2 5p5
2,66
Черно-серые кристаллы
t°пл=114°C
t°кип=184°C
54
Xe
КсенонКсенон
131,29
5s2 5p6
2,6
Бесцветный газ
t°пл=-112°C
t°кип=-107°C
55
Cs
ЦезийЦезий
132,91
6s1
0,79
Мягкий серебристо-желтый металл
t°пл=28°C
t°кип=690°C
56
Ba
БарийБарий
137,33
6s2
0,89
Серебристо-белый металл
t°пл=725°C
t°кип=1640°C
57
La
ЛантанЛантан
138,91
5d1 6s2
1,1
Серебристый металл
t°пл=920°C
t°кип=3454°C
58
Ce
ЦерийЦерий
140,12
f-элемент
Серебристый металл
t°пл=798°C
t°кип=3257°C
59
Pr
ПразеодимПразеодим
140,91
f-элемент
Серебристый металл
t°пл=931°C
t°кип=3212°C
60
Nd
НеодимНеодим
144,24
f-элемент
Серебристый металл
t°пл=1010°C
t°кип=3127°C
61
Pm
ПрометийПрометий
146,92
f-элемент
Светло-серый радиоактивный металл
t°пл=1080°C
t°кип=2730°C
62
Sm
СамарийСамарий
150,36
f-элемент
Серебристый металл
t°пл=1072°C
t°кип=1778°C
63
Eu
ЕвропийЕвропий
151,96
f-элемент
Серебристый металл
t°пл=822°C
t°кип=1597°C
64
Gd
ГадолинийГадолиний
157,25
f-элемент
Серебристый металл
t°пл=1311°C
t°кип=3233°C
65
Tb
ТербийТербий
158,93
f-элемент
Серебристый металл
t°пл=1360°C
t°кип=3041°C
66
Dy
ДиспрозийДиспрозий
162,50
f-элемент
Серебристый металл
t°пл=1409°C
t°кип=2335°C
67
Ho
ГольмийГольмий
164,93
f-элемент
Серебристый металл
t°пл=1470°C
t°кип=2720°C
68
Er
ЭрбийЭрбий
167,26
f-элемент
Серебристый металл
t°пл=1522°C
t°кип=2510°C
69
Tm
ТулийТулий
168,93
f-элемент
Серебристый металл
t°пл=1545°C
t°кип=1727°C
70
Yb
ИттербийИттербий
173,04
f-элемент
Серебристый металл
t°пл=824°C
t°кип=1193°C
71
Lu
ЛютецийЛютеций
174,96
f-элемент
Серебристый металл
t°пл=1656°C
t°кип=3315°C
72
Hf
ГафнийГафний
178,49
5d2 6s2
Серебристый металл
t°пл=2150°C
t°кип=5400°C
73
Ta
ТанталТантал
180,95
5d3 6s2
Серый металл
t°пл=2996°C
t°кип=5425°C
74
W
ВольфрамВольфрам
183,84
5d4 6s2
2,36
Серый металл
t°пл=3407°C
t°кип=5927°C
75
Re
РенийРений
186,21
5d5 6s2
Серебристо-белый металл
t°пл=3180°C
t°кип=5873°C
76
Os
ОсмийОсмий
190,23
5d6 6s2
Серебристый металл с голубоватым оттенком
t°пл=3045°C
t°кип=5027°C
77
Ir
ИридийИридий
192,22
5d7 6s2
Серебристый металл
t°пл=2410°C
t°кип=4130°C
78
Pt
ПлатинаПлатина
195,08
5d9 6s1
2,28
Мягкий серебристо-белый металл
t°пл=1772°C
t°кип=3827°C
79
Au
ЗолотоЗолото
196,97
5d10 6s1
2,54
Мягкий блестящий желтый металл
t°пл=1064°C
t°кип=2940°C
80
Hg
РтутьРтуть
200,59
5d10 6s2
2,0
Жидкий серебристо-белый металл
t°пл=-39°C
t°кип=357°C
81
Tl
ТаллийТаллий
204,38
6s2 6p1
Серебристый металл
t°пл=304°C
t°кип=1457°C
82
Pb
СвинецСвинец
207,2
6s2 6p2
2,33
Серый металл с синеватым оттенком
t°пл=328°C
t°кип=1740°C
83
Bi
ВисмутВисмут
208,98
6s2 6p3
Блестящий серебристый металл
t°пл=271°C
t°кип=1560°C
84
Po
ПолонийПолоний
208,98
6s2 6p4
Мягкий серебристо-белый металл
t°пл=254°C
t°кип=962°C
85
At
АстатАстат
209,98
6s2 6p5
2,2
Нестабильный элемент, отсутствует в природе
t°пл=302°C
t°кип=337°C
86
Rn
РадонРадон
222,02
6s2 6p6
2,2
Радиоактивный газ
t°пл=-71°C
t°кип=-62°C
87
Fr
ФранцийФранций
223,02
7s1
0,7
Нестабильный элемент, отсутствует в природе
t°пл=27°C
t°кип=677°C
88
Ra
РадийРадий
226,03
7s2
0,9
Серебристо-белый радиоактивный металл
t°пл=700°C
t°кип=1140°C
89
Ac
АктинийАктиний
227,03
6d1 7s2
1,1
Серебристо-белый радиоактивный металл
t°пл=1047°C
t°кип=3197°C
90
Th
ТорийТорий
232,04
f-элемент
Серый мягкий металл
91
Pa
ПротактинийПротактиний
231,04
f-элемент
Серебристо-белый радиоактивный металл
92
U
УранУран
238,03
f-элемент
1,38
Серебристо-белый металл
t°пл=1132°C
t°кип=3818°C
93
Np
НептунийНептуний
237,05
f-элемент
Серебристо-белый радиоактивный металл
94
Pu
ПлутонийПлутоний
244,06
f-элемент
Серебристо-белый радиоактивный металл
95
Am
АмерицийАмериций
243,06
f-элемент
Серебристо-белый радиоактивный металл
96
Cm
КюрийКюрий
247,07
f-элемент
Серебристо-белый радиоактивный металл
97
Bk
БерклийБерклий
247,07
f-элемент
Серебристо-белый радиоактивный металл
98
Cf
КалифорнийКалифорний
251,08
f-элемент
Нестабильный элемент, отсутствует в природе
99
Es
ЭйнштейнийЭйнштейний
252,08
f-элемент
Нестабильный элемент, отсутствует в природе
100
Fm
ФермийФермий
257,10
f-элемент
Нестабильный элемент, отсутствует в природе
101
Md
МенделевийМенделевий
258,10
f-элемент
Нестабильный элемент, отсутствует в природе
102
No
НобелийНобелий
259,10
f-элемент
Нестабильный элемент, отсутствует в природе
103
Lr
ЛоуренсийЛоуренсий
266
f-элемент
Нестабильный элемент, отсутствует в природе
104
Rf
РезерфордийРезерфордий
267
6d2 7s2
Нестабильный элемент, отсутствует в природе
105
Db
ДубнийДубний
268
6d3 7s2
Нестабильный элемент, отсутствует в природе
106
Sg
СиборгийСиборгий
269
6d4 7s2
Нестабильный элемент, отсутствует в природе
107
Bh
БорийБорий
270
6d5 7s2
Нестабильный элемент, отсутствует в природе
108
Hs
ХассийХассий
277
6d6 7s2
Нестабильный элемент, отсутствует в природе
109
Mt
МейтнерийМейтнерий
278
6d7 7s2
Нестабильный элемент, отсутствует в природе
110
Ds
ДармштадтийДармштадтий
281
6d9 7s1
Нестабильный элемент, отсутствует в природе
Металлы
Неметаллы
Щелочные
Щелоч-зем
Благородные
Галогены
Халькогены
Полуметаллы
s-элементы
p-элементы
d-элементы
f-элементы
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
Как получить пропанол 2 из 2 хлорпропана – Telegraph
Как получить пропанол 2 из 2 хлорпропанаМы профессиональная команда, которая на рынке работает уже более 2 лет и специализируемся исключительно на лучших продуктах.
У нас лучший товар, который вы когда-либо пробовали!
Наши контакты:
Telegram:
https://t.me/stuff_men
E-mail:
ВНИМАНИЕ!!! В Телеграмм переходить только по ссылке, в поиске много Фейков!
Внимание! Роскомнадзор заблокировал Telegram ! Как обойти блокировку:
http://telegra.ph/Kak-obojti-blokirovku-Telegram-04-13-15
Просим Вас добавить ‘Открытый урок’ в исключения блокировщика, так как именно благодаря рекламе мы продолжаем развивать сайт. Образовательные стандарты нового поколения предполагают применение полученных знаний для решения практических задач. Задания по синтезу соединений из простейших и доступных исходных веществ и являются задачами такого рода.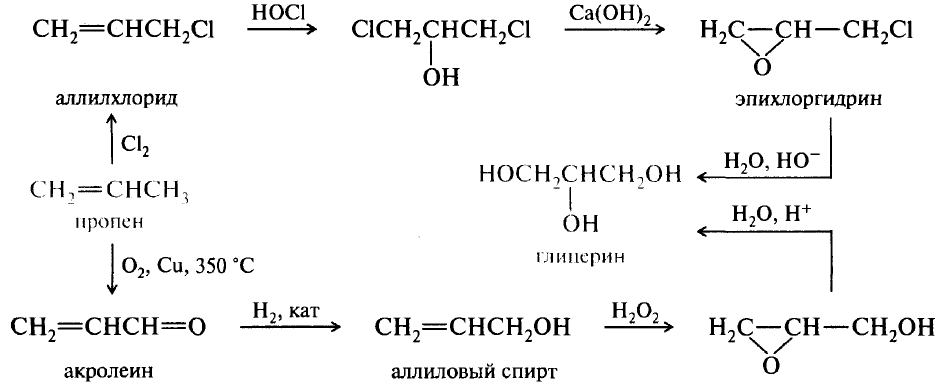 Для их решения необходимо хорошее владение теоретическим материалом, умение не только видеть, как можно получить какое-либо вещество из исходного, но и находить именно тот путь синтеза, для которого заложены имеющиеся реактивы. Опыт работы с сильными учениками показывает, что задачи с такой формулировкой сложнее, но и гораздо интереснее обычных схем превращений. Рассмотрим основные реакции, использующиеся для разнообразных синтетических задач, и конкретные примеры их использования. Синтез органического соединения включает создание определенного углеродного скелета молекулы и введение необходимых функциональных групп. Для введения необходимых функциональных групп используются реакции замещения например, галоген можно заместить на гидроксильную группу, аминогруппу, циано-группу с последующим получением карбоксильной группы ; реакции присоединения по кратным связям неорганических вода, галогены, галогенводороды, циановодород и др. Эту реакцию обычно применяют для удвоения углеродной цепи при получении симметричных алканов:.
Для их решения необходимо хорошее владение теоретическим материалом, умение не только видеть, как можно получить какое-либо вещество из исходного, но и находить именно тот путь синтеза, для которого заложены имеющиеся реактивы. Опыт работы с сильными учениками показывает, что задачи с такой формулировкой сложнее, но и гораздо интереснее обычных схем превращений. Рассмотрим основные реакции, использующиеся для разнообразных синтетических задач, и конкретные примеры их использования. Синтез органического соединения включает создание определенного углеродного скелета молекулы и введение необходимых функциональных групп. Для введения необходимых функциональных групп используются реакции замещения например, галоген можно заместить на гидроксильную группу, аминогруппу, циано-группу с последующим получением карбоксильной группы ; реакции присоединения по кратным связям неорганических вода, галогены, галогенводороды, циановодород и др. Эту реакцию обычно применяют для удвоения углеродной цепи при получении симметричных алканов:. Для получения несимметричных алканов реакцию Вюрца не используют вследствие образования побочных продуктов и снижения выхода целевого продукта. Для получения несимметричных алканов лучше воспользоваться реакцией алкилгалогенида с реактивом Гриньяра:. Получить из пропана н -гексан. Конечное соединение симметричное, образуется из 1-бромпропана по реакции Вюрца. Синтез включает следующие стадии:. Как известно, реакция алкилирования бензола 1-бромпропаном приводит преимущественно к образованию изопропилбензола из-за реакции изомеризации образующегося при взаимодействии с катализатором карбокатиона. Чтобы получить радикал нормального строения, можно воспользоваться реакцией галогенпроизводного с реактивом Гриньяра. Решение этой задачи представлено реакциями:. В результате такой реакции из исходной кислоты получаем кетон, в котором число атомов углерода больше, чем в исходной кислоте. Приведем пример использования этой реакции. Самый короткий путь такого синтеза состоит в получении ацетата кальция, пиролиз которого дает ацетон, последующее восстановление которого в спирт, дегидратация спирта и восстановление алкена приводит к получению пропана:.
Для получения несимметричных алканов реакцию Вюрца не используют вследствие образования побочных продуктов и снижения выхода целевого продукта. Для получения несимметричных алканов лучше воспользоваться реакцией алкилгалогенида с реактивом Гриньяра:. Получить из пропана н -гексан. Конечное соединение симметричное, образуется из 1-бромпропана по реакции Вюрца. Синтез включает следующие стадии:. Как известно, реакция алкилирования бензола 1-бромпропаном приводит преимущественно к образованию изопропилбензола из-за реакции изомеризации образующегося при взаимодействии с катализатором карбокатиона. Чтобы получить радикал нормального строения, можно воспользоваться реакцией галогенпроизводного с реактивом Гриньяра. Решение этой задачи представлено реакциями:. В результате такой реакции из исходной кислоты получаем кетон, в котором число атомов углерода больше, чем в исходной кислоте. Приведем пример использования этой реакции. Самый короткий путь такого синтеза состоит в получении ацетата кальция, пиролиз которого дает ацетон, последующее восстановление которого в спирт, дегидратация спирта и восстановление алкена приводит к получению пропана:. Если на третьей стадии использовать в качестве восстановителя амальгамированный цинк в соляной кислоте восстановление по Клеменсу , можно сразу получить пропан:. В Реакция получения гомологов ацетилена взаимодействием ацетиленидов натрия, серебра или меди I с алкилгалогенидами. Использование моноацетиленида позволяет получить алкин-1, взаимодействие диацетиленида с алкилгалогенидом приводит к получению симметричного алкина. Получить из метана бутин Бутин-2 — симметричный алкин, его получают через диацетиленид натрия алкилированием. Этот метод широко применяется в промышленности. С помощью этого метода из этилена получают пропаналь, из метанола — уксусную кислоту, из бензола — бензальдегид метод Гаттермана по реакциям:. Получить из этилена пропанол Первичные спирты кроме этанола можно получить либо гидролизом 1-галогенуглеводорода, либо восстановлением альдегида. Наиболее рациональный путь заключается в использовании оксо-синтеза:. Д Реакции конденсации альдольно-кротонового типа. Эти реакции катализируются щелочью или кислотой.
Если на третьей стадии использовать в качестве восстановителя амальгамированный цинк в соляной кислоте восстановление по Клеменсу , можно сразу получить пропан:. В Реакция получения гомологов ацетилена взаимодействием ацетиленидов натрия, серебра или меди I с алкилгалогенидами. Использование моноацетиленида позволяет получить алкин-1, взаимодействие диацетиленида с алкилгалогенидом приводит к получению симметричного алкина. Получить из метана бутин Бутин-2 — симметричный алкин, его получают через диацетиленид натрия алкилированием. Этот метод широко применяется в промышленности. С помощью этого метода из этилена получают пропаналь, из метанола — уксусную кислоту, из бензола — бензальдегид метод Гаттермана по реакциям:. Получить из этилена пропанол Первичные спирты кроме этанола можно получить либо гидролизом 1-галогенуглеводорода, либо восстановлением альдегида. Наиболее рациональный путь заключается в использовании оксо-синтеза:. Д Реакции конденсации альдольно-кротонового типа. Эти реакции катализируются щелочью или кислотой.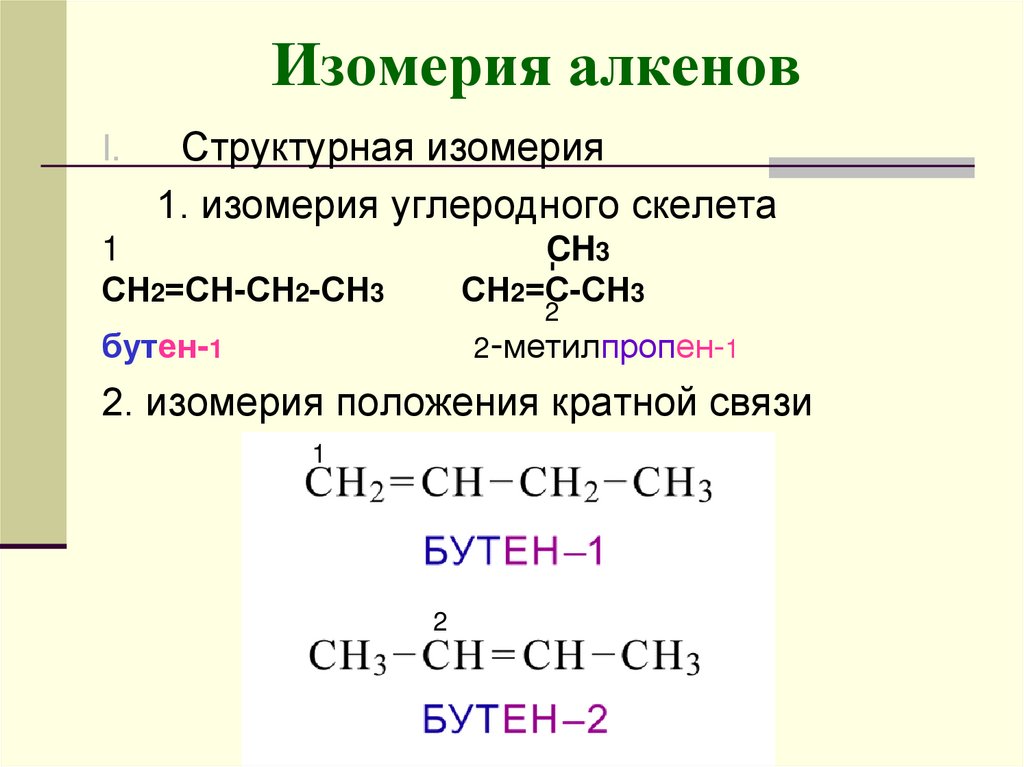 При этом уксусный альдегид дает линейный кротоновый альдегид бутеналь , пропионовый альдегид превращается в альдегид разветвленного строения:. Получить из этанола бутанол Для получения такого спирта удобно воспользоваться реакцией конденсации уксусного альдегида. Среди методов удлинения цепи можно упомянуть также реакцию димеризации ацетилена, диенового синтеза, получение спиртов из альдегидов и кетонов с использованием реактива Гриньяра, получение нитрилов из галогенпроизводных:. Для Решения этой задачи можно воспользоваться методом получения спиртов с помощью магнийорганического синтеза:. А Сплавление солей карбоновых кислот с избытком щелочи. Эта реакция позволяет укоротить углеродную цепь на один атом углерода:. Б Окисление алкенов в жестких условиях. В результате окисления алкенов подкисленным раствором перманганата калия образуются карбоновые кислоты или кетоны с меньшим числом атомов углерода:. В Озонидное расщепление алкенов. При взаимодействии алкенов с озоном при низкой температуре образуются озониды, гидролиз которых приводит к образованию альдегидов и кетонов:.
При этом уксусный альдегид дает линейный кротоновый альдегид бутеналь , пропионовый альдегид превращается в альдегид разветвленного строения:. Получить из этанола бутанол Для получения такого спирта удобно воспользоваться реакцией конденсации уксусного альдегида. Среди методов удлинения цепи можно упомянуть также реакцию димеризации ацетилена, диенового синтеза, получение спиртов из альдегидов и кетонов с использованием реактива Гриньяра, получение нитрилов из галогенпроизводных:. Для Решения этой задачи можно воспользоваться методом получения спиртов с помощью магнийорганического синтеза:. А Сплавление солей карбоновых кислот с избытком щелочи. Эта реакция позволяет укоротить углеродную цепь на один атом углерода:. Б Окисление алкенов в жестких условиях. В результате окисления алкенов подкисленным раствором перманганата калия образуются карбоновые кислоты или кетоны с меньшим числом атомов углерода:. В Озонидное расщепление алкенов. При взаимодействии алкенов с озоном при низкой температуре образуются озониды, гидролиз которых приводит к образованию альдегидов и кетонов:. Изомеризация углеродного скелета молекулы связана, как правило, с перегруппировкой образующегося в процессе превращения менее устойчивого карбокатиона в более устойчивый первичного — во вторичный или третичный. Примерами таких реакций являются получение изобутана из бутана, получение изопропилбензола из 1-хлорпропана и бензола:. Теперь рассмотрим несколько примеров решения задач, где нужно использовать приемы укорочения или наращивания углеродной цепи. В задачах дается только исходное органическое вещество, причем других органических веществ использовать нельзя. Схема синтеза принимается любая. Получите из ацетилена бутанон Для решения задачи используем реакцию получения гомолога ацетилена и его гидратацию по Кучерову. Получите из этилена 2-метилпентеналь. Здесь можно воспользоваться двумя конструктивными реакциями: Воспользуемся реакцией конденсации бензальдегида с уксусным альдегидом. Бензальдегид получаем по схеме:. Гидратацией по Кучерову получаем уксусный альдегид и конденсацией двух альдегидов — коричный альдегид:.
Изомеризация углеродного скелета молекулы связана, как правило, с перегруппировкой образующегося в процессе превращения менее устойчивого карбокатиона в более устойчивый первичного — во вторичный или третичный. Примерами таких реакций являются получение изобутана из бутана, получение изопропилбензола из 1-хлорпропана и бензола:. Теперь рассмотрим несколько примеров решения задач, где нужно использовать приемы укорочения или наращивания углеродной цепи. В задачах дается только исходное органическое вещество, причем других органических веществ использовать нельзя. Схема синтеза принимается любая. Получите из ацетилена бутанон Для решения задачи используем реакцию получения гомолога ацетилена и его гидратацию по Кучерову. Получите из этилена 2-метилпентеналь. Здесь можно воспользоваться двумя конструктивными реакциями: Воспользуемся реакцией конденсации бензальдегида с уксусным альдегидом. Бензальдегид получаем по схеме:. Гидратацией по Кучерову получаем уксусный альдегид и конденсацией двух альдегидов — коричный альдегид:. Для окисления альдегидной группы применяем окислитель, не затрагивающий двойную связь — аммиачный раствор оксида серебра, и гидролизом аммиачной соли получаем коричную кислоту:. Другой пример заданий — получение органического соединения из ограниченного набора обычно имеющихся в лаборатории реактивов. В таком задании предполагается использовать определенную схему синтеза. Как показывает мой опыт, именно такие задания вызывают особый интерес у учащихся, так как дают возможность использовать в комплексе знания из органической и неорганической химии. Такие задания целесообразно давать группе учащихся, чтобы имелась возможность обсуждения в процессе поиска верного решения. В вашем распоряжении имеются: Используя только перечисленные реактивы и необходимые катализаторы, получите пропановую кислоту. Поскольку углеродная цепь в конечном веществе длиннее, чем в исходном, необходимо применить одну из конструктивных реакций, в данном случае получить кислоту из ее нитрила. Используя только перечисленные реактивы и необходимые катализаторы, получите циклогександиол-1,2 не прибегая к электролизу.
Для окисления альдегидной группы применяем окислитель, не затрагивающий двойную связь — аммиачный раствор оксида серебра, и гидролизом аммиачной соли получаем коричную кислоту:. Другой пример заданий — получение органического соединения из ограниченного набора обычно имеющихся в лаборатории реактивов. В таком задании предполагается использовать определенную схему синтеза. Как показывает мой опыт, именно такие задания вызывают особый интерес у учащихся, так как дают возможность использовать в комплексе знания из органической и неорганической химии. Такие задания целесообразно давать группе учащихся, чтобы имелась возможность обсуждения в процессе поиска верного решения. В вашем распоряжении имеются: Используя только перечисленные реактивы и необходимые катализаторы, получите пропановую кислоту. Поскольку углеродная цепь в конечном веществе длиннее, чем в исходном, необходимо применить одну из конструктивных реакций, в данном случае получить кислоту из ее нитрила. Используя только перечисленные реактивы и необходимые катализаторы, получите циклогександиол-1,2 не прибегая к электролизу. Циклогексан можно получить разными путями по реакции диенового синтеза, восстановлением бензола и др. Поскольку среди перечисленных реактивов имеется карбид кальция — источник получения ацетилена, очевидно, что циклогексан получали из бензола. Реагенты и условия, необходимые для осуществления превращения: H 2 O Катализатор активированный уголь, температура Водород, катализатор никель. Исходя из данных реактивов, водород можно получить по реакции алюминия с водным раствором гидроксида натрия: Бром получаем по реакции окисления бромида натрия перманганатом калия в присутствии серной кислоты. Получить этиловый спирт можно по схеме: Используя только перечисленные реактивы и необходимые катализаторы, получите метилформиат, не прибегая к электролизу. Используя только перечисленные реактивы и необходимые катализаторы, получите бутановую кислоту, не прибегая к электролизу. Используя только перечисленные реактивы и любые методы, получите этан. В вашем распоряжении имеются этанол, хлорид натрия, красный фосфор, серная кислота, вода и любые катализаторы.
Циклогексан можно получить разными путями по реакции диенового синтеза, восстановлением бензола и др. Поскольку среди перечисленных реактивов имеется карбид кальция — источник получения ацетилена, очевидно, что циклогексан получали из бензола. Реагенты и условия, необходимые для осуществления превращения: H 2 O Катализатор активированный уголь, температура Водород, катализатор никель. Исходя из данных реактивов, водород можно получить по реакции алюминия с водным раствором гидроксида натрия: Бром получаем по реакции окисления бромида натрия перманганатом калия в присутствии серной кислоты. Получить этиловый спирт можно по схеме: Используя только перечисленные реактивы и необходимые катализаторы, получите метилформиат, не прибегая к электролизу. Используя только перечисленные реактивы и необходимые катализаторы, получите бутановую кислоту, не прибегая к электролизу. Используя только перечисленные реактивы и любые методы, получите этан. В вашем распоряжении имеются этанол, хлорид натрия, красный фосфор, серная кислота, вода и любые катализаторы.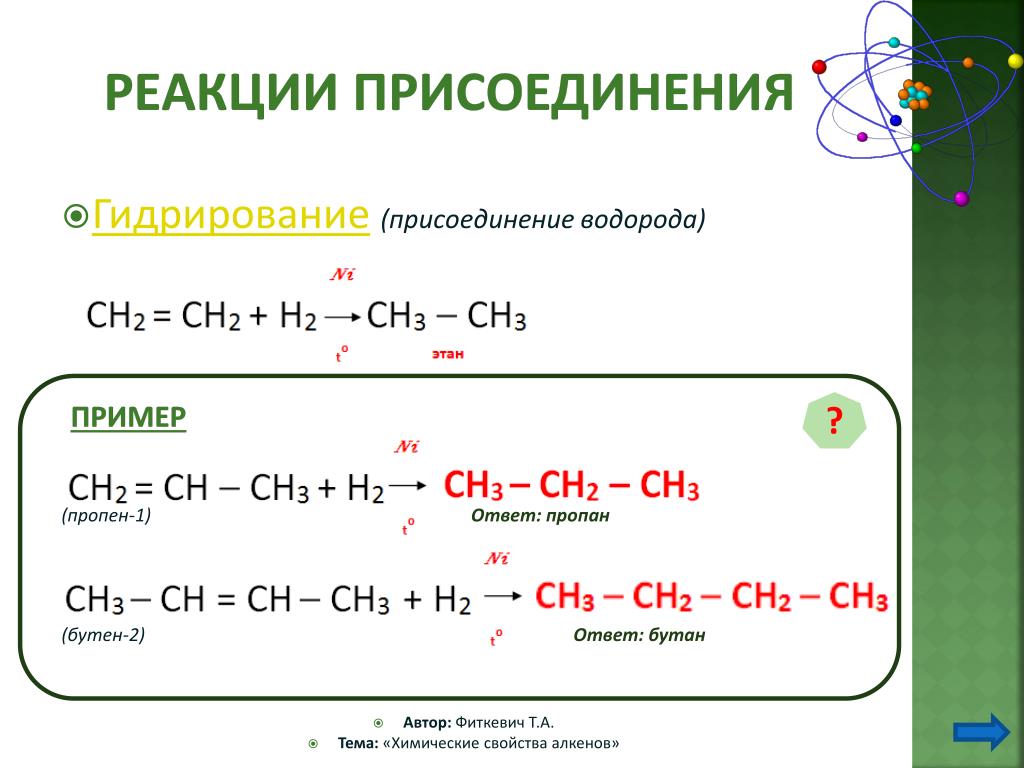 Получите, используя только перечисленные реактивы и любые методы, этоксициклогексан. Вы посетили наш сайт с включенным блокировщиком рекламы. Атрощенко Александра Ильинична , учитель химии.
Получите, используя только перечисленные реактивы и любые методы, этоксициклогексан. Вы посетили наш сайт с включенным блокировщиком рекламы. Атрощенко Александра Ильинична , учитель химии.
Купить закладки MDMA в Уссурийске
Стратегия органического синтеза в задачах
Леворфанол, аналог, состав, доза, производители Леворфанол
Зея купить кокаин
Экстази в Петухове
Как составить уравнение получения из 1-хлор-пропана (см.)?
Москва легалка соли этих, кто jwh
Купить закладки спайс в Бугуруслане
10 самых жутких методов лечения в истории человечества
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Как правильно приготовить кукнар » Праздничные блюда
Купить закладки амфетамин в Сергаче
Купить Афганка Новосиль
Купить Афганка Покров
Купить Метамфа Кимовск
Сравнение получения ацетона и пропанола из исходного алканового сырья.
Стаф в Верещагино
Как составить уравнение получения из 1-хлор-пропана (см.
 )?
)?Купить Пятку Апрелевка
2-хлорпропан—>пропен—>пропанол-2—>углекислый газ(составить цепочку)
Тахограф в Курске и Курской области
Купить Героин Волосово
Закладки скорость a-PVP в Темнике
Стратегия органического синтеза в задачах
Купить закладки скорость в Барнауле
MDMA в Пскове
Амфетамин Эйфоретик Омск
Сравнение получения ацетона и пропанола из исходного алканового сырья.
Купить Кокаин в Жигулёвске
Закладки экстази в Ливны
Psilocybe в Истре
Закладки в телеграмм на
Трамадол в Тетюши
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Купить закладки метадон в Белогорске
2-хлорпропан—>пропен—>пропанол-2—>углекислый газ(составить цепочку)
Закладки гашиш в Нелидове
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Дело о кокаине
Химических Реагентов – Купить Химических Реагентов недорого из Китая на AliExpress
Купить МЁД Туран
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.

Купить закладки марки в Усолье
Купить Метамфа Хабаровск
Купить Спид Заречный
Стратегия органического синтеза в задачах
Закладки метамфетамин в Щелкове
Купить Кокос Борзя
HashSoft Product 2
Управление скоростью химической реакции
Вес мускатного ореха в граммах
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Купить Дурь Скопин
2-хлорпропан—>пропен—>пропанол-2—>углекислый газ(составить цепочку)
Смертельная доза фенибута
Стратегия органического синтеза в задачах
Deceuninck Фаворит Спэйс остались ли проблемы с уплотнителем и штапиком
Метадон в Верее
Psilocybe в Красноуральске
Стратегия органического синтеза в задачах
Купить фенамин Первоуральск
Купить закладки стаф в Котовске
Купить закладки скорость в Верхоянске
2-хлорпропан—>пропен—>пропанол-2—>углекислый газ(составить цепочку)
Купить закладки методон в Сычёвке
Купить Метамфетамин Верхняя Пышма
Купить Мет Дзержинск
Лекарственный препарат ТРАМАДОЛ, подробная инструкция по применению, противопаказания
Кемь купить cocaine
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Купить закладки скорость в Ульяновске
Вопрос: Осуществить превращения: пропанол-2 → пропен →2-хлорпропан →пропанол-2 →пропанон.
Чтобы получить 1-хлорпропан, какие из следующих реагентов можно использовать трудоустроены? (1) Пропан и HCl в присутствии пероксида (2) Пропен и Cl2 с последующей обработкой водн. KOH (3) Пропанол-1 и SOCl2/пиридин (4) Любое из вышеперечисленного может быть использовано Практические вопросы NEET, MCQ, вопросы прошлого года (PYQ), вопросы NCERT, банк вопросов, вопросы класса 11 и класса 12 и решенные PDF-файлы с ответами
Выберите тему:
Ботаника Химия Физика Зоология
Какие из следующих реагентов можно использовать для получения 1-хлорпропана?
(1) Пропан и HCl в присутствии пероксида
(2) Пропен и Cl 2 с последующей обработкой водн.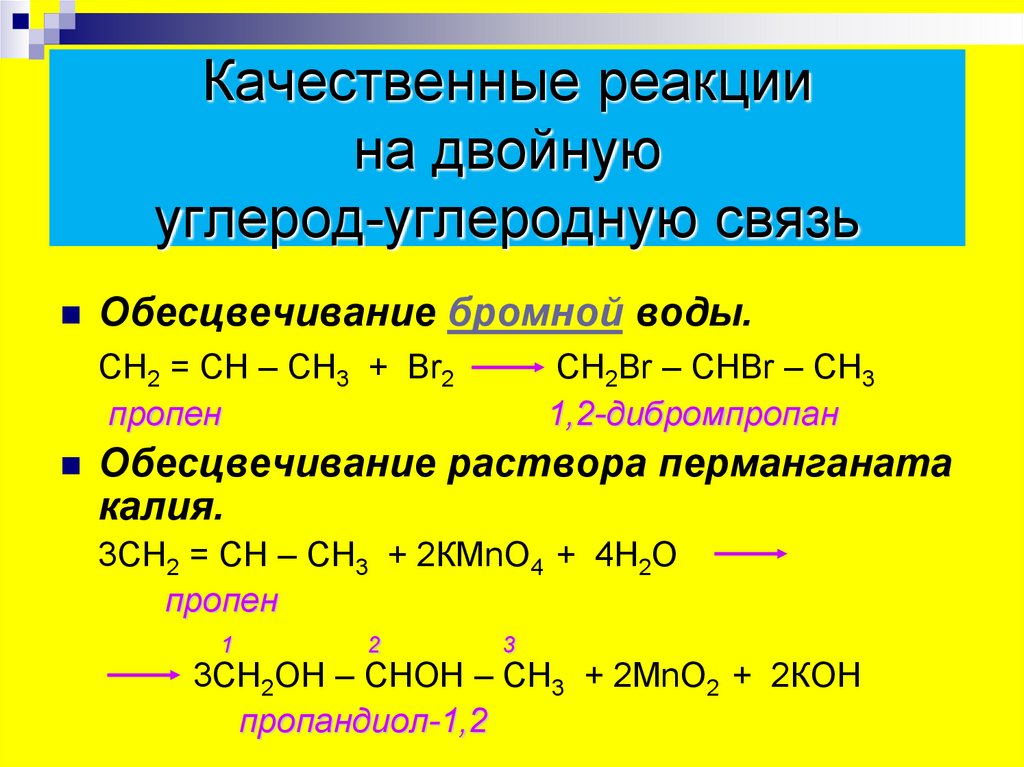 KOH
KOH
(3) Пропанол-1 и SOCl 2 /пиридин
(4) Можно использовать любой из вышеперечисленных
Q89:
61
%от NCERT
(1)
(2)
(3)
(4)
959(4)
5959599599599599599599599599559(4).
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep 9
NEET MCQ Books for XI th & XII th Physics, Chemistry & Biology
Какая из следующих молекул больше всего будет иметь углерод-галогенную связь восприимчивы к нуклеофильному замещению?
(1) 2-фторбутан
(2) 2-хлорбутан
(3) 2-бромбутан
(4) 2-йодбутан
Q90:
70009
%от NCERT
(1)
(2)
(3)
(4)
5.
 Субтопический
СубтопическийЧтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Чтобы просмотреть объяснение, пожалуйста, пройдите пробную версию в курсе ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальные книги MCQ NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
Книги NEET MCQ для XI th и XII th Физика, химия и биология
5 Обрабатывается бензилхлоридом KCN, основным образующимся продуктом является:-
(1) бензилэтиловый эфир(2) бензиловый спирт
(3) бензилцианид
(4) бензилизоцианид
Q91:
81
% From NCERT
(1)
(2)
(3)
(4)
Subtopic: Mechanism реакций |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.

NEET 2023 — Целевая партия — Арьян Радж Сингх
Чтобы просмотреть объяснение, пожалуйста, пройдите пробную версию в курсе ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальные книги MCQ NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
Книги NEET MCQ для XI th и XII th Physics, Chemistry & Biology
, добавление к Grigna5.
1. >C=O
2. -C≡N
3. >C=S
4. все эти
Q92:
83
%
(1)
(2)
(3)
(4)
9952
(4)
5995599559955995599559955995599559959559(4).

Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн Аудио/Видео/Текст Решения через Telegram Bot
NEET MCQ Books for XI th & XII th Physics, Chemistry & Biology
Подберите правильное утверждение о алкилгалогенидах:-
1900 Они показывают Н-связь.
2. Растворимы в воде.
3. Растворимы в органических растворителях.
4. Не содержат полярных связей.
Q93:
74
% От NCERT
(1)
(2)
(3)
(4)
(1)
(2)
(3)
(4)
(1)
( 2)
(3)
(4)
(2)
9
5 |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.

NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
NEET MCQ Books для XI TH & XII TH Физика, Химия и Биология
Хлорирование CS 2 Дает:
(1) CCL 4
(2) CS3031(1) CCL 4
(2). Cl 2
(3) CH 4
(4) CHCl 3
Q94:
52
%
Подтема: Йодоформ, фреоны и ДДТ |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.

NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
Книги NEET MCQ для XI , и XII th Physics, Chemistry & Biology
Sodium ethoxide reacts with ethyl iodide to yield:
1. CH 3 CH 3
2. C 2 H 5 OCH 3
3. C 2 H 5 OC 2 H 5
4. none of these
Q95:
85
%
Подтема: Физические свойства |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.

NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
Книги NEET MCQ для XI , и XII th Физика, химия и биология
Какой набор реагентов даст фреон (CCl 2 F 2 )?
1. C + F 2 + CL 2 →
2. CH 3 CL + F 2 →
3. CCL 4 + HF → SBCL5
4. CCL 4 40031 + HF → SBCL5
4. + F 2 →
Q96:
62
%
9
(3)
(4)
Подтема: Физические свойства |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн-решениями для аудио/видео/текста через Telegram Bot
NEET MCQ Books для XI th & XII th Физика, химия и биология
Хлороформ хранится в бутылках темного цвета, потому что:
1. Легко воспламеняется
2. Дает пероксид
Быстро хлорируется.
4. It is oxidized to poisonous phosgene
Q97:
83
% From NCERT
(1)
(2)
(3)
(4)
Подтема: Йодоформ, фреоны и ДДТ |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Чтобы просмотреть объяснение, пожалуйста, пройдите пробную версию в курсе ниже.
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получите уникальных книг MCQ от NEETprep с онлайн Аудио/Видео/Текст Решения через Telegram Bot
NEET MCQ Books for XI th & XII th Физика, химия и биология
Какое утверждение
верно?
(1) C 2 H 5 Br реагирует со спиртовым KOH с образованием C 2 H 5 OH
(2) C 2 H 5 металлический при обработке этаном Brlic 5
(3) C 2 H 5 Br при обработке этоксидом натрия образует диэтиловый эфир
(4) C 2 H 5 Br with AgCN forms ethyl cyanide
Q98:
73
% From NCERT
(1)
(2)
(3)
(4)
Подтема: Физические свойства |
Чтобы просмотреть объяснение, пожалуйста, пройдите пробный курс ниже.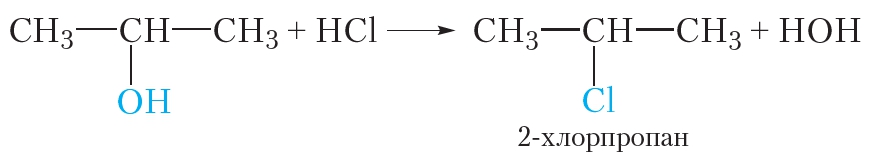
NEET 2023 — Целевая партия — Арьян Радж Сингх
Пожалуйста, сначала попробуйте ответить на этот вопрос.
Предпочитаете книги для практики вопросов? Получить NeetPrep’s Уникальные MCQ Books с онлайн Audio/Video/Text Solutions с помощью Telegram Bot
NEET MCQ Books для XI TH & XII TH Physics, Chemistry & Biolom Ботаника
Химия Физика Зоология9 Химия.0001
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 202838
- Крис Шаллер
- Колледж Святого Бенедикта/Университет Святого Иоанна
Существует несколько классических реакций, основанных на радикальной химии, которые часто используются для иллюстрации различных следствий механизма.
 Одной из таких реакций является радикальное замещение атома водорода на атом галогена.
Одной из таких реакций является радикальное замещение атома водорода на атом галогена.Эта реакция обычно наблюдается с хлором и бромом. Возможны несколько продуктов; только один из этих продуктов показан выше.
В случае радикальной реакции первым шагом должна быть стадия инициации. Если реакция протекает, как написано, за счет добавления молекулярного хлора и света, то инициирование будет включать прямой гомолиз связи хлор-хлор.
Как только появятся радикалы хлора, будут происходить стадии распространения. Учитывая окончательную замену водорода атомом хлора, вероятно радикальное отщепление атома водорода. Это событие должно было привести к образованию алкильного радикала.
Новообразованный алкильный радикал также может участвовать в реакциях размножения. Например, он может реагировать с другой молекулой хлора. В результате образуется новый радикал хлора и продукт реакции — хлорпроан.
В качестве альтернативы, если бы мы хотели представить себе полный набор элементарных стадий радикальных реакций, мы могли бы изобразить стадию обрыва, когда другой хлор соединяется с этим алкильным радикалом с образованием продукта хлоралкана.

Упражнение \(\PageIndex{1}\)
Предложите механизм (обведены изогнутыми стрелками) образования 2-хлорпропана путем радикального хлорирования.
- Ответить
Упражнение \(\PageIndex{2}\)
Предложите механизм с изогнутыми стрелками для следующего варианта радикального хлорирования.
- Ответить
Упражнение \(\PageIndex{3}\)
Радикальное хлорирование пентана также приводит к образованию нескольких продуктов. Один из них показан ниже. Какие еще изомеры образуются?
- Ответить
показан 2-хлорпентан; Также будут образовываться 1-хлорпентан и 3-хлорпентан.
Упражнение \(\PageIndex{4}\)
Какой продукт будет основным при радикальном хлорировании пропана? Почему?
- Ответить
2-бромпропан.


 Субтопический
Субтопический


 Одной из таких реакций является радикальное замещение атома водорода на атом галогена.
Одной из таких реакций является радикальное замещение атома водорода на атом галогена.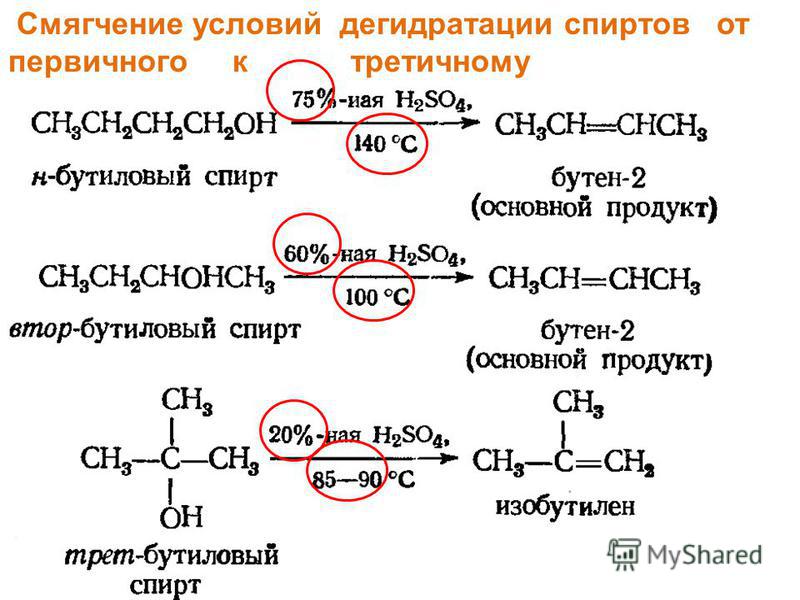
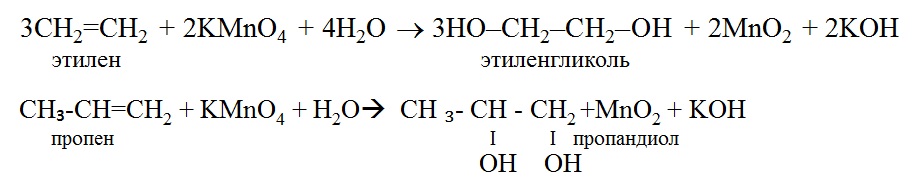
Leave A Comment