Внутренняя энергия. Температура — презентация онлайн
1. Внутренняя энергия. Температура
2. Закон сохранения энергии
п max, Ешарак = 0 Еп
ПотенциальнаяЕэнергия
превратилась
в кинетическую энергию шара Ек;
механическаяЕэнергия
шара
п ↓, Ек ↑
Е = Еп + Ек
превратилась
во внутреннюю энергию шара Евн
Ек max, Еп = 0
2
Еп = 0, Ек = 0
?
3. Основные положения МКТ
Молекулярно-кинетической теорией называютучение о строении и свойствах вещества на основе
представления о существовании атомов и молекул как
наименьших частиц химического вещества.
Основные положения МКТ:
1. Все вещества – жидкие, твердые и газообразные –
образованы из мельчайших частиц – молекул,
которые сами состоят из атомов.
2. Атомы и молекулы находятся в непрерывном
хаотическом движении.
3. Частицы взаимодействуют друг с другом силами,
имеющими электрическую природу (притягиваются и
отталкиваются).

В твердых телах
молекулы совершают
беспорядочные
колебания около
фиксированных
центров (положений
равновесия).
В жидкостях молекулы имеют
значительно большую свободу
для теплового движения. Они не
привязаны к определенным
центрам и могут перемещаться
по всему объему жидкости. Этим
объясняется текучесть
жидкостей.
В газах расстояния между
молекулами обычно
значительно больше их
размеров, каждая молекула
движется вдоль прямой
линии до очередного
столкновения с другой
молекулой или со стенкой
сосуда.
5. Фазы вещества и тепловые процессы
6. Взаимные превращения жидкостей и газов
Парообразование – это переход вещества изжидкого состояния в газообразное.
Конденсация – переход вещества из
газообразного состояния в жидкое.
Испарение – это парообразование, происходящее
со свободной поверхности жидкости.
С точки зрения молекулярно-кинетической
теории, испарение – это процесс, при котором с
поверхности жидкости вылетают наиболее
быстрые молекулы, кинетическая энергия
которых превышает энергию их связи с
остальными молекулами жидкости.
 Это приводит
Это приводитк уменьшению средней кинетической энергии
оставшихся молекул, т. е. к охлаждению жидкости.
При конденсации происходит выделение
некоторого количества теплоты в окружающую
среду.
7. Испарение и конденсация
8. Кипение
L – удельная теплотапарообразования
9. Изменение агрегатных состояний вещества: плавление и кристаллизация
Плавление — переход вещества из твёрдогосостояния в жидкое.
Отвердевание или кристаллизация переход вещества из жидкого состояния в
твердое.
Температура при которой вещество начинает
плавиться называется температурой
плавления.
Во время плавления вещества его
температура не изменяется, т.к. энергия,
получаемая веществом, тратится на
разрушение кристаллической решетки. При
отвердевании образуется кристаллическая
решетка, при этом энергия выделяется и
температура вещества не изменяется.
У аморфных тел нет определенной
температуры плавления.
10.
 Плавление и отвердевание
Плавление и отвердевание11. Температура кипения воды зависит от
1. мощности нагревателя2. вещества сосуда, в котором нагревается вода
3. атмосферного давления
4. начальной температуры воды
12. Весной при таянии льда в водоеме температура окружающего воздуха
1.2.
3.
4.
уменьшается
увеличивается
не изменяется
может увеличиваться или уменьшаться
13. Как изменяется внутренняя энергия кристаллического вещества в процессе его плавления?
1. увеличивается для любого кристаллическоговещества
2. уменьшается для любого кристаллического
вещества
3. для одних кристаллических веществ
увеличивается, для других – уменьшается
4. не изменяется
14. Горячая жидкость медленно охлаждалась в стакане. В таблице приведены результаты измерений ее температуры с течением времени.
1.2.
3.
4.
только в жидком состоянии
только в твердом состоянии
и в жидком, и в твердом состояниях
и в жидком, и в газообразном состояниях
Основные формулы
при нагревании и
охлаждении
при горении
5.
 Количество теплоты
Количество теплотыпри плавлении и
кристаллизации
при
парообразовании
и конденсации
Q cm T
Q qm
Q m
Q rm
16. Температура и тепловое движение
17. Тепловое движение. Температура
Тепловое движение – беспорядочное движение молекулвещества.
В жидкостях и газах молекулы беспорядочно движутся, соударяясь друг с
другом.
В твёрдых телах тепловое движение состоит в колебаниях частиц около
положения равновесия.
От скорости движения молекул зависит температура тела. Чем больше
скорость движения молекул, тем выше температура тела.
Обратим внимание на то, что тепловое движение отличается от
механического тем, что в нём участвует очень много частиц и каждая
движется беспорядочно.
18. Тепловое движение молекул
Беспорядочное хаотическое движениемолекул называется тепловым
движением. Доказательством
теплового движения является
броуновское движение и диффузия.
Броуновское движение – это тепловое
движение мельчайших частиц,
взвешенных в жидкости или газе,
происходящее под действием ударов
молекул окружающей среды.

Диффузией называется явление
проникновения двух или нескольких
соприкасающихся веществ друг в
друга.
Скорость диффузии зависит от
агрегатного состояния вещества и
температуры тела.
19. Источник информации о температуре
температуреИз жизненного опыта нам известно, что различные
тела могут быть нагреты до различной степени.
Однако ощущение тепла и холода является
субъективным фактором.
Проверим это на опыте.
!
?
!
Вывод: с помощью ощущений
судить о температуре
невозможно!
20. Физический смысл температуры
Каков физический смысл температуры? Для этого надоответить на вопрос, чем холодная вода отличается от горячей?
Тёплая вода состоит из таких же молекул, как и холодная.
Опыт по диффузии в горячей и холодной воде показывает: чем
выше температура, тем больше проникновение одного
вещества в другое. Причиной диффузии является движение
молекул. Так как в горячей воде диффузия происходит быстрее,
значит и скорость движения молекул в ней выше.

В теле с большей температурой молекулы в среднем движутся
быстрее. Температура вещества определяется не только
средней скоростью движения молекул, но и их массой.
Температура является мерой средней кинетической
энергией частиц тела.
21. Термометр
Итак, у нас возникла проблема: нужно найти такой признакили такое свойство тел, которое ясно указывало бы на то, как
тело нагрето. Таким признаком может быть расширение тел
при нагревании.
Чем более нагрето тело, тем больше его объём, тем
интенсивнее хаотичное движение молекул и атомов.
Прибор, в котором используется такое свойство тел –
термометр. От греческого «therme» — тепло и «metreo» измеряю
Жидкостный термометр – прибор, принцип действия
которого основан на использовании свойства теплового
расширения жидкости. В зависимости от
температурной области жидкостный термометр
заполняют ртутью, этиловым спиртом и другими
жидкостями.
Любой термометр показывает свою собственную
температуру.
 Для определения температуры среды
Для определения температуры средытермометр надо поместить в эту среду и подождать до
тех пор, пока температура прибора перестанет
изменяться, приняв значение, равное температуре
среды.
22. Температурная шкала Цельсия
Температурная шкала Цельсия была предложена в 1742 годушведским учёным А. Цельсием и названа в его честь. За ноль
градусов шкалы Цельсия принимают температуру таяния льда,
а за 100 градусов – температуру кипения воды при нормальном
атмосферном давлении (760 мм. рт. ст.). Интервал между этими
температурами разделён на 100 равных частей , по 1 градусу
Цельсия (1°С).
23. Шкалы температур
Шкала Цельсия:Шкала
Кельвина
Шкала
Фаренгейта
24. Абсолютная температура
Температура характеризует степень нагретости тела.Тепловое равновесие – это такое состояние системы тел,
находящихся в тепловом контакте, при котором не
происходит теплопередачи от одного тела к другому, и все
макроскопические параметры тел остаются неизменными.

Температура – это физический параметр, одинаковый для
всех тел, находящихся в тепловом равновесии.
Для измерения температуры используются физические
приборы – термометры.
Существует минимально возможная температура, при
которой прекращается хаотическое движение молекул. Она
называется абсолютным нулем температуры.
Температурная шкала Кельвина называется абсолютной
шкалой температур.
T t 273
25. На рисунке показана часть шкалы термометра, висящего за окном. Температура воздуха на улице равна …..
1. 180С.2. 140С
3. 210С.
4. 220С.
26. Согласно расчетам, температура жидкости должна быть равна 143 К. Между тем термометр в сосуде показывает температуру не более –1300 С. Это озн
Согласно расчетам, температура жидкости должна быть равна143 К. Между тем термометр в сосуде показывает температуру
не более –1300 С. Это означает, что
1.
2.
3.
4.
термометр не рассчитан на высокие температуры и требует замены
термометр показывает более высокую температуру
термометр показывает более низкую температуру
термометр показывает расчетную температуру
27.
 Какой из перечисленных ниже опытов (А, Б или В) подтверждает вывод молекулярно-кинетической теории о том, что скорость молекул растет при ув1. только А
Какой из перечисленных ниже опытов (А, Б или В) подтверждает вывод молекулярно-кинетической теории о том, что скорость молекул растет при ув1. только А2. только Б
3. только В
4. А, Б и В
28. Внутренняя энергия
29. Внутренняя энергия
Все тела состоят из молекул, которые непрерывно движутся ивзаимодействуют друг с другом. Они обладают одновременно
кинетической и потенциальной энергией. Эти энергии и
составляют внутреннюю энергию тела.
Внутренняя энергия — это энергия движения и взаимодействия
частиц, из которых состоит тело.
Зависит:
1) от температуры
Не зависит :
2 ) массы тела
1) от механического
движения
3 ) агрегатного
состояния
2) от положения тела
относительно других тел
Молекулы обладают
потенциальной
энергией, т.к.
взаимодействуют
друг с другом
Еп зависит от
расстояния между
молекулами
(агрегатного
состояния вещества)
30
Молекулы обладают
кинетической
энергией, т.
 к.
к.непрерывно движутся
Ек зависит от
скорости движения
молекул
(температуры)
Внутренняя энергия тела
Евн = Еп + Ек всех молекул тела
31. Внутренняя энергия связана с температурой
• При понижениитемпературы Земного
шара всего на один
градус выделилась бы
энергия, примерно в
миллиард раз
превосходящая
вырабатываемую
ежегодно всеми
электростанциями мира!
32. При испарении жидкость остывает. Молекулярно-кинетическая теория объясняет это тем, что чаще всего жидкость покидают молекулы, кинетическ
При испарении жидкость остывает. Молекулярно-кинетическаятеория объясняет это тем, что чаще всего жидкость покидают
молекулы, кинетическая энергия которых
1. равна средней кинетической энергии молекул жидкости
2. превышает среднюю кинетическую энергию молекул
жидкости
3. меньше средней кинетической энергии молекул
жидкости
4. равна суммарной кинетической энергии молекул
жидкости
33.
 Способы изменения внутренней энергии
Способы изменения внутренней энергии34. Изменение внутренней энергии
35. Внутренняя энергия может превращаться в механическую
36. Превращение механической энергии во внутреннюю
Механическаяэнергия может
превращаться во
внутреннюю
энергию
37. Первый закон термодинамики
Первый закон термодинамики – это закон сохранения ипревращения энергии для термодинамической системы.
Изменение внутренней энергии системы при переходе ее из
одного состояния в другое равно сумме работы внешних сил
и количества теплоты, переданного системе.
U A Q
Если работу совершает система, а не внешние силы:
Q U A
Количество теплоты, переданное системе, идет на
изменение ее внутренней энергии и на совершение
системой работы над внешними телами.
38. Идеальному газу сообщили количество теплоты 400 Дж. Газ расширился, совершив работу 600 Дж. Внутренняя энергия газа при этом
1. увеличилась на 1000 Дж2. увеличилась на 200 Дж
3.
 уменьшилась на 1000 Дж
уменьшилась на 1000 Дж4. уменьшилась на 200 Дж
Q A U U Q A 400 600 200 Äæ
39. Количество теплоты
Количеством теплоты называютколичественную меру изменения
внутренней энергии тела при
теплообмене (теплопередаче).
Количество теплоты, необходимое для
нагревания тела или выделяемого им
при охлаждении:
с – удельная теплоемкость – физическая
величина, показывающая, какое
количество теплоты требуется для
нагревания 1 кг вещества на 1 0С.
Количество теплоты, выделяемое при
полном сгорании топлива.
q – удельная теплота сгорания –
величина, показывающая, какое
количество теплоты выделяется при
полном сгорании топлива массой 1 кг.
Q cm t 2 t1
Q qm
40. Теплоемкость вещества. Теплотворность топлива
41. Расчет количества теплоты
43. Тела, имеющие разные температуры, привели в соприкосновение двумя способами ( I и II ). Какое из перечисленных ниже утверждений является верн
1. В положении I теплопередача осуществляется от тела 1 к телу 2.
2. В положении II теплопередача осуществляется от тела 1 к телу 2.
3. В любом положении теплопередача осуществляется от тела 2
к телу 1.
4. Теплопередача осуществляется только в положении II.
44. Теплопередача
Теплопередача – это самопроизвольный процесспередачи теплоты, происходящий между телами с
разной температурой.
45. Теплопроводность
Теплопроводность – это вид теплообмена, прикотором происходит непосредственная
передача энергии от частиц более нагретой
части тела к частицам его менее нагретой
части.
Само вещество не перемещается вдоль телапереносится лишь энергия.
Механизм теплопроводности
Амплитуда колебаний атомов в узлах кристаллической решетки
в точке А меньше, чем в точке В.
Вследствие взаимодействия атомов друг с другом амплитуда
колебаний атомов, находящихся рядом с точкой В, возрастает.
Теплопроводность веществ
Металлы
обладают хорошей
теплопроводностью
Меньшей — обладают жидкости
Газы плохо проводят тепло
50.
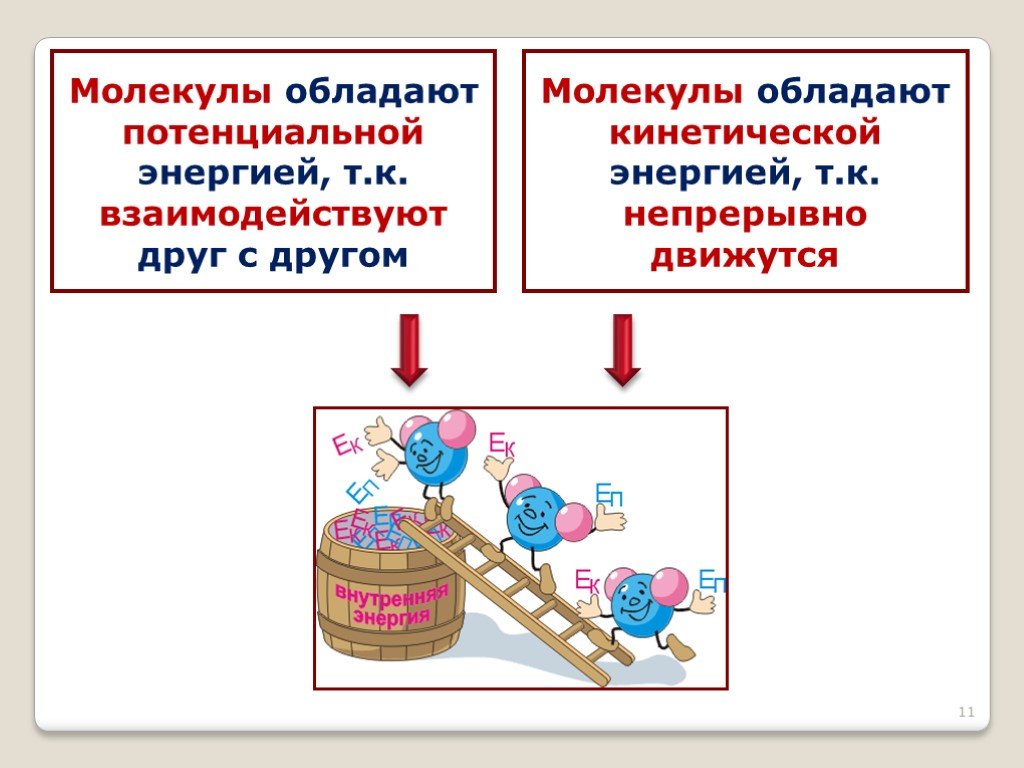 КонвекцияКонвекция – это перенос тепла струями
КонвекцияКонвекция – это перенос тепла струямижидкости или газа.
Конвекция в твердых телах и вакууме
происходить не может
Механизм конвекции в газах
Теплый воздух имеет меньшую плотность и со
стороны холодного воздуха на него действует сила
Архимеда, направленная вертикально вверх.
Механизм конвекции в жидкостях
А – жидкость нагревается
и вследствие
уменьшения ее
плотности, движется
вверх.
В – нагретая жидкость
поднимается вверх.
С – на место
поднявшейся жидкости
приходит холодная,
процесс повторяется.
В результате
конвекции
в атмосфере
образуются
ветры у моря это дневные
и ночные бризы.
охлаждается корпус
космического корабля,
обеспечивается водяное
охлаждение двигателей
внутреннего сгорания.
Где и почему именно там
размещают батареи в
помещениях?
57. Излучение
Солнце нагревает Землю, моря,океаны.
Однако причиной такой теплопередачи
не может быть ни теплопроводность,
ни конвекция!
Почему?
Тепло от костра передается человеку
путем излучения энергии,
так как теплопроводность воздуха мала,
а конвекционные потоки направлены вверх
ИЗЛУЧЕНИЕ — это теплообмен, при котором
энергия переносится различными лучами.

Механизм излучения
Нагретые тела
излучают
электромагнитные
волны
в различных
диапазонах.
Излучение может
распространяться
и
в вакууме
Около 50% энергии излучаемой Солнцем
является лучистой энергией, эта энергия источник жизни на Земле.
Почему одному мальчику жарко, а другому нет?
Темные тела лучше поглощают излучение и
быстрее нагреваются, чем светлые.
Темные тела быстрее охлаждаются
Какой из чайников быстрее остынет?
66. Применение в технике
сушка и нагревматериалов,
• приборы ночного
видения ( бинокли,
оптические прицелы),
• создание системы
самонаведения на
цель снарядов и
ракет.
67. Вопросы
Вопрос №1. Чашку с горячим чаемпереставили со стола на полку.
Как при этом изменилась внутренняя
энергия чая?
Ответ: Внутренняя энергия тела не
изменилась, т.к. она не зависит от
положения тела относительно
других тел.
67
Вопрос №2.
 Автомобиль в процессе
Автомобиль в процесседвижения изменил свою скорость
с 36 км/ч на 90 км/ч. Как при
этом изменилась его внутренняя
энергия?
Ответ: Внутренняя энергия тела
не изменилась, т.к. она не зависит
от механического движения тела.
68
Вопрос №3. Два одинаковых латунных
шара упали с одной и той же высоты.
Первый упал в глину, а второй,
ударившись о камень, отскочил и был
пойман рукой на некоторой высоте.
Который из шариков больше изменил
свою внутреннюю энергию?
Ответ: Первый. При падении
механическая энергия превращается во
внутреннюю. У второго шара только
часть механической энергии
превратилась во внутреннюю.
69
70. Домашнее задание
71. Лабораторная работа «Измерение температуры тела»
Цель работы: установление связи температуры тела с увеличениемкинетической энергии молекул.
Оборудование: термометр.
Ход работы
1. Зажмите термометр в кулаке, так чтобы видеть значение температуры на шкале.

2. Наблюдайте за подъёмом столбика ртути (спирта).
Ответьте письменно на вопросы :
1. Почему столбик ртути (спирта) поднимается вверх?
2. Когда столбик ртути (спирта) остановится?
3. Что измеряет термометр?
4. Можно ли вынимать термометр из среды, температуру которой измеряют? Почему?
5. Что можно сказать о величине кинетической энергии молекул ртути (спирта) при
подъёме столбика?
6. Каким прибором вы пользовались для определения температуры тела?
7. Какова цена деления этого прибора?
8. Какую минимальную (максимальную) температуру можно измерить этим прибором?
Вопросы
1. Какую энергию называют внутренней энергией?
2. В какую энергию превращается механическая
энергия мяча при его ударе о землю?
3. Может ли тело обладать механической энергией, но
не иметь при этом внутренней энергии?
4. Может ли тело обладать внутренней энергией, но не
иметь при этом механической энергии? Приведите
пример.
5. В одном стакане находится горячий чай, а в другом
стакане холодный компот такой же массы.
 Одинакова
Одинаковали их внутренняя энергия? Ответ обоснуйте.
72
73. Задачи
Количество теплоты. Тепловой баланс 8 класс онлайн-подготовка на Ростелеком Лицей
Введение
Все тела состоят из атомов и молекул, которые непрерывно движутся и взаимодействуют между собой. Нас интересует суммарная энергия их движения (кинетическая) и взаимодействия (потенциальная) – внутренняя энергия тела.
Внутреннюю энергию можно изменить двумя способами: выполняя работу и с помощью теплообмена.
Про механическую работу мы уже говорили, в ответвлении подробнее рассмотрим, как это связано с изменением внутренней энергии.
Механическая работа и превращение энергии
В механике мы использовали закон сохранения механической энергии:
Полная механическая энергия системы, в которой действуют только консервативные силы, остается постоянной.
Под полной механической энергией мы понимаем сумму кинетической и потенциальной энергии.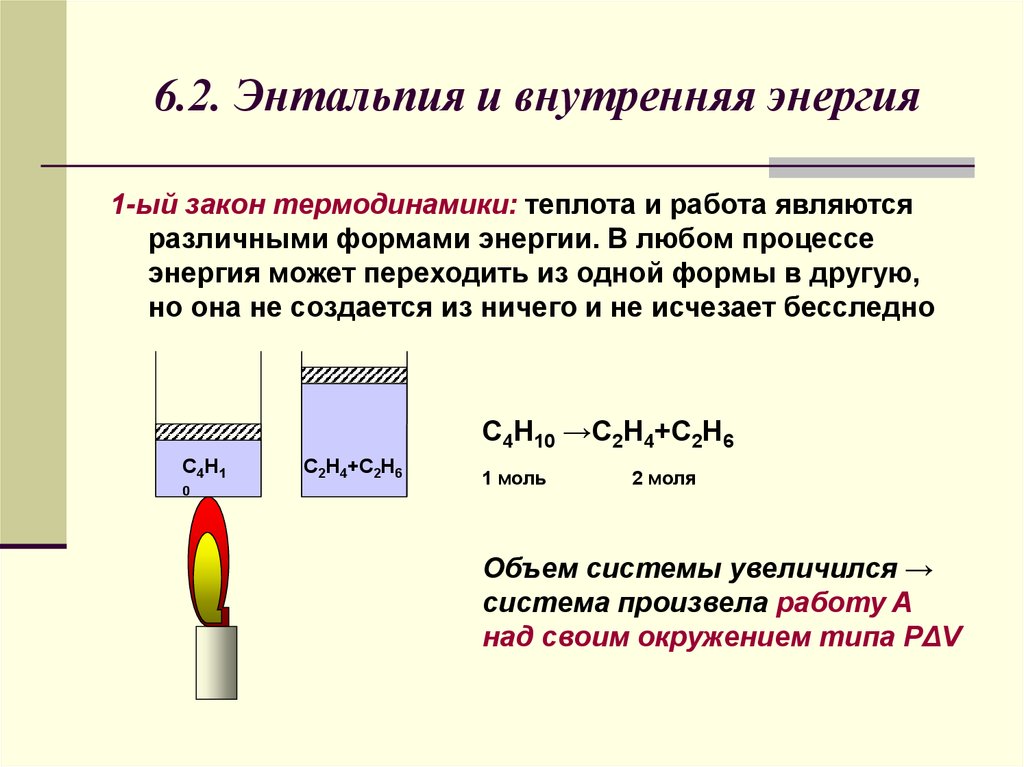 Значит, энергия превращается из кинетической в потенциальную, и наоборот, чтобы их сумма оставалась постоянной (см. рис. 1).
Значит, энергия превращается из кинетической в потенциальную, и наоборот, чтобы их сумма оставалась постоянной (см. рис. 1).
Рис. 1. Превращение кинетической и потенциальной энергий
Изменение кинетической энергии равно изменению потенциальной энергии со знаком минус – это значит, на сколько увеличилась кинетическая энергия, на столько же уменьшилась потенциальная. А работа консервативных сил равна этому изменению:
Что же происходит с энергией тела, если на него действуют неконсервативные силы, например сила трения? Механическая энергия не сохраняется, она превращается в другие виды энергии, в частности в тепловую (или внутреннюю энергию тела) (см. рис. 2).
Рис. 2. Превращение механической энергии в тепловую
Работа неконсервативной силы равна изменению механической энергии (а оно равно изменению внутренней энергии со знаком минус, для превращения кинетической энергии в потенциальную мы записывали так же).
При изучении тепловых явлений нас как раз интересует изменение внутренней энергии.
Передача энергии от более теплого объекта к менее теплому
Рассмотрим второй способ изменения внутренней энергии тела – это передача энергии от более теплого объекта к менее теплому. Назвали это теплопередачей и выделили виды теплопередачи: через излучение и через соударения молекул, назвав это теплопроводностью (см. рис. 3).
Рис. 3. Виды теплопередачи
Теплопередача может сопровождаться перемещением вещества, этот процесс мы назвали конвекцией.
Но для того чтобы количественно описывать тепловые процессы, нам недостаточно знать сам факт, что теплота передается.
Предположим, что в системе тел неконсервативные силы не совершают механическую работу. Рассмотрим энергию, которую передает или получает тело в результате теплообмена. Вследствие этого изменяется его внутренняя энергия. Эту полученную энергию, равную изменению внутренней энергии, назовем теплотой, а для ее количественного выражения часто будем употреблять название количество теплоты.
О терминах «теплота» и «количество теплоты»
Мы определили теплоту как энергию, которую передает или получает тело в процессе теплообмена. Это физическая величина, единицы измерения у нее те же, что и для энергии. То есть можно сказать «теплота равна 10 Дж» и т. д. Но в русском языке сложилась такая ситуация: если о многих других величинах можно сказать «какая масса?», «какая скорость?», то к теплоте более естественно применить вопрос «сколько?». То есть не «чему равна теплота?», а «сколько теплоты?», или, другими словами: «какое количество теплоты?». Это понятие, «количество теплоты», мы применяем наряду с понятием «теплота», но стоит помнить, что подразумевается одна и та же физическая величина. Просто иногда удобнее сказать «теплота передалась», а иногда «количество теплоты равно 10 Дж».
Обратите внимание: теплота равна изменению внутренней энергии тела. То есть мы не будем говорить об абсолютном количестве теплоты, а только о его изменении.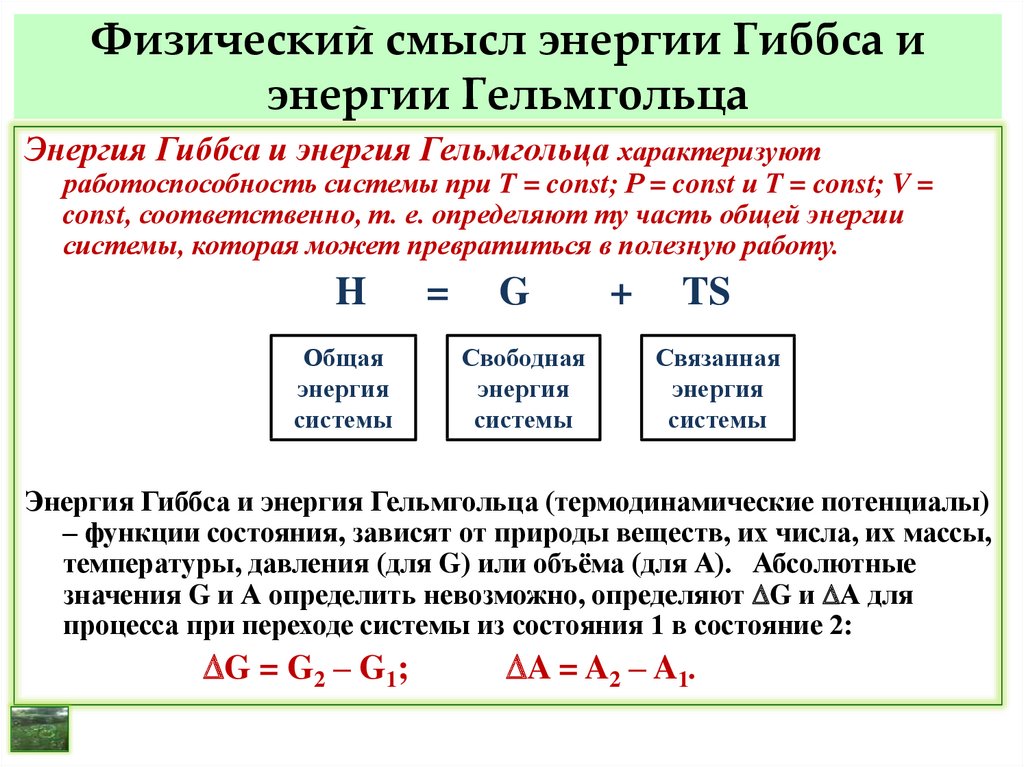 То есть отвечать на вопрос: «Сколько теплоты получило или передало тело?». А привычные нам понятия «тепло/холодно» лучше всего описывает такая физическая величина, как температура.
То есть отвечать на вопрос: «Сколько теплоты получило или передало тело?». А привычные нам понятия «тепло/холодно» лучше всего описывает такая физическая величина, как температура.
Ощущаем ли мы температуру?
Касаясь чашки с горячим чаем, вы чувствуете ее тепло (см. рис. 4).
Рис. 4. Чашка с горячим чаем
Кажется, что мы определяем ее температуру и можем судить о внутренней энергии. А попробуйте провести следующий опыт: опустите одну руку в теплую воду, другую – в холодную, чтобы руки «привыкли» к температуре (см. рис. 5).
Рис. 5. Проведение эксперимента
А затем поместите их обе в воду комнатной температуры. Одной рукой вы почувствуете холод, другой – тепло. Получается, что наши ощущения связаны не с абсолютным значением температуры тела, а с разностью температур тела и нашей руки и с направлением теплообмена между ними.
Одна рука чувствует тепло, поскольку теплота передается от воды к руке. А вторая рука чувствует холод, поскольку тепло передается от руки к воде. При этом в случае холодной воды это не вода передает руке холод, а рука отдает воде тепло.
При этом в случае холодной воды это не вода передает руке холод, а рука отдает воде тепло.
Конечно, мы иногда говорим «закрой дверь – холод напустишь» (как будто подразумеваем передачу именно холода), но это обывательский оборот, который закрепился в языке.
Например, при игре в пятнашки мы всегда двигаем сами «костяшки», но часто говорим о перемещении пустой клетки.
Мы говорим: «становится темно». Хотя темнота – это отсутствие света. Августин Блаженный говорил: «Нет зла, есть недостаток добра».
Так и с холодом – это отсутствие тепла. Нет передачи холода, есть теплопередача в том или ином направлении. Поэтому и лед, и чай, укутанные в шубу, будут некоторое время сохранять температуру, здесь у шубы одна и та же функция – теплоизоляция.
Количество теплоты
Обычно количество теплоты обозначается буквой Q. Количество теплоты – это изменение внутренней энергии при теплообмене, значит, эта величина измеряется, как и энергия, в джоулях: [Q] = Дж.
Обозначим внутреннюю энергию U. Тогда определение количества теплоты можно записать следующим образом:
Q = ΔU при равной нулю механической работе внешних сил (о чем мы договорились в начале урока).
Если тело получило 10 Дж теплоты и если тело потеряло 10 Дж теплоты – это не одно и то же (см. рис. 6).
Рис. 6. Получение и потеря теплоты
Как это обозначить? Для этого можем использовать удобный математический инструмент – отрицательные числа. Мы его уже использовали для обозначения направления движения. Если рассматривать прямолинейное движение вдоль одной прямой, удобно выбрать ось координат и одно направление считать положительным (см. рис. 7).
Рис. 7. Выбор положительного направления
В проекции на эту ось скорости тел 5 м/с и –5 м/с означают, что тела движутся со скоростью 5 м/с в противоположных направлениях.
Так и здесь: договоримся, что если тело получает теплоту (наши руки получили от теплой воды 10 Дж тепла), то Q положительно (запишем Q = 10 Дж), а если отдает – отрицательно, запишем Q = –10 Дж.
Остановимся пока на изучении тех случаев, когда агрегатное состояние вещества не меняется. Тогда если передать тепло телу, то оно нагреется, увеличится его температура (см. рис. 8)
.
Рис. 8. Агрегатное состояние вещества не изменяется при получении теплоты
Разберемся, как количественно описать этот процесс.
Чайник закипит быстрее, если в него залить теплую воду, а не холодную (см. рис. 9).
Рис. 9. Закипание чайника с теплой и холодной водой
То есть чем большей разности конечной и начальной температур нужно достичь, тем больше нужно передать энергии. Полный чайник будет закипать дольше, чем почти пустой (см. рис. 10).
Рис. 10. Закипание полного чайника и полупустого
То есть чем больше масса воды, тем больше нужно передать энергии, чтобы ее нагреть. И наверняка есть разница, нагреть на одни и те же 10 градусов килограмм воды или килограмм железа – это тоже нужно учесть (см. рис. 11).
Рис. 11. Нагревание разных веществ
Можно провести эксперименты и установить более точные закономерности.
Оказывается, количество теплоты, которое необходимо передать телу, прямо пропорционально изменению температуры: , где обозначает изменение температуры: конечная температура минус начальная .
Если тело отдает тепло, то оно охлаждается. Конечная температура будет меньше начальной: . Тогда . Количество теплоты также будет . Это согласуется с введенным понятием количества теплоты: если тело отдает тепло, то .
Экспериментально также было установлено, что: (количество теплоты, которое необходимо передать телу, прямо пропорционально массе тела).
Почему изменение внутренней энергии пропорционально массе?
Количество теплоты, которое получает тело, идет на увеличение его внутренней энергии. Внутренняя энергия – это суммарная энергия частиц вещества: атомов или молекул. Значит, изменение внутренней энергии должно быть пропорционально количеству частиц: .
Однако таким параметром, как количество молекул, мы пользуемся редко. Более удобной характеристикой, эквивалентной количеству частиц данного вещества, является масса.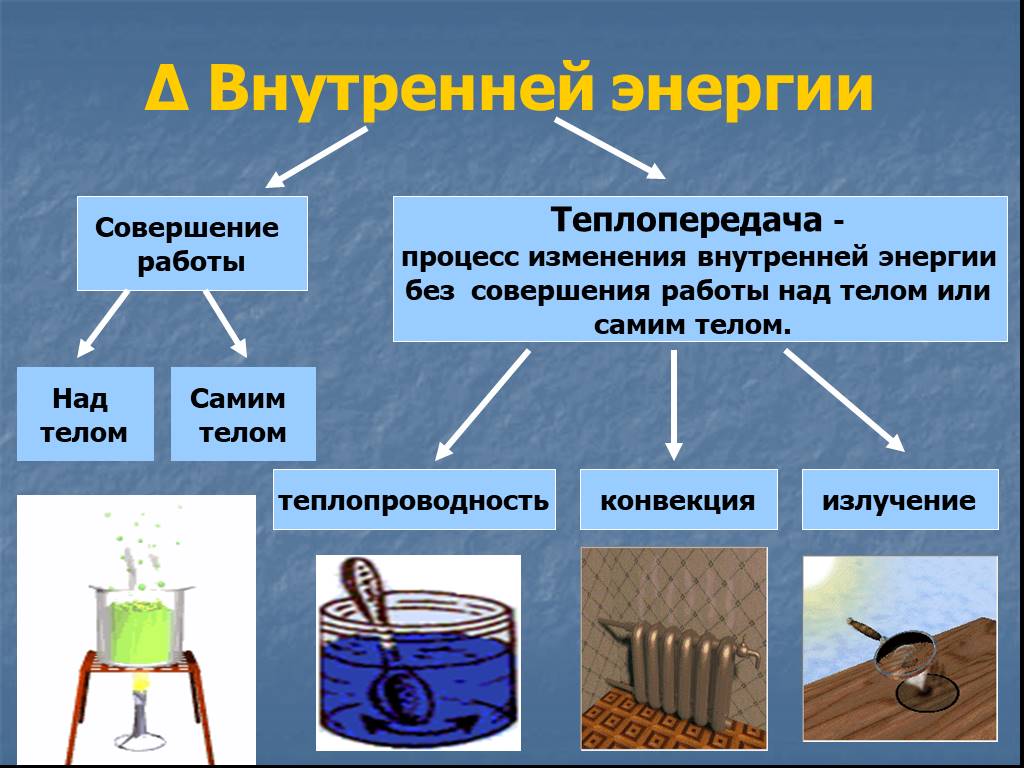
Масса вещества равна массе одной частицы (атома или молекулы), умноженной на количество частиц: , тогда количество молекул равно .
Получаем, что или , т. к. масса одной молекулы – величина постоянная для данного вещества и она будет заложена в коэффициенте пропорциональности, который определяется отдельно для каждого вещества и учитывает его параметры: массу молекул, связь между ними, связь кинетической энергии молекул и температуры и т. д.
Удельная теплоемкость
Количество теплоты пропорционально массе тела и изменению его температуры:
Кроме того, количество теплоты, необходимое для нагревания данной массы на данную температуру, зависит от вещества: для спирта нужно меньше теплоты, чем для воды (см. рис. 12), а для золота – меньше, чем для железа (см. рис. 13).
Рис. 12. Количество теплоты для нагревания воды и спирта
Рис. 13. Количество теплоты для нагревания железа и золота
Для данного вещества количество теплоты, которое нужно передать для нагревания данной m на данную , оказалось постоянной величиной.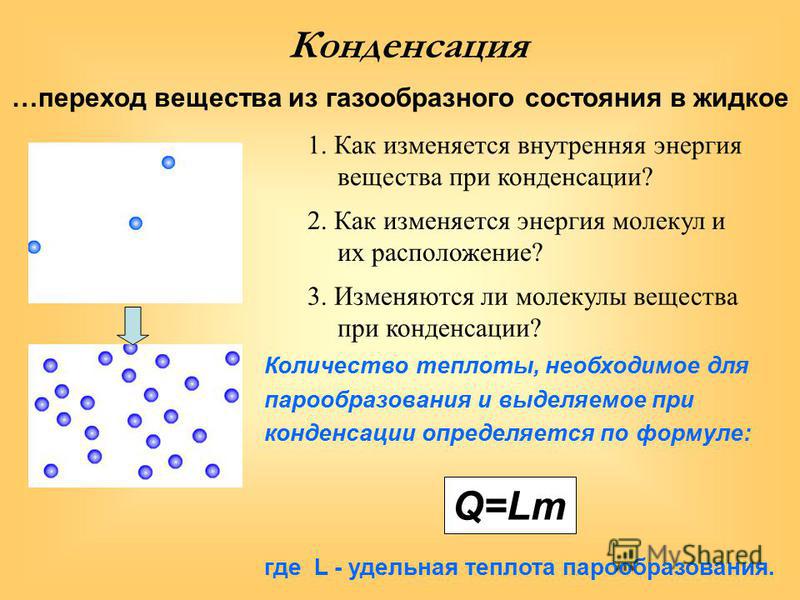
Отношение назвали удельной теплоемкостью, которую принято обозначать буквой c. Это количество теплоты, которое нужно передать 1 кг вещества, чтобы нагреть его на 1 °С (или 1 К, потому что мы говорим об изменении температуры, а цена деления этих двух шкал одинакова (см. рис. 14)).
Рис. 14. Шкалы температур Цельсия и Кельвина
Для разных веществ это отношение отличается.
Единицы измерения удельной теплоемкости:
Различные вещества имеют различные удельные теплоемкости. Почему это так – поговорим в ответвлении.
c = const
Удельная теплоемкость с зависит от температуры t. Чтобы нагреть один и тот же железный шарик с 10 градусов до 11 и с 200 до 201 – нужно разное количество теплоты (см. рис. 15).
Рис. 15. Нагрев одного и того же шарика на 1 градус
Изменение удельной теплоемкости с изменением температуры достаточно мало, поэтому для решения задач мы можем считать, что с = const и зависимость линейная (на участках, где не изменяется агрегатное состояние вещества (см. рис. 16)).
рис. 16)).
Рис. 16. Линейная зависимость на участках, где не изменяется агрегатное состояние вещества
На самом деле, с, кроме температуры, зависит и от давления, но обычно мы будем решать задачи, в которых описаны процессы при нормальном атмосферном давлении, поэтому и здесь можно считать с = const.
Почему у веществ различные удельные теплоемкости
Почему для нагревания одной и той же массы на одну и ту же температуру для разных веществ нужно разное количество энергии?
Мы определили внутреннюю энергию тела как сумму кинетической и потенциальной энергии всех частиц тела. Когда теплота передается телу, часть ее идет на увеличение кинетической энергии (а значит, увеличение температуры), а часть – на увеличение потенциальной энергии частиц (см. рис. 17).
Рис. 17. Внутренняя энергия тела
У разных веществ соотношение этих частей разное.
Например, двум разным телам передали 100 Дж теплоты (см. рис. 18).
рис. 18).
Рис. 18. Нагревание разных тел
У одного тела 40 Дж ушло в кинетическую энергию, а 60 – в потенциальную. У другого в кинетическую энергию перешло 20 Дж, 80 – в потенциальную. Итого тела получили одинаковое количество теплоты, но первое тело нагрелось больше, чем второе, т. к. кинетическая энергия его частиц увеличилась сильнее (40 Дж > 20 Дж). Это значит, что удельная теплоемкость второго вещества больше – ведь его труднее нагреть, чем первое.
Для разных веществ полученная энергия может распределяться по-разному – для нас это не ново.
Возьмем три мяча (см. рис. 19): хорошо накачанный, спущенный и деревянный.
Рис. 19. Опыт с тремя мячами
Если ударить по ним, сообщив одинаковую энергию, полетят они с разной скоростью. Часть переданной энергии пойдет на неупругую деформацию мяча и обуви бьющего, а часть – на увеличение кинетической энергии мяча. Для перечисленных мячей соотношение этих частей будет разное.
Значения удельных теплоемкостей различных веществ уже измерены, их можно найти в соответствующих таблицах.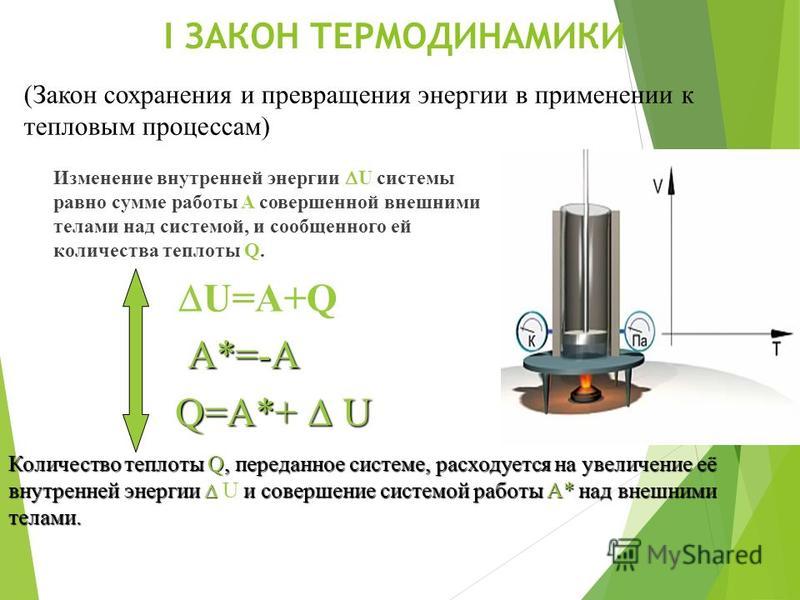
Итак, на основе всего вышесказанного можно записать формулу для расчета количества теплоты, необходимого для нагревания тела:
Процессы нагревания и охлаждения отличаются лишь знаком , так что формулу можно использовать и для расчета количества теплоты, которое выделяет тело при охлаждении.
Для задач, которые мы будем решать в ближайшее время, нам достаточно такого очевидного утверждения: тепло передается от тела с большей температурой к телу с меньшей температурой до тех пор, пока температуры этих тел не уравняются (см. рис. 20).
Рис. 20. Теплообмен между телами с разной температурой
Более точно эта закономерность сформулирована в виде законов термодинамики, но их мы будем подробно изучать позже.
Тепловой баланс
Мы сейчас рассматриваем изменение внутренней энергии тел через передачу теплоты. Если выделить систему тел, которые будем рассматривать вместе в рамках решения конкретной задачи, то возможны два варианта.
Первый – энергия может быть получена извне этой системы (см. рис. 21)
Рис. 21. Теплообмен с другими телами вне системы
(например, теплообмен с другими телами вне системы, превращение механической энергии в тепловую и т. д.). Второй вариант – считаем, что энергия передается посредством теплообмена только внутри системы, тогда суммарная энергия системы не меняется (см. рис. 22).
Рис. 22. Теплообмен только внутри системы
Рассмотрим первый случай, когда тепло передается системе тел извне.
Задача 1
В алюминиевой кастрюле массой 1,5 кг находится 5 кг воды при температуре 20 °С (см. рис. 23).
Рис. 23. Задача 1
Найти количество теплоты, необходимое для нагревания воды до температуры кипения. Передачей тепла в окружающую среду пренебречь.
Имеется два тела: кастрюля и вода. Нужно передать какое-то количество теплоты, чтобы нагреть их. Потерями тепла в окружающую среду пренебрегаем – значит, все тепло пойдет на нагревание кастрюли с водой.
Потери тепла
Предположим, что для выполнения условия задачи мы поставили кастрюлю с водой на электроплиту. Понятно, что часть тепла, которое выделяет плита, будет тратиться на нагревание кастрюли, окружающего воздуха и самой электроплиты (см. рис. 24).
Рис. 24. Потери тепла на нагревание кастрюли, окружающего воздуха и самой электроплиты
Это ненужные нам «потери тепла», как их называют. Но без них не обойтись – кастрюля и окружающий воздух неизбежно будут греться вместе с водой.
Обычно потери тепла незначительные и мы их можем не учитывать. Если в задаче отдельно не оговорено иное, потерями при решении пренебрегаем. Если же мы хотим получить более точное решение, придется учитывать (и рассчитывать) эти потери.
В нашей задаче в условии прямо сказано: «Передачей тепла в окружающую среду пренебречь».
Если бы в условии не были даны материал и масса кастрюли, то подразумевалось бы, что нагреванием самой кастрюли тоже можно пренебречь. Однако в данной конкретной задаче сказано, что кастрюля алюминиевая (то есть можно найти ее удельную теплоемкость по таблице), а также дана масса кастрюли. Значит, можно и нужно посчитать, какое количество теплоты пойдет на нагревание самой кастрюли.
Однако в данной конкретной задаче сказано, что кастрюля алюминиевая (то есть можно найти ее удельную теплоемкость по таблице), а также дана масса кастрюли. Значит, можно и нужно посчитать, какое количество теплоты пойдет на нагревание самой кастрюли.
Для нагревания алюминиевой кастрюли нужно:
Для нагревания воды нужно:
Всего нужно передать:
Массы воды и кастрюли даны в условии, удельные теплоемкости можно найти в таблице. Вода должна нагреться от до кипения, то есть до . Кастрюля нагревается вместе с водой, поэтому изменение ее температуры будет таким же:
Осталось подставить численные данные и найти ответ.
Решение задачи
Итак, мы получили систему уравнений:
Численные данные из условия:
Из таблицы:
Вычисляем:
Ответ: .
В предыдущем ответвлении мы говорили о том, учитывать ли потери теплоты.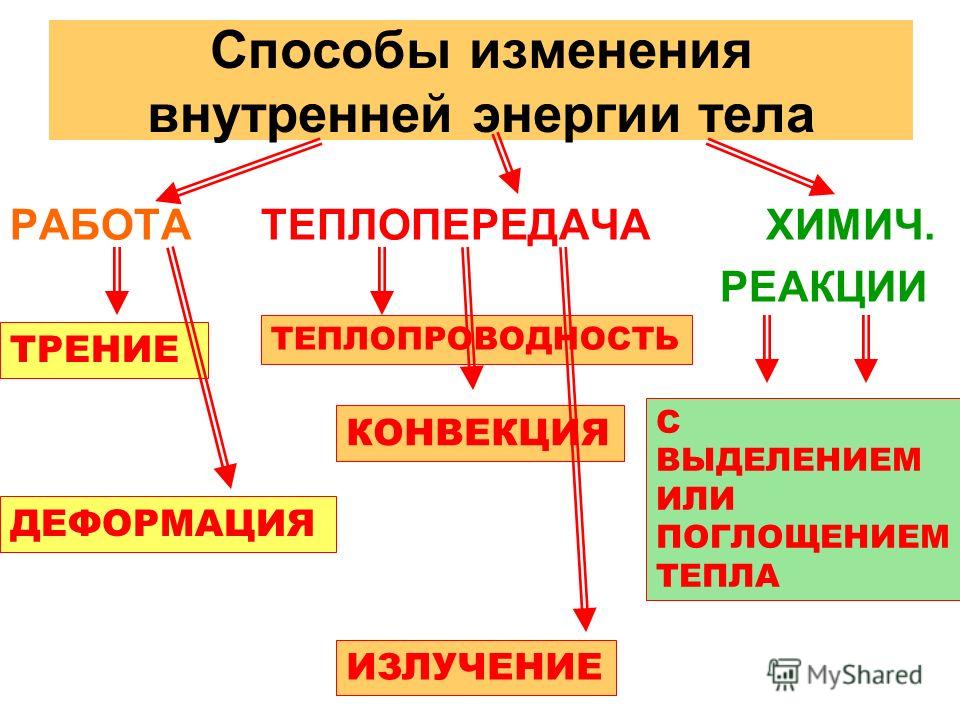 В данной задаче мы пренебрегли потерями на нагревание окружающего воздуха, но учли нагрев кастрюли. Если решить задачу, не учитывая нагрев кастрюли, останется количество теплоты, необходимое для нагревания только воды:
В данной задаче мы пренебрегли потерями на нагревание окружающего воздуха, но учли нагрев кастрюли. Если решить задачу, не учитывая нагрев кастрюли, останется количество теплоты, необходимое для нагревания только воды:
Как видим, этот результат отличается от полученного ранее приблизительно на 6 %. Много это или мало – зависит от цели. Если мы греем воду для чая, то погрешностью в 6 % можно пренебречь. Если же вода нужна для выращивания клеток в биологической лаборатории со строгим температурным режимом, то 6 % могут оказаться очень большой разницей и пренебрегать нельзя.
Теперь рассмотрим модель, в которой можно не учитывать теплообмен системы тел с окружающими телами: тепло только передается от одного тела к другому.
Задача 2
В чашке находится горячий чай при температуре 95 °С (см. рис. 25).
Рис. 25. Задача 2
Масса чая – 150 г. Определите массу холодной воды, которую нужно долить в чашку с чаем, чтобы понизить температуру чая до 60 °С. Температура холодной воды – 5 °С. Теплоемкость чая считать равной теплоемкости воды, потерями тепла пренебречь.
Температура холодной воды – 5 °С. Теплоемкость чая считать равной теплоемкости воды, потерями тепла пренебречь.
Почему чай будет остывать? Мы долили в чашку холодную воду, поэтому чай будет отдавать тепло, его температура будет уменьшаться (см. рис. 26).
Рис. 26. Доливание холодной воды в чашку
Вода будет получать тепло, ее температура будет увеличиваться. В некоторый момент температура воды станет равной температуре чая, теплообмен прекратится. В условии сказано, что потерями тепла можно пренебречь, значит, все тепло, которое отдал чай, получит вода.
Чай отдал , вода получила . Тогда .
Откуда в формуле появились модули
Было оговорено, что направление теплопередачи обозначать знаком количества теплоты: плюс – если тело получает теплоту, и минус – если отдает (см. рис. 27).
Рис. 27. Получение (слева) и отдача (справа) теплоты
Если записывать как , знак Q получится таким, как мы договорились.
Можно использовать такой подход: записать общее количество теплоты для всех тел ( и приравнять его к нулю – суммарная внутренняя энергия системы не изменилась, теплообмен вне системы равен нулю:
Q чая и воды имеют противоположные знаки.
Можно направление теплообмена учесть по-другому: записать модули и (то есть при вычислении просто от большей температуры отнимаем меньшую), но перенести в правую часть уравнения переданную теплоту, оставив в левой части полученную:
То есть сколько тепла отдал горячий чай, столько и получила холодная вода.
Решать задачи можно любым удобным способом, главное, чтобы направление теплообмена было учтено правильно.
Из условия: ; изменения температур: , . На этом физическая часть решения закончена, осталось лишь выразить неизвестную величину, подставить численные значение и получить ответ.
Решение задачи
Имеем систему уравнений:
Уравнений много, но все они очень простые. Подставим значения и найдем изменение температуры:
Второе и третье уравнение подставим в первое:
С учетом , сократим на теплоемкость:
Подставим численные значения:
Если в задаче будет больше тел, то алгоритм решения будет аналогичным:
1) определить, какие тела получают тепло, а какие отдают;
2) записать общее количество теплоты, которое было отдано и которое было получено телами;
3) приравнять модули полученного и отданного тепла.
Либо же не брать модули, оставить разные знаки Q для разных направлений теплообмена и сумму Q внутри замкнутой системы приравнять нулю, как мы показали в ответвлении.
А дальше останется только техника – математические расчеты.
Итоги
В подобных задачах всегда есть баланс: сколько теплоты одни тела отдают, столько другие тела получают. Они так и называются: задачи на тепловой баланс. В этом уроке мы рассмотрели процессы, при которых изменялась температура, но не рассмотрели процессы изменения агрегатного состояния вещества. Но мы можем взять лед при температуре 0 ℃, расплавить его и получить воду при 0 ℃ – ∆t равно нулю (см. рис. 28).
Рис. 28. Плавление льда
Греть его для этого нужно, энергии этот процесс требует. Значит, здесь что-то другое, модель не работает.
Например, тепло полученное от солнца, идет на то, чтобы расплавить лед в замерзших лужах. Другой пример: если надолго оставить на плите кастрюлю с водой, то тепло будет тратиться на испарение воды, превращение ее в пар. Как решать задачи с процессами агрегатных превращений – плавлением, парообразованием и пр. – мы рассмотрим на следующем уроке.
Как решать задачи с процессами агрегатных превращений – плавлением, парообразованием и пр. – мы рассмотрим на следующем уроке.
Список литературы
- Соколович Ю.А., Богданова Г.С. Физика: справочник с примерами решения задач. – 2-е издание, передел. – X.: Веста: издательство «Ранок», 2005. – 464 с.
- А.В. Перышкин. Физика 8 кл.: учеб. для общеобразоват. учреждений. – М.: Дрофа, 2013. – 237 с.
Дополнительные рекомендованные ссылки на ресурсы сети Интернет
- Сайт объединения учителей Санкт-Петербурга (Источник)
- Интернет-сайт «Класс!ная физика — для любознательных» (Источник)
- 3Интернет-сайт «Класс!ная физика — для любознательных» (Источник)
Домашнее задание
- Какие вы знаете способы изменения внутренней энергии?
- Назовите 3 вида теплопередачи. В каком из них теплопередача может сопровождаться перемещением вещества?
- Что такое количество теплоты, в каких единицах оно измеряется?
- Что такое удельная теплоемкость вещества? В каких единицах она измеряется? Где ее можно посмотреть?
- Металлическую деталь, масса которой 200 г, нагрели до 100 , а затем опустили в воду массой 800 г и температурой 20 .
 Через некоторое время температура воды и детали стала равна 25 °С. Определите удельную теплоемкость металлической детали. Тепловыми потерями пренебречь.
Через некоторое время температура воды и детали стала равна 25 °С. Определите удельную теплоемкость металлической детали. Тепловыми потерями пренебречь.
|
Теперь представьте, что такое же количество спирта помещено в большую колбу, из которой выкачан весь воздух. Энергия, необходимая для испарения спирта, меньше на 49,2 Дж. Почему требуется больше энергии, когда алкоголь испаряется в пластиковом пакете? Подумайте о том, что произошло, когда спирт испарился в колбе. Поскольку другого газа там не было, спирт мог свободно расширяться и занимать весь объем внутри колбы. С другой стороны, когда спирт в пакете испарялся, ему приходилось поднимать пакет. Ученые называют это энтальпией . Энтальпия – это энергия, вложенная в систему, которая не совершает работы по изменению объема системы. Математически мы можем записать это как: ДЭ = ДХ + ш где H — энтальпия, а DH — изменение энтальпии. Это еще один способ сформулировать Первый закон термодинамики (см. Модуль «Энергия»): все изменения энергии, которые претерпевает система во время любого процесса, полностью объясняются энтальпией и работой, поступающей в систему или покидающей ее. В общем случае, если в системе нет изменения громкости, DE и DH одинаковы. Однако при увеличении объема DH будет меньше DE из-за работы, связанной с отталкиванием атмосферы. Если есть уменьшение объема, DH будет больше, чем DE, потому что атмосфера действует на систему. Поскольку значение изменения энтальпии реакции зависит от состояния воздуха вокруг системы, что, в свою очередь, зависит от температуры и давления в данный момент, ученые остановились на стандартных значениях, о которых следует сообщать. Когда реакция протекает при давлении 1 атм, говорят, что условия равны 9.0126 стандартных условиях , а изменение энтальпии называется стандартным изменением энтальпии (DHº) (то же самое относится и к другим термодинамическим функциям, которые будут обсуждаться в последующих модулях). Каждый раз, когда вы видите символ термодинамической величины, за которым следует знак градуса (º), вы должны автоматически думать о стандартных условиях: 1 атм давления. Температура обычно также влияет на термодинамические значения, поэтому в таблицах этих значений также должно быть указано, при какой температуре они применяются. Чаще всего используется температура 25 ºC. В большей части химии, за исключением случаев, когда речь идет о газах, изменение объема невелико. | ||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||
7.3: Внутренняя энергия, работа и теплота
- Последнее обновление
- Сохранить как PDF
- Идентификатор страницы
- 156361
ф43.0
Цели обучения
- Определить тип работы с точки зрения давления и объема.

- Определить нагрев .
- Свяжите количество тепла с изменением температуры.
- Определите и рассчитайте изменения внутренней энергии системы.
Работа
Мы уже определили работу как силу, действующую на расстоянии. Оказывается, есть и другие эквивалентные определения работы, которые также важны в химии.
Когда определенный объем газа расширяется, он расширяется против внешнего давления (рис. 7.3.1 — Объем против давления)
То есть газ должен совершить работу. Предполагая, что внешнее давление P ext постоянно, количество работы, совершаемой газом, определяется уравнением V — изменение объема газа. Этот член всегда представляет собой конечный объем минус начальный объем,
Δ V = V конечная − V начальная
и может быть положительной или отрицательной, в зависимости от того, V конечная расширяется (сжимается больше) чем V начальный . Отрицательный знак в уравнении для работы важен и подразумевает, что по мере увеличения объема (Δ V положителен) газ в системе теряет энергии в виде работы. С другой стороны, если газ сжимается, Δ V отрицательно, а два отрицательных знака делают работу положительной, поэтому в систему добавляется энергия.
Отрицательный знак в уравнении для работы важен и подразумевает, что по мере увеличения объема (Δ V положителен) газ в системе теряет энергии в виде работы. С другой стороны, если газ сжимается, Δ V отрицательно, а два отрицательных знака делают работу положительной, поэтому в систему добавляется энергия.
Рис. 7.3.1 Объем в зависимости от давления
Когда газ расширяется против внешнего давления, он совершает работу.
Наконец, давайте рассмотрим единицы. Изменения объема обычно выражаются в таких единицах, как литры, а давление обычно выражается в атмосферах. Когда мы используем уравнение для определения работы, единицей измерения работы выступает литр·атмосфер, или л·атм. Это не очень распространенный агрегат для работы. Однако существует коэффициент пересчета между L·atm и общепринятой единицей работы, джоулями:
1 л·атм = 101,32 Дж
Используя этот коэффициент преобразования и предыдущее уравнение для работы, мы можем рассчитать работу, совершаемую при расширении или сжатии газа.
Пример \(\PageIndex{1}\):
Какую работу совершает газ, если он расширяется с 3,44 л до 6,19 л при постоянном внешнем давлении 1,26 атм? Выразите окончательный ответ в джоулях.
Решение
Сначала нам нужно определить изменение объема, Δ V . Изменение всегда представляет собой конечное значение минус начальное значение:
Δ V = V Окончательный — V Начальный = 6,19 л — 3,44 л = 2,75 л
Теперь мы можем использовать определение работы, чтобы определить работу. = − P ext · Δ V = −(1,26 атм)(2,75 л) = −3,47 л·атм
Теперь построим коэффициент пересчета из соотношения между литрами·атмосфер и джоулями:
\ [-3.47\not{L.atm}\times \times \frac{101.32\, J}{1\not{L.atm}}=-351\, J\]
При необходимости мы ограничиваем окончательный ответ тремя значащими цифрами.
Упражнение \(\PageIndex{1}\)
Проверь себя
Какова работа, совершаемая при расширении газа с 0,66 л до 1,33 л при внешнем давлении 0,775 атм?
Ответ
−53 Дж
Тепло
Тепло — еще один аспект энергии. Теплота — это передача энергии от одного тела к другому из-за разницы температур. Например, когда мы прикасаемся к чему-то руками, мы интерпретируем этот объект как горячий или холодный в зависимости от того, как передается энергия: если энергия передается в ваши руки, объект кажется горячим. Если энергия передается от ваших рук к объекту, ваши руки кажутся холодными. Поскольку теплота является мерой передачи энергии, теплота также измеряется в джоулях.
Теплота — это передача энергии от одного тела к другому из-за разницы температур. Например, когда мы прикасаемся к чему-то руками, мы интерпретируем этот объект как горячий или холодный в зависимости от того, как передается энергия: если энергия передается в ваши руки, объект кажется горячим. Если энергия передается от ваших рук к объекту, ваши руки кажутся холодными. Поскольку теплота является мерой передачи энергии, теплота также измеряется в джоулях.
Для данного объекта количество тепла ( q ) пропорционально двум вещам: массе объекта ( m ) и изменению температуры (Δ T ), вызванному передачей энергии. Мы можем записать это математически как
\[q\alpha \, m\times \Delta T\]
, где ∝ означает «пропорционально». Чтобы сделать пропорциональность равенством, мы включаем константу пропорциональности. В этом случае константа пропорциональности обозначается c и называется удельная теплоемкость , или, более кратко, удельная теплоемкость :
q = mc Δ T
где масса, удельная теплоемкость и изменение температуры перемножаются. Удельная теплоемкость — это мера того, сколько энергии необходимо для изменения температуры вещества; чем больше удельная теплоемкость, тем больше энергии необходимо для изменения температуры. Единицы удельной теплоемкости:
Удельная теплоемкость — это мера того, сколько энергии необходимо для изменения температуры вещества; чем больше удельная теплоемкость, тем больше энергии необходимо для изменения температуры. Единицы удельной теплоемкости:
\[\frac{J}{g.C}\, или\, \frac{J}{g.K}\]
в зависимости от единицы измерения Δ T . Вы можете заметить отход от требования выражать температуру в градусах Кельвина. Это потому, что изменение температуры имеет одно и то же значение, независимо от того, выражены ли температуры в градусах Цельсия или кельвинах.
Пример \(\PageIndex{2}\):
Рассчитайте теплоту, выделяемую при повышении температуры 25,0 г Fe с 22°C до 76°C. Удельная теплоемкость Fe составляет 0,449 Дж/г·°С.
Раствор
9{\circ}C)=610\, J\] Обратите внимание, что единицы g и °C сокращаются, оставляя J единицей тепла. Также обратите внимание, что это значение q по своей природе положительно, что означает, что энергия поступает в систему.
Упражнение \(\PageIndex{2}\)
Проверь себя
Рассчитайте количество тепла, которое выделяется, когда 76,5 г Ag повышают температуру с 17,8°C до 144,5°C. Удельная теплоемкость Ag составляет 0,233 Дж/г·°С.
Ответ
2,260 Дж
Как и в любом уравнении, когда в выражении для 9 известны все переменные, кроме одной0126 q , оставшуюся переменную можно определить с помощью алгебры.
Пример \(\PageIndex{3}\):
Для повышения температуры 373 г Hg на 104°C требуется 5408 Дж тепла. Какова удельная теплоемкость ртути?
Решение
Мы можем начать с уравнения для q , но теперь даны другие значения, и нам нужно решить для удельной теплоемкости. Обратите внимание, что Δ T дается непосредственно как 104°C. Замена,
5,408 Дж = (373 г) с 9{\circ}C}\]
Упражнение \(\PageIndex{3}\)
Проверь себя
Золото имеет удельную теплоемкость 0,129 Дж/г·°C.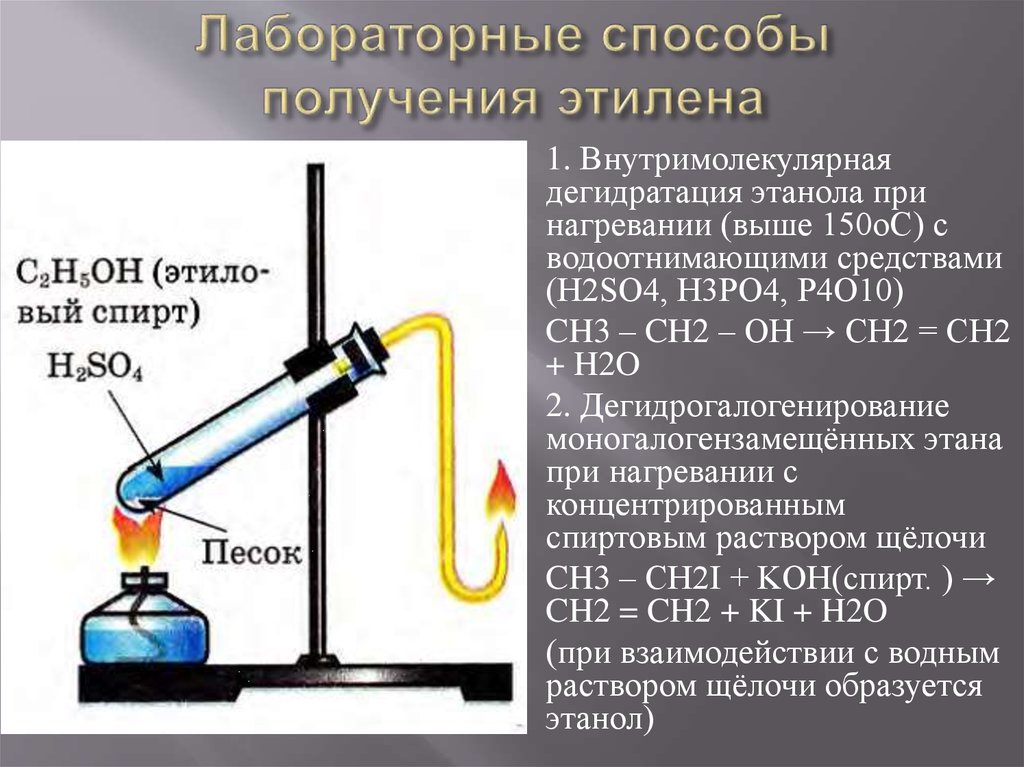 Если для повышения температуры образца золота на 99,9 °С требуется 1377 Дж, то какова масса золота?
Если для повышения температуры образца золота на 99,9 °С требуется 1377 Дж, то какова масса золота?
Ответ
107 г
| Вещество | Удельная теплоемкость (Дж/г·°C) | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| вода | 4.184 | |||||||||||||
| железо | 0,449 | |||||||||||||
| золото | 0,129 | |||||||||||||
| ртуть | 0,139 | |||||||||||||
| алюминий | 0,900 | |||||||||||||
| спирт этиловый | 2,419 | |||||||||||||
| магний | 1,03 | |||||||||||||
| гелий | 5.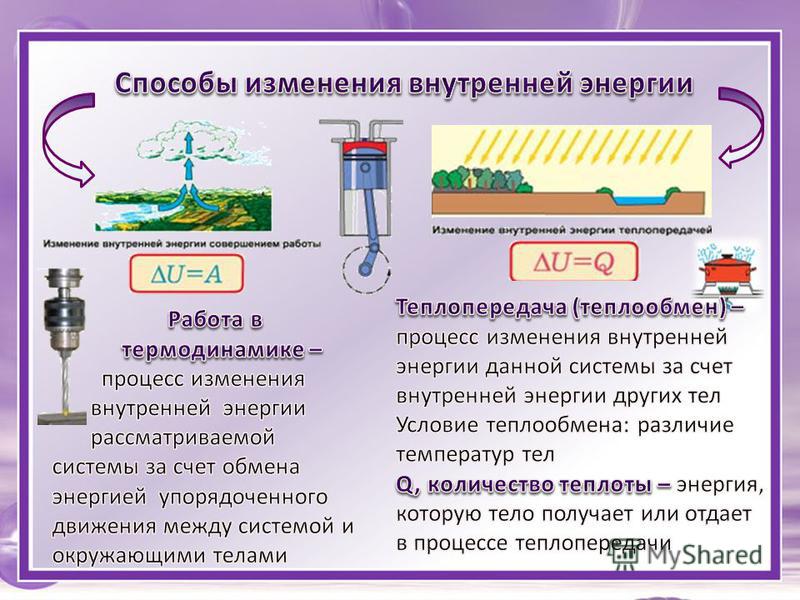 171 171 | |||||||||||||
| кислород | 0,918 | Таблица 7.3.1 Удельная теплоемкость различных веществ Эта энергия может принимать форму работы или тепла. Мы используем символ ΔE для обозначения любых изменений внутренней энергии системы и учитываем эти изменения с помощью работы и тепла 9.0057
| Энергия | Изменить | Знак |
|---|---|---|
| | Тепло, получаемое системой (эндотермическое) | +q |
| Потери тепла системой (экзотермические) | -к | |
| ш | Произведена работа над системой (сжатие) | + ш |
| Работа выполняется системой (расширение) | -ш |
При сохранении энергии любое изменение энергии системы должно учитывать любую энергию, полученную системой, и любую энергию, потерянную системой.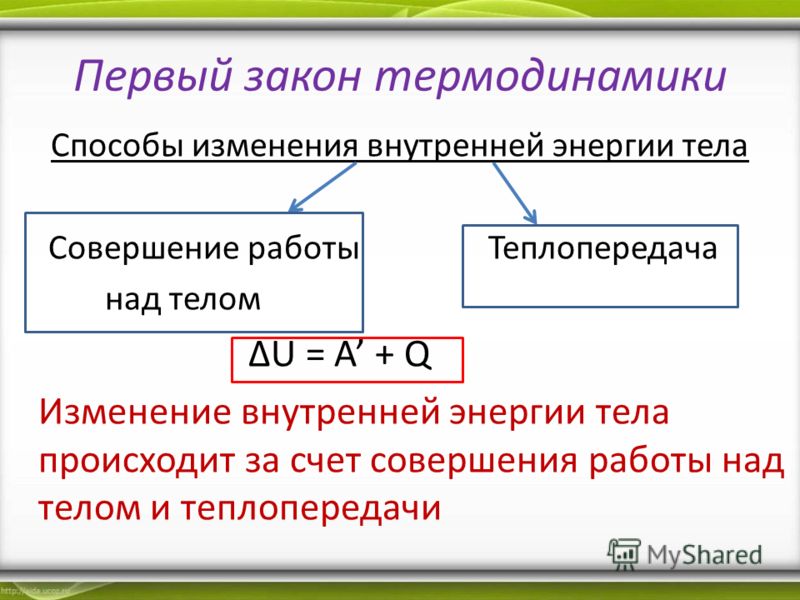
Пример \(\PageIndex{4}\):
Как изменится внутренняя энергия газа, если газ получит 10 кДж теплоты и расширится, совершив 5 кДж работы?
Раствор
Мы можем использовать
\[\Delta E = q + w\]
В качестве газа (наша система) получила 10 кДж тепла, q положительна
\[q = +10 \,кДж\]
Система работала, используя энергию в процессе, поэтому система потеряла энергии и Вт отрицательно.
\[w = -5\, кДж\]
Складываем вместе
\[\Delta E = q + w = 10 \,кДж + (-5 \,кДж) = 10\, кДж — 5 \ ,kJ = +5\, kJ\]
Таким образом, система получила всего 5 кДж энергии.
Ключевые выводы
- Работу можно определить как изменение объема газа при постоянном внешнем давлении.
- Тепло – это передача энергии за счет разницы температур.
- Теплота может быть рассчитана с точки зрения массы, изменения температуры и удельной теплоемкости.

- Полное изменение внутренней энергии системы равно сумме работы и теплоты
Упражнение \(\PageIndex{1}\)
- Дайте два определения работы.
Какой знак работы при увеличении объема пробы газа? Объясните, почему работа имеет этот знак.
Какова работа, когда газ расширяется с 3,00 л до 12,60 л при внешнем давлении 0,888 атм?
Какова работа, когда газ расширяется с 0,666 л до 2,334 л при внешнем давлении 2,07 атм?
Какова работа, когда газ сжимается с 3,45 л до 0,97 л при внешнем давлении 0,985 атм?
Какова работа, когда газ сжимается с 4,66 л до 1,22 л при внешнем давлении 3,97 атм?
Как и работа, знак теплоты может быть положительным или отрицательным. Что происходит с полной энергией системы, если теплота положительна?
Как и работа, знак теплоты может быть положительным или отрицательным.
 Что происходит с полной энергией системы, если теплота отрицательна?
Что происходит с полной энергией системы, если теплота отрицательна?Какова теплота, если 55,6 г железа повышают температуру с 25,6°С до 177,9°С? Теплоемкость Fe указана в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Какова теплота, если 0,444 г Au повышают температуру с 17,8°C до 222,5°C? Теплоемкость золота указана в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Какое тепло будет, если 245 г H 2 O охладить с 355 К до 298 К? Теплоемкость H 2 O указана в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Какое количество теплоты выделяется при охлаждении 100,0 г Mg с 725 К до 552 К? Теплоемкость Mg указана в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Чтобы поднять температуру образца металла массой 36,8 г с 22,9°C до 98,2°C, требуется 452 Дж тепла.
 Какова теплоемкость металла?
Какова теплоемкость металла?Требуется 2267 Дж тепла, чтобы поднять температуру образца металла массой 44,5 г с 33,9°С до 288,3°С. Какова теплоемкость металла?
Экспериментатор нагревает 336 Дж к образцу Hg весом 56,2 г. Каково его изменение температуры? Теплоемкость ртути указана в таблице 7.3.1 «Удельная теплоемкость различных веществ».
К 0,444 г образца H 2 O добавляют 23,4 Дж тепла. Каково его изменение температуры? Теплоемкость H 2 O находится в таблице 7.3.1 «Удельная теплоемкость различных веществ».
Алюминий неизвестной массы поглощает 187,9 Дж тепла и повышает свою температуру с 23,5°С до 35,6°С. Какова масса алюминия? Сколько это молей алюминия?

 Через некоторое время температура воды и детали стала равна 25 °С. Определите удельную теплоемкость металлической детали. Тепловыми потерями пренебречь.
Через некоторое время температура воды и детали стала равна 25 °С. Определите удельную теплоемкость металлической детали. Тепловыми потерями пренебречь.



 Таким образом, DH и DE похожи и могут использоваться взаимозаменяемо в хорошем первом приближении. Таким образом, в оставшейся части этого руководства вместо энергии будет использоваться энтальпия.
Таким образом, DH и DE похожи и могут использоваться взаимозаменяемо в хорошем первом приближении. Таким образом, в оставшейся части этого руководства вместо энергии будет использоваться энтальпия.

 Что происходит с полной энергией системы, если теплота отрицательна?
Что происходит с полной энергией системы, если теплота отрицательна? Какова теплоемкость металла?
Какова теплоемкость металла?
Leave A Comment