ЕГЭ 2018. Химия. Вариант 26 – iq2u – Тесты. Тест. Тесты онлайн. Онлайн тесты. Онлайн тест. Тест онлайн. Тестирование. Тесты с ответами. Пройти тест
Пройдите тест, узнайте свой уровень и посмотрите правильные ответы!
Категория:
Химия
Уровень:
ЕГЭ
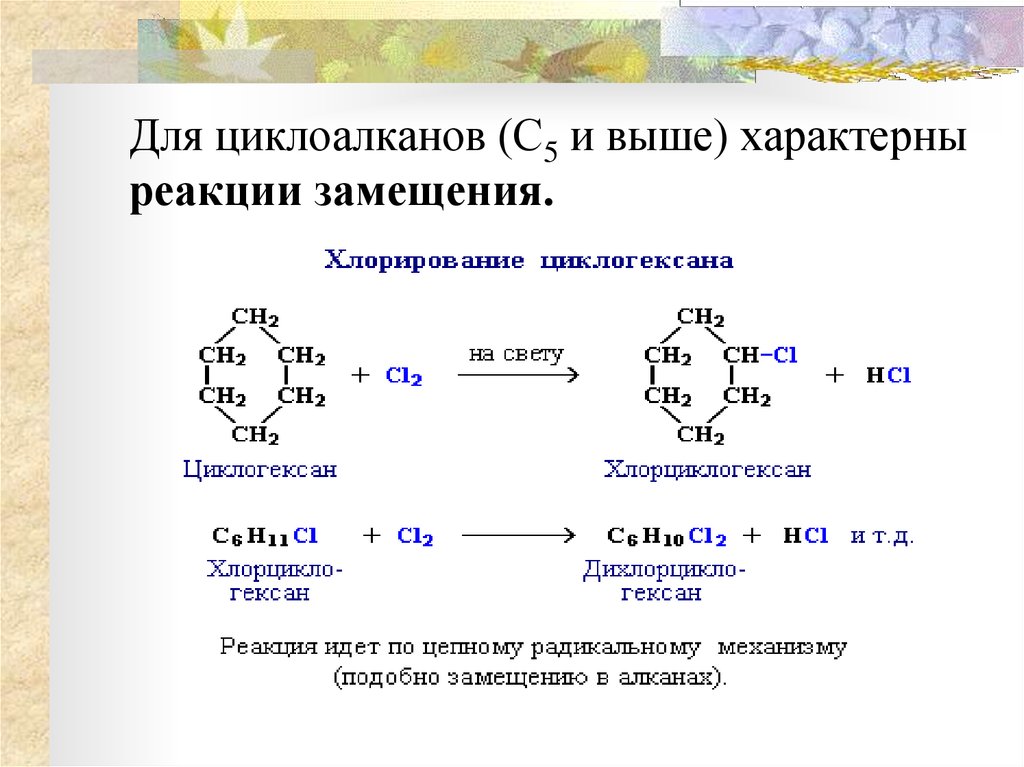
Циклопропан, в отличие от пропана, реагирует с
1) водородом
2) кислородом
3) хлором
4) бромом
5) бромоводородом
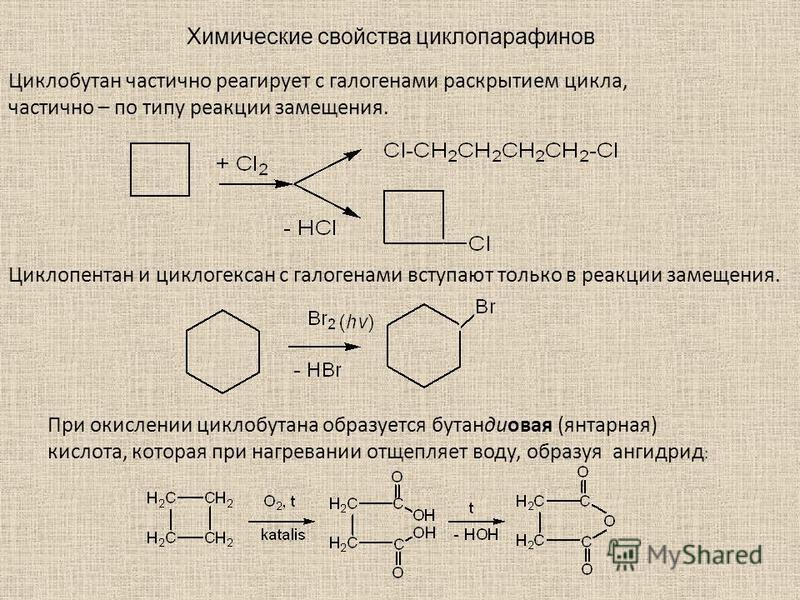
Из предложенного перечня веществ выберите два вещества, с которыми реагирует пропанол-1.

1) гидроксид натрия (р-р)
2) 2-метилбутан
3) калий
4) оксид углерода(IV)
5) бромоводородная кислота
Из предложенного перечня выберите два вещества, с которыми реагирует метиламин.
1) бутан
2) водород
3) кислород
4) бромоводород
5) алюминий
Установите соответствие между реагирующими веществами и органическим продуктом, который преимущественно образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) метан (изб.) и хлор
Б) ацетилен и водород
В) пропан и бром
Г) циклопропан и водород
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) тетрахлорметан
2) хлорметан
3) этан
4) 1-бромпропан
5) 2-бромпропан
6) пропан
А–2; Б–3; В–5; Г–6
А–2; Б–4; В–5; Г–6
А–5; Б–3; В–2; Г–6
А–2; Б–3; В–5; Г–4
Установите соответствие между реагирующими веществами и углеродсодержащим продуктом, который образуется при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.

РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) этанол и натрий
Б) этанол и бромоводород
В) этан и бром
Г) этанол и метанол
ПРОДУКТ ВЗАИМОДЕЙСТВИЯ
1) этилнатрий
3) бромэтан
4) бромэтен
5) метилэтанол
6) метилэтиловый эфир
А–2; Б–3; В–3; Г–5
А–2; Б–4; В–4; Г–6
А–1; Б–3; В–3; Г–6
А–2; Б–3; В–3; Г–6
Взаимодействие натрия с водой относится к реакциям:
1) каталитическим
2) гомогенным
3) практически необратимым
4) окислительно-восстановительным
5) обмена
Скорость реакции 2NO + O
2 = 2NO2 + Q уменьшится при1) внесении катализатора
2) уменьшении концентрации NO2
3) увеличении концентрации NO2
4) уменьшении давления в системе
5) уменьшении концентрации кислорода
Установите соответствие между формулой соли и продуктом, выделяющимся на аноде при электролизе водного раствора этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.

ФОРМУЛА СОЛИ
А) Na
Б) SnCI2
B) BeF2
Г) SnBr4
АНОДНЫЙ ПРОДУКТ
1) кислород
2) галоген
3) водород
4) фосфор
А–3; Б–2; В–3; Г–2
А–1; Б–4; В–1; Г–4
А–1; Б–2; В–1; Г–2
А–2; Б–1; В–1; Г–2
Установите соответствие между названием соли и средой ее водного раствора: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
НАЗВАНИЕ СОЛИ
А) гидросульфид калия
Б) гидросульфит натрия
В) ортофосфат калия
Г) хлорид хрома(III)
СРЕДА РАСТВОРА
1) нейтральная
2) кислотная
3) щелочная
А–3; Б–1; В–3; Г–1
А–3; Б–2; В–3; Г–2
А–3; Б–3; В–2; Г–2
А–1; Б–2; В–1; Г–2
Установите соответствие между уравнением химической реакции и направлением смещения химического равновесия при увеличении давления в системе: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.

УРАВНЕНИЕ РЕАКЦИИ
А) N2(г) +3H2(г) ⇄ 2NH3(г)
Б) 2H2(г) +O2(г) ⇄ 2H2O(г)
В) H2(г) +CI2(г) ⇄ 2HCI(г)
Г) SO2(г) +CI2(г) ⇄ SO2CI2(г)
НАПРАВЛЕНИЕ СМЕЩЕНИЯ ХИМИЧЕСКОГО РАВНОВЕСИЯ
2) в сторону исходных веществ
3) практически не смещается
А–1; Б–2; В–3; Г–1
А–3; Б–1; В–2; Г–1
А–1; Б–1; В–3; Г–2
А–1; Б–1; В–3; Г–1
Установите соответствие между веществами и реагентом, с помощью которого их можно отличить друг от друга: к каждой позиции, обозначенной буквой, подберите соответствующую позицию из второго столбца, обозначенную цифрой.
ВЕЩЕСТВА
А) ацетилен и этилен
Б) этилен и этан
В) этандиол-1,2 и этанол
Г) фенол и этанол
РЕАГЕНТ
1) Br2(aq)
2) [Ag(NH3)2]OH
3) AI(OH)3
4) H2SO4 (p-p)
5) Cu(OH)2
А–2; Б–1; В–5; Г–1
А–2; Б–1; В–4; Г–1
А–3; Б–1; В–5; Г–1
А–2; Б–3; В–5; Г–3
Наиболее токсичны для живого организма ионы:
1) меди
2) натрия
3) ртути
4) магния
5) калия
Мы занимаемся обработкой ваших ответов
Проверь себя, пройди другие тесты онлайн
- ЕГЭ 2019.

- ЕГЭ 2020. Химия. Вариант 17 Из предложенного перечня выберите два вещества, которые являются изомерами цис-бутена-2.циклобутанбутантранс-бутен-2бута…
- ЕГЭ 2020. Биология. Вариант 13 Установите последовательность процессов фотосинтеза. 1) преобразование солнечной энергии в энергию АТФ2) возбуждени…
- ОГЭ 2018. Химия. Вариант 52 Для полного растворения 19,6 г гидроксида меди(II) потребовалось 196 г раствора серной кислоты. Вычислите массовую долю …
- Характерные химические свойства альдегидов, предельных карбоновых кислот, сложных эфиров.
 10-11 классы Наиболее подвижный атом водорода в молекуле… Функциональная группа, в состав которой входят два атома кислорода — это….
10-11 классы Наиболее подвижный атом водорода в молекуле… Функциональная группа, в состав которой входят два атома кислорода — это…. - ЕГЭ 2017. География. Вариант 35 В каком из высказываний содержится информация о миграциях населения? Определите страну по её краткому описанию. Эта с…
- ЕГЭ 2018. Обществознание. Вариант 51 Учащиеся социально-экономического профиля проводят семинар «Акционерные общества в современной экономике». Одн…
- Классификация химических реакций в неорганической и органической химии. 10-11 классы Взаимодействие этилена с бромоводородом является реакцией: Реакция между магнием и соляной кислотой относится к реакциям…
- Химия. Взаимосвязь органических веществ. 10-11 классы Веществом Х в цепи превращений С6Н12О6 → Х → СН3СОН является: В схеме получения метана в лаборатории СН3СООNa .
 ..
.. - ЕГЭ 2017. Химия. Вариант 34 Между собой реагируют Из предложенного перечня выберите два соединения, которые реагируют с раствором HCI, но не реагиру…
- ЕГЭ 2019. Химия. Вариант 41 Установите соответствие между веществом и классом/группой, к которому(ой) это вещество принадлежит. ВЕЩЕСТВО А) плав…
Решутест. Продвинутый тренажёр тестов
Решутест. Продвинутый тренажёр тестов- Главная
- ЕГЭ
- Химия
- Химические свойства углеводородов
- Химические свойства алканов и циклоалканов
Решил заданий
Не решил заданий
Осталось заданий
История решения
1947 — не приступал 3738 — не приступал 7247 — не приступал 6103 — не приступал 5779 — не приступал 1886 — не приступалФормат ответа: цифра или несколько цифр, слово или несколько слов.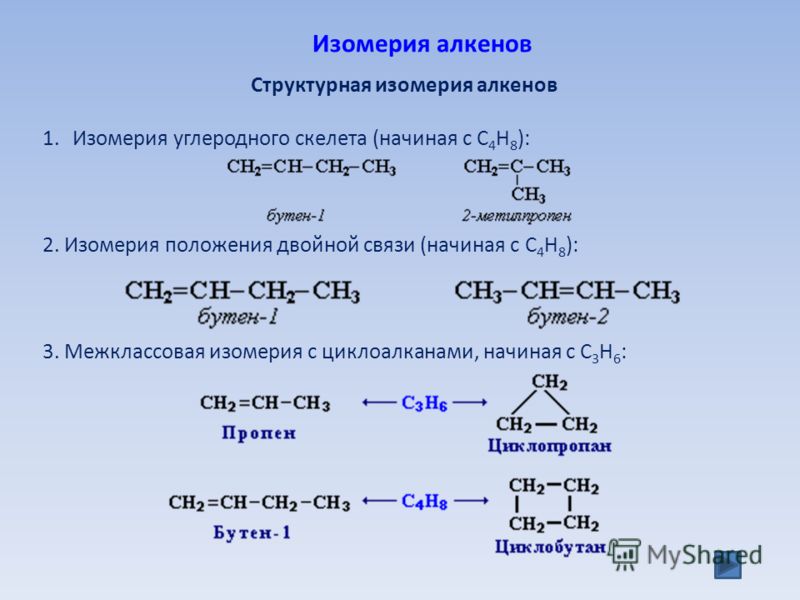 Вопросы на соответствие «буква» — «цифра» должны записываться как несколько цифр. Между словами и цифрами не должно быть пробелов или других знаков.
Вопросы на соответствие «буква» — «цифра» должны записываться как несколько цифр. Между словами и цифрами не должно быть пробелов или других знаков.
Примеры ответов: 7 или здесьисейчас или 3514
Раскрыть Скрыть
№1Не произойдет обесцвечивание бромной воды при пропускании через нее. В ответе укажите два верных вещества.
- этилена
- ацетилена
- этана
- циклопропана
- пропана
Какие два углеводорода могут реагировать с бромом на свету, но не реагируют с бромной водой?
- толуол
- пропен
- бутан
- бутадиен-1,3
- циклопропан
И циклопропан, и пропан реагируют с
- водородом
- кислородом
- водой
- хлором
- хлороводородом
Циклопропан, в отличие от пропана, реагирует с
- водородом
- кислородом
- хлором
- бромом
- бромоводородом
Не произойдет обесцвечивание бромной воды при пропускании через нее
- гексана
- бутана
- пропилена
- ацетилена
- пропена
В ответе укажите два верных утверждения.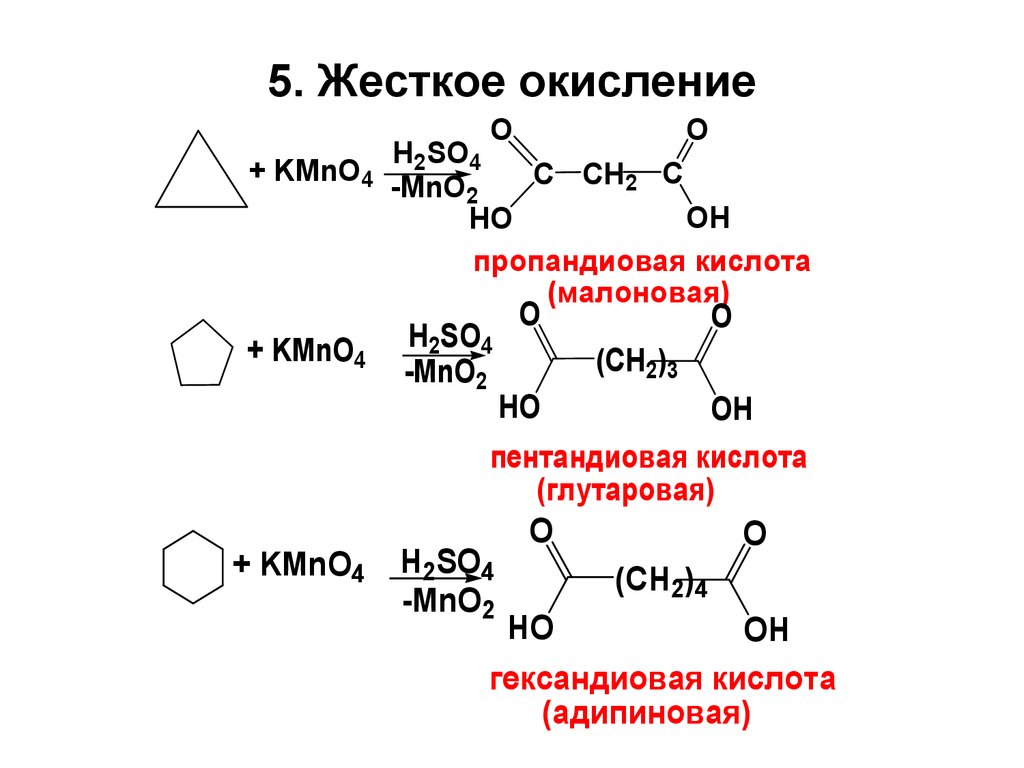 В отличие от пропана, циклопропан вступает в реакцию. В ответе укажите два верных утверждения.
В отличие от пропана, циклопропан вступает в реакцию. В ответе укажите два верных утверждения.
- дегидрирования
- гидрирования
- горения в кислороде
- гидрогалогенирования
- этерификации
Так твой прогресс будет сохраняться.
Регистрация
Мы отправили код на:
ИзменитьПолучить код повторно через 00:00
Я прочитал(-а) Политику конфиденциальности и согласен(-на) с правилами использования моих персональных данных
Ништяк!
Решено верно
Браво!
Решено верно
Крутяк!
Решено верно
Зачёт!
Решено верно
Чётко!
Решено верно
Бомбезно!
Решено верно
Огонь!
Решено верно
Юхууу!
Решено верно
Отпад!
Решено верно
Шикарно!
Решено верно
Блестяще!
Решено верно
Волшебно!
Решено верно
Реакции циклопропана и циклобутана: Pharmaguideline
Некоторые малые циклоалканы, включая циклопропан, ведут себя иначе, чем алканы.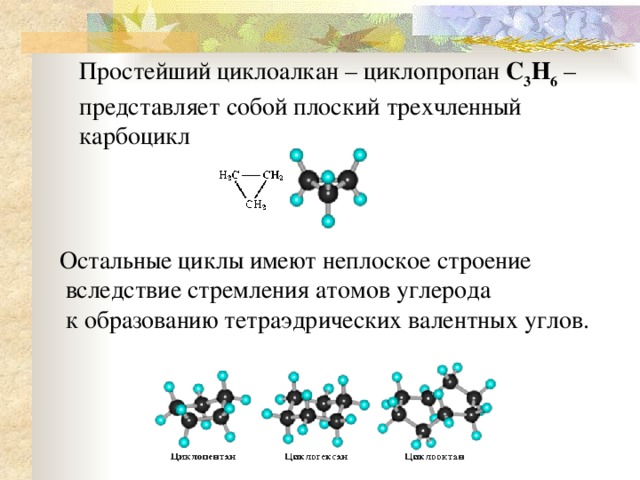 Реакция замещения, индуцированная УФ-излучением, протекает с циклопропаном, как и с нециклическими алканами. УФ-излучение не является необходимым для реакции. Можно разорвать кольцо циклопропана без УФ-излучения, так как происходят дополнительные реакции. Например, при добавлении брома к циклопропану образуется трибромпропан.
Реакция замещения, индуцированная УФ-излучением, протекает с циклопропаном, как и с нециклическими алканами. УФ-излучение не является необходимым для реакции. Можно разорвать кольцо циклопропана без УФ-излучения, так как происходят дополнительные реакции. Например, при добавлении брома к циклопропану образуется трибромпропан.
Если присутствует свет, это все равно может произойти, но также произойдет реакция замещения. Сжечь циклопропан очень трудно, потому что кольцо растягивается, что приводит к разрыву. Когда углерод образует четыре одинарные связи, валентные углы составляют 60° вместо нормального значения 109,5°. В углерод-углеродных связях перекрытие между орбиталями меньше, чем обычно, и пары связывающих электронов отталкиваются друг от друга. Если кольцо разорвано, система будет более стабильной.
Реакция Кори-Чайковского
В присутствии карбонильных соединений, таких как кетоны, сульфурильные соединения реагируют с образованием азиридинов и карбоновых кислот.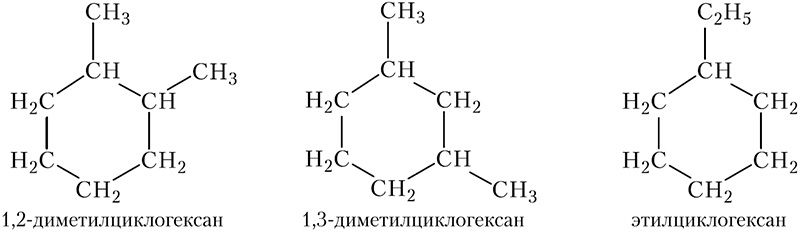
эпоксидирование
азиридинирование
Циклопропаны образуются при взаимодействии илидов серы с енонами.
Циклопропанирование
Реакция Вюрца
Образуется простой димер в результате двух эквивалентных молекул алкилгалогенида. Сочетание Вюрца — это органическая реакция, которая существует уже тысячи лет. Молекулярные версии реакции также были успешно использованы для получения соединений с напряженными кольцами:
При использовании двух разных алкилгалогенидов будет получена приблизительная статистическая смесь продуктов. Исходные материалы с различной скоростью реакции могут подвергаться более селективной несимметричной модификации.
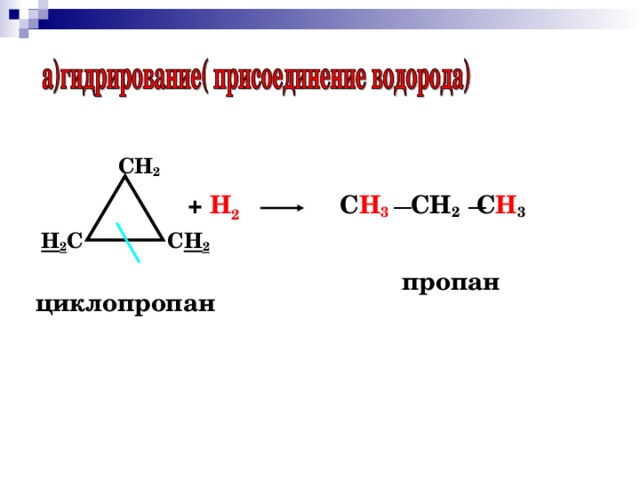
Гидрогенизация (раскрытие цикла) — Когда гидрирование циклоалканов происходит с катализаторами, такими как Ni или Pt, образуются насыщенные углеводороды. Процесс гидрирования усложняется с увеличением размера кольца. Циклоалканы с высоким содержанием углерода обычно выдерживают гидрирование без реорганизации.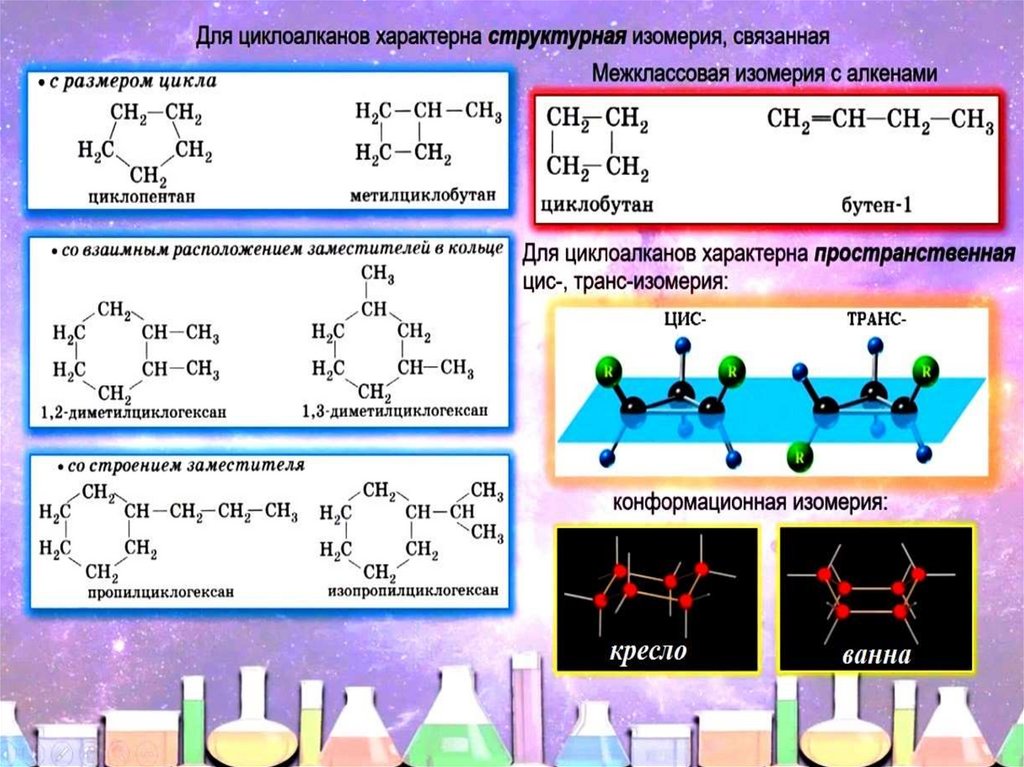 Эти выводы очевидны из условий следующих реакций.
Эти выводы очевидны из условий следующих реакций.
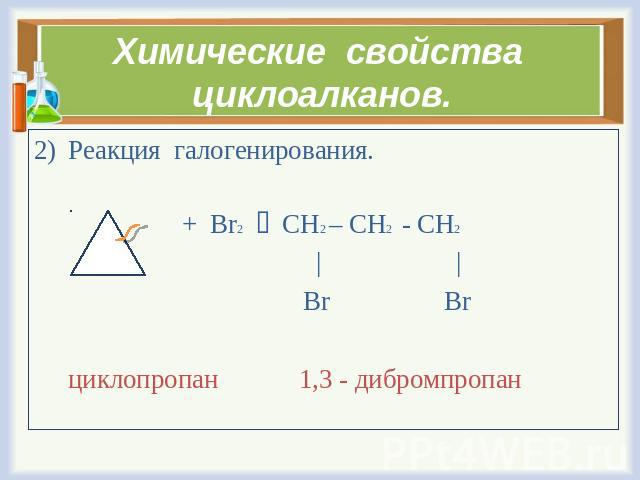
Галогенирование
Реакция присоединения галогена (ведущая к раскрытию кольца) — Темные реакции циклопропана с бромом и хлором дают продукты присоединения. Растворитель CCl2.
Реакция замещения с галогенами — При воздействии на циклоалканы УФ-светом хлор и бром вступают в реакцию с образованием продуктов замещения.
Реакции циклобутана
Гидрогенизация (раскрытие цикла) — Используя катализаторы, такие как Ni или Pt, циклоалканы можно гидрировать с получением насыщенных углеводородов. С увеличением размера кольца гидрирование становится более трудным. В целом верно, что высшие циклоалканы с шестью и более атомами углерода устойчивы к гидрированию. Следующие реакции иллюстрируют это.
Галогенирование
Реакция присоединения галогена (ведущая к раскрытию цикла) — Хромат и бром реагируют с циклопропаном в темноте с образованием продуктов присоединения. В качестве растворителя используется CCl2.
В качестве растворителя используется CCl2.
Позже стабильность циклоалкана определяется с помощью следующих двух тестов:
Теория деформации Байера
Теория деформации Байера придерживается следующих постулатов:
- Молекулярная планарность характеризует циклоалканы.
- Угловая деформация возникает, когда дисперсия валентного угла отклоняется от нормального тетраэдрического значения (1090 28′).
- По мере увеличения угловой деформации кольцо становится более нестабильным.
- Легче образовывать более стабильные кольца
С-С связи имеют положительный знак, означающий, что они изогнуты внутрь, а отрицательный знак означает, что они выгнуты наружу от нормального тетраэдрического угла. Только величина угловой деформации определяет степень деформации внутри кольца, независимо от угла. Следовательно, теория деформации Байера предполагает, что циклопропан должен быть сильно напряжен и, следовательно, наиболее нестабилен, поскольку он имеет наибольшую угловую деформацию.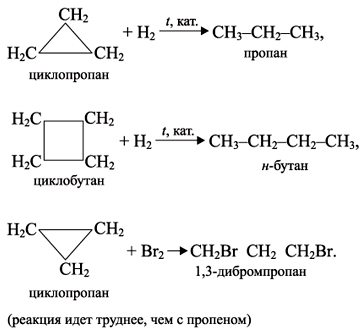
Теория Заксе-Мора
Именно Саксе и Мор (1918) предположили, что циклогексановые кольца и более высокие члены становятся стабильными, если они не ограничены одной плоскостью, как предполагал Байер, потому что атомы углерода не ограничены одной плоскостью. Предполагается, что в том случае, если кольцо примет складчатое или сморщенное состояние, нормальные тетраэдрические углы 1090 28′ сохранятся и, следовательно, растяжение внутри кольца будет уменьшено.
Получить тематические печатные документы в формате pdfПросмотреть здесь
Деформация кольца в циклопропане и циклобутане
Деформация кольца в циклопропане и циклобутане
В предыдущем посте мы видели, что циклопропан и циклобутан имеют необычно высокую «деформацию кольца» 27 ккал/моль и 26 ккал/моль соответственно. Мы определили это, сравнив теплоту сгорания колец различных размеров, и увидели, что ΔH сгорания на CH 2 практически постоянно, когда размеры колец превышают 12.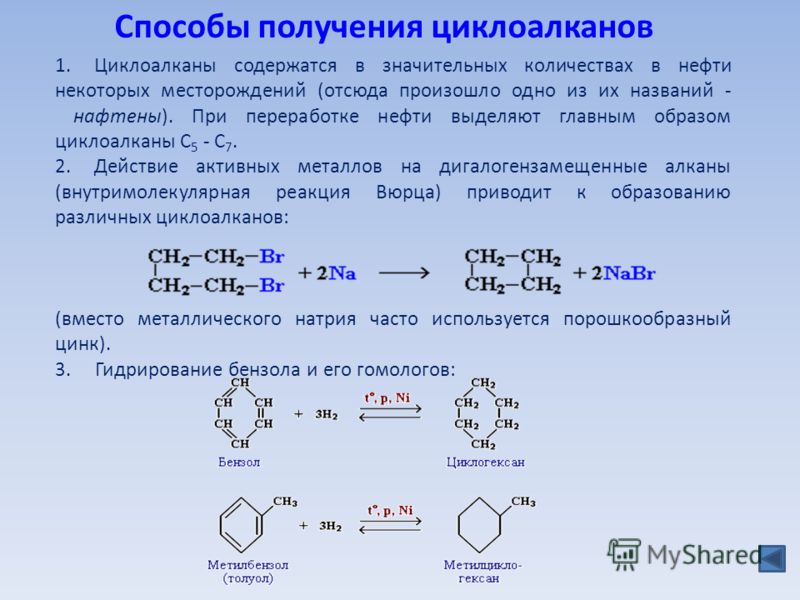
На основании этих расчетов мы увидели, что циклопропан и циклобутан гораздо более нестабильны, чем мы могли бы наивно ожидать от «ненапряженного» кольца такого размера . Кроме того, прочность связи С-С в циклопропане значительно слабее (65 ккал/моль), чем мы наблюдаем для типичной связи С-С (80-85 ккал/моль).
Следовательно, должна быть какая-то структурная особенность циклопропана и циклобутана, которая приводит к этому дополнительному напряжению.
Что это может быть? Давайте посмотрим.
Содержание
- угловая деформация у циклопропана и циклобутана
- Торсиональная деформация в циклопропане
- Торсиональный штамм в циклобутане — некоторые шайбы
- Сумма: кольцевой штамм в циклобутане и циклобутане
- .
1. Угловая деформация в циклопропане и циклобутанеПервое, на что следует обратить внимание при использовании циклопропана и циклобутана, это неидеальные валентные углы .
 Идеальный валентный угол в тетраэдрическом углероде составляет 109 градусов ( См. пост: Откуда мы знаем, что метан является тетраэдрическим )
Идеальный валентный угол в тетраэдрическом углероде составляет 109 градусов ( См. пост: Откуда мы знаем, что метан является тетраэдрическим )) значительно меньше идеального угла.
Это означает, что электронные облака, окружающие каждый атом, будут располагаться значительно ближе друг к другу, чем в идеале, а поскольку одинаковые заряды отталкивают , это будет энергетически менее благоприятный , чем для алкана с прямой цепью.
Дополнительная нестабильность, вызванная этим ограничением, называется угловой деформацией или деформацией фон Байера.
[ Примечание. Хотя атомы циклопропана образуют треугольник, электронные облака между каждым атомом не обязательно следуют его «линиям». Природа связи в циклопропане — глубокая тема. Майк Эванс снял на нее видео здесь.]
Так все просто? Угловая деформация — это все, о чем можно говорить? Не совсем так – есть еще один фактор, который следует учитывать.
2. Деформация при кручении в циклопропане
Из предыдущих глав, посвященных конформациям, вы можете вспомнить концепцию «деформации при кручении» (также известной как «деформация при скручивании») ( См. статью: Смещенные и затменные конформации этана ).
Хотя эти два слова часто вызывают путаницу в умах студентов, концепция очень проста: деформация, создаваемая простым вращением .
Вы когда-нибудь летали на игрушечном самолете с заводным винтом? По мере того, как вы крутите пропеллер, вы постепенно сталкиваетесь с все большим и большим сопротивлением резинок.
Когда завод завершится, вы по-настоящему почувствуете, как пропеллер впивается вам в палец! Резинки в этом случае испытывают партию деформации кручения. Освобождение пропеллера приводит к раскручиванию эластичных лент, что является движущей силой движения самолета.
То же самое и с молекулами.
В этане, например, вращение вокруг одинарной связи C-C приводит к двум основным конформациям: «затмеваемая» конформация, где два CH 3 группы прямо выровнены друг с другом вдоль оси С-С, и более благоприятна «шахматная» конформация, когда они смещены на 60 градусов.

Разница в энергии между этими двумя формами составляет около 3 ккал/моль (фактически 2,8 ккал/моль).
Таким образом, этан в закрытой конформации испытывает напряжение кручения (движущая сила вращения) около 3 ккал/моль.
В циклопропане соседние группы CH 2 также затмеваются. В отличие от этана, этот штамм нельзя разгрузить вращением (кольцо слишком жесткое).
Другими словами, группы CH 2 заблокированы в конформации затмения, что приводит к деформациям при кручении — очень похоже на пропеллер, который был закручен, но удерживается на месте. Как и в случае с винтовыми винтами, циклопропаны принято считать «подпружиненными» — позже мы увидим несколько примеров реакций, в которых высвобождение кольцевого напряжения является значительной движущей силой!
3. Деформация при кручении в циклобутане: возможно некоторое сморщиваниеЧто насчет циклобутана? Если бы циклобутан был полностью плоским, мы могли бы ожидать затмевающих взаимодействий между четырьмя группами CH 2 .

На самом деле циклобутан имеет небольшое пространство для маневра . В результате в одной плоскости находятся три атома углерода, а четвертый выглядит как «лоскут», слегка смещенный от плоскости.
Любой из четырех атомов углерода может быть «лоскутом» — в растворе происходит взаимопревращение между разными конформерами, и в среднем каждый углерод находится в роли «лоскута» равное количество времени. Тот факт, что циклобутановые кольца могут «сморщиваться» таким образом, приводит к небольшому снижению деформации при кручении.
4. Резюме: Деформация кольца в циклопропане и циклобутанеИ циклопропан, и циклобутан имеют большую деформацию кольца из-за сочетания угловой деформации и крутильной деформации .
Следите за будущими реакциями, движущей силой которых является «снятие напряжения кольца».
В следующем посте поговорим о 5- и 6-членных кольцах.
Вот вам загадка: внутренние углы пятиугольника равны 108°, а шестиугольника — 120°.

Только на основании этого можно ожидать, что циклопентан менее напряжен, чем циклогексан, поскольку угол ближе к идеальному углу тетраэдрического углерода.
На самом деле полная противоположность . Почему? Ответ в следующем посте.
Next post : Кольцевой штамм циклопентана и циклогексана
Примечания
(дополнительно) Ссылки и дополнительная литература
Поскольку циклопропан и циклобутан имеют небольшие размеры и жесткость из-за присущих им молекул, они обладают высокой реакционной способностью9.0127 деформация , потому что орбитали, участвующие в связывании, вынуждены отклоняться от идеального тетраэдрического угла sp 3 , равного 109,5°.
- Ueber Polyacetylenverbindungen
Адольф Байер
Бер. 1885 , 18 (2), 2269-2281
DOI: 10.1002/cber.18850180296
Оригинальная статья немецкого химика Адольфа фон Байера о деформации кольца. Несмотря на то, что эта статья носит совершенно иное название, деформация кольца обсуждается в самом конце статьи.
Несмотря на то, что эта статья носит совершенно иное название, деформация кольца обсуждается в самом конце статьи. - Оценка деформации углеводородов. Штамм в адамантане и его происхождение
Пол фон Р. Шлейер, Джеймс Эрл Уильямс и Бланшар К.Р. : 1021/ja00711a030
Ранняя статья профессора П. В. Р. Шлейера до его переезда в Германию в 1970-х годах. Адамантейн был его любимой темой, так как одна из его наиболее цитируемых статей — одностраничное сообщение в JACS по простому синтезу адамантана. В таблице VII этой статьи собрана большая коллекция энергий деформации различных углеводородов, в том числе циклопропана и циклобутана (28,13 и 26,90 ккал/моль соответственно). - Теоретический анализ свойств углеводородов. 1. Связи, структуры, концентрация зарядов и релаксация зарядов
Кеннет Б. Виберг, Ричард Ф. В. Бадер и Клемент Д. Х. Лау
Журнал Американского химического общества 1987, 109 (4), 985-1001
DOI: 1021/ja00238a004
Изменения в гибридизации связаны с изменениями электроотрицательности. Чем больше характер s конкретной углеродной орбитали, тем больше ее электроотрицательность. В результате атомы углерода, входящие в состав натянутых колец, более электроотрицательны, чем обычно, по отношению к водороду.
Чем больше характер s конкретной углеродной орбитали, тем больше ее электроотрицательность. В результате атомы углерода, входящие в состав натянутых колец, более электроотрицательны, чем обычно, по отношению к водороду. - Спектроскопия ядерного магнитного резонанса. Взаимодействие углерод-углерод в производных циклопропана
Фрэнк Дж. Вейгерт и Джон Д. Робертс
Журнал Американского химического общества 1967 , 89 (23), 5962-5963
DOI: 1021119996666966666666. В экспериментах были предложены значения 33% и 17% для s-характера связей С-Н и С-С циклопропана соответственно. Покойный профессор Дж. Д. (Джек) Робертс был гигантом в области физической органической химии и провел почти всю свою карьеру в Калифорнийском технологическом институте. Он активно занимался исследованиями в свои 9 лет.0! - Связующие свойства циклопропана и их химические последствия
Dr. Armin de Meijere
Armin de Meijere
Angew. хим. Междунар. Эд. 1979 , 18 (11), 809-826
DOI: 10.1002/anie.197908093
Обзор проф. его карьера. - Теоретическое определение молекулярной структуры и конформации. 20. Переоценка энергий деформации циклопропана и циклобутана углерод-углерод и энергии углерод-водородной связи, 1,3-взаимодействий и σ-ароматичности
Dieter Cremer and Juergen Gauss
Журнал Американского химического общества 1986 , 108 (24), 7467-7477
DOI: 10211128477
22. , и в этой статье изучается, почему энергии деформации циклопропана и циклобутана так близки. - Стереохимия циклобутана и гетероциклических аналогов
Роберт М. Мориарти
Темы стереохимии 1974 , 8
DOI : 10.1002/9780470147177.
- Ueber Polyacetylenverbindungen


 10-11 классы Наиболее подвижный атом водорода в молекуле… Функциональная группа, в состав которой входят два атома кислорода — это….
10-11 классы Наиболее подвижный атом водорода в молекуле… Функциональная группа, в состав которой входят два атома кислорода — это…. ..
.. Идеальный валентный угол в тетраэдрическом углероде составляет 109 градусов ( См. пост: Откуда мы знаем, что метан является тетраэдрическим )
Идеальный валентный угол в тетраэдрическом углероде составляет 109 градусов ( См. пост: Откуда мы знаем, что метан является тетраэдрическим )
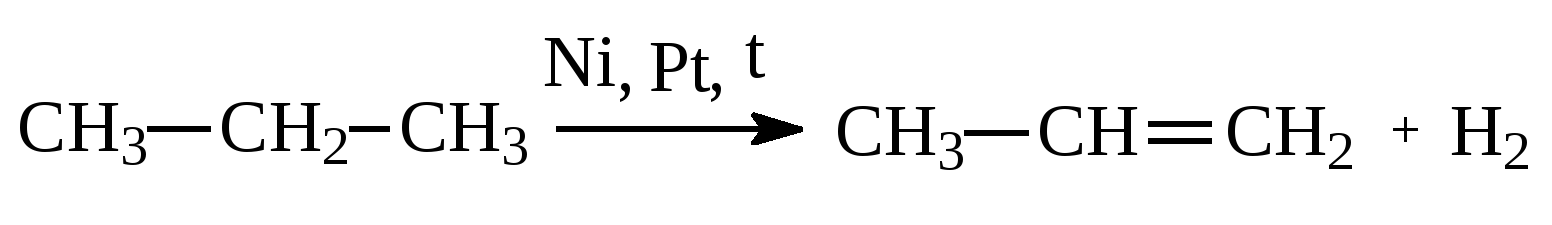
 Несмотря на то, что эта статья носит совершенно иное название, деформация кольца обсуждается в самом конце статьи.
Несмотря на то, что эта статья носит совершенно иное название, деформация кольца обсуждается в самом конце статьи.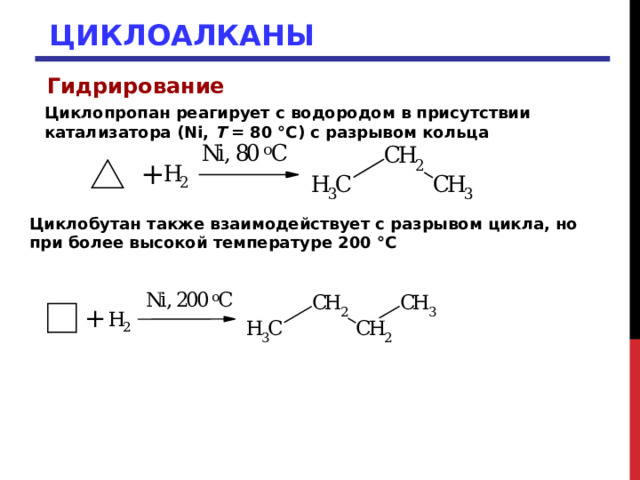 Чем больше характер s конкретной углеродной орбитали, тем больше ее электроотрицательность. В результате атомы углерода, входящие в состав натянутых колец, более электроотрицательны, чем обычно, по отношению к водороду.
Чем больше характер s конкретной углеродной орбитали, тем больше ее электроотрицательность. В результате атомы углерода, входящие в состав натянутых колец, более электроотрицательны, чем обычно, по отношению к водороду.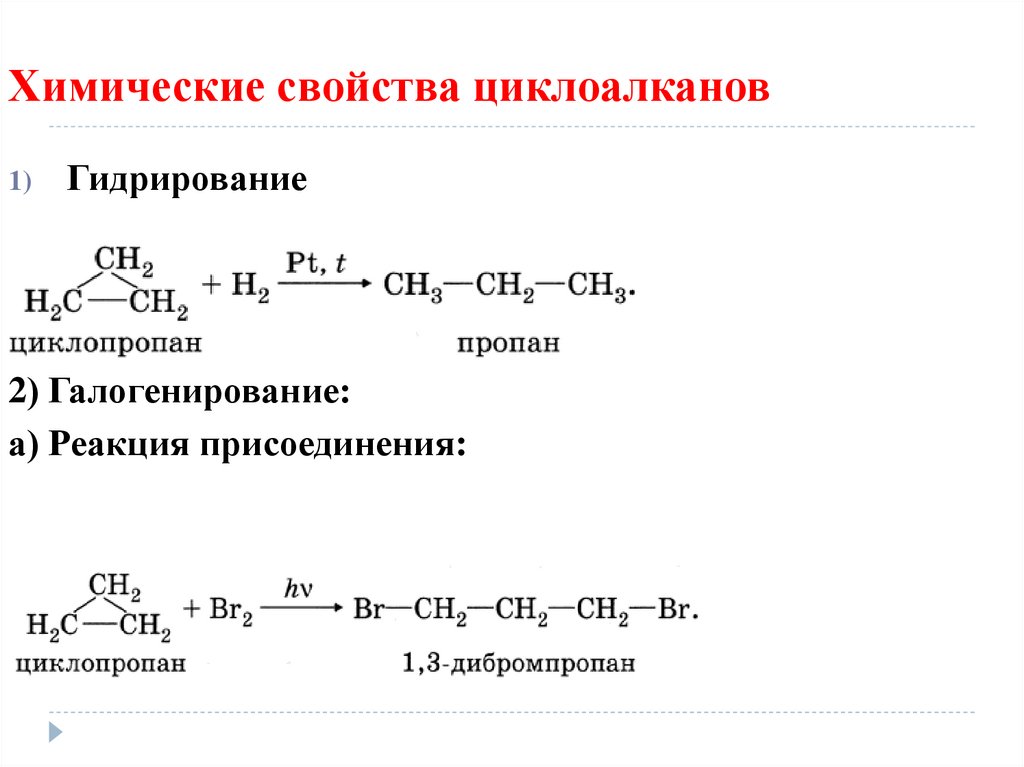 Armin de Meijere
Armin de Meijere 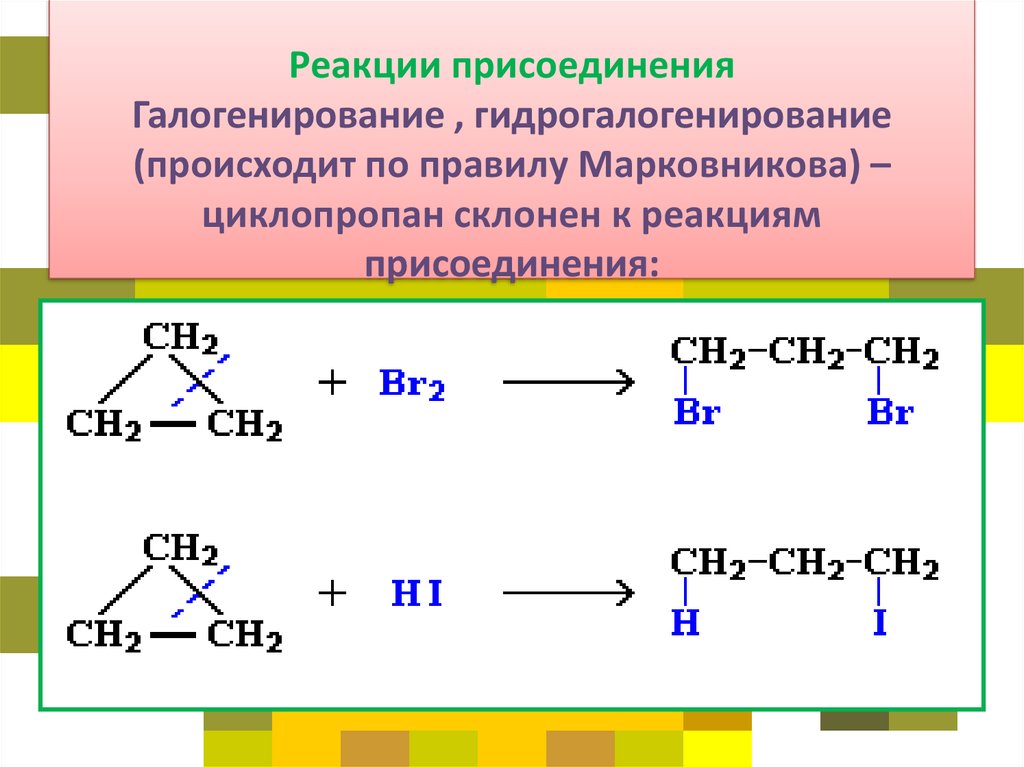
Leave A Comment