Тренажер задания 31 по химии алюминия
Тренажер задания 31 из ЕГЭ по химии алюминия, задачи на неорганическую химию (мысленный эксперимент) из экзамена ЕГЭ по химии, задания 31 по химии алюминия с текстовыми решениями и ответами.
1. В раствор, полученный при взаимодействии алюминия с разбавленной серной кислотой, по каплям добавили раствор гидроксида натрия до образования осадка. Выпавший осадок белого цвета отфильтровали и прокалили. Полученное вещество сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
2. К раствору сульфата алюминия добавили избыток гидроксида натрия. В полученный раствор небольшими порциями прибавили соляную кислоту, при этом наблюдали образование объемного осадка белого цвета, который растворился при дальнейшем прибавлении кислоты. В образовавшийся раствор прилили раствор карбоната натрия. Напишите уравнения описанных реакций.
3. Газ, выделившийся при взаимодействии хлористого водорода с перманганатом калия, пропустили через раствор тетрагидроксоалюмината натрия. Образовавшийся осадок отфильтровали, прокалили, и твердый остаток обработали соляной кислотой. Напишите уравнения описанных реакций.
Образовавшийся осадок отфильтровали, прокалили, и твердый остаток обработали соляной кислотой. Напишите уравнения описанных реакций.
4. Твердое вещество, образовавшееся при взаимодействии сернистого газа и сероводорода, при нагревании взаимодействует с алюминием. Продукт реакции растворили в разбавленной серной кислоте и в образовавшийся раствор добавили поташ. Напишите уравнения описанных реакций.
5. Продукт взаимодействия серы с алюминием (реакция протекает при нагревании) растворили в холодной разбавленной серной кислоте и в раствор добавили карбонат калия. Образовавшийся осадок отделили, смешали с едким натром и нагрели. Напишите уравнения описанных реакций.
6. К раствору кальцинированной соды добавили раствор хлорида алюминия, выделившееся вещество отделили и внесли в раствор едкого натра. В образовавшийся раствор по каплям прибавляли раствор хлороводородной кислоты до прекращения образования осадка, который отделили и прокалили. Напишите уравнения описанных реакций.
Напишите уравнения описанных реакций.
7. Нитрат алюминия прокалили, продукт реакции смешали с кальцинированной содой и нагрели до плавления. Образовавшееся вещество растворили в азотной кислоте и полученный раствор нейтрализовали раствором аммиака, при этом наблюдали выделение объемного студенистого осадка. Напишите уравнения описанных реакций.
8. Осадок, полученный при добавлении в раствор сульфата алюминия каустической соды, отделили, прокалили, смешали с кальцинированной содой и нагрели до плавления. После обработки остатка серной кислотой была получена исходная соль алюминия. Напишите уравнения описанных реакций.
9. В раствор кристаллической соды добавили хлорид алюминия, выделившийся осадок отделили и обработали раствором едкого натра. Полученный раствор нейтрализовали азотной кислотой, выделившийся осадок отделили и прокалили. Напишите уравнения описанных реакций.
10. Осадок, полученный при взаимодействии раствора соли алюминия и щелочи, прокали-ли. Продукт реакции растворили в концентрированном горячем растворе щелочи. Через полученный раствор пропустили углекислый газ, в результате чего образовался осадок. Напишите уравнения описанных реакций.
11. Вещество, которое образуется при электролизе расплава боксита в криолите, растворяется как в растворе соляной кислоты, так и в растворе щелочи с выделением одного и того же газа. При смешивании полученных растворов образуется объемный осадок белого цвета. Напишите уравнения описанных реакций.
12. Навеску алюминия растворили в разбавленной азотной кислоте, при этом выделилось газообразное простое вещество. К полученному раствору добавили карбонат натрия до полного прекращения выделения газа. Выпавший осадок отфильтровали и прокалили. Фильтрат упарили, полученный твердый остаток сплавили с хлоридом аммония. Выделившийся газ смешали с аммиаком и нагрели полученную смесь. Напишите уравнения описанных реакций
Выделившийся газ смешали с аммиаком и нагрели полученную смесь. Напишите уравнения описанных реакций
13. Оксид алюминия сплавили с карбонатом натрия, полученное твердое вещество растворили в воде. Через полученный раствор пропускали сернистый газ до полного прекращения взаимодействия. Выпавший осадок отфильтровали, а к профильтрованному раствору прибавили бромную воду. Полученный раствор нейтрализовали гидроксидом натрия. Напишите уравнения описанных реакций.
14. Навеску сульфида алюминия обработали соляной кислотой. При этом выделился газ и образовался бесцветный раствор. К полученному раствору добавили раствор аммиака, а газ пропустили через раствор нитрата свинца. Полученный при этом осадок обработали раствором пероксида водорода. Напишите уравнения описанных реакций.
15. Порошок алюминия смешали с порошком серы, смесь нагрели, полученное вещество обработали водой, при этом выделился газ и образовался осадок, к которому добавили избыток раствора гидроксида калия до полного растворения. Этот раствор выпарили и прокалили. К полученному твердому веществу добавили избыток раствора соляной кислоты. Напишите уравнения описанных реакций.
Этот раствор выпарили и прокалили. К полученному твердому веществу добавили избыток раствора соляной кислоты. Напишите уравнения описанных реакций.
16. Газ, выделившийся при взаимодействии хлористого водорода с бертолетовой солью, внесли в реакцию с алюминием. Продукт реакции растворили в воде и добавили гидроксид натрия до прекращения выделения осадка, который отделили и прокалили. Напишите уравнения описанных реакций.
17. Газ, выделившийся при нагревании раствора хлористого водорода с оксидом марганца (IV), внесли во взаимодействие с алюминием. Продукт реакции растворили в воде и добавили сначала избыток раствора гидроксида натрия, а затем соляную кислоту. Напишите уравнения описанных реакций.
18. Металлический алюминий растворили в растворе гидроксида натрия. Через полученный раствор пропустили избыток углекислого газа. Выпавший осадок прокалили, и полученный продукт сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
Напишите уравнения описанных реакций.
19) Оксид алюминия сплавили с карбонатом натрия. Полученный продукт растворили в соляной кислоте и обработали избытком аммиачной воды. Выпавший осадок растворили в избытке раствора гидроксида калия. Напишите уравнения описанных реакций.
20) Оксид алюминия сплавили с гидроксидом натрия. Продукт реакции внесли в раствор хлорида аммония. Выделившийся газ с резким запахом поглощен серной кислотой. Образовавшуюся среднюю соль прокалили. Напишите уравнения описанных реакций.
21) Порошок алюминия нагрели с порошком серы, полученное вещество обработали водой. выделившийся при этом осадок обработали избытком раствора гидроксида калия до его полного растворения. К полученному раствору добавили раствор хлорида алюминия и вновь наблюдали образование белого осадка. Напишите уравнения описанных реакций.
22) Осадок, полученный при взаимодействии растворов сульфата алюминия и нитрата бария, отфильтровали. Фильтрат обработали едким натром в мольном соотношении 1 : 3. Выпавший осадок отделили и прокалили. Полученное вещество обработали избытком раствора соляной кислоты. Напишите уравнения описанных реакций.
Фильтрат обработали едким натром в мольном соотношении 1 : 3. Выпавший осадок отделили и прокалили. Полученное вещество обработали избытком раствора соляной кислоты. Напишите уравнения описанных реакций.
23) При взаимодействии раствора сульфата алюминия с раствором сульфида калия выделился газ, который пропустили через раствор гексагидроксоалюмината калия. Образовавшийся осадок отфильтровали, промыли, просушили и нагрели. Твердый остаток сплавили с едким натром. Напишите уравнения описанных реакций.
24) Алюминиевый порошок смешали с серой и нагрели. Полученное вещество поместили в воду. Образовавшийся осадок разделили на две части. К одной части прилили соляную кислоту, а к другой – раствор гидроксида натрия. Напишите уравнения описанных реакций.
25) Металлический алюминий растворили в растворе гидроксида натрия. Через полученный раствор пропустили избыток углекислого газа. Выпавший осадок прокалили и полученный продукт растворили в разбавленной серной кислоте. Напишите уравнения описанных реакций.
Выпавший осадок прокалили и полученный продукт растворили в разбавленной серной кислоте. Напишите уравнения описанных реакций.
26) При взаимодействии оксида алюминия и азотной кислоты образовалась соль. Соль высушили и прокалили. Образовавшийся при прокаливании остаток подвергли электролизу в расплавленном криолите. Полученный металл нагрели с концентрированными гидроксида калия и нитрата калия. При этом выделился газ с резким запахом. Напишите уравнения описанных реакций.
27) К раствору гидроксида натрия добавили порошок алюминия. Через раствор полученного вещества пропустили избыток углекислого газа. Выпавший осадок отделили и про-калили. Полученный продукт сплавили с карбонатом натрия. Напишите уравнения описанных реакций.
28) Порошок металлического алюминия смешали с твердым йодом, и добавили несколько капель воды. К полученной соли добавили раствор гидроксида натрия до выпадения осадка.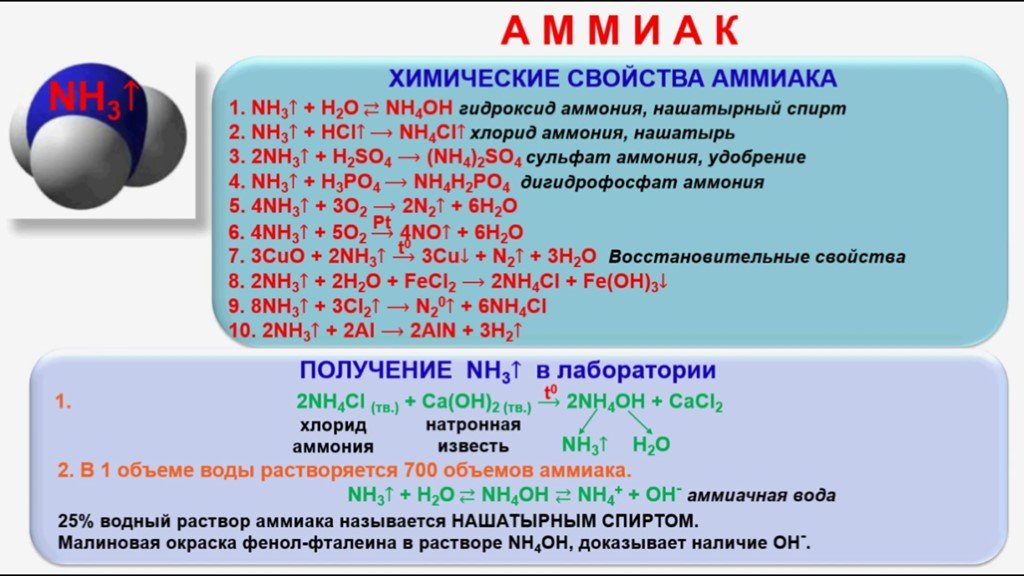 Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдается выпадение осадка. Напишите уравнения описанных реакций.
Образовавшийся осадок растворили в соляной кислоте. При последующем добавлении раствора карбоната натрия вновь наблюдается выпадение осадка. Напишите уравнения описанных реакций.
29) Алюминий растворили в соляной кислоте. К полученному раствору добавили избыток раствора карбоната калия. Выпавший осадок растворили в избытке раствора едкого калия, а выделившийся газ пропустили над раскаленным углем. Напишите уравнения описанных реакций.
30) Алюминий растворили в водном растворе горячего гидроксида натрия. к полученному раствору добавили по каплям разбавленную соляную кислоту до прекращения выпадения осадка. Выделившийся в период реакции газ пропустили над раскаленным оксидом меди (II). Полученное простое вещество растворили в разбавленной азотной кислоте. Напишите уравнения описанных реакций.
31) Алюминий вступил в реакцию с железной окалиной. Полученную смесь веществ растворили в концентрированном растворе гидроксида натрия и отфильтровали. Твердое вещество сожгли в атмосфере хлора, а фильтрат обработали концентрированным раствором хлорида алюминия. Напишите уравнения описанных реакций.
Твердое вещество сожгли в атмосфере хлора, а фильтрат обработали концентрированным раствором хлорида алюминия. Напишите уравнения описанных реакций.
Понравилось это:
Нравится Загрузка…
Хлорид алюминия гидроксид натрия
При добавлении к раствору хлорида алюминия раствора карбоната натрия выпадает осадок гидроксида алюминия и выделяется
Как определить массу десятипроцентного раствора гидроксида натрия, необходимого для взаимодействия с хлоридом алюминия?
3Наон+алхл3=алон3+4Нахл
13.35/133.5=0.1моль
0.1*3=0.3моль наон
м (наон) =0.3*40=12г
м раств =12*10=120г
Реакцией гидроксида натрия с соляной кислотой При нагревании до температуры 300 С хлорида натрия и хлорида алюминия образуется соединение тетрахлоралюминат натрия
Какое уравнение реакции получится если взяли хлорид алюминия прилили к нему по каплям гидроксид натрия
Рассчитайте массу осадка, который образуется при взаимодействии хлорида алюминия с 12 г гидроксида натрия
Реакция взаимодействия хлорида алюминия и гидроксида натрия:
AlCl3+3NaOH —>Al(OH)3 +3NaCl
12 г NaOH ——Х г Al(OH)3
3*40 ————78 г Al(OH)3
Х=12*78/3*40=7,8 г осадка -гидроксида алюминия
К примеру, если смешать его с хлорной кислотой в равном количестве, то получим алюминий хлорид с водой также в одинаковых пропорциях. Также еще одно вещество, с которым реагирует гидроксид алюминия, гидроксид натрия.
Также еще одно вещество, с которым реагирует гидроксид алюминия, гидроксид натрия.
Составте уравнение реакции и укажите тип:калий+кислород; хлорид алюминия+гидроксид натрия; оксид кальция +вода
Написать все возможные реакции,проходящие между веществами:вода,хлорид алюминия,оксид калия,гидроксид натрия,
Реакция обмена, замещения, соединения и разложения )
Взаимодействие амфотерных гидроксидов со щелочами в растворах происходит по уравнениямCuSO4 сульфат меди, K2SO3 сульфит калия, Na2CO3 карбонат натрия, Mg NO3 2 нитрат магния, NaNO2 нитрит натрия, NaCI хлорид натрия NaCIO…
Помогите с химией. определите массу осадка образующегося при взаимодействии хлорида алюминия с 12 г гидроксида натрия
2. Алюминий, гидроксид натрия р-р , гидрокарбонат натрия р-р , азотная кислота разб. р-р . 3. Алюминий, оксид марганца IV , водный7. Водные растворы гексагидроксоалюмината калия К3 А1 ОН 6 , хлорид алюминия, сероводорода и гидроксида рубидия.
Какая масса осадка выпадет после смешивания раствора хлорида алюминия с 200 граммами 12% раствора гидроксида натрия?
С какой целью интересуетесь?
Химические свойства гидроксида алюминия. Гидроксид алюминия при нагревании разлагается на оксид алюминия и водуЗапишем уравнение взаимодействия хлорида алюминия и гидроксида натрия
Гидроксид алюминия при нагревании разлагается на оксид алюминия и водуЗапишем уравнение взаимодействия хлорида алюминия и гидроксида натрия
К 100г 15% раствора гидроксида натрия добавили раствор хлорида алюминия,масса выпавшего осадка???
При взаимодействии хлорида алюминия с избытком гидроксида натрия образуется растворимый тетрагидроксоалюминат натрия, а не гидроксид алюминия, т. е. в данной реакции осадок не образуется
Если же реагенты брать в эквивалентном соотношении, то максимальная масса осадка составит (100*0,15/40)/3*78 = 9,75г (78 — молярная масса алюминия)
Ответ: от 0г до 9,75г в зависимости от соотношения реагентов (в условии не указано количество хлорида алюминия)
Составьте ионное уравнение взаимодействия хлорида алюминия с гидроксидом калия.Составьте уравнения реакций, характеризующих общие химические свойства щелочей, на примере гидроксидов натрия и кальция.
Сульфид натрия, хлорид алюминия, гидроксид калия, хлорид железа (III) уравнения 4 возможных реакций между ними
В последнем случае пойдёт окислительно-восстановительная реакция
2FeCl3 + 3Na2S —> 2FeS + S + 6NaCl
Опыт 2. Гидроксид алюминия, получение и свойства. В пробирку поместите несколько капель раствора хлорида алюминия и прибавьте по каплям раствор гидроксида натрия до выпадения осадка.
Гидроксид алюминия, получение и свойства. В пробирку поместите несколько капель раствора хлорида алюминия и прибавьте по каплям раствор гидроксида натрия до выпадения осадка.
Уравнение Реакции между раствором гидроксида натрия(избыток) и хлоридом алюминия
Составить формулы веществ: сульфат калия, хлорид алюминия, оксид магния, гидроксид натрия. К каким классам веществ они о
K2SO4 (соль) ALCl3 (соль) MgO (оксиды) NaOH (щелочь)
Взаимодействие алюминия с галогенами. Алюминий бурно реагирует со всем галогенами фтором F, хлором Cl, бромом Br и иодином I, с образованием соответственно фторида AlF3, хлорида AlCl3, бромида Al2Br6 и иодида Al2Br6.Реакция алюминия с гидроксидом натрия
Как одним реактивом различить водные растворы бромида водорода фторида натрия гидроксида калия хлорида алюминия
Если прилить AgNO3
бромид водорода — желтый осадок AgBr
фторид натрия — осадка нет
гидроксид калия — осадок Ag2O
хлорид алюминия — белый осадок AgCl
Сульфид натрия усиливает гидролиз хлорида алюминия и доводит его до конца, до А1 0Н д. В свою очередь, хлорид алюминия усиливает гидролиз сульфидаНапишите схему мицеллы гидроксида алюминия, образующегося по реакции гидролиза хлорида алюминия c.61 .
В свою очередь, хлорид алюминия усиливает гидролиз сульфидаНапишите схему мицеллы гидроксида алюминия, образующегося по реакции гидролиза хлорида алюминия c.61 .
Составьте уравнение реакций: а) гидроксида алюминия с гидроксидом натрия б) алюминия с хлоридом ртути(2)
Уважаемый! По вопросу (а) реакция не идет, потому. что там и там группы ОН. Процесс не химический. а физический. Может быть при каких-то условиях произойдет растворение гидроксида алюминия в гидроксиде натрия. Ну а если при растворении выделяется тепло или раствор становится холодным, тогда да, можно будет сказать. что прошла химическая реакция. Так. что. только опыт покажет.
Теперь по второму вопросу. У Вас очень интересный учитель по химии, скорее он (она) физ-химик. С хлоридом ртути детям вообще запрещено иметь дело, да и взрослые тоже иногда травятся. Производство опасное. А с алюминием у которого всегда есть окисная пленка, то процесс если он и пойдет при каких-то особых условиях, то сначала с оксидом алюминия, а потом уже может быть. … а может и нет. Привет учителю!!!!
… а может и нет. Привет учителю!!!!
Хлорид натрия и фосфорная кислота. 4 . медь и гидроксид калия.19. Как гидроксид алюминия, так и соляная кислота могут взаимодействовать с.
6)сульфат алюминия+хлорид бария 7)карбонат натрия+азотная кислота 8)сульфат меди(2)+гидроксид натрия
Al2(SO4)3+3BaCl2=2AlCl3+3BaSO4
Na2CO3+2HNO3=2NaNO3 + CO2↑ + h3O
CuSO4+2NaOH=Cu(OH)2↓ + Na2SO4
Даны вещества сера, гидроксид натрия, азотная кислота, ортофосфорная кислота.Даны вещества раствор хлорида алюминия, конц.водный раствор аммиака, раствор тетрагидроксоалюмината натрия, углекислый газ.
Помогите с химией 8 класс.
По скайпу могу-бесплатно.
7. Рассчитайте пороги коагуляции, определите знак заряда коллоидной частицы, напишите формулу мицеллы, если для коагуляции 10,0 мл золя гидроксида алюминия, полученного сливанием растворов хлорида алюминия и гидроксида натрия…
Почему при взаимодействии хлорида алюминия с карбонатом натрия образуется осадок гидроксида алюминия?
Посмотрю что другие ответчики напишут, интересно
13.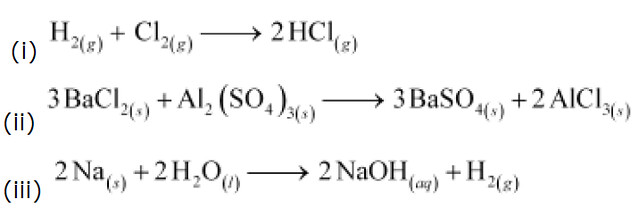 Гидроксид алюминия реагирует с каждым из двух веществ 14. Хлорид алюминия в растворе взаимодействует с.26. Металлический алюминий растворили в растворе гидроксида натрия.
Гидроксид алюминия реагирует с каждым из двух веществ 14. Хлорид алюминия в растворе взаимодействует с.26. Металлический алюминий растворили в растворе гидроксида натрия.
Потому что гидролизуется карбонат алюминия до СО2 и А1(ОН) 3 в момент получения
2AlCl3 + 3Na2CO3 + 3h3O = 2Al(OH)3 + 6NaCl + 3CO2
В трех пробирках присутствуют сульфат натрия, гидроксид алюминия и хлорид натрия. д
Различить можно по вкусу, не отравишься.
Химия Материалы к ЕГЭ . … Медь может вступать во взаимодействие с водным раствором 1 гидроксида натрия 2 хлорида кальция 3 кислота Оксид меди 2 серная кислота Хлорид бария фосфорная кислота Гидроксид серебра 1 йодоводородная кислота Алюминий …
MИУ ПИУ СИУ :1)AlCl3+NaOH-…МИУ ПИУ СИУ :2) Ba(No3)2+K3PO4-… Решить реакции
AlCl3 + 3NaOH=3NaCI + Al(OH)3
3Ba(NO3)2 + 2K3(PO4)=Ba3(PO4)2+6KNO3
Гидроксид алюминия избытка гидроксида натрия.? гидроксидом алюминия и оксидом меди I . ? хлоридом бария и сульфатом натрия. При действии на гидроксид кальция большого избытка отрофосфорной кислоты образуется.
Будте добры,подскажите названия:. h3 Al(OH)3 HCk AlCL3 CuSO4 AL(sO4)3 NaOH NaAlO2 Fe2O3 Al2O3
3) соляная кислота (хлороводород)
Натрий получают электролизом расплавленного хлорида натрия или гидроксида натрия.Калий в ряду стандартных электродных потенциалов расположен до алюминия, и его ионы восстанавливаются присоединяют электроны гораздо труднее, чем молекулы воды.
Приветик!
сульфат меди (2)
метаалюминат натрия
оксид железа (3)
Удачи!
Определить класс и дать название…(химия)
Оксид -углекислый газ, соль -хлорид кальция, основание (нерастворимое) — гидроксид меди, оксид-оксид натрия, кислота- серная, простое вещество металл -барий, основание (растворимое) -гидроксид натрия, соль- хлорид алюминия, оксид- оксид серы (сернистый газ), соль-иодид бария, это уже было: основание (растворимое) -гидроксид натрия, оксид-оксид калия, кислота-соляная, соль-хлорид магния, кислота-ортофосфорная (или просто фосфорная)
Осаждение гидроокиси олова с использованием гидроксида натрия. В процессе протекания химической реакции между гидроксидом натрия NaOH и хлоридом двухвалентного олова SnCl2 осаждают амфотерный гидроксидСплав олова и алюминия. Азотно кислое олово.
В процессе протекания химической реакции между гидроксидом натрия NaOH и хлоридом двухвалентного олова SnCl2 осаждают амфотерный гидроксидСплав олова и алюминия. Азотно кислое олово.
CO2, Na2O,SO2,k2O — оксиды — оксид углерода (IV), оксид натрия, оксид серы (IV), оксид калия, 1 и 3-й кислотный оксид, 2 и 4-й — основный оксид.
САСL2, ALCL3, BaI2, MgCl2 — соли: хлорид кальция, хлорид алюминия, йодид бария, хлорид магния
Сu(ОН) 2, NaОН — основания — гидроксид меди (ІІ), гидроксид натрия
Н2SO4, HCL, h4PO4 — кислоты: серная, соляная, ортофосфорная
Ва, Ca — простые вещества: барий, кальций
Напиште уравнение по химии! Срочно! Из AlCl3 надо получить Na[Al(OH)4]
Добавить гидроксид натрия, получится эта хрень + хлорид натрия
11. Раствор нитрата алюминия взаимодействует с каждым веществом пары 1 сульфат магния и хлорид натрия 2 гидроксид натрия и силикат калия 3 Таким образом подходит вариант 2 — образуется нерастворимый гидроксид алюминия и силикат алюминия, соответственно.
\\[ZnC{{l}_{2}}\\]; которые будут растворяться в избытке NaOH?(a)A,C и D(b)только C и D(c)B и только C(d)только A и D
Дата последнего обновления: 16 апреля 2023
•
Всего просмотров: 285k
•
Просмотров сегодня: 2.55k
Ответ
Проверено
285k+ просмотров
Некоторые неорганические соединения не реагируют с NaOH. Некоторые при реакции с NaOH могут выделять легковоспламеняющийся газ. Более полярные соли металлов могут растворяться в избытке NaOH. Соли металлов с d-блоком являются более полярными солями.
Полный пошаговый ответ:
Хлорид хрома при реакции с NaOH дает гидроксид хрома и соль NaCl.
Когда \[CrC{{l}_{3}}\] реагирует с избытком NaOH с образованием комплекса и соли NaCl.
\[CrC{{l}_{3}}+6NaOH\to Na[Cr{{(OH)}_{6}}]+3NaCl\]
Хлорид алюминия реагирует с NaOH с образованием гидроксида и соли алюминия.
При взаимодействии избытка NaOH с \[AlC{{l}_{3}}\] образуется \[NaAl{{O}_{2}}\] и вода. Реакция представлена как
Реакция представлена как
\[AlC{{l}_{3}}+3NaOH\to NaAl{{O}_{2}}+2{{H}_{2}}O\]
Когда \[ZnC{{l}_{2}}\] реагирует с избытком NaOH, он дает гидроксид цинка и соль NaCl.
\[ZnC{{l}_{2}}+2NaOH\to Zn{{(OH)}_{2}}+2NaCl\]
Только CuS не реагирует с NaOH с образованием гидроксида или комплекса. Это связано с тем, что сама по себе медь очень неактивна. Он не растворяется в NaOH до тех пор, пока не будет сильно сконцентрирован. Также CuS менее полярен, чем другие вышеперечисленные варианты.
Таким образом, с избыток NaOH.
Правильный ответ на вопрос — вариант (а).
Дополнительная информация:
Гидроксид натрия или каустическая сода обладают способностью растворять металлы и превращать их в гидроксиды. Это ионное соединение с температурой плавления 604,4 градуса по Фаренгейту. Он очень хорошо растворяется в воде. Он реагирует с кислотами, нейтрализуя раствор и образуя соль и воду. Это очень сильное основание, и его ионы представляют собой ион натрия и гидроксид-ион. В основном используется как чистящее средство.
В основном используется как чистящее средство.
Примечание:
В вопросе упоминается избыток NaOH. Поэтому в основном соединения при избытке NaOH дают комплексы либо оксида, либо гидроксида. Это связано с тем, что NaOH является полярным растворителем и сильным основанием.
Недавно обновленные страницы
Большинство эубактериальных антибиотиков получено из биологии ризобий класса 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологии класса 12 А0003
Канализационные или городские канализационные трубы не должны быть непосредственно очищены от микробов класса 12 по биологии NEET_UG
Очистка сточных вод осуществляется микробами A. B Удобрения класса 12 по биологии NEET_UG
Иммобилизация ферментов – это преобразование активного фермента класса 12 по биологии NEET_UG
Большинство антибиотиков относятся к эубактериям. получен из биологии ризобий класса 12 NEET_UG
Саламиновые биоинсектициды были извлечены из биологии класса А 12 NEET_UG
Какое из следующих утверждений относительно бакуловирусов класса 12 биологии NEET_UG
Канализационные или городские канализационные трубы не должны быть непосредственно 12-го класса биологии NEET_UG
Очистка сточных вод осуществляется микробами A. B Удобрения 12-го класса биологии NEET_UG
B Удобрения 12-го класса биологии NEET_UG
Иммобилизация ферментов – это преобразование активного фермента 12-го класса биологии NEET_UG
3
7777777Актуальные сомнения
Студенты также читают
Изложите наблюдения, которые вы сделали бы при добавлении гидроксида натрия к водному раствору хлорида алюминия. Приведите сбалансированные химические уравнения. 9
20 видео 3NaOH (водн.) +AlCl3(aq)→Al(OH)3(s)+NaCl(aq)
Гидроксид натрия + Хлорид алюминия → Гидроксид алюминия + Хлорид натрия
Был ли этот ответ полезен?
534
Ab Padhai каро бина объявления ке
Khareedo DN Про и дехо сари видео бина киси объявление ки rukaavat ке!
Похожие видео
Избыток разбавленного раствора гидроксида натрия постепенно добавляют при встряхивании к водному раствору сульфата цинка. Что бы вы заметили?
11480257
Приведите балансовое уравнение реакции алюминия с водным раствором гидроксида натрия.
15163172
Передайте следующую информацию в виде сбалансированного химического уравнения:
При добавлении водного раствора гидроксида натрия к водному раствору сульфата меди гидроксид меди выпадает в осадок, а сульфат натрия остается в растворе.
28395119
Укажите наблюдения, которые вы сделали бы при добавлении гидроксида натрия к водному раствору (i) сульфата железа (ii) хлорида алюминия.
34640257
Сбалансируйте химическое уравнение, включив физические состояния веществ для следующих реакций. а) Водные растворы хлорида бария и сульфата натрия реагируют с образованием нерастворимого сульфата бария и водного раствора хлорида натрия.
161345812
Избыток разбавленного раствора гидроксида натрия постепенно добавляют при встряхивании к водному раствору сульфата цинка. Что бы вы заметили?
357199718
(a) Как действует лакмус на:
(ii) Раствор газообразного аммиака в воде
(b) Назовите наблюдения, которые вы сделали бы при добавлении гидроксида натрия к водному раствору of :
(i) Сульфат железа
(ii) Хлорид алюминия
Приведите сбалансированные химические уравнения.

642777264
Что вы увидите, если добавить избыток разбавленного раствора NaOH и встряхнуть с водным раствором хлорида алюминия?
642896528
Напишите сбалансированное химическое уравнение с символами состояний для реакции: раствор гидроксида натрия (в воде) реагирует с раствором соляной кислоты (в воде) с образованием хлорида натрия и воды
642906640
सोडियम हाइड्रॉक्साइड Просмотреть еще ै तो सोडियम क्लोराइड विलयन तथा जल बनता है।
643055950
Напишите сбалансированное химическое уравнение Действие раствора гидроксида натрия на алюминий.
643925477
Напишите сбалансированное химическое уравнение
Действие раствора гидроксида натрия на алюминий
643925608
Между двумя водными растворами один представляет собой хлорид железа, а другой — хлорид алюминия. Как бы вы определили раствор хлорида железа с помощью водного раствора аммиака? Ответьте сбалансированным химическим уравнением.
643967068
Избыток разбавленного раствора гидроксида натрия постепенно добавляют при встряхивании к водному раствору сульфата цинка.

Leave A Comment